-
Medical journals
- Career
Dabigatran-etexilát v klinické praxi pro prevenci tromboembolických příhod u nemocných s fibrilací síní
Authors: M. Táborský 1,2; P. Heinc 1,2; Y. Hrčková 1,2
Authors‘ workplace: I. interní klinika – kardiologická Lékařské fakulty UP a FN Olomouc, přednosta doc. MUDr, Miloš Táborský, Ph. D., FESC, MBA 1; Komplexní kardiovaskulární centrum FN Olomouc, přednosta prof. MUDr. Petr Bachleda, CSc. 2
Published in: Vnitř Lék 2012; 58(10): 769-777
Category: Reviews
Overview
Dabigatran je první prezentované antikoagulancium nové generace, které ve studii RE-LY prokázalo v dávce 150 mg 2krát denně vyšší účinnost v prevenci CMP a systémové embolizace a srovnatelnou, resp. vyšší bezpečnost vzhledem k dobře kontrolovanému warfarinu. Dávka 110 mg 2krát denně prokázala srovnatelnou účinnost spojenou se superiorní bezpečností proti warfarinu. Klíčové a ojedinělé ve spektru moderních antikoagulancií je signifikantní snížení jak ischemických, tak krvácivých CMP v dávkování 150 mg 2krát denně. Dabigatran navíc zásadním způsobem usnadňuje management léčby pacientů s fibrilací síní tím, že nevyžaduje laboratorní kontroly, má prediktabilní farmakokinetiku, jednoduché dávkovací schéma bez nutnosti složité úpravy dávkování a nevykazuje interakce s potravou. Nicméně je třeba mít na paměti, že stále podáváme antikoagulans. Musíme proto přistupovat k indikaci této léčby s určitou rozvahou, znalostí renálních funkcí pacienta a stejně jako u každého antikoagulans si být vědomi, že nežádoucím účinkem může být krvácení. To však při dodržování indikačních kritérií, výše zmiňovaných výhodách a pečlivém klinickém sledování pacienta bude minimalizováno ve srovnání s dosud standardní léčbou warfarinem.
Klíčová slova:
dabigatran – fibrilace síní – tromboembolieÚvod
Fibrilace síní (FS) je nejčastější supraventrikulární arytmií, která postihuje minimálně 1–2 % populace, je spojena s vyšší mortalitou, zejména díky tromboembolickým (TE) komplikacím, z nichž nejčastější jsou cévní mozkové příhody (CMP). Pacienti s fibrilací síní jsou častěji hospitalizováni, mají nižší kvalitu života, sníženou zátěžovou kapacitu. Známý je také úzký vztah fibrilace síní a srdečního selhání [1]. Cílem moderní léčby fibrilace síní je především prevence tromboembolických komplikací na základě rizikové stratifikace pacienta, volba adekvátní léčebné strategie (kontrola rytmu, resp. kontrola frekvence), upstream terapie a tam, kde je indikováno, také provedení kauzální léčby arytmie pomocí katetrizační, resp. chirurgické ablace [2].
Poslední desetiletí je vyvíjena celá řada nových antitrombotik. Některá z nich, přestože byla již uvedena do klinické praxe, byla krátce nato z trhu stažena pro závažné nežádoucí účinky (např. ximelegatran). Proto také vývoj dalších molekul a jejich testování v klinických studiích fáze II a III a následné schválení FDA, resp. EMA trvalo poměrně dlouho. Patří sem přímé inhibitory trombinu, tzv. „gatrany“, a inhibitory faktoru X, tzv. „xabany“. V prevenci TE u FS byly jako první publikovány výsledky studie RE-LY [1], která ukázala příznivý efekt dabigatran-etexilátu, a zahájila tak zcela novou epochu antikoagulační léčby pacientů s nevalvulární fibrilací síní (FS), která je definována dle EPAR – Veřejné hodnotící zprávy léčivého přípravku Evropské unie, jako FS při absenci revmatické mitrální stenózy nebo náhrady srdeční chlopně) [3]. V recentně publikovaných Doporučeních pro léčbu fibrilace síní České kardiologické společnosti [4] má již dabigatran v indikaci prevence tromboembolických komplikací FS pevné místo. Od 1. 5. 2012 se stal dostupným pro nemocné ve výše uvedené indikaci v České republice, a to díky stanovení úhradového mechanizmu.
Výsledky studie RE-LY a jejich implementace do klinické praxe
Dabigatran-etexilát (dále jen „dabigatran“) (Pradaxa®, Boehringer Ingelheim) je reverzibilní přímý inhibitor trombinu. Je alternativním přípravkem k antagonistům vitaminu K (AVK), který však, díky jasné korelaci mezi plazmatickou koncentrací a stupněm jeho antikoagulačního účinku, nevyžaduje rutinní laboratorní kontrolu.
Účinnost dabigatranu byla hodnocena v rozsáhlém klinickém hodnocení fáze III RE-LY (Randomized evaluation of long term anticoagulant therapy) [5]. Bylo do ní zařazeno více než 18 000 pacientů a cílem bylo prokázat noninferioritu 2 zaslepeně podávaných dávek dabigatran-etexilátu (150 mg 2krát denně nebo 110 mg 2krát denně) vůči otevřeně podávanému warfarinu s cílem dosažení účinné antikoagulační léčby s rozmezím INR 2,0–3,0 z hlediska prevence cévní mozkové příhody a systémové embolie u pacientů s fibrilací síní a s nejméně jedním dalším rizikovým faktorem dle kritérií rizikové stratifikace [6]. Medián délky sledování pacientů ve studii byl 2 roky.
Primární sledovaným cílem účinnosti byl výskyt cévní mozkové příhody (CMP) a systémové embolie (SE). Dabigatran v dávce 150 mg 2krát denně byl superiorní vůči dobře kontrolovanému warfarinu (RR 0,65; 95% Cl 0,52–0,81; p = 0,001) – roční výskyt 1,11 % vs 1,71 % znamenal 35% redukci primárního endpointu. Dabigatran v dávce 110 mg 2krát denně byl srovnatelně účinný (noninferiorní) vůči dobře kontrolovanému warfarinu (RR 0,90; 95% Cl 0,74–1,10; p = 0,29) – roční výskyt 1,54 % vs 1,71 %.
Klinická prospěšnost podávání dabigatranu ve srovnání s warfarinem, pokud jde o prevenci cévní mozkové příhody a systémové embolie, je zachována napříč jednotlivými podskupinami, např. v podskupině s poruchou funkce ledvin, při současném užívání léků, jako jsou protidestičkové přípravky nebo inhibitory P-gp, a je nezávislá na věku, váze, pohlaví, etniku [6]. Konzistentní účinnost dabigatranu byla prokázána rovněž u všech pacientů bez ohledu na stupeň rizika CMP. I ve skupině s vysokým rizikem CMP/SE (CHADS2 3–6) byl dabigatran v dávce 150 mg 2krát denně účinnější než warfarin (RR 0,69; 95% Cl 0,51–0,93) [7].
Všech výsledků bylo dosaženo proti dobře kontrolovanému podávání warfarinu. Průměrná hodnota INR v požadovaném terapeutickém rozmezí INR 2,0–3,0 (hodnoceno stanovením procenta času každého centra v tomto rozmezí – cTTR) byla 64,4 %, medián TTR 67 %.
Primárním sledovaným cílem bezpečnosti podávání dabigatranu byl výskyt závažného krvácení. U dabigatranu v dávce 150 mg 2krát denně byl srovnatelný výskyt závažného krvácení vůči dobře kontrolovanému warfarinu (RR 0,93; 95% CI 0,81–1,07; p = 0,31) – roční výskyt 3,32 % vs 3,57 %. Dabigatran v dávce 110 mg 2krát denně signifikantně snížil výskyt závažného krvácení vůči dobře kontrolovanému warfarinu (RR 0,80; 95% CI 0,70–0,93; p = 0,003) – roční výskyt 2,87 % vs 3,57 %.
Zásadní pro klinickou praxi bylo významné snížení výskytu intrakraniálního krvácení, obávané komplikace léčby warfarinem, oběma dávkami dabigatranu: 150 mg 2krát denně – snížení relativního rizika o 59 % (RR 0,41; 95% CI, 0,28–0,60; p < 0,001; roční výskyt 0,32 % vs 0,76 %) a 110 mg 2krát denně snížení relativního rizika o 70 % (RR 0,30; 95% CI, 0,19–0,45; p < 0,001; roční výskyt 0,23 % vs 0,76 %).
Jedinci randomizovaní k podávání dabigatranu v obou dávkách měli výrazně nižší riziko všech krvácení a život ohrožujícího krvácení ve srovnání s warfarinem.
Shrnutí výsledků studie RE-LY pro klinickou praxi
Dabigatran je v dávce 150 mg 2krát denně účinnější a dabigatran v dávce 110 mg 2krát denně srovnatelně účinný v prevenci cévní mozkové příhody a systémové embolie proti standardní účinné léčbě warfarinem. Ve většině ostatních sledovaných parametrech je vyšší dávka dabigatranu účinnější a nižší dávka srovnatelně účinná nebo účinnější proti warfarinu. Obě dávky statisticky významně snižují výskyt hemoragických CMP proti standardní léčbě warfarinem. Dávka 150 mg 2krát denně zatím jako jediná z nových antikoagulans významně snižuje zároveň výskyt ischemických CMP, tedy největší riziko, pro které je antikoagulační léčba u pacientů s FS podávána. Dabigatran v dávce 150 mg 2krát denně byl srovnatelně bezpečný nebo bezpečnější a dabigatran v dávce 110 mg 2krát denně bezpečnější ve srovnání s warfarinem ve většině sledovaných parametrů. Obě dávky statisticky významně snížily výskyt obávaného intrakraniálního krvácení ve srovnání s warfarinem napříč všemi podskupinami pacientů.
Zásadní výsledky studie RE-LY jsou shrnuty v tab. 1.
Table 1. Závěry studie RE–LY. Klíčové závěry studie RE–LY [14]. ![Závěry studie RE–LY. Klíčové závěry studie RE–LY [14].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/be5b3e3a1b30d7fe1a53a5331fd66636.png)
Výsledky studie RE-LY vedly k tomu, že Evropská léková agentura 1. srpna 2011, po 50 letech terapie warfarinem, schválila dabigatran (Pradaxa®) pro klinickou praxi v Evropské unii jako první perorální antikoagulans pro pacienty s fibrilací síní [8]. Guidelines Americké společnosti hrudních lékařů (The American College of Chest Physicians – ACCP) o antitrombotické léčbě a prevenci trombózy (9. vydání) doporučují u pacientů s nevalvulární FS užívání dabigatranu v dávce 150 mg 2krát denně jako superiorní pro standardnímu podávání AVK [9].
Současné indikace léčby dabigatranem
Indikační kritéria pro prevenci tromboembolických příhod u nemocných s nevalvulární fibrilací síní fibrilací síní vycházejí ze vstupních a vylučovacích kritérií studie RE-LY. Podmínkou pro indikaci je přítomnost jednoho nebo více následujících rizikových faktorů:
- cévní mozková příhoda, tranzitorní ischemická ataka nebo systémová embolie v anamnéze,
- EF LK < 40 %,
- symptomatické srdeční selhání třídy II či vyšší dle klasifikace NYHA,
- věk ≥ 75 let,
- věk ≥ 65 let spojený s jedním z následujících onemocnění: diabetes mellitus, ischemická choroba srdeční nebo hypertenze.
Kromě těchto indikací uvedených v SPC dabigatranu [8] je nutno v každodenní klinické praxi respektovat indikační omezení daná plátci zdravotní péče. Přípravek může předepsat internista, kardiolog a neurolog v prevenci cévní mozkové příhody a systémové embolie u dospělých pacientů s nevalvulární FS indikovaných k antikoagulační léčbě při kontraindikaci warfarinu, tj.:
- nemožnosti pravidelných kontrol INR,
- nežádoucích účinků při léčbě warfarinem,
- nemožnosti udržet INR v terapeutickém rozmezí 2,0–3,0; tzn. 2 ze 6 měření nejsou v uvedeném terapeutickém rozmezí,
- předpokladu rezistence na warfarin, tj. nutnost podávat denní dávky více než 10 mg a dodržení výše uvedených indikačních kritérií dle SPC.
Kromě této indikace byl dabigatran již v roce 2008 schválen pro primární prevenci žilních tromboembolií u dospělých pacientů, kteří podstoupili elektivní operativní totální náhradu kyčelního nebo kolenního kloubu.
Doporučené dávkování dabigatranu u pacientů s FS v klinické praxi
Vyšší dávka 150 mg 2krát denně je indikována pro většinu pacientů z důvodu superiorní účinnosti. Nižší, bezpečnější dávku 110 mg 2krát denně mají užívat pacienti starší 80 let anebo ti, kteří současně užívají verapamil [10]. Nižší dávku je třeba zvážit na základě individuálního posouzení rizika tromboembolie nebo krvácení také u nemocných ve věku 75–80 let, u nemocných se středně závažnou poruchou funkce ledvin (clearance kreatininu 30–50 ml/min, tj. 0,5–0,83 ml/s), u pacientů s gastritidou, ezofagitidou nebo gastroezofageálním refluxem a u ostatních se zvýšeným rizikem krvácení. Před zahájením léčby dabigatranem by měla být zhodnocena funkce ledvin výpočtem clearance kreatininu (CrCl), aby byli z léčby vyloučeni pacienti s těžkou poruchou funkce ledvin (CrCl < 30 ml/min, resp. 0,5 ml/s), kdy je podávání dabigatranu kontraindikováno. U pacientů s poruchou funkce ledvin či starších 75 let je nutné kontrolovat funkci ledvin alespoň 1krát ročně a dále při všech stavech, kdy je předpoklad poklesu či zhoršení renálních funkcí (dehydratace, hypovolemie, septické stavy, chirurgické výkony apod.) [11]. Ve studii RE-LY byla pro výpočet CrCl používána metoda dle Cockgroft-Gaulta, nicméně volba metody záleží na zvyklostech každého pracoviště.
Schéma doporučeného dávkování s ohledem na renální funkce a rizika krvácení je shrnuto v tab. 2.
Table 2. Doporučené dávkování dabigatranu dle renálních funkcí a rizika krvácivých komplikací. Upraveno dle [14]. ![Doporučené dávkování dabigatranu dle renálních funkcí a rizika krvácivých komplikací. Upraveno dle [14].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/9d764ad935f92b4fe33d0b6692cb45c0.png)
Lékové interakce
Pro klinickou praxi musíme vzít v úvahu, že neléčíme nemocného pouze s fibrilací síní, ale i celou řadou konkomitantních onemocnění a s odpovídající komedikací. Z toho vyplývá nutnost zvažovat individualizovaně pro každého jedince potenciální lékové interakce. Dabigatran není metabolizován cestou CYP 450, a nejsou proto předpokládány související lékové interakce, přesto je nutno brát v úvahu veškerou medikaci, která zvyšuje, event. snižuje jeho plazmatickou koncentraci. Dabigatran je absolutně kontraindikován u pacientů užívajících dronedaron, systémově podávaný ketokonazol, takrolimus, cyklosporin a itrakonazol. Další molekuly, jejichž používání není doporučeno, resp. vyžaduje pečlivé klinické sledování, jsou uvedeny v tab. 3. V interní praxi je nutno věnovat pozornost zejména současnému používání nesteroidních antirevmatik, která zvyšují plazmatickou koncentraci dabigatranu až 50 %, a tím také zvyšují riziko krvácivých komplikací. To samé platí pro verapamil, kde zvýšení plazmatické koncentrace až o více než 100 % vede primárně k nutnosti podávat dabigatran pouze v nižší dávce, a to 2krát 110 mg denně [12,13].
Table 3. Dabigatran: lékové interakce. Upraveno dle [14] a [8]. ![Dabigatran: lékové interakce. Upraveno dle [14] a [8].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/a77cca455163af305c1598577905d0ba.png)
Bezpečný přechod z VKA na dabigatran a dabigatranu na VKA
V klinické praxi často narážíme na otázku, jak bezpečně přejít z warfarinu na dabigatran a obráceně. V zásadě je to velmi jednoduché. Je nutné monitorování INR, a pokud INR poklesne pod 2,0, je možno zahájit léčbu dabigatranem ve standardním schématu. Při přechodu z dabigatranu na warfarin je nutno vzít v úvahu renální funkce pacienta. Renální insuficience prodlužuje antikoagulační efekt dabigatranu. Proto při CrCl ≥ 50 ml/min (0,83 ml/s) zahájíme léčbu warfarinem 3 dny před vysazením dabigatranu a při CrCl ≥ 30–50 ml/min (0,5–0,83 ml/s) 2 dny před vysazením. Monitoring aktivovaného parciálního tromboplastinového času (aPTT) je vhodný u nemocných s renální insuficiencí při přechodu na VKA. Pokles aPTT na hodnoty blížící se normě indikuje možnost podání první dávky dabigatranu u těchto nemocných [14]. Další praktickou otázkou je přechod z parenterálních antikoagulancií na dabigatran. Zde se doporučuje podat první dávku dabigatranu 0–2 hod před další předpokládanou dávkou LMWH, u heparinu pak v době ukončení kontinuální infuzní léčby. Naopak při přechodu z dabigatranu na parenterální antikoagulancia je vhodné zahájit léčbu 12 hod po podání poslední dávky dabigatranu. Doporučení pro vzájemný přechod terapií jsou sumarizována v tab. 4.
Table 4. Doporučení pro konverzi léčby z warfarinu na dabigatran a z dabigatranu na warfarin. Upraveno dle [14]. ![Doporučení pro konverzi léčby z warfarinu na dabigatran a z dabigatranu na warfarin. Upraveno dle [14].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/63db0d786e485ebcb683e82f7f20ec43.png)
Monitorování léčby dabigatranem
Na rozdíl od warfarinu není nutné rutinní laboratorní monitorování. V praxi se opakovaně setkáváme se zasíláním vyšetření do laboratoře, aniž je k tomu nějaké racionále. Monitoring efektu léčby je však možný a může být prospěšný např. v případech podezření na předávkování, při závažném krvácení, nutnosti akutního chirurgického výkonu či k identifikaci pacientů se zvýšeným rizikem krvácení způsobeným nadměrnou expozicí vůči dabigatranu; podezření nebo známá interakce s jinými léky. Základním orientačním testem je aktivovaný parciální tromboplastinový čas (aPTT), který je běžně dostupný ve všech laboratořích a jeho prodloužení > 80 s nebo 2násobek horní hranice normálních hodnot (měřeno před podáním další dávky) při dávkování 150 mg 2krát denně je markerem zvýšeného rizika krvácení [8,14]. Řada laboratoří zavedla již měření dilutovaného trombinového času (Hemoclot®, HYPHEN BioMed, Neuville-sur-Oise, Francie) se stanovením kvantitativní hladiny dabigatranu v plazmě. Koncentrace dabigatranu v plazmě nad 200 ng/ml (asi 65 s) při podávání 150 mg 2krát denně je spojena se zvýšeným rizikem krvácení [8,15,16]. Vyšetření by měla být zásadně prováděna ráno před podáním další dávky, tedy v době předpokládané minimální koncentrace dabigatranu. Naopak normální hodnoty aPTT a trombinového času znamenají, že není klinický významný antikogulační účinek dabigatranu. Dalšími možnými markery jsou pro kvalitativní hodnocení ekarinový čas (ECT) a trombinový čas (TT). Ten je sice citlivým testem k měření antikoagulačního účinku dabigatranu, nicméně výsledky jsou závislé na použitém koagulometru, a proto nelze poskytnout referenční hodnoty. Pouze v případě normálních hodnot TT lze konstatovat, že není přítomen klinicky významný účinek dabigatranu. Protrombinový čas a INR mohou být falešně pozitivní a neměly by být vůbec prováděny. Možnosti monitorování léčby dabigatranem jsou uvedeny v tab. 5.
Table 5. Možnosti monitorace léčby dabigatranem [8]. ![Možnosti monitorace léčby dabigatranem [8].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/566a52ce8f4dfec08d9b7a9260fcde17.png)
Management pacientů léčených dabigatranem indikovaných k chirurgickým výkonům
Dočasné přerušení léčby dabigatranem je většinou indikováno u nemocných, kteří podstupují chirurgické výkony. Základním hlediskem, jak dlouho před výkonem je nutné léčbu přerušit, je vždy jeho urgentnost, riziko krvácení spojené s konkrétním výkonem a aktuální renální funkce pacienta.
Plánové chirurgické výkony
U plánovaných chirurgických výkonů vycházíme z rizika krvácení při konkrétních operacích a invazivních výkonech (tab. 6) a dále dobu přerušení léčby dabigatranem volíme dle renálních funkcí (tab. 7). Z důvodu rychlého nástupu i odeznění účinku není pro většinu výkonů nutná překlenovací léčba, event. je možno orientovat se dle koagulačních testů (aPTT, Hemoclot). Zahájení léčby po výkonu doporučujeme co nejdříve, poté co je dosaženo plné hemostatické funkce.
Table 6. Stratifikace rizika krvácení chirurgických a intervenčních výkonů. 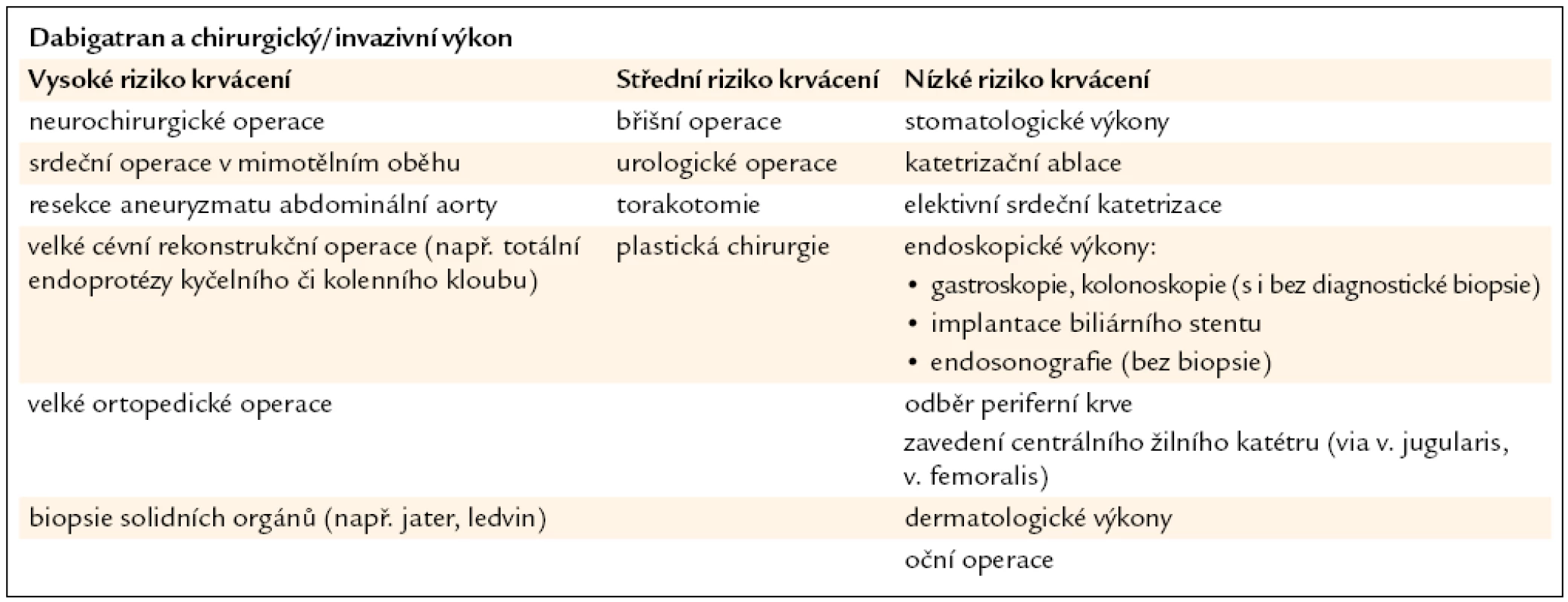
Table 7. Dočasné přerušení léčby dabigatranem dle renálních funkcí a závažnosti u plánovaných chirurgických nebo invazivních výkonů [8]. ![Dočasné přerušení léčby dabigatranem dle renálních funkcí a závažnosti u plánovaných chirurgických nebo invazivních výkonů [8].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/2b17148e22f8f9eb3446583a8c0a9f7b.png)
Akutní chirurgické výkony
U pacientů s indikací urgentních či semiurgentních výkonů (2–12 hod po poslední dávce dabigatranu) je vždy nutno pečlivě zvažovat riziko krvácení proti benefitu chirurgického výkonu. Ideálně výkon doporučujeme odložit o 12 hod od poslední dávky dabigatranu za monitoringu aPTT, resp. Hemoclot testu. Toto však není vždy možné. U výkonů z vitální indikace, které musí být realizovány bezprostředně, je předpoklad krvácivých komplikací. Pokud je možno, indikujeme hemodialýzu nebo hemoperfuzi přes aktivní uhlí ke snížení plazmatické koncentrace dabigatranu [17].
Reinicializace léčby dabigatranem po chirurgickém výkonu závisí na typu výkonu, stavu hemostázy pacienta a urgentnosti profylaxe tromboembolických komplikací. Pokud je hemostáza dostatečná, zahajujeme terapii 1 tobolkou 150, resp. 110 mg v závislosti na doporučené dávce a renálních funkcích 4 hod po výkonu. V následujících dnech pak již dávkujeme standardně 2krát denně. Pozor však na aktuální vývoj renálních funkcí, kde náhlé snížení může vést k výraznému a prolongovanému zvýšení plazmatické hladiny dabigatranu. Proto doporučujeme pečlivé sledování urey, kreatininu, resp. clearance kreatininu a event. monitorování léčby dabigatranem pomocí aPTT nebo Hemoclotu v pooperačním období a individualizaci dávkování dle aktuálních výsledků [8,14].
Je možné provést trombolytickou léčbu u pacientů s akutní ischemickou cévní mozkovou příhodou, kteří užívají dabigatran?
V léčbě akutních ischemických cévních mozkových příhod (CMP) je čas zahájení léčby výrazně kratší než např. u akutního infarktu myokardu. V případě akutní ischemické CMP musí být fibrinolytická léčba zahájena do 4,5 hod od vzniku příznaků, a to po vyloučení intrakraniálního krvácení. Pokud kvantitativní testy pro léčbu dabigatranem výrazně nepřesahují horní hranice referenčních hodnot, lze zvážit užití fibrinolytik. Pokud je aPTT delší než 80 s, resp. dilutovaný tromboplastinový čas delší než 65 s, pak je riziko závažné krvácivé komplikace zvýšeno a podání trombolytik nedoporučujeme. V této oblasti zatím není k dispozici dostatek informací [18–20].
Management krvácivých komplikací
V současné době musíme vycházet ze skutečnosti, že neexistuje specifické antidotum dabigatranu ani rivaroxabanu či apixabanu. Specifické protilátky jsou ve vývoji, byly prezentovány první výsledky studií [21,22], jejich rutinní použití v klinice lze očekávat v průběhu několika let. Výhodou oproti warfarinu je velmi krátký plazmatický poločas dabigatranu 12–14 hod. V případě krvácivé komplikace platí samozřejmě nutnost okamžitého přerušení léčby dabigatranem a identifikace zdroje krvácení. Protože dabigatran je vylučován převážně renální cestou, je nutné zajistit dostatečnou diurézu a protekci ledvin. Dále je doporučena standardní chirurgická či endoskopická hemostáza a podání volumexpanderů, plazmy či plné krve. V případě závažného krvácení zvažujeme podání obecných hemostatických agens, jako např. rekombinantního faktoru VIIa, nebo koagulačních faktorů II, IX nebo X, event. koncentrát protrombinového komplexu s cílem minimalizovat antikoagulační aktivitu dabigatranu a krvácivé projevy [23,24].
Postup a léčba krvácivých komplikací jsou uvedeny v tab. 8.
Table 8. Doporučené postupy v případě krvácení při léčbě dabigatranem. rFVIIa – rekombinantní aktivovaný faktor VII, PCC – koncentrát protrombinového komplexu. 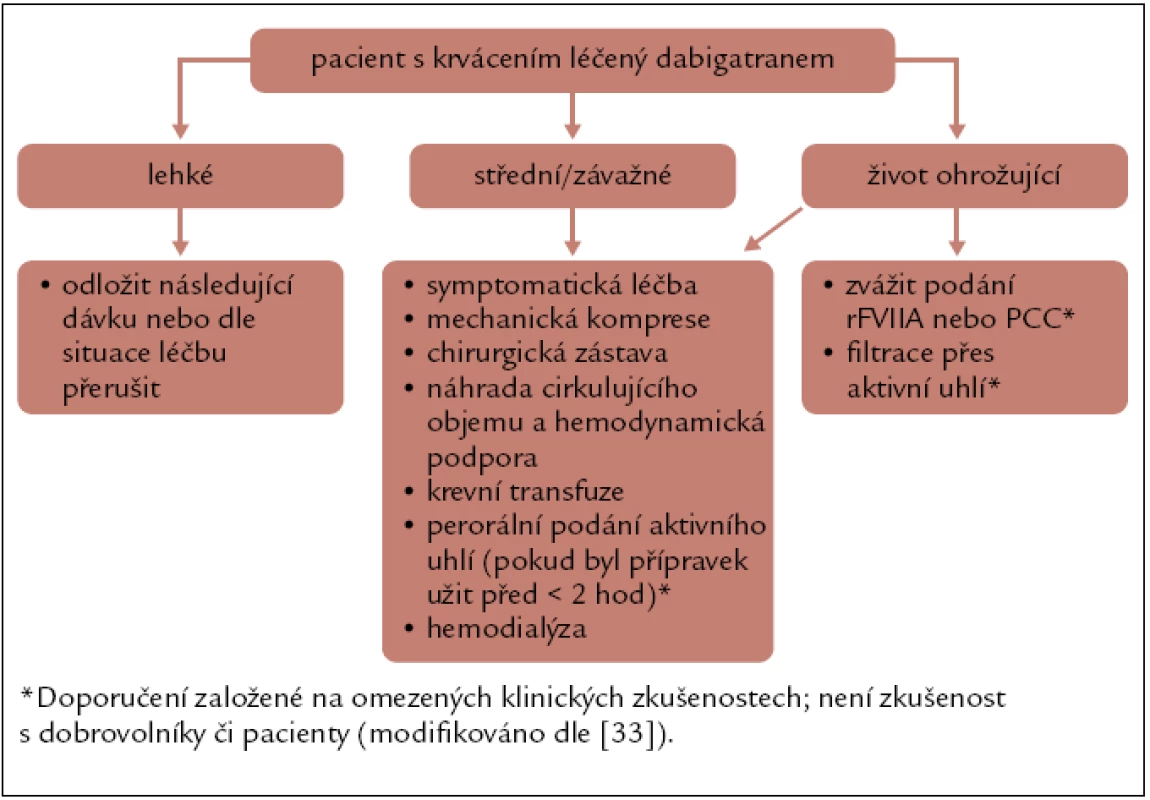
Dabigatran ve speciálních situacích
Akutní koronární syndromy, doporučení pro antitrombotickou léčbu po PCI u nemocných s FS léčených dabigatranem
Často diskutovanou otázkou je, zda léčba dabigatranem nevede ke zvýšení incidence akutních koronárních příhod u takto léčených pacientů. Ve studii RE-LY byl pozorován nesignifikantní nárůst rizika akutního infarktu myokardu (AIM) pro obě dávky dabigatranu a celkově byl výskyt AIM velmi nízký. 30 % sledované populace mělo při vstupu do studie ischemickou chorobu srdeční a v souhrnu údajů o přípravku (SPC) dabigatranu je přímo doporučováno jeho podání u této skupiny pacientů. Recentně publikovaná subanalýza všech akutních koronárních příhod studie RE-LY potvrdila, že dabigatran ve sledovaných dávkách 2krát 150 mg, resp. 2krát 110 mg nevedl k signifikantnímu nárůstu akutního infarktu myokardu ani jiných forem ischemické choroby srdeční (ICHS). Riziko vzniku AIM bylo stejné pro jedince jak s nízkým, tak vysokým rizikem ischemické příhody [24]. Důležité je, že celková a vaskulární mortalita byla nižší u dabigatranu, přičemž pro dávku 150 mg 2krát denně bylo snížení vaskulární mortality statisticky významné [7,8,25]. Je možno uzavřít, že léčba dabigatranem převyšuje svými benefity riziko AIM u naprosté většiny pacientů.
Důležitá je otázka prevence trombotických komplikací po provedené koronární angioplastice.
V rámci koronární intervence se nedoporučuje použití drug eluting stentů s nutností 12měsíční kombinační terapie, pokud není nezbytně nutné. Zatímco u warfarinu byla donedávna standardem u pacientů s FS po PCI tzv. trojitá terapie (warfarin, kyselina acetylsalicylová a clopidogrel), je u nových antitrombotik (prasugrel a ticagrelor), která jsou dnes v indikační třídě IA, naprostý nedostatek informací. Data pro současné podávání protidestičkové léčby (ASA nebo clopidogrel) a dabigatranu u pacientů s FS pocházejí ze studie RE-LY, kde bylo pozorováno, že současné podávání přibližně zdvojnásobuje riziko krvácení jak u dabigatranu, tak u warfarinu a nejvýhodnější je podání nižší dávky dabigatranu [8,16].
Nedávno publikovaná stanoviska Pracovní skupiny pro trombózu Evropské kardiologické společnosti nedávají zatím jednoznačné stanovisko ke kombinaci dabigatranu a standardních perorálních antitrombotik [26].
Kardioverze FS u nemocných léčených dabigatranem
Stávající doporučení ČKS pro léčbu FS [4] jasně hovoří o nutnosti minimálně 3týdenní antikoagulační léčby warfarinem před provedením kardioverze u nemocných s evidencí FS > 48 hod a následné léčbě minimálně 4 týdny po kardioverzi. Alternativně může být použito schéma s provedením jícnové echokardiografie (TEE) k vyloučení trombu v oušku levé síně. Navzdory skutečnosti, že při léčbě dabigatranem je dosaženo účinné antikoagulace již za 2 hod po podání léku, nelze pro nedostatek údajů provést kardioverzi dříve než za 3 týdny ve shodě s platnými guidelines.
Subanalýza studie RE-LY prokázala, že účinná léčba dabigatranem může být alternativou podávání warfarinu. 30denní výskyt CMP nebo systémové embolizace u 1 270 pacientů, kteří v průběhu studie podstoupili kardioverzi, byl 0,6 % u warfarinu a 0,8 % pro dabigatran 2krát 150 mg, resp. 0,3 % pro dabigatran 2krát 110 mg [27]. Pro klinickou praxi je důležité, že pokud pacient užívá dabigatran a podstupuje kardioverzi, není nutné léčbu přerušovat.
Katetrizační ablace FS a léčba dabigatranem
Současná guidelines ESC doporučují antikoagulační léčbu minimálně 3 měsíce po provedení katetrizační ablace FS, doporučení ČKS pak uvádějí interval 2–6 měsíců po výkonu. Přesto, že na letošním sjezdu Americké arytmologické společnosti (HRS) byla prezentována cela řada abstrakt o provedení ablace při nepřerušené léčbě dabigatranem, resp. zahájení léčby dabigatranem bezprostředně po provedení ablace, není v současné době pro tuto indikaci dostatek informací a nelze ji rutinně doporučit. Zvážení léčby dabigatranem po ablaci je individuální a mělo by být řízeno především mírou rizika tromboembolie [28].
Dabigatran u nemocných s mechanickou chlopenní náhradou
V současné době není možno doporučit užívání dabigatranu u nemocných s mechanickou chlopenní náhradou jak v aortální, tak v mitrální pozici pro nedostatek důkazů, protože tito nemocní byli vyloučeni ze studie RE-LY. K dispozici jsou výsledky studií in vitro [29,30]. Probíhá studie fáze II (Re-ALIGN trial), která zkoumá účinnost dabigatranu na prevenci komplikací, a to v dávkách 2krát 150, 220 a 300 denně [31].
Nežádoucí účinky při léčbě dabigatranem
K nejčastějším nežádoucím účinkům v klinické praxi i ve studii RE-LY patří dyspeptické obtíže, které se vyskytují u 5–10 % pacientů léčených dabigatranem [5]. Jsou charakterizovány jako bolesti žaludku, břicha, dyspepsie či břišní dyskomfort. Vyskytují se typicky více u žen než u mužů. V praxi se osvědčila jednoduchá opatření, a to podání dabigartanu s jídlem, zapití dostatečným množstvím tekutin, event. podání inhibitorů protonové pumpy (PPI), které je možné.
Management krvácivých komplikací je shrnut výše.
Praktické aspekty léčby
Při rozvaze o zahájení léčby dabigatranem je vždy nutno pečlivě zvažovat indikace a dostatečně edukovat pacienta o tom, proč mu byla předepsána antikoagulační léčba a o rizicích spojených s nedodržováním předepsaného dávkování. Podávání 2krát denně je zárukou vyrovnané účinnosti a bezpečnosti dabigatranu. Compliance pacientů k léčbě by měla zůstat zachována, protože většina z nich užívá medikaci 2krát a vícekrát denně. Pacient by měl být rovněž poučen o možných, zejména krvácivých komplikacích, a jak se zachovat, pokud nastanou. K edukaci slouží volně dostupné edukační materiály.
Každý nemocný by měl být také vybaven kartou o léčbě dabigatranem a kontaktem na ošetřujícího lékaře. U všech pacientů by měla před zahájením léčby být provedena clearance kreatininu tak, aby byli vyloučeni z léčby nemocní s těžkou poruchou renálních funkcí. Dále by pak měla následovat kontrola renálních funkcí minimálně 1krát ročně u pacientů nad 75 let, s poruchou funkce ledvin a vždy při zásadní změně zdravotního stavu.
Pokud se event. vyskytne krvácivá komplikace, je nutno hlásit tuto komplikaci léčby standardní cestou Oddělení farmakovigilance SÚKL [32]. Analýzou dat těchto nemocných lze předejít dalším komplikacím.
Dostatečná komunikace s pacientem, dodržování SPC a pečlivé klinické sledování nemocného pak minimalizují nežádoucí účinky i potenciální závažné komplikace léčby.
Závěr
Do současné doby standardní antikoagulační terapie warfarinem jako prevence tromboembolických komplikací u pacientů s fibrilací síní je spojena s řadou obtíží a komplikací, které snižují nejen její účinnost, ale i bezpečnost. Z důvodu úzkého terapeutického rozmezí je třeba monitorovat INR a udržovat jej v intervalu mezi 2,0–3,0 tak, aby nedošlo ke vzniku CMP (při hodnotách pod 2) nebo naopak ke krvácivým komplikacím – obávané intrakraniální krvácení (při hodnotách nad 3). Uspokojivou kompenzaci INR ovlivňuje mnoho faktorů – genetické faktory, individuální odpověď léčeného (variabilita), komorbidity, komedikace (včetně volně prodejných přípravků – zejména nesteroidních antirevmatik), strava, složité dávkovací schéma, sociální prostředí. Tuto složitost léčby warfarinem potvrzuje celá řada publikací, které prokazují, že přibližně 50 % léčených není uspokojivě kompenzováno a obdobné procento pacientů s FS warfarin vůbec nedostává.
Dabigatran představuje první prezentovanou léčivou látku, která se ve studii RE-LY prokázala v dávce 150 mg 2krát denně jako účinnější v prevenci CMP a systémové embolizace a srovnatelně bezpečná nebo bezpečnější ve srovnání s dobře kontrolovaným warfarinem. Dávka 110 mg 2krát denně prokázala srovnatelnou účinnost, ale superiorní bezpečnost. Klíčové a ojedinělé ve spektru moderních antikoagulancií je signifikantní snížení jak ischemických, tak krvácivých CMP v dávkování 150 mg 2krát denně. Tedy zásadní ukazatele, které by měli být rozhodující pro podání antikoagulační léčby u pacientů s fibrilací síní. Mělo by být podáno nejúčinnější antikagulans v prevenci ischemických iktů, které současně minimalizuje riziko krvácení, zejména obávaného intrakraniálního.
Dabigatran navíc zásadním způsobem usnadňuje management léčby pacientů s fibrilací síní tím, že nevyžaduje laboratorní kontroly, má prediktabilní farmakokinetiku, jednoduché dávkovací schéma bez nutnosti složité úpravy dávkování, má minimum lékových interakcí a nevykazuje interakce s potravou. Zároveň vzhledem k různé rizikovosti pacientů s fibrilací síní, z důvodu dalších komorbidit a medikace se v klinické praxi ukazuje jako výhoda možnost volby 2 dávek dabigatranu. Nicméně je třeba mít na paměti, že stále podáváme antikoagulans. Musíme proto přistupovat k indikaci této léčby s určitou rozvahou, znalostí renálních funkcí pacienta a stejně jako u každého antikoagulans si být vědomi, že nežádoucím účinkem může být krvácení, které ale při dodržování indikačních kritérií, výše zmiňovaných výhodách a pečlivém klinickém sledování pacienta bude minimalizováno ve srovnání s dosud standardní léčbou warfarinem. Přesvědčivé výsledky studie RE-LY jsou již potvrzovány v každodenní klinické praxi, kdy dabigatran užívá jako prevenci CMP celosvětově více než 1 000 000 pacientů s fibrilací síní. Pevně věřím, že dabigatran-etexilát (Pradaxa®) je budoucnost, která zkvalitní a usnadní antikoagulační léčbu od úrovně internistů, kardiologů, neurologů, praktických lékařů až po specializovaná centra zabývající se komplexním řešením fibrilace síní a tromboembolických komplikací.
doc. MUDr. Miloš Táborský, Ph.D., FESC, MBA
www.fnol.cz
e-mail: milos.taborsky@fnol.cz
Doručeno do redakce: 9. 8. 2012
Přijato po recenzi: 20. 8. 2012
Sources
1. DeWilde S, Carey IM, Emmas C et al. Trends in the prevalence of diagnosed atrial fibrillation, its treatment with anticoagulation and predictors of such treatment in UK primary care. Heart 2006; 92 : 1064–1070.
2. Camm AJ, Kirchhof P, Lip GY et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010; 31 : 2369–2429.
3. European Medicines Agency. Science Medicines Health. Pradaxa – dabigatran etexilate. Available from: http://www.emea.europa.eu/docs/en_GB/document_library/EPAR_-_Summary_for_the_public/human/000829/WC500041060.pdf.
4. Čihák R, Heinc P, Haman L et al. Doporučený postup ČKS pro léčbu fibrilace síní. Cor Vasa 2011; 53 (Suppl 1): 27–52.
5. Connolly SJ, Ezekowitz MD, Yusuf S et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009; 361 : 1139–1151.
6. Lip GY, Frison L, Halperin JL et al. Identifying patients at high risk of stroke despite anticoagulation: a comparison of contemporary stroke risk stratification schemes in an anticoagulated atrial fibrillation cohort. Stroke 2010; 41 : 2731–2738.
7. Connolly SJ, Ezekowitz MD, Yusuf S et al. Newly identified events in the RE-LY trial. N Engl J Med 2010; 363 : 1875–1876.
8. European Medicines Agency. Science Medicines Health. Pradaxa – dabigatran etexilate. Available from: http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/000829/human_med_000981.sjsp&jsenabled=true.
9. You JJ, Singer D, Howard PA et al. Antithrombotic therapy for atrial fibrillation: antithrombotic therapy and prevention of thrombosis, 9th ed. American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141 (Suppl 2): e531S–e575S.
10. Státní ústav pro kontrolu léčiv. Pradaxa. Dostupné z: http://www.sukl.cz/modules/medication/detail.php?code=0168373&tab=prices.
11. Blech S, Ebner T, Ludwig-Schwellinger E et al. The metabolism and disposition of the oral direct thrombin inhibitor, dabigatran, in humans. Drug Metab Dispos 2008; 36 : 386–399.
12. Reilly PA, Conrad CA, Faaij RA et al. Concomitant use of P-glycoprotein inhibitors with dabigatran or warfarin in the RE-LY trial. Eur Heart J 2011; 32 (Suppl 1): 6. Abstract 129.
13. Brunet A, Hermabessiere S, Benain X. Pharmacokinetic and pharmacodynamic interaction of dronedarone and dabigatran in healthy subjects. Eur Heart J 2011; 32 (Suppl 1): 618–619. Abstract P3566.
14. Huisman MV, Lip GY, Diener HC et al. Dabigatran etexilate for stroke prevention in patients with atrial fibrillation: resolving uncertainties in routine practice. Thromb Haemost 2012; 107 : 838–847.
15. Oldgren J, Alings M, Darius H et al. Risks for stroke, bleeding, and death in patients with atrial fibrillation receiving dabigatran or warfarin in relation to the CHADS2 score: a subgroup analysis of the RE-LY trial. Ann Intern Med 2011; 155 : 660–667.
16. Eikelboom J, Wallentin L, Connolly SJ et al. Risk of bleeding with 2 doses of dabigatran compared with warfarin in older and younger patients with atrial fibrillation: an analysis of the randomized evaluation of long-term anticoagulant therapy (RE-LY) trial. Circulation 2011; 123 : 2363–2372.
17. van Ryn J, Neubauer M, Flieg R et al. Successful removal of dabigatran in flowing blood with an activated charcoal hemoperfusion column in an in vitro test system. Pathophysiol Haemost Thromb 2010; 57 (Suppl 1): A94. Abstract P485.
18. Adams HP Jr, del Zoppo G, Alberts MJ et al. Guidelines for the early management of adults with ischemic stroke: a guideline from the American Heart Association/ American Stroke Association Stroke Council, Clinical Cardiology Council, Cardiovascular Radiology and Intervention Council, and the Atherosclerotic Peripheral Vascular Disease and Quality of Care Outcomes in Research Interdisciplinary Working Groups: The American Academy of Neurology affirms the value of this guideline as an educational tool for neurologists. Circulation 2007; 115: e478–e534.
19. De Smedt A, De Raedt S, Nieboer K et al. Intravenous thrombolysis with recombinant tissue plasminogen activator in a stroke patient treated with dabigatran. Cerebrovasc Dis 2010; 30 : 533–534.
20. Matute MC, Guillán M, García-Caldentey J et al. Thrombolysis treatment for acute ischaemic stroke in a patient on treatment with dabigatran. Thromb Haemost 2011; 106 : 178–179.
21. van Ryn J, Litzenburger T, Waterman A et al. Dabigatran anticoagulant activity is neutralized by an antibody selective to dabigatran in in vitro and in vivo models free. J Am Coll Cardiol 2011; 57 (Suppl 1): E1130.
22. Lu G, Deguzman FR, Karbarz MJ et al. Reversal of rivaroxaban mediated anticoagulation in animal models by a recombinant antidote protein (r-Antidote, PRT064445). Eur Heart J 2011; 32 : 640–641. Abstract 3712.
23. Eerenberg ES, Kamphuisen PW, Sijpkens MK et al. Reversal of rivaroxaban and dabigatran by prothrombin complex concentrate: a randomized, placebo-controlled, crossover study in healthy subjects. Circulation 2011; 124 : 1573–1579.
24. Uchino K, Hernandez AV. Dabigatran association with higher risk of acute coronary events: meta-analysis of noninferiority randomized controlled trials. Arch Intern Med 2012; 172 : 397–402.
25. Hohnloser SH, Oldgren J, Yang S et al. Myocardial ischemic events in patients with atrial fibrillation treated with dabigatran or warfarin in the RE-LY trial. Circulation 2012; 125 : 669–676.
26. Da Caterina R, Husted S, Wallentin L et al. New oral anticoagulans in atrial fibrillation and acute coronary syndromes: ESC Working Group on Thrombosis-Task Force on Anticoagulants in Heart Disease position paper. J Am Coll Cardiol 2012; 59 : 1413–1425.
27. Nagarakanti R, Ezekowitz MD, Oldgren J et al. Dabigatran versus warfarin in patients with atrial fibrillation: an analysis of patients undergoing cardioversion. Circulation 2011; 123 : 131–136.
28. Winkle RA, Mead RH, Engel G et al. The use of dabigatran immediately after atrial fibrillation ablation. J Cardiovasc Electrophysiol 2012; 23 : 264–268.
29. Maegdefessel L, Linde T, Krapiec F et al. In vitro comparison of dabigatran, unfractionated heparin, and low-molecular-weight heparin in preventing trombus formation on mechanical heart valves. Thromb Res 2010; 126: e196–e200.
30. McKellar SH, Abel S, Camp CL et al. Effectiveness of dabigatran etexilate for thromboprophylaxis of mechanical heart valves. J Thorac Cardiovasc Surg 2011; 141 : 1410–1416.
31. RE-ALIGN: A randomised, phase II study to evaluate the safety of oral dabigatran etexilate in patients after heart valve replacement. Available from: NCT01452347. www.clinicaltrials.gov.
32. O lécích.cz. Hlášení pro SÚKL. Dostupné z: http://www.olecich.cz/hlaseni-pro-sukl/nahlasit-nezadouci-ucinek.
33. van Ryn J, Stangier J, Haertter S et al. Dabigatran etexilate – a novel, reversible, oral direct thrombin inhibitor: interpretation of coagulation assays and reversal of anticoagulant activity. Thromb Haemost 2010; 103 : 1116–1127.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2012 Issue 10-
All articles in this issue
- Akutní infarkt myokardu u mladých – stala se někde chyba? – editorial
- Méně invazivní kardiochirurgické přístupy pro léčbu ischemické choroby srdeční – editorial
- Viscerální leishmanióza – editorial
- Festina lente! – editorial
- Akutní infarkt myokardu u mladých nemocných – závažné nedostatky v systému akutní a následné péče
- Existuje vzťah medzi zápalovými markermi, oxidačným stresom a pooperačnou fibriláciou predsiení?
- Diagnostika, prognostické faktory a léčba sarkoidózy – retrospektivní analýza
- Fyziologická úloha vitaminu C ve vztahu ke složkám imunitního systému
- Hypoglykemie – fenomén, nad kterým moderní diabetologie pomalu vítězí
- AII antagonisté (candesartan a irbesartan) v léčbě kardiovaskulárních onemocnění
- Febrilní pancytopenie a hepatosplenomegalie jako hlavní symptomy viscerální leishmaniózy
- Vysoké podezření na ICHS získané anamnézou nesmí vyvrátit negativita některých objektivních vyšetřovacích metod – zkušenost ambulantního internisty
- Dabigatran-etexilát v klinické praxi pro prevenci tromboembolických příhod u nemocných s fibrilací síní
- Efekt ivabradinu na tepovou frekvenci, vývoj funkce levé komory a koncentraci NT-proBNP u pacientů se systolickým chronickým srdečním selháním – příklady z praxe
- Diagnostické a léčebné postupy u arteriální hypertenze – verze 2012. Doporučení České společnosti pro hypertenzi
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Fyziologická úloha vitaminu C ve vztahu ke složkám imunitního systému
- Diagnostika, prognostické faktory a léčba sarkoidózy – retrospektivní analýza
- Akutní infarkt myokardu u mladých nemocných – závažné nedostatky v systému akutní a následné péče
- Febrilní pancytopenie a hepatosplenomegalie jako hlavní symptomy viscerální leishmaniózy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

