-
Medical journals
- Career
Kazuistika mladého pacienta s konstriktivní perikarditidou se subakutním průběhem
: M. Plachý 1; J. Špác 1; M. Souček 1; O. Hlinomaz 2; V. Feitová 3
: II. interní klinika Lékařské fakulty MU a FN u sv. Anny Brno, přednosta prof. MU Dr. Miroslav Souček, CSc., 2I. interní kardio‑angiologická klinika Lékařské fakulty MU a FN u sv. Anny Brno, přednosta prof. MU Dr. Jiří Vítovec, CSc., FESC, 3Klinika zobrazo 1
: Vnitř Lék 2010; 56(2): 149-153
: Case Reports
Chronická konstriktivní perikarditida je onemocnění postihující osrdečník, který ztrácí svou elasticitu, stává se tuhým a omezuje plnění srdečních komor. Nejčastěji se konstriktivní perikarditida rozvíjí po proběhlé akutní perikarditidě, typický je dlouhotrvající asymptomatické stadium s následným rozvojem pravostranného městnání a známek nízkého srdečního výdeje. Kazuistika popisuje případ 33letého pacienta, u něhož se po akutní idiopatické perikarditidě následně v krátké době 1 měsíce rozvinula perikardiální konstrikce s těžkým srdečním selháním, tvorbou otoků a pleurálních výpotků. Zprvu se na tuto diagnózu nemyslelo, diferenciální diagnostika se zaměřovala na primárně plicní postižení nebo autoimunitní onemocnění. Po odhalení pravé příčiny byla pacientovi provedena perikardektomie s následným dobrým efektem a úplnou úpravou stavu. Etiologie konstriktivní perikarditidy nebyla objasněna. Konstriktivní perikarditida je onemocnění v Evropě relativně vzácné, zvláště pak u mladých pacientů. Stanovení diagnózy a zavedení léčby je potřeba provést co nejdříve, abychom zamezili nárůstu operačního rizika a zvýšené pravděpodobnosti pooperačních diastolických abnormalit.
Klíčová slova:
konstriktivní perikarditida – idiopatická perikarditida – echokardiografie – pravostranná srdeční katetrizace s tonometriíÚvod
Perikard je dvouvrstevná membrána, která obepíná srdce, za normálních okolností podporuje vzájemnou interakci obou komor a vyvažuje jejich srdeční výdej. Perikardiální vak se vyznačuje nízkou poddajností, je schopen pojmout jen malé množství tekutiny do 250 ml, jeho další rozepjetí je spojeno se strmým nárůstem intraperikárdiálního tlaku. Patologické zvýšení intraperikardiálního tlaku pak omezuje diastolické plnění komor, a snižuje tím srdeční výdej [1]. Konstriktivní perikarditida (KP) vzniká v přítomnosti zesíleného, jizevnatého a v některých případech i kalcifikovaného perikardu, který navzdory vysokým plnicím tlakům omezuje diastolickou náplň komor [2]. Charakterickým znakem je ekvalizace diastolických tlaků ve všech čtyřech srdečních dutinách. Časná fáze diastolického plnění není narušena, avšak jakmile komory rozepjetím narazí na ztluštělý perikard, je další plnění náhle zastaveno, což odpovídá charakteristickému dip plateau na tlakové křivce z obou komor. KP často začíná iniciální epizodou akutní perikarditidy, která pak přechází do subakutní fáze organizace a resorpce perikardiálního výpotku. Po této fázi následuje chronické jizevnatění a fibrotizace perikardu s ukládáním kalcia [3]. V minulosti za většinou případů tohoto onemocnění stála tuberkulóza, v současné době je častou příčinou KP už jen v rozvojových zemích. V Evropě je toto onemocnění relativně vzácné, etiologie je v převážné většině povirová nebo se vyvolávající faktor nepodaří zjistit, tj. idiopatická. Dále se může rozvinout po kardiochirurgických operacích, po radioterapii mediastina [4].
Popis případu
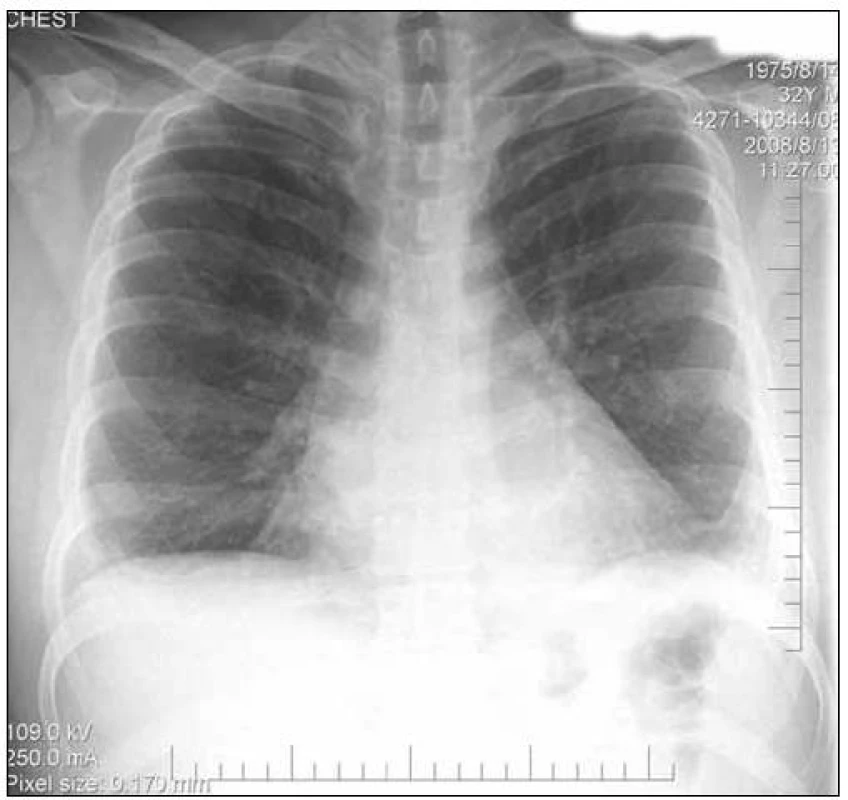
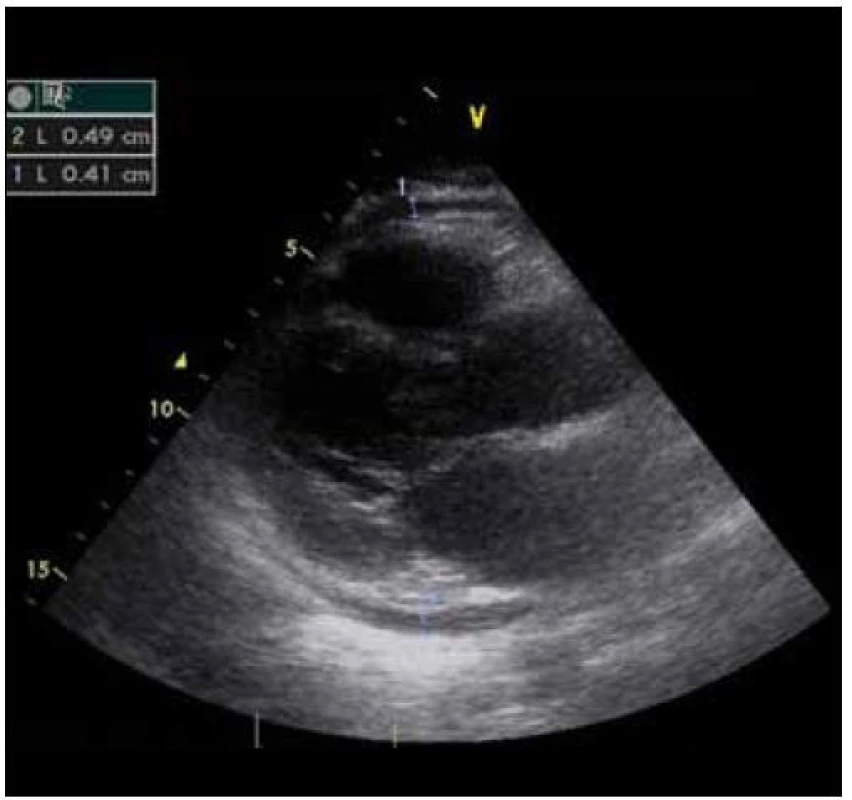
Kazuistika popisuje případ 33letého muže, aktivního sportovce, jehož velkým koníčkem bylo horolezectví. Dosud se pro nic neléčil, jen v roce 2005 při pobytu v Kirgizstánu prodělal vysokohorskou nemoc, po návratu přechodně kašlal, vyšetřen u lékaře však nebyl. Alergický na nic není, nekouří a nepije alkohol. Do té doby žádné léky trvale neužíval. Pracuje jako softwarový specialista. V srpnu roku 2008 byl praktickým lékařem odeslán k hospitalizaci na kardiologické pracoviště s podezřením na perikarditidu (echokardiograficky zjištěna přítomnost nevýznamného množství perikardiální tekutiny s jinak normální srdeční funkcí). Pacient udával zhoršující se námahovou dušnost trvající asi 2 měsíce, suchý dráždivý kašel, dále bodavé bolesti na hrudi v oblasti pod mečíkem, zejména při chůzi do kopce. Rychle se unaví, pozoroval intermitentně i průjmy. V létě roku 2008 byl očkován proti klíšťové encefalitidě, jinak virózu neprodělal, teploty neměl. Při fyzikálním vyšetření dominovala sinusová tachykardie, TF 104/ min, dýchání vlevo lehce oslabené, jinak byl nález fyziologický. Na EKG (obr. 1) kromě již zmíněné sinusové tachykardie byla patrná nízká voltáž komplexů QRS a ploše negativní vlny T difuzně a ST deprese do 1 mm laterálně. Koronární enzymy včetně troponinu však nevykazovaly vzestup. Laboratorně kromě mírného zvýšení CRP (24,5 mg/ l) a pozitivity D dimerů (4,360 mg/ l) byl nález bez pozoruhodností, RTG snímek hrudníku (obr. 2) byl bez známek dilatace srdečního stínu nebo venostázy, popisovány byly pouze pleurální změny vlevo bazálně. Echokardiografie (obr. 3) prokázala přítomnost perikardiální tekutiny cirkumkardiálně šíře 4 – 5 mm v systole, jinak byla systolická funkce levé komory (LK) normální, bez regionální poruchy kontraktility, bez nálezu chlopenní vady. Vzhledem k dechovým obtížím a pozitivitě D dimerů byla provedena CT angiografie plicnice, která vyloučila přítomnost plicní embolie, zobrazuje se ale oboustranně menší množství pleurálního výpotku, více vlevo a perikardiální výpotek, patologické zesílení perikardu nebylo popisováno. Na sonografii břicha se zobrazilo nevelké množství tekutiny kolem jater a v pravé jámě kyčelní, jinak byl nález v normě. Bakteriologický screening (výtěr z krku, sputum, moč a stolice) nezachytil přítomnost infekčního agens, taktéž sérologie na kardiotropní viry byla negativní. Pacient byl přeléčen empiricky širokospektrými antibiotiky (amoxycilin) a nesteroidními antiflogistiky. Subjektivní potíže postupně odezněly, došlo i k poklesu CRP, perikardiální výpotek nejevil tendenci k doplňování. Pacient byl předán do ambulantního kardiologického sledování na terapii nesteroidním antiflogistikem.
Obr. 1. EKG křivka – sinusová tachykardie, nízká voltáž komplexů QRS, ploše negativní T vlny difuzně a ST deprese do 1 mm laterálně. 
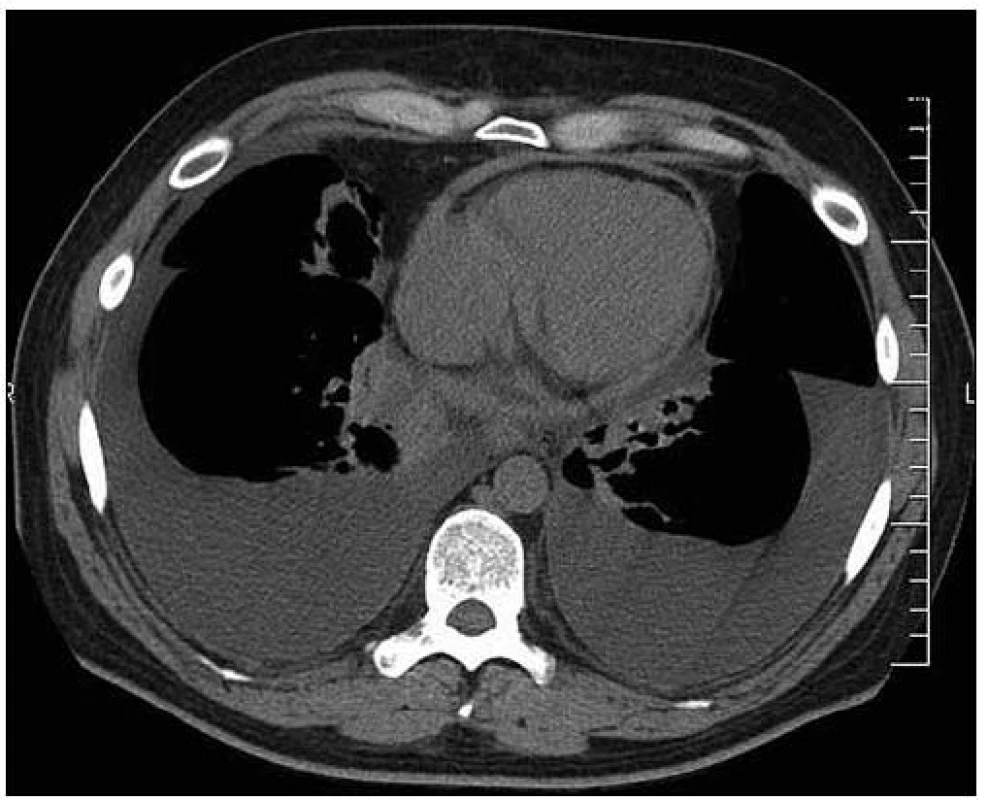
Ambulantní kontrola proběhla za měsíc od propuštění, pacient udával občasné torakalgie vlevo na hrudi píchavého charakteru, na dechové potíže si nestěžoval, otoky dolních končetin (DK) nepozoroval. Echokardiograficky tentokrát již zjištěno pouze stopové množství perikardiálního výpotku za zadní stěnou LK, ale došlo k podstatnému nárůstu levostranného pleurálního výpotku, CRP přetrvává mírně zvýšené. Při další kontrole za 5 týdnů už nebyl perikardiální výpotek detekovatelný, systolická srdeční funkce je normální, progredují však oboustranně pleurální výpotky s převahou levostranného postižení (obr. 4). Pacient se při námaze zadýchává, stěžuje si na občasné píchání vpravo na hrudi, DK jsou bez otoků. Pacient z kardiologického hlediska uzavřen jako stabilní a další dořešení předáno do kompetence plicního lékaře. Zde byl pacient podroben kompletní sérii vyšetření. Pacientovi byla provedena spirometrie, při které byla diagnostikována středně těžká kombinovaná ventilační porucha, středně těžce snížená difuzní plicní kapacita pro CO a lehká parciální respirační insuficience. Pro podezření na intersticiální plicní proces provedeno ještě HRCT plic (obr. 5), nálezu dominují oboustranné masivní pleurální výpotky s dystelektatickými změnami bazálních partií plic, popisovány jsou i bronchiektazie, zvláště ve středních a horních plicních polích. Pleurální výpotky byly punktovány, vypuštěno bylo postupně z každé strany přes litr tekutiny. Biochemicky měla tekutina charakter transudátu, bakteriologicky včetně vyšetření na TBC byla negativní, nebyly nalezeny onkologicky suspektní buňky. Ani bronchoskopie nevysvětlila příčinu potíží, nebyly shledány známky tumoru či patologických slizničních změn, BAL na původce atypických pneumonií a TBC byl negativní, zachycen byl pouze Enterococcus faecalis. Od plicního lékaře byl pacient zaléčen inhalačními bronchodilatancii a pro nález Enterococcus faecalis v BAL mu bylo podáváno makrolidové antibiotikum. Tato terapie však neměla výraznější efekt. Nakonec byl pacient odeslán i k imunologickému vyšetření (listopad roku 2008), aby se vyloučilo autoimunitní onemocnění s postižením serózních blan. Autoprotilátky byly negativní, bez nálezu imunodeficitu v buněčné nebo humorální imunitě, konstatován byl pouze mírný vzestup proteinů akutní fáze (CRP, α-1 - antitrypsin, orosomukoid). Nemoc má dále progresivní ráz, objevuje se ascites (dle UZ břicha z poloviny prosince roku 2008 je zjištěno několik litrů tekutiny), který punktován, vypuštěno přes 2 litry ascitu. Biochemicky i cytologicky byl nález obdobný jako u pleurálního punktátu.
3. Echokardiografie za 5 týdnů. 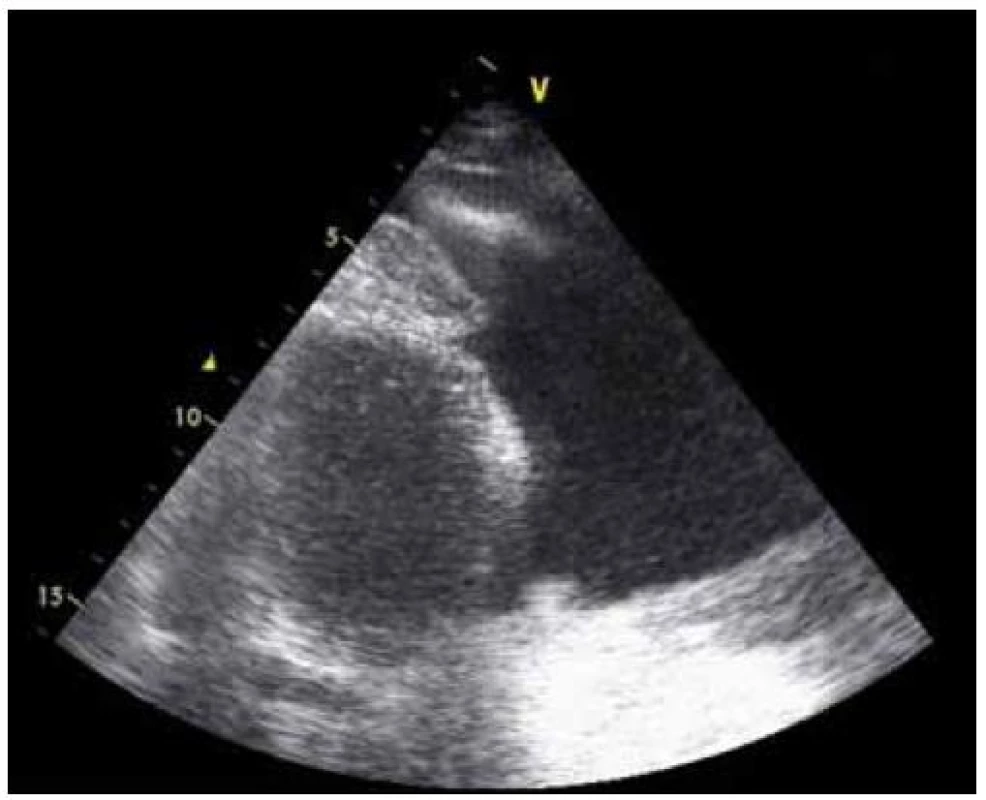
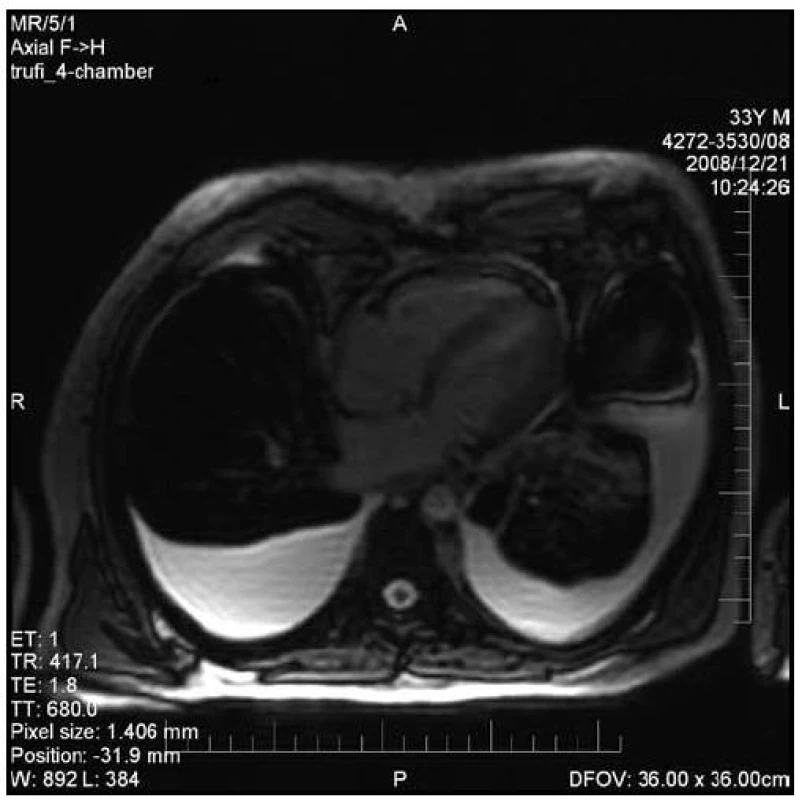
Stav pacienta se nelepšil, dochází k rychlému doplňování pleurálních výpotků a ascitu, pacient je dušný při minimální námaze, narůstají otoky DK. Za 4 měsíce od propuštění z hospitalizace je pacient odeslán na naši interní kliniku jako podezření na polyserozitidu. V klinickém obraze dominují známky pravostranného srdečního selhání, otoky DK po kolena, ascites s hepatomegalií, oboustranný fluidotorax, zvýšená náplň jugulárních žil. Laboratorní nález byl kromě přetrvávajícího mírného vzestupu CRP normální, mikrobiologie ani sérologie neprokázala infekční fokus, CT břicha neprokázalo ložiskový proces. Diagnóza polyserozitidy se zdála velmi nepravděpodobná vzhledem k absenci autoprotilátek. Normální odpady bílkovin do moči vyloučily přítomnost nefrotického syndromu. Podezření na konstriktivní perikarditidu jsme vyslovili po provedení echokardiografického vyšetření, nalezli jsme kolem hrotu a laterální stěny LK zesílenou rigidní odrazivou vrstvu (obr. 6), globální systolická funkce LK byla hraniční až nižší (EF LK 50 %), pohyb septa komor byl abnormní (septal bounce), velikost LK se měnila s respirací, byla přítomna dilatace dolní duté žíly s omezenou respirační variabilitou a kongesce jaterních žil. Vyšetření transmitrálního a transtrikuspidálního průtoku pulzním dopplerem vykazovalo typické respirační varírování, pulzní tkáňový doppler (PW TDI ) pohybu mitrálního anulu byl normální, což svědčilo proti restriktivní kardiomyopatii. Diagnózu perikardiální konstrikce jsme potvrdili jednak pravostrannou srdeční katetrizací, kdy byla tonometrií prokázána ekvalizace diastolických tlaků – pravá síň 28/ 22 (26) mm Hg, pravá komora 45/ 28 mm Hg, PA: 48/ 23 (33) mm Hg, tlak v zaklínění 32/ 25 (28) mm Hg a charakteristický obraz dip - plateau tlakové křivky z PK. Nakonec jsme pro potvrzení diagnózy doplnili ještě magnetickou rezonanci srdce, která prokázala difuzní koncentrického zesílení perikardu na 4 – 5 mm, při hrotu až na 6 mm (obr. 7). Poté následovala již kauzální léčba, byla provedena perikardektomie. Resekovaný perikard byl difuzně ztluštělý na 5 – 7 mm kolem celého srdce, mikroskopicky byl tvořený zánětlivě celulizovanou vazivovou tkání s přítomností pruhů kolagenu, bez nádorové infiltrace, imunohistochemicky bez průkazu cytokeratin pozitivních elementů. Avšak etiologii procesu nešlo z histologického obrazu stanovit. Již pooperační echokardiografické vyšetření ukázalo dobrý efekt operace, došlo k úpravě patologické variace transtrikuspidálního a transmitrálního toku, vzestupu EF LK, i když ne úplné normalizaci (55 %). Asi ještě měsíc po operaci přetrvávaly reziduální pleurální výpotky a otoky DK, které postupně při podávání malé dávky diuretika regredovaly. Přechodně se také ještě objevovaly subfebrilie. Stav pacienta se postupně naprosto upravil, i bez potřeby diuretik je nadále bez otoků DK a bez pleurálních výpotků. K normě se upravily i ventilační parametry, ustoupila hyperinflace plic, echokardiograficky je nález taktéž v mezích normy. Pacient se mohl vrátit ke svým oblíbeným sportovním aktivitám, není limitován symptomy.
5. Echokardiografie při stanovení diagnózy. 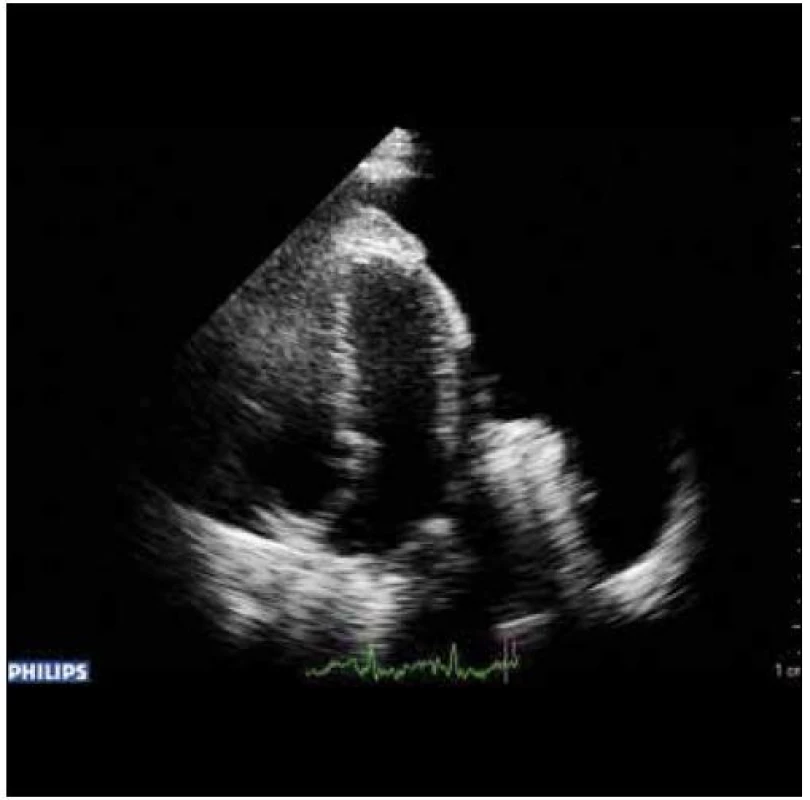
Diskuze
Konstriktivní perikarditida je v Evropě relativně vzácné onemocnění. Etiologie je až v polovině zjištěných případů idiopatická [3], i v našem případě se etiologii nepodařilo objasnit, ale je pravděpodobné, že šlo o virovou infekci, kterou se v době hospitalizace již nepodařilo sérologicky prokázat. Raritní v našem případu byl především rychlý průběh, od stanovení diagnózy exsudativní perikarditidy do projevů těžkého pravostranného oběhového selhání uběhl asi jen 1 měsíc. Bohužel se na srdeční selhání primárně nemyslelo a diferenciální diagnostika se zaměřovala především na plicní etiologii nebo imunologickou příčinu. Je pravděpodobné, že symptomy pacienta již při první hospitalizaci souvisely s mírným stupněm perikardiální konstrikce, zejména únavnost, námahová dyspnoe, intermitentní průjmy. Na možnost konstriktivní perikarditidy je nutno pomýšlet u pacientů s vysokým žilním systémovým tlakem, otoky končetin, ascitem a pleurálními výpotky [1].
Také pomocné vyšetřovací metody zapadaly do mozaiky obrazu tohoto onemocnění. EKG se snížením voltáže, inverzí T vln, sinusová tachykardie jako kompenzační mechanizmus nízkého srdečního výdeje. Dále normální velikost srdečního stínu při manifestním pravostranném městnání. CT angiografie plicnice vyloučila přítomnost plicní embolie, která by mohla způsobit cor pulmonale s podobnou symptomatologií. Na UZ a CT břicha se vyloučila možnost jaterní cirhózy či neoplastického procesu. Normální odpady bílkovin do moči svědčily proti nefrotickému syndromu. Nepřítomnost autoprotilátek pak byla argumentem proti polyserozitidě. Biochemický rozbor výpotků nesl znaky transudátu, cytologicky byla vyloučena onkologická příčina, bakteriologicky pak zejména specifický proces.
Nejpřínosnější byla v našem případě echokardiografie, široce dostupné a neinvazivní vyšetření. Neposkytuje sice žádný patognomický ukazatel typický čistě pro perikardiální konstrikci, ale když se dají jednotlivé ukazatele dohromady, můžeme vyslovit s velkou pravděpodobností podezření na tuto diagnózu [5,6]. Echokardiografie ukázala zesílený rigidní perikard, dále typické změny transmitrálního a transtrikuspidálního průtoku (> 25% snížení transmitrálního a zvýšení transtrikuspidálního E v inspiriu), byl patrný i septal bounce, nízký srdeční výdej a dilatace dolní duté žíly. V odlišení od restriktivní KMP může napovědět normální hodnota PW TDI pohybu mitrálního anulu (na rozdíl od restriktivní KMP není narušena časná fáze diastolického plnění, u restriktivní KMP je Ea patologicky snížené) [7]. Zlatým standardem v diagnostice je pak pravostranná srdeční katetrizace s tonometrií. Typický je nález ekvalizace pozdních diastolických tlaků ve všech čtyřech srdečních dutinách a charakteristický tvar dip plateau křivky z PK (dip je tvořen časnou fází plnění, která není omezena, ale jakmile komory při plnění narazí na rigidní perikard, dojde k rychlému vzestupu tlaku – plateau). Na rozdíl od perikardiální konstrikce je u restriktivní KMP vysoký systolický TK v pravé komoře (> 60 mm Hg) a vyšší diastolický TK v levé komoře oproti pravé (o 5 mm Hg) [4]. Patognomické pro konstriktivní perikarditidu je zesílení perikardu, přičemž se tloušťka více než 4 mm svědčí pro toto onemocnění. Nutno však podotknout, že ani normální tloušťka perikardu nevylučuje možnost konstrikce. V kvantifikaci zesílení perikardu jsou velmi citlivé CT a NMR, u NMR je udávána až 93% přesnost v diagnostice zesílení perikardu nad 4 mm, CT má navíc schopnost zobrazit přítomné kalcifikace [8]. Kauzální léčba je pouze chirurgická, symptomy lze přechodně tlumit diuretiky a vazodilatancii [9]. U našeho pacienta byla symptomatická léčba pouze parciálně úspěšná, docházelo k rychlému doplňování pohrudničních výpotků. Symptomy přetrvávaly i nějakou dobu po úspěšném odstranění perikardu. V literatuře se uvádí korelace přetrvávajících pooperačních diastolických abnormalit zejména u pacientů s dlouhotrvajícími symptomy pravostranného oběhového městnání [10].
Závěr
I když je incidence konstriktivní perikarditidy nízká, je potřeba u pacientů s projevy pravostranného oběhového selhání na ni vždy myslet. Stanovení diagnózy a zavedení léčby je potřeba provést co nejdříve, abychom zamezili nárůstu operačního rizika a zvýšené pravděpodobnosti pooperačních diastolických abnormalit.
MU Dr. Martin Plachý
www.fnusa.cz
e mail: plachy@fnusa.czDoručeno do redakce: 4. 10. 2009
Přijato po recenzi: 3. 11. 2009
Sources
1. Riedel M. Konstriktivní perikarditida. Kardiol Rev 2003, 2 : 69 – 75.
2. Hancock EW. Differential diagnosis of restrictive cardiomyopathy and constrictive pericarditis. Heart 2001; 86 : 343 – 349.
3. Myers RBH, Spodick DH. Constrictive pericarditis: clinical and pathophysiologic characteristics. Am Heart J 1999; 138 : 219 – 232.
4. Goldstein JA. Cardiac Tamponade, Constrictive Pericarditis, and Restrictive Cardiomyopathy. Curr Probl Cardiol 2004; 29 : 503 – 567.
5. Rajagopalan N, Garcia MJ, Rodriguez L et al. Comparison of new doppler echocardiographic methods to differentiate constrictive pericardial heart disease and restrictive cardiomyopathy. Am J Cardiol 2001; 87 : 86 – 94.
6. Oh JK, Hatle LK, Seward JB et al. Diagnostic role of doppler echocardiography in constrictive pericarditis. J Am Coll Cardiol 1994; 23 : 154 – 162.
7. Ha JW, Ommen SR, Tajik AJ et al. Differentiation of constrictive pericarditis from restrictive cardiomyopathy using mitral annular velocity by tissue Doppler echocardiography. Am J Cardiol 2004; 94 : 316 – 319.
8. Wang ZJ, Reddy GP, Gotway MB et al. CT and MR imaging of pericardial disease. Radiographics 2003; 23: S167 – S180.
9. Hoit BD. Management of effusive and constrictive pericardial heart disease. Circulation 2002; 105 : 2939 – 2942.
10. Senni M, Redfield MM, Ling LH et al. Left ventricular systolic and diastolic function after pericardectomy in patients with constrictive pericarditis. J Am Coll Cardiol 1999; 33 : 1182 – 1188.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2010 Issue 2-
All articles in this issue
- Prevalence of rheumatic manifestations and non‑organ specific autoimmunity in patients with autoimmune thyreopathy – editorial
- A few comments on the issue of infected myxoma – editorial
- Analysis and comparison of cohorts of patients with implantable cardioverter- defibrillator in primary and secondary prevention
- Prevalence of rheumatic manifestations and non‑organ specific autoimmunity in patients with autoimmune thyreopathy
- Probiotics in acute pancreatitis – a randomised, placebo- controlled, double‑blind study
- Risk of long‑term antisecretory treatment with proton pump inhibitors
- Direct renin inhibitor aliskiren in the treatment of cardiovascular and renal diseases
- The endocannabinoid system and interference with thrombogenesis
- Antithrombotic therapy in pregnancy
- Central diabetes insipidus in adult patients – the first sign of Langerhans cell histiocytosis and Erdheim‑Chester disease. Three case studies and literature review
- A case study of a young male patient with subacute constrictive pericarditis
- Infected myxoma as a cause of acute infective endocarditis
- Reappraisal of guidelines on hypertension management
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Central diabetes insipidus in adult patients – the first sign of Langerhans cell histiocytosis and Erdheim‑Chester disease. Three case studies and literature review
- Risk of long‑term antisecretory treatment with proton pump inhibitors
- A case study of a young male patient with subacute constrictive pericarditis
- Direct renin inhibitor aliskiren in the treatment of cardiovascular and renal diseases
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career