Echokardiografie u nemocných s ischemickou chorobou srdeční
Authors:
V. Chaloupka 1,2
Authors‘ workplace:
Interní kardiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Jindřich Špinar, CSc., FESC
1; Česká kardiologická společnost, předseda doc. MUDr. Václav Chaloupka, CSc.
2
Published in:
Vnitř Lék 2009; 55(9): 730-736
Category:
80th Birthday - prof. MUDr. Miloš Štejfa, DrSc., FESC
Overview
Echokardiografie hraje klíčovou roli při vyšetřování nemocných s ischemickou chorobou srdeční (ICHS). Je to dáno skutečností, že ICHS je nejčastějším srdečním onemocněním v rozvinutých zemích a také hlavní příčinou úmrtnosti. Echokardiografie se uplatňuje ve všech stadiích onemocnění, od včasného záchytu zátěží indukovaných asynergií přes diagnostiku infarktu myokardu a jeho komplikací až k sledování nemocných s chronickou formou ICHS a srdečním selháním. V neposlední řadě poskytuje důležité prognostické informace u nemocných s ICHS.
Klíčová slova:
echokardiografie – ischemická choroba srdeční – infarkt myokardu
Klidové echokardiografické vyšetření v diagnostice ICHS
Nemocný s významnou koronární stenózou může mít normální echokardiografický nález. Přesto nám může klidové vyšetření poskytnout řadu cenných informací o funkci a morfologii srdečních struktur. O velikosti a tvaru srdečních dutin, srdečních objemech a ejekční frakci (EF) levé komory (LK). Pro určení EF se v rutinní praxi často používá výpočet podle Teichholze z M-modu. To je možné za předpokladu, že LK není výrazně zvětšena a nejsou lokální poruchy kontrakce. Za nejpřesnější se pokládá hodnocení Simpsonovou metodou z dvourozměrného zobrazení (2-DE), která dělí LK na určitý počet válců o stejné výšce a výsledný objem představuje součet jednotlivých válců. Je si třeba uvědomit, že se vždy používají aproximace na různé geometrické útvary.
Zvýšená odrazivost kořene aorty a cípůaortální chlopně nás může upozornit na aterosklerotický proces. I u nemocných bez předchozího infarktu myokardu se mohou vyskytnout regionální poruchy kontrakce. Až na výjimky (např. pozánětlivé změny) jsou specifické pro ischemickou chorobu srdeční (ICHS).
Echokardiografie je schopná rozlišit také stavy spojené s diastolickou dysfunkcí. Diastolická dysfunkce představuje poruchu komorového plnění narušením relaxace nebo snížením poddajnosti komory. Je charakterizována zhoršenou časnou diastolickou relaxací. Levá komora je hůře plněna v časné diastole a zvýšeně v pozdní diastole. Výsledkem je prodloužení izovolumické fáze relaxace (IRT), snížení rychlosti časného plnění LK (E), zvýšení rychlosti síňového příspěvku (A), snížení poměru E/A a prodloužení sklonu decelerace (obr. 1). Levá komora se v důsledku fibrózy stává tužší, méně poddajnou a zvětšuje se levá síň. Dochází k zvýšení plnicího tlaku levé komory, zvýšení tlaku v levé síni a v plicnici. Mezi nejčastější příčiny patří hypertenze a ICHS [1].
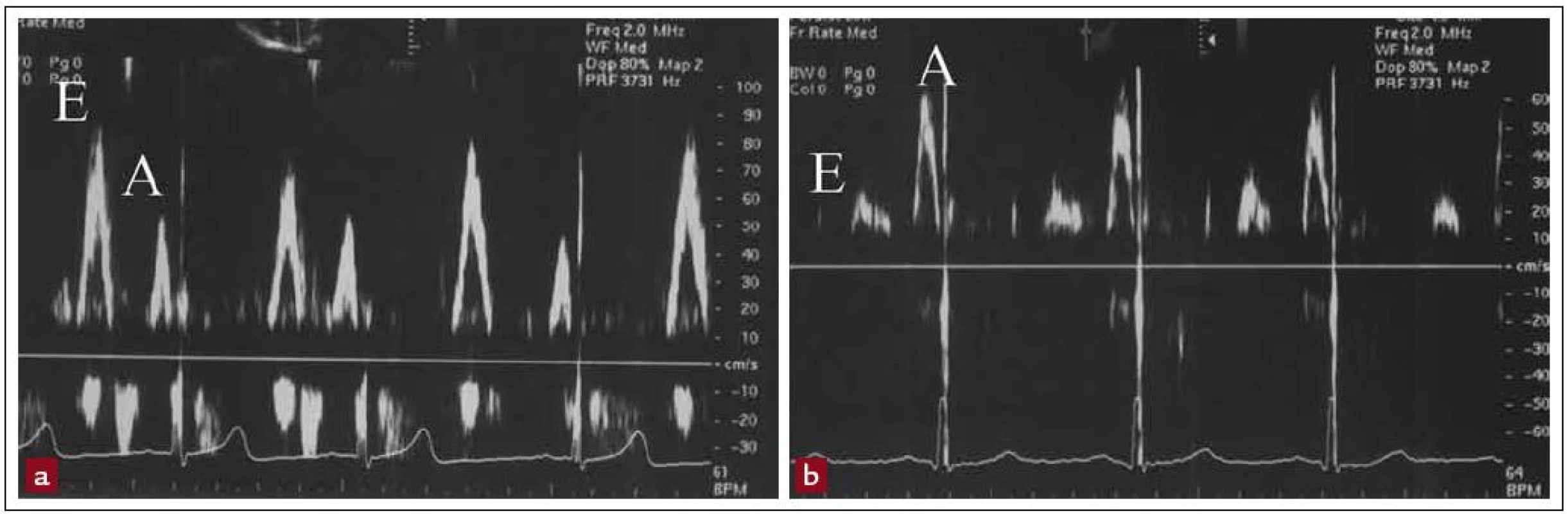
V praxi se pro posouzení diastolické funkce nejčastěji používá transmitrální dopplerovská echokardiografie se stanovením poměru vrcholové rychlosti rychlého plnění (vlna E) a vrcholové rychlosti síňového příspěvku (vlna A). Za normálních okolností je maximální rychlost časného plnění vyšší (E > A). Při dopplerovském vyšetření se stanovuje také izovolumická relaxační perioda (IRT), což je doba mezi ukončením průtoku krve aortálním ústím a začátkem časného plnění LK. Tyto parametry se stanovují poměrně jednoduše, ale jsou ovlivněné řadou faktorů, které přímo s diastolickou funkcí nesouvisí. K hodnocení diastolické dysfunkce slouží i jiné metody (např. hodnocení toku plicními žílami, tkáňový doppler, akustická kvantifikace).
Je známo, že poměr E/e’, tedy rychlost časného plnění z transmitrálního toku k časné diastolické rychlosti mitrálního prstence, dobře koreluje s plnicím tlakem LK [2]. Talreja et al vyšetřovali nemocné s EF větší než 50 % a námahovou dušností pravostrannou katetrizací a echokardiograficky. Ukázali velmi dobrou korelaci klidových i zátěžových hodnot. Zvýšení poměru E/e’ nad 15 bylo spojeno s hodnotou plnicího tlaku nad 20 mm Hg [3]. Tito autoři dříve ukázali, že u zdravých se při zátěži poměr E/e’nezvyšuje. Hodnoty E/e’ menší než 15 měly vysokou senzitivitu (89 %) pro normální hodnoty plniciho tlaku [4].
Zvětšena LS je především následkem chronicky zvýšeného enddiastolického tlaku LK a může se na ní podílet i mitrální regurgitace. Kalcifikace mitrálního prstence je častá u starších osob, diabetiků, déletrvající hypertenze a je jednou z příčin lehké mitrální regurgitace. Zpravidla začíná při kořeni zadního cípu mitrální chlopně.
K odhadu tlaku v plicnici se používá hodnocení křivky rychlosti toku v a. pul-monalis (akcelerační čas, tvar průtokové křivky), trikuspidální regurgitační gradient a lze použít i gradient pulmonální regurgitace.
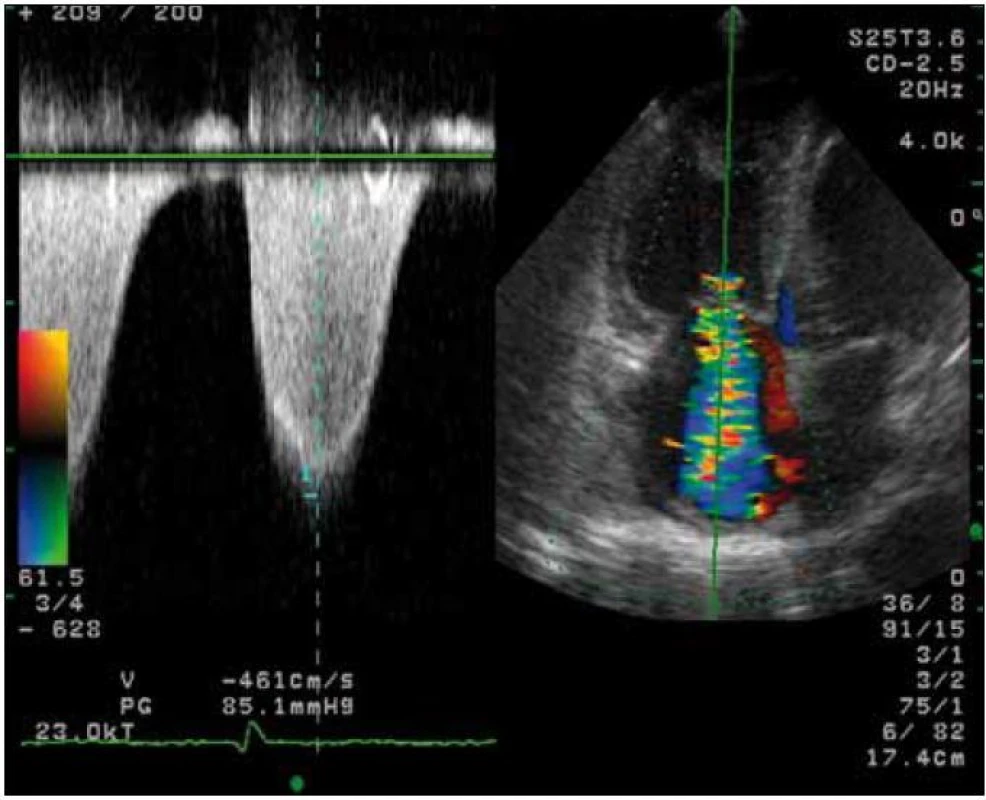
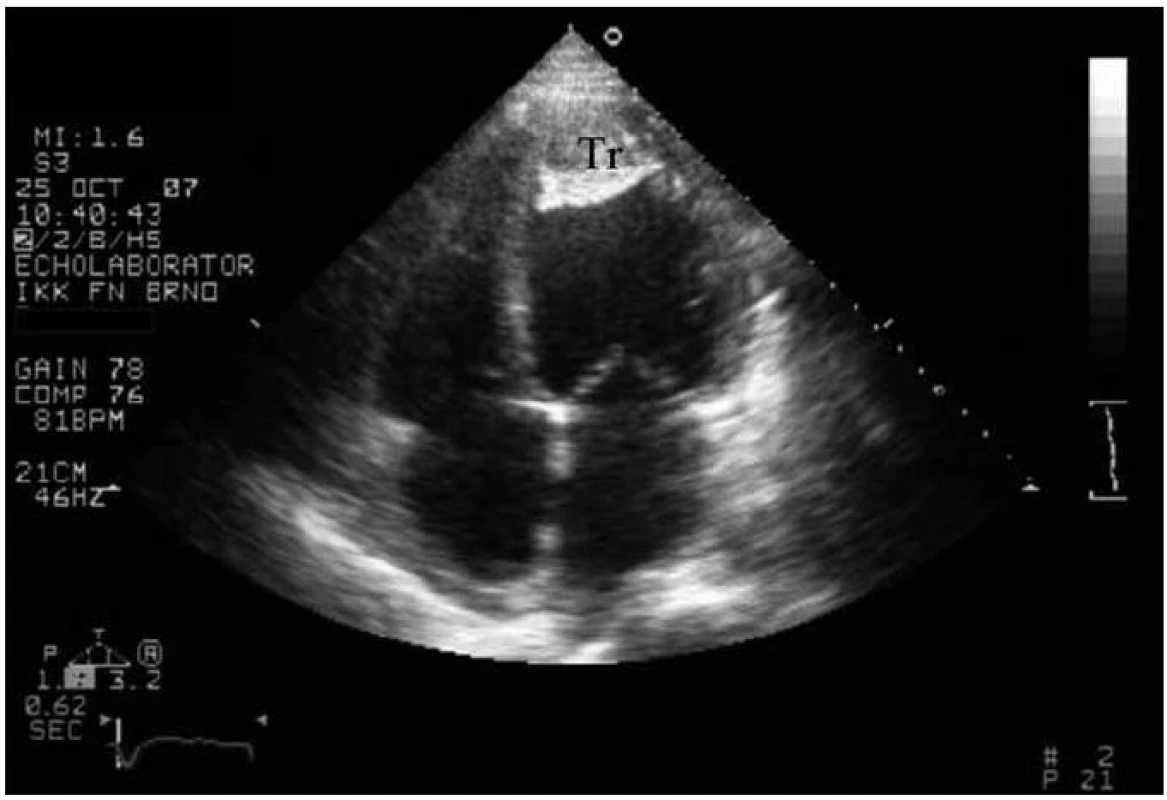
Nejpřesnější dopplerovskou meto-dou pro odhad tlaku v plicnici je stanovení vrcholového gradientu trikuspidální regurgitace, který hodnotíme kontinuálním dopplerem z čtyřdutinové projekce (obr. 2). Základem je stanovení vrcholové rychlosti regurgitace a výpočet gradientu mezi pravou komorou a pravou síní pomocí zjednodušené Bernoulliho rovnice D4V2. Pro odhad systolického tlaku v plicnici je třeba přičíst hodnotu tlaku v pravé síni (PS). Odhad tlaku v PS provádíme měřením rozměru dolní duté žíly a jeho změn v průběhu dýchání v subkostální projekci. Odhad hodnot tlaku v PS ukazuje tab. 1.
![Odhad tlaku v pravé síni podle šíře dolní duté žíly (VCI) a jejich změn s respirací [1].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/4fd117fb997f9bda3f3dd51312df008a.png)
V praxi je důležité u nemocných s ICHS také hodnocení morfologie a funkce pravé komory (PK). Aproximace na určitý geometrický útvar je u PK vzhledem k jejímu tvaru obtížná a v běžné praxi se zpravidla vystačí s kvalitativním hodnocením nebo hodnocením semikvantitativním. Je možné využít i odvozené ukazatele, podobně jako u LK. Pro hodnocení funkce PK se nejčastěji používá frakční změna plochy PK, měření systolické exkurze trikuspidálního anulu (TAPSE) a systolická rychlost trikuspidálního anulu pomocí tkáňového dopplera [5]. Ta velmi dobře koreluje s ejekční frakcí (EF) určenou radionuklidovou ventrikulografií. Hodnoty systolické rychlosti < 11,5 cm/s vykazovaly v práci Meluzína et al senzitivitu 90 % a specificitu 85 % pro hodnoty EF < 45 % [6] (obr. 3).
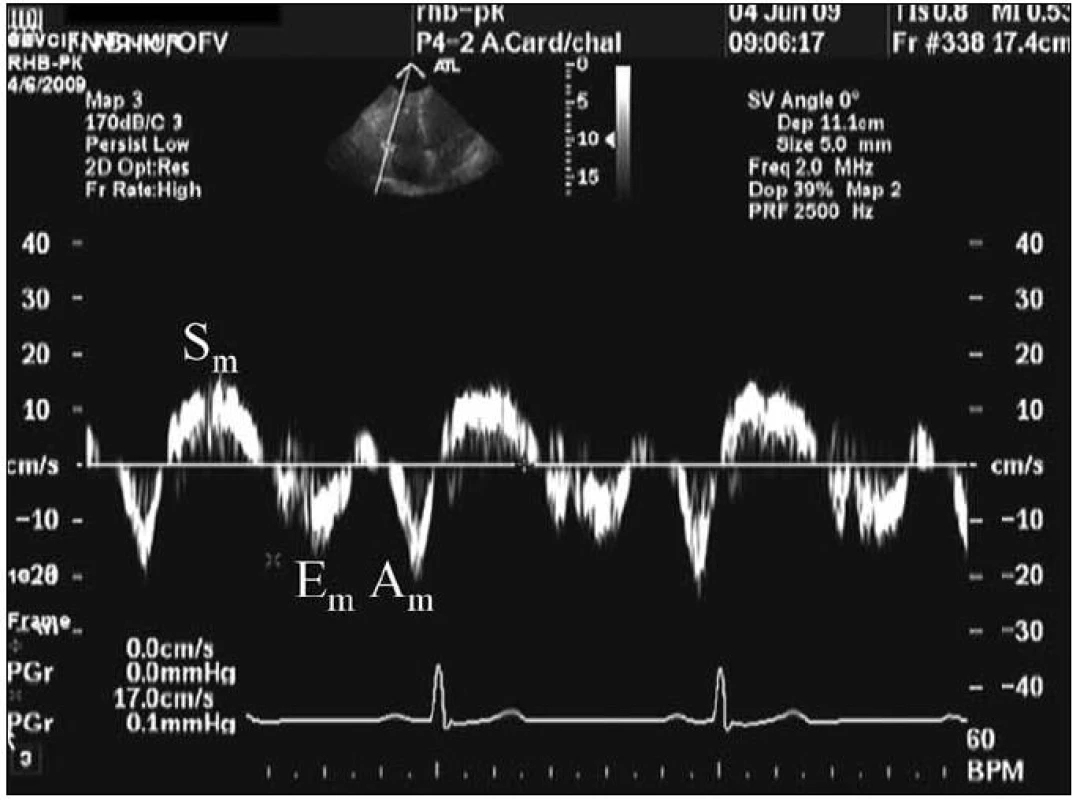
Myšlenka použití pohybu mitrálního nebo trikuspidálního prstence pro hodnocení funkce komor vychází z toho, že hrot je v průběhu srdečního cyklu poměrně stabilní a mitrální i trikuspidální anulus se v systole pohybují směrem k hrotu a zpět v diastole, jako následek kontrakce a relaxace longitudinálních svalových vláken.
Zátěžová echokardiografie
Zátěžová echokardiografie (ZE) umožňuje průkaz ischemického myokardu přímým zobrazením lokální poruchy funkce levé komory, která vzniká jako přímý důsledek ischemie. Vychází ze základních předpokladů, že kardiovaskulární zátěž vyprovokuje ischemii myokardu, ta se projeví poruchou kontrakce, tato porucha je více méně specifická pro ICHS a je diagnostikovatelná pomocí dvourozměrné echokardiografie. Ohraničené poruchy kontrakce jsou citlivým ukazatelem srdeční ischemie. Tyto změny se objevují již během několika vteřin po omezení krevního průtoku v postižené oblasti. Při normální kontrakci dochází k systolickému ztlušťování myokardu LK a jeho pohybu směrem do dutiny LK. Fyziologickou odpovědí na zátěž je hyperkinéza stěn LK, zvýšení systolického ztluštění, zmenšení systolické plochy LK a podstatně se neměnící plocha diastolická [7].
Hlavní známkou myokardiální ischemie je regionální asynergie vyjádřená 3 stupni:
- hypokinéza (snížení hybnosti a systolického ztlušťování)
- akinéza (absence hybnosti a systolického ztlušťování)
- dyskinéza (paradoxní systolický pohyb a možné systolické ztenčení stěny)
Zátěžové testy představují spojení registrační metody s různými formami zátěže. V současné době se nejčastěji používá zátěž dynamická a farmakologická.
Fyzická zátěž je obecně pokládána za nejfyziologičtější. Nejrozšířenější je zátěž pomocí bicyklové ergometrie (BE) nebo (hlavně v USA) pomocí běhátka. Používá se však i ve spojení s echokardiografií nebo radionuklidovým vyšetřením.
Farmakologické testy představují alternativní formy zátěže a k jejich většímu rozšíření došlo hlavně ve spojení s echokardiografií. V praxi se nejčastěji používají dobutamin a dypiridamol.
Dobutamin je syntetický katecholamin, používaný jako relativně selektivní pozitivně inotropní látka pro krátkodobou parenterální léčbu. Stimuluje především β1-receptory, ale má stimulační vliv i na β2 a α1 receptory kardiovaskulárního systému. Srdce obsahuje především β1-receptory, které zprostředkovávají pozitivně inotropní a chronotropní účinek.
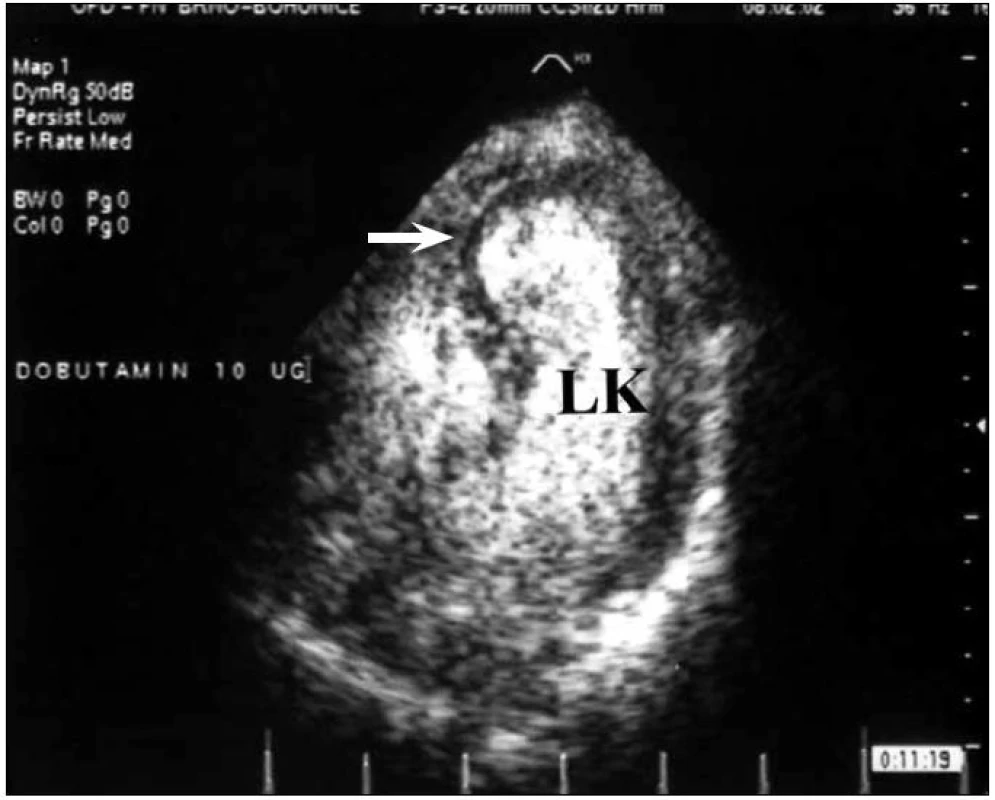
Výhodou dobutaminu je možnost dávkování zátěže postupně se zvyšující koncentrací. Navíc použití malých dávek dobutaminu má odlišný klinický význam než použití maximálního testu. Zatímco maximálního testu používáme k odhalení regionální poruchy hybnosti u nemocných se suspektní ischemickou chorobou nebo k vyprovokování nových asynergií a odhalení postižení více tepen, použití nízkých koncentrací 5–10 µg/kg/min má význam pro detekci viabilního myokardu [8].
Hlavní metody pro průkaz viability myokardu, pozitronová emisní tomografie, SPECT, dobutaminová echokardiografie a v poslední době i magnetická rezonance umožňují nejen průkaz přítomnosti dysfunkční viabilní tkáně, ale dovolují i její kvantifikaci, což umožňuje poměrně přesně předpovědět výsledek revaskularizace. Je to cenné především v situacích, kdy od revaskularizace očekáváme zlepšení funkce levé komory srdeční a ústup symptomů srdečního selhání.
Dipyridamol je pyrimidinový derivát, který byl původně určen jako koronární vazodilatační látka při léčbě anginy pectoris. Podaný ve vyšší dávce vede mechanizmem arteriolární vazodilatace ke zvýšenému průtoku krve myokardem. Vazodilatační účinek je způsoben zvýšenou plazmatickou hladinou endogenního adenozinu, který je účinný koronární vazodilatátor. U nemocných s významnou koronární stenózou je tepenné řečiště distálně od stenózy dilatováno, ve snaze zvýšit normální klidový průtok. Vazodilatační rezerva je limitována a při těsné stenóze vyčerpána. Normální koronární arterie však po podání dipyridamolu dosáhnou své plné vazodilatační kapacity a mohou se objevit rozdíly v regionálním průtoku (steal efekt). Právě tento efekt se využívá při perfuzní stress echokardiografii [9].
Diagnostická spolehlivost ZE ve smyslu senzitivity a specificity se obecně srovnává se SPECTem. Již v prvních pracích Quinones udával senzitivitu 85 % pro obě metody a specificitu 88 % pro ZE a 81 % pro SPECT. Pozdější práce ale udávají hodnoty senzitivity nižší [10,11].
Výtěžnost ZE zvyšuje použití kontrastní látky, hlavně v případě horší identifikace endokardu. Použití kontrastu je v podstatě dvojí: zlepšení identifikace endokardu a posouzení myokardiální perfuze. Optimální je současné sledování regionální kontrakce a perfuze současně. Zatímco pro zlepšení identifikace endokardu se kontrastní látka na některých pracovištích běžně používá, perfuzní stress echokardiografie (PSE) je stále záležitost spíše výzkumná. V letošním roce byla publikována multicentrická studie, která měla za cíl srovnat PSE se SPECTem v detekci ICHS. Použita byla nová kontrastní látka Imagify na souboru 662 nemocných. Hodnoty senzitivity a specificity jsou pro obě metody podobné [9].
Pravděpodobnost srdeční příhody (smrt, nefatální infarkt nebo koronární revaskularizace) je při normálním výsledku ZE extremně nízká. Na souboru 1 325 byl při 3letém sledování výskyt příhod nižší než 3 %. Multivariačními předpovědními ukazateli byla angina pectoris během testu, nízká tolerance zátěže < 7 MET u mužů a < 5 MET u žen, hypertrofie LK a pokročilý věk. Proto interpretace testu musí zahrnovat i symptomy nemocného a velikost zátěže [12].
Klasické hodnocení zátěžové echokardiografie, ať již dynamické, nebo farmakologické, je subjektivní. Ve snaze objektivizovat projevy ischemie použili někteří autoři různé ukazatele analýzy deformace myokardu v kombinaci s dobutaminem, protože citlivě reagují na pozitivně i negativně inotropní impulzy. Některé práce ukázaly slibné výsledky, ale počáteční nadšení v poslední době poněkud ochladlo, vzhledem k špatné reproducibilitě a technické náročnosti. V nedávno publikované práci australských autorů se peak SRs ukázal jako nezávislý předpovědní ukazatel prognózy při 7letém sledování [13,14].
Infarkt myokardu
U nemocných s bolestí na hrudi a nediagnostickým EKG může echokardiografické vyšetření rozhodujícím způsobem přispět ke stanovení správné diagnózy. Segmentární poruchy kontrakce stěny LK nastupují již během několika sekund po okluzi infarktové tepny. Předcházejí vývoji elektrokardiografických změn i vzniku bolesti na hrudi. Absence lokální asynergie LK u nemocného s bolestí na hrudi s vysokou pravděpodobností znamená, že bolest není způsobena akutní ischemií. Nález asynergie však nutně neznamená akutní ischemii. Může se přirozeně jednat i o staré změny po infarktu myokardu, méně často jako projev myokarditidy nebo kardiomyopatie. Abnormní pohyb septa pak můžeme vidět při bloku levého raménka Tawarova.
Echokardiografie se tedy především uplatní v diferenciální diagnóze bolesti na hrudi a vyloučení závažné ischemie. Zásadním způsobem může přispět k rozpoznání disekce aorty, plicní embolie nebo perikarditidy.
Komplikace infarktu myokardu
Echokardiografie je suverénní metodou v diagnostice většiny akutních komplikací infarktu myokardu. U nemocných s klinickým obrazem akutního selhání napomůže vyšetření k správné diagnóze. Nejčastější příčinou je rozsáhlá nekróza srdečního svalu s významným snížením ejekční frakce. Příčinou ale může být i infarkt pravé komory, provázený významným poklesem plnění LK. Příčinou těžké hypotenze může být také srdeční tamponáda při ruptuře volné stěny LK. K akutním komplikacím patří rovněž ruptura mezikomorové přepážky nebo akutní mitrální regurgitace způsobená rupturou papilárního svalu, nebo jeho dysfunkcí. Při echokardiografickém vyšetření se u nemocných s akutním infarktem myokardu poměrně často zjistí perikardiální výpotek, lokalizovaný za zadní stěnou LK. Může být klinicky němý nebo spojený s bolestí na hrudi a změnami elektrokardiogramu. Může přetrvávat i řadu týdnů. Častou komplikací infarktu myokardu jsou následné morfologické změny levé komory.
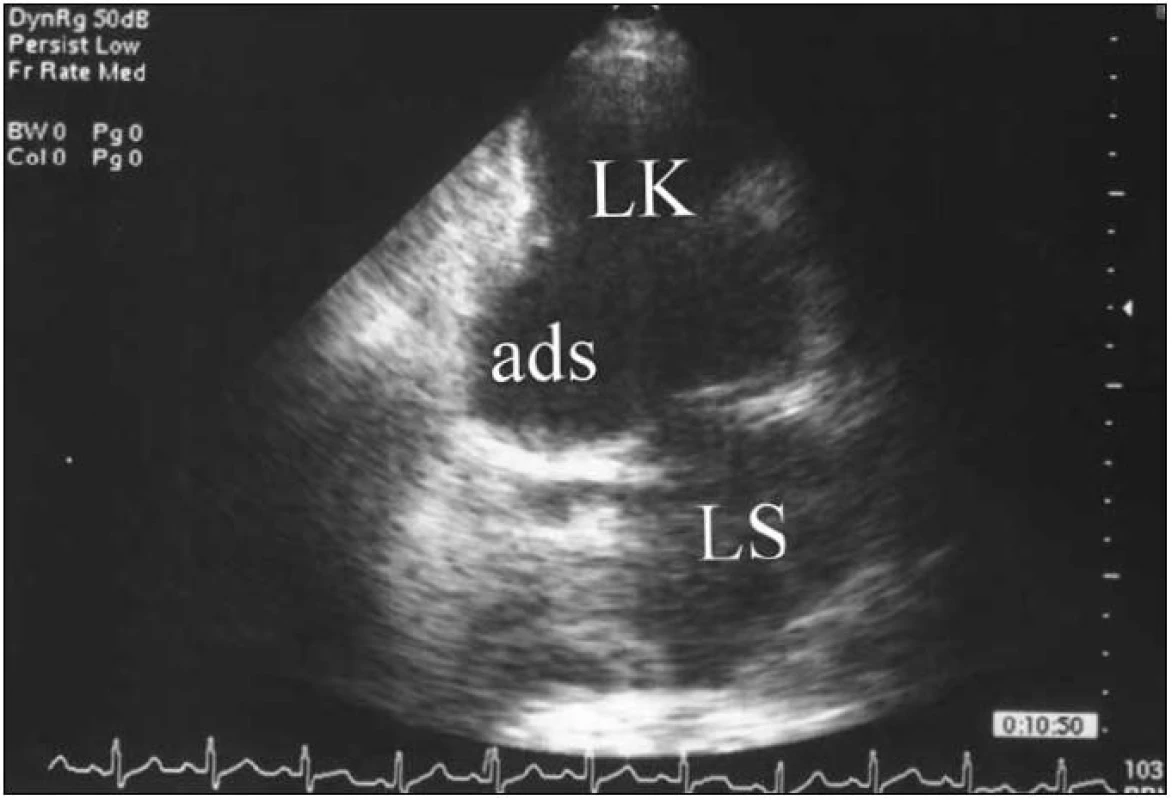
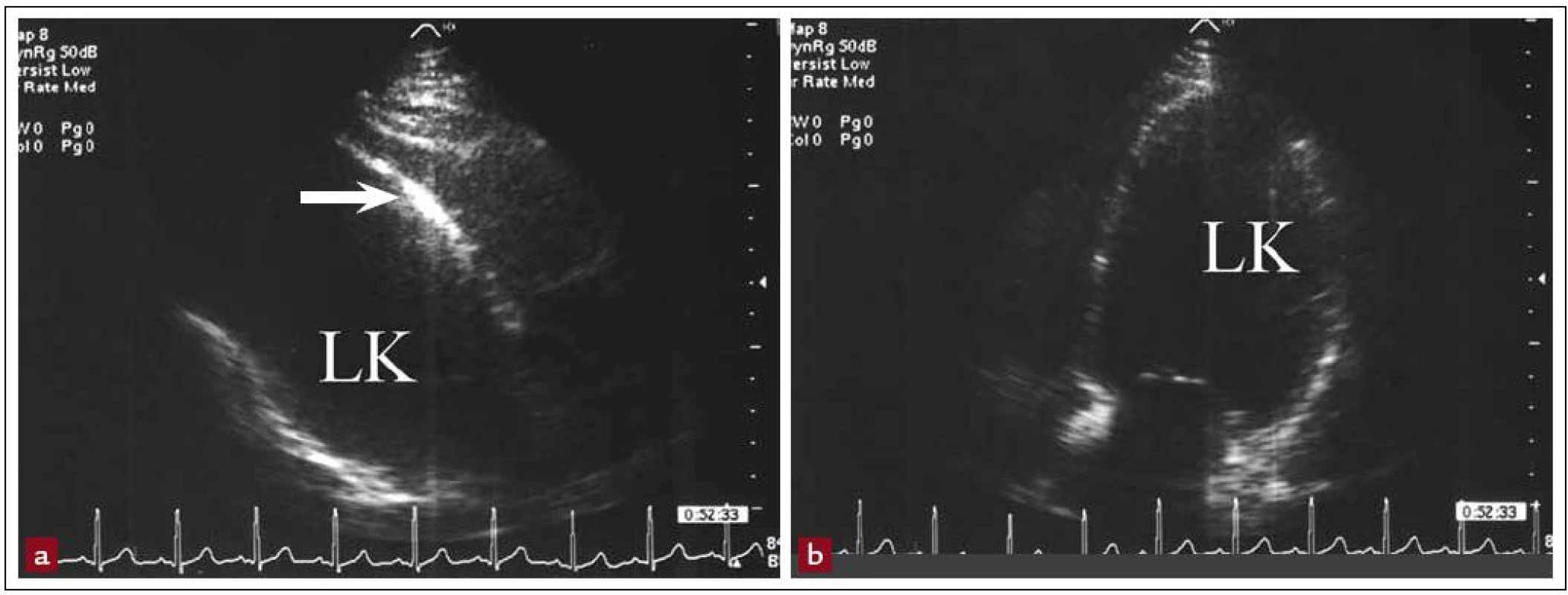
Srdeční aneuryzma je lokalizované vyklenutí a ztenčení stěny LK po infarktu myokardu, často s dyskinetickým, paradoxním pohybem v systole (obr. 4). Nejčastěji postihuje hrot LK, ale může vzniknout i v oblasti dolní stěny (obr. 5).
Nitrokomorové tromby se u nemocných s infarktem myokardu vytvářejí především v oblastech se zpomalením krevního toku, tedy především v aneuryzmatu LK. Většina trombů jsou nástěnné tromby v aneuryzmatu hrotu LK (obr. 6). Trombus se jeví jako oblast zvýšené echogenity v dutině LK, která je ohraničená od okolního endokardu a často prominuje do dutiny LK. Diagnóza může být někdy obtížná, nález je třeba hodnotit v obou na sebe kolmých pohledech od hrotu. Trombus je třeba odlišit od trabekulizace v hrotu. Při normální kinetice LK je výskyt trombu velmi nepravděpodobný. Diagnóze může napomoci použití kontrastní látky, kdy dojde k „defektu“ v rozsahu trombu. Riziko nitrokomorové trombózy spočívá v možnosti systémové embolizace.
Poinfarktová remodelace levé komory představuje expanzi infarktového ložiska a celkovou dilataci levé komory. Proces remodelace začíná bezprostředně po infarktu myokardu a pokračuje měsíce nebo roky, až nakonec vede k poruše globální funkce LK a manifestnímu srdečnímu selhání. Spouštěcím mechanizmem remodelace LK je expanze infarktového ložiska s narušením myofibril v infarktové oblasti s následným zmnožením vaziva. Makroskopicky se proces projeví ztenčením stěny v infarktové oblasti (obr. 7). Remodelace LK indukuje změny i v neinfarktových segmentech LK, zejména hypertrofii normálních buněk. To vede k tvarovým změnám a dilataci. Remodelace LK představuje v počátečním stadiu adaptaci LK ve snaze zajistit dostatečný tepový a minutový objem. Časem je tento adaptivní efekt překonán a proces vede ke zhoršení srdeční funkce jak v klidu, tak při námaze. Pro remodelaci LK jsou určujícími faktory velikost infarktu myokardu (IM), přední IM, srdeční selhání při přijetí a restrikční typ plnění LK.
Bolognese et al sledovali 284 nemoc-ných po PTCA angiograficky a echokardiograficky. Navzdory perfektně zprůchodněné infarktové tepně mělo 30 % nemocných po půl roce nárůst eddiastolického objemu o více než 20 %. Endsystolický objem a věk měly velkou předpovědní hodnotu srdeční smrti. Autoři zdůrazňují, že nemocní po IM by měli být opakovaně echokardiograficky vyšetřeni a léčeni veškerou dostupnou léčbou redukující remodelaci. Stejná skupina autorů se zaměřila na jednu z možných příčin výše zmíněné komplikace, a tou je integrita mikrovaskulární cirkulace. Před a po úspěšné angioplastice provedli intrakoronární myokardiální kontrastní echokardiografii a nemocné rozdělili na skupinu s adekvátní reperfuzí a na skupinu s mikrovaskulární dysfunkcí. Nemocní s mikrovaskulární dysfunkcí měli vyšší průměrné hodnoty kreatinkinázy, horší index hybnosti stěn LK a nižší EF. Objemy LK u těchto nemocných progresivně narůstaly a po šesti měsících byly větší než ve skupině s adekvátní reperfuzí. Mikrovaskulární dysfunkce byla také významným předpovědním ukazatelem srdeční smrti a srdečního selhání při 5letém sledování [15,16].
Ischemická mitrální regurgitace je nezávislý ukazatel špatné prognózy. Je způsobena různými formami ischemické choroby s poruchou kompetence mitrálního prstence v důsledku jeho dilatace.
Ischemická mitrální regurgitace má úzký vztah k remodelaci LK. Carraba et al rozdělili soubor 184 nemocných s akutním IM úspěšně léčených primární angioplastikou na 2 skupiny podle velikosti mitrální regurgitace. Tu určovali echokardiograficky pomocí efektivního regurgitačního ústí (ERO) a regurgitačního objemu (RV) (ERO 22,5 mm2 vs 5,8 mm2 a RV 36,7 vs 4,7 ml). Po 6 měsících byly známky remodelace ve skupině s významnou regurgitací zřetelně vyšší (66 % vs 22 %). Po dvou letech byla incidence srdečního selhání 39 % vs 12 % [17].
Stupeň mitrální regurgitace zvyšuje riziko mortality. Ukazují to i data z echokardiografické substudie studie VALIANT. Střední až těžká mitrální regurgitace byla nezávislým předpovědním ukazatelem mortality a hospitalizace pro srdeční selhání. Nemocní s progresí mitrální regurgitace během prvního měsíce po IM měli větší pravděpodobnost smrti i srdečního selhání [18].
Srdeční selhání je klinický syndrom doprovázející pokročilá stadia srdečních onemocnění. Ze všech příčin je nejčastější ICHS. Echokardiografie představuje suverénní metodu jak v diagnostice, tak v dlouhodobém sledování nemocných se srdečním selháním. Poskytne nám informaci o morfologických i funkčních ukazatelích srdečních oddílů, o progresi onemocnění, pokračující dilataci LK a snižující se kontrakční schopností její svaloviny. Z dopplerovského vyšetření toku v plicnici a na trikuspidální chlopni můžeme hodnotit přítomnost i stupeň plicní hypertenze. Diagnóza srdečního selhání se opírá o přítomnost srdeční dysfunkce. Pro posouzení celkové systolické funkce používáme hodnotu ejekční frakce. Za systolickou dysfunkci se zpravidla pokládají hodnoty ejekční frakce LK nižší než 40 %.
V současné době představuje echokardiografické vyšetření rutinní metodu u nemocných s ICHS. Poskytuje nám zásadní informace o morfologii a funkci srdečních oddílů i prognostické informace nezbytné pro léčbu nemocných.
doc. MUDr. Václav Chaloupka, CSc.
www.fnbrno.cz
e-mail: vchaloup@fnbrno.cz
Doručeno do redakce: 5. 6. 2009
Sources
1. Otto CM. Textbook of Clinical Echocardiography. Philadelphia: WB Saunders 2000.
2. Oh JK, Hatle L, Little WC. Diastolic heart failure can be diagnose by comprehensive two-dimensional and Doppler echocardiography. J Am Coll Cardiol 2006; 47: 500–506.
3. Talreja DR, Nishimura RA, Oh JK. Estimation of Left Ventricular Filling Pressure with Exercise by Doppler Echocardiography in Patients with Normal Systolic Function: A Simultaneous Echocardiographic-Cardiac Catheterization Study. J Am Soc Echocardiogr 2007; 20: 477–479.
4. Ha JW, Lulic F, Bailey KR et al. Effects of treadmill exercise on mitral inflow and annular velocities in healthy adults. J Am Coll Cardiol 2003; 91: 114–115.
5. Lindquist P, Calcutteea A, Henein A. Echocardiography in the assessment of right heart function. Eur Heart J 2008; 9: 225–234.
6. Meluzín J, Špinarová L, Bakala J et al. Pulsed Doppler tissue imaging of the velocity of tricuspid annular systolic motion. A new, rapid and non-invasive method of evaluating right ventricular function. Eur Heart J 2001; 22: 340–348.
7. Chaloupka V, Elbl L. Zátěžová echokardiografie. Praha: Maxdorf Jessenius 1997.
8. Yao SS, Chaundhry FA. Assessment of myocardial viability with dobutamine stress echocardiography in patients with ischemic left ventricular dysfunction. Echocardiography 2005; 22: 71–83.
9. Senior R, Monaghan M, Main ML et al. Detection of coronary artery disease with perfusion stress echocardiography using a novel ultrasound imaging agent: two Phase 3 international trials in comparison with radionuclide perfusion imaging. Eur J Echocardiogr 2009; 10: 26–35.
10. Quiñones MA, Verani MS, Haichin RM et al. Exercise echocardiography versus single-photon emission computed tomography in evaluation of coronary artery disease: Analysis of 292 patients. Circulation 1992; 85: 1026–1031.
11. Oh JK, Seward JB, Tajik AJ. The Echo Manual. 3th ed. Rochester: Lippincott Williams&Wilkins 2007.
12. McCully RB, Roger VL, Mahoney DW et al. Outcome after normal exercise echocardiography and predictors of subsequent cardiac events: Follow-up of 1325 patients. J Am Coll Cardiol 1998; 31: 144–149.
13. Bjork Ingul C, Rozis E, Slordahl SA et al. Incremental Value of Strain Rate to Wall Motion Analysis for Prediction of Outcome in Patients Undergoing Dobutamine Stress Echocardiography. Circulation 2007; 115: 1252–1259.
14. Kowalski M, Herregods MC, Herbots MC et al. The feasibility of ultrasonic regional strain and strain rate imaging in quantifying dobutamine stress echocardiography. Eur J Echocardiogr 2003; 4: 81–91.
15. Bolognese L, Neskovic AN, Parodi G et al. Left ventricular remodeling after primary coronary angioplasty: patterns of left ventricular dilation and long-term prognostic implications. Circulation 2002; 106: 2351–2357.
16. Bolognese L, Carrabba N, Parodi G et al. Impact of microvascular dysfunction on left ventricular remodeling and long-term clinical outcome after primary coronary angioplasty for acute myocardial infarction. Circulation 2004; 109: 1121–1126.
17. Carrabba N, Parodi G, Shehu M et al. Impact of early mitral regurgitation on left ventricular remodeling and heart failure after successful angioplasty for acute myocardial infarction. Circulation 2006; 114: 345. Abstract 1752.
18. Amigoni M, Meris A, Thune JJ et al. Mitral regurgitation in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both: prognostic significance and relation to ventricular size and function. Eur Heart J 2007; 28: 326–333.
Labels
Diabetology Endocrinology Internal medicineArticle was published in
Internal Medicine

2009 Issue 9
Most read in this issue
- Hladiny cholesterolu v závislosti na věku
- Chronická B-lymfatická leukemie a jí podobné stavy
- Jaterní cirhóza a její léčba
- Transplantace krvetvorných buněk
