-
Medical journals
- Career
Dlouhodobé výsledky srdeční resynchronizační léčby u pacientů s těžkým srdečním selháním
Authors: A. Bulava 1,2; J. Lukl 1; M. Hutyra 1; D. Marek 1
Authors‘ workplace: I. interní klinika Lékařské fakulty UP a FN Olomouc, přednosta prof. MUDr. Jan Lukl, CSc. 1; Kardiocentrum Nemocnice České Budějovice, a. s., ředitel MUDr. Ladislav Pešl 2
Published in: Vnitř Lék 2007; 53(11): 1153-1163
Category: Original Contributions
Overview
Úvod:
Srdeční resynchronizační léčba (SRL) se ukázala být velice účinnou léčebnou strategií u pacientů s těžkým chronickým srdečním selháním (CHSS).Cíl práce:
Zjistit míru klinické odezvy pacientů na SRL, stanovit v této populaci pacientů morbiditu a mortalitu, vysledovat příčiny a prediktory úmrtí. Ověřit, zda parametry tkáňové dopplerovské echokardiografie dokáží předpovědět odpověď na SRL.Pacienti a metody:
Před, po implantaci SRL systému a za 12 měsíců bylo provedeno echokardiografické vyšetření a v průběhu sledování pacientů byla zaznamenávána relevantní klinická data.Výsledky:
Do studie bylo zařazeno 102 pacientů (71 mužů, 31 žen) průměrného věku 71 ± 9 let. 68 % pacientů mělo ischemickou chorobu srdeční, 29 % idiopatickou dilatační kardiomyopatii. 75 % pacientů bylo ve funkční třídě NYHA III, 25 % NYHA IV. Po dobu sledování 711 ± 329 dnů zemřelo 26 pacientů a 35 pacientů bylo hospitalizováno. 34 % všech hospitalizací nastalo pro akutní exacerbaci CHSS. Pacienti se vstupní funkční klasifikací NYHA IV měli vyšší 1 - i 2letou mortalitu ve srovnání s pacienty ve třídě NYHA III. Podíl klinických respondérů dosáhl 64 % po 12 měsících SRL. U 58 % pacientů došlo po roce SRL k relativnímu nárůstu ejekční frakce levé komory (EF LK) o ≥ 30 %. 1/3 pacientů měla po roce EF LK ≥ 45 % s minimálními symptomy CHSS. Jako prediktory reverzní remodelace levé byly nalezeny nižší pokročilost základní choroby (EFLK > 23 %, konečný diastolický diametr levé komory < 65 mm, konečný diastolický objem levé komory < 160 ml a konečný systolický objem levé komory < 120 ml) a interventrikulární mechanické zpoždění > 45 ms.Závěr:
SRL je bezpečnou metodou s vysokou úspěšností. Problémem zůstává identifikace respondérů. Známky menší pokročilosti srdeční choroby společně s interventrikulárním mechanickým zpožděním byly identifikovány jako citlivé prediktory odpovědi na léčbu.Klíčová slova:
biventrikulární stimulace - srdeční resynchronizační léčba - tkáňová dopplerometrie - reverzní remodelace levé komory - predikce respondérůÚvod
Biventrikulární stimulace (BVS) je dnes již zavedenou metodou léčby chronického srdečního selhání (CHSS) [2,5,15]. V této metodě léčby však stále přetrvává řada kontroverzí. Hlavním problémem je fakt, že až 30 % pacientů neodpovídá na tuto terapii adekvátním zlepšením klinickým symptomů srdečního selhání [1,14].
Cílem práce bylo zhodnotit naše zkušenosti s biventrikulární stimulací u pacientů s pokročilým srdečním selháním, zejména zjistit míru klinické odpovědi pacientů s CHSS indikovaných podle současných doporučení k srdeční resynchronizační léčbě (SRL) po implantaci biventrikulární stimulace, stanovit v této populaci pacientů morbiditu a mortalitu, vysledovat příčiny a prediktory úmrtí a retrospektivně ověřit hypotézu, že parametry tkáňové dopplerovské echokardiografie (TDI) všeobecně dnes považované za odraz významné komorové asynchronie, dokáží předpovědět pozitivní echokardiografickou a klinickou odpověď na SRL. Dále jsme zhodnotili učební křivku na našem pracovišti, peri - a postimplantační komplikace a celkovou úspěšnost implantace resynchronizačních systémů.
Pacienti a metody
Pacienti byli indikováni k implantaci biventrikulárního kardiostimulátoru nebo biventrikulárního implantabilního kardioverteru-defibrilátoru (ICD) podle doporučených postupů České kardiologické společnosti [21]. Pacienti zahrnutí do studie museli splňovat následující vstupní kritéria: ischemická choroba srdeční (ICHS) nebo idiopatická dilatační kardiomyopatie (DKMP), pokročilé srdeční selhání (funkční třída NYHA III nebo IV) po dobu minimálně 6 měsíců, EKG s morfologií bloku levého Tawarova raménka (BLTR) nebo bloku pravého Tawarova raménka (BPTR) se současně přítomným levým předním hemiblokem (LAHB), QRS komplex ≥ 150 ms (v případě šířky QRS komplexu mezi 120 ms a 150 ms přítomnost známek komorové dyssynchronie), PQ interval ≥ 160 ms, ejekční frakce levé komory (EF LK) ≤ 35 %, vyčerpané možnosti standardní farmakoterapie. Optimální medikamentózní léčba zahrnovala kličková diuretika, spironolakton, inhibitory angiotenzin-konvertujícího enzymu (ACEI) nebo blokátory receptorů typu 1 pro angiotenzin II (ATRB) a betablokátory (BB), pokud byly tolerovány.
Echokardiografický protokol
Před implantací, do 48 hodin po implantaci a za 12 měsíců byli pacienti vyšetřeni echokardiograficky. Vyšetření bylo provedeno podle doporučených postupů Americké společnosti pro echokardiografii [20] na komerčně dostupném přístroji (Vivid 7, GE Vingmed Ultrasound). Protokol zahrnoval měření základních echokardiografických parametrů ve standardních projekcích a provedení tkáňové dopplerometrie. Ejekční frakce levé komory (EF LK) byla stanovena podle Simpsonova pravidla se softwarovou korekcí pro použití dvou projekcí (apikální 4dutinová a apikální 2dutinová projekce). V klasickém pulzním dopplerovském módu (PW) byly měřeny následující intervaly: globální CO interval (COGLOB) (tj. interval trvající od uzavření mitrální chlopně do jejího znovuotevření, který byl měřen z průtoku na mitrální chlopni od konce A vlny předcházejícího srdečního cyklu do začátku E vlny následujícího srdečního cyklu), globální EA interval (EAGLOB), tj. interval diastolického plnění levé komory, měřený z průtoku na mitrální chlopni od začátku E vlny do konce A vlny téhož srdečního cyklu). Z průtoku ve výtokovém traktu levé komory byl stanoven preejekční interval LPEP (měřený od začátku QRS komplexu do začátku toku ve výtokovém traktu levé komory), ejekční interval LVET (interval délky trvání toku ve výtokovém traktu levé komory) a dále byl stanoven integrál průtoku přes aortální ústí (VTIAO). Podobně byl stanoven preejekční (RPEP) a ejekční (RVET) interval z průtoku ve výtokovém traktu pravé komory, jakož i VTIPU jako integrál průtoku přes pulmonální ústí. Interventrikulární mechanické zpoždění (IVMD) bylo stanoveno jako rozdíl mezi LPEP a RPEP. Z naměřených intervalů byl dále spočten Teiův index funkce levé komory, který zahrnuje poruchu jak systolické tak i diastolické funkce (myocardial performance index) [22]. CO a EA intervaly byly korigovány Bazettovým vzorcem (interval/√RR interval).
Tkáňová dopplerometrie (TDI) zahrnovala následující měření v pulzním dopplerovském (PW) módu získaná z bazálních partií levé komory při zvoleném 4segmentovém modelu (septum - SEP, spodní stěna - INF, boční stěna - LAT, přední stěna - ANT): regionální CO interval (tj. interval od konce regionální A vlny předcházejícího srdečního cyklu do začátku regionální E vlny následujícího srdečního cyklu měřený na příslušném bazálním segmentu levé komory), tvořený 3 komponentami: regionálním izovolumickým kontrakčním časem (ICT), regionálním ejekčním časem (LVET) a regionálním izovolumickým relaxačním časem (IRT). Podobně byl měřen regionální EA interval jako interval od začátku regionální E vlny do konce regionální A vlny téhož srdečního cyklu na příslušném bazálním segmentu levé komory. Všechny CO a EA intervaly byly korigovány Bazettovým vzorcem (interval/√RR interval). Všechny intervaly byly měřeny 3krát a hodnoty použité pro další statistickou analýzu průměrovány.
V PW TDI módu měřeny časy od počátku QRS komplexu na povrchovém EKG k počátku komorové kontrakce (Q-Sbg) a do vrcholu komorové kontrakce (Q-Sm) na všech 4 bazálních segmentech LK (asi 1,5-2 cm od mitrálního anulu). Rozdíl Q-Sbg intervalů na septu a laterální stěně určoval septolaterální zpoždění do počátku systolické regionální fáze (SLD-POČ). V offline analýze barevného TDI zobrazení bylo stanoveno septolaterální zpoždění mezi vrcholy systolické kontrakce na septu a laterální stěně se vzorkovacím objemem umístěným na bazálních segmentech LK (SLD-VRCH). Výpočtem byly dále stanoveny tyto parametry: rozdíl v délce trvání CO intervalů na septu a laterální stěně (COD-SL) a rozdíl mezi maximálním a minimálním trváním CO intervalu na všech 4 segmentech LK (COD-MAX).
Klinická odezva na srdeční resynchronizační léčbu
Pacienti byli klasifikováni podle kompozitního klinického skóre podle Packera [17], které rozděluje respondenty po léčbě na „zlepšené“, „nezměněné“ a „zhoršené“. Pozitivní klinickou odezvu na SRL jsme definovali jako klasifikace „zlepšení“ při poklesu NYHA třídy o ≥ 1 stupeň a zároveň absenci hospitalizace pro akutní exacerbaci CHSS (vyjma případů, kdy došlo ke ztrátě biventrikulární stimulace) nebo smrti.
Statistické zpracování
Získaná data byla zpracována za pomocí statistického softwaru SPSS pro MS Windows, verze 14.0. Spojité proměnné jsou vyjádřeny jako průměr ± standardní odchylka doplněné o rozptyl hodnot (minimum - maximum), není-li uvedeno jinak. Srovnání spojitých veličin bylo provedeno za pomocí párového Studentova t-testu mezi stejnými skupinami a za pomocí nepárového Studentova t-testu, pokud byly srovnávány skupiny různé. Srovnání opakovaných měření v celém souboru bylo provedeno za použití metody analýzy rozptylu (ANOVA) a doplněnou Tukeyovou-Kramerovou metodou korekce hodnot p. Kategoriální data byla srovnána testem χ2 a případně také Fisherovým exaktním testem. Přežívání bylo vyjádřeno pomocí Kaplanových-Meierových křivek a vzájemné srovnání skupin bylo provedeno za pomocí log rank testu. K predikci pozitivní echokardiografické odpovědi na SRL byla užita univariantní a posléze i multivariantní analýza za pomocí logistického regresního modelu. Hodnoty sensitivity a specificity predikce jednotlivými sledovanými parametry byly získány za použití ROC analýzy. Hodnota p < 0,05 byla považována statisticky signifikantní.
Výsledky
Do studie bylo zařazeno 102 pacientů splňujících vstupní kritéria a indikovaných k zavedení biventrikulárního kardiostimulátoru (n = 76) nebo biventrikulárního ICD (n = 26). Všichni pacienti byli sledováni po dobu minimálně 12 měsíců, nezemřeli-li dříve. Charakteristiku souboru přináší tab. 1.
Table 1. Vstupní demografická a klinická data studijní populace. 
Klinické výsledky srdeční resynchronizační léčby
Průměrná doba sledování pacientů činila 711 ± 329 (26 - 1 372) dnů. Během této doby aktivní aplikace SRL došlo v celém souboru pacientů k výraznému zlepšení symptomů CHSS podle klasifikace NYHA (obr. 1) doprovázené možným snížením dávek kličkových diuretik a spironolaktonu a zvýšením dávek karvedilolu (obr. 2).
Graf 1. Vývoj funkční klasifikace dle NYHA u pacientů po srdeční resynchronizační léčbě. 
Graf 2. Vývoj průměrných dávek diuretik a beta-blokátorů u pacientů po srdeční resynchronizační léčbě. 
Od 4. měsíce po SRL došlo ke statisticky signifikantnímu snížení dávek furosemidu ve srovnání se vstupními hodnotami (p < 0,01), u spironolaktonu ke statisticky významnému snížení dávek došlo již po 1 měsíci SRL (p < 0,01). Dávka carvedilolu mohla být významně navýšena až po 6 měsících SRL (p < 0,01). Pozitivní klinická odpověď na SRL byla po 6 měsících zaznamenána celkem u 72 pacientů (70,6 %), bez významného rozdílu po rozdělení pacientů podle základního srdečního onemocnění: 45 pacientů s ICHS (65,2 %) a 27 pacientů s DKMP (81,8 %), p = NS. Po 12 měsících na SRL pozitivně odpovědělo celkem 65 pacientů (63,7 %): 41 pacientů s ICHS (59,4 %) a 24 pacientů s DKMP (72,7 %), p = NS.
Za období 12 měsíců po implantaci resynchronizačního systému došlo celkem k 57 hospitalizacím u 35 pacientů: pacienti s ICHS nebyli hospitalizováni statisticky významně častěji než pacienti s DKMP (36,2 % vs 30,3 %, p = NS). Pacienti se vstupní klasifikací NYHA IV byli hospitalizováni významně častěji ve srovnání s pacienty ve třídě NYHA III (64,0 % vs 24,7 %, p = 0,0003). Příčiny hospitalizace shrnuje obr. 3.
Graf 3. Příčiny hospitalizace u pacientů po srdeční resynchronizační léčbě (n celkem = 102). 
ASS – akutní exacerbace chronického srdečního selhání, KT/FiK – výskyt komorové tachykardie nebo fibrilace komor, ZSRL – ztráta srdeční resynchronizační léčby pro fibrilaci síní nebo jinou supraventrikulární arytmii, OTS – ortotopická transplantace srdeční, SYN – synkopa, PSS – porucha stimulačního systému, AP – angina pectoris, EK – extrakardiální příčiny Během doby sledování, tj. 711 ± 329 (26 - 1 372) dnů, došlo celkem k 26 úmrtím (25,5 %), z toho 21 pacientů s ICHS a 5 pacientů s DKMP. K úmrtí došlo za průměrně 470 ± 296 (26-1 150) dní od implantace resynchronizačního systému. Příčiny smrti shrnuje obr. 4. Zemřelí pacienti se od přežívajících nelišili v pohlaví, průměrném věku, a vstupní šíři QRS komplexu. U přežívajících pacientů však došlo k výraznějšímu zkrácení QRS komplexu při SRL (131 ± 16 ms vs 149 ± 18 ms, p < 0,0001), užívali celkově nižší dávky kličkových diuretik (44 ± 25 mg vs 114 ± 105 mg, p < 0,00001) i spironolaktonu (26 ± 17 mg vs 36 ± 25 mg, p = 0,03). Vstupní globální EF LK (tj. před implantací SRL) byla u zemřelých výrazně nižší než u přežívajících (19 ± 5 % vs 24 ± 7 %, p < 0,001).
Graf 4. Příčiny smrti u pacientů se srdeční resynchronizační léčbou (n celkem = 102). 
Pacienti, kteří v průběhu sledování zemřeli, měli závažnější symptomy srdečního selhání dle klasifikace NYHA. Kaplan-Meierovy křivky přežívání podle NYHA třídy před implantací SRL jsou zachyceny na obr. 5.
Graf 5. Kumulativní přežívání pacientů se srdeční resynchronizační léčbou podle třídy NYHA před implantací. 
Elektrokardiografické a stimulační parametry
Po zavedení SRL došlo k signifikantnímu zúžení QRS komplexu (136 ± 18 ms vs 185 ± 24 ms, p < 0,0001). Nebyla nalezena žádná korelace mezi elektrickým zpožděním mezi pravo - a levokomorovou elektrodou a žádným z hodnocených echokardiografických parametrů odrážející mechanickou asynchronii. Stimulační prahy jednotlivých elektrod udává tab. 2.
Table 2. Stimulační prahy v pravé síni (PS), pravé komoře (PK) a levé komoře (LK). 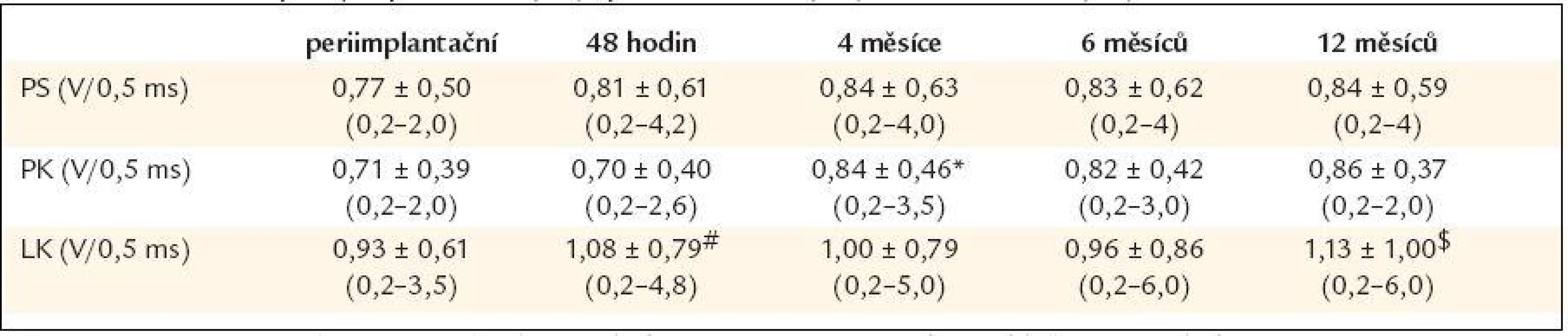
PS – pravá síň, PK – pravá komora, LK – levá komora, hodnoty jsou průměr ± směrodatná odchylka (rozmezí hodnot). * p < 0,001 vs 48 hod po implantaci, # p < 0,001 vs perimplantační hodnoty, $ p = 0,02 vs 6 měsíců Echokardiografické výsledky srdeční resynchronizační léčby
Již v akutní fázi 48 hod po aplikaci SRL došlo k významnému zvýšení průměrné ejekční frakce levé komory (EF LK), snížení konečného diastolického diametru levé komory (LVEDD) a ke zmenšení konečného diastolického (LVEDV), resp. systolického objemu levé komory (LVESV). Další a výraznější zlepšení všech těchto parametrů nastalo po 12 měsících SRL (tab. 3). Na konci 12 měsíčního období mělo 32 pacientů (tj. 31,4 %) téměř normální nebo normální EF LK (tj. ≥ 45 %). U 59 pacientů (tj. u 57,8 %) jsme zaznamenali po 12 měsících relativní nárůst EF LK o více než 30 % ve srovnání se vstupní hodnotou.
Table 3. Vybrané echokardiografické parametry u pacientů před srdeční resynchronizační léčbou a za 48 hod a 12 měsíců po začátku srdeční resynchronizační léčby. 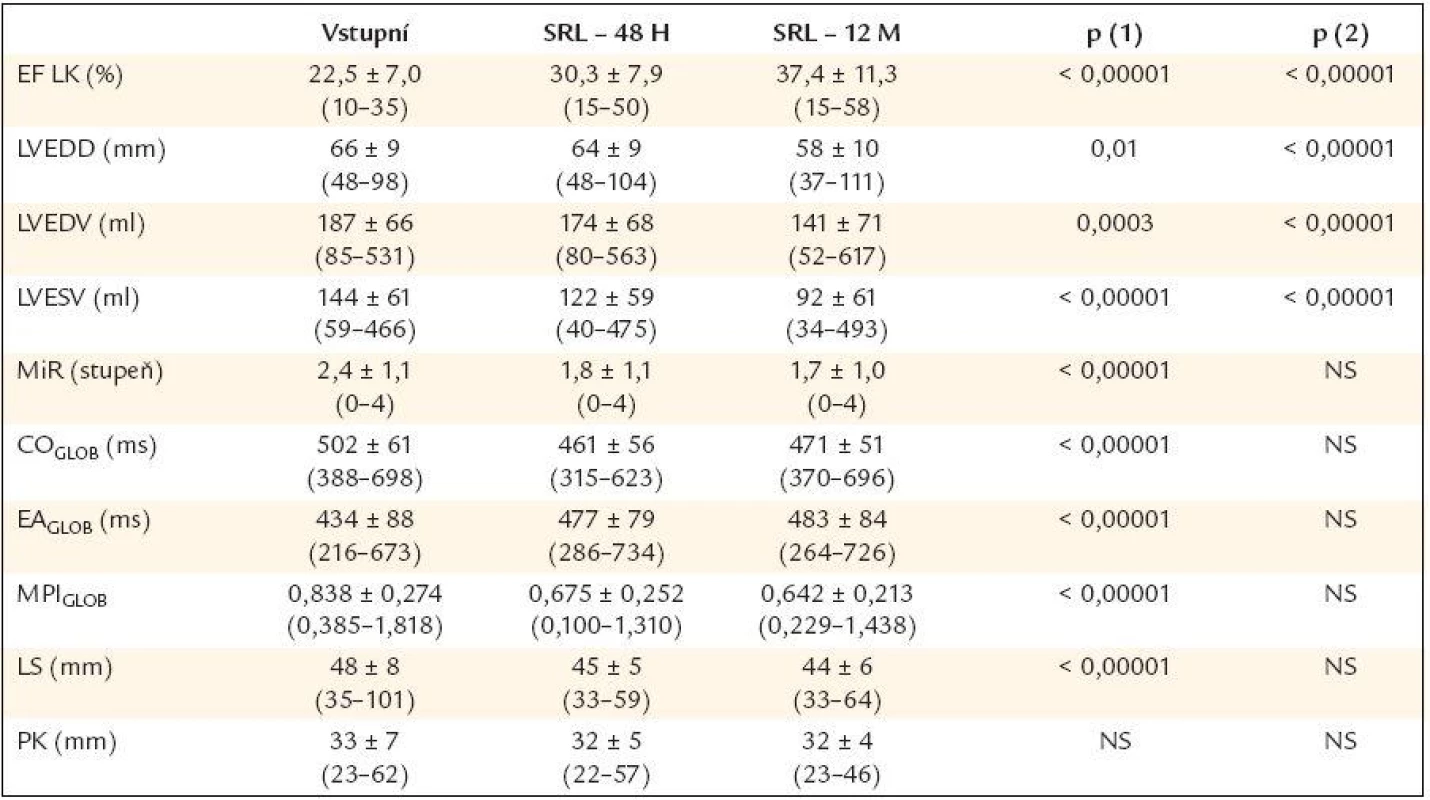
EF LK – ejekční frakce levé komory, LVEDD – end-diastolický diametr levé komory, LVEDV – end-diastolický objem levé komory, LVESV – end-systolický objem levé komory, MiR – mitrální regurgitace, COGGLOB – globální systolický interval, EAGLOB – globální diastolický interval, MPIGLOB – Teiův index, LS – levá síň, PK – pravá komora, p (1) – hodnota p při porovnání vstupní hodnoty a hodnoty při SRL po 48 hod, p (2) – hodnota p při porovnání hodnoty při SRL po 48 hod a za 12 měsíců. Z parametrů asynchronie bylo již po 48 hod významně zkráceno interventrikulární mechanické zpoždění (IVMD) a interval SLD-POČ (tab. 4), ostatní parametry výrazně ovlivněny nebyly. Při porovnání intervalů lokální systoly (CO intervaly) na jednotlivých bazálních segmentech levé komory před a po resynchronizaci (tab. 5) bylo zjištěno, že u všech došlo aplikací SRL k signifikantnímu zkrácení (v průměru o asi 50-70 ms) a k recipročnímu prodloužení intervalů lokální diastoly (EA intervaly).
Table 4. Parametry tkáňové dopplerometrie u pacientů před srdeční resynchronizační léčbou a za 48 hod a 12 měsíců po začátku srdeční resynchronizační léčby. 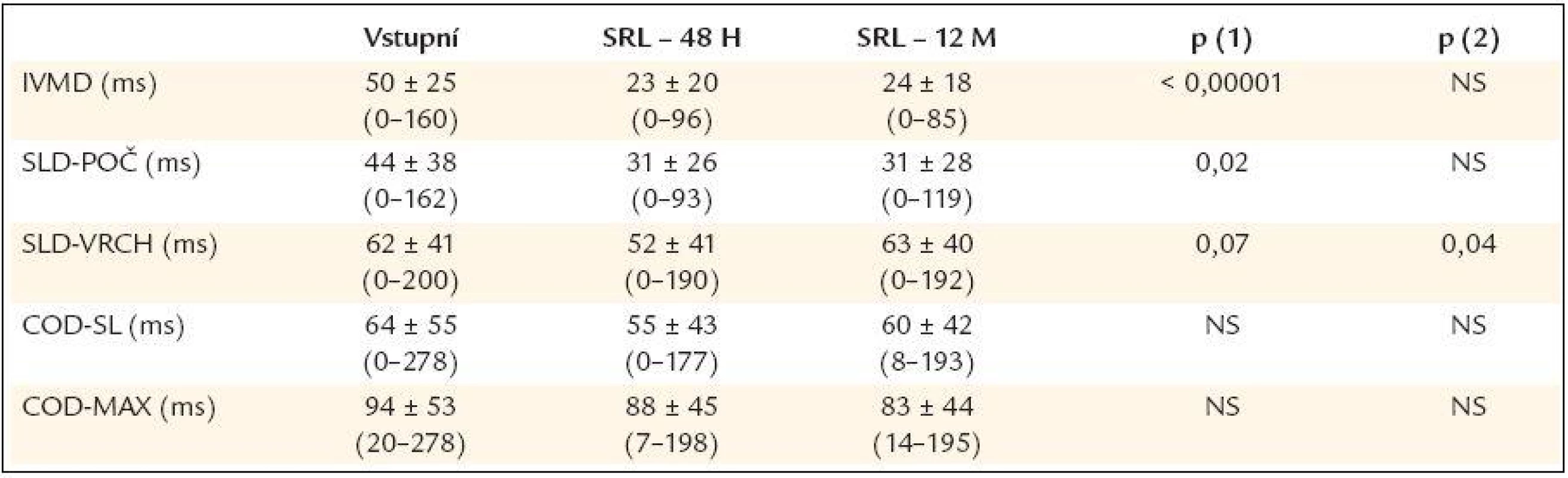
IVMD – interventrikulární mechanické zpoždění, SLD-POČ – rozdíl v Q-Sb intervalech na septu a laterální stěně, SLD-VRCH – septolaterální zpoždění mezi vrcholy systolické kontrakce na septu a laterální stěně, COD-SL – rozdíl v délce trvání CO intervalů na septu a laterální stěně, CODMAX – rozdíl mezi maximálním a minimálním CO intervalem na všech čtyřech měřených segmentech levé komory, p (1) – hodnota p při porovnání vstupní hodnoty a hodnoty při SRL po 48 hod, p (2) – hodnota p při porovnání hodnoty při SRL po 48 hod a za 12 měsíců. Table 5. Intervaly lokální systolické a diastolické fáze (korigované na RR interval) u pacientů před srdeční resynchronizační léčbou a za 48 hod a 12 měsíců po začátku srdeční resynchronizační léčby. 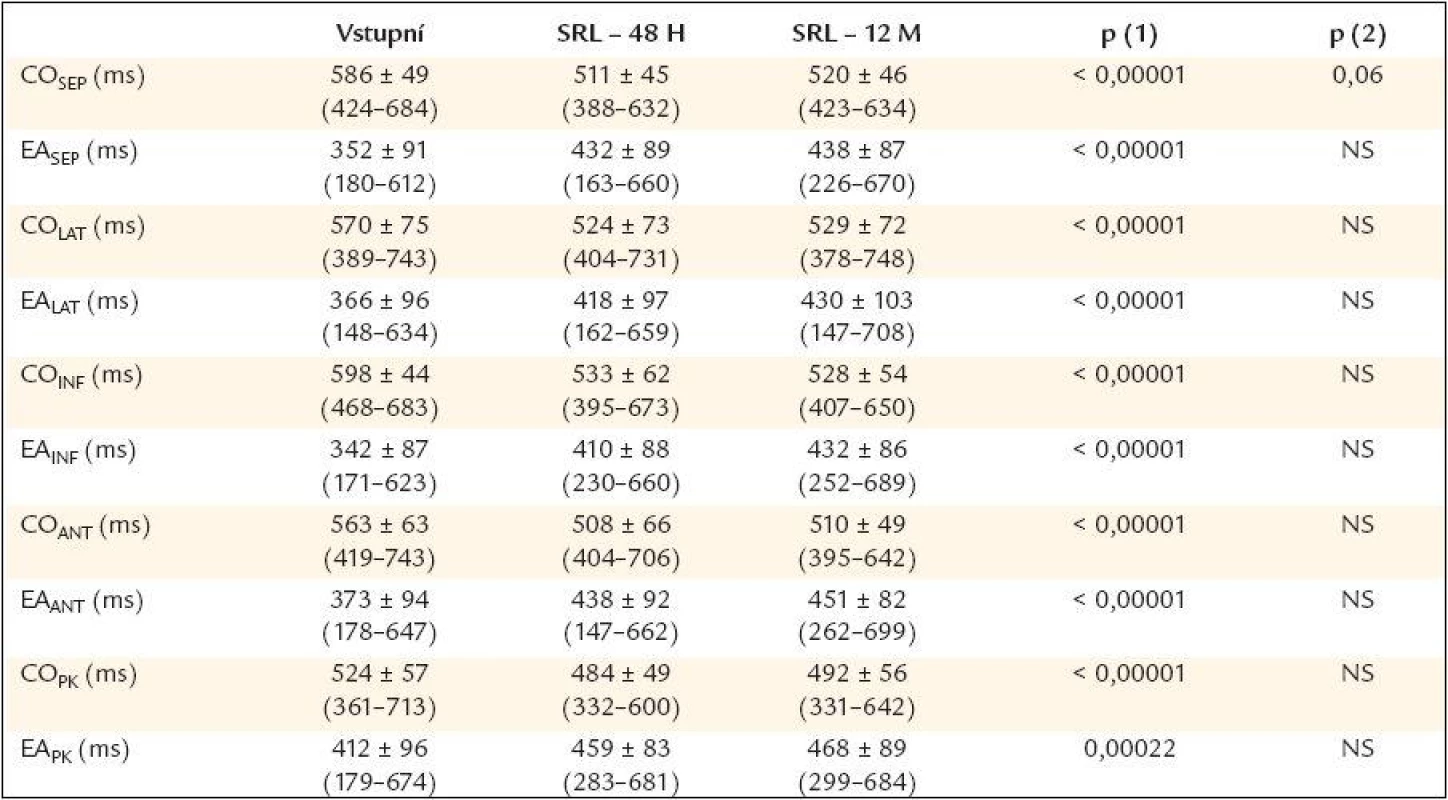
CO – interval od konce A vlny předcházejícího srdečního cyklu do začátku E vlny následujícího srdečního cyklu (closure-opening), tj. lokální systolická fáze, EA – interval od začátku E vlny do konce A vlny téhož srdečního cyklu, tj. lokální diastolická fáze, SEP – septální bazální segment levé komory, LAT – laterální bazální segment levé komory, INF – spodní bazální segment levé komory, ANT – přední bazální segment levé komory, PK – volný bazální segment pravé komory Predikce echokardiografické odpovědi na srdeční resynchronizační léčbu a míra reverzní remodelace levé komory srdeční
Pro predikci absolutního zlepšení EF LK na 45 % nebo více se v univariantním modelu ukázaly být významné vstupní parametry LVEDD, LVEDV, LVESV, EF LK a IVMD a elektrický interval zpoždění mezi pravou a levou komorou (spRV-LV). V multivariantní analýze se pak jako významné prediktory ukázaly být pouze EF LK a IVMD: zvýšení IVMD o 10 ms zvyšovalo šance na zlepšení EF LK na ≥ 45 % 1,96krát (OR = 1,96, 95 % CI = 1,22 - 3,16). Zvýšení vstupní EF LK o 5 % pak zvyšovalo šance na zlepšení EF LK na ≥ 45 % po roce SRL 1,39krát (OR = 1,39, 95 % CI = 1,07 - 1,80). Mezní hodnoty, senzitivita a specificita jsou uvedeny v tab. 6.
Table 6. Prediktory a jejich výpovědní hodnota pro absolutní nárůst ejekční frakce levé komory na 45 % a více po 12 měsících srdeční resynchronizační léčby. 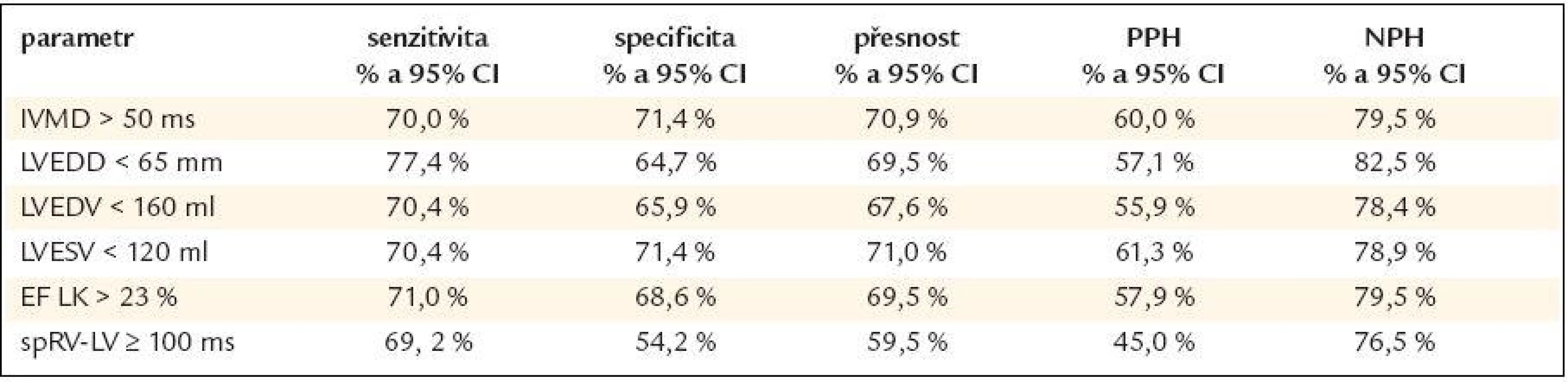
95% CI – 95 % interval spolehlivosti, PPH – pozitivní prediktivní hodnota, NPH – negativní prediktivní hodnota, IVMD – interventrikulární mechanické zpoždění, LVEDD -end-diastolický diametr levé komory, LVEDV – end-diastolický objem levé komory, LVESV – end-systolický objem levé komory, EF LK – ejekční frakce levé komory, spRV-LV – interval od endokardiálního potenciálu snímaného pravokomorovou elektrodou k endokardiálnímu potenciálu snímaného levokomorovou elektrodou za spontánního rytmu Úspěšnost implantační procedury a komplikace
Od ledna roku 2002 do prosince roku 2006 bylo na našem pracovišti přistoupeno k implantaci srdečního resynchronizačního systému celkem u 151 pacientů [9]. Celkový průměrný čas výkonu činil 151 ± 71 min (50-420 min) a skiaskopický čas 25 ± 20 min (2,7-104 min). Implantace byla úspěšná u 144 ze 151 pacientů (95 %). U 2 pacientů nebyl úspěšně kanylován koronární sinus, u dalších 2 nebyla nalezena vhodná větev k implantaci levokomorové elektrody. U těchto 4 pacientů byla následně levokomorová elektroda implantována epikardiálně z levé laterální torakotomie. U 2 pacientů došlo perioperačně k velké disekci koronárního sinu vyžadující přerušení implantace a reimplantaci v druhé době. U 1 pacienta pak došlo k perforaci drobné větve koronárního sinu a úniku kontrastní látky do perikardu bez známky tamponády srdeční. I u tohoto pacienta byl resynchronizační systém následně implantován v druhé době. Celková úspěšnost transvenózního zavedení elektrod tak činila 97 %.
Perioperační komplikace zahrnovaly: disekci koronárního sinu (n = 8, tj. 5,3 %), pneumotorax (n = 2, tj. 1,3 %, oba si vyžádaly pleurální drenáž), edém plic (n = 1, tj. 0,7 %), astmatický záchvat (n = 1, tj. 0,7 %), porušení izolace původní elektrody při upgradu (n = 1, tj. 0,7 %), nesprávné zapojení elektrod v přístroji (n = 1, tj. 0,7 %), kompletní AV blokádu (n = 1, tj. 0,7 %), indukci fibrilace komor při manipulaci s elektrodami (n = 1, tj. 0,7 %), rupturu větve koronárního sinu bez tamponády (n = 1, tj. 0,7 %), tamponádu po extrakci dočasné stimulace (n = 1, tj. 0,7 %).
Diskuse
SRL ve formě BVS se v posledním desetiletí ukázala být účinným doplňkem standardní farmakologické léčby CHSS u pacientů se špatnou systolickou funkcí levé komory a poruchami vedení elektrického vzruchu. Řada studií poslední doby potvrdila příznivé účinky SRL na klinický stav a funkční zdatnost pacientů [1,10], reverzní remodelaci levé komory, počet hospitalizací i mortalitu [8,12,26]. Při použití standardních indikačních kritérií [14] pro implantaci BVS se však můžeme setkat s tím, že až 30 % pacientů nebude na tuto léčbu odpovídat příznivě [1,14].
Tento fakt je do jisté míry očekávatelný, neboť žádná medicínská léčba nemůže z principu garantovat 100% účinnost. Nicméně pravdou je, že precizní definování vhodného pacienta k léčbě SRL je důležité nejen z etického důvodu, ale i z hlediska ekonomického (nákladnost léčby biventrikulárním kardiostimulátorem se pohybuje v řádu 200 000-250 000 Kč a léčby biventrikulárním defibrilátorem v řádu 950 000-1 100 000 Kč). Situaci ještě navíc komplikuje fakt, že vysoké procento „nonrespondérů“ SRL může mít více příčin:
- špatně vybraný pacient, tj. SRL byla navozena u neindikovaného pacienta, např. v případech, v nichž byla mechanická asynchronie levé komory odhadnuta jen nepřímo (na podkladě širokého QRS komplexu); za předpokladu synchronie za bazálních podmínek může biventrikulární stimulace naopak i komorovou asynchronii navodit (!)
- špatné umístění elektrod, při níž není a ani nemůže být dosaženo optimální levokomorové synchronizace
- suboptimální programace přístroje (AV zpoždění, VV zpoždění a další)
- inhibice biventrikulární stimulace (např. často přítomné supraventrikulární arytmie, nejčastěji fibrilace síní nebo také frekventní předčasné komorové stahy)
- přítomnost komorbidit, které výrazně limitují prospěch ze SRL
- potřeba dalších terapeutických zásahů (léčba ischemie - revaskularizace, chirurgická léčba významné chlopenní vady apod)
- pokročilé srdeční selhání v konečném stadiu (end-stage kardiomyopatie) aj
Naše vlastní výsledky získané na středně velké populaci pacientů se středně těžkým až těžkým srdečním selháním (NYHA III, IV) potvrzují účinnost SRL v léčbě CHSS refrakterního na farmakoterapii. Průměrná NYHA klasifikace se po 6 i 12 měsících SRL významně zlepšila a u pacientů bylo možno významně redukovat dávku diuretik a za pečlivého sledování dotitrovat vyšší dávky betablokátorů, než které pacienti tolerovali před léčbou SRL. Možnost up-titrace betablokátorů a její vliv na prognózu pacientů nebyl v dostupné literatuře podle našich znalostí dosud dokladován. Z betablokátorových studií však víme, že vyšší dávky jsou obecně spjaty s příznivější prognózou. Do jaké míry to platí i pro pacienty s CHSS léčené SRL však zatím není známo. Přežívání pacientů po SRL je však výrazně závislé na tíži symptomů CHSS před implantací: jednoroční mortalita u pacientů s funkční třídou NYHA III byla 3% (2letá pak 10%), kdežto u pacientů ve třídě NYHA IV činila 33 % (2letá pak 50 %). V případě ekonomických limitů by zřejmě měla být SRL rezervována pro pacienty s NYHA III klasifikací, neboť tito z léčby profitují výrazněji a déle.
Procento klinických respondérů dosáhlo v naší skupině pacientů 71 % po 6 měsících SRL a 64 % po 12 měsících SRL, což jsou výsledky odpovídající většině dříve publikovaných prací selektující pacienty k implantaci biventrikulární stimulace jen na podkladě šíře QRS komplexu [1,7,19,28]. Retrospektivní analýza prospektivní nerandomizované studie SCART ukázala, že pokud jsou do výběru pacientů indikovaných k SRL zahrnuta i echokardiografická kritéria dyssynchronie LK, pak lze podíl klinických respondérů SRL zvýšit (83 % v této studii) [3]. Vzhledem k tomu, že i všichni naši pacienti měli přítomen alespoň některý z parametrů indikující levokomorovou asynchronii podobně jako ve studii SCART, jsou naše výsledky diskrepantní. Vyšší procento respondérů SRL ve studii SCART než v naší práci lze pravděpodobně vysvětlit odlišnou populací zahrnutou do studie SCART, kde bylo 14 % pacientů klasifikováno dokonce do třídy NYHA II. Avšak i ve studii SCART klesl po zahrnutí echokardiografické odpovědi (absolutní nárůst EFLK ≥ 5 % po 6 měsících SRL) počet respondérů SRL na 68 %.
V naší práci jsme dále prokázali, že SRL významně zlepšuje globální systolické parametry kontrakce levé komory i její synchronii, a to bezprostředně po aplikaci této léčby (do 48 hod) i v dlouhodobém horizontu 12 měsíců. Už záhy po iniciaci biventrikulární stimulace dochází ke zlepšení EF LK, zmenšení konečného diastolického diametru i objemů LK a tento trend významných změn pokračuje i po 12 měsících, což je v souladu s publikovanými pracemi [1,11,12,26]. Došlo ke zkrácení lokálních systolických intervalů na jednotlivých segmentech levé komory doprovázené odpovídajícím prodloužení intervalů diastolických, což obojí vede k lepší synchronii stahu LK a k optimalizaci jejího plnění. Také jsme ukázali, že v globálním měřítku se tyto změny udají hned po aplikaci SRL a průměrné hodnoty za 12 měsíců SRL již nejsou odlišné. Jiným měřeným parametrem synchronie LK bylo tzv. septolaterální zpoždění (SLD-POČ, SLD-VRCH). Statisticky významné zkrácení nastalo po SRL jen u SLD-POČ, u SLD-VRCH jde jen o trend. Vysvětlujeme si to vysokou variabilitou měření těchto intervalů, která kriticky závisí na volbě a umístění vzorkovacího objemu při off-line analýze. Tento parametr, ač některými autory proklamován [26,29,30], nepovažujeme proto za spolehlivý.
Stálou otázkou, na níž dosud neexistuje uspokojivá odpověď a která zaujímá přední místo v četných diskusích o resynchronizační léčbě je, které vstupní parametry nejlépe předpoví pozitivní odezvu na SRL. Pro významnou reverzní remodelaci LK (EF ≥ 45 %) byly univariantním modelu kromě IVMD odhaleny jako významné prediktory end-diastolický diametr LK, enddiastolický a endsystolický objem LK a ejekční frakce LK, nikoliv však septo-laterální zpoždění! Tyto výsledky potvrzují známou skutečnost: čím horší EF a čím dilatovanější komora, tím horší je prognóza [24], což zřejmě platí i pro odpověď na SRL, jak bylo prokázáno v naší práci i v jiných studiích [13]. Parametry asynchronie srdeční kontrakce se v řadě studiích jeví jako významný prediktor odezvy na SRL, zvláště pak parametry intraventrikulární asynchronie LK [6,16,18,27,28]. Interventrikulární asynchronie (měřená hodnotou IVMD) byla dlouho považovaná za „druhořadý“ parametr, ale v poslední době se v literatuře množí údaje o tom, že i tato proměnná dokáže s velkou výpovědní hodnotou předpovědět pozitivní klinickou i echokardiografickou odezvu na SRL [3,23].
Definitivní odpověď, jaké parametry komorové dyssynchronie budeme používat pro hodnocení potenciálních kandidátů SRL, by měla přinést studie PROSPECT, která je plánována jako prospektivní studie testující řadu konvečních i nekonvenčních echokardiografických parametrů u asi 300 pacientů ve více než 70 centrech v USA i v Evropě [25].
Rozvoj biventrikulární stimulace a její široké rozšíření s sebou přinášejí i otázky bezpečnosti a úspěšnosti při aplikaci této léčby, které budou zajímat nejen lékaře provádějící implantace a odesílající lékaře, ale především pacienty samotné. Úspěšnost transvenózního zavedení levokomorové elektrody se časně po zavedení této metody do léčby CHSS ve 2. polovině 90. let minulého století pohybovala kolem 70-80 % a procento dislokací až kolem 30 %, přičemž ke konci 90. let minulého století a počátkem 21. století již dosahovala 90 % a procento dislokací se snížilo na 11 % [4]. Podle zkušenosti našeho centra [9] dosahuje úspěšnost v transvenózním zavedení levokomorové elektrody až 97 % při minimálním riziku závažných komplikací.
Limitace práce
Hlavní limitaci práce vidíme v tom, že prezentujeme retrospektivní analýzu dat u pacientů prospektivně a nerandomizovaně zařazených do této studie se všemi potenciálními nedostatky, které tento přístup skýtá. Pacienti splňující vstupní kritéria však byli zařazováni konsekutivně. Hodnocený vzorek populace, která mohla být sledována po dobu alespoň 12 měsíců, byl relativně méně robustní. Navíc v naší populaci pacientů léčených SRL byla roční mortalita kolem 10 %, což dále limitovalo počet získaných kontrolních echokardiografických vyšetření.
Další limitací práce je, že pro identifikaci respondérů SRL nebyly použity všechny dostupné echokardiografické možnosti. Rozhodli jsme se nepoužívat parametry vrcholového strainu derivované z rychlostních dat tkáňové dopplerometrie vzhledem k tomu, že podle našich zkušeností není u řady pacientů validní vyšetření možno provést (limitovaná kvalita získaného vyšetření). Metody 2D strainu (speckle-tracking) a 3D echokardiografie nebyly v době plánování této práce ještě běžně klinicky dostupné.
Závěr
Biventrikulární stimulace se objevila před více než desetiletím a ukázala se být velice účinnou léčebnou strategií u pacientů s těžkým srdečním selháním, depresí systolické funkce levé komory srdeční a intraventrikulárními poruchami vedení elektrického vzruchu. Biventrikulární stimulace je metodou bezpečnou a při velice nízkém procentu komplikací a nutných reoperací je úspěšnost transvenózního zavedení vysoká a na našem pracovišti se blíží bezmála 100 %.
Největším problémem zůstává správná selekce pacientů a identifikace respondérů srdeční resynchronizační léčby. Známky menší pokročilosti srdeční choroby (tj. ejekční frakce levé komory > 23 %, konečný diastolický diametr levé komory < 65 mm, konečný diastolický objem levé komory < 160 ml a konečný systolický objem levé komory < 120 ml) společně s interventrikulárním mechanickém zpožděním > 50 ms a elektrickým zpožděním mezi pravou a levou komorou ≥ 100 ms byly identifikovány jako citlivé prediktory.
MUDr. et Mgr. Alan Bulava, Ph.D.
www.nemcb.cz
email: alanbulava@seznam.cz
Doručeno do redakce: 29. 3. 2007
Přijato po recenzi: 25. 5. 2007
Sources
1. Abraham WT, Fisher WG, Smith AL et al. Cardiac resynchronization in chronic heart failure. N Engl J Med 2002; 346 : 1845-1853.
2. Abraham WT, Hayes DL. Cardiac resynchronization therapy for heart failure. Circulation 2003; 108 : 2596-2603.
3. Achilli A, Peraldo C, Sassara M et al. Prediction of Response to Cardiac Resynchronization Therapy: The Selection of Candidates for CRT (SCART) Study. Pacing Clin Electrophysiol 2006; 29(Suppl 2): S11-S19.
4. Alonso C, Leclercq C, D’Allonnes FR et al. Six year experience of transvenous left ventricular lead implantation for permanent biventricular pacing in patients with advanced heart failure: Technical aspects. Heart 2001; 86 : 405-410.
5. Auricchio A, Abraham WT. Cardiac resynchronization therapy: current state of the art: cost versus benefit. Circulation 2004; 109 : 300-307.
6. Bax JJ, Bleeker GB, Marwick TH et al. Left ventricular dyssynchrony predicts response and prognosis after cardiac resynchronization therapy. J Am Coll Cardiol 2004; 44 : 1834-1840.
7. Bax JJ, Marwick TH, Molhoek SG et al. Left ventricular dyssynchrony predicts benefit of cardiac resynchronization therapy in patients with end-stage heart failure before pacemaker implantation. Am J Cardiol 2003; 92 : 1238-1240.
8. Bristow MR, Saxon LA, Boehmer J et al. Cardiac-resynchronization therapy with or without an implantable defibrillator in advanced chronic heart failure. N Engl J Med 2004; 350 : 2140-2150.
9. Bulava A, Lukl J. Five-year experience with transvenous electrode implantation for biventricular pacing in patients with chronic heart failure. Bratislavské lekárské listy 2007; 108 : 21-22.
10. Cazeau S, Leclercq C, Lavergne T et al. Effects of multisite biventricular pacing in patients with heart failure and intraventricular conduction delay. N Engl J Med 2001; 344 : 873-880.
11. Cleland JG, Coletta AP, Lammiman M et al. Clinical trials update from the European Society of Cardiology meeting 2005: CARE-HF extension study, ESSENTIAL, CIBIS-III, S-ICD, ISSUE-2, STRIDE-2, SOFA, IMAGINE, PREAMI, SIRIUS-II and ACTIVE. Eur J Heart Fail 2005; 7 : 1070-1075.
12. Cleland JG, Daubert JC, Erdmann E et al. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med 2005; 352 : 1539-1549.
13. Diaz-Infante E, Mont L, Leal J et al. Predictors of lack of response to resynchronization therapy. Am J Cardiol 2005; 95 : 1436-1440.
14. Hunt SA, Abraham WT, Chin MH et al. ACC/AHA 2005 Guideline Update for the Diagnosis and Management of Chronic Heart Failure in the Adult: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Update the 2001 Guidelines for the Evaluation and Management of Heart Failure): developed in collaboration with the American College of Chest Physicians and the International Society for Heart and Lung Transplantation: endorsed by the Heart Rhythm Society. Circulation 2005; 112: e154-e235.
15. Kautzner J, Riedlbauchova L. Biventricular cardiac pacing. Vnitř Lék 2003; 49 : 734-739.
16. Notabartolo D, Merlino JD, Smith AL et al. Usefulness of the peak velocity difference by tissue Doppler imaging technique as an effective predictor of response to cardiac resynchronization therapy. Am J Cardiol 2004; 94 : 817-820.
17. Packer M. Proposal for a new clinical end point to evaluate the efficacy of drugs and devices in the treatment of chronic heart failure. J Card Fail 2001; 7 : 176-182.
18. Penicka M, Bartunek J, De Bruyne B et al. Improvement of left ventricular function after cardiac resynchronization therapy is predicted by tissue Doppler imaging echocardiography. Circulation 2004; 109 : 978-983.
19. Pitzalis MV, Iacoviello M, Romito R et al. Cardiac resynchronization therapy tailored by echocardiographic evaluation of ventricular asynchrony. J Am Coll Cardiol 2002; 40 : 1615-1622.
20. Quinones MA, Otto CM, Stoddard M et al. Recommendations for quantification of Doppler echocardiography: a report from the Doppler Quantification Task Force of the Nomenclature and Standards Committee of the American Society of Echocardiography. J Am Soc Echocardiogr 2002; 15 : 167-184.
21. Táborský M, Kautzner J, Bytešník J et al. Zásady pro implantace kardiostimulátorů a implantabilních kardioverterů-defibrilátorů. Cor Vasa 2005; 47 : 59-68.
22. Tei C, Ling LH, Hodge DO et al. New index of combined systolic and diastolic myocardial performance: a simple and reproducible measure of cardiac function - a study in normals and dilated cardiomyopathy. J Cardiol 1995; 26 : 357-366.
23. Toussaint JF, Lavergne T, Kerrou K et al. Basal asynchrony and resynchronization with biventricular pacing predict long-term improvement of LV function in heart failure patients. Pacing Clin Electrophysiol 2003; 26 : 1815-1823.
24. White HD, Norris RM, Brown MA et al. Left ventricular end-systolic volume as the major determinant of survival after recovery from myocardial infarction. Circulation 1987; 76 : 44-51.
25. Yu CM, Abraham WT, Bax J et al. Predictors of response to cardiac resynchronization therapy (PROSPECT) - study design. Am Heart J 2005; 149 : 600-605.
26. Yu CM, Chau E, Sanderson JE et al. Tissue Doppler echocardiographic evidence of reverse remodeling and improved synchronicity by simultaneously delaying regional contraction after biventricular pacing therapy in heart failure. Circulation 2002; 105 : 438-445.
27. Yu CM, Fung JW, Zhang Q et al. Tissue Doppler imaging is superior to strain rate imaging and postsystolic shortening on the prediction of reverse remodeling in both ischemic and nonischemic heart failure after cardiac resynchronization therapy. Circulation 2004; 110 : 66-73.
28. Yu CM, Fung WH, Lin H et al. Predictors of left ventricular reverse remodeling after cardiac resynchronization therapy for heart failure secondary to idiopathic dilated or ischemic cardiomyopathy. Am J Cardiol 2003; 91 : 684-688.
29. Yu CM, Lin H, Zhang Q et al. High prevalence of left ventricular systolic and diastolic asynchrony in patients with congestive heart failure and normal QRS duration. Heart 2003; 89 : 54-60.
30. Yu CM, Zhang Q, Chan YS et al. Tissue Doppler velocity is superior to displacement and strain mapping in predicting left ventricular reverse remodelling response after cardiac resynchronisation therapy. Heart 2006; 92 : 1452-1456.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2007 Issue 11-
All articles in this issue
- Diagnostický prínos použitia implantovaného slučkového rekordéra (Reveal Plus) u pacientov so synkopou nejasnej etiológie
- Dlouhodobé výsledky srdeční resynchronizační léčby u pacientů s těžkým srdečním selháním
- Využití stanovení glykogenfosforylázy BB v diagnostice algické formy akutních koronárních syndromů
- Bazický fibroblastový růstový faktor (bFGF) a cévní endotelový růstový faktor (VEGF) jsou zvýšeny v plazmě periferní krve nemocných s chronickou lymfocytární leukemií a klesají po intenzivní léčbě obsahující fludarabin
- Variabilita plazmatických hladin big endotelinu a NT-proBNP u nemocných se srdečním selháním v chronickém hemodialyzačním programu
- Endoskopická diagnostika a léčba biliárních komplikací po laparoskopické cholecystektomii
- Vliv obezity na genovou expresi adiponektinu a jeho receptorů v subkutánní tukové tkáni
- Rituximab (MabThera®) - nový biologický lék v terapii revmatoidní artritidy
- Syndrom horní duté žíly: definice, etiologie, fyziologie, symptomy, diagnostika a léčba
- Význam endoskopické cytoskopie u vyšetření trávicího traktu
-
Diagnostika a léčba chronické hepatitidy B
Doporučený postup České hepatologické společnosti České lékařské společnosti J. E. Purkyně a Společnosti infekčního lékařství České lékařské společnosti J.E. Purkyně
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Syndrom horní duté žíly: definice, etiologie, fyziologie, symptomy, diagnostika a léčba
- Rituximab (MabThera®) - nový biologický lék v terapii revmatoidní artritidy
- Diagnostický prínos použitia implantovaného slučkového rekordéra (Reveal Plus) u pacientov so synkopou nejasnej etiológie
- Endoskopická diagnostika a léčba biliárních komplikací po laparoskopické cholecystektomii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

