-
Medical journals
- Career
Diagnostika a léčba chronické hepatitidy B
Doporučený postup České hepatologické společnosti České lékařské společnosti J. E. Purkyně a Společnosti infekčního lékařství České lékařské společnosti J.E. Purkyně
Authors: P. Husa 1; S. Plíšek 2; J. Šperl 3; P. Urbánek (koordinátoři) 4; J. Galský 5; P. Hůlek 6; P. Kümpel 7; V. Němeček 8; M. Volfová (abecedně) 9
Authors‘ workplace: Klinika infekčních chorob Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MUDr. Petr Husa, CSc. 1; Infekční klinika Lékařské fakulty UK a FN Hradec Králové, přednosta doc. MUDr. Václav Dostál 2; Klinika hepatogastroenterologie IKEM Praha, přednosta doc. MUDr. Julius Špičák, CSc. 3; Interní klinika 1. lékařské fakulty UK a ÚVN Praha, přednosta doc. MUDr. Miroslav Zavoral, Ph. D. 4; Infekční oddělení nemocnice Mělník, přednosta prim. MUDr. Jan Galský, Ph. D. 5; II. interní klinika Lékařské fakulty UK a FN Hradec Králové, přednosta prof. MUDr. Jaroslav Malý, CSc. 6; Infekční oddělení Slezské nemocnice Opava, přednosta prim. MUDr. Petr Kümpel 7; Národní referenční laboratoř pro virové hepatitidy Státního zdravotního ústavu v Praze, ředitel MUDr. Jaroslav Volf, Ph. D. 8; Hepato-Gastroenterologie HK s r. o., Hradec Králové 9
Published in: Vnitř Lék 2007; 53(11): 1221-1230
Category: Guidelines
Tento doporučený postup byl schválen výbory Česká hepatologické společnosti České lékařské společnosti J.E. Purkyně a Společnosti infekčního lékařství České lékařské společnosti J.E. Purkyně a byl současně zaslán k publikaci i v časopise Klinická mikrobiologie a infekční lékařství v září roku 2007.
Overview
Chronická hepatitida B je v celosvětovém měřítku jedním z nejčastějších infekčních onemocnění. V České republice je prevalence 0,56 %. Antivirová léčba chronické hepatitidy B prokazatelně zvyšuje kvalitu života a při splnění indikačních kritérií a standardních terapeutických postupů je jednoznačně levnější než léčba komplikací pokročilé jaterní cirhózy či hepatocelulárního karcinomu. Pro léčbu chronické hepatitidy B byly v České republice v době vydání tohoto doporučení kategorizovány 4 léky - pegylovaný interferon (IFN) α-2a, konvenční IFNα, lamivudin (LAM) a adefovir dipivoxil (ADV). V řadě jiných vyspělých států světa byly pro léčbu schváleny i entecavir (ETV) a telbivudin (LdT). Nejúčinnější dostupnou léčbu představuje v současnosti pegylovaný IFNα-2a, proto by měl být lékem první volby pro iniciální terapii chronické hepatitidy B, HBeAg pozitivní i negativní formy, pokud nejsou přítomny kontraindikace léčby IFNα. Použít lze i konvenční (standardní, klasický) IFNα, který je ale podle výsledků klinických studií méně účinný než pegylovaný IFNα-2a. Hlavní předností interferonů oproti ostatním komerčně dostupným lékům je relativně kratší a jasně definovaná doba léčby, velká pravděpodobnost setrvalosti dosaženého útlumu virové replikace a sérokonverze HBeAg/anti-HBe (u HBeAg pozitivní formy onemocnění) a absence vzniku mutant HBV rezistentních na IFN během léčby. Pokud je IFNα (pegylovaný i konvenční) kontraindikovaný, neúčinný nebo špatně tolerovaný, je na místě podání ADV, ETV, LAM nebo LdT. Léčba LAM a LdT je často provázena vznikem mutant HBV, které jsou na lamivudin nebo LdT rezistentní, proto není preferována.
Klíčová slova:
chronická hepatitida B - pegylovaný interferon (IFN) α-2a - interferon (IFN) α - lamivudin - adefovir dipivoxil - entecavir – telbivudin1. Proč léčit chronickou infekci virem hepatitidy B?
Podle kvalifikovaných odhadů je celosvětově chronicky infikováno virem hepatitidy B (HBV) asi 350 milionů lidí. Česká republika patří mezi státy s nízkou prevalencí infekce HBV. Podle posledních sérologických přehledů z roku 2001 je 0,56 % našich občanů chronicky infikováno HBV. Ročně je hlášeno 300-500 případů akutních virových hepatitid B. Do chronického stadia přejde méně než 5 % akutních hepatitid B u dospělých imunokompetentních pacientů. Imunokompromitovaní nemocní (pacienti v chronickém hemodialyzačním programu, pacienti podstupující protinádorovou či imunosupresivní léčbu, koinfikovaní virem lidského imunodeficitu - HIV) mají sníženou schopnost rozeznat a/nebo eliminovat infekci HBV, a proto u nich přechází infekce HBV do chronicity ve více než 50 %. Pravděpodobnost chronicity u novorozenců infikovaných HBV vertikálně od matky je vyšší než 90 %, při infikování dětí mladších 5 let je pravděpodobnost vzniku chronické infekce HBV 25-50 %. Infekce novorozenců a malých dětí jsou v současné době v České republice naprosto výjimečné díky screeningu všech těhotných žen na přítomnost HBsAg a následné pasivní a aktivní imunizaci novorozenců HBsAg pozitivních matek. Navíc od roku 2001 je v naší republice prováděna plošná vakcinace dětí od 13. týdne věku a 12letých proti HBV.
Infekce HBV může vyvolat závažná, život ohrožující poškození jater - fulminantní hepatitidu, jaterní cirhózu a prokázaný je i příčinný vztah mezi HBV infekcí a hepatocelulárním karcinomem (HCC) - primární rakovinou jater. Jaterní cirhóza vyvolaná infekcí HBV patří mezi obecně uznávané indikace transplantace jater. Dostupné terapeutické možnosti mají jak krátkodobý, tak dlouhodobý přínos. Léčba jednoznačně zvyšuje kvalitu života a je „cost effective“, tj. při splnění indikačních kritérií a při použití standardních postupů je terapie levnější, než léčba komplikací pokročilé jaterní cirhózy.
2. Přirozený průběh a klinický obraz HBV infekce
Infekce HBV je spojena s velmi heterogenním spektrem jaterních onemocnění:
- Akutní hepatitida B - většinou benigní onemocnění končící ve většině případů spontánním uzdravením, v 0,1-1 % případů probíhá onemocnění fulminantně s vysokou mortalitou.
- Chronická hepatitida B - infekce trvající déle než 6 měsíců. Jde o nesourodou skupinu nemocných, kterou lze rozdělit z hlediska přirozeného vývoje chronické HBV (resp. přítomnosti koinfekce jiným hepatotropním virem) infekce na následující podskupiny:
A. Fáze přirozeného vývoje chronické HBV infekce:
- a) Chronická hepatitida B ve fázi replikační, HBeAg pozitivní forma. Jedná se o HBsAg i HBeAg pozitivní pacienty s vysokou viremií (HBV DNA v séru > 20 000 IU/ml, což odpovídá přibližně 105 kopií/ml dle staršího způsobu vyjadřování viremie), aktivita ALT je obvykle zvýšena, může být i normální. V jaterní biopsii jsou prokazatelné středně nebo vysoce závažné zánětlivě-nekrotické změny. Jedná se o infekci tzv. „wild“ typem HBV, tj. nemutovaným virem.
- b) Chronická hepatitida B ve fázi replikační, HBeAg negativní forma. HBsAg pozitivní, ale HBeAg negativní pacienti s relativně vysokou viremií (HBV DNA v séru je většinou mezi 2 000-20 000 IU/ml, což odpovídá 104-105 kopií/ml), menší část nemocných má HBV DNA v séru vyšší než 20 000 IU/ml (105 kopií/ml). Aktivita ALT je obvykle alespoň intermitentně zvýšena, může však být i trvale normální. V jaterní biopsii jsou prokazatelné středně nebo vysoce závažné zánětlivě-nekrotické změny. Negativita HBeAg je podmíněna mutací v tzv. pre-core nebo v basal core promotor (BCP) oblasti genomu viru.
- c) Chronická hepatitida B ve fázi nízké replikace, tzv. inaktivní nosiči HBsAg. HBsAg pozitivní a HBeAg negativní, pacienti s normálním ALT a nízkou viremií. HBV DNA bývá < 2 000 IU/ml (104 kopií/ml). V jaterní biopsii nelze prokázat významné zánětlivé změny.
- d) Stav po hepatitidě B, tzv. fáze HBsAg negativity. HBsAg je negativní, prodělanou HBV infekci lze identifikovat jen na podkladě anamnestických protilátek (pozitivita celkových anti-HBc protilátek). Perzistence HBV v organizmu i po dosažení HBsAg negativity je trvalá, u některých HBsAg negativních jedinců s izolovanou pozitivitou anti-HBc lze prokázat nízkou úroveň viremie (HBV DNA v rozmezí 2-20 IU/ml, tedy 101-102 kopií/ml), u jiných nelze HBV DNA v séru prokázat ani nejcitlivější polymerázovou řetězovou reakcí (PCR) v reálném čase. I u nich však lze většinou prokázat nízkou koncentraci HBV DNA v jaterní tkání.
B. Koinfekce HBV s dalšími viry:
- a) koinfekce s virem hepatitidy D (HDV): hladina HBV DNA v séru je u těchto nemocných většinou < 2 000 IU/ml (103 kopií/ml). Výskyt infekce HDV je v podmínkách České republiky raritní.
- b) koinfekce s virem hepatitidy C (HCV): replikace HCV v naprosté většině případů utlumí replikaci HBV, proto je většinou vysoká hladina HCV RNA a nízká (až neprokazatelná) HBV DNA v séru.
- c) koinfekce s virem lidského imunodeficitu (HIV): tito nemocní mají většinou vysokou hladinu HBV DNA v séru, nižší pravděpodobnost dosažení spontánní sérokonverze HBeAg/anti-HBe, závažnější histologický jaterní nález a zvýšenou mortalitu na jaterní choroby. U koinfekce HIV/HBV se častěji vyskytují případy s negativitou HBsAg v séru, ale pozitivitou celkových protilátek anti-HBc, vysokou hladinou HBV DNA v séru a významnými histologickými změnami v játrech. Proto je velmi důležité u všech HIV-pozitivních osob testovat nejen přítomnost HBsAg v séru, ale i celkových protilátek anti-HBc, a v případě průkazu těchto protilátek stanovit HBV DNA v séru. V literatuře jsou popsána závažná vzplanutí chronické infekce HBV u HIV pozitivních pacientů s původně nízkou hladinou CD4 lymfocytů po zlepšení stavu imunitního systému v důsledku vysoce účinné antiretrovirové terapie (HAART).
Poznámky k přirozenému vývoji chronické infekce HBV
Fáze imunotolerance HBV: pacienti s chronickou hepatitidou B ve fázi replikační - skupiny (a) a (b) ve výše uvedeném dělení - mohou mít i při vysoké viremii normální aktivitu ALT v séru díky imunotoleranci viru. Přechodná fáze imunotolerance, trvající i roky, bývá v počáteční fází vývoje chronické hepatitidy B. Trvalá imunotolerance je typická pro nemocné, infikované vertikálně od matky. Mechanizmus poškození jater virem hepatitidy B je imunitně zprostředkovaný, replikace HBV sama nevede k destrukci hepatocytu. HBsAg pozitivní pacienty s imunotolerancí HBV a inaktivní nosiče lze odlišit pouze kvantitativním vyšetřením viremie. Fáze imunotolerance trvá nejčastěji 15-25 let
HBeAg negativní forma chronické hepatitidy B: tato forma chronické hepatitidy B je častá ve Středomoří a v Asii. V České republice není její výskyt přesně zmapován, ale vzhledem k relativnímu stárnutí populace osob chronicky infikovaných HBV její výskyt stále narůstá. V důsledku mutace v precore nebo BCP oblasti genomu HBV se netvoří HBeAg, přestože virus se aktivně replikuje. Většina nemocných s HBeAg negativní formou chronické hepatitidy má nižší viremii, než je tomu u HBeAg pozitivních nemocných, což ale neznamená, že jde o méně závažnou infekci. Naopak jde většinou o nemocné infikované HBV významně delší dobu než v případě HBeAg pozitivity, proto více ohrožené jaterní cirhózou a HCC. Pro HBeAg negativní chronickou hepatitidu B je typické kolísání aktivity ALT.
„Okultní“ HBV infekce: pacienti jsou HBsAg negativní s prokazatelnou přítomností HBV DNA v játrech nebo i v séru. Obvykle jsou identifikováni díky jinak nevysvětlitelnému zvýšení aktivity ALT nebo nálezu HBV DNA u osob s pozitivitou celkových protilátek anti-HBc jako jediným markérem infekce HBV nebo u osob s kombinací pozitivních celkových protilátek anti-HBc a nízce pozitivních protilátek anti-HBs. Příčiny vzniku okultní HBV infekce nejsou známé, ale uvažuje o vlivu imunitní odpovědi hostitele nebo interferenci s jiným agens (např. HCV, HIV) a příčinou může být i několik současných mutací v genomu HBV, které činí HBsAg sérologicky neprokazatelným.
3. Diagnostika infekce HBV
Přehled sérologických a molekulárně genetických nálezů u infekce HBV a jejich význam je uveden v tab. 1. Uvedené nálezy představují nejčastější a nejjednodušší možné varianty. V případech různých mutací virového genomu se mohou sérologické nálezy významně lišit. Při nejasnostech je proto vhodné konzultovat specializované pracoviště. Jako klinicky významná úroveň replikace HBV se uvádí hladina > 20 000 IU/ml (105 kopií/ml) u HBeAg pozitivní chronické hepatitidy B. U HBeAg negativní chronické hepatitidy B se jako významná bere většinou hladina HBV DNA v séru vyšší než 2 000 IU/ml (104 kopií/ml), s přihlédnutím k aktivitě ALT, histologickému nálezu, věku a přítomnosti rizikových faktorů HCC.
Table 1. Typické sérologické a molekulárně genetické nálezy jednotlivých stadií přirozeného vývoje infekce HBV. 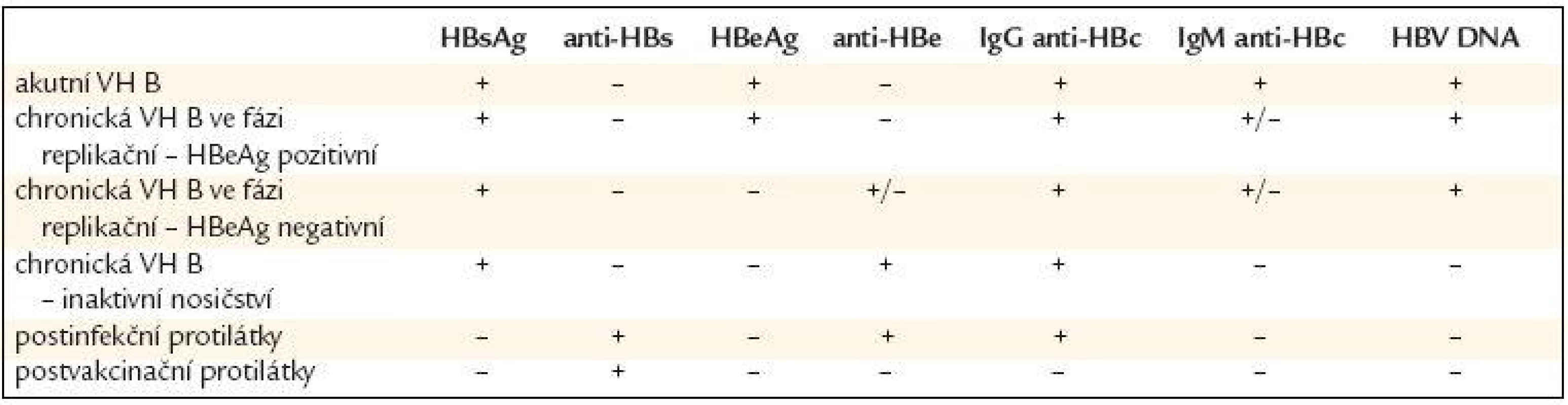
VH B – virová hepatitida B K průkazu HBV DNA v séru se používá především PCR. V současnosti se většinou používá vysoce senzitivní PCR v reálném čase. Výsledky získané touto metodou jsou udávány v mezinárodních jednotkách (International Units) na mililitr (IU/ml). Je nezbytně nutné kvantifikovat množství viru v séru validovanými testy s citlivostí alespoň v řádu stovek IU/ml. Hladinu HBV DNA vyjádřenou v IU/ml lze orientačně přepočítat na kopie na mililitr pomocí vzorce: HBV DNA (IU/ml) × 5 = HBV DNA (kopie/ml).
Kvantitativní stanovení HBV DNA v séru je nutné provést:
- a) vždy před zahájením antivirové terapie - léčíme jen osoby s významnou viremii (HBV DNA v séru > 20 000 IU/ml (105 kopií/ml), u HBeAg negativní chronické hepatitidy B se jako významná bere hladina HBV DNA v séru > 2 000 IU (104 kopií/ml), s přihlédnutím k aktivitě ALT, histologickému nálezu, věku a přítomnosti rizikových faktorů HCC;
- b) v průběhu protivirové léčby v 3-6měsíčních intervalech k monitorování účinku léčby a k podchycení vzniku rezistentních mutant viru;
- c) v době skončení protivirové léčby a po 3, 6 a 12 měsících po skončení této léčby k posouzení úspěšnosti protivirové léčby a odhalení možného návratu aktivní virové replikace.
4. Antivirová terapie chronické infekce virem hepatitidy B
Před zahájením antivirové léčby infekce HBV musí být splněna následující kritéria:
- a) přítomnost chronické infekce HBV, tedy doba trvání infekce > 6 měsíců;
- b) přítomnost významné virové replikace (u HBeAg pozitivní formy HBV DNA v séru > 20 000 IU/ml, u HBeAg negativní formy hladina HBV DNA v séru > 2 000 IU);
- c) biochemická či morfologická aktivita nebo progredující fibróza jater.
Pro všechny dostupné léčebné možnosti platí, že vyšší naději na terapeutický úspěch mají osoby s vyšší počáteční aktivitou sérových aminotransferáz. Pacienti s vysokou viremií a normální či minimálně zvýšenou aktivitou ALT mají malou naději na úspěch v časově omezené léčbě. Tito pacienti by měli být léčeni jen při histologicky prokazatelné progredující fibróze jater nebo při výskytu extrahepatální komplikace HBV infekce (polyarteriitis nodosa či glomerulonefritida spojená s infekcí HBV).
Pro léčbu chronické infekce HBV lze použít následující léky:
- pegylovaný interferon (PEG-IFN) α-2a,
- interferon (IFN) α, tzv. konvenční, klasický nebo standardní,
- lamivudin (LAM),
- adefovir dipivoxil (ADV),
- entecavir (ETV),
- telbivudin (LdT).
Pegylovaný IFNα-2a se podává v dávce 180 μg 1krát týdně podkožně. Doba léčby je 48 týdnů u pacientů HBeAg pozitivních i negativních. Je nejúčinnějším lékem ve smyslu dosahování sérokonverzí HBeAg/anti-HBe či setrvalých virologických odpovědí (u HBeAg negativní formy).
Doporučená dávka konvenčního IFNα je 5-10 milionů mezinárodních jednotek (IU) 3krát týdně subkutánně po dobu 4-6 měsíců, nebo denně po dobu 4 měsíců u HBeAg pozitivních nemocných. U infekce HBeAg-minus mutantním virem je doporučována delší doba léčby, zpravidla 12 měsíců.
Při léčbě lamivudinem u dospělých, s kreatininovou clearance > 50 ml/min, se denně podává 100 mg přípravku v 1 dávce. Doba podávání LAM nebyla zatím jednoznačně stanovena. Většinou se udává, že by měla u infekce virem, který tvoří HBeAg, trvat do sérokonverze HBeAg/anti-HBe, ale nejméně 1 rok. Pro snížení nebezpečí obnovení virové replikace po skončení léčby je vhodné podávat LAM ještě minimálně 6 měsíců po dosažení sérokonverze HBeAg/anti-HBe. U infekce HBeAg-minus mutantním virem se obecně doporučuje léčba dlouhodobá, ve většině případů trvalá. Cílový bod léčby, kterým je u HBeAg pozitivních pacientů sérokonverze HBeAg/anti-HBe, není při léčbě HBeAg negativních nemocných jasně stanoven. Může jím být až sérokonverze HBsAg/anti-HBs, ke které však dochází během léčby zřídka. Po vysazení antivirové léčby dochází často k relapsu onemocnění, i když v době léčby není HBV DNA v séru opakovaně prokázána ani vysoce senzitivní metodou PCR v reálném čase. Léčba LAM je často provázena vznikem mutant HBV, které jsou na lamivudin částečně nebo úplně rezistentní. Frekvence výskytu těchto rezistentních mutant HBV s délkou léčby narůstá (23 % po 1 roce léčby, 46 % po 2 letech, 55 % po 3 letech, 71 % po 4 letech a 65 % po 5 letech léčby).
Doporučená dávka adefoviru dipivoxilu je 10 mg denně. Tento lék je v České republice kategorizován pouze pro léčbu nemocných, u kterých se vyvinula v průběhu léčby mutanta viru rezistentní na LAM. Obecně je však doporučován i pro léčbu dosud neléčených (naivních) pacientů HBeAg pozitivních i negativních. Pro délku léčby ADV platí stejná doporučení jako pro léčbu LAM. Předností ADV je účinnost i u LAM rezistentních mutací a pozdější vznik a nižší frekvence výskytu ADV rezistentních mutací při dlouhodobé léčbě, než je tomu u lamivudinu.
Entecavir je dle výsledků klinických studií in vitro účinnější než LAM nebo ADV a je účinný i na mutanty viru rezistentní na lamivudin, i když méně než na divoký (wild) typ viru. Podává se 1krát denně perorálně v dávce 0,5 mg pacientům dosud neléčeným lamivudinem a v dávce 1 mg denně při infekci mutantou HBV rezistentní na LAM.
Telbivudin je podle výsledků klinických studií účinnější než LAM v potlačení virové replikace. Denní dávka LdT je 600 mg per os. Do 2 let léčby vznikají mutanty rezistentní na LdT zhruba u 25 % léčených. Mutanty HBV rezistentní na LdT jsou zkříženě rezistentní i na LAM.
Entecavir ani telbivudin nebyly v době vydání tohoto Doporučeného postupu v České republice kategorizovány pro léčbu chronické infekce HBV.
Další účinné léky na léčby chronické infekce HBV (dosud neschválené pro léčbu chronické infekce HBV v České republice):
- emtricitabin (FTC),
- tenofovir (TDF),
- clevudin (LFMAU).
Emtricitabin je strukturálně podobný LAM, proto je léčba provázena vznikem stejných rezistentních mutant HBV, jako je tomu u LAM. V klinické studii byl podáván v denní dávce 200 mg. Tenofovir je nukleotidový analog strukturálně podobný ADV. Protože je méně nefrotoxický než ADV, je možné jej bezpečně podávat v mnohem vyšší dávce než ADV (300 mg vs 10 mg denně). V této dávce vede k významně vyšší redukci sérové HBV DNA než ADV. Kombinovaný preparát Truvada, který obsahuje FTC a TDF, se používá pro léčbu infekce HIV a je účinný i při chronické infekci HBV. Clevudin je pro léčbu chronické infekce HBV schválen zatím jen v Jižní Koreji. Denní dávka je 30 mg.
5. Kontraindikace léčby chronické infekce virem hepatitidy B
- nepřítomnost významné virové replikace (absolutní kontraindikace)
- nepřítomnost biochemické či morfologické aktivity či progredující fibrózy (relativní kontraindikace)
- kontraindikace léčby interferonem α (konvenčním i pegylovaným):
- dekompenzovaná jaterní cirhóza Child-Pugh B nebo C
- nekontrolované neurologické a psychiatrické onemocnění
- klinicky významná periferní neutropenie (< 1,2 x 109/l)
- trombocytopenie (< 50 x 109/l)
- autoimunitní onemocnění (relativní kontraindikace)
- aktivní toxikomanie, alkoholizmus
- gravidita a laktace
- dekompenzovaný nebo nestabilní diabetes mellitus
- závažná kardiovaskulární onemocnění (infarkt myokardu, městnavé srdeční selhání, klinicky závažné arytmie, těžká hypertenze, chlopenní vady)
- orgánové transplantace s výjimkou jater
- věk nad 70 let (relativní kontraindikace - závisí na celkovém stavu a motivaci pacienta)
- kontraindikace léčby lamivudinem: léčba LAM prakticky nemá kontraindikace. Při jeho podání pacientům s renální insuficiencí (kreatininová clearance < 50 ml/min) je třeba redukovat dávky podle tab. 2. Objevují se i práce vyhodnocující jeho podávání v graviditě, které nezaznamenaly žádný teratogenní efekt, naopak došlo k poklesu vertikálního přenosu HBV na plod. Tento postup však nelze zatím jednoznačně považovat za standardní.
- kontraindikace léčby adefovirem dipivoxilem: rovněž léčba ADV nemá známé kontraindikace. Při jeho podání pacientům s renální insuficiencí (kreatininová clearance < 50 ml/min) je třeba prodlužovat intervaly mezi jednotlivými dávkami podle tab. 3.
- kontraindikace entecaviru: léčba ETV prakticky nemá kontraindikace. Při jeho podání pacientům s renální insuficiencí (kreatininová clearance < 50 ml/min) je třeba redukovat dávky podle tab. 4.
- kontraindikace telbivudinu: rovněž léčba LdT nemá známé kontraindikace. Při jeho podání pacientům s renální insuficiencí (kreatininová clearance < 50 ml/min) je třeba prodlužovat intervaly mezi jednotlivými dávkami podle tab. 5.
Table 2. Redukce dávky lamivudinu při renální nedostatečnosti. 
Table 3. Prodlužování intervalu mezi jednotlivými dávkami adefoviru dipivoxilu při renální nedostatečnosti. 
Table 4. Redukce dávky entecaviru při renální nedostatečnosti. 
Table 5. Prodlužování intervalu mezi jednotlivými dávkami telbivudinu při renální nedostatečnosti. 
6. Cíle a strategie léčby chronické infekce virem hepatitidy B
Primárním cílem léčby je redukce hladiny HBV DNA, tj. vymizení či výrazné potlačení virové replikace a její udržení na minimální možné úrovni co nejdelší dobu, nejlépe trvale. Dosažení tohoto cíle je spojeno s histologickým zlepšením, poklesem až normalizací aktivity ALT, snížením rizika rozvoje hepatocelulárního karcinomu.
V současné době lze v léčbě chronické hepatitidy B rozlišit 2 základní postupy léčby. V první řadě se jedná o časově omezenou léčbu. U HBeAg pozitivní formy chronické hepatitidy je cílem dosažení sérokonverze HBeAg/anti-HBe a snížení viremie pod hranici detekovatelnosti metodou PCR, které trvají i po ukončení léčby. U HBeAg negativní formy chronické hepatitidy B je cílem časově omezené léčby snížení viremie pod hranici detekovatelnosti metodou PCR, které trvá i po skončení léčby tzv. setrvalá virologická odezva. Lékem volby pro časově omezenou léčbu je PEG-IFNα-2a. Použít lze i konvenční (standardní, klasický) IFNα, který je ale podle výsledků klinických studií méně účinný než PEG-IFNα-2a.
Nepodaří-li se časově omezenou léčbou dosáhnout sérokonverze HBeAg/anti-HBe nebo setrvalé virologické odpovědi u HBeAg negativní formy, nebo jsou-li kontraindikace léčby interferonem α, jsou pacienti s aktivní chronickou hepatitidou či progredující jaterní fibrózou indikováni k dlouhodobé časově neomezené léčbě, jejímž cílem je dlouhodobě suprimovat replikaci HBV a zastavit, či zpomalit progresi jaterního onemocnění. Lékem volby pro dlouhodobou léčbu jsou ADV nebo ETV, naproti tomu LAM či LdT jsou pro dlouhodobou léčbu méně vhodné vzhledem k velké pravděpodobnosti vzniku mutant HBV rezistentních na tyto preparáty. Pro trvání dlouhodobé léčby chronické hepatitidy B neplatí dosud žádná standardní doporučení, rozhodnutí o ukončení závisí na zhodnocení případu ošetřujícím lékařem. Nepochybně lze léčbu ukončit, dojde-li k vymizení HBsAg, u imunosuprimovaných pacientů je ale nutno počítat s možností závažné rekurence onemocnění i po vymizení HBsAg.
7. Optimální léčba chronické infekce virem hepatitidy B
Pro léčbu chronické hepatitidy B jsou v současnosti v České republice kategorizovány 4 léky - PEG-IFNα-2a, konvenční IFNα, LAM a ADV. V řadě jiných vyspělých států světa jsou pro léčbu schváleny i ETV a LdT. Nejúčinnější dostupnou léčbu představuje v současnosti PEG-IFNα-2a, proto by měl být lékem první volby pro iniciální terapii chronické hepatitidy B, HBeAg pozitivní i negativní formy, pokud nejsou přítomny kontraindikace léčby interferonem α. Použít lze i konvenční (standardní, klasický) IFNα, který je ale podle výsledků klinických studií méně účinný než PEG-IFNα-2a. Hlavní předností interferonů oproti ostatním komerčně dostupným lékům je relativně kratší a jasně definovaná doba léčby, velká pravděpodobnost setrvalosti dosaženého útlumu virové replikace a sérokonverze HBeAg/anti-HBe (u původně HBeAg pozitivních pacientů) a absence vzniku mutant HBV rezistentních na interferon během léčby. Pokud je interferon α (pegylovaný i konvenční) kontraindikovaný, neúčinný nebo špatně tolerovaný, je na místě podání ADV, ETV, LAM nebo LdT. Léčba LAM a LdT je často provázena vznikem mutant HBV, které jsou na lamivudin nebo LdT částečně nebo úplně rezistentní, proto není preferována. Vznik těchto mutací (genotypová rezistence) se in vitro projeví sníženou citlivostí HBV na podávaný lék (fenotypová rezistence) a klinicky opětovným vzestupem HBV DNA v séru v průběhu antivirové léčby (virologický breakthrough) a většinou i vzestupem aktivity ALT (biochemický breakthrough), tab. 6.
Table 6. Definice termínů týkajících se rezistence na nukleosidová či nukleotidová analoga používaná k léčbě chronické infekce HBV. 
V České republice bylo možné v době vydání tohoto Doporučeného postupu po neúspěšné léčbě PEG-IFNα-2a nebo konvenčním IFNα, nebo při kontraindikacích léčby těmito léky, podat pouze LAM a teprve v případě vzniku rezistentní mutanty viru ADV.
Kombinovaná léčba LAM a IFNα, pegylovaným nebo konvenčním, není účinnější než monoterapie interferony. Kombinovaná terapie dvěma nukleosidovými analogy či kombinací nukleosidového a nukleotidového analoga není dle výsledků klinických studií u dosud neléčených (naivních) pacientů účinnější než monoterapie, co se týče dosažení setrvalé virologické odpovědi. U zvláště ohrožených osob - cirhotiků (zejména dekompenzovaných), pacientů před a po transplantaci jater, imunosuprimovaných pacientů - je kombinovaná léčba LAM a ADV spojena se menším nebezpečím vzniku rezistentních mutant HBV a fatálních vzplanutí hepatitidy (flare-up) při nahrazování lamivudinu adefovirem. Kombinovaná léčba následující vznik rezistence na původní antivirovou terapii je uvedena v kapitole 8.
8. Terapie chronické infekce virem hepatitidy B u zvláštních skupin pacientů
A. Pacienti, kteří nereagovali na předchozí léčbu konvenčním IFNα
U pacientů, kteří již byli léčeni konvenčním IFNα a nedošlo u nich k dlouhodobému efektu, je vhodná léčba PEG-IFNα-2a (48 týdnů) nebo dlouhodobá léčba ADV či ETV. Dlouhodobá léčba LAM či LdT není obecně preferována vzhledem k vysoké pravděpodobnosti vzniku rezistence na tyto léky během dlouhodobého podávání. V době vydání tohoto Doporučeného postupu je však léčba LAM jedinou možností.
B. Pacienti primárně rezistentní na nukleosidová či nukleotidová analoga
Jako primární rezistence na léčbu LAM, ADV, ETV či LdT je definován stav, při němž dojde během prvních 24 týdnů léčby k poklesu hladiny HBV DNA v séru o méně než 2 dekadické logaritmy IU/ml. V těchto případech je nutné přejít na léčbu jiným vhodným lékem schváleným pro léčbu chronické infekce HBV.
C. Pacienti s rezistencí na nukleosidová či nukleotidová analoga vzniklou během léčby
Pokud dojde během antivirové léčby k vzestupu hladiny HBV DNA v séru minimálně o 1 dekadický logaritmus oproti nejnižší hladině dosažené během léčby (nadir), vzniká podezření na vznik mutanty HBV rezistentní na podávaný lék. Je třeba zopakovat stanovení HBV DNA v séru a v případě potvrzení vzestupu hladiny HBV DNA provést následující opatření:
- a) zkontrolovat komplianci pacienta (až 30 % virologických breakthrough je způsobeno nedostatečnou kompliancí)
- b) pokud je to možné, potvrdit vznik rezistentní mutanty HBV in vitro
- c) přejít na alternativní léčbu (viz níže)
- d) výjimečně lze antivirovou léčbu bez náhrady ukončit (pouze u pacientů s kompenzovanou jaterní chorobou, zejména mladých). Potom je však nutné monitorovat hladinu HBV DNA v séru a aktivitu ALT minimálně každé 3 měsíce a v případě výrazného vzestupu viremie a zejména aktivity ALT je nutné zahájit antivirovou léčbu podle principů uvedených níže.
- rezistence na lamivudin: v případě vzniku rezistentní mutanty na LAM jsou obecně možné následující možnosti následné léčby:
- přidání ADV k LAM
- přidání TDF k LAM
- ukončení léčby LAM, zahájení léčby lékem Truvada (kombinace TDF a FTC)
- ukončení léčby LAM, zahájení léčby ETV
V době vydání tohoto Doporučeného postupu bylo v České republice možné jen přidání ADV k LAM. V této indikaci lze uvažovat i o podání PEG-IFNα-2a. Výsledky klinické studie s omezeným počtem pacientů ukazují dobrou účinnost a vysokou bezpečnost léčby PEG-IFNα-2a u těchto pacientů.
- Rezistence na adefovir dipivoxil: v případě vzniku rezistentní mutanty na ADV jsou obecně možné následující možnosti následné léčby:
- přidání LAM k ADV,
- ukončení léčby ADV, zahájení léčby lékem Truvada (= kombinace TDF a FTC),
- zahájit léčbu ETV, ev. tento lék přidat k ADV.
V době vydání tohoto Doporučeného postupu bylo v České republice možné jen přidání LAM k ADV. V této indikaci lze uvažovat i o podání PEG-IFNα-2a. Výsledky klinické studie s omezeným počtem pacientů ukazují dobrou účinnost a vysokou bezpečnost léčby PEG-IFNα-2a u těchto pacientů.
- rezistence na entecavir: v případě vzniku rezistentní mutanty na ETV je možné zahájit léčbu ADV nebo TDF nebo tyto léky přidat k ETV.
V době vydání tohoto Doporučeného postupu nebyl entecavir v České republice kategorizován.
- rezistence na telbivudin: platí stejná doporučení jako při vzniku rezistence na LAM
V době vydání tohoto Doporučeného postupu nebyl telbivudin v České republice kategorizován.
D. Pacienti s kompenzovanou jaterní cirhózou (Child A)
Pacienti s kompenzovanou jaterní cirhózou jsou indikováni k léčbě, pokud sérová hladina HBV DNA > 2 000 IU/ml (104 kopií/ml). Pokud je u těchto pacientů zvýšená sérová aktivita ALT, mají být léčeni bez ohledu na výši viremie. Do úvahy přichází především léčba ADV či ETV, zatímco léčba LAM či LdT není preferována vzhledem k nebezpečí vzniku rezistentních mutant HBV.
V době vydání tohoto Doporučeného postupu byl z výše uvedených léků v České republice kategorizován pouze LAM. Pokud se lékař rozhodne pro léčbu pegylovaným či konvenčním IFNα, je na místě velká opatrnost vzhledem k nebezpečí dekompenzace jaterní cirhózy.
E. Pacienti s dekompenzovanou jaterní cirhózou (Child B a C)
U pacientů s dekompenzovanou jaterní cirhózou může IFNα (konvenční i pegylovaný) vyvolat akutní exacerbaci aktivity jaterní choroby, která může skončit nezvládnutelným jaterním selháním. Tento stav je navíc komplikován prohloubením leukopenie, neutropenie a trombocytopenie účinkem IFNα. Následuje riziko vzniku závažných bakteriálních komplikací či krvácivých projevů. Z uvedených důvodů je léčba IFNα, pegylovaným i konvenčním, u cirhotiků ve stadiu Child-Pugh C kontraindikována vždy a ve stadiu Child-Pugh B v naprosté většině případů.
Léčba těchto závažně nemocných pacientů by měla být prováděna buď přímo lékaři transplantačního centra, nebo v úzké součinnosti s nimi, vzhledem k nezbytnosti provedení transplantace jater v horizontu maximálně několika měsíců. Jako nejúčinnější se jeví u dekompenzovaných cirhotiků kombinace LAM a ADV. Oproti monoterapii jednotlivými preparáty je kombinovaná léčba spojena s nižší frekvencí vzniku rezistentních mutant HBV a rychleji je dosaženo signifikantní suprese virové replikace. Lamivudin může být velmi pravděpodobně nahrazen telbivudinem, ale zatím není dostatek dat o účinnosti a bezpečnosti tohoto léku u pacientů s dekompenzovanou cirhózou. Totéž platí pro monoterapii entecavirem.
Výsledky dosud publikovaných studií ukazují, že léčba LAM může u významné části nemocných s jaterní cirhózou zlepšit jaterní funkce. Přitom se ale ukazuje, že větší naději na úspěch má tato terapie u méně pokročilých jaterních procesů. Přežívání pacientů je více závislé na stupni závažnosti cirhózy v době zahájení léčby, než na přítomnosti či absenci HBeAg nebo výši HBV DNA před léčbou. Mladší věk, vyšší ALT a vyšší počet trombocytů představují významné příznivé předpovědní faktory klinické odezvy na léčbu. I přes zlepšení jaterních funkcí se však u části nemocný může vyvinout hepatocelulární karcinom. Vzácné, ale dokumentované, jsou i případy vzniku rezistentních mutant viru v průběhu léčby, jejichž objevení je provázeno rychlou dekompenzací jaterní cirhózy. Ve většině případů se však vzniklé YMDD mutanty projeví jen vzestupem sérové hladiny HBV DNA bez klinické manifestace. V případě selekce mutanty rezistentní na LAM je jedinou možností léčba ADV.
V době vydání tohoto Doporučeného postupu byly z výše uvedených léků v České republice kategorizovány pouze LAM a ADV.
F. Nemocní před a po transplantací jater pro konečná stadia chronické infekce virem hepatitidy B
Před transplantací jater se pacientům zařazeným na čekací listinu podává LAM, k němuž se v případě vzniku rezistence na LAM přidává ADV. Přidání ADV k LAM je rovněž vhodné v případě čekání na transplantaci jater delším než 6 měsíců. U pacientů s vysokou vstupní viremií je kombinovaná terapie LAM a ADV vhodná hned od zařazení na čekací listinu, protože se touto kombinací snižuje frekvence vzniku rezistentních mutant HBV a rychleji je dosaženo signifikantní suprese virové replikace. Po transplantaci jater je standardní profylaxí rekurence infekce HBV podávání kombinace LAM a hyperimunního imunoglobulinu proti HBV (HBIg). Při objevení rekurence infekce HBV, která představuje selhání profylaxe, se léčba HBIg ukončuje, protože hrozí vznik sérové nemoci při jejím pokračování, a přidává se ADV k LAM. Při selhání účinnosti léčby kombinací LAM a ADV je na místě léčba ETV.
V době vydání tohoto Doporučeného postupu nebyl ETV České republice kategorizován.
G. Imunosuprimovaní pacienti s hepatitidou B v anamnéze
Replikace HBV sama o sobě nevede k destrukci infikovaných hepatocytů, virus není ve většině případů cytopatogenní. Imunosupresivní léčba sice sníží imunitní reakci namířenou proti infikovaných hepatocytům, na druhou stranu oslabí imunitní kontrolu replikace viru. Zvyšuje se podíl infikovaných hepatocytů, replikace HBV výrazně stoupá a dosáhne úrovně, při které již vede k přímému poškození infikovaných hepatocytů, a HBV se tím stává cytopatogenní. Klinickým korelátem popsaných pochodů je rozvoj fibrotizující cholestatické hepatitidy, což je závažné život ohrožující onemocnění, během několika měsíců vede bez účinné léčby u většiny případů k selhání jater. Stav, při němž vede imunosupresivní léčba k výraznému nárůstu replikace HBV a vzplanutí hepatitidy u dosud inaktivního nosiče HBsAg, se označuje jako reaktivace chronické hepatitidy B. Rekurencí se rozumí stav, při němž se pacient, který prodělal hepatitidu B a vymizel u něj HBsAg ze séra, stane znovu HBsAg pozitivním a replikace HBV rychle roste. Virová nukleová kyselina totiž perzistuje trvale v hepatocytech ve formě tzv. cccDNA (covalently closed circular DNA), a to i u pacientů, kteří se stali HBsAg negativními. K úplné eliminaci HBV nikdy nedojde. Stav dříve nazývaný eliminací viru je jen účinnou imunitní kontrolou replikace s poklesem viremie pod hranici detekovatelnosti. Ztráta imunitní kontroly replikace viru vlivem imunosupresivní léčby tak vede k rekurenci hepatitidy B.
K reaktivaci replikace HBV dochází u 20-50 % inaktivních nosičů HBsAg podstupujících imunosupresivní či protinádorovou terapii. Reaktivace replikace HBV je častější, pokud chemoterapeutické režimy obsahují kortikosteroidy. Reaktivací hepatitidy B jsou ohroženi nejvíce pacienti s maligními lymfomy léčení rituximabem, ale i pacienti se solidními tumory, pacienti po transplantaci kostní dřeně, pacienti po orgánových transplantacích, dále pacienti s autoimunitními chorobami léčení klasickými imunosupresivy a nově i anti-TNF a anti-CD20 protilátkami. Reaktivace byla popsána i po intraarteriální embolizaci HCC. Reaktivace hepatitidy B obvykle přichází po 2-4 cyklech chemoterapie a klinický obraz kolísá od asymptomatického zvýšení aktivity aminotransferáz (50 %) k obrazu těžké akutní hepatitidy s ikterem (10 %), nejzávažnější variantou je fulminantní selhání jater (5 %).
V současné době je u pacientů HBsAg pozitivních preferována léčba preemptivní, která se zahajuje nejméně 1 týden před chemoterapií nebo imunosupresí. U pacientů s nízkou vstupní viremií (HBV DNA v séru < 2 000 IU/ml) se doporučuje podávat protivirové léky ještě 6 měsíců po skončení imunosupresivní či protinádorové terapie. Toto ukončení léčby je však možné jen u pacientů, u kterých se nepředpokládá opakování chemoterapie. V opačném případě je nutná léčba celoživotní. Léčba pacientů s vysokou vstupní viremií (> 2 000 IU/ml) musí pokračovat až do dosažení stejných cílových kritérií jako u imunokompetentních pacientů.
U pacientů s pozitivitou anti-HBc protilátek a negativitou HBsAg v séru, kteří jsou v riziku rekurence replikace HBV, není preemptivní protivirová léčba zatím jednoznačně doporučována. V každém případě jsou ale nutné pravidelné kontroly během imunosupresivní léčby či chemoterapie a zahájení protivirové léčby okamžitě při průkazu rekurence, resp. prvním vzestupu ALT.
K zábraně reaktivace či rekurence hepatitidy B se používá LAM nebo LdT, pokud lze předpokládat trvání léčby ≤ 12 měsíců (vzhledem k nebezpečí vzniku rezistence). V případě předpokládaného delšího trvání protivirové profylaxe jsou preferovány ADV a zejména ETV, který má rychlejší nástup účinku.
V době vydání tohoto Doporučeného postupu bylo v České republice jedinou možností podání LAM a přidání ADV v případě vzniku rezistence HBV na LAM.
H. Děti s chronickou hepatitidou B
Obecně se doporučuje se léčit děti ve věku ≥ 2 roky (ostatní indikační kritéria jsou stejná jako u dospělých). Použít lze však jen konvenční IFNα-2a nebo 2b nebo lamivudin. Ostatní léky nejsou pro léčbu dětí schváleny.
Doporučená dávka IFNα je dávku 6 MU/m2, maximálně 10 MU, 3krát týdně. Doba léčby je stejná jako u dospělých pacientů. Dávka LAM byla stanovena na 3 mg/kg/den, maximálně však 100 mg denně. Úspěšnost léčby dětí je srovnatelná s dospělými pacienty jak při použití IFNα, tak LAM. Při vyšší vstupní aktivitě ALT se úspěšnost léčby zvyšuje.
Lamivudin byl v České republice zatím registrován pouze pro léčbu chronické hepatitidy B u dospělých pacientů a u dětí nad 16 let. Léčba mladších dětí přichází do úvahy jen v rámci klinických studií.
I. Nemocní s renální nedostatečností a hemodialyzovaní nemocní
Léčba IFNα se u těchto nemocných neliší od doporučení platných pro ostatní pacienty s chronickou hepatitidou B. U pacientů s renální insuficiencí (kreatininová clearance < 50 ml/min) je nutné upravit denní dávky LAM, ADV, ETV a LdT v závislosti na hodnotách kreatininové clearance (tab. 2-5). U hemodialyzovaných pacientů nejsou zatím doporučení optimálních dávek lamivudinu jednoznačná. Dávkování ADV, ETV a LdT u hemodialyzovaných pacientů se řídí doporučeními uvedeným v tab. 3-5. PEG-IFNα-2a se podává u hemodialyzovaných pacientů v dávce 135 µg 1krát týdně podkožně.
J. Pacienti s koinfekcí HBV + HIV
Výrazným prodloužením délky života a zlepšením jeho kvality v důsledku vysoce aktivní antiretrovirové terapie (HAART) u HIV pozitivních osob se stává léčba chronické infekce HBV u těchto nemocných plně indikovanou. Kritéria pro léčbu chronické infekce HBV jsou u pacientů s koinfekcí HBV/HIV stejná, jsou při infekci pouze HBV.
Proti HBV i HIV jsou současně účinné LAM, FTC, TDF a ETV, ale při terapii LAM vzniká u pacientů s koinfekcí HBV/HIV po 4 letech podávání rezistence na LAM v 90 %, proto monoterapie LAM není u těchto pacientů vhodná.
Doporučení pro různé pacienty s koinfekcí HBV/HIV lze shrnout následovně:
- pacient, který dosud nevyžaduje HAART, by měl mít chronickou infekci HBV léčenu PEG-IFNα-2a nebo ADV
- pacient, u kterého je plánováno zahájení HAART i léčby HBV, byl měl dostat LAM v kombinaci s TDF nebo kombinaci TDF a FTC (Truvada)
- pacient úspěšně léčený HAART, která neobsahuje lék účinný i proti HBV, by měl být léčen PEG-IFNα-2a, ADV nebo ETV dohromady s pokračující HAART
- pokud vznikne rezistence na LAM, je nutné přidat TDF nebo ADV
- pokud selže HAART, je nutné do následné terapie HIV infekce zařadit lék účinný na infekci HIV i HBV
K. Pacienti s koinfekcí HBV a HDV
Infekce HDV je zatím v podmínkách České republiky naprosto ojedinělá. Musíme na ní myslet zejména u cizinců. Cílem léčby je u těchto nemocných útlum replikace HDV (HBV DNA bývá většinou negativní i metodou PCR díky supresivnímu vlivu HDV na replikaci HBV), který je většinou spojen s normalizací ALT a histologickým zlepšením. Výsledky terapie koinfekce HBV/HDV nejsou dobré. V klinických studiích byl prokázán příznivý vliv podávání konvenčního IFNα (9 MU 3krát týdně) nebo PEG-INF α-2a po dobu 1 roku. Obnovení replikace HDV je po ukončení léčby pravidlem, ale histologický efekt přetrvává nejméně 10 let po léčbě. Lamivudin není účinný a kombinace PEG-IFN a ribavirin (RBV) nezvyšuje účinnost léčby.
L. Pacienti s koinfekcí HCV a HBV
Neexistují zatím žádná obecně platná doporučení pro léčbu pacientů s koinfekcí HBV/HCV. Je nutný individuální přístup a postupné uplatňování nových zkušeností s léčbou těchto problémových pacientů. U naprosté většiny těchto pacientů replikace HCV tlumí replikaci HBV, proto lze zpravidla v séru prokázat HCV RNA, zatímco sérová hladina HBV DNA je pod hranicí detekovatelnosti. Pro současnou infekci potom svědčí pozitivita HBsAg, někdy jen průkaz celkových protilátek anti-HBc. Podle výsledků klinických studií je kombinovaná terapie PEG-IFN a RBV u koinfikovaných pacientů stejně účinná vzhledem k infekci HCV, jako při samostatné infekci HCV. K trvalému zvládnutí infekce HBV však nedochází a naopak útlum replikace HCV může vést k výraznému nárůstu replikace HBV s následnou akutní exacerbací chronické hepatitidy B s možnými závažnými klinickými následky (rychlá progrese chronické hepatitidy do jaterní cirhózy, dekompenzace cirhózy).
9. Význam jaterní biopsie a způsob provedení histologického hodnocení
Provedení jaterní biopsie se doporučuje k verifikaci chronické jaterní léze, vyloučení spoluúčasti jiných příčin jaterního poškození a posouzení pokročilosti jaterního postižení. Histologické hodnocení se provádí stejně jako u jiných chronických hepatitid (Knodell, Ishak). Odmítnutí tohoto výkonu pacientem či jeho neprovedení z důvodů nebezpečnosti zákroku u komplikovaného pacienta (hemofilie, trombocytopenie, koagulační poruchy, jaterní hemangiomy apod) nesmí být důvodem k neposkytnutí léčby, pokud se jedná o klinicky a laboratorně jasně indikované případy. V některých případech však může být jaterní biopsie nezbytná pro správné indikování léčby. Jde zejména o pacienty s dlouhodobě normální aktivitou ALT, u kterých má význam kontinuální posuzování progrese fibrózy ve vzorcích, získaných s odstupem několika let.
10. Způsob dispenzarizace pacientů s infekcí virem hepatitidy B
V České republice je ze zákona nařízena povinná izolace nemocných s akutní hepatitidou na infekčních klinikách či odděleních. Dále jsou pacienti nejméně 12 měsíců kontrolováni v jaterních poradnách při těchto pracovištích. Pokud infekce přejde do chronicity, je nutná dlouhodobá, ev. celoživotní dispenzarizace v jaterních poradnách infekčních, gastroenterologických nebo interních pracovišť. V případě vzniku HCC na gastroenterologii a onkologii. Volba daného pracoviště se může v různých regionech České republiky lišit a závisí na pokročilosti jaterního procesu a na personálním a přístrojovém vybavení dostupných pracovišť.
prof. MUDr. Petr Husa, CSc.
www.fnbrno.cz
e-mail: phusa@fnbrno.cz
Doručeno do redakce: 9. 9. 2007
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2007 Issue 11-
All articles in this issue
- Diagnostický prínos použitia implantovaného slučkového rekordéra (Reveal Plus) u pacientov so synkopou nejasnej etiológie
- Dlouhodobé výsledky srdeční resynchronizační léčby u pacientů s těžkým srdečním selháním
- Využití stanovení glykogenfosforylázy BB v diagnostice algické formy akutních koronárních syndromů
- Bazický fibroblastový růstový faktor (bFGF) a cévní endotelový růstový faktor (VEGF) jsou zvýšeny v plazmě periferní krve nemocných s chronickou lymfocytární leukemií a klesají po intenzivní léčbě obsahující fludarabin
- Variabilita plazmatických hladin big endotelinu a NT-proBNP u nemocných se srdečním selháním v chronickém hemodialyzačním programu
- Endoskopická diagnostika a léčba biliárních komplikací po laparoskopické cholecystektomii
- Vliv obezity na genovou expresi adiponektinu a jeho receptorů v subkutánní tukové tkáni
- Rituximab (MabThera®) - nový biologický lék v terapii revmatoidní artritidy
- Syndrom horní duté žíly: definice, etiologie, fyziologie, symptomy, diagnostika a léčba
- Význam endoskopické cytoskopie u vyšetření trávicího traktu
-
Diagnostika a léčba chronické hepatitidy B
Doporučený postup České hepatologické společnosti České lékařské společnosti J. E. Purkyně a Společnosti infekčního lékařství České lékařské společnosti J.E. Purkyně
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Syndrom horní duté žíly: definice, etiologie, fyziologie, symptomy, diagnostika a léčba
- Rituximab (MabThera®) - nový biologický lék v terapii revmatoidní artritidy
- Diagnostický prínos použitia implantovaného slučkového rekordéra (Reveal Plus) u pacientov so synkopou nejasnej etiológie
- Endoskopická diagnostika a léčba biliárních komplikací po laparoskopické cholecystektomii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

