-
Medical journals
- Career
DIABETES MELLITUS LÉČBA U STARŠÍCH PACIENTŮ V ČR. Doporučený diagnostický a terapeutický postup pro všeobecné praktické lékaře
: MUDr. Igor Karen 1; Prof. MUDr. Štěpán Svačina, DrSc. 2; Mba Mba 2; MUDr. Božena Jurašková, Ph.D. 3
: Geriatrie a Gerontologie 2019, 8, č. 2: 78-95
:
1 SOUČASNÁ SITUACE A ALGORITMY LÉČBY GERIATRICKÝCH PACIENTŮ S DIABETES MELLITUS V KLINICKÉ PRAXI V ČR
Doporučené postupy (DP) v diabetologii jsou vyvěšeny na stránkách České diabetologické společnosti ČLS JEP (ČDS) (www.diab.cz), na stránkách Společnosti všeobecného lékařství ČLS JEP (SVL) (www.svl.cz) a publikovány v časopise DMEV. Speciální DP pro starší pacienty ještě před několika málo lety neexistovaly, a proto vznikla společná skupina ČDS, České geriatrické a gerontologické společnosti ČLS JEP (ČGGS) a SVL, která v roce 2014 uveřejnila první společný DP. Nyní (na počátku roku 2019) přinášíme jeho novelizaci.
Starší populace diabetiků je z diabetologického hlediska členěna takto:
- a) Pacienti jinak zdraví, bez komplikací diabetu s dobrou životní prognózou – tedy soběstační, v dobrém funkčním stavu.
- b) Pacienti s komorbiditami s horší životní prognózou, z geriatrického hlediska křehcí s omezenou soběstačností.
- c) Pacienti nesoběstační vyžadující dlouhodobou péči.
- d) Za zvláštní skupinu je třeba s ohledem na management diabetu považovat pacienty se závažným kognitivním deficitem.
V současné době postupují lékaři u pacientů obvykle individuálně s cílem eliminovat zejména riziko hypoglykemie.
2 SCREENING A DIAGNOSTIKA DM U STARŠÍCH NEMOCNÝCH
Diabetes mellitus (DM) postihuje ve stáří až třetinu české populace. Výsledkem lepší kvality péče je skutečnost, že se vyššího věku dožívají nejen dříve diagnostikovaní pacienti s diabetem 2. i 1. typu, ale DM ve vyšším věku i nově vzniká. DM 1. typu (DM1) vzniklý ve vyšším věku, jako všechna autoimunitní onemocnění ve stáří, často progreduje pomalu, pod klinickým obrazem LADA (latent autoimmune diabetes in adults). DM 2. typu (DM2) je nejběžnějším typem diabetu ve stáří. Jeho rozvoj akceleruje přítomnost složek metabolického syndromu či souběžná terapie steroidy, psychofarmaky, imunosupresivy a dalšími dlouhodobě užívanými léky, například thiazidy. Riziko nevýznamně zvyšuje i léčba statiny.
Klasifikace starší populace z geriatrického hlediska
Starší populaci klasifikujeme obvykle z geriatrického hlediska takto:
- Starší pacient (senior) – pacient starší 65 let.
- Geriatrický pacient může být definován také jako člověk vyššího věku, u něhož involuční a chorobné změny ovlivňují natolik funkční stav a schopnosti, že dochází ke zhoršení adaptability, zhoršení regulačních mechanismů a zhoršení tolerance k zátěži.
Kritéria rozdělení pacientů seniorského věku
Senioři mohou být členěni do tří skupin podle funkční zdatnosti, rizikovosti a potřeby zdravotnických služeb.
- Senioři zdatní – s dobrou výkonností, kteří se ve zdravotnických diagnostických a terapeutických postupech nemusejí lišit od postupů pro mladší jedince. Nepotřebují geriatrickou péči, ale měli by být edukováni a podrobováni preventivním prohlídkám.
- Nezávislí senioři (většina seniorů) – nepotřebují za normálních okolností dispenzarizaci ani žádnou pečovatelskou či ošetřovatelskou službu. Dochází u nich k přechodnému zhoršení jejich kondice vlivem zátěže v podobě operace, infektu, závažného onemocnění, extrémních výkyvů počasí, náhlé změny sociální situace apod.
- Senioři křehcí – jedinci s chronickým rizikem pádů, zhoršením kognitivních schopností (mírný až střední stupeň demence), psychickou labilitou – depresí, s nestabilním stavem při onemocnění kardiovaskulárního aparátu, arytmiemi, kteří potřebují dispenzarizaci, event. napojení na nouzovou signalizaci. Tito pacienti zpravidla využívají spolu se zdravotnickými službami i služby sociální, domácí péči apod.
Screeningová a diagnostická kritéria diabetu a prediabetu jsou stejná ve všech věkových skupinách.
Screening
Screening diabetu a prediabetu ve stáří provádíme aktivně 1× ročně a navíc glykemii monitorujeme při každém nově vzniklém onemocnění (infekce, systémová a celková onemocnění, změny medikace apod.).
Screeningové vyšetření u prediabetu je pozitivní, pokud je zjištěna:
- zvýšená glykemie nalačno (IFG, impaired fasting glucose), která je definována nálezem glykemie nalačno z venózní plazmy v rozmezí 5,6–6,9 mmol/l, nebo
- porušená glukózová tolerance (IGT, impaired glucose tolerance), která je definována hodnotami glykemie ve venózní plazmě ve 120. minutě v rozmezí 7,8–11,0 mmol/l po provedení standardního orálního glukózového tolerančního testu (oGTT) se 75 g glukózy.
Jako alternativní diagnostické kritérium se do budoucna jeví zvýšení glykovaného hemoglobinu (HbA1c) v rozmezí odpovídajícím 39 – 47 mmol/mol (dle IFCC konsenzu od roku 2012), které je podmíněno více zvýšením glykemie nalačno než glykemie postprandiální. V ČR však v současné době není toto vyšetření dostatečně laboratorně standardizováno, a proto zatím nemůže být plně využíváno.
Diagnostika
Diabetes mellitus může být diagnostikován pomocí stanovení glykemie v žilní plazmě třemi různými způsoby:
- přítomností klasických příznaků diabetu + náhodné glykemie ≥ 11,1 mmol/l,
- glykemií nalačno ≥ 7,0 mmol/l,
- glykemií ve 120. minutě oGTT ≥ 11,1 mmol/l.
Normální hodnoty glykemií jsou stanoveny následovně:
- normální glykemie nalačno je v rozmezí 3,9–5,5 mmol/l,
- normální glukózová tolerance znamená glykemii ve120. minutě oGTT < 7,8 mmol/l při normální glykemii nalačno.
Pro praxi
Screeningová a diagnostická kritéria diabetu a prediabetu jsou stejná ve všech věkových skupinách. K diagnostickým účelům je doporučeno použít stanovení glykemie v žilní plazmě standardní laboratorní metodou. Navíc je u seniorů při nálezu klinických symptomů svědčících pro diagnózu DM dostatečné zjištění náhodné glykemie z kapilární krve, která je vyšší nebo rovna 11,1 mmol/l.
3 KOMPLIKACE DIABETU VE STÁŘÍ A CÍLOVÉ HODNOTY LÉČBY
Mikro - i makrovaskulární komplikace diabetu vznikají v závislosti na výši hyperglykemie a na délce jejího trvání. Riziko vzniku mikrovaskulárních komplikací diabetu je ve stáří nižší, při špatné kompenzaci však dochází k progresi již existujících mikrovaskulárních komplikací. Již prediabetes přináší výrazné makrovaskulární riziko, a to je ještě výraznější u diabetu.
Ještě více však staršího diabetika s kardiovaskulárními komplikacemi, a zejména kognitivní poruchou, ohrožuje hypoglykemie. Z uvedených důvodů je u rizikových pacientů léčba kompromisem mezi těmito riziky.
Cílové hodnoty kompenzace diabetu volíme individuálně na základě komplexního posouzení přínosů a rizik léčby, nutno zde podotknout, že především křehkost a věk ovlivňují významně cíle léčby (tab. 1).
1. Cílové hodnoty pro léčbu hyperglykemie, které by měly minimalizovat riziko hypoglykemie 
Riziko hypoglykemie se zvyšuje za následujících podmínek: Při léčbě inzulinem a deriváty sulfonylurey, s vyšším věkem, s dobou trvání DM, při jaterní a renální insuficienci, při nepravidelných stravovacích návycích, při období hladovění a malnutrici (např. spojené s onkologickým onemocněním), při nepravidelném, ale i nadměrném cvičení, při nadměrném příjmu alkoholu, při opakovaném výskytu hypoglykemií či při jejich sníženém vnímání. Riziko hypoglykemie se zvyšuje vlivem některých hypoglykemizujících léků, při poruše kognitivních funkcí či při jiných závažných psychických poruchách, např. při depresi.
Pacient se závažnou hypoglykemií po perorálních antidiabetikách (PAD) by měl být vždy hospitalizován, neboť hrozí riziko recidivy. Pacienty s hypoglykemií po inzulinu hospitalizujeme při komplikacích a závažných komorbiditách.
3.1 AKUTNÍ KOMPLIKACE DM
- Hypoglykemie
- Diabetická ketoacidóza
- Hyperglykemický hyperosmolární stav
- Laktátová acidóza
3.1.1 Hypoglykemie
Hypoglykemie je definována jako laboratorní hodnota glykemie nižší než 3,9 mmol/l a je nejčastější komplikací léčby inzulinem a dalšími antidiabetiky, nejčastěji sulfonylureovými či glinidy. Až na zcela vzácné případy spontánní hypoglykemie v počátečních stadiích dosud neléčeného DM2 (vlivem snadno navoditelné hyperinzulinemie) jde vždy o iatrogenní komplikaci. Příčinou je hyperinzulinemie, způsobená nejčastěji vynecháním, zpožděním či malým množstvím jídla a/nebo zvýšenou fyzickou námahou při nezměněné dávce inzulinu, sulfonylurey, glinidu nebo dalších antidiabetik. Nebezpečí hypoglykemie se výrazně zvyšuje po požití alkoholu, zvláště při současném nedostatečném příjmu potravy (deplece jaterního glykogenu a inhibice jaterní glukoneogeneze) a při snížené funkci ledvin (snížená clearance inzulinu, nedostatečná renální glukoneogeneze a reabsorpce). Hypoglykemii diagnostikujeme glukometrem nebo v laboratoři a klasifikujeme podle závažnosti jako asymptomatickou, symptomatickou nezávažnou (pacient ji zvládne sám) nebo symptomatickou závažnou včetně poruchy vědomí (vyžaduje zásah druhé osoby).
Klinické příznaky jsou adrenergní (třes, pocení, tachykardie) a neuroglykopenické, dané nedostatkem glukózy v centrálním nervovém systému (CNS) (poruchy kognice, zmatenost, nevolnost, agresivita, křeče). Pokročilá neuroglykopenie vede k poruchám vědomí až kómatu. U seniorů převažují neuroglykopenické (centrální) poruchy. U některých pacientů se po opakovaných hypoglykemiích a také vlivem stárnutí postupně ztrácí kontraregulační odpověď na hypoglykemii a pacienti ji hůře rozpoznávají (syndrom nerozpoznávaných hypoglykemií, defektní kontraregulace). Ať už v důsledku autonomní neuropatie, a/nebo adaptace mozkových buněk na hypoglykemické stavy dochází ke změnám hypoglykemického prahu a hypoglykemie se může projevit přímo poruchou vědomí bez varovných adrenergních příznaků.
Riziko hypoglykemie: Hypoglykemie může pacienty ohrozit maligní arytmií, akutním koronárním syndromem, neurologickým postižením CNS s ložiskovými příznaky imitujícími cévní mozkovou příhodu, generalizovanými křečemi nebo sekundárními komplikacemi, jako jsou aspirace zvratků, úraz, dopravní nehoda. Adrenergní odpověď při hypoglykemii je riziková zejména u starších pacientů s anamnézou ischemické choroby srdeční (ICHS). Dlouhodobá hluboká hypoglykemie může vést k trvalému poškození nebo smrti mozku.
Léčba: Základem pomoci při hypoglykemii je podání glukózy pacientovi co nejrychleji, a to bezodkladně v adekvátním množství tak, aby byla zajištěna normalizace glykemie na běžné hodnoty. Běžnou nezávažnou hypoglykemii je pacient schopen zvládnout sám perorálním příjmem kombinace rychle vstřebatelných a komplexních sacharidů a pečlivým selfmonitoringem. Při nemožnosti podání per os je nutno glukózu podat intravenózně. Při hypoglykemii po inzulinu s poruchou vědomí lze jako první pomoc u pacientů s dostatečnou zásobou jaterního glykogenu aplikovat intramuskulárně glukagon, je-li k dispozici (aplikace je prováděna poučeným laikem, nejčastěji rodinným příslušníkem). Tento postup je neúčinný při dlouhotrvající hypoglykemii (deplece glykogenu), po požití většího množství alkoholu a není vhodný u starších pacientů. Většinou je v rámci první pomoci nutno aplikovat glukózu intravenózně. Po závažné hypoglykemii navozené sulfonylureou či dlouhodobě působícími inzuliny by měla být vždy zvážena hospitalizace pro riziko recidivy (dlouhý biologický poločas sulfonylurey). Po proběhlé hypo glykemii je nutné rozebrat její příčiny a zabránit recidivě pečlivou edukací, případně úpravou antidiabetické léčby. Zásady zvládání hypoglykemických stavů jsou uvedeny níže.
Pacient s hypoglykemií – zásady léčby
Bez poruchy vědomí:
- pacient zvládne sám,
- 200 ml sladkého nápoje (oslazený čaj, sladký nápoj typu kola – ne light!, džus) nebo 10–20 g hroznového cukru (2–4 tbl. po 5 g), sladký gel,
- dále 20–30 g komplexních sacharidů – pečivo, přílohy,
- kontrola glykemie po 15–20 minutách, pokud hypoglykemie přetrvává, postup opakovat,
- pokud přetrvává i po dalších 15–20 minutách, nutný příjem dvojnásobného množství sacharidů, než je uvedeno výše, • nevhodná je čokoláda a tučná jídla,
- časná kontrola ošetřujícím lékařem, zvážení úpravy léčby.
S poruchou vědomí:
- 40–60 ml 40% glukózy i. v., pokud není k dispozici, použít adekvátně vyšší objemy roztoku glukózy o nižší koncentraci,
- kontrola glykemie po 5–10 minutách, pokud hypoglykemie přetrvává, postup opakovat,
- po zvládnutí hypoglykemie jídlo se 30–40 g komplexních sacharidů – pečivo, přílohy,
- glukagon, je-li k dispozici a indikován,
- po nekomplikovaném průběhu není hospitalizace nutná,
- hospitalizace je nutná, pokud není úprava stavu kompletní (přetrvávají neurologické nebo psychiatrické příznaky) či je zde riziko opakování hypoglykemie v krátkém čase,
- časná kontrola ošetřujícím lékařem, zvážení úpravy léčby.
Trvající porucha vědomí:
- trvá porucha vědomí po verifikované hypoglykemii (glykemie byla nízká a již je normální nebo zvýšená): transport do nemocnice, monitorované lůžko, pokračuje infuze glukózy,
- porucha vědomí, hypoglykemie nebyla verifikována (např. při první kontrole glykemie je přítomná normální nebo vyšší glykemie): transport do nemocnice, monitorované lůžko, nemusí jít o následek hypoglykemie.
Hypoglykemie po sulfonylureovém perorálním antidiabetiku (PAD):
- riziko rekurence,
- vhodná hospitalizace a infuzní aplikace glukózy ≤ 24 hodin podle klinického a laboratorního nálezu,
- časná kontrola ošetřujícím lékařem, vysazení sulfonylurey, změna léčby.
Po zvládnutí hypoglykemie:
- 20–40 g komplexních sacharidů v potravě – pečivo, přílohy,
- častější selfmonitoring glykemie,
- zjistit příčinu,
- zabránit opakování,
- u recidivující hypoglykemie změnit strategii léčby, zvolit vyšší cílové hodnoty glykemie a HbA1c.
3.1.2 Diabetická ketoacidóza
Diabetická ketoacidóza se může v ordinaci praktického lékaře vyskytnout jako první příznak DM1. Její časná diagnostika je velmi důležitá. Může být prvním projevem DM1 u pacientů, kteří ignorovali klinické známky diabetu (polyurii, polydipsii, hubnutí) a o své nemoci nevěděli. Časté je zvracení a bolesti břicha připomínající náhlou příhodu břišní. Pro pokročilou ketoacidózu s poruchou vědomí včetně kómatu je typické hluboké a rychlé, tzv. Kussmaulovo dýchání. Může být nápadný acetonový foetor a aceton v moči. Po zjištění hyperglykemie (obvykle nad 18–20 mmol/l) je nutný neodkladný transport do nemocnice. Základní lékařskou první pomocí je zavedení žilního vstupu a hydratace, nejlépe fyziologickým roztokem, event. inzulinová léčba velmi malými dávkami, v terénu může být zahájena až po iniciální rehydrataci s krátkým odstupem. Pacient má být co nejrychleji dopraven do nemocnice posádkou RLP a patří na monitorované lůžko (JIP, JIMP). Základním léčebným opatřením je rehydratace, inzulinoterapie, suplementace a monitorace kalia a podpora základních životních funkcí.
3.1.3 Hyperosmolární hyperglykemický stav
Hyperosmolární hyperglykemický stav se rozvíjí u pacientů s DM2 a je obvykle provázen velmi vysokou glykemií (> 40–60 mmol/l) a těžkou dehydratací. Velmi často jde o starší pacienty, mnohdy léčené diuretiky, u nichž stav progreduje po dobu několika dnů a může dospět do stadia kómatu. Často je provázen dalšími komplikacemi (CMP, tromboembolie, infekce). Stav má relativně vysokou mortalitu. Nutný je neodkladný transport do nemocnice. Podobně jako při ketoacidóze je základní lékařskou první pomocí zavedení žilního vstupu a hydratace, nejlépe pomocí fyziologického roztoku. Léčba pacienta za hospitalizace je prakticky shodná jako u pacientů s keto acidózou.
3.1.4 Laktátová acidóza
Laktátová acidóza se může vyskytnout u všech stavů, které jsou spojeny s tkáňovou hypoxií (oběhové a respirační selhání, kardiogenní šok), i u pacientů bez diabetu. Riziko laktátové acidózy je zvýšené u pacientů s DM2 léčených metforminem v případě, pokud nejsou respektovány kontraindikace podávání metforminu (renální insuficience, těžší respirační insuficience, jaterní insuficience či těžší jaterní poškození nebo pokročilé srdeční selhání s hypoxií). Laktátová acidóza se může rozvinout relativně rychle např. při dehydrataci a prerenálním selhání ledvin. Při pokročilé laktátové acidóze můžeme nacházet Kussmaulovo dýchání. Základní lékařskou první pomocí je zavedení žilního vstupu, hydratace, podpora základních životních funkcí a transport na JIP. Mortalita na laktátovou acidózu je vysoká. Dnes tuto komplikaci můžeme nejčastěji vidět u těch pacientů, kdy lékař nerespektoval uvedené kontraindikace metforminu (nejčastěji renální insuficienci) a pokračoval v této terapii.
3.2 DALŠÍ KOMPLIKACE DM
U diabetiků ve stáří pátráme aktivně po známkách dekompenzace. Křehký geriatrický pacient s diabetem by měl být individuálně léčen tak, aby klinické symptomy hyperglykemie (žízeň, polyurie, ztráta hmotnosti) nebyly přítomny, a individuálně není vždy nutné dosahovat cílových hodnot léčby.
Prognózu u starších diabetiků zlepšuje dobrá léčba hypertenze a léčba dyslipidemie. Efekt redukce hmotnosti na zlepšení prognózy není obvykle po 70. roce věku prokazatelný a obézní mohou mít i lepší prognózu než štíhlí – tzv. paradox obezity. Po 70. roce obvykle již neindikujeme bariatrické chirurgické výkony.
Mezi další komplikace diabetu patří mikrovaskulární komplikace jako diabetická retinopatie, neuropatie, nefropatie kombinované etiologie a syndrom diabetické nohy. Z dalších komplikací jsou to infekce (respirační, kožní, močové, parodontu), postižení trávicího traktu (např. poruchy motility), erektilní dysfunkce. Po těchto projevech je třeba aktivně pátrat a zvážit konzultaci příslušného specialisty.
3.3 DISPENZÁRNÍ KONTROLY
Dispenzární kontroly i u starších pacientů provádíme podle schválených doporučení, další kontroly je nutné individuálně přizpůsobit funkčnímu stavu a prognóze i reálným možnostem a spolupráci pacienta (přizpůsobení je nutné zejména u křehkých pacientů).
Frekvence vyšetřování u zdatného geriatrického pacienta s diabetem se neliší od mladší populace (tab. 2). Ke kontrole zveme obvykle 1× za 3 měsíce se stanovením glykemie nalačno či postprandiální glykemie a monitoringem HbA1c (1× za 3–6 měsíců dle kompenzace), změřením krevního tlaku, pulzu a hmotnosti (výpočtem BMI), inspekcí dolních končetin (DK). 1× ročně palpačně zjistíme pulzaci tepen DK či pomocí oscilo metrického vyšetření indexu kotníkových tlaků (ABI, ankle brachial index) či dopplerovského vyšetření DK, dále 1× ročně vyšetříme z krve Na+, K+, Cl−, ureu, kreatinin, kyselinu močovou, AST, GMT, lipidové spektrum (celkový cholesterol, LDL-cholesterol, HDL-cholesterol, triglyceridy) a vypočteme glomerulární filtraci podle rovnice CKD -E PI (při hraničních hodnotách eGFR je vhodné frekvenci monitorace zvýšit na 1× za 3–6 měsíců), vyšetříme moč + sediment, albuminurii, natočíme EKG, fyzikálně a orientačně neurologicky vyšetříme. Oční vyšetření, především očního pozadí, 1× ročně je nedílnou součástí komplexní péče o tyto pacienty. Fakultativně zvážíme vyšetření štítné žlázy (fT4, TSH) (viz tab. 2). V rámci komplexní péče je vhodné zrekapitulovat stav očkování, zejména proti tetanu, pneumokokovým infekcím, chřipce, event. zvá ží me i vak ci naci proti klíšťové encefalitidě.
2. Náplň dispenzární prohlídky u pacientů s DM 2. typu – zdatných seniorů
(Doporučení klinických a laboratorních vyšetření)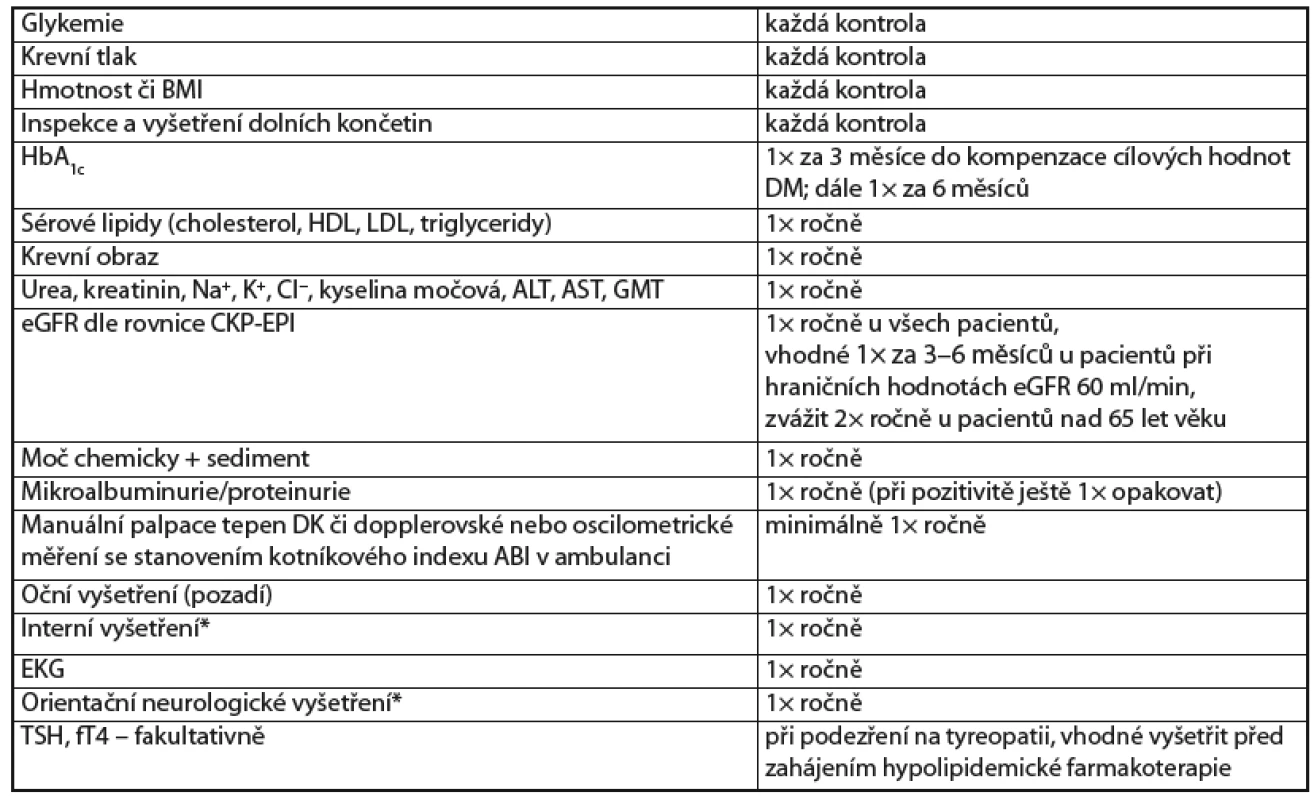
* Provádí dispenzarizující lékař– zaměření na postižení velkých cév a známky ischemické choroby srdeční, dolních končetin a CNS (cílená anamnéza a objektivní vyšetření včetně poslechu krkavic, stehenních tepen a palpace periferních tepen). Nález při interním vyšetření vede k indikaci dalších laboratorních vyšetření (krevní obraz, enzymy apod.). U křehkého geriatrického pacienta s diabetem provádíme urgentní kontrolu při jiném závažném onemocnění či známkách dekompenzace diabetu. Ve stabilizovaném stavu lze výše uvedené intervaly prodloužit na 6–12 měsíců.
4 ALGORITMUS LÉČBY DM STARŠÍCH PACIENTŮ
Komplexní léčbou diabetu rozumíme soubor opatření, která zahrnují nejen léčbu hyperglykemie, ale také léčbu hypertenze, dyslipidemie, obezity a dalších komorbidit.
4.1 LÉČBA HYPERGLYKEMIE
Léčba hyperglykemie se opírá o využití režimových opatření a farmakologické léčby.
4.1.1 Nefarmakologická léčba hyperglykemie
Při doporučeních a edukaci dietních a pohybových opatření postupujeme u starších pacientů vždy individuálně, zejména pak u pacientů s kognitivním deficitem a závažnou polymorbiditou. U pacientů závislých na péči stanovujeme individuální plán společně s pečujícími. Dbáme vždy také o dostatek tekutin, bílkovin a vápníku. Často je možný ales poň „pasivní“ monitoring, tj. bez úprav režimu. Zdatné starší diabetiky edukujeme naopak stejně jako diabetiky mladší.
Důležitá je zpětná vazba se zapsáním cílů edukace do dokumentace s individuálním vyhodnocením znalostí i dosažených cílů.
Pro staršího pacienta je i chůze dostatečným pohybem, optimálně by měla být pravidelná, asi 30–40 minut denně. Efekt je však bezprahový a každá pravidelná fyzická aktivita, byť i menší intenzity a frekvence, má pozitivní efekt pro organismus. Edukujeme správnou techniku chůze s odlehčením nosných kloubů, například nordic walking, chodítka a podobně.
Východiskem adekvátní komunikace je posouzení kognitivních funkcí a případně depresivity (test hodin [clock test], pětislovní test). Můžeme tak učinit v rozhovoru s pacientem, ale pro přesnější a rychlejší zjištění je vhodné použít některé orientační či podrobnější testy.
Pro posouzení depresivity můžeme použít některou ze škál (například GDS dle Yesavage). Základními testy, které v praxi používáme pro posouzení kognitivních funkcí, jsou MiniCOG (Screening pro kognitivní poruchy u starších dospělých) a MMSE (Mini-Mental State Examination). Pokud tyto testy nemáme po ruce, můžeme použít alespoň test hodin nebo MoCA (Montrealský kognitivní test). Komunikaci s pacientem i způsob, jakým mu budeme poskytovat informace, bychom měli přizpůsobit zejména stavu kognitivních funkcí. Pokud je kognitivní porucha výrazná, měli bychom pamatovat také na poskytnutí písemných informací a poučení rodinného příslušníka.
4.1.2 Farmakologická léčba hyperglykemie
U nemocných s DM 2. typu je lékem první volby metformin. Při jeho intoleranci, kontraindikacích či nesplnění stanovených cílů léčby postupujeme k dalšímu kroku (viz „Algoritmus volby léků…“ na 2. straně obálky). U všech pacientů nepřihlížíme dnes primárně k věku. Použijeme metformin, pokud není kontraindikován nebo netolerován. Pokud nestačí, následuje otázka, zda má pacient kardiální či renální onemocnění. Pokud ano, léčíme vždy glifloziny nebo GLP-1 agonisty. Jen u ostatních pacientů máme možnost jiné volby. Je-li u křehkých pacientů riziko hypoglykemie, máme možnost volit také DPP-4 inhibitory nebo thiazolidindiony. Avšak u obézních znovu preferujeme GLP-1 agonisty a glifloziny.
V rámci terapie DM2 je na prvním místě bezpečnost a minimalizace stavů hypoglykemií, zejména u křehkých a závislých geriatrických pacientů. Z těchto důvodů je v léčbě diabetu vhodná preference monoterapie, v případě kombinační terapie spolu s metforminem upřednostňujeme preparáty ze skupiny DPP-4 inhibitorů. (Nejuniverzálnější se jeví linagliptin, který můžeme podávat i při těžkém poškození ledvin i jater.) Velmi výhodné by bylo podání gliflozinů a inkretinových analog, pokud by byly uvolněny pro předpis praktickým lékařům (za předpokladu zhodnocení interakcí, dostatečné hydratace a poučení pacienta). Krajní alternativou je volba novějších derivátů sulfonylurey s nízkým rizikem hypoglykemie (gliklazid, gli mepirid).
Jako další bezpečnější alternativa je možnost použití GLP-1 agonistů u křehkých geriatrických pacientů.
Křehkost u geriatrických pacientů je definována obvykle jako přítomnost některého z následujících znaků: dekondice, hypokineze, psychomotorické zpomalení, zvýšená únavnost, omezení soběstačnosti, kognitivní porucha, depresivita, závažné komplikace při interkurentním onemocnění či jiné závažné změně. Křehký geriatrický pacient s diabetem s krátkou životní prognózou při dalších závažných onemocněních by měl být individuálně léčen tak, aby klinické symptomy hyperglykemie (žízeň, polyurie, ztráta hmotnosti) nebyly přítomny, a není individuálně vždy nutné dosahovat cílových hodnot léčby diabetu.
Doporučení pro snížení hladin glukózy u křehkých starších lidí s diabetem
- Předepsané léky snižující hladinu glukózy by měly mít nízké riziko hypoglykemie, málo významné nežádoucí účinky a měly by být cenově výhodné.
- Při podávání léků starším křehkým pacientům začínáme nízkými dávkami a postupně je pomalu zvyšu jeme.
- Glykemický cíl by měl být stanoven individuálně na základě přítomnosti přidružených onemocnění a s přihlédnutím ke kognitivnímu a funkčnímu stavu pacienta. U mírně až středně křehkých starších pacientů je cílo vý rozsah HbA1c 7–8,0 % (53–64 mmol/mol) vhodný v závislosti na schopnosti pacienta postarat se o sebe a na přítomnosti dalších rizikových faktorů hypoglykemie. U velmi až těžce křehkých je bezpečnější rozmezí HbA1c 7,5–8,5 % (59–69 mmol/mol).
- Mnoho křehkých starších dospělých pacientů má zdravotní potíže, které ovlivňují měření HbA1c. V takových případech se namísto cílových hodnot HbA1c soustředíme na náhodné hladiny glukózy v krvi v rozmezí 6,7–11,1 mmol/l.
- Metformin by měl být používán jako první léčebná linie kvůli nízkému riziku hypoglykemie, nízké ceně a dobré snášenlivosti. U křehkých pacientů je třeba pozorně sledovat úbytek hmotnosti a vedlejší gastrointestinální účinky.
- Inhibitory DPP-4 by měly být vzaty v úvahu u starších dospělých pacientů s menším snížením hladiny postprandiální glykemie nebo v kombinaci s bazálním inzulinem.
- GLP-1 agonisté by měly být používány ke snížení postprandiální glykemie. Mají malé riziko hypoglykemie, ale jsou k dispozici pouze v injekční formě. Mělo by se zvážit, kdy je potřeba podpora pečovatele pro aplikaci injekcí vzhledem k dávkování jednou za týden a ke kombinaci s bazálním inzulinem. Je třeba věnovat zvýšenou pozornost případům, kde by mohlo být další hubnutí problémem.
- Sulfonylureová a nesulfonylureová sekretagoga inzulinu mají vysoké riziko hypoglykemie a u starších dospělých by neměla být používána kvůli dalším nežádoucím účinkům. Jsou však levná.
- Před zahájením léčby inzulinem by měla být hodnocena fyzická a kognitivní schopnost křehkého staršího dospělého. Pokud je zapotřebí další snížení hladiny glukózy, měl by být bazální inzulin v jedné denní dávce kombinován s jinými neinzulinovými přípravky.
- Intenzivní terapie s komplexním režimem inzulinu se u starších dospělých pacientů nedoporučuje. U křehkých starších pacientů s diabetem by měla být cílem zjednodušená léčba.
- Pečovatelé by měli být proškoleni v problematice hypoglykemie.
Výhody a nevýhody jednotlivých lékových skupin jsou uvedeny v tabulce 3.
3. Přínosy a nevýhody lékových skupin používaných při léčbě diabetu
Komentář: Každá skupina léků může být použita u křehkých seniorů s diabetem, avšak mějte na paměti, že při předepisování bezpečného, ale účinného léku snižujícího hladinu glukózy je třeba vzít v úvahu řadu faktorů.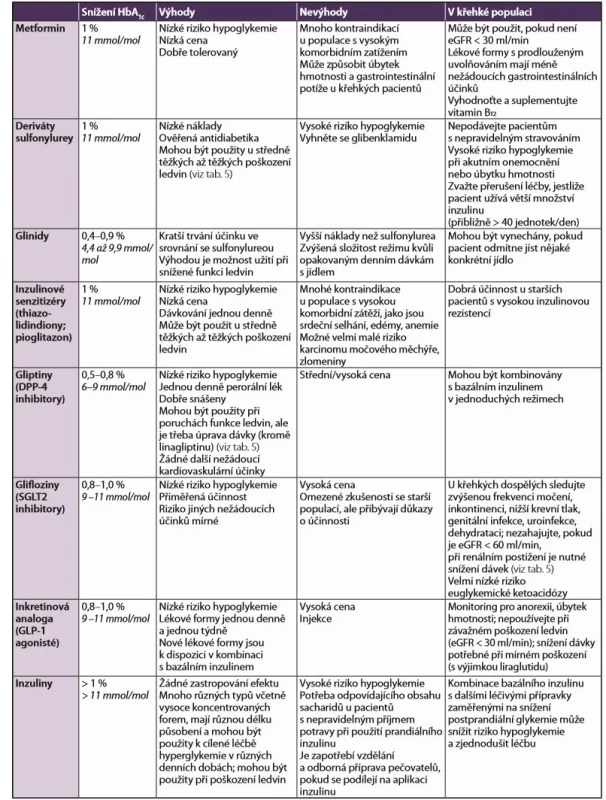
Pozn.: DPP4 – dipeptidylpeptidáza 4, eGFR – odhad glomerulární filtrace, GLP1 – glukagonu podobný peptid 1, HbA1c – glykovaný hemoglobin, SGLT2 – sodíkoglukózový kotransportér 2 4.1.3 Obecná doporučení pro inzulinovou léčbu u starších diabetiků
Zahájení inzulinové léčby (tab. 4) je u starších diabetiků 2. typu poměrně často odkládáno. Důvodem jsou obavy jak lékařů, tak i pacientů a jejich rodin z rizik, která inzulinová léčba ve vyšším věku přináší (hypoglykemie, složitost aplikace). Starší diabetici často připisují své potíže, které jsou příznakem hyperglykemie (slabost, únava), nesprávně stáří. Jedna či dvě denní dávky inzulinu však u mnoha starších diabetiků podstatně zlepší kvalitu života. Perorální antidiabetika lze případně v kombinaci s inzulinem ponechat.
4. Inzulinoterapie ve stáří 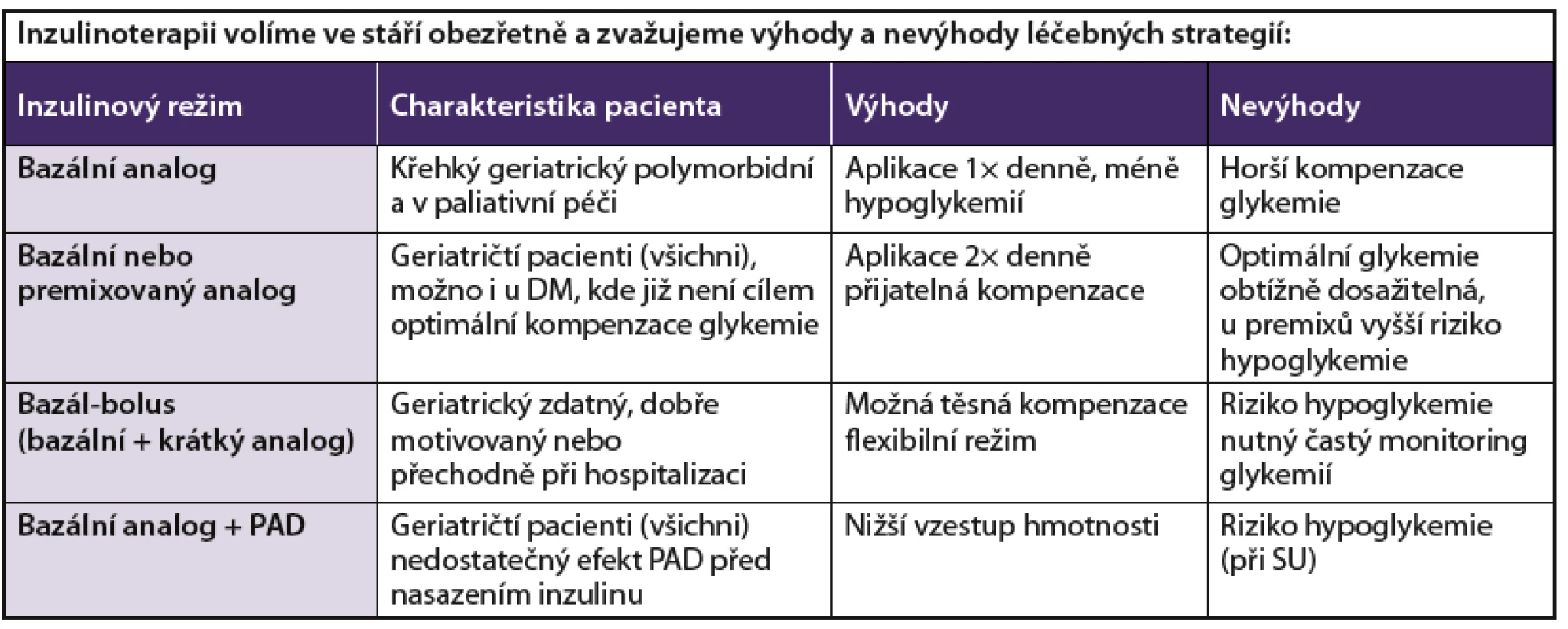
Pozn.: DM – diabetes mellitus, PAD – perorální antidiabetika, SU – sulfonylurea U starších diabetiků jsou obvykle nejvhodnější a dostačující jednoduché inzulinové režimy. Frekvence aplikace inzulinu je limitována podmínkami pacienta. Pro křehké geriatrické pacienty je dostačující aplikace dlouze účinkujícího inzulinového analoga (glargin, detemir, degludek) jednou denně. Je možno použít premixované směsi krátce a středně dlouho účinkujícího inzulinu, premixované inzuliny jsou však spojeny s vyšším rizikem hypoglykemie než léčba samotným bazálním inzulinem. V současné době jsou často využívány také výhody premixovaných inzulinových ana log. Intenzifikované inzulinové režimy, které jsou nutné pro dosažení hodnot blízkých normoglykemiím, je možné použít pouze u zdatných starších diabetiků s velmi dobrou motivací, mobilních a mentálně zdatných, kteří jsou nezávislí na pomoci druhých a nemají jiná závažná onemocnění, nebo u pacientů s vynikajícím sociálním zázemím.
U starších nemocných s diabetem 1. typu je inzulin stále jedinou možností léčby, nicméně pokud již není cílem léčby DM optimální kompenzace glykemie (např. pro těžkou non-compliance, závažný kognitivní deficit nebo onemocnění se zásadním dopadem na životní prognózu pacienta), je možné ustoupit od intenzifikovaného inzulinového režimu a můžeme zkusit využít režim dvou dávek premixovaného či dlouze působícího inzulinového analoga v jedné dávce.
4.1.4 Antidiabetika při zhoršené renální funkci
Ve stáří je běžné zhoršení renálních funkcí, u diabetiků navíc může jít o projevy diabetické nefropatie, hypertenzní nefropatie či o chronickou intersticiální nefritidu z opakovaných infekcí močových cest. Navíc s ohledem na snížení svalové a kostní hmoty (sarkopenii) není kreatininemie a vylučování kreatininu vždy vhodným ukazatelem renální funkce. Proto využíváme vypočítanou glomerulární filtraci podle rovnice CKD-EPI. Velmi důležité je, že omezení renálních funkcí výrazně limituje podávání některých antidiabetik, ale i antihypertenziv. Antidiabetika volíme při poškození ledvin podle tabulky 5.
5. Základní antidiabetika – možnost použití při chronickém onemocnění ledvin (podle stupňů CKD) na základě SPC jednotlivých přípravků 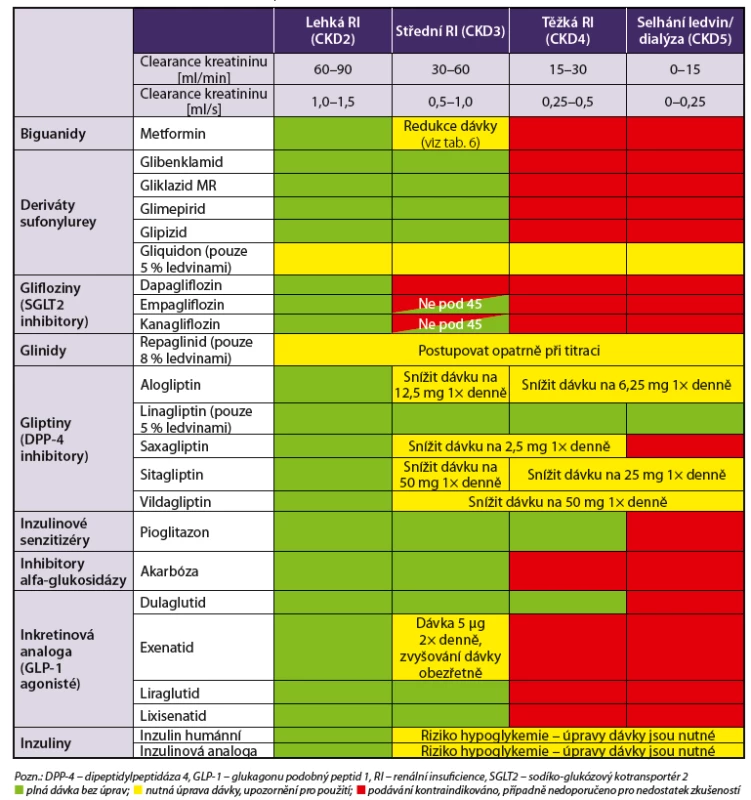
Metformin je podle novějších názorů možno u již léčených pacientů ponechat v dávce redukované na 50 % při glomerulární filtraci 0,5–1,0 ml/s, a tedy u pacientů se středně závažným postižením ledvin. Při filtraci pod 0,5 ml/s metformin již nepodáváme. Maximální denní dávky metforminu ve vztahu k eGFR jsou uvedeny v tabulce 6.
6. Úprava dávkování metforminu při zhoršených renálních funkcích 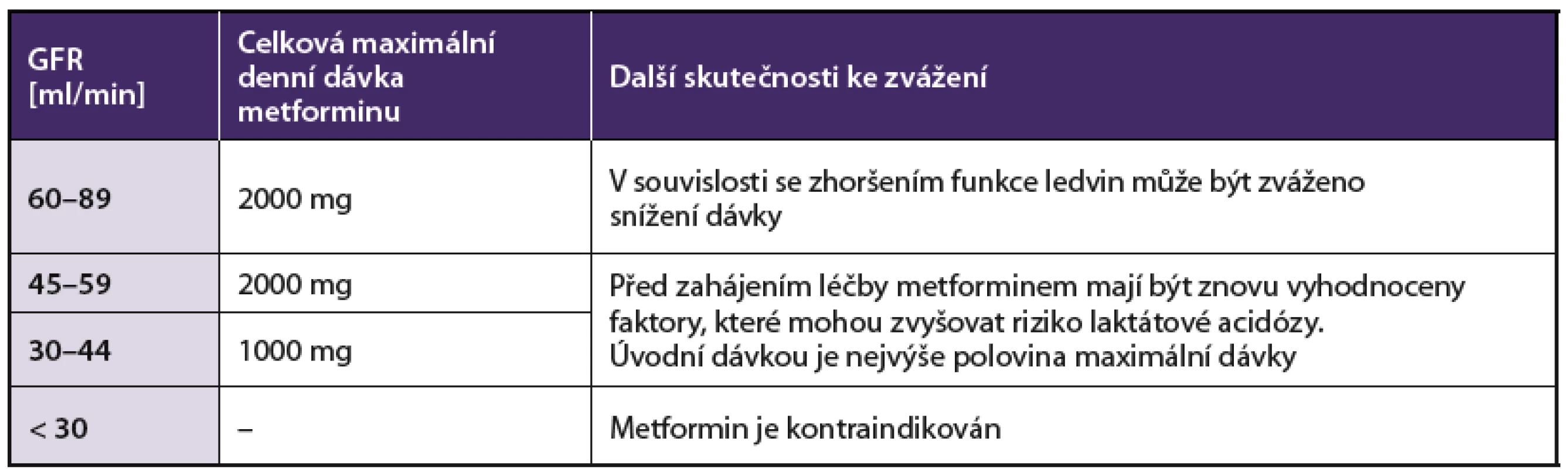
Pozn.: GFR –rychlost glomerulární filtrace V hraničních případech je nutné kontrolovat častěji eGFR.
Velmi zajímavé jsou signály o pozitivních onkologických efektech metforminu. Podle některých studií snižuje výskyt nádorů u pacientů s DM až o 40 %.
4.2 DALŠÍ SPECIFIKA LÉČBY DIABETU VE STÁŘÍ
4.2.1 Kyselina acetylsalicylová
Starší diabetik, který není léčen antikoagulancii a nemá kontraindikace, by měl dostávat 100 mg kyseliny acetylsalicylové denně, a to pouze v sekundární prevenci kardiovaskulárních onemocnění.
4.2.2 Léčba hypertenze
Antihypertenzní terapie zpomaluje rozvoj kognitivních poruch; nejvíce důkazů je pro dihydropyridinové blokátory kalciových kanálů (BKK), zejména nitrendipin, ale existují data i pro inhibitory ACE a blokátory AT₁.
Léčba arteriální hypertenze (AH): Dosažení cílových hodnot kolem 130/80 mmHg (dle Doporučení České společnosti pro hypertenzi, SVL ČLS JEP a dalších odborných společností) při použití monoterapie nebo mnohem častěji kombinace antihypertenziv s různým mechanismem účinku. U osob nad 80 let má být nově cílová hodnota systolického krevního tlaku (sTK) mezi 130–139 mmHg oproti původním cílovým hodnotám mezi 140–150 mmHg.
V léčbě AH se preferují ve dvojkombinaci dlouhodobě působící inhibitory konvertující enzymy, tj. inhibitory ACE nebo blokátory AT₁ receptorů, tj. sartany (souhrnně blokátory RAAS – renin-angiotenzin-aldosteronového systému), a BKK, do další kombinace ve smyslu trojkombinace nízké dávky thiazidových diuretik (DIU) s preferencí indapamidu či amiloridu, následovat by měl nově spironolakton v nízkých dávkách a poté až centrálně působící antihypertenziva rilmenidin, moxonidin či centrálně i periferně působící urapidil, dále i metabolicky neutrální betablokátory. Doporučují se metabolicky pozitivní či neutrální antihypertenziva, mezi něž řadíme zejména první dvě uvedené skupiny antihypertenziv.
Na základě výsledků klinických studií preferujeme z inhibitorů ACE molekuly perindoprilu, ramiprilu a trandolaprilu, z blokátorů AT₁ receptorů preferujeme novější molekuly typu telmisartanu, candesartanu, irbesartanu, valsartanu a eprosartanu. Z diuretik by se měla preferovat co nejvíce šetrná a co nejméně diabetogenní, a to indapamid 1,25 mg přes 1,5 do maximálně 2,5 mg/denně či uvedený amilorid nebo velmi nízké dávky hydrochlorothiazidu od 6,25 mg přes 12,5 mg, výjimečně do maximálně 25 mg/denně. Z betablokátorů jsou preferovány pro výše uvedené důvody zejména bisoprolol, metoprolol, nebivolol, carvedilol. Antihypertenzní terapie zpomaluje rozvoj kognitivních poruch; nejvíce důkazů je pro dihydropyridinové BKK, především nitrendipin, ale existují data i pro inhibitory ACE a blokátory AT₁. Při léčbě diuretiky je ve zvýšené míře nutno kontrolovat mineralogram.
4.2.3 Léčba dyslipidemie
Základem intervence dyslipidemie je podávání statinu k dosažení primárního léčebného cíle, tedy cílové hodnoty LDL-cholesterolu (LDL-c). Koncentrace LDL-c je u nekomplikovaného diabetika 2. typu stanovena pod 2,5 mmol/l, při přítomnosti dalších rizikových faktorů (hypertenze, renální onemocnění, pozitivní rodinná anamnéza) nebo v sekundární prevenci u diabetiků s ICHS či ischemickou chorobou dolních končetin (ICHDK) jako koncentrace LDL-c < 1,8 mmol/l (tab. 7). U nemocných s významnou hypertriglyceridemií (triglyceridemie nad 2,5 mmol/l) výhodně používáme sekundární cílový ukazatel nonHDL-cholesterol (nonHDL-c = celkový cholesterol – HDL-cholesterol), jehož cílové hodnoty jsou o 0,8 mmol/l vyšší než příslušná cílová hodnota LDL-c.
7. Cílové hodnoty sérových lipidů pro diabetiky 
[Doporučení pro diagnostiku a léčbu dyslipidemií v dospělosti, Česká společnost pro aterosklerózu, 2017.] S ohledem na nutnost snížit ve většině případů hladiny LDL-c razantně, používáme nejčastěji atorvastatin a rosuvastatin, tedy statiny s nejvyšší hypolipidemickou účinností. Titrace dávky k cílové hodnotě je většinou nezbytností. Nedosáhneme-li ani při použití maximálních nebo nejvyšších tolerovaných dávek statinů cílových hodnot LDL-c, je namístě kombinace s blokátory intestinální absorpce cholesterolu – ezetimibem. Další možnost představuje kombinace s pryskyřicí (sekvestranty žlučových kyselin), jejíž použití limituje neuspokojivá tolerance nemocnými.
U nemocných s trvající hypertriglyceridemií po dosažení cílové hodnoty LDL-c při terapii statinem indikujeme kombinační léčbu statin a fenofibrát. Bezpečnost této kombinace je srovnatelná s monoterapií statinem. Za popsaných podmínek snižuje kombinace statin + fenofibrát riziko makrovaskulárních i mikrovaskulárních komplikací diabetu. Hypolipidemická léčba statinem je plně indikována i u diabetiků s chronickým renálním onemocněním. V tomto kontextu využíváme preferenčně atorvastatin, jehož dávku není nutné redukovat ani v pokročilých fázích postižení renálních funkcí na rozdíl od rosuvastatinu.
U pacientů s velmi vysokým rizikem (diabetes + manifestní kardiovaskulární onemocnění) je žádoucí dosáhnout hodnot LDLcholesterolu < 1,8 mmol/l, totéž platí i pro diabetiky s dalšími rizikovými faktory (chronické renální onemocnění, arteriální hypertenze, pozitivní rodinná anamnéza předčasné manifestace aterosklerózy, kouření atd.).
4.2.4 Deprese a psychózy
Starší diabetici by měli mít pravidelný screening deprese (např. Geriatrická škála deprese) po třech měsících a při každé změně klinického stavu. Při volbě antidepresiv je vhodné stále zvažovat vliv na změnu hmotnosti. Při podání neuroleptik je třeba si vždy uvědomit riziko vzniku dekompenzace diabetu včetně vzácných závažných stavů připomínajících ketoacidotické diabetické kóma. Je nutné připomenout, že i pacienty s psychózou se daří obvykle dobře edukovat v dietě a fyzické aktivitě, event. je lze odeslat do specializovaných center na psychiatrických klinikách.
4.2.5 Problém polypragmazie
S počtem podávaných léků klesá adherence pacientů k léčbě, stoupá riziko interakcí léků. Adherenci lze zvýšit mimo jiné využitím fixních kombinací léků. K častým vedlejším účinkům léků patří rizika pádů a dyspeptické obtíže znemožňující adekvátní dietní léčbu. 4.2.6 Močová inkontinence Pacient by měl být aktivně dotazován na močovou inkontinenci. Ta je u diabetiků častější a může být známkou infekce močového traktu.
4.2.7 Riziko pádů
Riziko pádů u diabetika je časté, souvisí s medikací, s horším pocitem žízně a kolísající hydratací i s diabetickou viscerální neuropatií. Rizika je třeba vyhodnocovat a eliminovat (úpravou medikace a adekvátní hydratací).
4.2.8 Bolesti u diabetika
Je třeba aktivně pátrat po známkách diabetické somatické i viscerální neuropatie. Vyhodnocovat přítomnost neuropatické bolesti. Ta je bohužel běžně nedostatečně diagnostikována a diabetici nejsou dostatečně léčeni, jak farmakologicky, tak psychoterapeutickými postupy.
4.2.9 Syndrom diabetické nohy
Dolní končetiny pacientů vyšetřujeme aktivně při každé kontrole včetně posouzení prokrvení končetiny. Věnujeme pozornost každému kožnímu defektu a pacienta včas odesíláme do specializované ambulance pro diabetickou nohu.
4.2.10 Demence
Je nezbytné věnovat pozornost prvním příznakům možné kognitivní poruchy (například 10 příznaků, které by vás měly varovat, viz www.alzheimer.cz) a provádět pravidelný screening.
Testy kognitivních funkcí: MiniCOG, MMSE a další.
Jedná se o syndrom ve vyšším věku častý a je významný s ohledem na průběh i možnost terapie diabetu. Syndrom zahrnuje poruchu kognitivních funkcí (paměť, myšlení, orientace, řečové, gnostické a praktické funkce) a funkcí exekutivních. Nejčastější příčinou jsou Alzheimerova choroba, vaskulární faktory (u diabetu zejména významné a akcentované), jež jsou příčinou vaskulární demence, dále následují jiná, zejména neurodegenerativní onemocnění. Tyto změny vznikají zpravidla postupně v řádu měsíců či let, ale demence může být i sou částí následků jiných devastujících poruch mozku (CMP, traumatické poranění mozku [TBI], intoxikace a další). Rozvoj demence souvisí také přímo s diabetem 2. typu, hypertenzí a mozkovou inzulinorezistencí. Demence je u starších diabetiků častá. Vždy individuálně hodnotíme zejména riziko hypoglykemie. Klíčová je u pacientů s demencí kontrola příjmu stravy a kontrolované podání léků a inzulinu. Pokud je to možné, je vhodné neomezovat fyzickou aktivitu.
Využíváme rozdělení demencí na jednotlivá stadia:
- Mírná kognitivní porucha: Jedná se o mírnou poruchu kognitivních funkcí, která se může (ale nemusí) projevit ve výsledcích testů. Nejsou změny soběstačnosti. Nejedná se o demenci – stejný postup jako u ostatních starších pacientů, je však zapotřebí dbát na správnou terapii a dohled. Pozor na hypoglykemii.
- Mírná demence: Demence je diagnostikovaná, do určité míry omezuje soběstačnost, zejména v instrumentálních aktivitách denního života (IADL). Léčba DM je stejná jako v předcházejícím bodě.
- Střední fáze demence: Omezení v IADL, postupná deteriorace běžných denních činností (ADL), ale dobrá kvalita života po relativně dlouhé období, pacienti profitují ze smysluplných aktivit – zde je zapotřebí individuální titrace podle stavu pacienta. Pacienti zpravidla špatně tolerují hypoglykemii, někteří také hyperglykemii. Význam tu mají hodnoty hraniční, které nezpůsobují ještě typické příznaky hypo - či hyperglykemie a mohou se manifestovat jako delirium.
- Těžká demence a terminální fáze: Opět individuálně, cílem je zachovat kvalitu života a komfort nemocného.
V praxi se můžeme setkat i s přechodnou poruchou kognice:
- Delirium: Je akutní stav insuficience vyšších kognitivních mozkových funkcí a kvalitativní porucha vědomí. Vzniká akutně v řádu hodin či dnů. Kromě lékařského postupu, který spočívá v odstranění navozující příčiny (metabolické, infekční, toxické; případně může jít o nežádoucí účinky léků apod.), je důležitý zejména komplexní ošetřovatelský proces prováděný poučeným personálem.
Pro praxi
Nejčastější formou demence je smíšená forma – nikoliv Alzheimerova demence (přesná diagnostika z likvoru, MR, proto je namístě větší opatrnost). Při zjištění poruchy kognice je nutné vyloučit kardiovaskulární či endokrinologickou etiologii – provedení dalších pomocných vyšetření, jako např. EKG, ultrazvuku srdce, Holterovu monitoraci EKG, vyšetření hormonů štítné žlázy, hladiny vitaminu B12, MR nebo CT mozku. Provedení diferenciální diagnostiky poruchy kognice je nezbytné s ohledem na nárůst mylné diagnostiky demence (internista, geriatr, neurolog, psychiatr).
4.2.11 Perioperační péče
Operace starších osob včetně předoperační přípravy by měla být vedena citlivě, konkrétní zdravotní péče se neliší. Individuálně je nutno eliminovat riziko hypoglykemie, více monitorovat glykemie, vysazovat metformin perioperačně (není nutné před krátkými a nekomplikovanými výkony u pacientů se stabilními renálními funkcemi, pokud je v pooperačním období obnoven příjem stravy do 24 hod.), vhodná je šetrná inzulinoterapie a časná rehabilitace.
Často se zapomíná na vyšetření DK a kontrolu kompenzace DM (zhoršení při hospitalizaci je časté). U hospitalizovaných pacientů je vhodné využít hospitalizaci ke kontrole hlavních složek metabolického syndromu (krevního tlaku, lipidů a obezity) a upravit nebo před dimisí znovu nasadit léky.
4.2.12 Očkování
Proočkovanost diabetiků proti chřipce a pneumokokům je ve světě vysoká a u nás je podceňována. Pro praxi je vhodné upozornit, že proti pneumokokovým infekcím existuje očkování. Je vhodné ho zvážit u všech pacientů s DM. Očkování se provádí pomocí očkovacích látek konjugované vakcíny Prevenar 13 bez ohledu na věk pacientů, od 65. roku je hrazeno u všech pacientů z veřejného zdravotního pojištění. Současně je nutné zmínit možnost každo ročního očkování proti chřipce, které je uvedeno ve vyhlášce MZ ČR a pro všechny pacienty s DM je hrazeno z veřejného zdravotního pojištění.
Lze rovněž zvážit vakcinaci proti klíšťové meningoencefalitidě, neboť ČR je endemickou zemí a klíšťata se vyskytují prakticky v celé republice. Vzhledem k nárůstu volnočasových aktivit ve volné přírodě je riziko pro aktivní jedince vyšší. Imunizaci můžeme realizovat prakticky celoročně, v teplých obdobích roku lze využít zkrácené schéma jak u očkovací látky FSME Immun, tak i u vakcíny Encepur. Podrobnosti k očkování viz DP Očkování v ordinaci VPL aktualizace 2014 (novelizace v roce 2019).
4.2.13 Léčba obezity
Ve stáří není redukce hmotnosti provázena takovým efektem jako v mladším středním věku. Dokonce se může uplatňovat tzv. paradox obezity, kdy obézní mají lepší prognózu než štíhlí. Hmotnost ve stáří redukujeme jen tehdy, když je redukce hmotnosti provázena zlepšením kompenzace diabetu či jeho remisí. Rovněž kloubní onemocnění si často vyžádají redukci hmotnosti. Bez věkového omezení lze podávat orlistat. Centrálně působící antiobezitikum naltrexon/bupropion podáváme pacientům nad 65 let věku s opatrností, nad 75 let nepodáváme. Podávání liraglutidu v indikaci léčby obezity se nedoporučuje od 75 let věku. Bariatrická chirurgie je dnes vyhrazena pacientům orientačně do 65 let, i když rozhodující je posouzení biologického věku.
5 ZÁVĚR – DOPAD TĚCHTO DOPORUČENÍ PRO KLINICKOU PRAXI
5.1 OBECNÁ DOPORUČENÍ
Pro praxi jsou důležitá zejména tato opatření:
- Senioři zdatní s dobrým funkčním a kognitivním stavem a dobrou životní prognózou by měli mít péči a cílové hodnoty stejné jako mladší diabetici. Zásadním požadavkem je nepřítomnost těžkých hypoglykemií.
- Senioři křehcí (z mnoha aspektů rizikoví) by měli mít individuální cíle léčby nastavené tak, aby nedocházelo k výrazným výkyvům glykemie a nebyli tak ohroženi akutními hyperglykemickými komplikacemi.
- Ostatní kardiovaskulární rizikové faktory by měly být sledovány individuálně. Léčba hypertenze a dyslipidemie a léčba kyselinou acetylsalicylovou by měla být realizována podle studií provedených u starší populace. Doporučení podle klinických studií u mladších lze užít u pacientů s prognózou quoad vitam, která odpovídá obvyklé délce klinických studií v primární i sekundární prevenci (zhruba 5 let).
- Screening diabetických komplikací má být prováděn u těch komplikací, které by staršího diabetika ohrozily funkčně.
- Starší pacienti s diabetem by měli být léčeni primárně podle svých vlastních potřeb, a tedy nezávisle na prostředí, kde žijí (domácí prostředí, ústavní péče apod.), ovšem se zřetelem na socioekonomické postavení.
- Léky volíme individuálně a na prvním místě přihlížíme vždy k riziku hypoglykemie.
5.2 DOPORUČENÍ PRO VOLBU CÍLOVÝCH HODNOT KOMPENZACE DM
Cíle léčby však mají být vždy stanoveny individuálně se zřetelem ke stavu pacienta a přítomnosti přidružených nemocí. Na základě výsledků studií doporučují experti rozlišovat pacienty s DM2 podle výše rizika (riziko hypoglykemie a přítomnost dalších komplikací) a přizpůsobit podle ní cílové hodnoty. Pacienty s nízkým rizikem je možné vést k těsnější kompenzaci HbA1c do 45 mmol/mol. U pacientů se středním rizikem či dalšími komorbiditami se snažíme o kompenzaci do 53 mmol/mol včetně, kdežto diabetici s vyšším rizikem mohou mít cílové hodnoty HbA1c v pásmu mezi 54–60 mmol/mol. U nesoběstačných (závislých) imobilních křehkých pacientů s diabetem se doporučují dokonce hodnoty HbA1c v pásmu kolem 70 mmol/mol i vyšší.
Je nutné rozlišovat, zdali se jedná o seniory zdatné, nezávislé či křehké; křehké s omezenou soběstačností, případně úplně nesoběstačné (závislé). Podle těchto kategorií seniorů bychom se měli řídit i ve snaze o kompenzaci DM.
5.3 DISPENZÁRNÍ PROHLÍDKY U ZDATNÝCH SENIORŮ S DM2
Náplň dispenzární prohlídky je uvedena v tabulce 2 v kapitole 3.3 (str. 7).
5.4 KÓDY VYKAZOVANÉ ZDRAVOTNÍM POJIŠŤOVNÁM U PACIENTŮ S DM2 V ORDINACI VPL
- Kód 01201 – péče o stabilizovaného kompenzovaného diabetika 2. typu všeobecným praktickým lékařem.
Tento diabetik není v pravidelné péči diabetologa a je dispenzarizován u VPL.Dále je možno si požádat o kódy:
- Kód 01441 – stanovení glukózy glukometrem. Tento kód lze již vykazovat a použít při dispenzární prohlídce, a to ve frekvenci 3× ročně (1× ročně musí být vyšetřena glykemie ve spádové biochemické laboratoři).
- Kód 81327 – albumin – průkaz v moči vykazujeme ve frekvenci 1× ročně.
- Kód 12024 – oscilometrické vyšetření dolních končetin v ambulanci a stanovení indexu kotníkových tlaků (ABI). Vykazujeme ve frekvenci 1× ročně.
Pro toto vyšetření jsou celkem 3 oblasti indikace:- ICHDK susp.,
- DM 2. typu,
- věk 60 let + 1 rizikový faktor.
Toto vyšetření lze realizovat a vykázat příslušné zdravotní pojišťovně 1× ročně u všech dispenzarizovaných a léčených pacientů v ordinaci VPL.
- Kód 09532 – prohlídka osoby dispenzarizované. Pro chronické onemocnění pacienta dispenzarizovaného s DM2 v příslušné ambulanci ve frekvenci 4× ročně à 3 měsíce.
- Kód 09127 – EKG vyšetření vykazujeme ve frekvenci 1× ročně pro uvedenou diagnózu.
- Kód 01445 – stanovení HbA1c v ambulanci lékařem. Vykazujeme 1–3× ročně v ambulanci podle kompenzace a 1× ročně posíláme do spádové biochemické laboratoře.
- Kód 09123 – analýza moči chemicky. Vykazujeme ve frekvenci 1× ročně pro uvedenou diagnózu.
6 REKAPITULACE PRO PRAXI – CÍLOVÉ HODNOTY, KTERÉ BY MĚLY MINIMALIZOVAT RIZIKO STARŠÍHO A GERIATRICKÉHO PACIENTA
- HbA1c pod 45 mmol/mol – velmi přísné cílové hodnoty, za předpokladu, že jsou dosaženy bez výskytu hypoglykemií u pacientů bez komplikací. Z geriatrického hlediska jde o zdatné a nezávislé nemocné.
- HbA1c do 60 mmol/mol – u většiny starších nemocných s přidruženými závažnými chorobami, u nichž hypoglykemie zvyšují riziko kardiovaskulární. Z geriatrického hlediska jde obvykle o křehké pacienty s omezenou soběstačností.
- HbA1c do 70 mmol/mol – volnější kompenzaci volíme u pacientů s anamnézou těžké hypoglykemie, horší životní prognózou, s pokročilými komplikacemi a komorbiditami. Patří sem i pacienti s hůře dosažitelnou kompenzací. Z geriatrického hlediska jde o nesoběstačné (závislé) imobilní křehké pacienty.
- Nemocné se zcela krátkou životní prognózou léčíme jen symptomaticky, aby nehubli a neměli žízeň a polyurii, glykemie ani HbA1c nejsou u těchto pacientů pro léčbu rozhodující.
- Hodnota HbA1c 53 mmol/mol je obvyklou hranicí, kdy u zdatných seniorů revidujeme léčbu. Tato hodnota orientačně odpovídá glykemiím nalačno do 7,2 mmol/l a postprandiálně do 10 mmol/l (selfmonitoring).
Sources
1. Karen I, Svačina Š. Diabetes mellitus. Doporučený diagnostický a léčebný postup pro všeobecné praktické lékaře. Aktualizace 2018, SVL ČLS JEP. (https://www.svl.cz/files/files/Doporucene-postupy/2017/DP-DM-2018.pdf ).
2. Matějovská Kubešová H, Býma S. Demence. Doporučený diagnostický a léčebný postup pro všeobecné praktické lékaře. Aktualizace 2018, SVL ČLS JEP. (https://www.svl.cz/files/files/Doporucene-postupy/2017/DP-Demence.pdf ).
3. Býma S, Hradec J. Prevence kardiovaskulárních onemocnění. Doporučený diagnostický a léčebný postup pro všeobecné praktické lékaře. Aktualizace 2018, SVL ČLS JEP. (https://www.svl.cz/files/files/Doporucene-postupy/2017/DP-Prevence-KVO.pdf ).
4. Češka R, Herber O, et al. Dyslipidemie. Doporučený diagnostický a léčebný postup pro všeobecné praktické lékaře. Aktualizace 2017, SVL ČLS JEP. (https://www.svl.cz/files/files/Doporucene-postupy/2017/DP-Dyslipidemie.pdf ).
5. Hradec J, Býma S. Ischemická choroba srdeční. Doporučený diagnostický a léčebný postup pro všeobecné praktické lékaře. Aktualizace 2018. SVL ČLS JEP. (https://www.svl.cz/files/files/Doporucene-postupy/2017/DP-ICHS.pdf ).
6. Fried M, Svačina Š, et al. Moderní trendy v léčbě obezity a diabetu. Praha: Axonite, 2018. (https://www.axonite.cz/Moderni-trendy - -v-lecbe-obezity-a-diabetu-d222.htm).
7. Sinclair AJ; Expert Working Group. An international position statement on the management of frailty in diabetes mellitus. J Frailty Aging 2018;7(1):10–20.
8. Davies MJ, et al. Management of hyperglycaemia in type 2 diabetes. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD), 2018. Diabetologia 2018;61(12):2461–249.
9. Karen I, Filipovský J, a kol. Arteriální hypertenze. Doporučený diagnostický a léčebný postup pro všeobecné praktické lékaře. Aktua lizace 2014, SVL ČLS JEP. (https://www.svl.cz/files/files/Doporucene-postupy-od-2013/DP-AH-2014.pdf ).
10. Holt MR, et al. Diabetes care in extended-care facilities appropriate intensity of care. Diabetes Care 2007;30 : 1454–1458.
11. Inzucchi SE, et al. Management of hyperglycaemia in type 2 diabetes: a patient-centered approach. Position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia 2012;55(6):1577–96.
12. Munshi M, Lipitz LA (eds). Geriatric diabetes. Informa Healthcare New York, London, 2007.
13. Sinclair AJ, et al. European Diabetes Working Party for Older People. Clinical guidelines for type 2 diabetes mellitus. Executive sum mary. Diabetes Metab 2011;37 (Suppl 3):S27–38.
14. Sinclair AJ. (ed). Diabetes in old age. Wiley Blackwell, 2009.
15. Doporučené postupy České diabetologické společnosti ČLS JEP. (www.diab.cz).
16. Doporučené postupy Společnosti všeobecného lékařství ČLS JEP. (https://www.svl.cz/doporucene-postupy/).
17. DM sekce SVL ČLS JEP. (https://www.svl.cz/o-nas/dm-sekce/).
18. Yesavage JA, Brink TL, Rose TL, Lum O, Huang V, Adey M, Leirer VO. Development and validation of a geriatric depression screening scale: A preliminary report. J Psych Res1982;17 : 37–49.
19. Stránky České alzheimerovské společnosti. (www.alzheimer.cz).
Labels
Geriatrics General practitioner for adults Orthopaedic prosthetics
Article was published inGeriatrics and Gerontology

2019 Issue 2-
All articles in this issue
- Editorial
- Specifics of acute urological care in elderly patients
- TRUS/MRI fusion prostate biopsy in patient over 65 years – results and complication rate analysis.
- Are robot-assisted radical prostatectomies safe in patients over 65?
- Risk and complications of the robotic partial nephrectomy in patients in age over 65 years
- The treatment of the water and electrolyte disturbances in geriatric patients.
- A Geriatrician in a General Practitioner´s Shoes
- Ohlédnutí za Celostátním gerontologickým kongresem
- DIABETES MELLITUS LÉČBA U STARŠÍCH PACIENTŮ V ČR. Doporučený diagnostický a terapeutický postup pro všeobecné praktické lékaře
- Geriatrics and Gerontology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Risk and complications of the robotic partial nephrectomy in patients in age over 65 years
- The treatment of the water and electrolyte disturbances in geriatric patients.
- TRUS/MRI fusion prostate biopsy in patient over 65 years – results and complication rate analysis.
- Are robot-assisted radical prostatectomies safe in patients over 65?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

