-
Medical journals
- Career
Horečka jako častý symptom
: H. Matějovská Kubešová
: Geriatrie a Gerontologie 2015, 4, č. 4: 169-172
: Review Article
Přehledný článek uvádí patofyziologické poznámky o vzniku a významu horečky v lidském organismu a vlivu horečky na jednotlivé orgánové soustavy. Podrobně je rozebrána etiologie horečky od nejčastějších příčin, jako jsou infekce, nádory či revmatologické choroby, po příčiny podstatně méně frekventované, jako polékové horečky nebo horečky neznámého původu. V závěru článku je popsán algoritmus diagnostiky horečky.
Klíčová slova:
horečka – etiologie horečky – horečka neznámé etiologie – infekce – revmatologické choroby – nádoryPatofyziologické poznámky
Normální tělesná teplota lidského těla se pohybuje v rozmezí 36,0–36,9 °C a podléhá cirkadiánnímu rytmu s kolísáním v rozmezí +0,5 °C – typicky v ranních hodinách dosahuje nejnižších hodnot, v podvečerních hodinách nevyšších hodnot(1, 2). Názory různých autorů na tzv. normální rozmezí tělesné teploty se liší. Například Harrisonova učebnice interny z roku 1994 Petersdorf (1994) ještě uvádí oproti našim tradičním názorům normální rozmezí tělesné teploty v klidu 35,8–37,7 °Cv ústní dutině a 36,1–38,3 °C v rektu(3). Pro geriatrické pacienty se zdá být toto rozmezí příliš volné, neboť mnohé nesporné zánětlivé choroby se manifestují pouze subfebriliemi. Naopak Falsey 2015 upozorňuje, že v případě influenzy poskytuje horečka u starších nemocných příznak s pouze 57% senzitivitou a 71% specificitou a za horečku by měla být považována již teplota nad 37,3 °C(4). Stejně tak u divertikulitidy byla teplotní reakce významně nižší u nemocných nad 65 let než u nemocných ve věku 55–64 let(5).
Teplotní rozmezí je regulováno prostřednictvím signálů vnitřních a vnějších termoreceptorů, ovlivňujících aktivitu hlavního termoregulačního centra v preoptické části hypotalamu, aktivita tohoto samotného centra však může být ovlivněna v rámci vaskulární encefalopatie nebo vystupňování degenerativních změn např. při Alzheimerově chorobě. Receptory periferní se rozdělují na receptory pro tepelné vjemy umístěné v horním a středním koriu a reagující na teplotu 30–50 °C s maximem reakce při 45 °C. Receptory pro chlad jsou rozmístěné asi 10x hustěji než receptory tepelné v epidermis a v horní vrstvě koria. Reagují v rozmezí 10–45 °C s maximem reakce při 28 °C. Také tato souhra může být u nemocných vyššího věku alterována procesem atrofie kůže se zánikem potních žláz, který může být autoimunitně stupňován, a také vymizením podkožního tuku jako izolační vrstvy při malnutrici s kachexií(1).
Akrální části těla se chovají poikilotermně, tedy jejich teplota se částečně přizpůsobuje teplotě okolí, čímž zabraňují ztrátám tepla. Jádro organismu se naopak chová homoiotermně, tedy i při velkých změnách okolní teploty jeho teplota kolísá minimálně. Receptory pro vnímání teploty vnitřních orgánů jsou rozmístěny v oblasti dolní části mozkového kmene, ve spinální míše, v nitrobřišních orgánech a v perivazálních pleteních velkých žil.
Zvýšení tělesné teploty až horečka vzniká přenastavením regulačních mechanismů na vyšší teplotu, což vyvolá pocit chladu, zimnici, třesavku a kontrakci kožních i kosterních svalových vláken. Horečka je definována jako zvýšení tělesné teploty nad 38 °C, hodnoty mezi 37,0 °C a 37,9 °C jsou označovány za zvýšenou teplotu. Vzestup teploty je po dosažení maximální hodnoty následován jejím poklesem za zčervenání kůže a masivní produkce potu. Nastavení regulace na vyšší teplotu probíhá prostřednictvím prostaglandinů produkovaných v oblasti hypotalamu. Jejich zvýšená produkce je provokována pyrogeny – interleukiny IL-1, IL-6, interferony β-IFN, μ-IFN, tumor necrosis factor-α. Produkce těchto cytokinů je stimulována monocyty nebo makrofágy aktivovanými kontaktem s infekčním agens. Dalším pyrogenem se mohou stát endotoxiny produkované samotnými bakteriemi nebo partikule bakteriálního těla, nejčastěji části jádra. U horečky neinfekčního původu jsou pyrogeny produkovány vlivem probíhajícího sterilního zánětu. Horečka však může vzniknout i bez přítomnosti pyrogenů, např. při intrakraniálním krvácení, trombóze, silné hemolýze, mozkových nádorech, poruchách hypotalamu, městnání sekretu například v paranazálních dutinách.
Vliv horečky na jednotlivé orgánové soustavy
Soustava kardiovaskulární reaguje zvýšením tepové frekvence přibližně o 10/min na každý stupeň zvýšení tělesné teploty, současně dochází ke zvyšování minutového objemu. Reakce krevního tlaku je rozdílná podle aktuálního stupně vazodilatace či vazokonstrikce. Snížení schopnosti vazokonstrikce a vazodilatace ve vyšším věku, spolu s obleněním krevního oběhu při imobilizaci však tyto reakce různým způsobem modifikuje. Na vrcholu a při poklesu teploty dochází k intenzivní vazodilataci, což obvykle vede k poklesu systolického a diastolického tlaku, a zejména u starších nemocných může vyústit až v kolapsový stav(1,2).
Reakce soustavy dýchací je způsobena vyšší teplotou krve protékající regulačními dechovými centry, což vyvolává tachypnoi se zvýšeným výdejem oxidu uhličitého.
V trávicím traktu dochází při horečce ke snížení sekrece ve splanchniku a zároveň ke zvýšení resorpce v oblasti kolon, což vede ke snížení chuti k jídlu a zahuštění stolice až se vznikem zácpy.
V ledvinném parenchymu se při vyšší tělesné teplotě zvyšuje propustnost bazální membrány s následným únikem proteinů – doprovodným příznakem horečnatého stavu je proteinurie. Vlivem zvýšené kožní perspirace se při horečce mění poměry v bilanci tekutin – při nezvýšeném příjmu tekutin je pro udržení osmolality nutná intenzivnější reabsorpce vody v tubulech a je produkováno menší množství moči o vysoké specifické hmotnosti. Vícedenní trvání nepříznivé bilance tekutin vede postupně ke snížení intravaskulárního objemu tekutin až vzniku prerenálního ledvinného selhání.
Centrální nervový systém je horečkou ovlivněn nejčastěji ve smyslu útlumu, apatie, a zejména u seniorů je to dezorientace až delirantní stavy.
Význam horečky
Horečka je významným obranným mechanismem organismu napomáhajícím zejména likvidaci infekčních agens, ale je také projevem aktivace zánětlivých neinfekčních či nádorových procesů.
Zvýšení tělesné teploty jako součást obranných procesů proti infekci má efekt na urychlení chemotaxe a zintenzivnění fagocytózy, dále na urychlení tvorby protilátek a tvorby protivirově působícího interferonu. Výsledkem těchto procesů, k jejichž efektivnímu průběhu je zapotřebí adekvátní sérová hladina železa, mědi a zinku, je zpomalení růstu až usmrcení mikrobů.
Pro klinickou praxi z těchto poznatků vyplývá, že příliš úzkostlivé tlumení teplot omezuje přirozené obranné schopnosti organismu, a dále fakt, že zakořeněná zvyklost odebírat vzorky krve k hemokultivaci při teplotě „nad 38 °C“, jak se často ordinuje, se může častěji míjet účinkem, protože v té fázi jsou již všechny obranné mechanismy plně rozvinuty a zachycený mikrob již nemusí být viabilní. Proto se doporučuje odebírat vzorek krve pro efektivní hemokultivaci v okamžiku bakteriemie, tedy v době, kdy pacient pociťuje zimnici, třesavku, ale teplota teprve začíná stoupat. Z tohoto pohledu může být problematické zachycení vzestupu teploty u nemocných s kognitivní poruchou.
Etiologie horečky
Pro základní orientaci se používá dělení na tzv. velkou a malou trojku. Velká trojka, tedy infekce, revmatologické choroby a nádory, pravděpodobně zahrne až 80–90 % možných příčin vzniku horečky. Takzvaná malá trojka, tedy horečka provokovaná léky, habituální hypertermie či horečka předstíraná, zahrnuje sice velmi malé procento ze spektra možných příčin, o to těžší je ale její původ vypátrat (tab. 1). Zbývajících 10 % příčin horečky zůstává po prvních pokusech a zjištění neobjasněno a řadí se do skupiny horeček neznámého původu – fever of unknown origine (FUO). Distribuce příčin horečky se bude geograficky lišit – například skupina čínských autorů popsala 500 případů horečky nejasné etiologie a popsala 46,2 % infekčních teplot, z toho třetina byla tuberkulózního původu, 11,6 % nádorových teplot a 19,8 % nemocných s horečkou při systémových chorobách pojiva. Zbývající podíl byly teploty různého původu – 12,8 % a horečky nezjištěné etiologie – 9,6 %(6).
1. Základní rozdělení možných příčin horečky 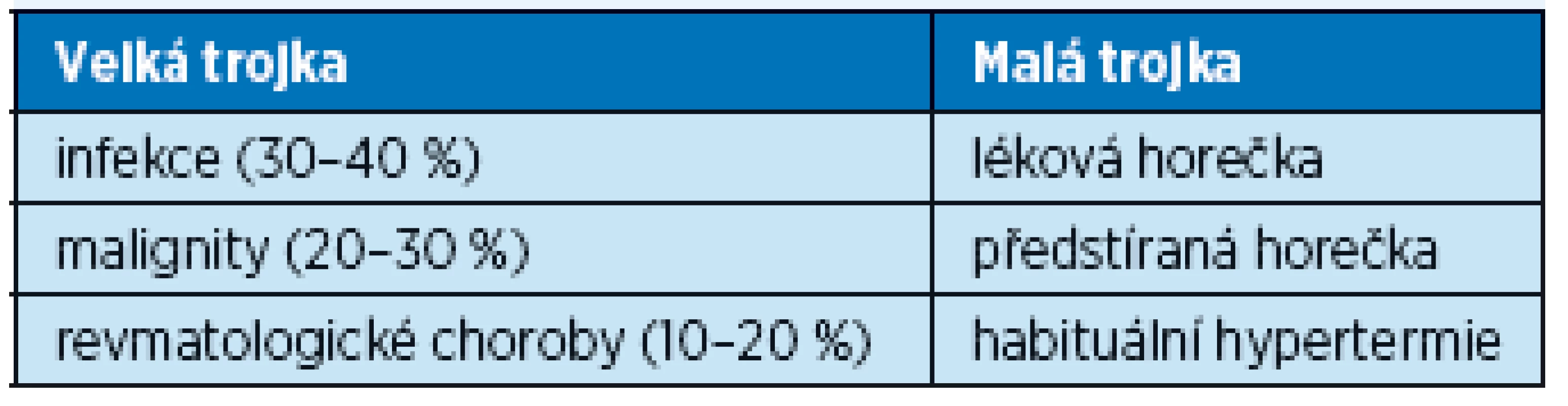
Kritéria FUO jsou splněna tehdy, pokud se horečka objevuje opakovaně nad 37,8 °C po dobu trvající déle než 3 týdny, kde příčina teplot není zřejmá ani po 3denním vyšetřování při hospitalizaci nebo po 3 ambulantních návštěvách. Přehled možných příčin horečky neznámého původu ukazuje tabulka 2.
2. Přehled možných příčin horečky neznámého původu 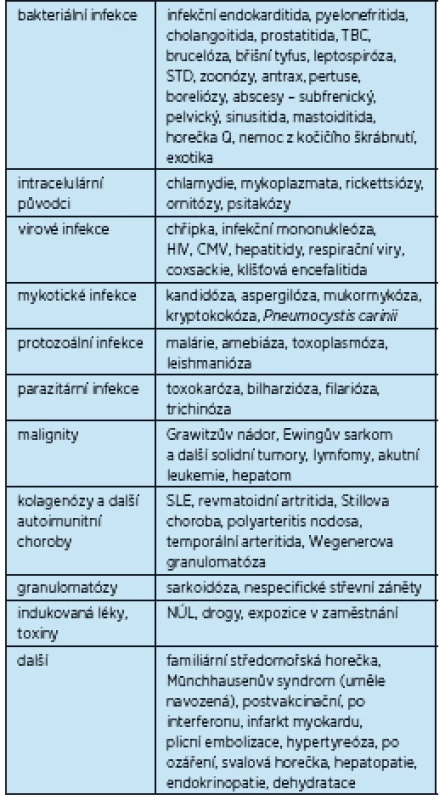
Postup pátrání po příčině horečky
V anamnéze aktuálních obtíží se cíleně ptáme na trvání horečky, na výskyt nočního pocení, průjmů, úbytek hmotnosti, únavnost, cefaleu, světloplachost, závrať. Vyhodnocení průběhu horečky v čase je v současné éře antibiotik méně přínosné, jako diagnosticky cenný zůstává průběh horečky při malárii, horečka undulujícího typu při Hodgkinově lymfomu a inverze teplot při tuberkulóze(7). Při zjišťování dalších okolností se zajímáme o kontakt s infekcí, se zvířaty, případné oděrky z poslední doby a způsob jejich ošetření, imunizace či zákroky v poslední době, implantace cizích materiálů, abúzus, rizikové sexuální chování(8). Cesty do zahraničí je v současné době nutno prodiskutovat s nemocným cíleně vzhledem k narůstající rozmanitosti zemí, kam se naši občané vydávají(9). Dále pátráme po prodělané chorobě, která by mohla vést k imunodeficitu, a odebíráme kompletní farmakologickou anamnézu včetně volně prodejných medikamentů, zejména nově zavedených, a potravinových doplňků. V této souvislosti se nově objevily zprávy o výskytu maligního neuroleptického syndromu při podávání quetiapinu jako atypického neuroleptika, kde se výskyt této komplikace neočekává tak často jako při podávání typických neuroleptik(10).
Fyzikální vyšetření provádíme komplexně, opakovaně, se zaměřením na kožní povrch – exantém, petechie, Oslerovy uzly, třískové hematomy, dále opakovaně palpačně vyšetřujeme všechny dostupné uzliny, štítnou žlázu, temporální arterie. Vyšetření per rectum napomůže diagnostice případných nitrobřišních procesů(2).
Z laboratorních metod je obvykle nutno odebírat základní parametry opakovaně a vyhodnocovat jejich dynamiku. Sedimentace erytrocytů si stále zachovává svůj přínos – hodnoty nad 100/hod. doprovází většinu malignit, větší rozdíl mezi hodnotou za první a druhou hodinu svědčí spíše pro zánětlivou etiologii. Krevní obraz s diferenciálním rozpočtem napomůže k rozlišení bakteriální infekce od dalších typů infekcí, proteiny akutní fáze – CRP, případně fibrinogen, dále hladiny dusíkatých látek, jaterní testy a transaminázy včetně laktátdehydrogenázy, sérové hladiny celkové bílkoviny a albuminu. Odběr hemokultur se snažíme načasovat na období zimnice a třesavky. Při nejasném nálezu i dynamice pokračujeme odběrem hodnot nádorových markerů, i když je nutno si uvědomit, že až na výjimku PSA se pohybujeme v senzitivitě i specificitě nepřesahující 60 % – tedy negativní výsledek nemusí znamenat, že konkrétní nemocný malignitu nemá(11).
Při rozvahách o původu horečky se neobejdeme bez výsledků mikroskopického a kultivačního vyšetření všech dostupných biologických materiálů, jejichž odběr je nutno technicky zabezpečit proti kontaminaci jak při samotném odběru, tak při následné manipulaci. Vzorky obvykle necháváme vyšetřit na různých typech kultivačních médií.
Sérologická vyšetření je nutno také provádět opakovaně, většinou s časovým odstupem 10 dnů až několik týdnů k vyhodnocení dynamiky, což se týká zejména hepatitid, viru infekční mononukleózy (EBV), cytomegalovirózy (CMV), viru lidské imunodeficience (HIV), chlamydií, mykoplazmat apod. Využití polymerázové řetězcové reakce prozatím v našich podmínkách jeví vysokou senzitivitu a nízkou specificitu, proto se v rutinní praxi objevuje jen zřídka.
Pro odhalení původu horečky neinfekčního původu se snažíme o základní orientaci v aktivitě imunologických parametrů – antinukleárních antigenů (ANA), protilátek proti cytoplazmě neutrofilů (ANCA), protilátek proti DNA – dvouvláknové dsDNA. Zjištění vyšší hladiny cirkulujících imunokomplexů svědčí pro vyšší intenzitu vytváření komplexu antigen–protilátka(12). Tuberkulinovou reakci lze v současné době vysokého výskytu alergií využít jen jako podpůrného momentu vyjadřujícího celkovou zvýšenou pohotovost obranného systému. Využíváme všech naznačených patologií k odběru biologického materiálu, a tím urychlení stanovení přesné diagnózy(13).
Základním zobrazovacím vyšetřením při pátrání po původu horečky je rtg snímek orgánů hrudníku, paranazálních dutin a panoramatický snímek čelistí. K vyloučení abscesu či jiného zánětlivého postižení v dutině břišní je indikováno v první fázi ultrazvukové vyšetření břicha a malé pánve. Při rizikové anamnéze, změně velikosti srdečního stínu, odhalení nově vzniklého srdečního šelestu či kožních hematomů je indikováno echokardiografické vyšetření z transtorakálního či lépe z transezofageálního přístupu.
Další postup
Pokud základní sestava vyšetření nevedla k odhalení příčiny horečky, rozšiřujeme spektrum sérologických vyšetření i o původce řidčeji se vyskytující, jako jsou antropozoonózy, břišní tyfus, leptospiróza, STD, zoonózy, antrax, pertusse, borreliózy, horečka Q, nemoc z kočičího škrábnutí, exotické choroby, rickettsiózy, ornitózy, psitakózy atd. – většinou již po konzultaci s mikrobiologem. Rozšiřujeme po konzultaci s imunologem také spektrum imunologických vyšetření.
Na řadu přicházejí vyšetření endoskopická s cílem odhalení lokalizované infekce či jiné patologie – bronchoskopie s bronchoalveolární laváží, kolonoskopie, gastrofibroskopie, rektoskopie(14).
Souběžně doplňujeme i spektrum zobrazovacích metod o CT, případně NMR břicha a hrudníku, PET CT či vyšetření značenými leukocyty a vyšetření bioptická – nejčastěji z kožních morf či svalu, exstirpace uzliny, sternální punkce nebo trepanobiopsie(15, 16).
Závěry pro praxi
- Proces stárnutí snižuje schopnost organismu vyvinout horečku jako jednu z obranných reakcí, vzestup teplot je u staršího nemocného při stejném typu onemocnění nižší než u mladšího nemocného.
- Při horečkách septického charakteru je efektivnější odběr krve na hemokultivaci již při pocitu zimnice a při třesavce, tedy při bakteriemii, než při plném rozvinutí horečky.
- Etiologie horečky je z 80–90 % infekční, revmatologická nebo onkologická („velká trojka“), zbývající podíl tvoří polékové reakce, předstíraná horečka či habituální hypertermie („malá trojka“).
- Zvýšení tělesné teploty nad 37,8 °C v trvání 3 týdny, aniž byl zjištěn její původ, je horečka neznámého původu.
Autorka prohlašuje, že v souvislosti s publikací článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny farmaceutickou firmou.
prof. MUDr. Hana Matějovská Kubešová, Ph.D.
Klinika interní, geriatrie a praktického lékařství
LF MU a FN Brno
prof. MUDr. Hana Matějovská Kubešová, Ph.D.
e-mail: kubes@med.muni.cz
Vysokoškolské vzdělání ukončila v roce 1982 na Lékařské fakultě Masarykovy univerzity v Brně, na téže fakultě absolvovala doktorské studium v r. 1993, habilitační řízení v r. 1997 a profesorské řízení v r. 2003. Od roku 1999 je přednostkou Kliniky interní, geriatrie a praktického lékařství LF MU a FN Brno. V roce 2011 byla zvolena předsedkyní České gerontologické a geriatrické společnosti ČLS JEP..
Sources
1. Kalvach Z, Zadák Z, Jirák R a kol.: Gerontologie a geriatrie. Grada-Avicenum 2005.
2. Špinar J, Ludka O a kol.: Propedeutika a vyšetřovací metody vnitřních nemocí. Praha: Grada Publishing 2013.
3. Petersdorf RG: Hypothermia and hyperthermia. In: Harrison´s principles of internal medicine, Vol. 2. 13th edition. New York: McGraw-Hill 1994 : 2473–2479.
4. Falsey AR, Baran A, Walsh EE. Should clinical case definitions of influenza in hospitalized older adults include fever? Influenza Other Respir Viruses 2015; Suppl 1 : 23–29.
5. Iyer R, Longstreth GF, Chu LH, et al. Acute colonic diverticulitis: diagnostic evidence, demographic and clinical features in three practice settings. J Gastrointestin Liver Dis 2014; 23(4): 379–386.
6. Jun-Cai TU, Ping Z, Xiao-Juan LI, et al. Clinical etiologies of fever of unknown origin in 500 cases. Zhongguo Yi Xue Ke Xue 2015; 37(3): 348–351.
7. Havránek P. Teploty nejasného původu. Doporučené postupy pro praktické lékaře. ČLS JEP 2001.
8. Mc Gregor AC, Moore DA. Infectious cases of fever of unknowm origin. Clin Med 2015; 15(3): 285–287.
9. Korzeniewski K, Gawel B, Krankowska D et al. Fever of unknown origin in returning travellers. Int Marit Health 2015; 66(2): 77–83.
10. Schattner A, Kitroser E, Cohen JD. Fatal Neuroleptic Malignant Syndrome Associated With Quetiapine. Am J Ther 2015; Jun 30.
11. Foggo V, Cavenagh J. Malignant causes of fever of unknown origin. Clin Med 2015; 292–294.
12. Lachmann HJ. Autoinflammatory syndromes as causes of fever of unknown origin. Clin Med 2015; 15(3): 295–298.
13. Malegová J, Koten L, Horák P. Stillova nemoc dospělých – obtížná cesta k diagnóze přes horečku a výpotky nejasné etiologie. Vnitř Lék 2014; 60(5–6): 520–526.
14. Lecoules S, Carmoi T, Klotz C, et al. Fever as the presenting manifestation of colon cancer: a case series of 11 patients. Rev Med Interne 2013; 34(3): 136–140.
15. Goldman S. Positron emission tomography in inlammatory disorders. Rev Med Brux 2012; 33(4): 436–442.
16. Řehák Z, Fojtík Z, Staníček J. 18FDG PET v diagnostice vaskulitidy velkých cév. Vnitř Lék 2006; 52(11): 1037–1044.
Labels
Geriatrics General practitioner for adults Orthopaedic prosthetics
Article was published inGeriatrics and Gerontology

2015 Issue 4-
All articles in this issue
- Fever as a frequent symptome
- Diarrhoeal diseases in general practitioner’s work
- Peptic ulcer disease and Helicobacter pylori infection in the elderly
- Urinary tract infections in geriatric population
- Treatment of non-healing wounds at geriatric patiens
- Travelling of seniors – prevention of infections during travels do exotic countries
- Geriatric care as the impulse for implementing a new concept of infection prevention and control
- Streptococcal and pneumococcal infections from the geriatrist´s view
-
Features of adherence to drug therapy elderly:the impact of the diseaseand form of the drug
(the results of research in the urban population of Ecuador)
- Geriatrics and Gerontology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Fever as a frequent symptome
- Diarrhoeal diseases in general practitioner’s work
- Streptococcal and pneumococcal infections from the geriatrist´s view
- Treatment of non-healing wounds at geriatric patiens
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


