-
Medical journals
- Career
Přehled dotazníků a škál hodnotících motorické příznaky pacientů s Parkinsonovou nemocí
Authors: R. Kozáková; R. Bužgová; R. Zeleníková; L. Sikorová
Authors‘ workplace: Vedoucí: prof. PhDr. Darja Jarošová, Ph. D. ; Lékařská fakulta ; Ústav ošetřovatelství a porodní asistence ; Ostravská univerzita v Ostravě
Published in: Prakt. Lék. 2018; 98(3): 116-120
Category: Of different specialties
Overview
U pacientů s Parkinsonovou nemocí (PN) je vhodné z důvodu progrese a specifickým příznakům nemoci poskytování multidisciplinární péče, jejímž cílem je udržení co nejlepší kvality života pacienta i jeho rodiny. V zahraničí jsou využívány dotazníky a škály k hodnocení stavu pacienta, zjišťování progrese nemoci a následnému zajištění individualizované péče. Cílem tohoto přehledového článku je popsat a analyzovat škály používané při hodnocení pa - cientů s PN v oblasti motorických funkcí. Vyhledáváním v elektronických databázích bylo nalezeno 22 škál určených pro pacienty s PN. Pro hodnocení funkčního stavu je nejčastěji využívána škála MDS-UPDRS (Movement Disorder Society Unified Parkinson’s Disease Rating Scale). Využití této škály je doporučováno v klinické praxi i ve výzkumu.
Klíčová slova:
Parkinsonova nemoc – dotazníky – kvalita života – multidisciplinární péče – škályÚVOD
Parkinsonova nemoc (PN) je chronické, progresivní a nevyléčitelné onemocnění centrálního nervového systému. Jedná se o neurodegenerativní onemocnění, které typicky začíná asi kolem 60. roku a projevuje se motorickými a non-motorickými příznaky.
Dle dostupných údajů týkající se evropské populace se prevalence PN odhaduje ve věkové skupině nad 65 let věku na více než 1/100 (22). Podobné údaje z České republiky zatím nejsou k dispozici; počet nemocných se odhaduje na 10 000až 15 000. Onemocnění postihuje o něco více muže, poměr mužů k ženám se odhaduje na 1,2 : 1 (1). Prevalence se zvyšuje v případě familiárního výskytu onemocnění (asi na 5 %).
Parkinsonova nemoc se vyznačuje klasickou trias základních příznaků: bradykineze, rigidita a klidový tremor, které se v důsledku progrese onemocnění zhoršují. V pozdním stadiu jsou přítomny tzv. pozdní motorické komplikace s kolísavým stavem hybnosti (tzv. motorické fluktuace) a přítomností mimovolních pohybů (tzv. dyskinezí) (6). Zjevným důsledkem patologického děje s různě rychlou progresí je charakteristický syndrom, ve kterém se obvykle kombinuje porucha kognitivních funkcí s poruchami hybnosti a chování. Poruchy kognitivních funkcí charakterizují exekutivní dysfunkce a u některých pacientů se rozvíjí demence (1). Motorické komplikace a výskyt non-motorických příznaků spolu úzce souvisí, např. zhoršení motoriky má negativní vliv na psychosociální pohodu pacientů a zvyšují jejich závislost na pomoci jiných při aktivitách denního života a sociální stigma. Vyúsťují do výrazného snížení kvality života pacientů, jejich rodiny a blízkých (5).
Pro udržení kvality života pacienta je nutné jednotlivé příznaky nemoci opakovaně hodnotit v jednotlivých fázích nemoci z důvodu plánování vhodných intervencí multidisciplinárním týmem.
Pro hodnocení funkčního stavu pacientů jsou u nás i v zahraničí využívány různé škály i dotazníky, a to jak v klinické praxi, tak ve výzkumu. Použití škál u pacientů s PN může pomoci multidisciplinárnímu týmu zhodnotit aktuální problémy pacienta a pomoci zajistit adekvátní, individualizovanou péči.
Cílem tohoto přehledového článku je popsat škály používané při hodnocení pacientů s PN v oblasti motorických příznaků. Na základě tohoto přehledu budou vybrány vhodné škály, které budou v rámci projektu AZV MZ ČR č. 17-29447A s názvem Neuropaliativní a rehabilitační přístup pro zachování kvality života pacientů v pokročilé fázi vybraných neurologických onemocnění validovány pro české prostředí.
METODIKA
Škály a dotazníky využívané při hodnocení pacientů s PN byly vyhledávány v elektronických databázích: Medline, Scopus, Proquest Public Health a Web of Knowledge (období 1965–2017). Klíčová slova pro vyhledávání byla následující: parkinsons disorders, scale, assessment, patient needs, measures, instrument, questionnaire, needs assessment. Do přehledu byly zařazeny škály splňující tato kritéria: Byla hodnocena reliabilita a validita, využití škály u pacientů s PN v různém prostředí péče. V přehledu škál je uvedena vnitřní konzistence, která vyjadřuje schopnost testu poskytovat shodné výsledky při opakování studií podobného charakteru. Celkem bylo nalezeno 22 nástrojů určených pro pacienty s PN, které jsou vhodné a jsou také využívány u pacientů s PN.
VÝSLEDKY A DISKUZE
Přehled specifických škál hodnotících motorické symptomy pacientů s PN je uveden v tabulce 1.
Table 1. Přehled škál hodnotících motorické symptomy u pacientů s Parkinsonovou nemocí 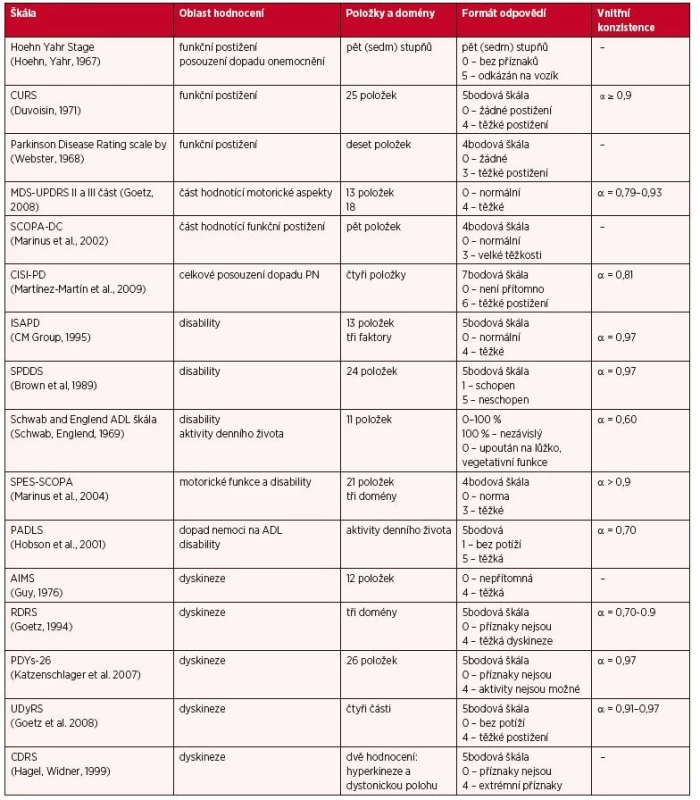
PL 2018/3 tab 11 
CURS – Columbia University Rating Scale, MDS-UPDRS – Movement Disorder Society Unified Parkinson’s Disease Rating Scale, CISI-PD – Clinical impression of Severity index, ISAPD – Intermediate Scale for Assessment of Parkinson disease, SPDDS – Self-assessment Parkinsons Disease Disability Scale, SCOPA-DC – Scales for Outcomes in Parkinson’s disease – diary card, SPES-SCOPA – Scales for Outcomes in Parkinson’s disease , PADLS – Parkinson’s Disease Activities of Daily Living Scale, AIMS – Abnormal Involuntary Movement Scale, RDRS – Rush dyskinesia Rating Scale, PDYs-26 – Parkinson disease dyskinesia scale, UDyRS – Unified Dyskinesia Rating Scale, CDRS – Clinical Dyskinesia Rating Scale, LFADLDS – Lang-Fahn activities of daily living dyskinesia scale, WOQ – Wearing off Questionare Škály hodnotící motorické symptomy u pacientů s PN
Jedna z prvních škál hodnotících motorické symptomy pa-cientů s PN byla škála Hoehnové a Yahrova (15). Původní škála rozlišovala pět stupňů funkčního omezení, její modifikovaná verze z roku 1990 rozlišuje sedm stupňů funkčního omezení. Celková dysfunkce související s PN je v H-Y škále hodnocena ze dvou aspektů. Prvním z nich je rozsah motorického postižení a druhým aspektem je stupeň postižení rovnováhy a chůze. Tíže postižení je klasifikována na základě progrese z jednostranného (stadium 1) do oboustranného motorického postižení bez poruchy rovnováhy (stadium 2). Přítomnost poruchy rovnováhy bez závislosti pacienta na cizí pomoci je hodnocena jako stadium 3, porucha rovnováhy se ztrátou fyzické nezávislosti, ale se zachovanou schopností stoje a chůze jako stadium 4. Stupeň postižení, kdy je pacient neschopen stoje a chůze, upoután na invalidní vozík či lůžko, je hodnocen jako stadium 5. Modifikovaná verzi H-Y škály obsahující sedm stupňů je rozšířena o dva mezistupně: stadium 1.5 charakterizované přítomností jednostranného motorického a axiální postižení a stadium 2.5 charakterizované přítomností oboustranného motorického postižení s pozitivitou pull testu. V modifikované podobě je obsažena v V. části UPDRS.
K dalším škálám hodnotících funkční postižení se řadí škála CURS (Columbia University Rating Scale), která byla vytvořena v roce 1971 (4). Škála hodnotí symptomy v pěti oblastech: brady/hypokineze, třes, rigidita, posturální stabilita a ostatní oblasti.
Webstrova škála byla vytvořena již v roce 1968 (26) a hodnotí deset příznaků (bradykineze rukou, rigidita, postura, souhyb horních končetin při chůzi, chůze, tremor, mimika, seborea, řeč, soběstačnost). Každý příznak je ohodnocen 0 až 3 body, přičemž 0 bodů znamená normální funkci. Tato škála hodnotí závažnost onemocnění. Změny bodového hodnocení v průběhu času u pacientů odrážejí změny v důsledku progrese onemocnění nebo terapeutických zásahů.
Nejčastěji je v současné chvíli používána MDS-UPDRS (Movement Unified Parkinson’s disease rating scale) (8). Jedná se o revidovanou verzi dotazníku UPDRS z roku 2001. V nové verzi zůstalo zachováno původní rozdělení do čtyř částí. První část je určena pro hodnocení non-motorických aspektů denního života, druhá část pro hodnocení motorických aspektů denního života. Každá z nich obsahuje 13 položek, které se hodnotí buď na základě rozhovoru s pacientem, nebo je hodnotí pacient s pečovatelem. Třetí část zaměřená na vyšetření motorického stavu je téměř identická s původní verzí UPDRS, rozdíl je pouze v tom, že ke každému vyšetřovanému úkonu byla vytvořena jednotná specifická instrukce. Obsahuje v 18 oddílech celkem 33 jednotlivých položek. Čtvrtá část určená k hodnocení přítomnosti a tíže motorických komplikací onemocnění si zachovala původní podobu. Škála byla přeložena do více jazyků s ověřením reliability – jako například do francouzštiny, němčiny, španělštiny, italštiny, japonštiny a turečtiny.
Dalšími široce využívanými instrumenty pro upřesnění potíží pacientů s PN jsou škály SCOPA (Scales for Outcomes in Parkinson’s disease). Motorické příznaky hodnotí SPES-SCOPA (17), který obsahuje 21 položek a tři domény: funkční postižení, aktivity denního života a motorické komplikace. Existují čtyři možnosti odpovědí, které se pohybují od 0 (normální) do 3 (těžké). SCOPA-DC (Scales for Outcomes in Parkinson’s disease – diary card) je vedena deníkovou formou, kdy po dobu 3 dnů jsou zaznamenávány potíže týkající se chůze, schopnosti měnit pozice, hybnosti horních končetin a spánku.
Závažnost celkového dopadu PN posuzuje CISI-PD (The Clinical Impression of Severity Index for Parkinson’s Disease). Tento index (18) je tvořen čtyřmi položkami (motorické příznaky a komplikace, kognitivní stav a postižení), které jsou hodnocené na škále 0 (vůbec ne) až 6 (velmi závažné nebo těžké postižení). Celkové skóre se vypočte součtem bodů. Jinou škálou, pomocí které pacient subjektivně hodnotí dopad PN na aktivity denního života, je pětistupňová škála PADLS (Parkinson’s disease Activities of Daily Living Scale) (14).
K hodnocení disability bylo vytvořeno také několik škál, např. ISAPD (Intermediate Scale for Assessment of Parkinson’s disease), která byla vytvořena v roce 1995 (3). Škála hodnotí symptomy související s PN ve třech doménách: aktivity denního života, chůzi a pohyblivost a řeč a stravování. Další škálou je SPDDS (Self assessment Parkinson’s disease disability scale) vytvořená Brownem a Marsdenem v roce 1989 (2). Škála zahrnuje 24 položek, které se zabývají individuálním výkonem pacienta v každodenním životě a využívá k tomu pětibodovou Likertovu škálu pro každou položku, která je nastíněna následovně: 1 – schopen jednat samostatně a bez potíží, 2 – schopen jednat samostatně s malou námahou, 3 – schopen jednat sám s velkým úsilím nebo malou pomocí, 4 – schopný jednat jen s velkou pomocí nebo 5 – neschopen jednat vůbec. Skóre se pohybuje od 24 do 120, přičemž vyšší skóre ukazují na závažnější poruchu. Nástrojem hodnotícím celkový stupeň funkční nezávislosti a disability je Schwabova a Englandova škála (22). Jednotlivec je požádán o hodnocení své funkce pomocí 11bodové stupnice (10 % přírůstků) ze 100 % (zcela nezávislé; dělat všechny práce bez pomalosti, obtížnosti nebo poruchy, v podstatě normální, nevědomé jakékoliv obtížnosti) až 0 % (vegetativní funkce jako polykání, močový měchýř a střeva nefungují).
K hodnocení tíže dyskineze byly nalezeny následující škály. Škála AIMS (Abnormal Involuntary Movement Scale) posuzuje závažnost abnormálních pohybů na jednotlivých částech těla (11). Škála obsahuje 12 položek podle hodnocené části těla, každá z těchto položek je klasifikována podle tíže postižení do pěti stupňů (0 až 4). Maximální skóre je 40. Další škála RDRS (Rush Dyskinesia Rating Scale) (10) slouží k posouzení tíže dyskinezí na základě hodnocení míry jejich interference s pohybem v průběhu tří motorických úkolů: chůze, pití z poháru, oblékání a zapínání kabátu. V roce 2007 (16) byla vytvořena škála PDYS-26 (Parkinson’s Disease Dyskinesia Scale), která zahrnuje 26 položek hodnocených pacientem, který kvantifikuje vliv dyskineze na aktivity denního života. Jednotlivé položky jsou orientovány na základní, instrumentální a sociální denní aktivity. Otázky se týkají interference dyskineze s těmito aktivitami. Tíže dyskineze se hodnotí na pětibodové stupnici 0 až 4. K nejnovějším škálám lze zařadit UDysRS (Unified Dyskinesia Rating Scale) vytvořenou v roce 2008 (9). Obsahuje jak autoevaluační otázky, které zodpovídá pa-cient nebo příbuzný, tak položky, jež jsou posuzovány lékařem. Cílem má být co nejobjektivnější posouzení abnormálních pohybů souvisejících s PN. Škála je složena ze čtyř částí. První dvě části jsou zaměřeny na anamnestické údaje vnímání dopadu „off“-dyskines a „on“-dyskines pacientem a hodnocení provádí pacient s dopomocí lékaře. Třetí část je určena k objektivnímu posouzení typu abnormálního pohybu a jeho distribuci na konkrétní části těla. Hodnocení se provádí pozorováním pacienta při provádění čtyř motorických úkolů: komunikace, pití ze šálku, oblékání a během vyšetření. Ve čtvrté části se hodnotí tíže dyskineze na jednotlivých částech těla v průběhu stejných aktivit jako ve třetí části. Další škálou je CDRS (Clinical Dyskinesia Rating Scale), jež vyhodnocuje hyperkinezi a dystonickou polohu, skórovanou pro každou oblast těla (obličej, krk, horní končetiny, dolní končetiny) (12). Skóre se pohybuje od 0 (žádné potíže) do 4 (extrémní), s použitím intervalů 0,5 bodů povolených pro šest položek. Maximální celkové skóre pro každou podskupinu (dyskineze a dystonie) je 28. Hodnocení vychází z pozorování pacienta v klidu a během aktivace.
Škála LFADLDS (The Lang-Fahn Activities of Daily Living Dyskinesia Scale) se pokouší zachytit míru postižení u pacientů s PN (19). Hodnotí se pět aktivit (rukopis nebo kreslení, krájení potravin a manipulačních potřeb, oblékání, hygiena a chůze), které mohou být postiženy dyskinezí. Při absenci dyskineze je přidělena 0 a schopnost vykonávat činnost představuje funkci v nejlepším stavu. Čtyřmi body jsou ohodnoceni pacienti, kteří nejsou schopni vykonat úkol samostatně či potřebují asistenci.
Další škálou je WOQ-19 (Wearing off Questionare), která kombinuje otázky zaměřené na motorické a non-motorické symptomy (24). Z motorických symptomů se jedná o třes, potíže s rovnováhou, zpomalení pohybu, zhoršení obratnosti, ztuhlost, svalové křeče a potíže při vstávání z křesla. Zkrácenou verzí je dotazník WOQ-9, který obsahuje devět otázek zaměřených na motorické i non-motorické symptomy související s wearing-off (25). Z motorických symptomů jsou zde obsaženy třes, zhoršená obratnost, svalové křeče, zpomalení hybnosti a ztuhlost.
Hauserův deník jde o autoevaluační deník, jež je v 30minutových intervalech vyplňován pacientem, který vybírá k hodnocení svého stavu vždy jednu ze čtyř kategorií: spánek, „off“ stav, „on“ stav s obtěžujícími dyskinezemi a „on“ stav bez obtěžujících dyskinezí (13). Současně zaznamenává dávku a dobu užití dopaminergní medikace. Součástí deníku jsou písemné instrukce podrobně popisující jednotlivé kategorie hybnosti. Nezbytná je však podrobná edukace a trénink pa-cienta v hodnocení hybného stavu a jeho záznamů do deníku. Deník nám pomáhá zhodnotit množství „off“ a „on“ period v průběhu dne a závislost hybného stavu pacienta na čase a dávce podávané dopaminergní medikace. Je velmi užitečným nástrojem zejména při ambulantních kontrolách, ale velmi přínosným je i v průběhu hospitalizace, kdy nám pomáhá monitorovat hybný stav pacienta po celých 24 hodin.
Analogií Hauserova deníku je CAPSIT-PD On-Off Diary, který v hodnocení stavu hybnosti rozlišuje kategorie; „off“ stav, částečný „off“ stav, „on“ stav bez dyskinezí a „on“ stav s dyskinezemi (21).
ZÁVĚR
U pacientů s onemocněním PN je doporučován multidisciplinární přístup. Využití hodnotících dotazníků a škál může lékařům a ostatním členům multidisciplinárního týmu pomoci hodnotit progresi nemoci a aktuální potřeby pacienta pro péči. Pro další výzkum doporučujeme překlad vybraných dotazníků a jejich validaci pro možné využití v České republice.
Střet zájmů: žádný.
ADRESA PRO KORESPONDENCI:
PhDr. Radka Kozáková, PhD.
Ústav ošetřovatelství a porodní asistence
Lékařská fakulta Ostravské univerzity
Syllabova 19, 703 00 Ostrava-Zábřeh
e-mail: radka.kozakova@osu.cz
Sources
1. Bednařík J, Ambler Z, Růžička E, a kol. Klinická neurologie – část spe-ciální I. Praha: Triton 2010.
2. Brown RG, MacCarthy B, Jahanshahi M, Marsden CD. Accuracy of self-reported disability in patients with parkinsonism. Arch Neurol 1989; 46(9): 955–959.
3. Cooperative Multicentric Group, Martínez-Martin P, Gil-Nagel A, Morlán Gracia L, et al. Intermediate scale for assessment of Parkinson’s disease. Characteristics and structure. Parkinsonism Relat Disord 1995; 1(2): 97–102.
4. Duvoisin RC. The evaluation of extrapyramidal disease. In: De Ajuriaguerra J, Gauthier G. (eds.) Monoamines, noyaux gris centraux et de syndrome de Parkinson. Masson: Paris 1971; 313–325.
5. Elman LB, Houghton DJ, WU GF, et al. Palliative care in amyotrophic lateral sclerosis, Parkinson´s disease, and multiple sclerosis. J Palliat Med 2007; 10(2): 433–457.
6. García-Ruiz PJ, Del Val J, Fernández IM, Herranz A. What factors influence motor complications in Parkinson disease? – a 10 year prospective study. Clin Neuropharmacol 2012; 35 : 1–5.
7. Goetz CC. The Unified Parkinson’s Disease Rating Scale (UPDRS): status and recommendations. Mov Disord 2003; 18(7): 738–750.
8. Goetz CG, Fahn S, Martinez-Martinin P, et al. Movement Disorder Society – sponsored revision of the unified Parkinson’s disease rating scale (MDS-UPDRS): process, format and clinimetric testing plan. Mov Disord 2007; 22 : 41–47.
9. Goetz CG, Nutt JG, Stebbins GT. The unified dyskinesias rating scale: presentation and clinimetric profile. Mov Disord 2008; 23(16): 2398–2403.
10. Goetz CG, Stebbins GT, Shale HM, et al. Utility of an objective dyskinesia rating scale for Parkinson’s disease: inter - and intrarater reliability assessment. Mov Disord 1994; 9(4): 390–394.
11. Guy W. ECDEU assessment manual for psychopharmacology. Washington, DC: Governement Printing Office 1976.
12. Hagell P, Widner H. Clinical rating of dyskinesias in Parkinson’s disease: utility and reliability of a new rating scale. Mov Disord 1999; 14(3): 448–455.
13. Hauser RA, Friedlander J, Zesiewicz TA, et al. A home diary to assess functional status in patients with Parkinsonś disease with motor fluctuations and dyskinesia. Neuropharmacol 2000; 23(2): 75–81.
14. Hobson JP, Edwards NI, Meara RJ. The Parkinson’s disease Activities of Daily Living Scale: a new simple and brief subjective measure of disability in Parkinson’s disease. Clin Rehabil 2001; 15(3): 241–246.
15. Hoehn MM, Yahr MD. Parkinsonism: onset, progression and mortality. Neurology 1967; 17(5): 427–442.
16. Katzenschlager R, Schrag A, Evans A, et al. Quantifying the impact of dyskinesias in PD. The PDYS-26: a patient-based outcome measure. Neurology 2007; 69(6): 555–563.
17. Marinus J, Visser M, Stiggelbout AM, et al. Activity-based diary for Parkinson‘s disease. Clin Neuropharmacol 2002; 25(1): 43–50.
18. Martinez-Martin P, Tolosa E, Hernandez B, et al. Validation of the „QUICK“ questionnaire – A tool for diagnosis of „wearing-off“ in patients with Parkinson’s disease. Mov Disord 2008; 23(6): 830–836.
19. Parkinson Study Group. Evaluation of dyskinesias in a pilot, randomized, placebo-controlled trial of remacemide in advanced Parkinson disease. Arch Neurol 2001; 58(10): 1660–1668.
20. Ramaker C, Marinus J, Stiggelbout AM, van Hilten BJ. Systematic evaluation of rating scales for impairment and disability in Parkinson´s disease. Mov Disord 2002; 17(5): 867–876.
21. Reimer J, Grabowski M, Lindvall O, Hagell P. Use and interpretation of on/off diaries in Parkinson’s disease. J Neurol Neurosurg Psychiatry 2004; 75(3): 396–400.
22. Schwab RS, England AC. Projection technique for evaluating surgery in Parkinson’s disease. In: Gillingham FJ, Donaldson IML. (eds.) Third symposium on Parkinson’s disease. Edinburgh: E. and S. Livingstone 1969; 152–157.
23. von Campenhausen S, Bornschein B, Wick R, et al. Prevalence and incidence of Parkinson’s disease in Europe. Eur Neuropsychopharmacol 2005; 15(4): 473–490.
24. Stacy M, Hauser, R. Development of a patient questionnaire to facilitate recognition of motor and non-motor wearing-off in Parkinson’s disease. J Neural Transm 2007; 114(2): 211–217.
25. Stacy MA, Murphy JM, Greeley DR, et al. The sensitivity and specificity of the 9-item Wearing-off Questionnaire. Parkinsonism Relat Disord 2008; 14(3): 205–212.
26. Webster D. Critical analysis of the disability of Parkinson’s disease. Mod Treat 1968; 5(2): 393–397.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2018 Issue 3-
All articles in this issue
- Předoperační anemie: výskyt, příčiny, následky, diagnostika a léčba
- Základy respirační fyzioterapie pro praktické lékaře
- Názory občanů České republiky na vybrané aspekty činnosti všeobecných praktických lékařů – 2017
- Přehled dotazníků a škál hodnotících motorické příznaky pacientů s Parkinsonovou nemocí
- Optoelektronické skenování jako nástroj pro měření antropometrických rozměrů dolních končetin
- Zdravotní gramotnost a potřeba komunitních center zdraví
- Liečba protilátkových imunodeficiencií subkutánnymi imunoglobulínmi
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Předoperační anemie: výskyt, příčiny, následky, diagnostika a léčba
- Přehled dotazníků a škál hodnotících motorické příznaky pacientů s Parkinsonovou nemocí
- Liečba protilátkových imunodeficiencií subkutánnymi imunoglobulínmi
- Základy respirační fyzioterapie pro praktické lékaře
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

