-
Medical journals
- Career
Srdeční selhání se zachovanou ejekční frakcí levé komory
: V. Melenovský
: Klinika kardiologie ; Přednosta: prof. MUDr. Josef Kautzner, DrSc. ; Institut klinické a experimentální medicíny, Praha
: Prakt. Lék. 2010; 90(4): 235-238
: Of different specialties
Epidemiologické studie posledních dvou desetiletí ukazují, že až polovina pacientů s definitivní diagnózou srdečního selhání nemá významně sníženou ejekční frakci levé komory. Výskyt srdečního selhání se zachovanou systolickou funkcí v populaci stoupá a jeho dlouhodobá prognóza je podobně nepříznivá jako u systolické dysfunkce. Nejčastěji se s tímto onemocněním setkáváme u starších pacientů, častěji u žen, s dlouholetou anamnézou arteriální hypertenze a/nebo diabetu. Přestože se jedná o časté onemocnění, patofyziologie není zcela objasněna. Na vzniku obtíží se podílejí poruchy diastolického plnění levé komory, významnou roli však hrají i extraventrikulární mechanismy, jako je snížená kontraktilní rezerva srdce, zvýšená tuhost arteriálního řečiště, porušená mechanická funkce levé síně a abnormality autonomního nervového systému.
V dlouhodobé léčbě jsou doporučována diuretika, omezení přísunu soli, léčba rizikových faktorů onemocnění a především důsledná kontrola arteriální hypertenze. V protikladu k srdečnímu selhání při systolické dysfunkci, žádná z dosud provedených randomizovaných studií neprokázala příznivý efekt testovaných farmakoterapeutických postupů na mortalitu, a tak studium touho typu srdečního selhání představuje jednu z aktuálních priorit kardiovaskulárního výzkumu.Klíčová slova:
srdeční selhání, ejekční frakce, diastolická dysfunkce, arteriální hypertenze, hypertrofie levé komory.Epidemiologie a patofyziologie
Epidemiologické studie posledních dvou desetiletí ukazují, že až polovina pacientů s definitivní diagnózou srdečního selhání nemá významně sníženou systolickou funkci levé komory, alespoň jak lze usuzovat z hodnot klidové ejekční frakce. Registry jako je EuroHeart Failure Survey (1) nebo americký ADHERE (2), shodně potvrzují, že 46 %, respektive 51 % pacientů hospitalizovaných s definitivní diagnózou srdečního selhání nemá systolickou dysfunkci (EF<40 %). Nemocniční mortalita pacientů se srdečním selháním se zachovanou ejekční frakcí (SS-ZEF) je sice nižší, délka hospitalizace a cena za péči je však stejná jako u nemocných se systolickou dysfunkcí (3).
Po epizodě hospitalizace je pětiletá mortalita podobně vysoká (65 % vs. 68 %) jako u osob se systolickým srdečním selháním – rozhodně se nejedná o benignější formu srdečního selhání (4).
Retrospektivní analýzy hospitalizací na Mayo Clinic ukázaly, že výskyt tohoto typu srdečního selhání stoupá, a to jak absolutně, tak relativně ve srovnání s výskytem systolického selhání. Zatímco prognóza pacientů se systolickou dysfunkcí se postupně zlepšuje v důsledku zavedení účinných postupů léčby, mortalita pacientů s SS-ZEF se za posledních 15 let nezměnila (4). Protože celková prevalence manifestního srdečního selhání v evropské populaci je odhadována na 2 % (5), tento druh srdečního selhání může mít v ČR až 70–100 000 osob.
V kardiocentrech a univerzitních nemocnicích se s SS-ZEF setkáváme relativně méně často, protože převážná část těchto pacientů je hospitalizována v regionálních zařízeních a je léčena častěji internistou či geriatrem než kardiologem. V ambulantní sféře se s tímto onemocněním též setkávají pneumologové či specialisté na léčbu plicní hypertenze, vyšetřující příčinu dušnosti u pacientů bez jednoznačně snížené systolické funkce LK.
V širším slova smyslu smyslu se můžeme s nálezem podobným SS-ZEF setkat u
- významných chlopenních vad,
- tachyarytmie,
- hypertrofické kardiomyopatie,
- infiltrativního postižení myokardu,
- onemocnění perikardu,
- difuzní koronární ischémii, či
- při závažné plicní hypertenzi (Obr. 1)
1. Diferenciální diagnóza srdečního selhání se zachovanou ejekční frakcí. 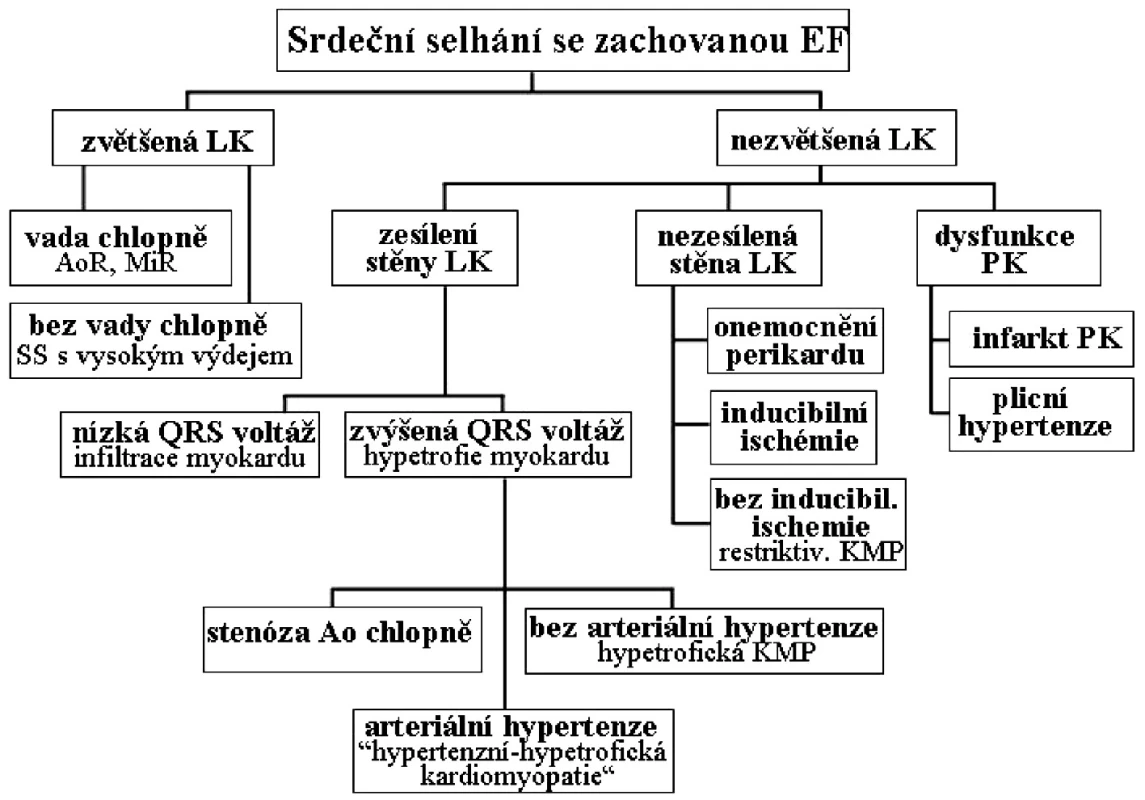
(Upraveno podle Guidlines of Heart Failure Society of America) (9) a tyto kategorie je nutno zvážit v diferenciální diagnóze. Avšak zdaleka nejčastěji se s tímto syndromem setkáváme v „klasické“ podobě u starších pacientů, častěji u žen, s dlouholetou anamnézou arteriální hypertenze a/nebo diabetu, kteří mají koncentrickou remodelaci či hypertrofii levé komory, zvětšenou levou síň a abnormality diastolického plnění LK.
Přestože se jedná o častou diagnózu, patofyziologie tohoto onemocnění není zcela objasněna. Často bývá přítomna porucha diastolického plnění levé komory – zpomalená časná diastolická relaxace či zvýšená pasivní tuhost komory (6). Porucha diastolické funkce levé komory však není zcela unikátní a patognomický rys SS-ZEF, protože jistý stupeň diastolických abnormalit lze najít u většiny starších hypertoniků, kteří jsou zcela bez známek srdečního selhání (7). Podobně i echokardiografický nález střední až závažné diastolické dysfunkce při dopplerovské echokardiografii není synonymem SS-ZEF, protože frekvence výskytu toho nálezu v populaci je asi o řád vyšší než SS-ZEF (8). Proto je jistý odklon od termínu „diastolické srdeční selhání“, který implikuje znalost mechanismu, ve prospěch popisného termínu “srdeční selhání se zachovanou ejekční frakcí“ (9).
K rozvoji klinických obtíží dochází zřejmě v důsledku několika kooperujících, částečně nezávislých faktorů (tab. 1), které přispívají k poruchám diastoly a jejichž podíl je u jednotlivých pacientů různý. Normální EF je velmi hrubý ukazatel kontraktilního stavu a nevylučuje přítomnost subklinické systolické dysfunkce (10), která se manifestuje sníženou kontraktilní rezervou levé komory během zátěže (11). Významnou roli při vzniku projevů onemocnění hrají extraventrikulární mechanismy, jako je zvýšená tuhost aorty (7), abnormální autonomní kardiovaskulární odpověď na zátěž se sníženou chronotropní a vazodilatační rezervou (11) či snížená kontraktilita levé síně (12) (tab. 1).
1. Mechanismy odpovědné za rozvoj symptomů srdečního selhání při zachované EF 
Výskyt SS-ZEF je velmi silně vázán na vysoký věk a izolovanou systolickou hypertenzi, v jejímž vzniku hraje klíčovou úlohu ztráta poddajnosti aorty. Ke zvýšení cévní tuhosti dochází v důsledku věkem podmíněné degradace elastinu stěny velkých cév a dále při diabetu či onemocnění ledvin (13), které též vytváří predispozici k srdečnímu selhání. Důsledkem cévních změn je vzestup pulzatilního zatížení srdce, následné zesílení stěn levé komory (koncentrická remodelace), fibróza myokardu a dynamická porucha relaxace (14). Zvýšená tuhost cévního řečiště, spolu s relativně zachovanou kontraktilitou LK vede k tomu, že tito pacienti mají zvýšenou závislost systémového krevního tlaku na aktuální náplni levé komory (15).
Levostranná insuficience má často paroxysmální charakter, kdy vzestup krevního tlaku vede k rychle vznikajícímu plicnímu edému v důsledku přesunu tekutiny do nejvíce poddajného části cévního řečiště – do plicní cirkulace. Plicní kongesce většinou dobře reaguje na vazodilatační a diuretickou léčbu. Příliš výrazný pokles plnícího tlaku levé komory vede naopak snadno k hypotenzi a k snížení perfúze orgánů, především ledvin.
Diagnóza
U pacientů, jejichž symptomy vedou k hospitalizaci pro kardiální dekompenzaci, je diagnóza SS-ZEF poměrně jednoduchá a vyžaduje jen vyloučení jiných patologických stavů (obr. 1). Situace je složitější u pacientů s mírnějšími obtížemi, kdy projevy onemocnění nejsou zcela jednoznačné a lze je snadno zaměnit s následkem obezity, ztráty kondice či nekardiovaskulárního onemocnění.
K diagnóze SS-ZEF lze použít doporučení Evropské společnosti pro srdeční selhání (HFA) (obr. 2) (16). Pro diagnózu SS-ZEF svědčí přítomnost typických známek a symptomů srdečního selhání (námahová dušnost, otoky končetin, intolerance námahy) v kombinaci s nálezem zachované ejekční frakce LK zachycené zobrazovací metodou (9) a s neinvazivním nálezem zvýšeného plnícího tlaku levé komory, odhadovaného z poměru E a E’ rychlostí, to znamená poměru časné diastolické rychlosti transmitrálního průtoku k časné diastolické rychlosti mitrálního annulu (17).
2. Doporučená diagnostická kritéria pro srdeční selhání se zachovanou EF. 
(Upraveno podle doporučení Evropské společnosti pro srdeční selhání-HFA ESC) (16) Pokud poměr E/E’ dosahuje hraničních hodnot (8–15), pak k diagnóze SS-ZEF přispívá
- nález zvýšeného objemu levé síně (12),
- nález hypertrofie levé komory,
- fibrilace síní, nebo
- zvýšené hladiny BNP (18), které však často nedosahuje hodnot pozorovaných u systolické dysfunkce.
Nutno však zmínit, že tato diagnostická kritéria dosud nebyla dosud prospektivně validována na velkém souboru pacientů a interpretace poměru E/E’může být ovlivněna řadou faktorů, například přítomností mitrální regurgitace.
Poměrně spolehlivým markerem přítomnosti onemocnění ze zdá být zvětšení objemu levé síně (12). V důsledku asymetrické expanze levé síně je výpovědní hodnota levosíňových objemů vyšší než průměr levé síně měřený v parasternální projekci. Až 80 % pacientů s SS-ZEF má plicní hypertenzi definovanou jako echokardiograficky – odhadovaný systolický tlak v plicnici > 35 mm Hg (19), na kterém se podílí jednak přenos zvýšeného plnícího tlaku z plicního řečiště, ale i zvýšení odporu v plicním řečišti. K odlišení primární plicní hypertenze a plicní hypertenze doprovázející SS-ZEF je u některých pacientů nezbytné provést pravostrannou katetrizaci.
Terapie
Léčba akutně dekompenzovaného SS-ZEF s městnáním v plicním řečišti spočívá v udržení adekvátní oxygenace, diuretické léčbě a především ve vazodilatační léčbě. Základem léčby je podání vazodilatancií jako je isosorbid-dinitrát s cílem snížení systolického tlaku o 30 mm Hg během prvních patnácti minut a s návratem do dlouhodobých hodnot systémového krevního tlaku během 6 hodin od zahájení léčby (20). Dále podáváme kličková diuretika (20), která je nutné dávkovat s jistou opatrností a je vhodné se vyvarovat paušálního podávání vysokých dávek. Charakter plicního městnání je totiž redistribuční, a kontrakce intravaskulárního objemu po nadměrné diuréze může vést k hypotenzi se zhoršením renální a orgánové perfúze. K udržení adekvátní saturace arteriální krve nad 95 % lze použít obličejovou masku. V případě nedostatečné oxygenace či eliminace CO2 je nutné zahájit plicní ventilaci.
Jako perspektivní nový přístup se jeví neinvazivní ventilace pomocí těsné obličejové masky a ventilátoru s použitím režimu CPAP (continuous positive pressure) či IPPV (intermitent positive pressure ventilation). Při těchto postupech není nutná tracheální intubace, což snižuje výskyt komplikací a zkracuje pobyt na intenzivní péči. Předpokladem tohoto přístupu je však dobrá spolupráce pacienta a schopnost udržet volné dýchací cesty.
Doporučení pro dlouhodobou léčbu nemocných s SS-ZEF jsou postavena převážně na zkušenostech, neboť u tohoto typu srdečního selhání bylo provedeno dosud jen minimum randomizovaných mortalitních studií (21), zvláště ve srovnání se systolickým srdečním selháním.
Základem léčby jsou diuretika, které přinášejí symptomatický benefit a snižují i riziko primomanifestace SS-ZEF (22). Ke kontrole retence tekutin je vhodná dieta s omezením soli. Dále je doporučována důsledná kontrola hypertenze, s upřednostněním léků s vyšším potenciálem navození regrese koncentrické hypertrofie LK jako jsou ACE inhibitory či blokátory AT receptoru (23). Nicméně velké studie, které testovaly tyto dvě lékové skupiny u SS-ZEF dopadly nepřesvědčivě.
Studie CHARM-preserved studovala efekt candesartanu u 3 023 pacientů se srdečním selháním NYHA II-IV a EF LK > 40 % sledovaných po dobu 3,5 roku. Výsledkem studie bylo snížení kardiovaskulárních úmrtí a rehospitalizací u aktivně léčené skupiny o 11 %, což nebylo statisticky významné, hladina významnosti byla dosažena pouze pro redukci rehospitalizací (24).
Studie PEP-CHF (perindopril for elderly people with chronic heart failure) sledovala efekt podávání perindoprilu u 850 pacientů s chronickým srdečním selháním, zachovalou systolickou funkcí a věkem nad 70 let (25). Primární endpoint – úmrtí či neplánovaná hospitalizace pro srdeční selhání, nebyl na konci studie významně ovlivněn (p=0,55), avšak v prvním roce léčby byl v aktivně léčené skupině dokumentován pokles hospitalizací a zlepšení symptomů srdečního selhání. Obě tyto studie byly zatíženy buď nedostatečnou statistickou sílou (PEP-CHF), či zahrnutím málo symptomatických pacientů se spornou diagnózou SS-ZEF a nízkým zastoupením žen s hypertenzí (CHARM-preserved).
Tyto nedostatky neměla nedávno ukončená studie I-PRESERVE. Do této studie bylo zařazeno 4 128 SS-ZEF pacientů v NYHA II-IV třídě, kteří byli léčeni irbesartanem či placebem přidaným k běžné medikaci. Během sledování po dobu 50 měsíců nebyl zjištěn rozdíl ve výskytu úmrtí či kardiovaskulární hospitalizace (p=0,35). Dosud probíhají intenzivní debaty jak interpretovat nedostatečný efekt léků inhibujících renin-angiotensinový systém na mortalitu tohoto onemocnění. Příčinou může být vysoký podíl nekardiovaskulárních úmrtí u polymorbidních pacientů, který komplikuje design mortalitních studií. Vysvětlením ale může být i to, že SS-ZEF je svým mechanismem principiálně jiné onemocnění, a léky které pomáhají u systolické dysfunkce, nemusí fungovat u tohoto typu srdečního selhání.
V probíhajícím projektu TOPCAT, který je sponzorován americkým NIH, je sledován efekt dlouhodobého podávání spironolaktonu u 4 500 pacientů; výsledky této studie lze ale očekávat až v roce 2011. Studie DIG (Digitalis Investigators Group) ukázala, že u pacientů se srdečním selháním, sinusovým rytmem a ejekční frakcí nad 45 %, digoxin nemá významný efekt na mortalitu či celkovou kardiovaskulární morbiditu (26). O vlivu betablokátorů na prognózu u SS-ZEF existuje jen minimum informací a dosud nebyla provedena klinická studie zaměřená na tuto skupinu pacientů.
Studie SENIORS sledovala efekt nebivovolu u 2 128 pacientů s věkem > 70 let a srdečním selháním bez ohledu na EF LK. Příznivý efekt na primární endpoint (mortalita a kardiovaskulární hospitalizace) byl pozorován jak v podskupině s nízkou (<35 %), tak i relativně zachovanou (>35 %) ejekční frakcí (27). Na druhou stranu betablokátory můžou zhoršovat nedostatečnou odpověď tepové frekvence na zátěž, která je u těchto pacientů častá – až 20 % z nich má těžkou chronotropní inkompetenci, která přispívá k intoleranci zátěže (11). Na základě tohoto poznatku byla zahájena studie RESET, zjišťující zda obnovení chronotropní kompetence pomocí adaptivní stimulace síní kardiostimulátorem může zlepšit projevy SS-ZEF.
Dalším novým, již klinicky testovaným terapeutickým přístupem k léčbě SS-ZEF, je inhibice fosfodiesterázy 5, která se ve zvýšené míře nachází jak v plicní tkáni, tak i v myokardu pacientů s hypertrofií srdce či srdečním selháním. Právě probíhající NIH-sponzorovaná studie RELAX sleduje dlouhodobý efekt podávání sildenafilu na symptomy srdečního selhání a toleranci zátěže.
K zavedení nových přístupů k léčbě akutních i chronických forem SS-ZEF je nutno zpřesnit diagnostiku, vyvinout klinické či biochemické markery dovolující přesnější identifikaci této jednotky a dále lépe pochopit mechanismy odpovědné za manifestaci onemocnění, které budou cílem specifičtější, více kauzální léčby. Léky příznivě ovlivňující tuhost velkých tepen či léky navozující regresi hypertrofie myokardu nezávisle na ovlivnění systémového tlaku představují v tomto směru nejslibnější kandidáty (28). S ohledem na epidemicky narůstající počet pacientů s tímto typem srdečního selhání a absenci léků ovlivňujících prognózu onemocnění, je zřejmé že SS-ZEF představuje jednu z hlavních priorit kardiovaskulárního výzkumu.
Práce byla podpořena grantem IGA MZ ČR: NS10497-3/2009
MUDr. Vojtěch Melenovský, CSc.
Klinika kardiologie
Institut klinické a experimentální medicíny
Vídeňská 1958/9,
140 21 Praha 4
E-mail: vojtech.melenovsky@ikem.cz
Sources
1. Lenzen, M.J., Scholte op Reimer, W.J., Boersma, E. et al. Differences between patients with a preserved and a depressed left ventricular function: a report from the EuroHeart Failure Survey. Eur. Heart J. 2004, 25(14), p. 1214-1220.
2. Yancy, C.W., Lopatin, M., Stevenson, L.W. et al. Clinical presentation, management, and in-hospital outcomes of patients admitted with acute decompensated heart failure with preserved systolic function: a report from the Acute Decompensated Heart Failure National Registry (ADHERE) Database. J. Am. Coll. Cardiol. 2006, 47(1), p. 76-84.
3. Liao, L., Jollis, J.G., Anstrom, K.J. et al. Costs for heart failure with normal vs. reduced ejection fraction. Arch. Intern. Med. 2006, 166(1), p. 112-118.
4. Owan, T.E., Hodge, D.O., Herges, R.M. et al. Trends in prevalence and outcome of heart failure with preserved ejection fraction. N. Engl. J. Med. 2006, 355(3), p. 251-259.
5. Swedberg, K., Cleland, J., Dargie, H. et al. Guidelines for the diagnosis and treatment of chronic heart failure: executive summary (update 2005): The Task Force for the Diagnosis and Treatment of Chronic Heart Failure of the European Society of Cardiology. Eur. Heart J. 2005, 26(11), p. 1115-1140.
6. Zile, M.R., Baicu, C.F., Gaasch, W.H. Diastolic heart failure—abnormalities in active relaxation and passive stiffness of the left ventricle. N. Engl. J. Med. 2004, 350(19), p. 1953-1959.
7. Kawaguchi, M., Hay, I., Fetics, B. et al. Combined ventricular systolic and arterial stiffening in patients with heart failure and preserved ejection fraction: implications for systolic and diastolic reserve limitations. Circulation 2003, 107(5), p. 714-720.
8. Redfield, M.M., Jacobsen, S.J., Burnett, J.C. Jr. et al. Burden of systolic and diastolic ventricular dysfunction in the community: appreciating the scope of the heart failure epidemic. JAMA 2003, 289(2), p. 194-202.
9. Heart Failure Society Of America. Evaluation and management of patients with heart failure and preserved left ventricular ejection fraction. J. Card. Fail. 2006, 12(1), e80-e85.
10. Yu, C.M., Lin, H., Yang, H. et al. Progression of systolic abnormalities in patients with “isolated” diastolic heart failure and diastolic dysfunction. Circulation 2002, 105(10), p. 1195-1201.
11. Borlaug, B.A., Melenovsky, V., Russell, S.D. et al. Impaired chronotropic and vasodilator reserves limit exercise capacity in patients with heart failure and a preserved ejection fraction. Circulation 2006, 114(20), p. 2138-2147.
12. Melenovsky, V., Borlaug, B.A., Rosen, B. et al. Cardiovascular features of heart failure with preserved ejection fraction versus nonfailing hypertensive left ventricular hypertrophy in the urban Baltimore community: the role of atrial remodeling/dysfunction. J. Am. Coll. Cardiol. 2007, 49(2), p. 198-207.
13. Zieman, S.J., Melenovsky, V., Kass, D.A. Mechanisms, pathophysiology, and therapy of arterial stiffness. Arterioscler. Thromb. Vasc. Biol. 2005, 25(5), p. 932-943.
14. Leite-Moreira, A.F., Correia-Pinto, J., Gillebert, T.C. Afterload induced changes in myocardial relaxation: a mechanism for diastolic dysfunction. Cardiovasc. Res. 1999, 43(2), p. 344-353.
15. Chen, CH., Nakayama, M., Nevo, E. et al. Coupled systolic-ventricular and vascular stiffening with age: implications for pressure regulation and cardiac reserve in the elderly. J. Am. Coll. Cardiol. 1998, 32(5), p. 1221-1227.
16. Paulus, W.J., Tschope, C., Sanderson, J.E. et al. How to diagnose diastolic heart failure: a consensus statement on the diagnosis of heart failure with normal left ventricular ejection fraction by the Heart Failure and Echocardiography Associations of the European Society of Cardiology. Eur. Heart. J. 2007, 28(20), p. 2539-2550.
17. Bruch, C., Grude, M., Muller, J. et al. Usefulness of tissue Doppler imaging for estimation of left ventricular filling pressures in patients with systolic and diastolic heart failure. Am. J. Cardiol. 2005, 95(7), p. 892-895.
18. Maisel, A.S., McCord, J., Nowak, R.M. et al. Bedside B-Type natriuretic peptide in the emergency diagnosis of heart failure with reduced or preserved ejection fraction. Results from the Breathing Not Properly Multinational Study. J. Am. Coll. Cardiol. 2003, 41(11), p. 2010-2017.
19. Lam, C.S., Roger, V.L., Rodeheffer, R.J. et al. Pulmonary hypertension in heart failure with preserved ejection fraction: a community-based study. J. Am. Coll. Cardiol. 2009, 53(13), p. 1119-1126.
20. Nieminen, M.S., Bohm, M., Cowie, M.R. et al. Executive summary of the guidelines on the diagnosis and treatment of acute heart failure: the Task Force on Acute Heart Failure of the European Society of Cardiology. Eur. Heart J. 2005, 26(4), p. 384-416.
21. Špinar, J., Hradec, J., Meluzín, J. Doporučení pro diagnostiku a léčbu chronického srdečního selhání ČKS 2006. Cor. Vasa 2007, 49(1), K5-K34.
22. Davis, B.R., Kostis, J.B., Simpson, L.M. et al. Heart failure with preserved and reduced left ventricular ejection fraction in the antihypertensive and lipid-lowering treatment to prevent heart attack trial. Circulation 2008, 118(22), p. 2259-2267.
23. Devereux, R.B., Dahlof, B., Gerdts, E. et al. Regression of hypertensive left ventricular hypertrophy by losartan compared with atenolol: the Losartan Intervention for Endpoint Reduction in Hypertension (LIFE) trial. Circulation 2004, 110(11), p. 1456-1462.
24. Yusuf, S., Pfeffer, M.A., Swedberg, K. et al. Effects of candesartan in patients with chronic heart failure and preserved left-ventricular ejection fraction: the CHARM-Preserved Trial. Lancet 2003, 362(9386), p. 777-781.
25. Cleland, J.G., Tendera, M., Adamus, J. et al. The perindopril in elderly people with chronic heart failure (PEP-CHF) study. Eur. Heart J, 2006, 27(19), p. 2338-2345.
26. The Digitalis Investigation Group. The effect of digoxin on mortality and morbidity in patients with heart failure. N. Engl. J. Med. 1997, 336(8), p. 525-533.
27. Flather, M.D., Shibata, M.C., Coats, A.J. et al. Randomized trial to determine the effect of nebivolol on mortality and cardiovascular hospital admission in elderly patients with heart failure (SENIORS). Eur. Heart J. 2005, 26(3), p. 215-225.
28. Kass, D.A., Bronzwaer, J.G., Paulus, W.J. What mechanisms underlie diastolic dysfunction in heart failure? Circ. Res. 2004, 94(12), p. 1533-1542.
29. Hundley, W.G., Kitzman, D.W., Morgan, T.M. et al. Cardiac cycle-dependent changes in aortic area and distensibility are reduced in older patients with isolated diastolic heart failure and correlate with exercise intolerance. J. Am. Coll. Cardiol. 2001, 38(3), p. 796-802.
30. Arques, S., Ambrosi, P., Gelisse, R. et al. Hypoalbuminemia in elderly patients with acute diastolic heart failure. J. Am. Coll. Cardiol. 2003, 42(4), p. 712-716.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2010 Issue 4-
All articles in this issue
-
Evolution and evolutionary theory for physicians.
IV. Life on Earth - Urologic care of patients after spinal cord injury
- What should a general practitioner know about drinking water? Part I.: Water in health promotion.
- Myocarditis
- Occurrence of polycystic ovary syndrome and hyperadrogenemia in women with type 1 diabetes mellitus
- The prevalence of asymptomatic individuals with high risk of cardiovascular disease in the Czech population and their adherence to primary prevention targets
- Heart failure with preserved systolic function of the left ventricle
- Development of spiritual care in the University Hospital Motol
- Prevention of lung cancer due to radon
- Subcutaneous traumatic rupture of the tibialis anterior tendon
- All of the facts belong only to the problem, not to its solution: relationship between science, ethics and religion
-
Evolution and evolutionary theory for physicians.
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Myocarditis
- Subcutaneous traumatic rupture of the tibialis anterior tendon
- Occurrence of polycystic ovary syndrome and hyperadrogenemia in women with type 1 diabetes mellitus
- Heart failure with preserved systolic function of the left ventricle
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

