-
Medical journals
- Career
Intrapankreaticky uložená akcesorní slezina jako raritní solidní léze pankreatu
Authors: Krlínová I. 1; Shon F. 1; Štiková Z. 2; Maxa V. 3; Mareš L. 4; Šabata L. 3
Authors‘ workplace: Gastroenterologické oddělení, Nemocnice České Budějovice, a. s. 1; Patologické oddělení, Nemocnice České Budějovice, a. s. 2; Oddělení nukleární medicíny, Nemocnice České Budějovice, a. s. 3; Radiologické oddělení, Nemocnice České Budějovice, a. s. 4
Published in: Gastroent Hepatol 2018; 72(6): 522-526
Category:
doi: https://doi.org/10.14735/amgh2018522Overview
Incidence solidních lézí pankreatu (SLP) stoupá v důsledku narůstajícího počtu provedených zobrazovacích vyšetření. Často se jedná o náhodný nález. Zvláštním případem SLP je intrapankreaticky uložená akcesorní slezina (IPAS). Ve dvou kazuistikách prezentujeme benigní raritní nález IPAS. V prvním případě se jedná o 62letého muže s diagnózou časného karcinomu colon ascendens, kdy byla diagnóza IPAS stanovena postoperativně histopatologicky. Ve druhém případě prezentujeme 50letou ženu sledovanou pro cystu ledviny, kdy byla diagnóza IPAS stanovena pomocí zobrazovacích metod, konkrétně tomografické scintigrafie (Technetium-99m SPECT – single-photon emission computed tomography). Vzhledem k tomu, že se jedná o benigní lézi pankreatu, je snahou stanovit diagnózu pomocí zobrazovacích a specifických metod k detekci slezinné tkáně (SPECT značenými erytrocyty, kontrastní ultrasonografie s užitím mikrogranulí a magnetické rezonance rozšířené o SPIO (superparamagnetic iron oxide)). Další možností dovyšetření léze je endosonograficky navigovaná tenkojehlová biopsie. Stanovení diagnózy je však často obtížné. Značná část SLP je potenciálně maligní, a proto je většina případů indikována k chirurgické resekci. Diagnóza IPAS je poté zjištěna až z definitivního resekátu.
Klíčová slova:
intrapankreatická akcesorní slezina – diferenciální diagnóza – nádory slinivky břišní
Úvod
Incidence solidních lézí pankreatu (SLP), zjednodušeně klasifikované jako neoplastické a non-neoplastické, jsou v poslední době častějším nálezem v důsledku narůstajícího počtu provedených zobrazovacích vyšetření a díky jejich zlepšené kvalitě. Prioritou je v co nejkratší době určit, zda se jedná o ložisko indikované k operaci, ložisko neresekabilní nebo ložisko vhodné k sledování. Ve dvou kazuistikách prezentujeme pacienty se solidní lézí v kaudě pankreatu, u nichž byla diagnostikována intrapankreaticky uložená akcesorní slezina (IPAS).
Kazuistika č. 1
Pacient, 62 let, hypertonik, s anamnézou prodělané lehké akutní pankreatitidy v srpnu 2016, se dostavil v říjnu 2016 plánovaně ke koloskopii pro rektoragii v anamnéze. V colon ascendens byl snesen metodou endoskopické mukózní resekce plošný 20mm polyp typu O– IIa LST v NBI NICE II– III. Již během endoskopického výkonu bylo vyjádřeno podezření na malignizovaný polyp, které se histologicky potvrdilo. Mikroskopicky byl popsán plošný polyp 17 × 13 × 5 mm s těžkými dysplastickými změnami (high-grade dysplasia) s přechodem v invazivní hlenotvorný adenokarcinom. Maligní nádorové struktury se šířily do submukózy těsně na hranici tunica muscularis propria, pT1 (SM3). V rámci stagingu bylo doplněno CT břicha, na němž bylo popsáno solidní ložisko benigního vzhledu v kaudě pankreatu velikosti 14 mm. V laboratorních výsledcích byly onkomarkery (CEA, CA 72-4, CA 19-9, AFP) negativní. Doplnili jsme endosonografii pankreatu, v jejímž obraze se ložisko jevilo jako hyperechogenní 11 mm, mírně nehomogenní, dobře ohraničené. Nemělo infiltrativní charakter ani vzhled typického adenokarcinomu, vzhled byl nespecifický, nález byl suspektní z nefunkčního neuroendokrinního tumoru. S těmito doplněnými vyšetřeními byl pacient prezentován na chirurgicko-gastroenterologické indikační vizitě, kde byl doporučen operační výkon v jedné době. Byla provedena pravostranná hemikolektomie a resekce kaudy pankreatu. V resekátu tlustého střeva nebyly prokázány nádorové buňky, sedm lymfatických uzlin bylo bez průkazu metastáz. V resekátu pankreatu bylo paracentrálně ohraničené ložisko velikosti 11 × 7 × 10 mm. Mikroskopicky ložisko odpovídalo tkáni přídatné sleziny (obr. 1 a 2). Okolní tkáň slinivky byla normální stavby. Pooperační průběh byl komplikován infekcí močových cest, fluidotoraxem a podezřením na abscesové ložisko (febrilní stav a nárůst C reaktivního proteinu na 330 mg/ l). Byla zahájena antibiotická terapie a byla provedena CT navigovaná miniinvazivní drenáž tekutinové kolekce kaudy pankreatu. Následně byla provedena pro fluidotorax punkce pleurální dutiny vlevo pod ultrazvukovou (UZ) kontrolou. Stav pacienta se stabilizoval, následoval postupný ústup obtíží, byla obnovena pasáž, kontrolní laboratorní hodnoty byly uspokojivé. Celková pooperační doba hospitalizace čítala 44 dní.
Image 1. Histologický nález – intrapankreatická akcesorní slezina (IPAS) oddělená od pankreatické tkáně vazivovým pouzdrem (barvení hematoxylin-eozinem, zvětšení 50×). Fig. 1. Histopathological image – intrapancreatic accessory spleen (IPAS) separated by a fibrous capsule from the pancreatic tissue (Haematoxylin and eosin staining, magnifi cation 50×). 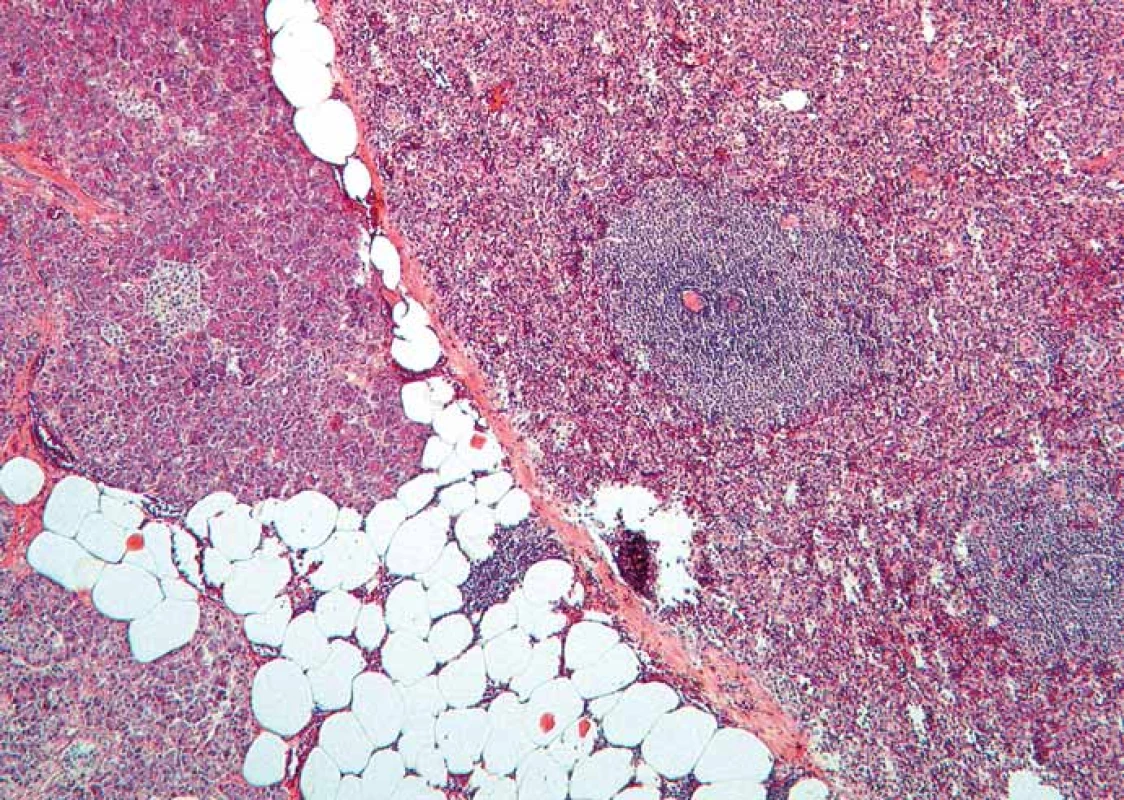
Image 2. Histologický nález – intrapankreatická akcesorní slezina (IPAS) oddělená od pankreatické tkáně vazivovým pouzdrem (barvení hematoxylin-eozinem, zvětšení 100×). Fig. 2. Histopathological image – intrapancreatic accessory spleen (IPAS) separated by a fibrous capsule from the pancreatic tissue (Haematoxylin and eosin staining, magnifi cation 100×). 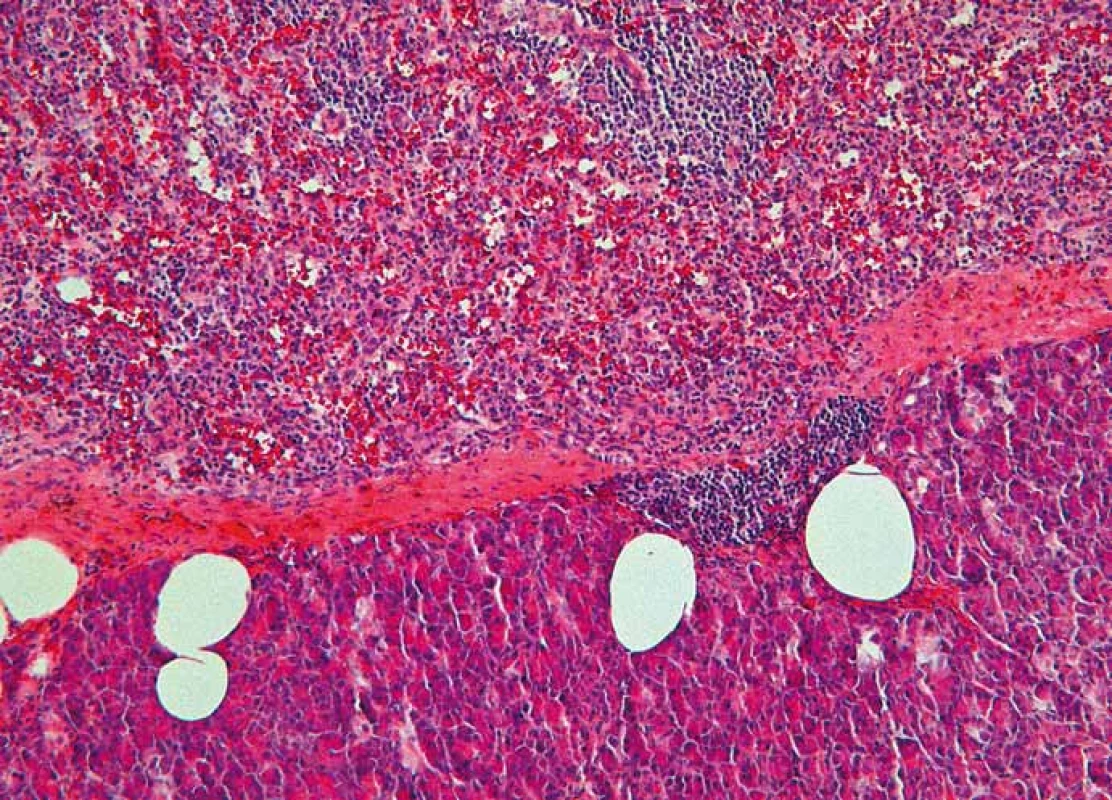
Kazuistika č. 2
Pacientka, 50 let, bez významných komorbidit, asymptomatická, bez zažívacích obtíží či bolestí břicha, s objektivním nálezem bez pozoruhodností, základní laboratoř bez nápadností, sledována urologem pro cystu levé ledviny a kalcifikaci ve střední části pravé ledviny. V rámci sledování bylo na CT břicha v březnu 2014 popsáno ložisko 19 × 32 mm v oblasti kaudy pankreatu, nejspíše benigní etiologie (obr. 3). V opakovaných laboratořích bylo CEA a CA 19-9 negativní, CA 72-4 19,1 IU/ ml v březnu 2014 a 8,5 IU/ ml v červnu 2015. Při kontrolním CT v lednu 2015 se jevilo ložisko jako stacionární. Magnetická rezonance (MR) břicha v květnu 2016 s nálezem oválné expanze 30 × 20 mm, bez patrné progrese růstu útvaru, okolní parenchym slinivky bez patologie, bez patologických zvětšených uzlin (obr. 4). Při endosonografii v červnu 2017 se jevil pankreas homogenní, v ocase pankreatu fazolovitý, mírně hypoechogenní útvar 33 × 20 mm, homogenní struktury s centrálním septem, stejného charakteru jako parenchym sleziny (obr. 5). Endoskopistou bylo vysloveno podezření na akcesorní slezinu a na doporučení byla doplněna Technetium-99m tomografická scintigrafie (SPECT – single-photon emission computed tomography; pro nedostupnost nebylo provedeno vyšetření SPECT značenými atenuovanými erytrocyty), na níž se potvrdilo, že ložisko pankreatu obsahuje slezinnou tkáň a s největší pravděpodobností se jedná o IPAS (obr. 6 a 7). Pacientka je nyní sledována ambulantním gastroenterologem.
Image 3. CT s nálezem intrapankreaticky uložené akcesorní sleziny (IPAS) (šipky). Fig. 3. A CT scan showing an intrapancreatic accessory spleen (IPAS) (arrows). 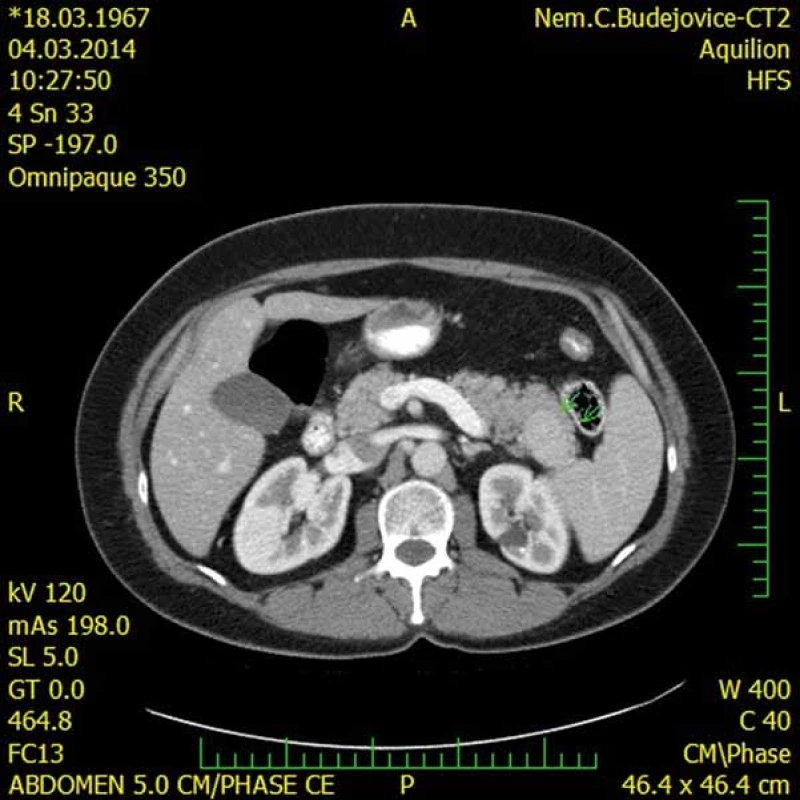
Image 4. Intrapankreaticky uložená akcesorní slezina (IPAS) na magnetické rezonanci (šipky). Fig. 4. Magnetic resonance imaging scan showing an intrapancreatic accessory spleen (IPAS) (arrows). 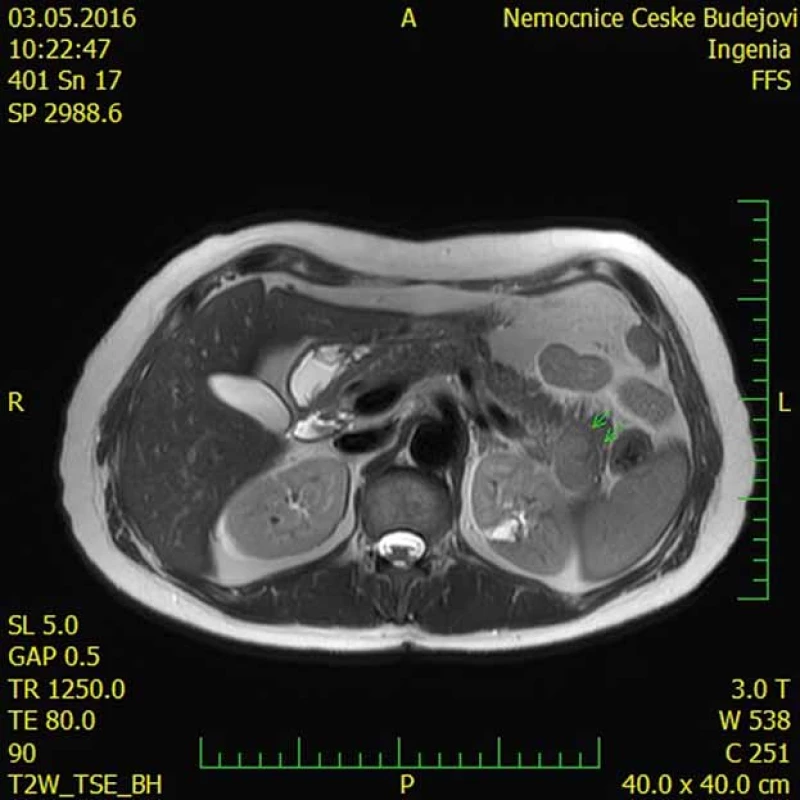
Image 5. Endoskopická ultrasonografi e pankreatu s obrazem intrapankreaticky uložené akcesorní sleziny (IPAS). Fig. 5. An endoscopic ultrasound scan showing an intrapancreatic accessory spleen (IPAS). 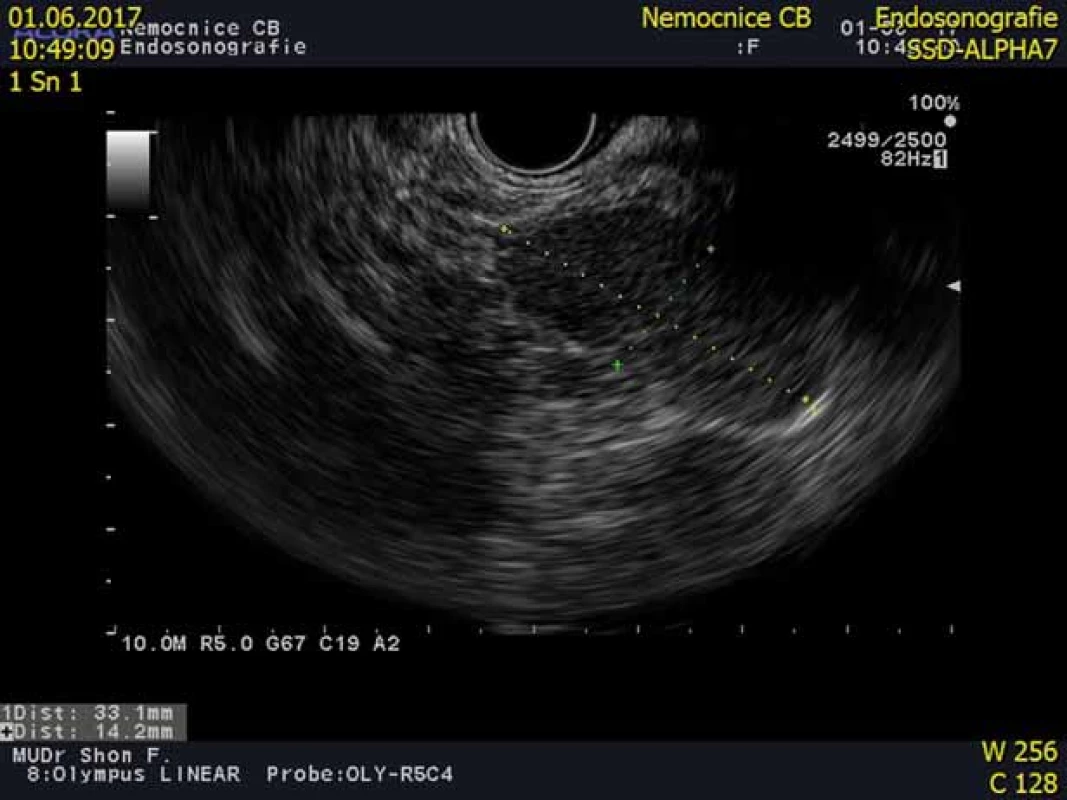
Image 6. Tc-99m SPECT ve 3 rovinách – transverzální, frontální a sagitální, intrapankreatická akcesorní slezina (IPAS). S – slezina, J – játra Fig. 6. Tc-99m SPECT in 3 projections – transversal, frontal and sagittal – showing an intrapancreatic accessory spleen (IPAS). S – spleen, J – liver 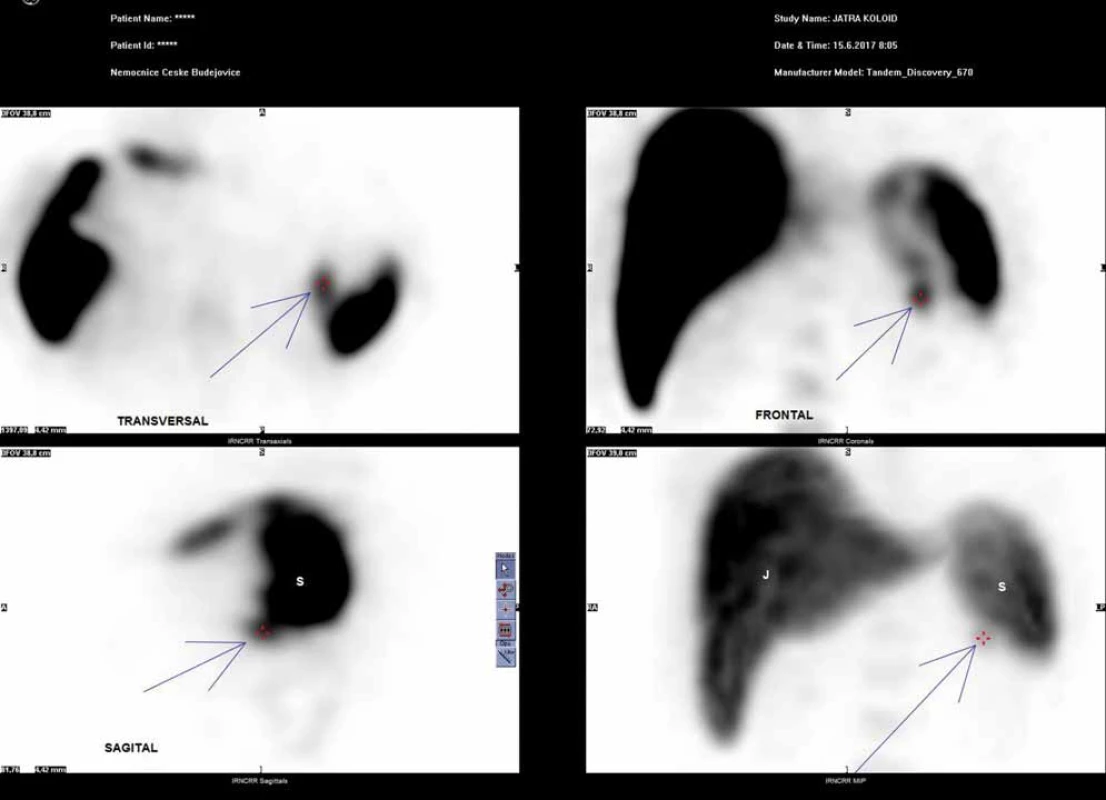
Image 7. Tc-99m SPECT 3D – intrapankreatická akcesorní slezina (IPAS). S – slezina, J – játra Fig. 7. Tc-99m SPECT 3D – intrapancreatic accessory spleen (IPAS). S – spleen, J – liver 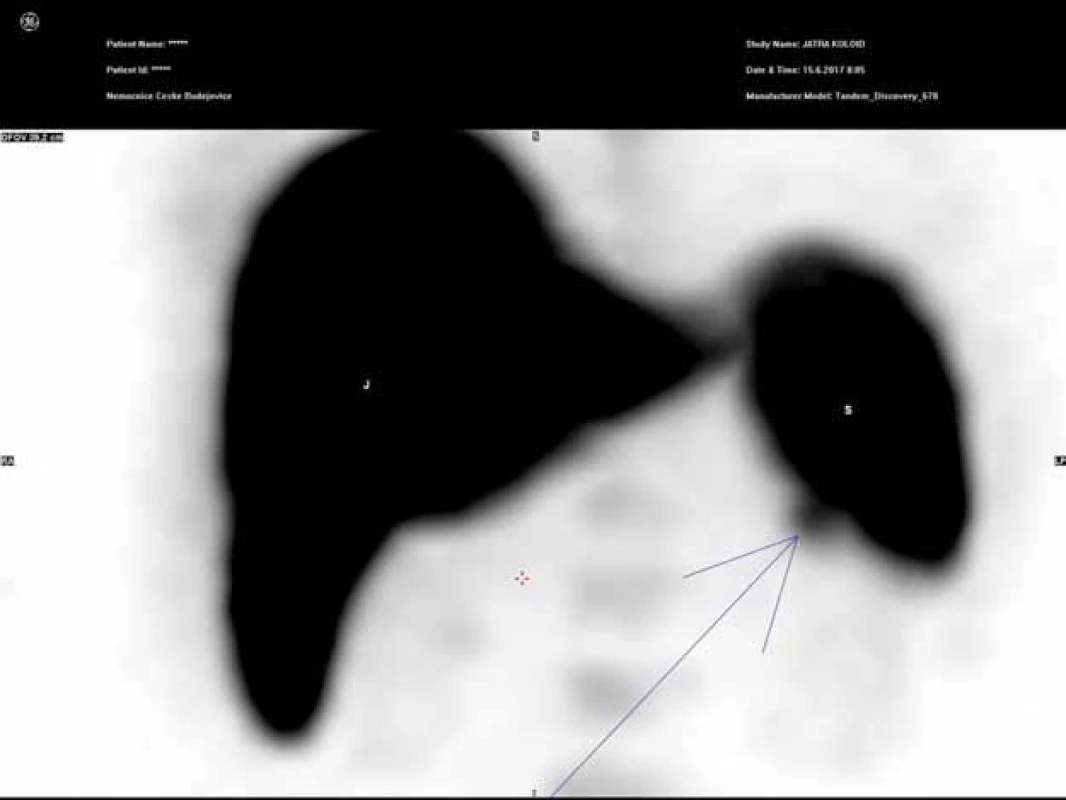
Diskuze
Asymptomatické léze pankreatu jsou diagnostikovány nejčastěji při sonografii a CT. Více než polovina náhodně nalezených pankreatických lézí má charakter solidního ložiska. Část resekčních výkonů na pankreatu je prováděna právě pro náhodně nalezená ložiska (v literatuře 10– 23 % všech resekcí), protože významná část z nich je potenciálně maligní (30– 35 %) nebo maligní (> 50 %) [1]. Benigních pankreatických lézí solidního charakteru je pouze 10– 20 %, nejčastěji se jedná o fokální chronickou pankreatitidu toxonutritivní etiologie [1]. Vzácně může být nalezena IPAS. IPAS je benigní léze související s embryologickou aberací vývoje sleziny. Nicméně se nejedná o tak raritní lézi, jak se původně předpokládalo. V Halpertově studii byla z 3 000 pitev přítomna akcesorní slezina ve 364 (12 %) případech, z toho v 61 (17 %) případech se jednalo o IPAS [2].
Kauda pankreatu je druhou nejčastější lokalizací akcesorní sleziny po oblasti hilu sleziny, ale vzhledem ke své malé velikosti nebývá prostřednictvím zobrazovacích metod často patrná. Vzhledem k tomu, že IPAS je benigní léze, která ve většině případů nevyžaduje žádnou léčbu, pokud není spojená s hematologickým onemocněním typu idiopatické trombocytopenické purpury, je žádoucí stanovit diagnózu pomocí zobrazovacích metod, tedy co nejméně invazivně. Bohužel, často bývá diagnóza IPAS stanovena až postoperativně histopatologicky [3– 6].
Zobrazovací metody typu CT, MR nebo UZ obvykle popisují IPAS jako okrouhlý či oválný vaskularizovaný útvar, který je dobře ohraničen od pankreatického parenchymu. Toto zobrazení je necharakteristické, zvláště u malých lézí, a je shodné i pro diagnózy neuroendokrinního tumoru, solidního pseudopapilárního tumoru či dobře vaskularizované metastázy (např. u tumoru ledviny) [7]. Jako vysoce specifická metoda (až 90 %) k detekci slezinné tkáně se jeví SPECT značenými atenuovanými erytrocyty (Tc-99m Heat-damaged Red Blood Cell Scintigraphy) [8,9]. Dalšími diagnostickými modalitami založenými na funkčním zobrazení slezinné tkáně jsou kontrastní UZ s užitím mikrogranulí Levovist (Schering, Berlin, Germany) [9,10] a MR po podání superparamagnetického kontrastního činidla (MR rozšířené o SPIO) [9,11]. Citlivost těchto metod však může být nízká, zejména pokud je nízké množství funkční splenické tkáně (< 1 cm) [12]. Endosonograficky navigovaná tenkojehlová biopsie (EUS-FNA – endoscopic ultrasound-fine needle aspiration) je další možností, jak diagnostikovat IPAS, a tím ušetřit pacienta zbytečné operace [13,14].
Závěr
Incidence SLP stoupá v důsledku narůstajícího počtu provedených zobrazovacích vyšetření. Prioritou je v co nejkratší době určit, zda se jedná o ložisko indikované k operaci nebo ložisko vhodné ke sledování. IPAS je raritní benigní léze kaudy pankreatu, na kterou bychom neměli v diferenciální diagnostice zapomínat. Při podezření na IPAS je v první řadě doporučeno užití specifické zobrazovací metody (SPECT značenými atenuovanými erytrocyty, MR rozšířená o SPIO či kontrastní UZ). Další možností dovyšetření léze je EUS-FNA. Navzdory přibývající dostupnosti diagnostických metod je diferenciální diagnostika obtížná. Nesmíme zapomínat, že značná část solidních lézí pankreatu je potenciálně maligní (30– 35 %) nebo maligní (> 50 %), a proto bývají pacienti ve většině případů řešeni chirurgicky a diagnóza IPAS bývá stanovena postoperativně histopatologicky. SPECT značenými atenuovanými erytrocyty nebo EUS-FNA může ušetřit některé pacienty zbytečné operace pankreatu.
Doručeno: 23. 4. 2018
Přijato: 12. 5. 2018
MU Dr. Ivana Krlínová
Gastroenterologické oddělení
Nemocnice České Budějovice, a. s.
B. Němcové 585/ 54
370 01 České Budějovice
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Sources
1. Trna J, Kala Z. Klinická pankreatologie. Praha: Mladá fronta 2016 : 239– 241.
2. Halpert B, Gyorkey F. Lesions observed in accessory spleens of 311 patients. Am J Clin Pathol 1959; 32(2): 165– 168.
3. Meyer-Rochow GY, Gifford AJ, Samra JS et al. Intrapancreatic splenunculus. Am J Surg 2007; 194(1): 75– 76.
4. Touré L, Bédard J, Sawan B et al. Case note: intrapancreatic accessory spleen mimicking a pancreatic endocrine tumour. Can J Surg 2010; 53(1): E1– E2.
5. Meiler R, Dietl KH, Novák K et al. Intrapancreatic accessory spleen. Int Surg 2010; 95(2): 183– 187.
6. Katuchova J, Baumohlova H, Harbulak P et al. Intrapancreatic accessory spleen. A case report and review of literature. JOP 2013; 14(3): 261– 263. doi: 10.6092/ 1590-8577/ 1231.
7. Zeman M, Zembala-Nożyńska E, Sczasny J et al. Intrapancreatic accessory spleen imitating a pancreatic neoplasm. Pol Przegl Chir 2011; 83(10): 568– 570. doi: 10.2478/ v10035-011-0090-9.
8. Ota T, Tei M, Yoshioka A et al. Intrapancreatic accessory spleen diagnosed by technetium-99m heat-damaged red blood cell SPECT. J Nucl Med 1997; 38(3): 494– 495.
9. Kim SH, Lee JM, Han JK et al. Intrapancreatic accessory spleen: findings on MR imaging, CT, US and scintigraphy, and the pathologic analy-sis. Korean J Radiol 2008; 9(2): 162– 174. doi: 10.3348/ kjr.2008.9.2.162.
10. Ota T, Ono S. Intrapancreatic accessory spleen: diagnosis using contrast enhanced ultrasound. Br J Radiol 2004; 77(914): 148– 149.
11. Kim SH, Lee JM, Han JK et al. MDCT and superparamagnetic iron oxide (SPIO) – enhanced MR findings of intrapancreatic accessory spleen in seven patients. Eur Radiol 2006; 16(9): 1887– 1897.
12. Kim SH, Lee JM, Lee JY et al. Contrast-enhanced sonography of intrapancreatic accessory spleen in six patients. AJR Am J Roentgenol 2007; 188(2): 422– 428.
13. Lin J, Jing X. Fine-needle aspiration of intrapancreatic accessory spleen, mimic of pancreatic neoplasms. Arch Pathol Lab Med 2010; 134(10): 1474– 1478. doi: 10.1043/ 2010-0238-CR.1.
14. Ardengh JC, Lopes CV, Kemp R et al. Pancreatic splenosis mimicking neuroendocrine tumors: microhistological diagnosis by endoscopic ultrasound guided fine needle aspiration. Arq Gastroenterol 2013; 50(1): 10– 14.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology
2018 Issue 6-
All articles in this issue
- Detská gastroenterológia a hepatológia
- Obezitologie a bariatricko-metabolická chirurgie
- Ultrasonografické hodnotenie steatózy pečene u obéznych pediatrických pacientov
- Vliv expozice anti-TNFα in utero na vývoj imunitního systému exponovaných dětí – kontrolovaná multicentrická studie
- Wilsonova choroba v dětském věku – dvě kazuistiky
- Parciální jejunální diverze – technické aspekty a počáteční zkušenosti
- Novinky ve farmakoterapii obezity
- Psychologické aspekty chirurgické léčby obezity
- Hepatopatie jako první projev systémové AL amyloidózy
- Meckelův divertikl jako příčina náhlé příhody břišní
- Intrapankreaticky uložená akcesorní slezina jako raritní solidní léze pankreatu
- Krvácení jako komplikace chronické pankreatitidy
- Správná praxe při oplachu endoskopů
- Endoskopická léčba rektálního syndromu při lipomu rekta technikou „loop and let go“
- Výběr z mezinárodních časopisů
- Široká problematika žlučových kyselin a jejich účinků pohledem XXV. Bile Acid Meeting: Bile Acids in Health and Disease 2018
- Správná odpověď na kvíz
- Poděkování recenzentům
- První biosimilární adalimumab – SB5
- Hepatitida B u osob infikovaných virem lidské imunodeficience v Porto-Novo – prevalence a související faktory
-
Novel developments in endoscopy of the proximal GIT
Oliver Pech (Germany) – Gastro Update Europe 2018, Prague
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Meckelův divertikl jako příčina náhlé příhody břišní
- Hepatopatie jako první projev systémové AL amyloidózy
- Wilsonova choroba v dětském věku – dvě kazuistiky
- Endoskopická léčba rektálního syndromu při lipomu rekta technikou „loop and let go“
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

