-
Medical journals
- Career
Terapie akutního kašle u dětí – současný stav znalostí medicíny založené na důkazech
Authors: J. Tuková; P. Koťátko
Authors‘ workplace: Klinika dětského a dorostového lékařství UK 1. LF a VFN, Praha přednosta prof. MUDr. J. Zeman, DrSc.
Published in: Čes-slov Pediat 2013; 68 (6): 364-371.
Category: Review
Overview
Akutní kašel je jedním z nejčastějších příznaků u dětí. Kauzální terapií lze příčinu kašle odstranit u menšiny pacientů, v praxi je kašel obvykle tlumen symptomaticky. Účinnost antitusik není dosud spolehlivě doložena a terapie těmito léky je často spojena s neúměrnou toxicitou, zvláště u menších dětí do šesti let věku. Některá mukolytika se zdají v léčbě kašle účinná, jejich použití u dětí do dvou let však není vhodné pro riziko paradoxní hypersekrece hlenu.
V článku prezentovaný přehled doporučení léčby akutního kašle u dětí je limitovaný absencí kvalitních vědeckých studií u dětí léčených pro kašel při akutním respiračním infektu.klíčová slova:
akutní kašel, antitusika, mukoaktivní substance, medicína založená na důkazechÚvod
Akutní kašel u dětí je jedním z nejčastějších příznaků a důvodů návštěvy lékaře. Spotřeba léků určených k symptomatické terapii kašle u dětí s respiračním infektem tvoří přední místo mezi volně prodejnými i na recept vázanými farmaky. SÚKL uvádí, že v roce 2010 bylo v ČR spotřebováno téměř 10 milionů balení léků ze skupiny R05 – Léčiva proti nachlazení a kašli za více než 600 mi-lionů korun (podíl dětí na spotřebě není u nás znám, ale předpokládá se, že je výrazně vyšší než u dospělých) [1]. Studie v USA zaznamenala u 10 % náhodně vybraných dětí užívání těchto léčiv za poslední týden [2]. Bezpečnost a účinnost řady těchto přípravků však není dosud dostatečně vědecky doložena. Současné přehledové práce expertů i odborné pediatrické společnosti varují před používáním antitusik u malých dětí pro neprokázanou účinnost a tomu neúměrnou toxicitu [3–8].
Cílem této práce je shrnout současné znalosti medicíny založené na důkazech v této oblasti a navrhnout doporučení léčby akutního kašle u dětí.
Definice, druhy akutního kašle a jeho příčiny
Kašel je fyziologický obranný reflex sloužící k eliminaci cizích částic, plynů a sekretů z dýchacích cest. Po náhlém inspiriu následuje intenzivní kontrakce výdechových svalů proti uzavřené glottis. Receptory reflexního oblouku kašle jsou umístěny nejen v dýchacích cestách, nýbrž i v zevním zvukovodu, perikardu či gastrointestinálním traktu. Akutní kašel u dětí představuje obtíže trvající méně než 3 týdny. Jeho zdaleka nejčastější příčinou je akutní respirační infekce, na jejímž vzniku se podílejí především viry a bakterie, vzácněji plísně a parazité. Na dalším místě se jako příčina akutního kašle u dětí uvádí alergie a aspirace (mikroaspirace). Nejen u dětí batolecího věku u náhle vzniklého akutního kašle vždy zvažujeme i možnost aspirace cizího tělesa. Častou příčinou chronického kašle u dětí bývá asthma bronchiale či gastroezofageální reflux s možnými aspiracemi (mikroaspiracemi), jindy syndrom zadní rýmy (postnasal drip). Kašel se však vyskytuje běžně i u dětí bez dalších projevů nemoci, jedná se o tzv. očekávaný kašel.
Dvě studie zkoumající frekvenci kašle u zcela zdravých dětí bez známek infektu zaznamenaly průměrně 34 epizod kašle/24 hodin, resp. 0–141 epizod kašle za 24 hodin [9, 10]. Pokud je kašel protrahovaný a vyčerpávající, ztrácí svou ochrannou funkci a výrazně narušuje kvalitu života jedince, jedná se o kašel patologický. Ten může vést až k závažným komplikacím (synkopa, pneumothorax, fraktury žeber, celkové vyčerpání atd.) [11].
Kauzální terapie akutního kašle
U menšiny pacientů lze kašel léčit kauzálně. Takto postupujeme u kašle jako astmatického ekvivalentu, kdy primární příčinou kašle je obstrukce dýchacích cest. Kašel ustupuje po nasazení bronchodilatační a protizánětlivé léčby (kortikoidy). Pacientům s kašlem na podkladě alergie často pomohou režimová opatření a úprava zevního prostředí, ev. podávání antihistaminik. V případě aspirace cizího tělesa je indikována bronchoskopie. Antirefluxní opatření a léčba uleví dětem, jejichž kašel je provokován gastroezofageálním refluxem. Syndrom zadní rýmy může ustat po odstranění zbytnělé adenomatoidní vegetace. U části pacientů je kašel provokován bakteriálním infektem (akutní bakteriální bronchitida, pneumonie či sinusitida a jiné), lékem volby jsou antibiotika.
Pozornost je třeba věnovat pacientům se závažným klinickým a/či epidemiologickým podezřením na pertusi. Zde je indikována antibiotická léčba již v počátku obtíží, neboť oddalování terapie do výsledků sérologických či kultivačních vyšetření by efekt léčby mohlo limitovat.
Symptomatická léčba kašle
Obvykle však nelze léčbu cílit na etiologické agens a lékař či pacient sám volí terapii symptomatickou. Farmaka tlumící kašel (antitusika) jsou používána k supresi záchvatovitého suchého dráždivého kašle. Naopak léky usnadňující clearance hlenu z dýchacích cest (mukoaktivní substance) jsou užívány při kašli produktivním. Antitusika se podle mechanismu účinku dělí na centrální a periferní (tab. 1).
Table 1. Vybraná antitusika řazená podle mechanismu účinku. 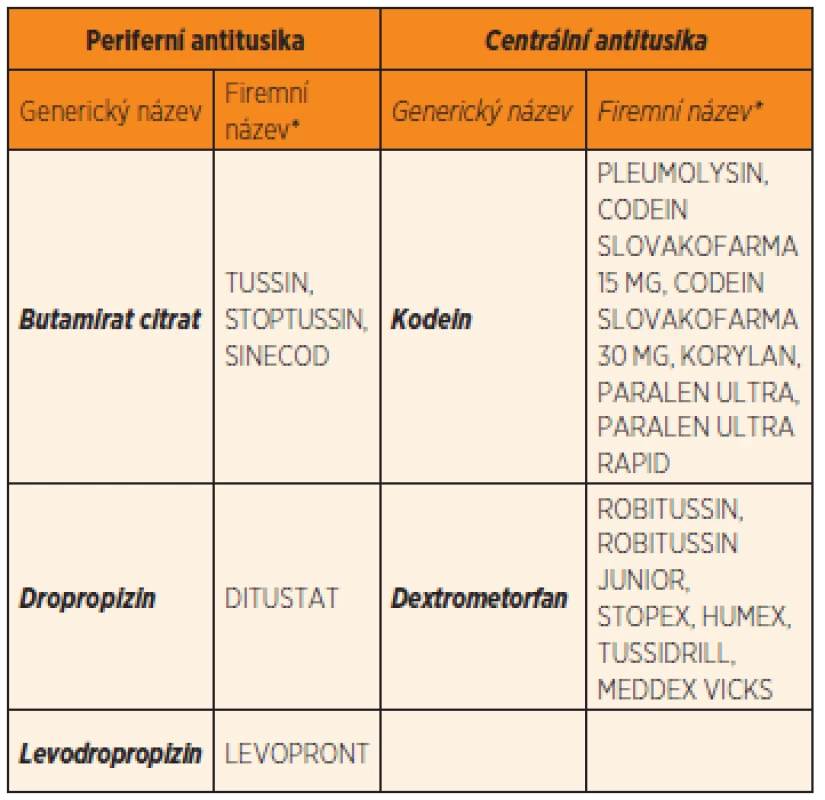
*Komerční názvy přípravků obsahujících dané generikum (a v SPC uvádějících mezi indikacemi léčbu kašle) registrované v ČR (květen 2013), zdroj SÚKL Jelikož je u léčby kašle znám významný placebo efekt (až 30 %), je třeba klinickou účinnost těchto léků posuzovat v randomizovaných kontrolovaných studiích (RCT) s placebem [6]. U léčiv na kašel existuje velké riziko toxicity. U periferních antitusik je hlavním nežádoucím účinkem nauzea, zvracení a bolest břicha. Tento projev toxicity často lékaři mylně hodnotí jako dávivý kašel s následným zvracením. U centrálních antitusik se objevuje obstipace, působení na centrální nervový systém (agitace, sedace až útlum dechového centra) a při delším užívání riziko návyku. U dětí je riziko toxicity vyšší, neboť u většiny přípravků je dávkování odvozeno ze studií dospělých. Mezi 2–5 lety věku se obvykle podává ¼ dávka, u dětí mezi 6–11 lety ½ dávka z dávky pro dospělého člověka. Riziko toxicity dále stoupá pro existenci vícesložkových přípravků, kde neinformovaní rodiče mohou stejnou látku podávat ve více přípravcích [12].
Kodein jako zlatý standard
Zlatým standardem léčby kašle u dospělých i dětí zůstává již desítky let kodein. Jeho účinnost je tedy klíčová pro vývoj a schvalování nových antitusik. Studie z 60. a 70. let na malých souborech dospělých pacientů s chronickou obstrukční plicní nemocí jeho účinnost oproti placebu dokládají (tab. 2) [13–15].
Table 2. Randomizované placebem kontrolované studie hodnotící efekt kodeinu. 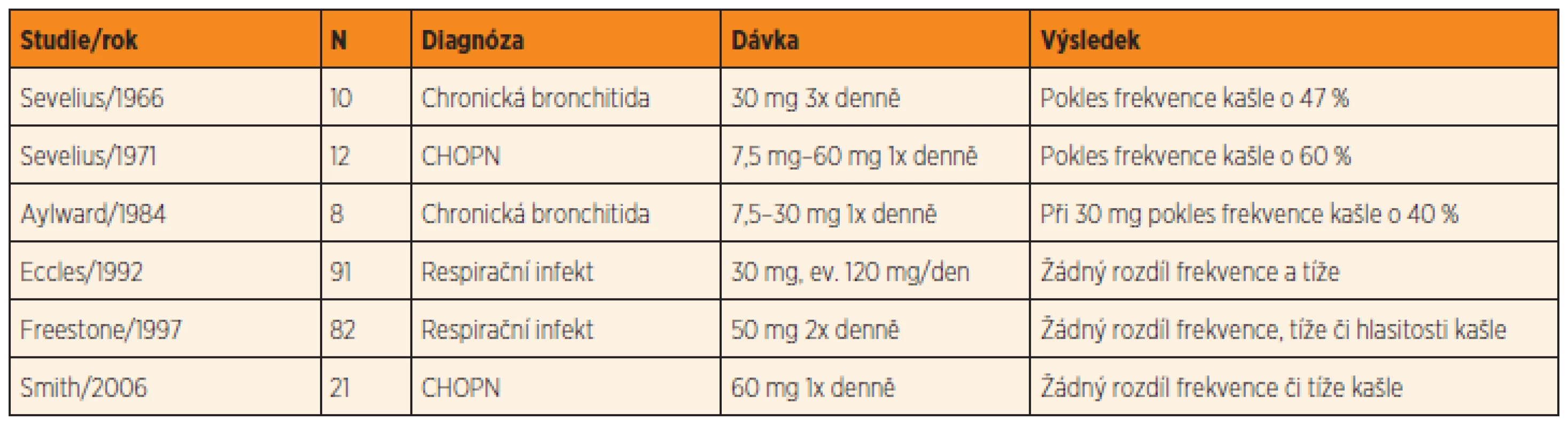
N – počet pacientů, CHOPN – chronická obstrukční plicní nemoc Studie v této indikaci u dospělých nemusí odrážet efekt léčby v nejčastějších indikacích u dětí. Recentní rozsáhlejší RCT studie navíc efekt kodeinu v tlumení kašle zpochybňují, obzvláště u kašle spojeného s akutním respiračním infektem [16–18]. Také metaanalýza (databáze Cochrane) efekt kodeinu u dětí (i dospělých) s akutním respiračním infektem neprokazuje [3]. Americká pediatrická společnost (AAP) varuje před podáváním antitusik včetně kodeinu u dětí s akutním respiračním infektem a doporučuje symptomatickou terapii [19].
Dextrometorfan
Jiný široce používaný lék ze skupiny centrálních antitusik představuje dextrometorfan. Výsledky RCT studií u dospělých pacientů s respiračním infektem jsou nejednotné (tab. 3) [15, 20–22], u dětí jediná RCT studie efekt neprokazuje [23].
Table 3. Studie hodnotící efekt dextrometorfanu na supresi kašle. 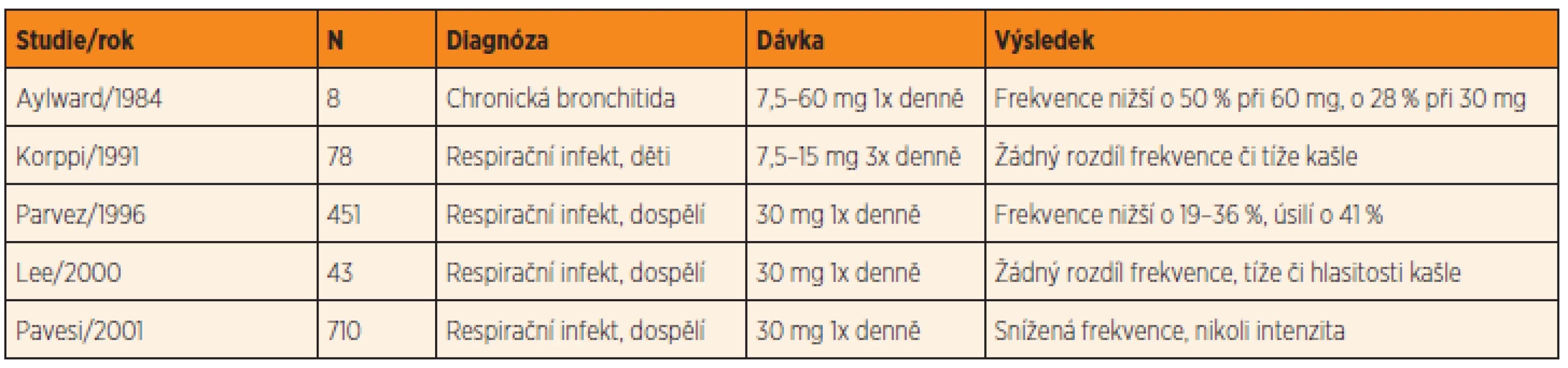
N – počet pacientů Velmi zajímavé jsou však dvě zcela nové studie hodnotící antitusický efekt dextrometorfanu, medu či podpůrné terapie u dětí s akutním infektem. U obou studií je med účinnější než dextrometorfan (a difenhydramin) či symptomatická léčba (tab. 4) [24–25]. Závěr těchto studií je třeba ověřit dalším výzkumem, neboť obě práce byly zatíženy velkým rizikem statistické chyby (nezaslepeno, problematická randomizace atd.) [26].
Table 4. Dvě randomizované studie porovnávající efekt dextrometorfanu a medu. 
N – počet pacientů, DXM – dextrometorfan Ostatní dostupná léčiva tlumící kašel
Zatímco antihistaminika druhé generace neovlivňují frekvenci ani intenzitu kašle, starší antihistaminika první generace podle metaanalýz u dospělých mírně kašel tlumí [7, 27]. U dětí nejsou k dispozici RCT studie. Z periferních antitusik byl americkou společností hrudních lékařů (ACCP) navržen v doporučeních pro léčbu akutní a chronické bronchitidy levodropropizin, stejná společnost však v dalším bodu doporučení uvádí, že periferní ani centrální antitusika nemají být podávána u pacientů s infekcí horních cest dýchacích [7]. Levodropropizin byl zkoumán jedinou RCT studií u dospělých s bronchitidou, kde se zdál být účinný [28]. Pro další volně prodejné i na recept vázané přípravky na kašel nejsou dostupná data, která by jejich účinnost jasně prokázala či vyvrátila [3]. Naopak u řady antitusik byla doložena nemalá toxicita. Jako příklad uvádíme počet 1519 dětí do 2 let věku, u kterých bylo hlášeno v USA za rok 2004/2005 ošetření na pohotovosti pro předávkování či nežádoucí účinky léků proti nachlazení či kašli. Navíc u 3 kojenců mladších 6 měsíců bylo podání léků na kašel a nachlazení hodnoceno jako přímá příčina úmrtí [8].
Mukoaktivní substance
Léčiva této skupiny snižují tvorbu hlenu či usnadňují jeho clearance z dýchacích cest (tab. 5) [29]. Podle metaanalýzy byl zjištěn u N-acetylcysteinu a karbocysteinu mírný efekt při akutním infektu [30]. Tento účinek byl doložen jen u dětí nad dva roky, zároveň bylo zaznamenáno riziko paradoxní hypersekrece hlenu u desítek dětí do dvou let věku. Ambroxol má navíc antioxidační účinek a antitusický efekt vyvolaný místním anestetickým účinkem, blokádou sodíkových kanálů neuronů. Dvě dostupné RCT zkoumající toto léčivo přinesly odlišné výsledky [31, 32]. Erdostein této skupině dominuje množstvím RCT studií, které prokazují jeho účinnost. Tato látka snižuje vazkost hlenu, omezuje adhezi bakterií, má i antioxidační účinky. Lék potencuje účinek antibiotik u bakte-riálních infekcí (synergie). Podle současných studií Erdostein účinně tlumí kašel u infektů dolních cest dýchacích [33, 34].
Table 5. Přehled léčiv ze skupiny mukoaktivních substancí. 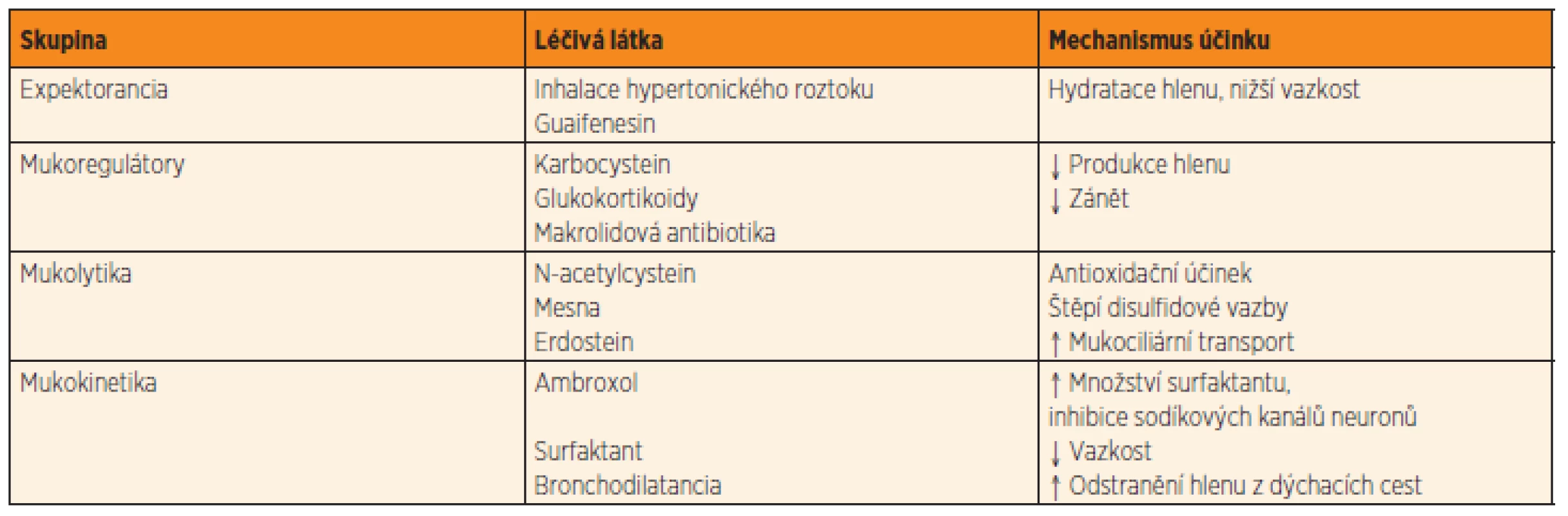
Přínos podávání mukolytik u pacientů s akutní pneumonií nebyl doložen pro nedostatek dat [35], dostupné studie efekt bromhexinu a ambroxolu nevylučují. Účinnost expektorancia guaifenesinu není dosud doložena RCT studií.
Kašel při akutní laryngitidě
Specifická terapie je nutná v případě kašle u akutní laryngitidy. Zde dochází k otoku a zánětlivé infiltraci měkkých tkání v oblasti glottis, v nejužším místě dýchacích cest, stav může vést až k akutní respirační insufi-cienci. U mírných forem otok sliznic ustoupí po inhalaci studeného vzduchu, dítě s projevy dyspnoe obvykle vyžaduje podání kortikoidů a nebulizaci ředěného roztoku adrenalinu. Závažné stavy vyžadují transport RZP a hospitalizaci na JIRP ev. s nutností intubace.
Doporučení některých odborných společností
ACCP v doporučeních z roku 2006 uvádí, že antitusika u dětí s akutním infektem nejsou indikována, navíc mohou vést k závažné morbiditě až mortalitě těchto dětí [7]. Centrum pro kontrolu léčiv CDC v roce 2007 vydává zprávu lékařům o riziku závažného postižení či fatálního předávkování podáním léčiv proti kašli a nachlazení dětem do 2 let věku [36]. Medicines and Healthcare products Regulatory Agency (MHRA) v roce 2009 dokonce kontraindikuje antitusika u dětí do 6 let a nabádá k opatrnosti u 6–12letých [37].
Léčba kašle při akutním respiračním infektu podle medicíny založené na důkazech
Obecně léčba kašle není indikována při běžném nachlazení, kataru horních cest dýchacích. Farmaka neovlivňují průběh choroby [38, 39]. Doporučuje se zvýšený příjem tekutin, antipyretika při horečnatém průběhu onemocnění, nosní hypertonické kapky, odsávání sekretů z nosu, zvlhčený vzduch [19], zvýšená poloha. Lze se pokusit ulevit pacientovi i podáním medu, přestože účinnost tohoto opatření je nutno doložit (ne kojencům – riziko botulismu!). U pacientů s narušenou mukociliární clearance (pacienti s cystickou fibrózou, bronchiektaziemi, ciliární dyskinezí) je jako prevence i léčba akutních respiračních infektů nutná důsledná respirační fyzioterapie a inhalační léčba.
Antitusika jsou indikována, pokud kašel neplní obrannou funkci a závažně narušuje kvalitu života pacienta. Používají se v případech, kdy přínos léčby významně převažuje nad možnými projevy toxicity léku. Tento patologický kašel se projevuje jako protrahovaný, vysilující, neproduktivní. V takovém případě lze u dětí nad 2 roky podat antihistaminika 1. generace, ev. léčiva ze skupiny periferních antitusik spojené s méně závažnou toxicitou (butamirát, dropropizin, levodropropizin). Kontraindikována jsou antitusika u pacientů s produktivním kašlem a u všech jedinců s narušenou mukociliární clearance. Nemají být podávána dětem do dvou let (ev. do 6 let věku). Nelze je použít u pacientů s respirační insuficiencí či k tlumení kašle při asthma bronchiale.
Vybraná mukolytika jsou indikována u pacientů s produktivním kašlem k podpoře clearance hlenů. Jejich role u léčby pneumonií není zatím doložena. Jen velmi uvážlivě mohou být podávána u dětí s asthma bronchiale či opakovanými obstrukcemi dýchacích cest pro riziko vyvolání či zhoršení bronchospazmu. Při akutní dušnosti u těchto pacientů je podání mukolytik kontraindikováno. Nedoporučují se rovněž u jedinců s omezeným kašlacím reflexem (děti do 2 let, jedinci s muskuloskeletálním onemocněním atd.). Kombinace antitusik a mukolytik nemá racionální podklad a není vhodná!!!
Závěr
V současné době nelze pro nedostatek kvalitních vědeckých studií u dětí s akutním kašlem efekt léčiv na kašel a nachlazení spolehlivě doložit ani vyvrátit. Výzkum je komplikován subjektivním vnímáním kašle dětmi i rodiči, částečnou volní kontrolou kašle (u všech přípravků není dostupné placebo), rozsáhlou množinou možných příčin kašle, náročným výběrem pacientů (nelze zajistit účast dětí bez epizod tzv. očekávaného kašle).
S přihlédnutím ke skutečnosti, že kašel při akutním respiračním infektu je obvykle sebelimitující obtíží a že u řady dostupných antitusik neexistuje dostupné bezpečné dávkovací schéma pro děti, je třeba pečlivě zvážit možný přínos i riziko podání těchto léčiv, zvláště u mladších dětí. Tento postup je však v praxi ztížen očekáváním rodičů, kteří od lékaře žádají terapeutický zásah.
Poděkování
Za laskavou revizi a cenné připomínky děkujeme docentu Jozefu Hozovi.
Práce byla podpořena grantem RVO-VFN 64165/2012.
Nákup videoendoskopického systému použitého při práci byl podpořen projektem OPPK „Materiálně-technická základna pro výzkum v oblasti diagnostiky a léčby civilizačních a onkologických onemocnění a jejich závažných rizik ve VFN v Praze“, reg. č. CZ.2.16/3.1.00/24012 spolufinancovaným z Evropského fondu pro regionální rozvoj.
Došlo: 29. 11. 2012
Přijato: 1. 9. 2013
MUDr. Jana Tuková, Ph.D.
Klinika dětského a dorostového lékařství
UK 1. LF a VFN
Ke Karlovu 2
128 00 Praha 2
e-mail: jana.tukova@vfn.cz
Sources
1. Hodnocení dodávek distribuovaných léčivých přípravků za rok 2010 [naposledy viděno 22. 05. 2013]. Dostupné z http://www.sukl.cz/hodnoceni-dodavek-distribuovanych-lecivych-pripravku-za-rok.
2. Vernacchio L, Kelly JP, Kaufman DW, et al. Medication use among children <12 years of age in the United States: results from the Slone Survey. Pediatrics 2009; 124 (2): 446–454.
3. Smith SM, Schroeder K, Fahey T. Over-the-counter (OTC) medications for acute cough in children and adults in ambulatory settings. Cochrane Database Syst Rev 2012; 15; 8: CD001831.
4. Goldman RD. Codeine for acute cough in children. Can Fam Physician 2010; 56 (12): 1293–1294.
5. Paul IM. Therapeutic options for acute cough due to upper respiratory infections in children. Lung 2012; 190 (1): 41–44.
6. Dicpinigatis PV, Colice GL, Goolsby MJ, et al. Acute cough: a diagnostic and therapeutic challenge. Cough 2009; 5 : 11.
7. Bolser DC. Cough suppressant and pharmacologic protussive therapy: ACCP evidence-based clinical practice guidelines. Chest 2006; 129 (Suppl 1): 238S–249S.
8. Centers for Disease Control and Prevention (CDC). Infant deaths associated with cough and cold medications--two states, 2005. MMWR Morb Mortal Wkly Rep 2007; 56 (1): 1–4.
9. Munyard P, Bush A. How much coughing is normal? Arch Dis Child 1996; 74 (6): 531–534.
10. Chang AB, Phelan PD, Robertson CF, et al. Frequency and perception of cough severity. J Paediatr Child Health 2001; 37 (2): 142–145.
11. Irwin RS, Boulet LP, Cloutier MM, et al. Managing cough as a defense mechanism and as a symptom. A consensus panel report of the American College of Chest Physicians. Chest 1998; 114 (2): 133S–181S.
12. Vernacchio L, Kelly JP, Kaufman DW, et al. Medication use among children <12 years of age in the United States: results from the Slone Survey. Pediatrics 2009; 124 (2): 446–454.
13. Sevelius H, Colmore JP. Objective assessment of antitussive agents in patients with chronic cough. J New Drugs 1966; 6 (4): 216–223.
14. Sevelius H, McCoy JF, Colmore JP. Dose response to codeine in patients with chronic cough. Clin Pharmacol Ther 1971; 12 (3): 449–455.
15. Alward M, Maddock J, Davies DF, et al. Dextro-methorphan and codeine: comparison of plasma kinetics and antitussive effects. Eur J Respir Dis 1984; 65 (4): 283–291.
16. Eccles R, Morris S, Jawad M. Lack of effect of codeine in the treatment of cough associated with acute upper respiratory tract infection. J Clin Pharm Ther 1992; 17 (3): 175–180.
17. Smith J, Owen E, Earis J, et al. Effect of codeine on objective measurement of cough in chronic obstructive pulmonary disease. J Allergy Clin Immunol 2006; 117 (4): 831–835.
18. Freestone C, Eccles R. Assessment of the antitussive efficacy of codeine in cough associated with common cold. J Pharm Pharmacol 1997; 49 (10): 1045–1049.
19. American Academy of Pediatrics, Committee on Drugs. Use of codeine - and dextromethorphan-containing cough remedies in children. Pediatrics 1997; 99 (6): 918–920.
20. Parvez L, Vaidya M, Sakhardande A, et al. Evaluation of antitussive agents in man. Pulm Pharmacol 1996; 9 (5–6): 299–308.
21. Lee PCL, Jawad MS, Eccles R. Antitussive efficacy of dextromethorphan in cough associated with acute upper respiratory tract infection. J Pharm Pharmacol 2000; 52 (9): 1137–1142.
22. Pavesi L, Subburaj S, Porter-Shaw K. Application and validation of a computerized cough acquisition system for objective monitoring of acute cough: a meta-analysis. Chest 2001 Oct; 120 (4): 1121–1128.
23. Korppi M, Laurikainen K, Pietikäinen M, Silvasti M. Antitussives in the treatment of acute transient cough in children. Acta Paediatr Scand 1991; 80 (10): 969–971.
24. Paul IM, Beiler J, McMonagle A, et al. Effect of honey, dextromethorphan, and no treatment on nocturnal cough and sleep quality for coughing children and their parents. Arch Pediatr Adolesc Med 2007; 161 (12): 1140–1146.
25. Shadkam MN, Mozaffari-Khosravi H, Mozayan MR. A comparison of the effect of honey, dextromethorphan, and diphenhydramine on nightly cough and sleep quality in children and their parents. J Altern Complement Med 2010; 16 (7): 787–793.
26. Oduwole O, Meremikwu MM, Oyo-Ita A, et al. Honey for acute cough in children. Cochrane Database Syst Rev 2012; 14; 3: CD007094.
27. Arroll B. Non-antibiotic treatments for upper-respiratory tract infections (common cold). Respir Med 2005; 99 (12): 1477–1484.
28. Allegra L, Bossi R. Clinical trials with the new antitussive levodropropizine in adult bronchitic patients. Arzneimittelforschung 1988; 38 (8): 1163–1136.
29. Balsamo R, Lanata L, Egan CG. Mucoactive drugs. Eur Respir Rev 2010; 19 (116): 127–133.
30. Duijvestijn YC, Mourdi N, Smucny J, et al. Acetyl-cysteine and carbocysteine for acute upper and lower respiratory tract infections in paediatric patients without chronic broncho-pulmonary disease. Cochrane Database Syst Rev 2009; 21 (1): CD003124.
31. Germouty J, Jirou-Najou IL. Clinical efficacy of ambroxol in the treatment of bronchial stasis. Clinical trial in 120 patients at two different doses. Respiration 1987; 51 (Suppl 1): 37–41.
32. Guyatt GH, Townsend M, Kazim F, et al. A controlled trial of ambroxol in chronic bronchitis. Chest 1987; 92 (4): 618–620.
33. Balli F, Bergamini B, Calistru P, et al. Clinical effects of erdosteine in the treatment of acute respiratory tract diseases in children. Int J Clin Pharmacol Ther 2007; 45 (1): 16–22.
34. Titti G, Lizzio A, Termini C. A controlled multicenter pediatric study in the treatment of acute respiratory tract diseases with the aid of a new specific compound, erdosteine (IPSE, Italian Pediatric Study Erdosteine). Int J Clin Pharmacol Ther 2000; 38 (8): 402–407.
35. Chang CC, Cheng AC, Chang AB. Over-the-counter (OTC) medications to reduce cough as an adjunct to antibiotics for acute pneumonia in children and adults. Cochrane Database Syst Rev. 2012; 15; 2: CD006088.
36. Centers for Disease Control and Prevention (CDC). Infant deaths associated with cough and cold medications — Two states, 2005. MMWR Morb Mortal Wkly Rep 2007; 12; 56 : 1–4.
37. Overview – Risk: Benefit of OTC cough and cold medicines in children [naposledy viděno 22.05.2013]. Dostupné z http://www.mhra.gov.uk/home/groups/pl-p/documents/websiteresources/con041374.pdf.
38. Irwin RS, Curley FJ, Bennett FM. Appropriate use of antitussives and protussives. A practical review. Drugs 1993; 46 (1): 80–91.
39. Chung KF. Current and future prospects for drugs to suppress cough. IDrugs 2003; 6 (8): 781–786.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2013 Issue 6-
All articles in this issue
- Minimálně invazivní operace vpáčeného hrudníku
- Terapie akutního kašle u dětí – současný stav znalostí medicíny založené na důkazech
- Kolik dospívajících je v Česku ohroženo postižením mozku při zneužívání alkoholu?
- Radiologická diagnostika močových cest u dětí na Fakultě dětského lékařství UK v Praze ve druhé polovině dvacátého století
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Minimálně invazivní operace vpáčeného hrudníku
- Terapie akutního kašle u dětí – současný stav znalostí medicíny založené na důkazech
- Radiologická diagnostika močových cest u dětí na Fakultě dětského lékařství UK v Praze ve druhé polovině dvacátého století
- Kolik dospívajících je v Česku ohroženo postižením mozku při zneužívání alkoholu?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

