-
Medical journals
- Career
Kopřivka – klasifikace, diagnostika, léčba
Authors: P. Brodská
Authors‘ workplace: Dermatovenerologická klinika LF UK a FN Plzeň přednosta prof. MUDr. Karel Pizinger, CSc.
Published in: Čes-slov Derm, 89, 2014, No. 2, p. 55-62
Category: Reviews (Continuing Medical Education)
Overview
Kopřivka je časté onemocnění, charakterizované vznikem pomfů a/nebo angioedému. Především chronická kopřivka významně snižuje kvalitu života. V článku jsou uvedeny nejnovější doporučení týkající se klasifikace, diagnostiky a léčby kopřivky. Tento souborný referát se opírá především o společné stanovisko a doporučení k léčbě a diagnostice kopřivky, které bylo vypracováno experty z několika evropských států.
Klíčová slova:
kopřivka – pomfus – angioedém – klinický obraz – diagnostika - léčbaÚVOD
Kopřivka je časté onemocnění. Dvacet až třicet procent populace bylo v životě postiženo alespoň jedním výsevem kopřivky. Prevalence se pohybuje mezi 1–6 % [15]. Častěji jsou postiženy děti a mladší dospělí. Kopřivka je heterogenní skupina chorob, charakterizovaná vznikem kopřivkových pomfů či angioedému. Pomfus (pupen) je plošné vyvýšení kůže, růžové barvy, někdy je v důsledku stlačení cév edémem v centru bledý anebo obklopen světlým haló. Velikost pomfů kolísá od několika milimetrů až po velké plochy (urticaria gigantea či geographica). Pupeny jsou prchavé, obvykle mizí beze stopy do 24 hodin, mohou svědit či pálit. Svědění nevede ke škrábání, nýbrž ke tření projevů, a proto nebývají přítomné exkoriace. Pomfy někdy při regresi nabývají anulární či circinární uspořádání. Asi u třetiny kopřivek bývá současně přítomen angioedém (Quinckeho edém) [3]. Angioedém je akutně vznikající nezánětlivý lokalizovaný otok kůže a podkoží, který nejčastěji postihuje víčka, rty, genitál a končetiny. Angioedém trvá déle jak 24 hodin a odeznívá pomaleji, většinou do 3 dnů. Symptomy, jako je ztížené dýchání, chrapot, průjmy, mohou vznikat při postižení sliznic dýchacích cest a zažívacího traktu. Kopřivku může také provázet celková nevolnost, nauzea a může se rozvinout až anafylaktický šok.
ETIOLOGIE A PATOGENEZE
Společným znakem většiny kopřivek je aktivace a degranulace mastocytů. Degranulací mastocytů dochází k uvolnění v nich obsažených látek (látek vazoaktivních – histaminu, prostaglandinů D2, leukotrienů C4 a B4 proteoglykanů – heparinu, chondroitinsulfátu E, hyaluronanu; cytokinů – interleukinů: IL-3, IL-4, IL-5, IL-6, IL-8, IL-13, tumor nekrotizujícího faktoru α – TNF α, GM-CSF – faktoru stimulujícího granulocyto-makrofágové kolonie, chemotaktických faktorů pro eozinofily a neutrofily, proteolytických enzymů – tryptázy, chymázy, karboxypeptidázy, katepsinu G), které působí především vazodilatačně, zvyšují permeabilitu cévní stěny, stimulují volná nervová zakončení [15]. Degranulace může být vyvolána různými mechanismy. U akutní kopřivky jde často o anafylaktický typ reakce zprostředkovaný stykem alergenu s IgE protilátkami navázanými na membráně žírných buněk ve tkáních nebo bazofilech v periferní krvi. Dále může k degranulaci mastocytů dojít cestou aktivace komplementu (uvolněním anafylatoxinů C3a a C5a). Především u chronické urtikárie mohou být také přítomny autoimunitní protilátky proti IgE nebo častěji proti vysoko afinitnímu IgE receptoru (FcεRI) mastocytů a bazofilů. Řada látek může působit přímo na mastocyty jako histaminové liberátory (morfin, kodein, radiokontrastní látky, žlučové kyseliny, potraviny, léky, bakteriální toxiny, štípnutí hmyzem, fyzikální vlivy). Přímým liberátorem histaminu jsou i neuropeptidy jako substance P (ale i např. vazoaktivní intestinální peptid, somatostatin, neurotenzin, kalcitonin) obsažené v kožních nervových vláknech, které mohou hrát roli např. u cholinergní urtikárie, kde provokující stimul se zdá být čistě nervového původu [15].
HISTOLOGICKÝ NÁLEZ
Histologický nález je u kopřivkových pomfů poměrně chudý a nespecifický. Je přítomen edém horních a středních vrstev dermis, s dilatací postkapilárních venul a lymfatických cév v horním koriu. Perivaskulárně bývá smíšený zánětlivý infiltrát, složený z neutrofilů, eozinofilů, makrofágů a lymfocytů. U angioedému je nález podobný, ale otok pozorujeme spíše ve spodních vrstvách dermis a v subcutis [17]. Převaha neutrofilů v zánětlivém infiltrátu nutí zvážit souvislost s vzácnými autoinflamatorními onemocněními (např. Schnitzlerův syndrom) [6].
FORMY URTIKÁRIÍ
Kopřivka by měla být klasifikována nejprve podle doby trvání, zda jde o onemocnění akutní, do 6 týdnů nepřetržitého průběhu, nebo chronické. Chronická kopřivka se dělí do dvou hlavních podskupin podle toho, zda se příznaky objevují spontánně, nebo jsou vyvolány prokazatelným podnětem (tab. 1). Různé typy se mohou vyskytovat i současně. Pojem chronická idiopatická kopřivka se nyní nahrazuje termínem chronická spontánní kopřivka [8].
Table 1. Typy kopřivek 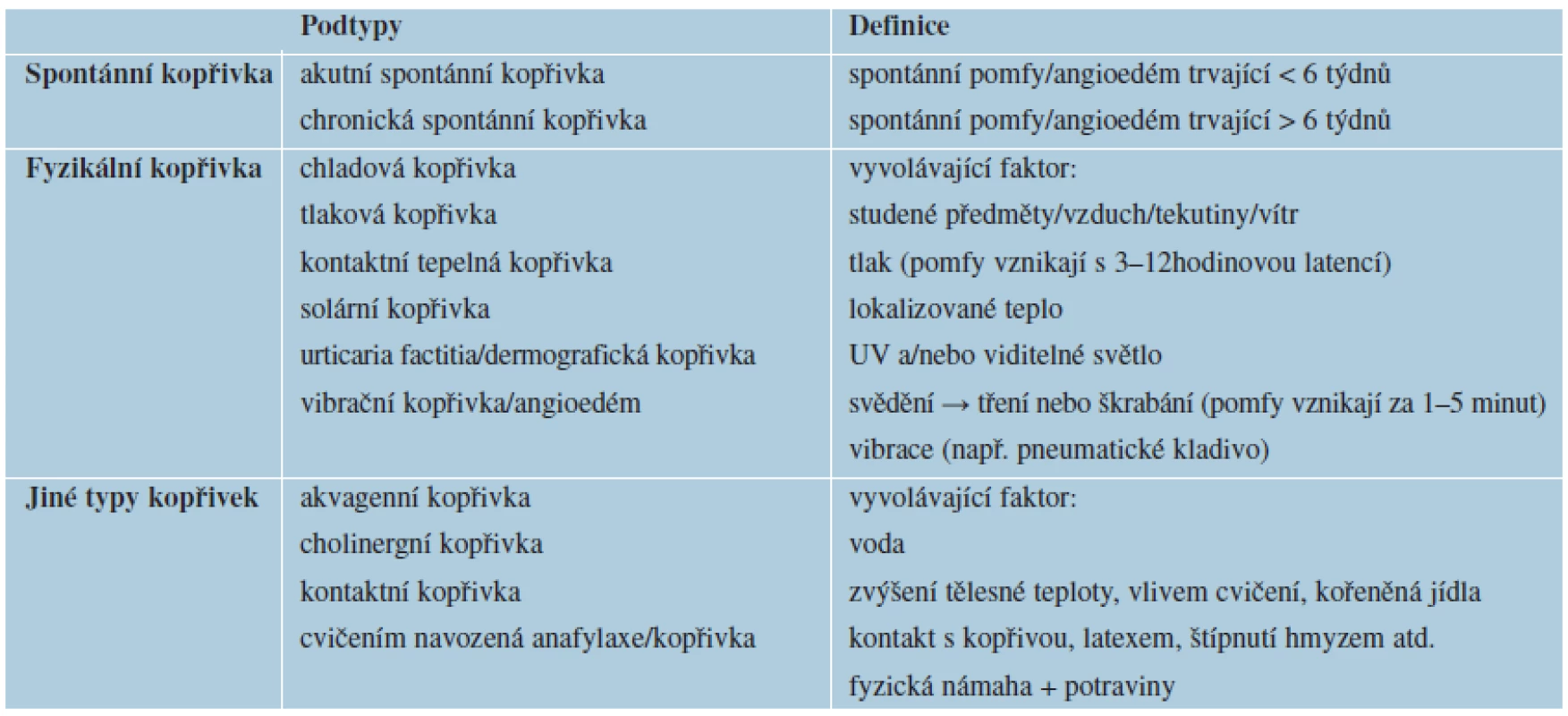
podle EAACI/GA2LEN/EDF/WAO, 2009 [17] Chronická kopřivka je definována jako onemocnění s urtikariálními výsevy kontinuálními či recidivujícími alespoň dvakrát týdně po dobu delší 6 týdnů, které může přetrvávat i desítky let. Průměrně tato forma trvá 2–3 roky. Přibližně u poloviny případů jde o chronickou spontánní urtikárii, jejíž příčina zůstává neobjasněná [15]. U 30 až 50 % nemocných s chronickou spontánní urtikárií lze prokázat vznik pomfů po injekci autologního séra [17]. Příčinou jsou protilátky proti vysoko afinitnímu IgE receptoru (FcεRI) mastocytů a bazofilů, méně často protilátky proti IgE [17]. Při testu s autologním sérem se aplikuje 0,05 ml séra intradermálně na volární stranu předloktí. Jako negativní kontrola je použit fyziologický roztok, jako pozitivní kontrola slouží histamin. Výsledek hodnotíme za 30 minut a za pozitivní považujeme pomfus o 1,5 mm větší, než je kontrola s fyziologickým roztokem. Test je možno provést jen u dospělých pacientů. Toto vyšetření je ale poměrně nespecifické a není plně standardizováno [17].
Fyzikální kopřivky jsou opakovaně vyvolané stejným fyzikálním stimulem. Do této skupiny řadíme: chladovou kontaktní kopřivku, tlakovou kopřivku (pozdní tlaková kopřivka, urticaria mechanica, mechanická kopřivka pozdního typu), lokalizovanou tepelnou kopřivku, solární kopřivku, urticaria factitia (dermografická kopřivka časného typu, symptomatický dermografismus), vibrační angioedém [16]. V doporučeních z roku 2009 jsou kopřivky akvagenní, cholinergní, kontaktní a vyvolané cvičením řazeny zvlášť (tab. 1) [17]. Cholinergní kopřivka postihuje až 20 % populace a vzniká zvýšením tělesné teploty. Ke vzniku cholinergní kopřivky může dojít při zpocení, po požití horkých jídel nebo při psychickém stresu. Výsev kopřivkových pomfů u cholinergní kopřivky je typicky symetrický a pupeny jsou drobné, do 3 mm velké, bývá jich velké množství a zpravidla do 1 hodiny mizí. U urticaria factitia pacient pociťuje svědění kůže a kopřivka vzniká v místě tření, škrabání nebo vzniká v místě tlaku na kůži tupým předmětem (plastický dermografismus). Projevy během 15 minut odeznívají. Oproti tomu u tlakové kopřivky (urticaria mechanica) dochází v místě působení plošného tlaku větší intenzity po 2–6 hodinách ke vzniku většího lokalizovaného, někdy až bolestivého otoku. Otok může přetrvávat déle než 24 hodin. Může být provázen zvýšenou teplotou, bolestmi kloubů, svalů a únavou [16].
ANGIOEDÉM
Angioedém (angioneurotický edém, Quinckeho edém) je akutní nezánětlivý otok kůže a podkoží, obvykle ohraničený. Získaná forma angioedému provází často kopřivku. Nejčastěji je způsoben ACE inhibitory, penicilinem, nesteroidním antiflogistiky, antagonisty angiotensin II receptorů a kontrastními látkami. Sekundárně může být přítomen u chronických zánětlivých, lymfoproliferativních nebo autoimunitních onemocnění (tab. 2). Postižení pacienti bývají starší 40 let.
Table 2. Typy angioedému [1, 9] ![Typy angioedému [1, 9]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/bb17e3bafb758933ff1600e8c0a51f92.png)
Oproti tomu, hereditární angioedém (HAE) je vzácný. Odhaduje se, že v Evropě trpí hereditárním angioedémem 10 000 až 50 000 osob [1]. Většina pacientů s HAE uvádí výskyt prvních záchvatů před dosažením věku dvaceti let. Jedná se o autozomálně dominantní mutaci genu pro C1-inhibitor. U 85 % nemocných s hereditárním angioedémem je snížená syntéza C1-inhibitoru a u téměř 15 % pacientů jde o dysfunkci C1 – inhibitoru v plazmě. Nově byl popsán třetí typ HAE s normální hladinou C1 – inhibitoru vyskytující se především u žen. Uvažuje se o možné mutaci genu pro koagulační faktor XII (Hagemanův faktor) [9]. Nedostatek sérového inhibitoru první složky komplementu vyvolává nekontrolovanou aktivaci C1 složky komplementu a kinin--kalikreinového systému s uvolněním bradykininu, který je příčinou zvýšené cévní permeability a edematózního prosáknutí podkoží nebo submukózy sliznic. Téměř všichni pacienti s hereditárním angioedémem trpí záchvaty silných bolestí břicha, nevolností, zvracením, průjmy vyvolanými otoky střevní stěny [1]. Obzvláště nebezpečný je otok krku, nosu a jazyka. Mortalita hereditárního angioedému se pohybuje kolem 30 % [15]. Mezi možné spouštěče záchvatů HAE patří trauma, tělesná nebo duševní zátěž, chirurgické výkony, nachlazení, chřipka, bodnutí hmyzem. Trauma uvnitř dutiny ústní během stomatologického výkonu zvyšuje u pacientů s HAE pravděpodobnost vzniku život ohrožujícího otoku horních dýchacích cesta a jazyka [1].
DIFERENCIÁLNÍ DIAGNOSTIKA KOPŘIVEK
V rámci diferenciální diagnózy kopřivek je nutné odlišit především urtikariální vaskulitidu. Diagnózu potvrdíme histologicky a vyšetřením přímou imunofluorescencí. Jde o leukocytoklastickou vaskulitidu z cirkulujících imunokomplexů, kde kromě kůže mohou být postiženy i vnitřní orgány. Pomfy přetrvávají déle než 24 hodin, mohou zanechávat pigmentace a spíše pálí a bolí. Dále diferenciální diagnostika zahrnuje erytémová svědivá onemocnění, exantémy, tinea corporis, urtikariální fázi bulózního pemfigoidu [15]. Urticaria pigmentosa (kožní mastocytóza), urtikariální vaskulitida, familiární chladová kopřivka, vrozený nebo získaný deficit C1 inhibitoru již nejsou považovány za podtypy kopřivky [17]. Pomfy nebo angioedém mohou být také jedním ze symptomů u autoinflamatorních onemocnění a syndromů uvedených v tabulce 3, které bývají provázeny nálezem neutrofilů v histologickém vyšetření [6]. Nově byla také definována skupina onemocnění s ekzematózně urtikariálními projevy, která je nazývána urtikariální dermatitida [4].
Image 1. Doporučený diagnostický algoritmus 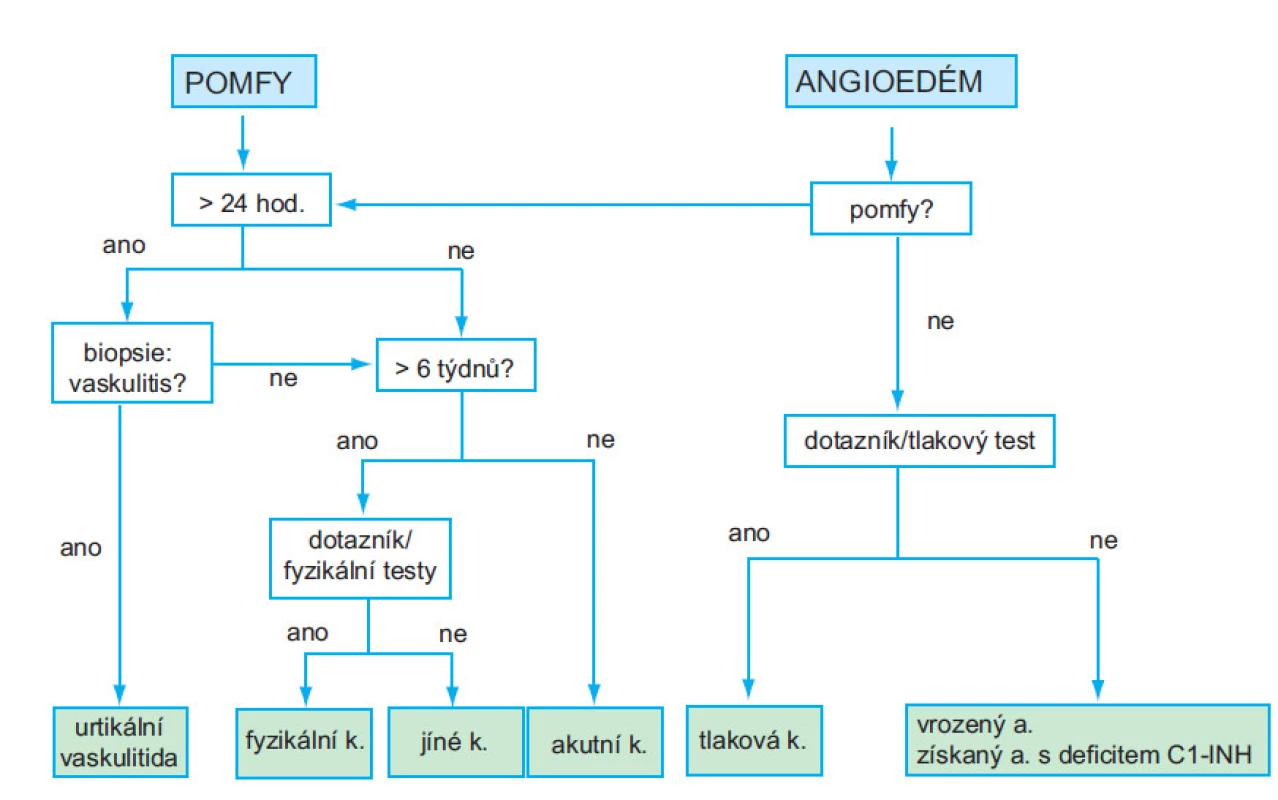
EAACI/GA2LEN/EDF/WAO, 2009 [17] Table 3. Příklady vzácných autoinflamatorních onemocnění s urtikariálními projevy a/nebo angioedémem [6] ![Příklady vzácných autoinflamatorních onemocnění s urtikariálními projevy a/nebo angioedémem [6]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/671b855b0dee1caa48c4e2d38b5f4ea2.png)
Stanovení závažnosti kopřivky
K objektivnímu stanovení závažnosti onemocnění a monitorování úspěšnosti terapie je vhodné použít hodnocení aktivity kopřivky, tzv. UAS – Urticaria Activity Score (tab. 4). Vzhledem ke změnám intenzity a aktivity kopřivky je doporučeno hodnocení 7 po sobě následujících dnů, které provádí sám pacient. Vhodné je použití tohoto skórovacího schématu v klinických studiích [17].
Table 4. Skóre k určení aktivity kopřivky (UAS – Urticaria Activity Score) [17] ![Skóre k určení aktivity kopřivky (UAS – Urticaria Activity Score) [17]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/52cd7096bba9eb1cdf2bf82d02006965.png)
Doporučené diagnostické testy
Diagnóza urtikárie je většinou snadná z klinického obrazu. Určení příčiny je však velmi svízelné a většinou neúspěšné. Na obrázku 1 je znázorněn postup při diagnostice různých typů kopřivky podle doporučení EAACI (European Academy of Allergology and Clinical Immunology), GA2LEN (Global Allergy and Asthma European Network), EDF (European Dermatology Forum), WAO (World Allergy Organisation) z roku 2009 [17]. Diagnostické laboratorní vyšetřování by mělo vyplývat v první řadě z pečlivé anamnézy. Specialisty z EAACI/GA2LEN/EDF/WAO byl vypracován okruh otázek určených k pátrání po příčině kopřivky (tab. 5).
Table 5. Anamnestický dotazník 
podle EAACI/GA2LEN/EDF/WAO, 2009 [17] U akutní kopřivky se necílené laboratorní testy nedoporučují, důležitá je především důkladná anamnéza. Často udávaným spouštěcím faktorem u dětí jsou například virové infekce horních cest dýchacích [13]. U dětí i dospělých mohou kopřivku vyvolat různé potraviny, antibiotika nebo nesteroidní antiflogistika [13]. Léková etiologie kopřivky je uváděna jen asi v 10 % případů [3]. Specifické alergologické testy (kožní prick testy, vyšetření specifických IgE protilátek v séru atd.) jsou vhodné jen při důvodném podezření na alergii prvního typu (anafylaktického typu), např. při podezření na potravinovou alergickou reakci zjištěnou na základě anamnestických údajů. Potravinovou alergii je ale vhodné ověřit provokačním testem optimálně s kontrolou placebem. Provokačnímu testu by měla předcházet eliminační dieta.
U pacientů s chronickou kopřivkou je vhodné rutinně vyšetřit krevní obraz s diferenciálním počtem, sedimentaci, C reaktivní protein. Necílené laboratorní testy nejsou doporučovány. Při kopřivkových výsevech opakujících se téměř denně je potravinová alergická reakce I. typu velmi málo pravděpodobná. Je nutno ji ale zvažovat u projevů opakovaně vznikajících v nestejných časových intervalech bez kopřivky, přesahujících dobu 6 týdnů (urticaria acuta intermittens) [15]. Na druhou stranu dietní pseudoalergeny (potraviny bohaté na histamin nebo histaminové liberátory) mohou hrát u chronické kopřivky velkou roli. Mezi potraviny bohaté na histamin patří například červené víno, rybí konzervy (např. tuňák), kyselé zelí. Typickými představiteli histaminových liberátorů, potravin uvolňujících histamin, jsou alkohol, vaječný bílek, ryby nebo jahody. Po těchto potravinách v jídelníčku je nutné cíleně pátrat. Chronické perzistující bakteriální, virové, parazitární nebo mykotické infekce mohou také hrát určitou roli. Přesto vyšetření na fokální infekci, pokud není podpořeno klinickým podezřením, bývá skoro vždy nepřínosné. Helicobacter pylori, streptokoky, stafylokoky, yersinia, Giardia lamblia, Mycoplasma pneumonie, hepatitidy, noroviry, Parvovirus B19, Anisakis simplex, Entamoeba sp., Blastocystis sp. atd. bývají uváděny jako spouštěcí faktory u různých skupin pacientů i v závislosti na různých geografických oblastech. Například infekce Anisakis simplex, což jsou nematoda mořských ryb, je popisována jako častý spouštěč kopřivkových projevů u národů, kde jsou syrové ryby běžnou součástí stravy [17]. Jako častý spouštěč jsou uváděna také nesteroidní antirevmatika a salicyláty [10]. Necílený onkoscreening také není v nejnovějších evropských pokynech doporučován [17]. Chronická spontánní urtikárie může provázet různá imunologicky zprostředkovaná onemocnění, jako jsou tyreopatie, jiná endokrinní onemocnění, inzulin-dependentní diabetes mellitus, revmatoidní artritida, perniciózní anémie, celiakie atd. [3]. Chladová kopřivka, která při koupání ve studené vodě může progredovat až do anafylaktické reakce, může v některých případech provázet například hepatitidy B a C nebo lymfoproliferativní onemocnění. V krvi pacientů s chladovou kopřivkou mnohdy nalézáme kryoglobuliny, chladové aglutininy a kryofibrinogen [3]. Další možné diagnostické testy jsou shrnuty v tabulce 6, vždy ale platí, že rozsáhlá diagnostika musí být podpořena relevantními anamnestickými údaji.
Přesné provedení fyzikálních testů není zcela jasně standardizováno – obr. 2a, 2b. Sledujeme vznik pomfů, erytému nebo svědění, případně angioedému v souvislosti s konkrétním fyzikálním stimulem (chlad, teplo, tlak, fyzická námaha, vibrace) – viz tabulka 6. Ke sjednocení provedení testů u chladové kopřivky byl vyvinut tzv. TempTest a k vyšetření dermografismu u urticaria factitia je možné využít tzv. dermografometr [17]. Tyto přístroje by měly být použity i během klinických studií. Dermografismus můžeme běžně vyšetřit tahem a tlakem tužkovitého předmětu po kůži zad [16]. Fyziologickou reakcí je červený dermografismus, u pacientů s atopickým ekzémem může být přítomen bílý dermografismus. Plastický dermografismus svědčí pro diagnózu urticaria factitia nebo urticaria factitia tarda (latence vzniku 1–8 hodin). Při podezření na tlakovou kopřivku (urticaria mechanica) provádíme tlakový test. Závaží o hmotnosti 2–10 kg upevníme na širokém pruhu přes rameno na dobu 10–30 min, reakci hodnotíme opakovaně za 3–12 hodin [10]. Test s vodou (např. přiložením obvazu smočeného ve vodě o teplotě 36 °C, po dobu 20 minut) může prokázat akvagenní kopřivku. Chladové testy se zkumavkou naplněnou ledem nebo vodou o teplotě 4–10 °C, fixovanou na volární stranu předloktí na 5–10 min, provádíme k ozřejmení chladové kopřivky. Tepelný test prováděný při podezření na lokalizovanou tepelnou kopřivku probíhá obdobně jako chladový test, jen ve zkumavce je voda o teplotě 45 °C. Při námahovém testu necháváme pacienta cvičit do zapocení. Při podezření na solární kopřivku se malá plocha kůže exponuje zdrojem umělého záření (UVA, UVB nebo viditelné světlo) [16].
Table 6. Diagnostické testy u různých typů kopřivek 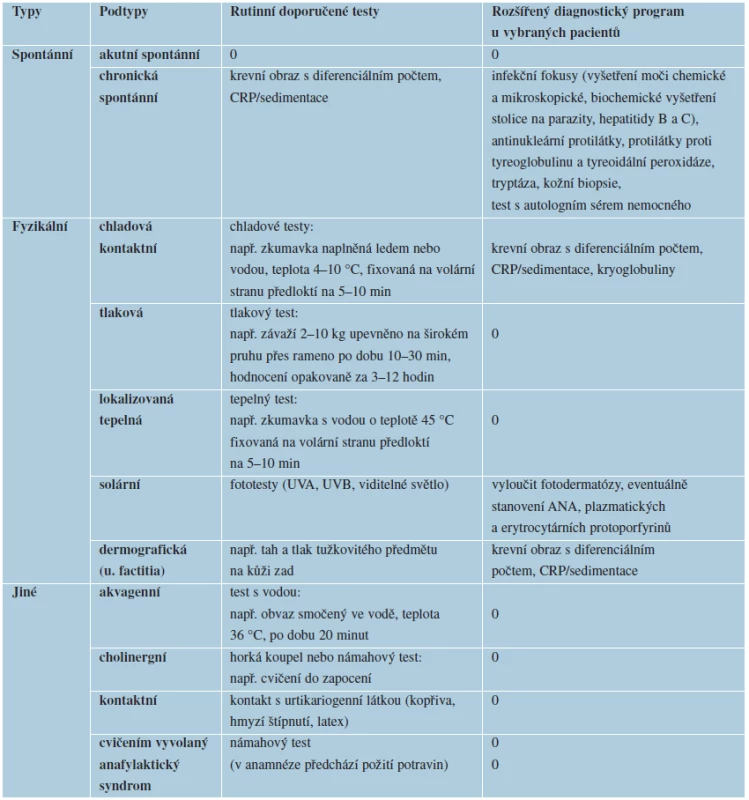
podle EAACI/GA2LEN/EDF/ WAO, 2009 [17] TERAPIE
I přesto, že kopřivka není vždy alergického původu, jsou nesedativní H1 antihistaminika druhé generace lékem první volby u akutní i chronické formy. Pokud je příčina kopřivky známa, je samozřejmě vhodné ji eliminovat (např. při potvrzené potravinové alergii). Přínos diety (s omezením přírodních salicylátů, konzervačních látek, barviv a jiných pseudoalergenů) je u chronické kopřivky kontroverzní a zpravidla nehraje žádnou roli, pokud vliv potravin nebyl prokázán provokačním testem [3]. Bohužel u velké části pacientů vyvolávající faktor zůstává neobjasněn.
V roce 2012 byly doporučené postupy EAACI/ /GA2LEN/EDF/WAO z roku 2009 [18] mírně upraveny především ohledně terapie [10]. Podle nejnovějších pokynů je vhodné při léčbě chronické kopřivky postupovat podle třístupňového algoritmu. První linií léčby jsou nesedativní H1 - antihistaminika druhé generace ve standardním dávkování. U dospělých pacientů, kteří po 2 týdnech nereagují na standardní léčbu, je doporučeno dávku vybraných nesedativních H1 – antihistaminik zvýšit až na čtyřnásobek [10, 18]. Četné studie ukazují, že navýšení dávky nesedativních antihistaminik druhé generace potlačí svědění a tvorbu pomfů účinněji než kombinace více různých druhů antihistaminik [12, 14]. Toto navýšení zatím není doporučeno u dětí [12, 14]. Pokud po 1–4 týdnech, i přes toto navýšení, symptomy dále přetrvávají, je vhodné ke stávající terapii přidat omalizumab, cyklosporin A nebo antagonistu leukotrienů, preparát montelukast. Vzhledem k nedostatku důkazů o účinnosti dapsonu nebo H2-antihistaminik, tyto preparáty již v nejnovějších doporučeních nefigurují [10]. Ke zmírnění akutního výsevu, při exacerbaci chronických kopřivkových projevů nebo při dýchacích obtížích je doporučeno podat krátkodobě (maximálně na 7–10 dní) celkové kortikosteroidy. Kromě H1-antihistaminik ve standardním dávkování (tab. 7) jsou všechny ostatní možnosti léčby „off-label“. V České republice jsou preparáty montelukast (antagonista leukotrienů, SINGULAIR®) a omalizumab (anti IgE protilátka, XOLAIR®) preskripčně omezeny jen pro terapii astmatu. Z dlouhodobé medikace je vhodné vysadit salicyláty a nesteroidní antirevmatika, jelikož mohou působit jako spouštěč kopřivky nebo mohou vést ke zhoršení již probíhajících projevů chronické kopřivky [7]. Při bolestech je možné je nahradit koxiby, selektivními inhibitory cyklooxygenázy II, které urtikárii nezhoršují [7]. Adrenalin aplikovaný intramuskulárně či subkutánně představuje život zachraňující lék při anafylaxi či těžkém laryngálním edému. V tabulce 8 jsou doporučení EAACI/GA2LEN/ /EDF/WAO pro terapii fyzikálních kopřivek. Lokální léčba zahrnuje protisvědivé prostředky např. s 1% mentolem.
Table 7. Antihistaminika – příklady 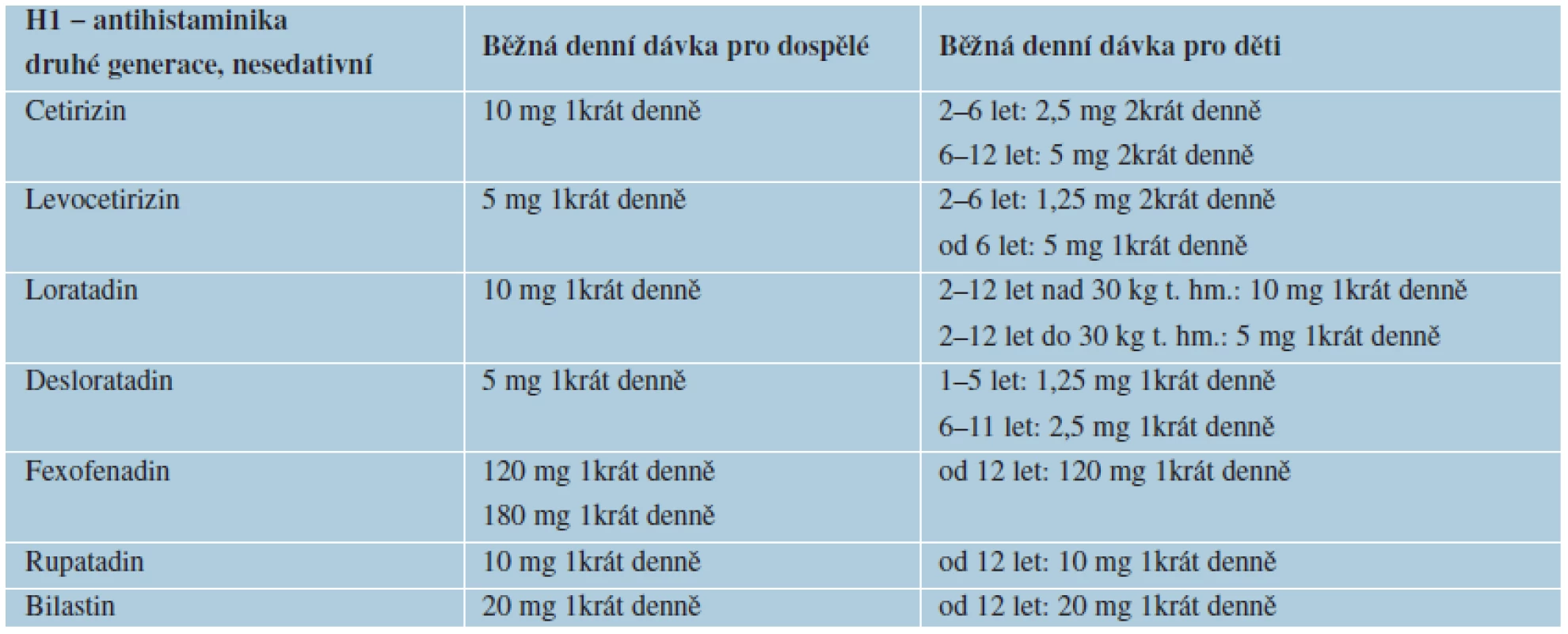
cetirizin (např. ANALERGIN®, ZODAC®, ZYRTEC®), levocetirizin (např. XYZAL®), loratadin (např. CLARITINE®, FLONIDAN®), desloratadin (např. AERIUS®), fexofenadin (např. EWOFEX®), rupatadin (např. TAMALIS®), bilastin (např. XADOS®) Table 8. Terapie fyzikálních kopřivek 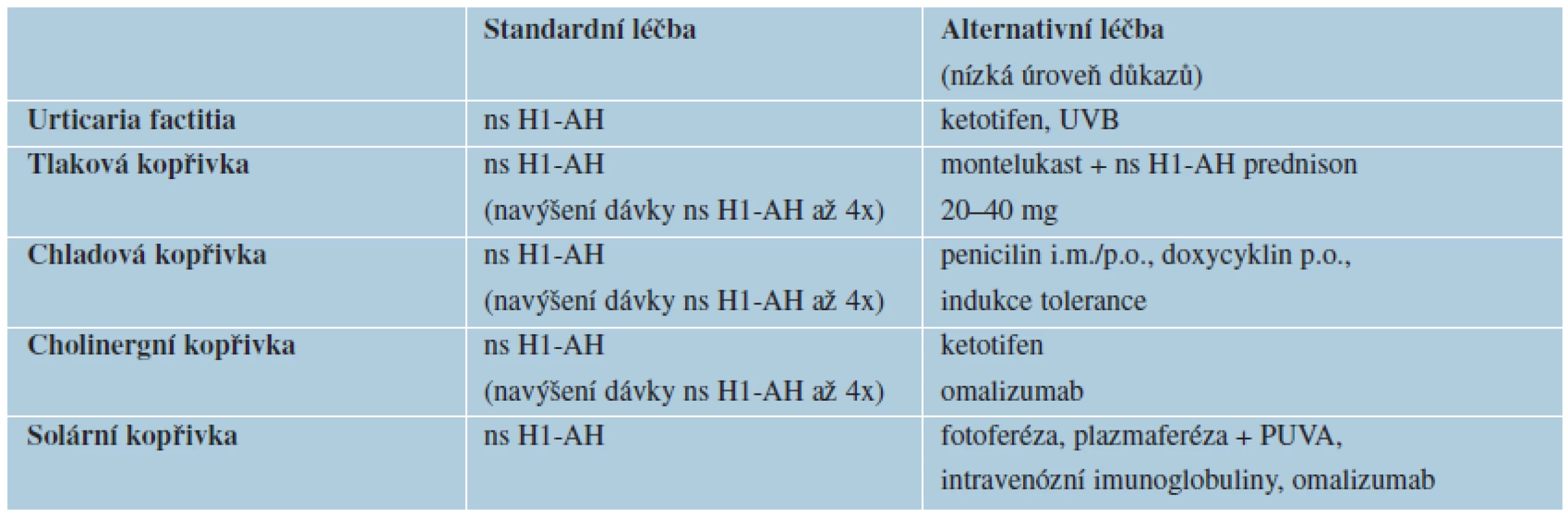
ns H1-AH = nesedativní H1 – antihistaminika ZÁVĚR
Kopřivka je heterogenní skupina chorob, charakterizovaná vznikem kopřivkových pomfů či angioedému. Jde o časté onemocnění. Kopřivka by měla být klasifikována nejprve podle doby trvání, tedy zda se jedná o onemocnění akutní nebo chronické. Chronická kopřivka se dělí do dvou hlavních podskupin podle toho, zda se příznaky objevují spontánně, nebo jsou vyvolány prokazatelným podnětem. Diagnostické laboratorní vyšetřování by mělo vyplývat v první řadě z pečlivé anamnézy. V budoucnu je nutné především optimalizovat léčbu chronické kopřivky. Jako velmi slibná terapeutická možnost pro pacienty s těžkou formou kopřivky ze zdá být anti IgE protilátka omalizumab [3, 5, 11]. Je také nutné standardizovat provedení fyzikálních testů, stejně tak provedení testu s autologním sérem.
Do redakce došlo dne 27. 2. 2014.
Adresa pro korespondenci:
MUDr. Petra Brodská
Dermatovenerologická klinika LF UK a FN Plzeň
Dr. E. Beneše 13
305 99 Plzeň
e-mail: BRODSKAP@fnplzen.cz
Sources
1. AGOSTONI, A., AYGOREN-PURSUN, E., BINKLEY, K. E. et al. Hereditary and acquired angioedema: problems and progress: proceedings of the third C1-esterase inhibitor deficiency workshop and beyond. J. Allergy Clin. Immunol., 2004, 114, p. 51–131.
2. BRODSKÁ, P., SCHMID-GRENDELMEIER, P. Treatment of severe cold contact urticaria with omalizumab: case reports. Case Rep. Dermatol., 2012, 4, p. 275–280.
3. CETKOVSKÁ, P., PIZINGER, K., ŠTORK, J. Kožní změny u interních onemocnění. Grada: Praha 2010, 1. vydání, s. 223–226.
4. HANNON, G. R., WETTER, D. A., GIBSON, L. E. et al. Urticarial dermatitis: Clinical features, diagnostic evaluation, and etiologic associations in a series of 146 patients at Mayo Clinic (2006-2012). J. Am. Acad. Dermatol., 2014, 70, p. 263–268.
5. KAPLAN, A., LEDFORD, D., ASHBY, M. J. et al. Omalizumab in patients with symptomatic chronic idiopathic/spontaneous urticaria despite standard combination therapy. Allergy Clin. Immunol., 2013, 132, p. 101–109.
6. KRAUSE, K., GRATTAN, C. E., BINDSLEV-JENSEN, C. et al. How not to miss autoinflammatory diseases masquerading as urticaria. Allergy, 2012, 67, p. 1465–1474.
7. MASTALERZ, L., SETKOWICZ, M., SZCZEKLIK A. Mechanism of chronic urticaria exacerbation by aspirin. Curr. Allergy Asthma Rep., 2005, 5, p. 277–283.
8. MAURER, M., BINDSLEV-JENSEN, C., GIMENEZ - -ARNAU, A. et al. Chronic idiopathic urticaria (CIU) is no longer idiopathic: time for an update. Br. J. Dermatol., 2013, 168, p. 455–456.
9. MAURER, M., MAGERL, M., METZ, M. et al. Practical algorithm for diagnosing patients with recurrent wheals or angioedema. Allergy, 2013, 68, p. 816–819.
10. MAURER, M., MAGERL, M., METZ, M., ZUBERBIER, T. Revisions to the international guidelines on the diagnosis and therapy of chronic urticaria. J. Dtsch. Dermatol. Ges., 2013. doi: 10.1111/ddg.12194.
11. MAURER, M., ROSÉN, K., HSIEH, H. J. N. et al. Omalizumab for the treatment of chronic idiopathic or spontaneous urticaira. Engl. J. Med., 2013, 7, 368, p. 924–935.
12. MUROTA, H., KATAYAMA, I. Assessment of antihistamines in the treatment of skin allergies. Curr. Opin. Allergy Clin. Immunol., 2011, 11, p. 428–437.
13. SÁNCHEZ-BORGES, M., ASERO, R., ANSOTEGUI, I. J. et al. Diagnosis and treatment of urticaria and angioedema: a worldwide perspective. World Allergy Organ J., 2012, 5, p. 125–147.
14. SIMONS, F. E. R., SIMONS, K. J. Histamine and H1-antihistamines: Celebrating a century of progress. J. Allergy Clin. Immunol., 2011, 128, p. 1139–1150.
15. ŠTORK, J. et al. Dermatovenerologie. Praha: Galén, 2008, s. 131–139.
16. VIKTORINOVÁ, M. Kopřivka a angioedém. Galén: Praha 2001, 1. vydání, s. 57–74.
17. ZUBERBIER, T., ASERO, R., BINDSLEV-JENSEN, C. et al. EAACI/GA2LEN/EDF/WAO guideline: definition, classification and diagnosis of urticaria. Allergy, 2009, 64, p. 1417–1426.
18. ZUBERBIER, T., ASERO, R., BINDSLEV-JENSEN C. et al. EAACI/GA2LEN/EDF/WAO guideline: management of urticaria. Allergy, 2009, 64, p. 1427–1443.
Labels
Dermatology & STDs Paediatric dermatology & STDs
Article was published inCzech-Slovak Dermatology

2014 Issue 2
Most read in this issue- Kopřivka – klasifikace, diagnostika, léčba
- Akutní hemoragický edém dětí – leukocytoklastická vaskulitida
- Proctitis gonorrhoica chronica
- Epidermálna bariéra u atopickej dermatitídy a jej hodnotenie meračom transepidermálnej straty vody
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career



