-
Medical journals
- Career
Léčba hospitalizovaných nemocných s depresí – stačí nám antidepresiva?
Authors: E. Češková
Authors‘ workplace: Psychiatrická klinika LF MU a FN, Brno přednostka prof. MUDr. E. Češková, CSc.
Published in: Čes. a slov. Psychiat., 105, 2009, No. 5, pp. 196-201.
Category: Original Article
Overview
V současné době většinu hospitalizovaných s depresí tvoří těžší a farmakorezistentní deprese. Cílem naší práce bylo zjistit diagnostické spektrum a léčbu hospitalizovaných pacientů s rekurentní depresivní poruchou. Analyzovali jsme retrospektivně chorobopisy hospitalizovaných nemocných od ledna 2005 do prosince 2006 s touto diagnózou. Během sledovaného dvouletého období bylo hospitalizováno 115 nemocných (87 žen a 28 mužů) celkem 150krát. Celkem 79,2 % hospitalizací bylo pro středně těžkou a těžkou depresi, 11 % pro psychotickou depresi. Monoterapie antidepresivy (AD) byla realizována u 52/150 (34,6 %) hospitalizací, monoterapie antipsychotiky u 17/150 (11,3 %). Z AD byl nejvíce užíván mirtazapin a escitalopram, z antipsychotik olanzapin a quetiapin. Kombinace AD byla aplikována u 18/150 (12 %) hospitalizací. Nejčastější kombinací byla kombinace SSRI s mirtazapinem a venlafaxinu s mirtazapinem. Nejužívanější léčebnou strategii představovala augmentace AD atypickými antipsychotiky - u 54/150 (36 %) hospitalizací. Nejčastěji augmentovanými AD byly specifické inhibitory zpětného vychytávání serotoninu a AD byla nejčastěji augmentována olanzapinem a sulpiridem, resp. amisulpridem. Navíc k uvedeným strategiím byla použita augmentace stabilizátory nálady během 36/150 (24 %) a elektrokonvulzivní léčbou 27/150 (18 %) hospitalizací. Průměrné denní dávky olanzapinu a quetiapinu byly při augmentaci nižší než při monoterapií.
Klíčová slova:
rekurentní depresivní porucha, monoterapie, antidepresiva, atypická antipsychotika, augmentace, kombinace.ÚVOD
V současné době, kdy se částečně přesunula diagnostika a léčba depresí do primární linie, se psychiatři setkávají převážně s problematickými depresemi, jak z hlediska diagnostiky, tak terapie. Většinu hospitalizovaných s depresí tvoří těžší a farmakorezistentní deprese.
Dle MKN 10 výzkumných kritérií je závažná deprese definována přítomností minimálně 6 příznaků, včetně 3 základních. Avšak v rutinní klinické praxi je závažnost spíše hodnocena dle intenzity symptomů, nutnosti hospitalizace, somatického syndromu (endogenní deprese dle předchozí klasifikace) a tendencí k suicidálnímu jednání. Závažné deprese se vyskytují u většiny, ne-li u všech hospitalizovaných nemocných s depresí a přibližně u 1/3 ambulantních léčených. Údaje o výskytu závažných (středně těžkých a těžkých dle MKN 10) depresivních epizod nebyl v ČR publikován. Závažné deprese méně reagují na placebo, monoterapii specifickými inhibitory zpětného vychytávání serotoninu (SSRI). Nedaří se dosáhnout ve větší míře remise a je nutné sáhnout k polyterapii [1, 10, 11]. Jsou různé podtypy závažné deprese (rekurentní, „double depression“, melancholie, psychotická, bipolární deprese), častá je v rámci rekurentní deprese. Psychotická deprese, která tvoří 15-19 % depresivních epizod, je vždy považována za závažnou. Většina nebo téměř všechny závažné deprese jsou farmakorezistentní, což odvisí od použité definice farmakorezistence. Nejčastěji v klinické praxi bývá farmakorezistentní deprese definována jako neúspěch dvou (event. jedné) adekvátních léčebných kúr AD. Rezistenci na léčbu lze považovat za určité kontinuum, které začíná nedostatečnou reakcí na první antidepresivum (AD). Pro studie zabývající se touto problematikou je nezbytná exaktnější definice, např. určení stupně rezistence [1]. Dostupné algoritmy léčby těchto stavů doporučují změnu AD, augmentaci nebo kombinaci AD. Je však obecně známo, že realita všedního dne se poněkud liší od doporučovaných postupů.
CÍL STUDIE
Cílem naší práce bylo zmapovat základní klinické charakteristiky a léčbu hospitalizovaných nemocných s rekurentní depresí. Tyto orientační údaje mohou do určité míry odrážet posun ve spektru hospitalizovaných nemocných a používaných léčebných postupech, včetně akceptování stávajících algoritmů.
METODA
Analyzovali jsme retrospektivně chorobopisy konsekutivně hospitalizovaných nemocných na Psychiatrické klinice v Brně od ledna 2005 do prosince 2006 s diagnózou rekurentní deprese (F33 dle MKN 10). Za relevantní byla považována diagnóza při propuštění. Výběr základních klinických charakteristik vycházel z možností standardně vedeného chorobopisu. Pro statistickou analýzu byla použita deskriptivní statistika, t-test a χ2 test.
VÝSLEDKY
Během sledovaného dvouročního období bylo hospitalizováno na Psychiatrické klinice v Brně celkem 115 nemocných (87 žen a 28 mužů) s diagnózou rekurentní depresivní porucha celkem 150x. Charakteristika souboru je uvedena v tabulce 1.
Table 1. Charakteristika souboru nemocných hospitalizovaných s rekurentní depresí. 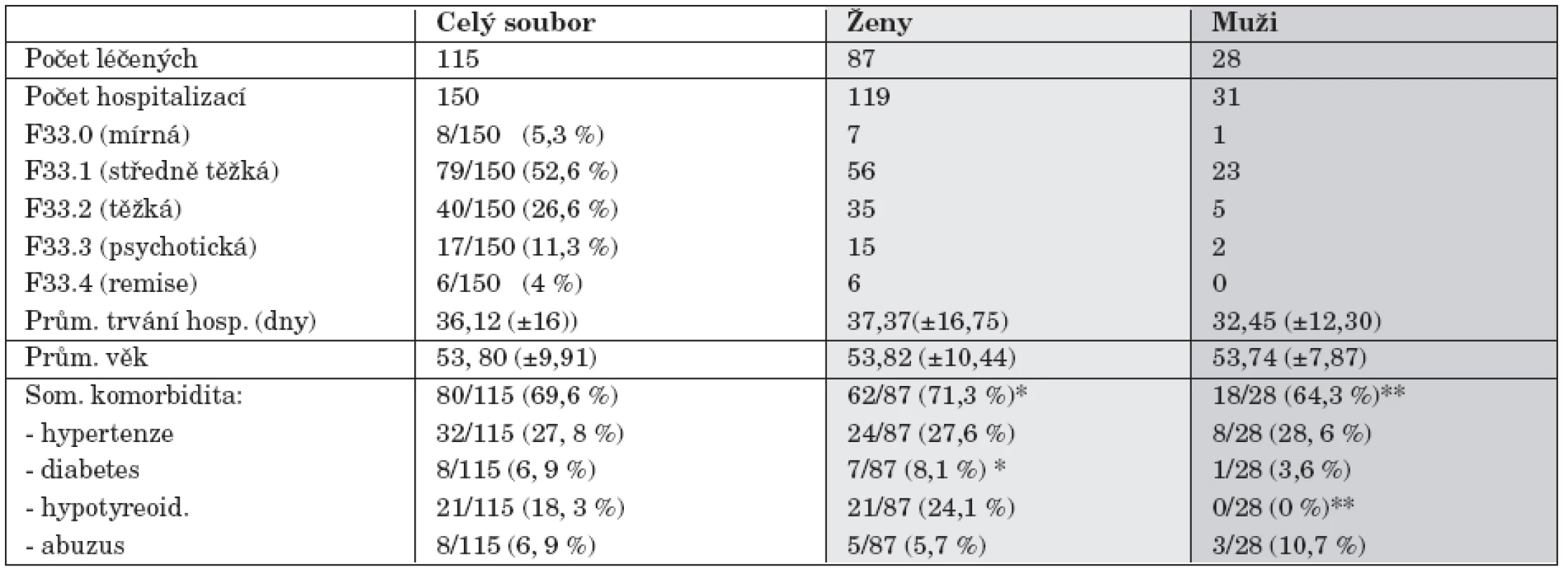
** signif. rozdíl mezi muži a ženami (p<0,01) Celkem 79, 2 % hospitalizací bylo pro středně těžkou nebo těžkou depresi, 11,3 % pro psychotickou depresi, 5,3 % pro mírnou depresi a 4 % hospitalizací byly realizovány v remisi (jednalo se o opakované hospitalizace u jedné nemocné pro aplikaci udržovací elektrokonvulzivní léčby).
Průměrná doba hospitalizace byla 36,1 dní, s kratší dobou u mužů (NS). Průměrný věk byl 53 roků, téměř stejný u mužů a žen. Somatická komorbidita byla vysoká, vyskytovala se u 69,6 % nemocných a výskyt byl signifikantně vyšší u žen než u mužů (p<0,01). Hypertenze byla nejčastěji pozorovanou somatickou komorbiditou u obou pohlaví. Diabetes byl nalezen u 7 % léčených, častěji se vyskytoval u žen. Hypotyreoidismus byl pozorován pouze u žen (p<0,01) a abuzus návykových látek (hlavně alkoholu) byl častější u mužů (NS). Většina nemocných byla hospitalizována s touto diagnózou poprvé nebo podruhé, a to 45,3 % hospitalizací (tab. 2).
Table 2. Pořadí hospitalizací pro diagnózu rekurentní deprese. 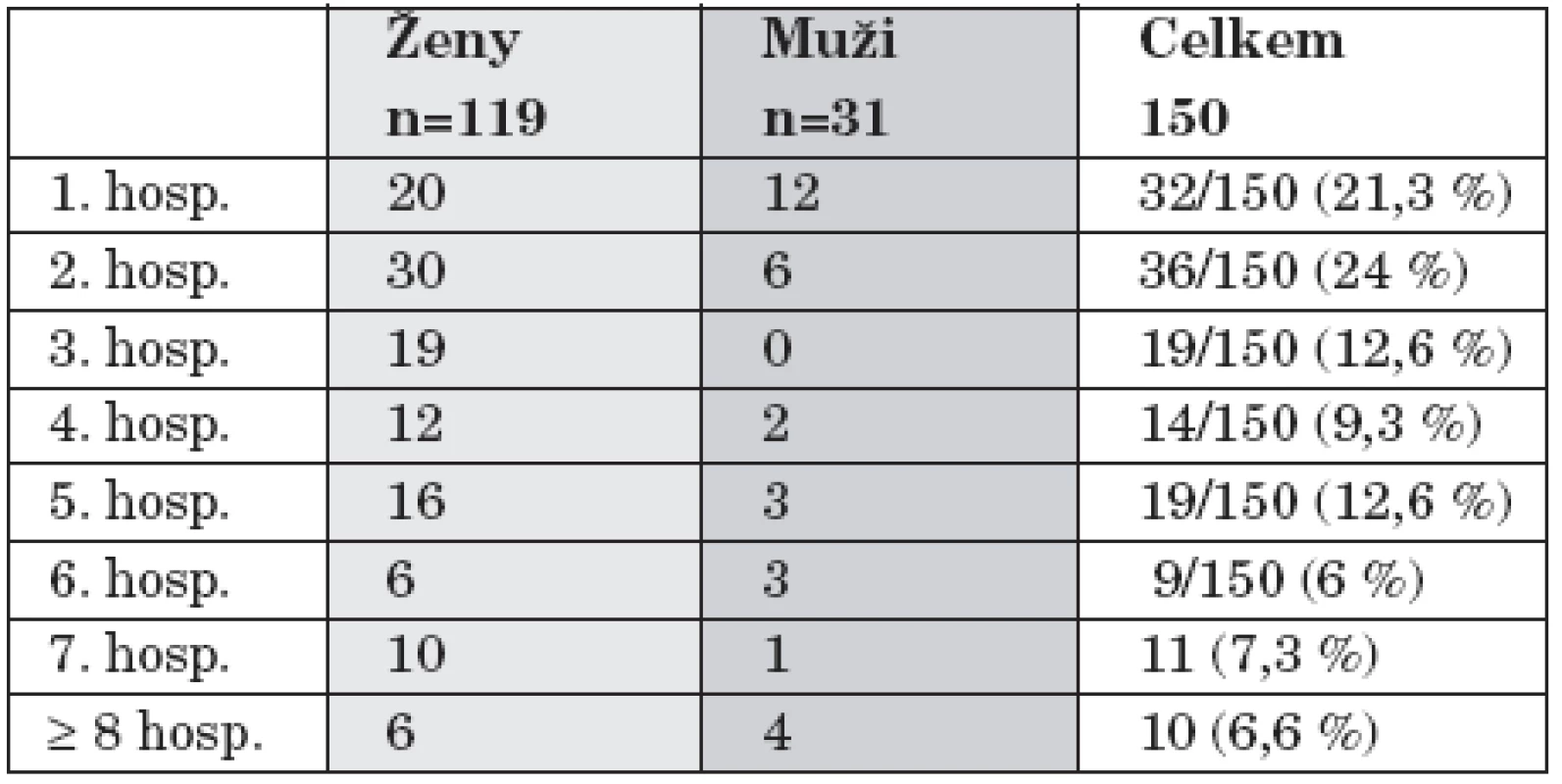
Opakované hospitalizace
24/115 (20, 8 %) nemocných bylo hospitalizováno během sledovaného období opakovaně: 19/24 (78,2 %) 2x, 3/24 (12,5 %) 3x, 1/24 (4,2 %) 4x, 1/24 (4,2 %) 8x. Ženy byly častěji opakovaně hospitalizovány (21/87, 24,1%) než muži (3/28, 10,7 %).
LÉČBA
Monoterapie
Monoterapie AD byla aplikována v průběhu 52/150 (34,6 %) hospitalizací. Nejčastěji byla použita duální AD (27/52, tj. 51, 9 %) a z těchto mirtazapin (během 22 hospitalizací), následovala SSRI (21/52, tj. 40,3 %) s nejčastěji podávaným escitalopramem (při 11 hospitalizacích). Amitriptylin byl podáván v průběhu jedné a trazodon dvou hospitalizací. Monoterapie stabilizátory nálady byla použita v průběhu dvou hospitalizací (tab. 3).
Table 3. Monoterapie antidepresi 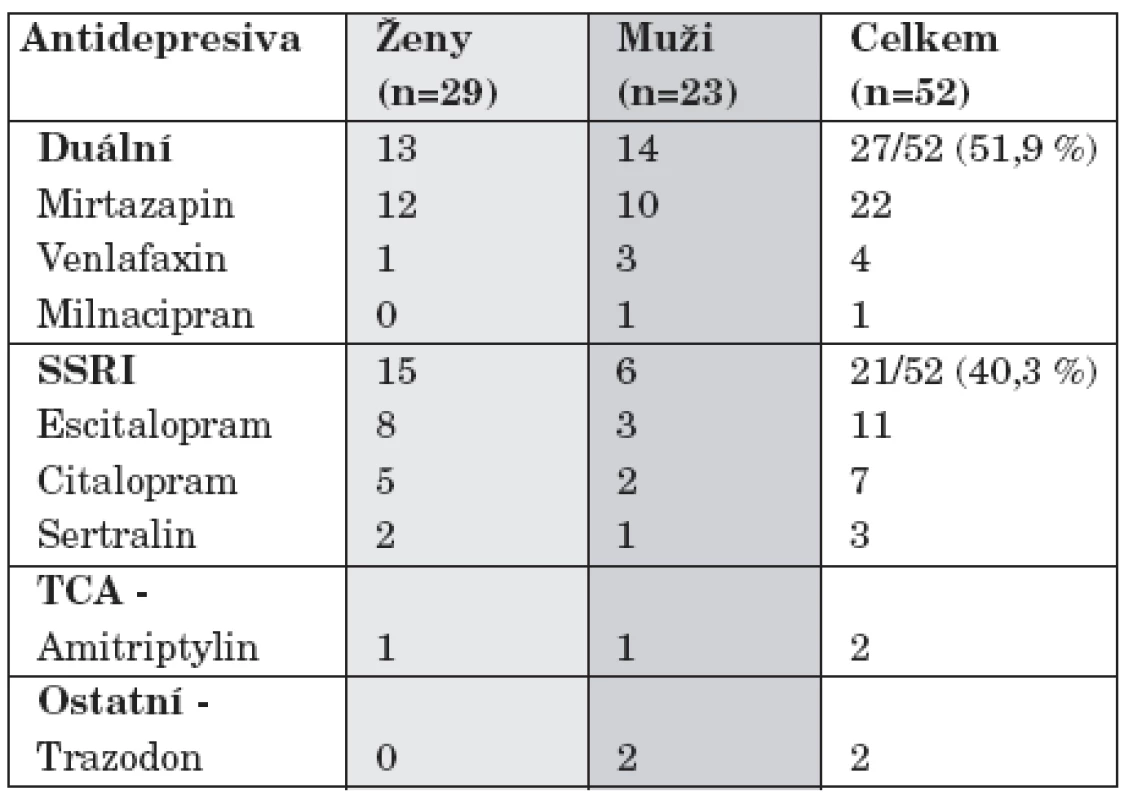
Monoterapie antipsychotiky byla prováděna pouze atypickými antipsychotiky (AAP) během 17/150 (11,3 %) hospitalizací. Nejčastěji užitým AAP byl olanzapin (8/17, 47 %) a quetiapin (5/17, 29,4 %) (tab. 4).
Table 4. Monoterapie atypickými antipsychotiky. 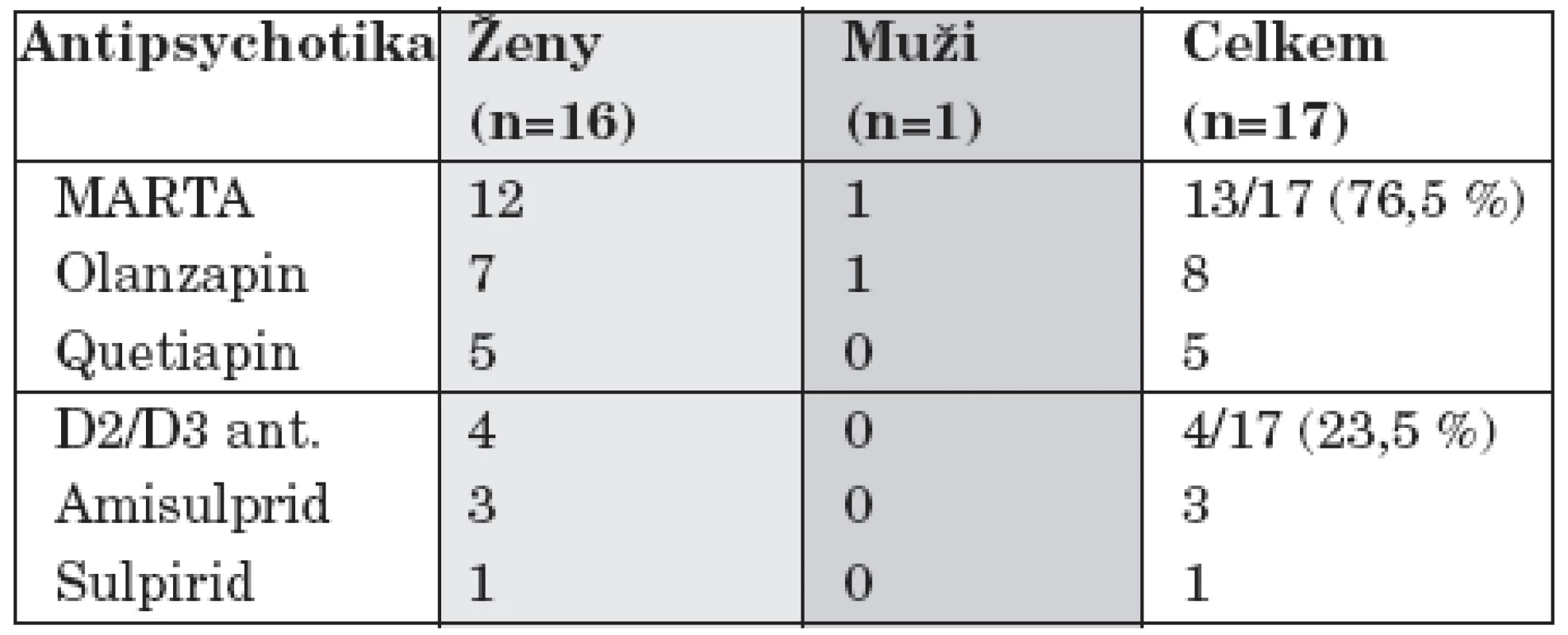
Kombinace AD
Byla použita u 18/150 (12 %) hospitalizací. Nejčastěji byla užita kombinace SSRI s mirtazapinem - 11/18 (61,1 %) a kombinace venlafaxinu s mirtazapinem - 4/18 (22,2 %) hospitalizací (tab. 5).
Table 5. Kombinace antidepresiv 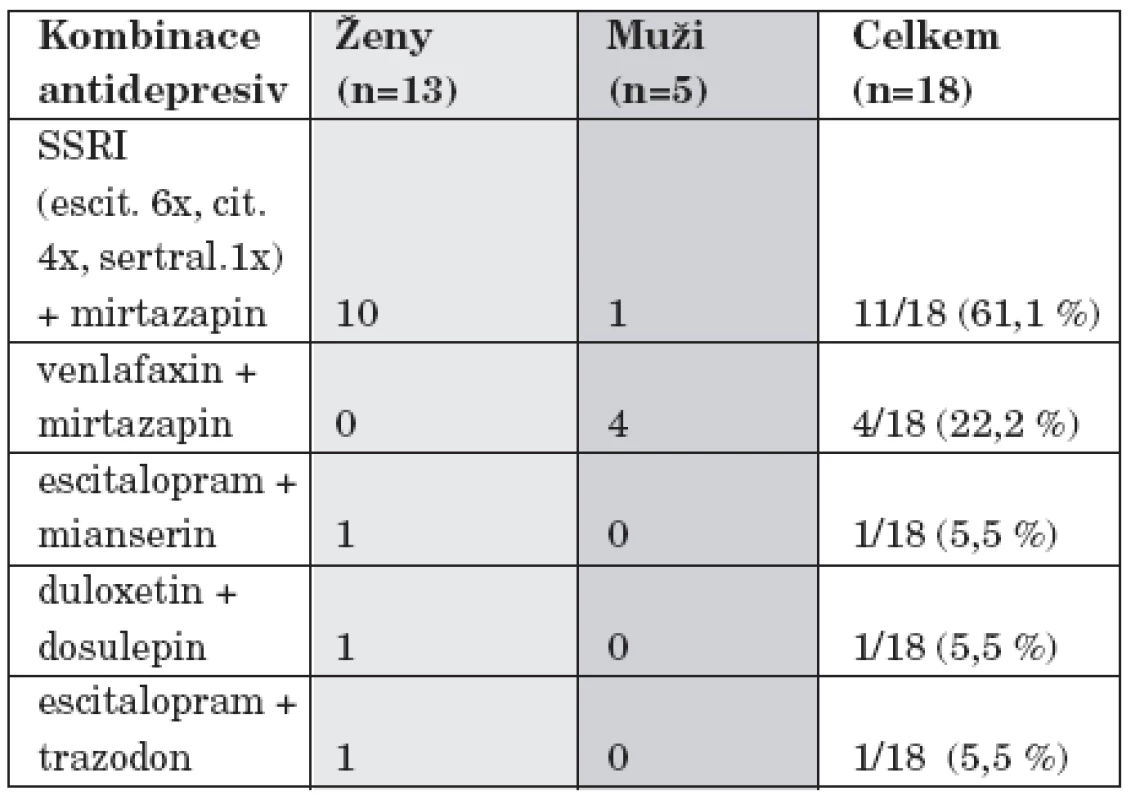
Augmentace
Augmentace AAP byla nejčastější užitou léčebnou strategií - při 54/150 (36 %) hospitalizací. Nejčastěji augmentovanými AD byly SSRI (36/54, 66,6 %). AD byla nejčastěji augmentována olanzapinem (20/54, 37 %) a sulpiridem nebo amisulpridem (17/54, 31,5 %) (tab. 6).
Table 6. Augmentace antidepresiv atypickými antipsychotiky. 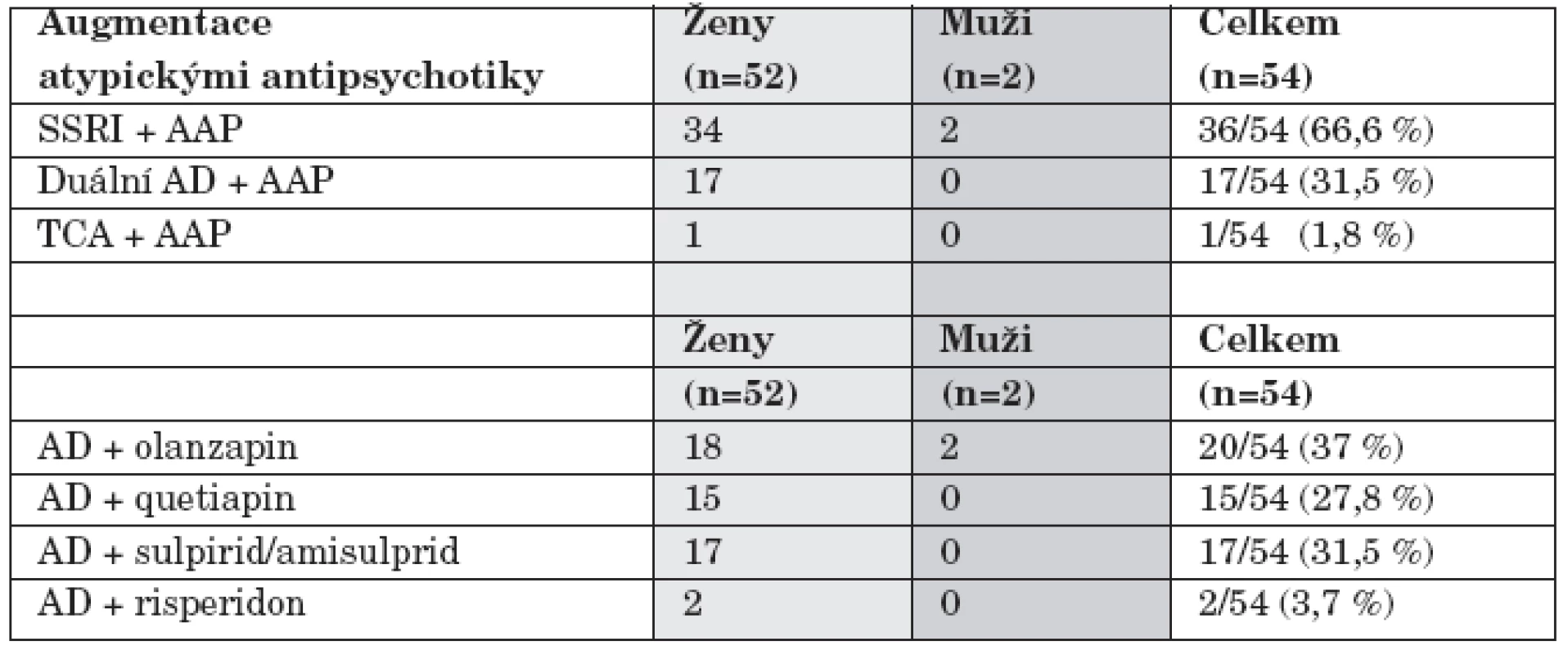
Průměrná denní dávka olanzapinu a quetiapinu při propuštění byla signifikantně nižší při augmentaci ve srovnání s monoterapií (p=0,03, respektive p=0,04). Průměrná denní dávka amisulpridu a sulpiridu při propuštění byla téměř stejná u obou strategií, tj. monoterapii a augmentaci (tab. 7).
Table 7. Průměrné denní dávky atypických antipsychotik. 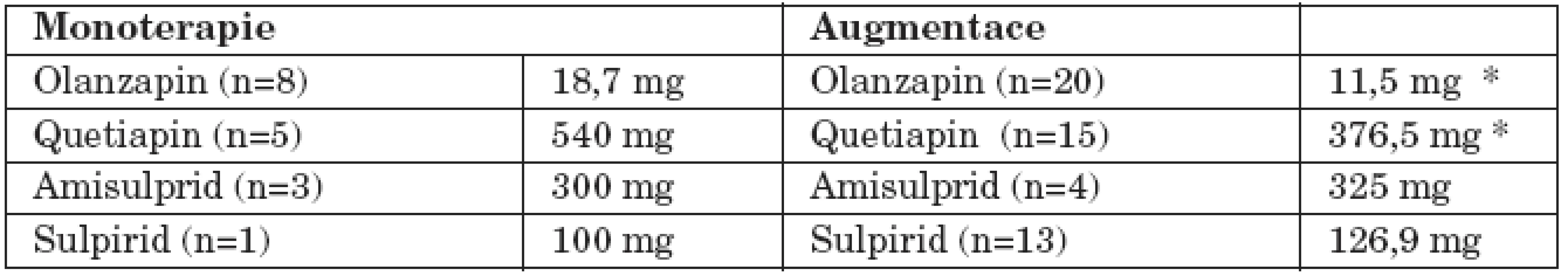
* signif. rozdíl mezi monoterapií a augmentací (p<0,05) Augmentace stabilizátory nálady byla použita u 36/150 (24 %) hospitalizací: lithiem při 15/36 (41,6 %), lamotriginem při 9/36 (25 %), valproátem u 9/36 (25 %) a karbamazepinem u 3/36 (8,3 %) hospitalizací. Augmentace lithiem byla nejvíce použita při augmentaci a současném podávání AD a AAP (v průběhu 8 hospitalizací), augmentace lamotriginem byla nejčastěji použita při monoterapii AD (u 6 hospitalizací). Augmentace farmakoterapie elektrokonvulzivní léčbou byla užita při 27/150 (18 %) hospitalizací.
Bez psychofarmak
U 7/150 (4,6 %) krátkých hospitalizací byla pouze podávána elektrokonvulzivní terapie v rámci udržovací léčby.
DISKUSE
Lze předpokládat, že u většiny našich nemocných se jednalo o závažnou depresi vzhledem k tomu, že vyžadovali hospitalizaci. Nepochybně je možné většinu hospitalizovaných nemocných považovat do určité míry za farmakorezistentní, protože v průběhu ambulantní farmakoterapie neuspěli, i když neúspěch ambulantní léčby není důkazem farmakorezistence. Náš soubor byl také charakterizován vysokou komorbiditou (70%), zvláště u žen. Ženy mají vyšší riziko onemocnění štítné žlázy a korekce preklinického hypotyroidismu tyreoidálními hormony může u depresivních žen k účinnosti přispívat [2]. V našem souboru již byla medikace tyreoidálními hormony zavedena a ženy s ní přicházely k hospitalizaci (21/87 žen, tj. 24,1 %).
Většina nemocných (45,3 %) byla hospitalizována s diagnózou rekurentní depresivní porucha poprvé nebo podruhé. Je známo, že závažnost depresivních epizod stoupá v průběhu choroby [15]. Můžeme spekulovat, že nemocní byli úspěšně léčeni v průběhu prvních epizod ambulantně a s následnými epizodami se deprese stávala závažnější a terapeuticky hůře zvládatelná.
U našeho souboru hospitalizovaných nemocných byla v rámci monoterapie nejčastěji užita duální AD s mirtazapinem na prvním místě. I když jsme v rámci této retrospektivní analýzy nehodnotili předchozí ambulantní léčbu, lze předpokládat, že většina již byla SSRI léčena, a proto léčba duálními AD se širším mechanismem účinku se jeví opodstatněná. Metaanalýza srovnávající záměnu AD v rámci skupiny oproti změně za jinou skupinu ukázala u depresivních nemocných rezistentních na SSRI významně vyšší výskyt remisí při změně na AD jiné skupiny než na jiné SSRI [21]. Dalším často užitým AD byl escitalopram. Escitalopram je alosterický inhibitor zpětného vychytávání serotoninu a účinností se blíží spíše duálním AD [20]. Z metaanalýz srovnávajících účinnost inhibitorů zpětného vychytávání serotoninu a noradrenalinu (SNRI) a SSRI vyplynulo, že venlafaxin je o něco účinnější než skupina SSRI (rozdíly v dosažení remisí 5-1%) a rozdíl oproti escitalopramu prokázán nebyl [22].
Při monoterapii antipsychotiky byla užita výhradně AAP, nejčastěji olanzapin, dále quetiapin a amisulprid v nižších dávkách. V publikovaných kontrolovaných studiích byla augmentace fluoxetinu olanzapinem účinnější než monoterapie olanzapinem [25, 26]. Byly již provedeny placebem kontrolované studie s úspěšným podáváním quetiapinu XR u velké deprese, zatím však nebyly publikovány in extenzo a byly pouze prezentovány ve formě posterů nebo sdělení [3]. Antidepresivní efekt nižších dávek amisulpridu je již znám dlouho a je v praxi často využíván [6].
Lepší snášenlivost novějších AD vedla k častějšímu užívání kombinací AD. Nejčastější byla kombinace SSRI nebo venlafaxinu s mirtazapinem. Účinnost této kombinace byla potvrzena malými, dvojitě slepými kontrolovanými studiemi [5, 14]. Kombinace AD s různými mechanismy účinku je považována za racionální polyfarmacii, avšak zatím je nedostatek větších, placebem kontrolovaných studií.
Nejvíce užívanou strategií byla augmentace AD AAP. Z komplexního receptorového vazebného profilu AAP, jejich účinku na neurotransmitéry, regionální aktivity a neuroplastických vlastností lze usuzovat na jejich vlastní antidepresivní aktivitu. Tato léčebná strategie má také nejvíce důkazů účinnosti. Metaanalýza dvojitě slepých, randomizovaných, placebem kontrolovaných studií (10 studií, n=1500), publikovaných od r. 1980, ukázala dosažení remise u 47,4 % při augmentaci, vs. 22,3 % při kombinaci s placebem [23]. Od té doby vyšly další kontrolované studie poukazující na úspěšnou augmentaci quetiapinem [8], risperidonem [16, 18] a nedávno také aripiprazolem [4, 17, 19] při léčbě akutní depresivní epizody. Výhody AAP zahrnují vlastní antidepresivní aktivitu a mohou zvládat úzkost a agitovanost. Nevýhodou je snášenlivost a cena, avšak v našem souboru při augmentaci byly průměrné dávky olanzapinu a quetiapinu nižší než průměrné dávky při monoterapii. Dávky sulpiridu a amisulpridu byly podobné u obou strategií. Toto není překvapující, protože antidepresivní efekt byl prokázán při podávání nízkých dávek jak sulpiridu tak amisulpridu [6, 7]. Zatím není zcela jasné, zda užití nízkých dávek AAP je spojeno i s nižším výskytem metabolických nežádoucích účinků. Některá data naznačují, že přírůstek hmotnosti souvisí s dávkou, přinejmenším při podávání olanzapinu a quetiapinu, konzistentní data chybí. U části sledovaných nemocných jsme měli k dispozici i údaje o hmotnosti při přijetí a při propuštění, ze kterých vyplynulo, že k přírůstku hmotnosti docházelo nejčastěji na augmentaci AAP již v rámci akutní léčby.
Při augmentaci stabilizátory nálady byla v našem souboru nejčastěji použita augmentace lithiem. Augmentace lithiem je doporučována ve většině algoritmů léčby jako hlavní léčebná strategie u nemocných, kteří nereagují na monoterapii AD. Ve dvou nedávno publikovaných metaanalýzách byla augmentace lithiem signifikantně účinnější než augmentace placebem (40% vs. 17%), avšak většina studií byla malá [9]. V literatuře jsou údaje, které podporují také augmentaci lamotriginem [13]. V menší otevřené studii byla přídatná léčba lamotriginem k AD stejně účinná jako augmentace lithiem. Je zapotřebí větší, placebem kontrolované studie [24]. Účinnost elektrokonvulzivní terapie je obecně známa. Také použití více augmentačních přístupů pouze potvrzuje, že se jednalo o závažné, farmakorezistentní deprese.
Interpretace uvedených dat je limitována metodikou studie. Jednalo se o retrospektivní analýzu chorobopisného materiálu. Hospitalizace, diagnostika a léčba nemocných probíhala v naturalistických podmínkách akutních lůžkových oddělení psychiatrické kliniky. Řada dalších klinických charakteristik, které jsou relevantní pro volbu léčby, nebyla standardně uváděna a nebylo možné je využít.
ZÁVĚRY A SHRNUTÍ
Naše výsledky jsou v souhlase s představou, že pro depresivní poruchu jsou hospitalizováni zvláště nemocní s větším počtem prodělaných epizod a vysokou komorbiditou. Augmentace AD AAP představuje stále častěji užívanou strategii v léčbě závažné deprese a deprese nereagující na ambulantní léčbu, což je ve shodě s aktuálními algoritmy léčby. Výhody AAP jsou v tom, že některá z nich mají vlastní vnitřní antidepresivní efekt a mohou zvládat anxietu a agitovanost. Nevýhodou zvláště při dlouhodobém podávání mohou být nežádoucí vedlejší účinky a cena, i když průměrné dávky olanzapinu a quetiapinu byly nižší než v monoterapii AP. Kombinace AD jsou další častou léčbou. Kombinace AD s různými mechanismy je možné považovat za racionální polyfarmacii, ale chybí větší, placebem kontrolované údaje. Tento přístup umožnila dostupnost nových AD.
Prof. MUDr. Eva Češková, CSc.
Psychiatrická klinika LF MU aFN
Jihlavská 20
625 00 Brno
Sources
1. Anderson, I. M., Ferrier, I. N., Baldwin, R. C. et al.: Evidence-based guidelines for treating depressive disorders with antidepressants: a revision of the 2000 British Association for Psychopharmacology guidelines. J. Psychopharmacol., 22, 2008, pp. 343-396.
2. Altschuler, L. L., Bauer, M., Frye M. et al.: Does thyreoid supplementation accelerate tricyclic antidepressant response? A review and meta-analysis of the literature. Am. J. Psychiatry, 158, 2001, pp. 1617-1622.
3. Bauer, M., Nizar El-Khalili, N., Liebowitz, M. et al.: Extended release quetiapine fumarate (QNuetiapine XR) as adjunct to antidepressant therapy in patients with major depressive disorder (MDD): A Pooled Analysis of Studies MDD 6 (Pearl) and MDD 7 (Onyx). Postere prezentovaný na 47. ACNP (American College of Neuropsychopharmacology, 47th Annual Meeting), 7.-11. 12. 2008, Scottsdale, Arizona
4. Berman, R. M., Marcus, R. N., Swanink, R. et al.: The efficacy and safety of aripiprazole as adjunctive therapy in major depressive disorder: a multicenter, randomized, double-blind, placebo-controlled study. J. Clin. Psychiatry, 68, 2007, pp. 843-853.
5. Carpenter, L. L., Yasmin, S., Price, L. H.: A double-blind, placebo-controlled study of antidepressant augmentation with mirtazapine. Biol. Psychiatry, 51, 2002, pp. 183-188.
6. Česková E.: Amisulprid – nové benzamidové antipsychotikum II. generace. (Souhrnné sdělení). Čes. a slov. Psychiat., 96, 2000, s. 418-415.
7. Češková, E.: Deniban v léčbě dystymie. Čes. a slov. Psychiat. 103, 2007, s. 73-79.
8. Chaput, Y., Mangan, A., Gendron, A.: The co-administration of quetiapine or placebo to cognitive-behavior therapy in treatment refractory depression: a preliminary trial. BMC Psychiatry 28, 2008, p. 73.
9. Crossley, N. A., Bauer, M.: Acceleration and augmentation of antidepressants with lithium for depressive disorders: two meta-analyses of randomized, placebo-controlled trials. J. Clin. Psychiatry, 68, 2007, pp. 935-940.
10. Danish University Antidepressant Group (DUAG): Citalopram: clinical effect profile in comparison with clomipramine. A controled multicenter study. Psychopharmacology, 90, 1986, pp. 131-138.
11. Danish University Antidepressant Group (DUAG): Paroxetine: a selective serotonin reuptake inhibitor showing better tolerance, but weaker antidepressant effect than clomipramine in controlled multicenter study. J. Affect. Disord., 18, 1990, pp. 289-299.
12. Fava, M.: Diagnosis and definition of treatment-resistant depression. Biol. Psychiatry, 15, 2003, pp. 649-659.
13. Gutierrez, R. L., McKercher, R. M., Galea, J., Jamison, K. L.: Lamotrigine augmentation strategy for patients with treatment-resistant depression. CNS Spectr., 10, 2005, pp. 800-805.
14. Hannan, N., Hamzah, Z., Akinpeloye, H. O., Meagher, D.: Venlafaxine –mirtazapine combination in the treatment of persistent depressive illness. J. Psychopharmacol, 21, 2007, pp. 161-164.
15. Leasing, L. V.: Severity of depressive episodes during the course of depressive disorder. Br. J. Psychiatry, 192, 2008, pp. 290-293.
16. Keitner, G. I., Garlow, S. J., Ryan, C. E. et al.: A randomized, placebo.controlled trial of risperidone augmentation for patients with difficult-to treat unipolar, non-psychotic major depression. J. Psychiatr. Res., 43, 2009, pp. 205-214.
17. Khan, A.: The efficacy and safety of aripiprazole s adjunctive therapy in major depressive disorder: A multicenter, randomized, double-blind, placebo-controlled study. J. Clin. Psychiatry, 68, 2007, pp. 843-853.
18. Mahnoud, R. A., Pandina, G. J., Turkoz, I. et al.: Risperidone for treatment–refractory major depressive disorder: a randomized trial. Ann. Intern. Med., 147, 2007, pp. 593-602.
19. Marcus, R. N., McQuade, R. D., Carson, W. H. et al.: The efficacy and safety of aripiprazole as adjunctive therapy in major depressive disorder. A second multicenter, randomized, double blind, placebo-controlled study. J. Clin. Psychoparmacol., 28, 2008, pp. 156 -65.
20. Miller, B.: Escitalopram versus serotonin reuptake inhibitors. Encephale, 34, 2008, pp. 280-283.
21. Papakostas, G. I., Fava, M., Thase, M. E.: Treatment of SSRI-resistant depression: a meta-analysis comparing within–versus across-class switches. Biol. Psychiatry, 63, 2008, pp. 699-704.
22. Papakostas, G. I., Thase, M. E., Fava, M. et al.: Are antidepressant drugs that combine serotonergic and noradrenergic mechanisms of action more effective than the selective serotonin reuptake inhibitors in treating major depressive disorder? A meta-analysis of studies of newer agents. Biol. Psychiatry, 62, 2007, pp. 1217-1227.
23. Papakostas, G. I., Shelton, R. C., Smith, J., Fava, M.: Augmentatin of antidepressants with atypical antipsychotic medications for treatment –resistant major depressive disorder. A meta-analysis. J. Clin. Psychiatry, 68, 2007, pp. 224-236.
24. Schindler, F., Anghelescu, I. G.: Lithium versus lamotrigine augmentation in treatmetn resistant unipolar depression. A randomized, open-label study. Int. Clin. Psychopharmacol., 22, 2007, pp. 179-182.
25. Shelton, R. C., Williamson, D., Corya, S. A. et al.: Olanzapine/fluoxetine combination for treatment resistant depression. A controlled study of SSRI and nortriptyline resistance J. Clin. Psychiatry, 66, 2005, pp. 1289-1297.
26. Thase, M. E., Corya, S. A., Osuntokun, O. et al.: A randomized, double-blind comparison of olanzapine/fluoxetine combination, olanzapine, and fluoxetine in treatment-resitant major depressive disorder. J. Clin. Psychiatry, 68, 2007, pp. 224-236.
Labels
Addictology Paediatric psychiatry Psychiatry
Article was published inCzech and Slovak Psychiatry

2009 Issue 5
Most read in this issue- Léčba hospitalizovaných nemocných s depresí – stačí nám antidepresiva?
- Komorbidita bipolární afektivní poruchy s jinými psychickými poruchami
- Schizofrenie v dětství a adolescenci
- Užívání těkavých látek v České republice – souhrn dostupných údajů
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

