-
Medical journals
- Career
Kvalita života u soběstačných pacientů po cévní mozkové příhodě
Authors: T. Fadrná 1,2; D. Školoudík 1
Authors‘ workplace: Ústav ošetřovatelství, FZV UP v Olomouci 1; Neurochirurgická klinika, LF OU a FN Ostrava 2
Published in: Cesk Slov Neurol N 2017; 80/113(3): 323-327
Category: Original Paper
doi: https://doi.org/doi: 10.14735/amcsnn2017csnn.eu1Overview
Cíl:
Cílem studie bylo zjistit, zda se liší kvalita života u soběstačných pacientů po cévní mozkové příhodě (CMP) ve srovnání s kontrolní skupinou.Soubor a metodika:
Do studie byli zařazeni soběstační pacienti, dispenzarizovaní v neurosonologické laboratoři pro stenózu karotické tepny, ve věku 50 – 80 let, kteří v posledním roce neprodělali CMP ani jiné závažné onemocnění, neměli demenci, depresi nebo jiné psychiatrické onemocnění a podepsali informovaný souhlas. Pacienti s CMP v anamnéze byli zařazeni do skupiny A, ostatní pacienti byli zařazeni do kontrolní skupiny B. Všichni pacienti vyplnili dva standardizované dotazníky kvality života (WHOQOL-BREF, EQ-5D-3L).Výsledky:
Z 584 konsekutivních pacientů splnilo zařazovací kritéria 504 pacientů, z nichž 344 vyplnilo kompletně oba dotazníky kvality života – 145 pacientů po CMP (78 mužů, věk 70,4 ± 7,0 let), 199 pacientů v kontrolní skupině (86 mužů, věk 68,9 ± 8,3 let). Pacienti po CMP se od pacientů v kontrolní skupině nelišili v žádné doméně dotazníku WHOQOL-BREF – fyzické zdraví (p = 0,09), psychologická stránka (p = 0,45), sociální vztahy (p = 0,34), prostředí (p = 0,45); v hodnocení kvality života (p = 0,16), hodnocení současného zdravotního stavu (p = 0,57), spokojenosti se zdravotním stavem (p = 0,44), pohyblivosti (p = 0,22), sebeobsluze (p = 0,07), běžných denních činnostech (p = 0,23), bolesti (p = 0,53) ani úzkosti (p = 0,63).Závěr:
Soběstační pacienti po CMP nemají zhoršenou kvalitu života.Klíčová slova:
cévní mozková příhoda – kvalita života – dotazník – zdravíÚvod
Cévní mozková příhoda (CMP) je třetí nejčastější příčina úmrtí a nejčastější příčina invalidizace nejen v České republice, ale i v dalších evropských zemích [1]. Epidemiologická analýza předpokládá, že v roce 2015 postihla CMP celosvětově 15 miliónů lidí, což zahrnuje enormní náklady na léčbu [2,3]. Každý šestý pacient na následky CMP umírá, dalších 50 % pacientů zůstává po CMP nesoběstačných a jen 10 % pacientů přežívá zcela bez následků [4,5]. Díky pokroku v akutní léčbě (intravenózní trombolýza, endovaskulární léčba, neurointenzivní péče) dochází ke snížení úmrtnosti a počtu nesoběstačných pacientů po CMP, avšak i přes maximální léčbu je šance na plnou soběstačnost jen okolo 50 % [5–8].
Motorická postižení a postižení řeči však nejsou jedinými limitujícími následky po CMP [4]. Demence, deprese, inkontinence a další nemotorické potíže jsou relativně časté problémy u pacientů po CMP, které mohou významně zhoršovat kvalitu života takto postižených osob. Vyskytují se u 40–70 % pacientů po CMP [9,10]. Běžně používané testy hodnotící motorické postižení a soběstačnost těchto pacientů, např. NIHSS škála, Scandinavian Stroke Scale, modifikovaná Rankinova škála (mRS), Barthelové index a další jsou schopny hodnotit pouze fyzické, resp. funkční postižení, ale nezohledňují vlastní vnímání svého zdraví, mentální a emoční stránky postižení pacientů [11,12]. Proto se hodnocení kvality života stává běžným nástrojem pro evaluaci účinnosti léčby a následků po CMP.
Cílem projektu bylo zjistit, zda neinvalidizující CMP zhoršuje kvalitu života. Nulová hypotéza předpokládá, že neexistuje rozdíl v jednotlivých doménách kvality života mezi pacienty, kteří prodělali CMP, avšak zůstali soběstační a mezi pacienty bez CMP v anamnéze.
Materiál a metodika
Jedná se o prospektivní kvantitativní průřezovou výzkumnou studii se standardizovanými dotazníky World Health Organization Quality of Life short version (WHOQOL-BREF) a EuroQol-5D (EQ-5D-3L). Pro zjištění jak obecných aspektů kvality života respondentů, tak i specifických aspektů u pacientů po CMP byl pro hodnocení kvality života vybrán jeden obecný dotazník (WHOQOL-BREF) a jeden specifický dotazník pro pacienty po CMP (EQ-5D-3L). Pro omezení vlivu dalších faktorů byla vybrána cílová skupina z pacientů v primární a sekundární prevenci CMP, kteří mají diagnostikováno aterosklerotické postižení krčních tepen a jsou v dispenzarizaci v neurosonologické laboratoři.
Soubor tvoří dvě skupiny pacientů s aterosklerotickým postižením krčních tepen. Do skupiny A byli zařazeni soběstační pacienti s aterosklerotickým postižením krčních tepen, kteří prodělali CMP. Do skupiny B (kontrolní skupiny) byli zařazeni soběstační pacienti s aterosklerotickým postižením krčních tepen, kteří nikdy CMP neprodělali.
Studie byla provedena ve shodě s Helsinskou deklarací z roku 1975 (revize 2004 a 2008) a schválena lokální etickou komisí Fakulty zdravotnických věd Univerzity Palackého v Olomouci (UPOL-7279/1040-2016). Všichni pacienti podepsali informovaný souhlas.
Pacienti
Do studie byli v průběhu 3 měsíců zařazeni pacienti dispenzarizovaní v neurosonologické laboratoři, kteří splnili následující vstupní kritéria:
- a) soběstačnost s mRS 0–2 body,
- b) dispenzarizace v neurosonologické laboratoři pro stenózu karotické tepny nad 20 % (dle metodiky studie ECST),
- c) věk 50–80 let (vč.),
- d) podpis informovaného sou
Vylučující kritéria byla:
- a) závažné onemocnění vč. CMP v posledních 12 měsících;
- b) demence s Mini-Mental State Examination ≤ 25 bodů;
- c) psychiatrické onemocnění vč. deprese;
- d) těžké postižení zraku nebo sluchu neumožňující vyplnění dotazníků kvality života;
- e) onemocnění v terminálním stadiu s pravděpodobnou dobou přežití méně než 2 roky;
- f) aktivní onkologické onemocnění;
- g) pobyt v domově pro seniory, domově s pečovatelskou službou nebo hospitalizace ve zdravotnickém zařízení vč. hospice či léčebny dlouhodobě nemocných.
Dotazníky
Po zařazení do studie pacienti vyplnili dva standardizované dotazníky kvality života.
Z dotazníků mapujících celkovou kvalitu života byl vybrán dotazník WHOQOL-BREF (krátká verze), který obsahuje 26 otázek zaměřených na faktory ovlivňující kvalitu života. Dvě samostatné otázky posuzující kvalitu života a zdraví a 24 otázek ze čtyř domén – fyzického zdraví, psychologické, sociálních vztahů a prostředí. Každé otázce byla přiřazena pětibodová Likertova škála, na které respondent hodnotil, jak jednotlivé faktory ovlivňují kvalitu jeho života. Pro vyhodnocení jednotlivých domén kvality života bylo použito doménové skóre:
Skóre domény fyzického zdraví = ((6 – – Q3) + (6 – Q4) + Q10 + Q15 + Q16 + Q17 + + Q18) × 4.
Skóre psychologická domény = (Q5 + Q6 + + Q7 + Q11 + Q19 + (6 – Q26)) × 4.
Skóre domény sociálních vztahů = (Q20 + + Q21 + Q22) × 4.
Skóre domény prostředí = (Q8 + Q9 + + Q12 + Q13 + Q14 + Q23 + Q24 + Q25) × 4.Oficiální česká verze dotazníku byla použita se souhlasem The World Health Organization.
Ze specifických dotazníků určených pro pacienty po CMP byl použit dotazník EQ-5D-3L, který obsahuje pět domén kvality života respondenta – pohyblivost, sebeobsluha, zvládání běžných činností, bolest a deprese. Ke každé otázce je možno vybrat jednu ze tří odpovědí (1 – bez potíží/žádná, 2 – s potížemi/střední, 3 – neschopen/extrémní), které hodnotí závažnost vlivu jednotlivých faktorů na kvalitu života. Jako poslední je 100bodová škála, na které respondent určí současnou úroveň zdravotního stavu (0 – nejhorší stav, který si lze představit, 100 – nejlepší stav, který si lze představit). Oficiální česká verze dotazníku byla použita se souhlasem EuroQol Research Foundation.
Klinické vyšetření
Před zařazením do studie byly provedeny u všech pacientů testy Mini-Mental State Examination a Mini-International Neuropsychiatric Interview k vyloučení demence a deprese. Po splnění vstupních a vylučujících kritérií vyplnili pacienti zařazení do studie vizuální analogovou škálu bolesti, byla zaznamenána anamnestická data vč. aktivních a proběhlých onemocnění, užívaných léků, věku, pohlaví, vzdělání a sociální situace pacienta – zda má partnera a s kým bydlí. Bylo provedeno fyzikální vyšetření se změřením krevního tlaku, výšky a váhy pacienta s vypočtením body mass indexu, neurologické vyšetření se zhodnocením soběstačnosti pomocí mRS a neurosonologické vyšetření se změřením procenta stenózy v karotických tepnách.
Cílové parametry pro statistickou analýzu
Primární endpoint bylo hodnocení kvality života ve čtyřech doménách dotazníku WHOQOL-BREF a pěti doménách dotazníku EQ-5D-3L. Sekundárními endpointy bylo hodnocení celkové kvality života a zdraví z dotazníku WHOQOL-BREF a hodnocení současného zdravotního stavu z dotazníku EQ-5D-3L.
Velikost souboru byla stanovena k průkazu statisticky významného rozdílu v minimálně jedné doméně kvality života mezi skupinou A a kontrolní skupinou B, a to min. o 0,5 bodu v Likertově škále. Dle výpočtu byl určen minimální počet respondentů v každé skupině 138 při hladině alfa = 0,05 a síle (beta) 80 %. Při předpokladu 60 % návratnosti dotazníků a max. 10 % inkompletně vyplněných dotazníků byl stanoven počet oslovených respondentů v každé skupině (A i B) na 252.
Statistika
Demografická data jsou uvedena formou průměru a směrodatné odchylky nebo počtu a percentuálního zastoupení. Pro statistické srovnání demografických dat v obou skupinách byl použit Studentův t-test pro parametrická data s normálním rozložením, Mannův-Whitneyův U-test v případě dichotomických veličin, Kruskalův-Wallisův test pro kvalitativní veličiny s více úrovněmi a Fisherův přesný test pro srovnání procentuální míry četnosti skupin nominálních dat.
Pro statistické srovnání výsledků ve čtyřech doménách dotazníku WHOQOL-BREF (fyzické zdraví, psychologická doména, sociální vztahy, prostředí), hodnocení kvality života a zdraví v dotazníku WHOQOL-BREF a hodnocení současného zdravotního stavu v dotazníku EQ-5D-3L byl použit Mannův-Whitneův U-test. Pro srovnání výsledků v jednotlivých doménách dotazníku EQ-5D-3L byl použit Fisherův přesný test. Všechny statistické testy byly provedeny na hladině signifikance p ≤ 0,05. Ke statistickému zpracování byl použit statistický software IBM SPSS Statistics 22 (SPSS, Chicago, IL, USA).
Výsledky
Z 584 oslovených respondentů 504 splnilo vstupní a vylučující kritéria. Celkem 344 (68,3 %) z nich kompletně vyplnilo oba dotazníky. CMP prodělalo v minulosti 145 pacientů (78 mužů, průměrný věk 70,4 ± 7,0 let) a byli zařazeni do skupiny A, 199 pacientů CMP v anamnéze neudávalo (86 mužů, průměrný věk 68,9 ± 8,3 let) a byli zařazeni do skupiny B. Pacienti ve skupině A byli signifikantně častěji hypertonici (89,7 vs. 79,4 %; p = 0,012) a měli častěji hypercholesterolémii (63,4 vs. 49,7 %; p = 0,012) ve srovnání s kontrolní skupinou B (tab. 1).
Table 1. Demografické údaje respondentů. 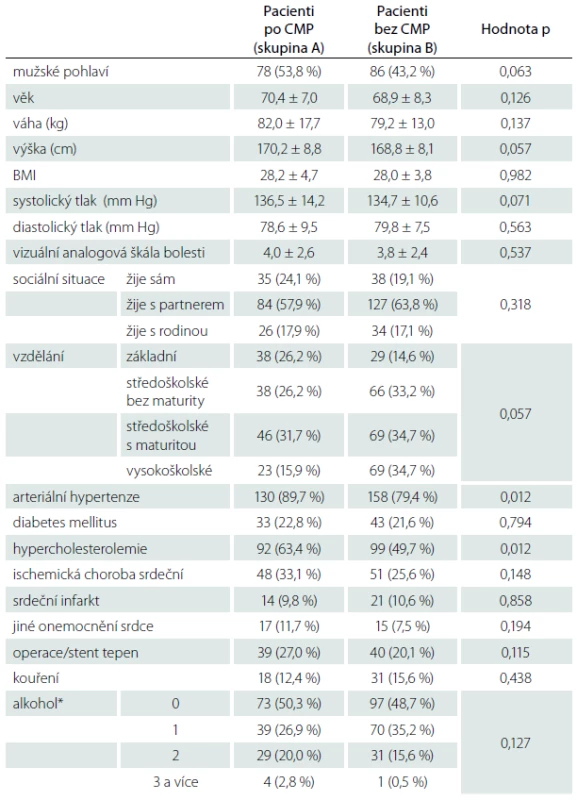
BMI – Body Mass Index, CMP – cévní mozková příhoda, *jednotky denně (20 g alkoholu). Výsledky hodnocení kvality života pomocí dotazníků WHOQOL-BREF a EQ-5D-3L jsou uvedeny v tab. 2. V žádné z domén dotazníku WHOQOL-BREF, žádné z domén z dotazníku EQ-5D-3L ani v hodnocení kvality života, kvality a současné úrovně zdravotního stavu nebyl nalezen signifikantní rozdíl mezi skupinou pacientů po prodělané CMP a kontrolní skupinou (p > 0,05 ve všech případech).
Table 2. Výsledky hodnocení kvality života u pacientů po neinvalidizující CMP a pacientů bez anamnézy CMP. 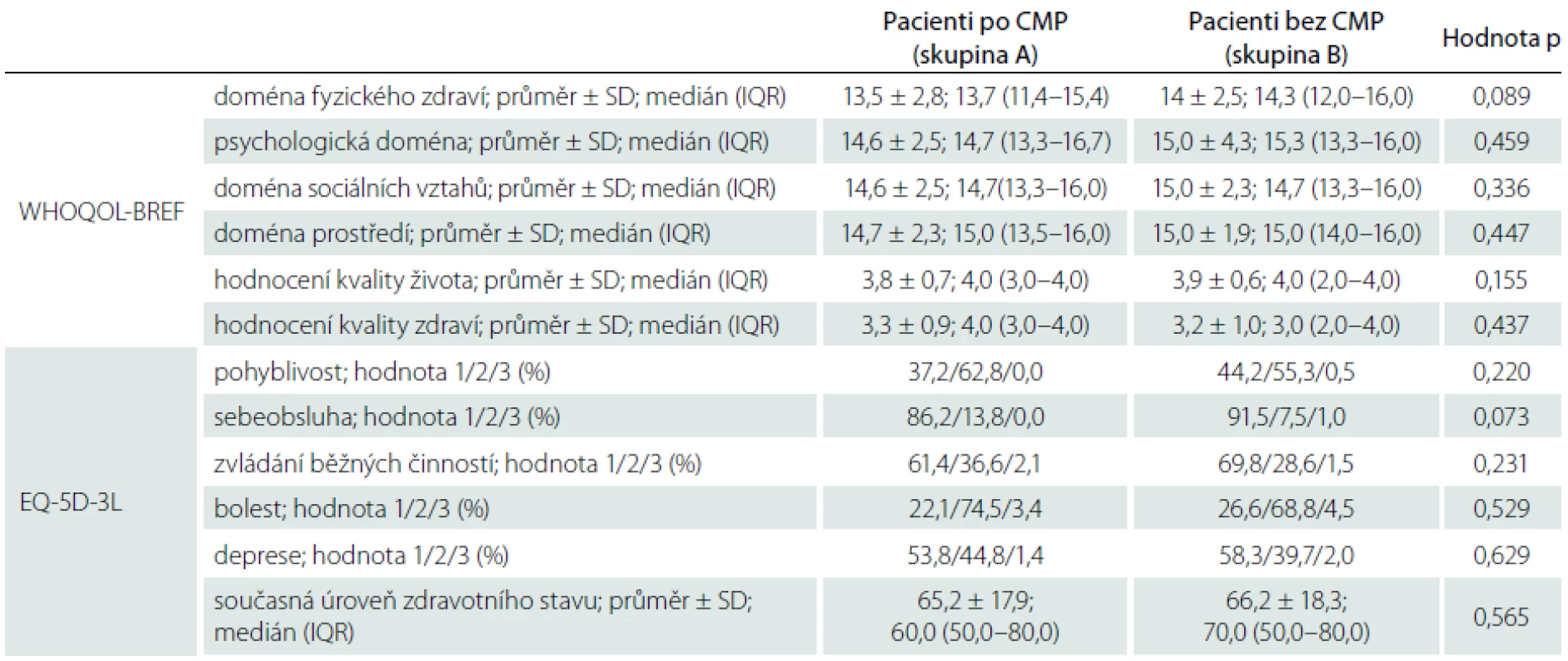
CMP – cévní mozková příhoda, EQ-5D-3L – EuroQol-5D, IQR – interkvartilové rozmezí, SD – směrodatné odchylka, WHOQOL-BREF – World Health Organization Quality of Life short version. Ženy hodnotily kvalitu života v doméně sociálních vztahů signifikantně lépe než muži (15,1 ± 2,3 vs. 14,5 ± 2,4; p = 0,020). Naopak muži hodnotili signifikantně lépe než ženy zvládání běžných denních činností (1,4 ± 0,5 vs. 1,3 ± 0,5; p = 0,043). Pacienti s diabetes mellitus byli méně spokojeni se svým zdravotním stavem (3,1 ± 1,0 vs. 3,3 ± 0,9; p = 0,032) a hůř hodnotili současnou úroveň zdravotního stavu (61,1 ± 16,7 vs. 67,1 ± 18,3; p = 0,006) než pacienti bez tohoto onemocnění. Pacienti s ischemickou chorobou srdeční hodnotili hůř svou kvalitu života v doméně bolest než pacienti bez ischemické choroby srdeční (1,9 ± 0,5 vs. 1,8 ± 0,5; p = 0,045). Pacienti žijící s partnerem hodnotili lépe jak celkovou kvalitu života (3,7 ± 0,8 vs. 4,0 ± 0,6; p = 0,030), tak kvalitu života v doméně fyzické zdraví (13,1 ± 2,7 vs. 14,1 ± 2,5; p = 0,017) než pacienti, kteří žili sami.
Diskuze
V naší studii bylo prokázáno, že neinvalidizující CMP nezhoršuje signifikantně kvalitu života u nedepresivních a nedementních pacientů. Pacienti, kteří prodělali CMP, a následně dosáhli soběstačnosti, nehodnotili svou kvalitu života a zdraví, pohyblivost, sebeobsluhu, zvládání běžných činností, bolesti, deprese, ani položky v doménách fyzické zdraví, psychologické zdraví, sociální vztahy a prostředí signifikantně hůř než lidé, kteří nikdy CMP neprodělali. Z toho vyplývá, že hodnocení soběstačnosti po 3 měsících jako hlavního kritéria úspěšnosti léčby CMP, především trombolytické a endovaskulární léčby ischemické CMP, by mělo být dostatečné i pro hodnocení udržení kvality života u těchto pacientů.
Hodnocení kvality života by se mělo skládat z hodnocení jak funkční a fyzické, tak kognitivní, psychologické a sociální složky. Výsledek takového hodnocení pak lépe odráží pacientovo vnímání nejen funkčního stavu, ale také svého zdraví celkově. V mnohých případech se můžeme setkat s pacienty s minimálními fyzickými a funkčními následky po CMP, kteří hodnotí kvalitu svého života velmi špatně a naopak [13].
Pro hodnocení kvality života bylo vyvinuto mnoho dotazníků [13]. Část z nich jsou dotazníky obecné, určené pro běžnou populaci, např. World Health Organization Quality of Life (WHOQOL), World Health Organization Quality of Life short version (WHOQOL-BREF), Medical Outcomes Short Form Health Survey (SF-36), jeho zkrácená verze Medical Outcomes Short Form Health Survey (SF-12), Sickness Impact Profile (SIP), EuroQOL, Quality of Life Index (QLI), Reintegration to Normal Living Index (RLNI), Nottingham Health Profile (NHP). Výhodou těchto dotazníků je široká využitelnost u pacientů s různým typem onemocnění a možnost posoudit vliv různých onemocnění a následných léčebných postupů. Většina takových dotazníků je vytvořena jako sebehodnotící nástroj, který vyplňuje sám pacient. Tyto nástroje však nejsou vhodné pro pacienty s demencí či řečovou poruchou. Variantou zde jsou dotazníky pro příbuzné a opatrovníky, které však mohou přinášet velmi zkreslené výsledky, protože mohou více odrážet názory opatrovníka než pacienta. Další limitací je nízká senzitivita detekovat rozdíly v kvalitě života v selektované populaci, která hodnotí většinu položek maximální nebo naopak minimální hodnotou. V neposlední řadě limitací mnohých dotazníků je časová náročnost vyplnění [13].
Z těchto důvodů jsou vytvářeny specifické pro pacienty s určitým onemocněním. U pacientů po CMP se používají např. EuroQol-5D pětiúrovňový nebo tříúrovňový (EQ-5D-5L a EQ-5D-3L), Stroke Adapted Sickness Impact Profile (SASIP30), Stroke Impact Scale (SIS), Stroke Specific Quality of Life Measure (SSQOL) [13]. Tyto dotazníky bývají časově méně náročné, ale nepokrývají dostatečně vliv jiných onemocnění.
Pro účely naší studie byly vybrány dva dotazníky, jeden obecný a jeden specifický. Dotazník WHOQOL-BREF, který poskytuje zdravotníkům poměrně snadný způsob, jak zhodnotit kvalitu života [14], a dotazník EQ-5D-3L, který hodnotí specifické oblasti u pacientů po CMP [15]. Proběhlé studie potvrdily, že oba dotazníky jsou validní a umožní objektivizovat kvalitu života respondentů [14,16].
Kvalita života je závislá na mnoha faktorech. V prezentované studii muži hodnotili signifikantně lépe zvládání běžných denních činností než ženy. Podobné výsledky popsali také van Eeden et al [17]. Dalšími faktory ovlivňujícími kvalitu života pacientů po iktu byly v prezentované studii diabetes mellitus a ischemická choroba srdeční, což bylo popsáno také dalšími autory [18–21].
Kvalitu života může ovlivnit tíže i charakter perzistujícího deficitu [22–25]. Korejská studie ukázala, že pacienti s lézí faciálního nervu hodnotili kvalitu života signifikantně hůř než pacienti s dysartrií [23]. V dalších studiích hodnotili svou kvalitu života hůř také pacienti se zrakovým deficitem nebo hemiparézou po iktu [24,25]. Také recidiva iktu zhoršuje kvalitu života [25]. Naopak ani u pacientů s iktem, kteří museli podstoupit chirurgickou léčbu (dekompresní kraniektomii, evakuaci hematomu nebo klipsaci aneuryzmatu), nemusí dojít k zhoršení kvality života, pokud zůstanou soběstační [26]. V naší studii měla většina pacientů jen minimální nebo žádný perzistující deficit, takže nebylo možno vliv jednotlivých typů neurologického postižení posoudit.
Velmi důležitým faktorem ovlivňujícím hodnocení kvalitu života je doba od prodělaného iktu. Během prvních 6 měsíců dochází u většiny pacientů ke zlepšení hodnocení kvality života, především pokud absolvují rehabilitaci [27], nicméně až u 35 % pacientů může dojít ke zhoršení kvality života, především pokud došlo k recidivě iktu nebo přetrvává těžší neurologický deficit [22,28]. Poté zůstává kvalita života min. 5 let stabilní [22].
Neméně důležitým faktorem, který ovlivňuje kvalitu života, je sociální situace. V naší studii pacienti žijící sami hodnotili kvalitu života hůř než pacienti žijící s partnerem, podobně jako ve studii z Appalachia [29]. Dalšími faktory, které ovlivňují kvalitu života, jsou chronická bolest, deprese a demence [30]. Bolest však není typickým následkem iktu a v naší studii nebyla bolest častější ani výraznější u pacientů po iktu než v kontrolní skupině. Pro vyloučení vlivu deprese a demence, které však můžou být relativně častým následkem iktu, nebyli pacienti s těmito symptomy i jiným psychiatrickým onemocněním do studie zahrnuti.
Hlavní limitací prezentované studie je výběr respondentů. Do studie byli vybráni jen pacienti s aterosklerotickým postižením karotických tepen, díky čemuž mohli být částečně opomenuti pacienti s jinou etiologií iktu. Druhou limitací je monocentrický charakter studie. Je potřeba také zdůraznit, že do studie nebyli zařazeni pacienti s depresí, demencí, větším zrakovým nebo sluchovým postižením.
Závěr
Výsledky studie prokázaly, že u pacientů po CMP, kteří zůstali soběstační a neměli demenci ani depresi, nedošlo k signifikantnímu zhoršení kvality života a zdraví. Tito pacienti hodnotili svou pohyblivost, sebeobsluhu, zvládání běžných činností, bolesti, deprese, položky v doménách fyzické zdraví, psychologické zdraví, sociální vztahy a prostředí shodně jako pacienti, kteří nikdy CMP neprodělali.
Studie byla podpořena grantem Univerzity Palackého v Olomouci IGA_FZV_2016_004.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Ing. Táňa Fadrná
Neurochirurgická klinika
LF OU a FN Ostrava
17. listopadu 1790
708 52 Ostrava
e-mail: tana.fadrna@seznam.cz
Přijato k recenzi: 20. 12. 2016
Přijato do tisku: 8. 2. 2017
Sources
1. Rasmussen PA. Stroke management and the impact of mobile stroke treatment units. Cleve Clin J Med 2015;82(12 Suppl 2):S17 – 21. doi: 10.3949/ccjm.82.s2.04.
2. Bonita R, Beaglehole R. Stroke prevention in poor countries: time for action. Stroke 2007;38(11):2871 – 2. doi: 10.1161/STROKEAHA.107.504589.
3. Škoda O, Herzig R, Mikulík R, et al. Klinický standard pro diagnostiku a léčbu pacientů s ischemickou cévní mozkovou příhodou a s tranzitorní ischemickou atakou – verze 2016. Cesk Slov Neurol N 2016;79/112(3):351 – 63. doi: 10.14735/amcsnn2016351.
4. Pollock A, Baer G, Campbell P, et al. Physical rehabilitation approaches for the recovery of function and mobility following stroke. Cochrane Database Syst Rev 2014;4:CD001920. doi: 10.1002/ 14651858.CD001920.pub3.
5. Chen CJ, Ding D, Starke RM, et al. Endovascular vs medical management of acute ischemic stroke. Neurology 2015;85(22):1980 – 90. doi: 10.1212/ WNL.0000000000002176.
6. Balami JS, Sutherland BA, Edmunds LD, et al. A systematic review and meta-analysis of randomized controlled trials of endovascular thrombectomy compared with best medical treatment for acute ischemic stroke. Int J Stroke 2015;10(8):1168 – 78. doi: 10.1111/ ijs.12618.
7. Volný O, Krajina A, Bar M, et al. Konsenzus a návrh algoritmu léčby – mechanická trombektomie u akutního mozkového infarktu. Výsledky intervenčních studií MR CLEAN, ESCAPE, SWIFT PRIME, EXTEND-IA, REVASCAT. Cesk Slov Neurol N 2016;79/ 112(1):100 – 10. doi: 10.14735/amcsnn2016100.
8. Šaňák D, Neumann J, Tomek A, et al. Doporučení pro rekanalizační léčbu akutního mozkového infarktu – verze 2016. Cesk Slov Neurol N 2016;79/112(2):231–4. doi: 10.14735/amcsnn2016231.
9. Carota A, Dieguez S, Bogousslavsky J. Psychopathology of stroke. Psychol Neuropsychiatr Vieil 2005;3(4):235 – 49.
10. Fisher AR. Development of clinical practice guidelines for urinary continence care of adult stroke survivors in acute and rehabilitation settings. Can J Neurosci Nurs 2014;36(3):16 – 31.
11. Kasner SE. Clinical interpretation and use of stroke scales. Lancet Neurol 2006;5(7):603 – 12.
12. Ghandehari K. Challenging comparison of stroke scales. J Res Med Sci 2013;18(10):906 – 10.
13. Kranciukaite D, Rastenyte D. Measurement of quality of life in stroke patients. Medicina 2006;42(9):709 – 16.
14. The WHOQOL Group. Development of the world health organization WHOQOL-BREF quality of life assessment. Psychol Med 1998;28(3):551 – 8.
15. Golicki D, Niewada M, Buczek J, et al. Validity of EQ-5D-5L in stroke. Qual Life Res 2015;24(4):845–50. doi: 10.1016/J.JVAL.2014.08.1906.
16. Janssen MF, Birnie E, Haagsma JA, et al. comparing the standard EQ-5D three-level system with a five-level version. Value Health 2008;11(2):275 – 84.
17. van Eeden M, van Heugten C, van Mastrigt GA, et al. The burden of stroke in the Netherlands: estimating quality of life and costs for 1-year poststroke. BMJ Open 2015;5(11):e008220. doi: 10.1136/bmjopen-2015-008220.
18. Glasziou P, Alexander J, Beller E, et al; ADVANCE Collaborative Group. Which health-related quality of life score? A comparison of alternative utility measures in patients with Type 2 diabetes in the ADVANCE trial. Health Qual Life Outcomes 2007;5 : 21.
19. Hayes A, Arima H, Woodward M, et al. Changes in Quality of Life Associated with Complications of Diabetes: results from the ADVANCE Study. Value Health 2016;19(1):36 – 41. doi: 10.1016/j.jval.2015.10.010.
20. Lee HT, Shin J, Lim YH, et al. Health-related quality of life in coronary heart disease in Korea: the Korea National Health and Nutrition Examination Survey 2007 to 2011. Angiology 2015;66(4):326 – 32. doi: 10.1177/0003319714533182.
21. Xie J, Wu EQ, Zheng ZJ, et al. Patient-reported health status in coronary heart disease in the United States: age, sex, racial, and ethnic differences. Circulation 2008;118(5):491 – 7. doi: 10.1161/CIRCULATIONAHA.107.752006.
22. Luengo-Fernandez R, Gray AM, Bull L, et al.; Oxford Vascular Study. Quality of life after TIA and stroke: ten-year results of the Oxford Vascular Study. Neurology 2013;81(18):1588 – 95. doi: 10.1212/WNL.0b013e3182a9f45f.
23. Chang WH, Sohn MK, Lee J, et al. Impact of central facial palsy and dysarthria on quality of life in patients with stroke: the KOSCO study. NeuroRehabilitation 2016;39(2):253 – 9. doi: 10.3233/ NRE-161355.
24. Sand KM, Wilhelmsen G, Naess H, et al. Vision problems in ischaemic stroke patients: effects on life quality and disability. Eur J Neurol 2016;23(Suppl 1):1 – 7. doi:10.1111/ene.12848.
25. Min KB, Min JY. Health-related quality of life is associated with stroke deficits in older adults. Age Ageing 2015;44(4):700 – 4. doi: 10.1093/ ageing/afv060.
26. Green T, Demchuk A, Newcommon N. Aggressive surgical interventions for severe stroke: impact on quality of life, caregiver burden and family outcomes. Can J Neurosci Nurs 2015;37(2):15 – 25.
27. Katona M, Schmidt R, Schupp W, et al. Predictors of health-related quality of life in stroke patients after neurological inpatient rehabilitation: a prospective study. Health Qual Life Outcomes 2015;13 : 58. doi: 10.1186/s12955-015-0258-9.
28. Sangha RS, Caprio FZ, Askew R, et al. Quality of life in patients with TIA and minor ischemic stroke. Neurology 2015;85(22):1957 – 63. doi: 10.1212/ WNL.0000000000002164.
29. Theeke L, Horstman P, Mallow J, et al. Quality of life and loneliness in stroke survivors living in Appalachia.
J Neurosci Nurs 2014;46(6):E3 – 15. doi: 10.1097/JNN.0000000000000097.
30. Choi-Kwon S, Choi JM, Kwon SU, et al. Factors that Affect the Quality of Life at 3 Years Post-Stroke. J Clin Neurol 2006;2(1):34 – 41. doi: 10.3988/ jcn.2006.2.1.34.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2017 Issue 3-
All articles in this issue
- Vertebrogenní algický syndrom – medicína založená na důkazech a běžná klinická praxe. Existuje důvod něco změnit?
- Výsledky endokrinních funkcí hypofýzy po transsfenoidálních operacích afunkčních makroadenomů
- Radiologické nálezy u donošených novorozenců s hypoxicko-ischemickou encefalopatií
- Token test – validační studie české verze u osob vyššího věku a pacientů s neurodegenerativním onemocněním mozku
- Měření simulace – Test mince v ruce
- Efekty cílené orofaciální rehabilitace u pacientů s poruchou řečových funkcí po cévní mozkové příhodě
- Zobrazení difuzních tenzorů u pacientů s idiopatickým normotenzním hydrocefalem
- Anti-NMDAR protilátky u demyelinizačních onemocnění
- Pyridoxin dependentní epilepsie – kazuistiky
- Klasifikace nádorů centrálního nervového systému – WHO 2016 Update
- Kvalita života u soběstačných pacientů po cévní mozkové příhodě
- Myotonická dystrofie – jednota v různosti
- Febrilní křeče – méně je někdy více
- Riziko poškození plodu v důsledku rentgenových výkonů u gravidních žen
- Úspěšná léčba meningoencefalitidy vyvolané Cryptococcus gattii Ommaya rezervoárem a intratékální injekcí amfotericinu B – kazuistika
- Diferenciální diagnostika bithalamické a palidální hypointenzity – kazuistika s mutací HEXB
- Signifikantní edém mozku u neprasklé arteriovenózní malformace – kazuistika
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Myotonická dystrofie – jednota v různosti
- Riziko poškození plodu v důsledku rentgenových výkonů u gravidních žen
- Vertebrogenní algický syndrom – medicína založená na důkazech a běžná klinická praxe. Existuje důvod něco změnit?
- Febrilní křeče – méně je někdy více
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

