-
Medical journals
- Career
Chirurgická léčba revmatického postižení kraniocervikálního přechodu
Authors: P. Vaněk
Authors‘ workplace: 1. LF UK a ÚVN Praha
Published in: Cesk Slov Neurol N 2012; 75/108(3): 273-282
Category: Minimonography
Overview
Revmatoidní artritida představuje chronické zánětlivé onemocnění, které se manifestuje multiorgánovým postižením. Typickým projevem je chronická symetrická polyartritida vedoucí ke vzniku kloubních destrukcí a deformit. Páteř je onemocněním nejčastěji postižena v oblasti kraniocervikálního přechodu. Zvýšená laxita vazů vede k rozvoji nestability, jejímiž nejběžnějšími projevy jsou atlantoaxiální dislokace a kraniální migrace zubu čepovce. Popsaná nestabilita může vést až ke vzniku a progresi neurologického postižení, včetně náhlého úmrtí. Včasné zavedení agresivní farmakoterapie může zpomalit progresi onemocnění, nicméně při radiologické progresi nestability nebo vzniku neurologického postižení je chirurgická léčba jedinou smysluplnou léčebnou modalitou. Indikací k chirurgické terapii může být i bolest nezvládnutelná konzervativní léčbou odpovídající popsané nestabilitě. Multidisciplinární spolupráce je nezbytným předpokladem optimálního dlouhodobého výsledku léčby.
Klíčová slova:
kraniocervikální přechod – revmatoidní artritida – nestabilita – chirurgická léčbaÚvod
Revmatoidní artritida (RA) je chronické zánětlivé onemocnění, jehož hlavní projevy se týkají synoviální výstelky kloubů, šlach a tíhových váčků. Základním projevem tohoto onemocnění je infiltrace kloubního prostředí zánětlivými buňkami, s hyperplazií synoviální tkáně a postupnou destrukcí chrupavky a přiléhající kosti. Klinicky se nejčastěji projevuje chronickou symetrickou polyartritidou s následným vznikem kloubních destrukcí a deformit. Mimokloubní manifestace onemocnění může vést k postižení kůže, očí, laryngu, plic, ledvin, kardiovaskulárního, hematopoetického či lymfatického systému [1]. RA představuje nejčastější zánětlivé onemocnění, které postihuje krční páteř, a to v 80 % případů v segmentu prvního a druhého krčního obratle (C1/C2), ve zbylých 20 % případů se onemocnění manifestuje mezi C3–C7. Chronická synovitida může v této oblasti vést ke vzniku atlantoaxiální nestability, jež se může klinicky manifestovat bolestí krku a hlavy, závratěmi, pare-steziemi, stejně tak i v pozdějším stadiu významnějšími komplikacemi vyplývajícími z komprese horní krční míchy. Vlastní dynamika tohoto postižení je obtížně predikovatelná, u některých nemocných je radiologický nález dlouhodobě stabilní, v jiných případech dochází k rychlé dekompenzaci a rozvoji významné, až život ohrožující nestability [2].
První záznam o postižení krční páteře revmatickým procesem byl v novodobé medicínské literatuře publikován v roce 1890, kdy Garrod prezentoval soubor 500 nemocných léčených pro RA, u nichž byla ve 178 (36 %) případech poškozena i krční páteř [3]. Davis je autorem první zprávy o náhlém úmrtí revmatika následkem komprese horní krční míchy při atlantoaxiálním posunu, která byla publikována v roce 1951 [4]. Kornblum et al ve své práci o rok později položili základ současnému náhledu na souvislost mezi RA a vznikem nestability v oblasti horní krční páteře [5].
Etiologie a patofyziologie
Etiologie onemocnění není známa, předpokládá se společný vliv dědičných a zevních faktorů. Predispozicí je nosičství některých alel HLA-DR4 či HLA-DR1 (70–90 % nemocných). Větší část nemocných má sérové autoprotilátky (IgM) namířené proti autologním imunoglobulinům (IgG) (revmatoidní faktory) a proti citrulinovým peptidům (ACPA, Anti-Citrullinated Protein Antibodies), přičemž produkce ACPA se dává v poslední době i do souvislosti s kouřením.
Patologickoanatomicky je pro onemocnění charakteristický vznik bohatě vaskularizované, zánětlivé granulační tkáně (pannu). Významnou roli v udržování zánětu hraje převaha tvorby prozánětlivých cytokinů, především tumor nekrotizujícího faktoru α (TNFα), interleukinu 6 (IL-6) a interleukinu 1 (IL-1). Tyto cytokiny atrahují a mobilizují buňky imunitního systému v krevním řečišti a podněcují aktivaci a proliferaci synoviocytů. Dochází k tvorbě a uvolňování proteáz, které destruují kloubní chrupavku, subchondrální kost, šlachy a ligamenta. Destruktivní synovitidou navozené poškození kolagenních vláken je odpovědné za vznik mnohočetných mikrotrhlin ve struktuře šlach a vazů, přičemž jejich následné zhojení fibrózními jizvami vede k významnému zvýšení jejich laxity. Pro postižení horní krční páteře je typická kombinace dvou jevů – vznik nestability na podkladě zvýšené laxity vazů a přímá komprese neurologických struktur vlastním pannem [1,2].
Anatomie a biomechanika kraniocervikálního přechodu
Oblast okciput (C0)/C1 a C1/C2 jsou jediné segmenty páteře, kde se kloubní spojení realizuje bez přítomnosti meziobratlové ploténky. Tyto dva segmenty jsou spojeny výhradně synoviálními klouby, z čehož plyne výrazná vulnerabilita při postižení RA [6]. Stabilita atlantoaxiálního komplexu závisí dominantně na integritě ligamentum transversum atlantis. Ligamenta alaria a apikální ligamenta představují sekundární stabilizační systém komplexu. Kloubní plošky C1/C2 jsou orientovány, na rozdíl od subaxiální krční páteře, v axiální rovině a nepředstavují žádnou překážku případnému posunu. Za fyziologických okolností nedovoluje u dospělého člověka závěsný aparát ventrální posun mezi C1/C2 větší než 3 mm. Fielding et al považují stabilizační funkci sekundárních stabilizátorů za nedostatečnou, při ruptuře ligamentum transversum se může atlas v anteflexi, i při intaktních sekundárních stabilizátorech, posunout bez omezení až o 5 mm [6–8]. Při revmatickém rozvolnění příčného vazu současně se sekundárními stabilizátory může docházet ke skluzu o 10 mm a více. Uvážíme-li, že předozadní rozměr páteřního kanálu v oblasti C2 je 14 mm, je riziko vzniku míšní léze více než zřejmé [9]. Další manifestací nestability C1/C2 je kraniální migrace zubu čepovce. Ta vzniká na podkladě destrukce laterálních mas C2, popř. C1 nebo sklouznutím C1 v dlouhé ose zubu C2 při rozvolnění závěsného aparátu [10].
Epidemiologie a přirozený průběh onemocnění
Prevalence onemocnění RA je 1 % populace v Evropě a Spojených státech [1,11]. Postižení krční páteře u nemocných léčených pro RA se udává v rozmezí 17–88 %. V obdobně širokém rozpětí se pohybuje referovaný výskyt neurologických komplikací v souvislosti s RA (11–70 %) [12–14]. Jistě rovněž nepřekvapí, že velmi nejasná data jsou i směrem k výskytu, vzniku a progresi atlantoaxiální dislokace. Ta jsou závislá na délce observace, sledované populaci, různých radiologických a neurologických klasifikacích. Riise et al na pokladě sledování 241 nemocných RA dospěli k závěru, že atlantoaxiální posun vzniká v průměru po 3,9 letech od stanovení diagnózy RA u nemocného [15]. Ale podle jiných pramenů je prevalence tohoto nálezu až 12 % do dvou let od počátku onemocnění [9]. Postižení míchy v souvislosti s RA změnami v oblasti horní krční páteře může mít pro své nositele katastrofické následky. V roce 1997 byla publikována sestava 21 nemocných, kteří odmítli navrženou chirurgickou léčbu pro myelopatii při revmatickém postižení horní krční páteře. U žádného z nemocných nedošlo během dalších tří let ke zlepšení v klinickém obraze, ale ve všech případech došlo k progresi neurologického postižení, jejímž výsledkem bylo upoutání nemocného na lůžko [16]. Riise et al došli k závěrům, že riziko úmrtí nemocného s revmatickou nestabilitou v oblasti horní krční páteře je osmkrát vyšší než u nemocných bez tohoto postižení [15]. V současné době není možné určit rychlost progrese revmatických změn v oblasti horní krční páteře, stejně tak jako se nedá předvídat vznik míšního postižení pro jednotlivého nemocného. Pokud se však již objeví myelopatie, je její progrese u neléčených nemocných jistá. Nezbývá tedy než zopakovat, že podcenění tohoto nálezu může vést k významné invaliditě, až úmrtí nemocného [17]. Mikulowski et al označili jako příčinu úmrtí, ve studovaném souboru 104 nemocných s RA, v 10 % případů míšní kompresi v oblasti C1/C2 [18]. Zároveň je zřejmé, že současná chirurgická léčba revmatické nestability horní krční páteře přináší nejlepší výsledky u nemocných bez známek míšního postižení [19,20].
Klinický obraz
Kvůli většinou těžkému postižení pohybového aparátu revmatickým procesem, bolestivým kloubním deformitám a svalovým atrofiím, je objektivní neurologické vyšetření nemocných s RA poměrně svízelnou záležitostí. Mnoho nemocných může být i přes významnou instabilitu v oblasti horní krční páteře asymptomatických [21]. Nemocní by tedy měli nejméně jednou za půl roku podstoupit neurologické vyšetření, v ideálním případě vždy stejným lékařem. Opakované vyšetření stejným lékařem představuje optimální způsob, jak odhalit často jemné změny v klinickém obraze překryté základním onemocněním.
Nejčastějším steskem nemocných je bolest v oblasti kraniocervikálního přechodu, jež bývá přítomna až v 40–80 % případů [22]. Může být spojena s bolestí v okcipitální krajině, iritace velkého okcipitálního nervu (C2) se může projevovat okcipitální neuralgií, obličejovou bolestí i bolestí propagující se do ucha. Nemocní mohou udávat pocit dopředného sklouznutí hlavy při předklonu doprovázeném akustickými fenomény praskání a křupání. Mohou být přítomny známky myelopatie – progresivní oslabování, deficit jemné motoriky prstů, výdržnosti, parestezie končetin, poruchy rovnováhy, spasticita, hyperreflexie, iritační pyramidové jevy. Anteflexe hlavy může být rovněž provázena elektrizujícími výboji do trupu a končetin (Lhermitteovo znamení). Vzniklá kraniocervikální nestabilita se může manifestovat i symptomatologií komprese vertebrálních arterií – tinitem, vertigem, poruchami vizu, diplopií, dysfagií [23–25].
Jelikož se v klinickém obraze revmatologických nemocných může sčítat symptomatologie související s mnohočetným kloubním postižením s poškozením periferních nervů a míšních kořenů při kompresi v rámci vzniklých deformit, zároveň s progredující myelopatií, bylo pro přehlednější terapeutickou kategorizaci nemocných vypracováno několik jednoduchých skórovacích systémů [26,27]. Ranawatova klasifikace představuje nejrozšířenější systém funkčního hodnocení RA nemocných, se kterým se můžeme setkat v revmatologické a revmatochirurgické literatuře (tab. 1) [26].
Table 1. Ranawatova klasifikace. 
Grafické vyšetření
Nativní rentgen krční páteře představuje základní grafické vyšetření, které je nutné u revmatika provést nejméně každého půl roku. Při odhalení známek revmatické nestability, zvláště v oblasti horní krční páteře (např. ADI > 4 mm), je třeba nemocného konzultovat s chirurgem se zkušeností s danou problematikou.
Standardně jsou pořizovány snímky v předozadní, bočné a transorální projekci, doplněné o dynamické projekce. Nativní rentgenový snímek je schopen dobře detekovat revmatické změny krční páteře, jako jsou kostní eroze, snížení disků, deteriorace osového postavení krční páteře a v neposlední řadě známky rozvíjející se nestability v oblasti kraniocervikálního přechodu [28,29]. Nejčastěji se setkáváme se čtyřmi různými typy radiologických nálezů potvrzujících revmatické postižení krční páteře – 1. izolovaná atlantoaxiální dislokace, 2. kraniální migrace zubu čepovce, 3. subluxace v oblasti subaxiální krční páteře a 4. kombinace dvou předchozích nálezů či všechny tři najednou [2].
Stupeň atlantoaxiální dislokace je na bočném rentgenovém snímku charakterizován dvěma rozměry – předním (ADI) a zadním (PADI) atlantodentálním intervalem. ADI představuje vzdálenost mezi zadní stranou předního oblouku atlasu a ventrálním okrajem zubu čepovce v rovině kruhu C1 na bočném snímku v předklonu. Jak již bylo uvedeno, za patologický je u dospělého člověka považován posun větší než 3 mm [7]. Chirurgická léčba je u nemocných s RA indikována podle různých pramenů nejčastěji při ADI 8 mm, nicméně existují i soubory nemocných stabilizovaných při ADI 9 nebo 10 mm [12,23,30]. ADI se logicky zvýrazňuje v předklonu a v záklonu může docházet až k jeho normalizaci. Současná kraniální migrace zubu čepovce může způsobit zmenšení ADI, situaci popisujeme jako „pseudostabilizaci“ C1/C2, nicméně tento stav zdánlivé grafické úpravy patologie s sebou nese vyšší riziko vzniku neurologického postižení než samotná izolovaná dislokace [31,32]. Svou roli ve velikosti naměřeného ADI může sehrát i individuální variabilita rozměru kruhu C1. Z výše jmenovaných důvodů představuje PADI preferovaný způsob měření atlantoaxiální dislokace, jelikož tento interval lépe zohledňuje reziduální rozměr páteřního kanálu. PADI je definován jako vzdálenost mezi zadním aspektem zubu čepovce a předním okrajem zadního oblouku C1 měřená v rovině kruhu C1 na bočném nativním rentgenovém snímku v předklonu. Pokud je naměřený PADI nad 14 mm, riziko rozvoje neurologické symptomatologie se limitně blíží nule, v opačném případě tento nález předpovídá rozvoj neurologického postižení s 97% senzitivitou a 52% specifi-tou (obr. 1) [20,33].
Image 1. Způsob měření předního atlantodentálního intervalu (ADI) a zadního atlantodentálního intervalu (PADI) na nativním rentgenovém snímku v bočné projekci a předklonu. 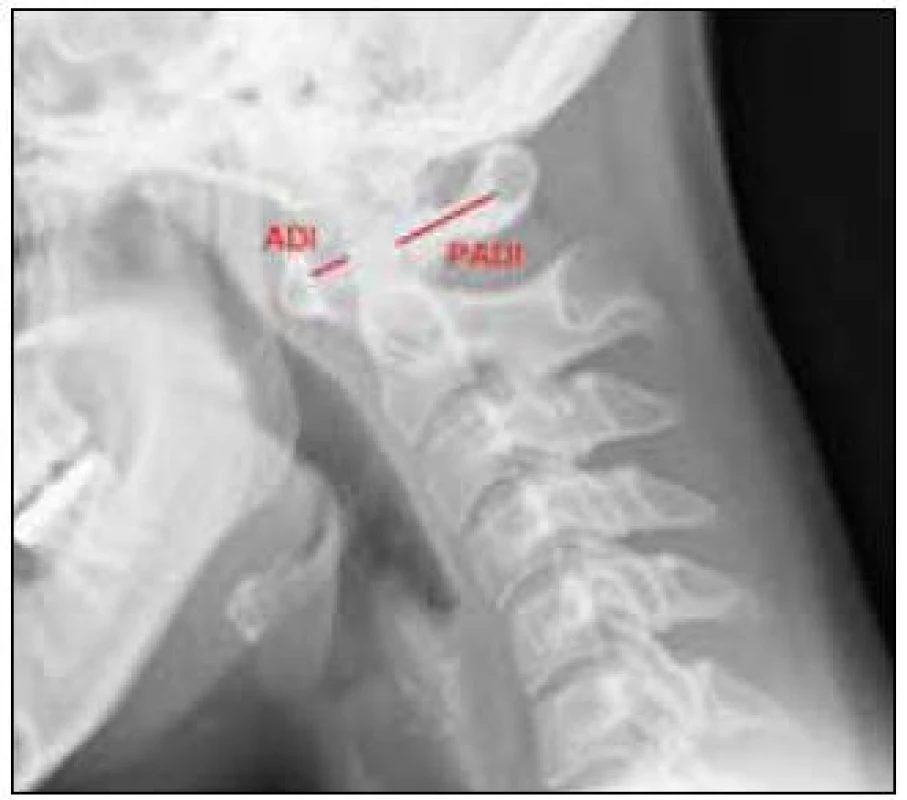
Velikost kraniální migrace zubu čepovce se na bočném rentgenovém snímku v revmatochirurgii poměřuje buď vztahem špičky zubu čepovce k definovaným čarám – McGregorově [34], McRaeově [35] či Chamberlainově linii [36], nebo specifickými indexy – Ranawatův [26] a Redlund-Johnellův index [37] (tab. 2, obr. 2, 3). Ranawatův index je dominantně závislý na změnách mezi C1 a C2, zatímco Redlund-Johnellův index lépe popisuje situaci úseku C0–C2. Hlavním úskalím měření na nativním rentgenovém snímku, a to nejen u revmatiků, je často velmi obtížná identifikace jednotlivých anatomických bodů. Nejlépe zobrazitelnými body na bočném nativním rentgenovém snímku jsou tvrdé patro a obratel C1 (dobře rozpoznatelné na 93 %, resp. 88 % nálezů), naopak nejsložitěji se lokalizuje apex zubu čepovce (dobře rozpoznatelný na 34 % nálezů) [38]. Pokud nativní rentgenové vyšetření prokáže u revmatika posun C1/C2 nebo je vysloveno podezření na kraniální migraci zubu čepovce, je nezbytné doplnit dokonalejší grafické zobrazení. Stejně tak je to nezbytné při klinickém podezření na kompresi dolního kmene, prodloužené míchy či horní krční míchy, a to i při zcela normálním rentgenovém nálezu.
Table 2. Radiologická kritéria kraniální migrace zubu čepovce založená na bočném nativním rentgenovém snímku kraniocervikálního přechodu. 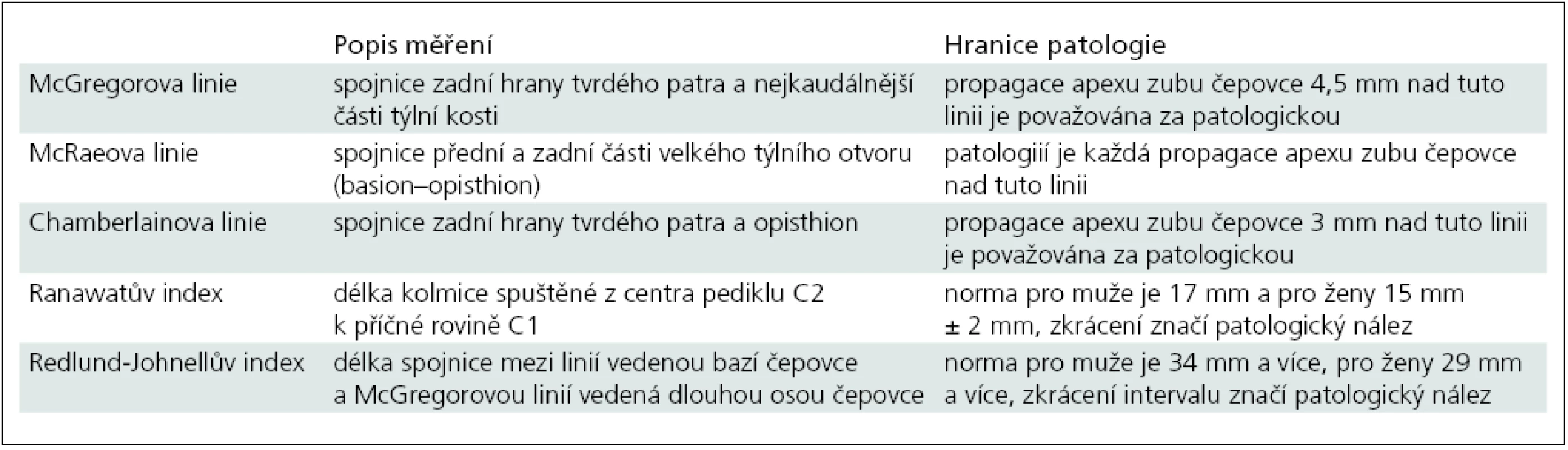
Image 2. Parametry pro určení kraniální migrace zubu čepovce – Chamberlainova, McRaeova linie a Ranawatův index červeně, modře obrys C2, pedikl C2 a příčná rovina proložená kruhem C1. 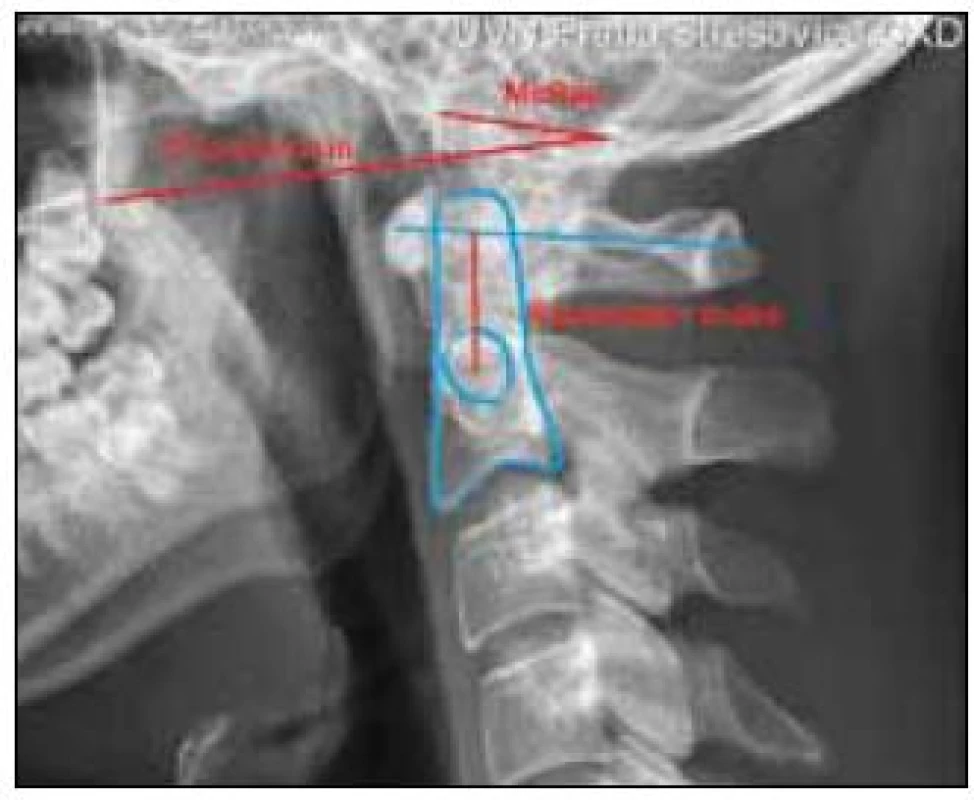
Image 3. Parametry pro určení kraniální migrace zubu čepovce – McGregorova linie a Redlund-Johnellův index červeně, modře obrys C2, pedikl C2 a rovina proložená bazí C2. 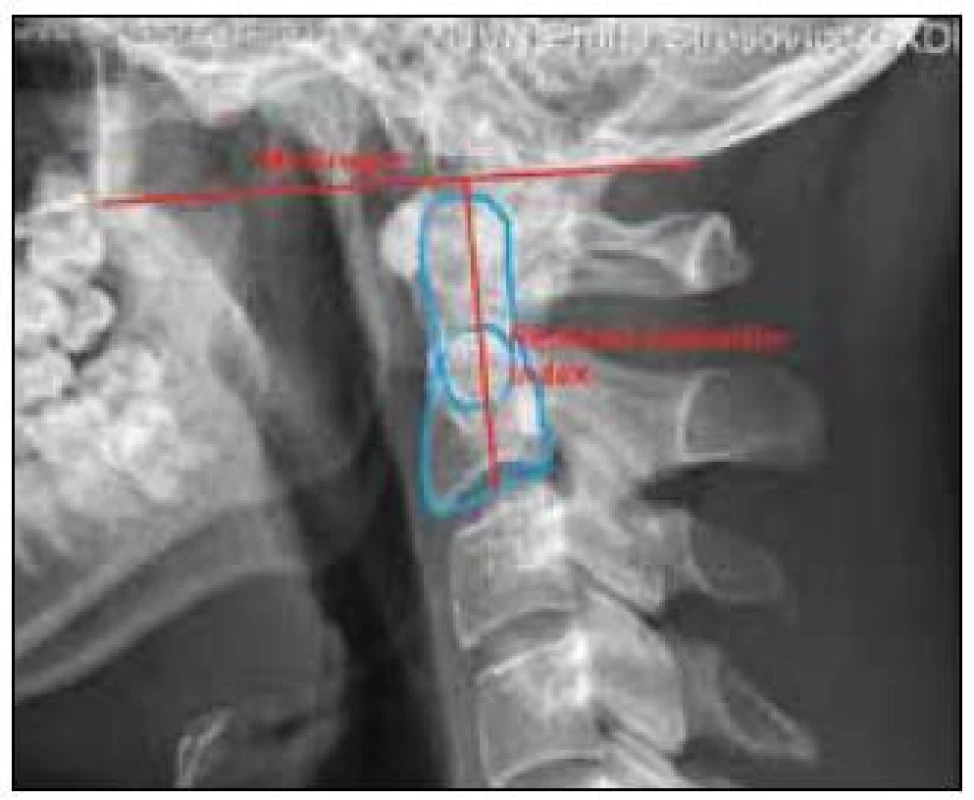
Magnetická rezonance (MR) představuje vyšetření volby pro zjištění komprese nervových struktur. MR je schopna odhalit útlak způsobený kostními strukturami, stejně tak jako měkkotkáňovými masami, a je jediným neinvazivním vyšetřením, které umožňuje ohodnotit velikost revmatického pannu [39–41]. Kromě přímé vizualizace kraniální migrace zubu čepovce je možné nález objektivizovat i změřením cervikomedulárního úhlu (úhel, který svírají roviny proložené předním okrajem horní krční míchy a prodloužené míchy – norma 135–175°). Hodnoty menší něž 135° značí kraniální migraci zubu s rizikem neurologického postižení (obr. 4) [42]. Standard dnes představuje provedení dynamických MR projekcí krční páteře v předklonu a v záklonu. Zatímco k významnější změně velikosti cervikomedulárního úhlu nedochází, tak až u 12 % nemocných s patologickými hodnotami posunu C1/C2 je odhalena komprese míchy při předklonu, která není patrná při vyšetření v neutrální poloze (obr. 5) [43,44].
Image 4. MR obraz kraniální migrace zubu čepovce s vyznačeným měřením cervikomedulárního úhlu (122° v tomto konkrétním případě). 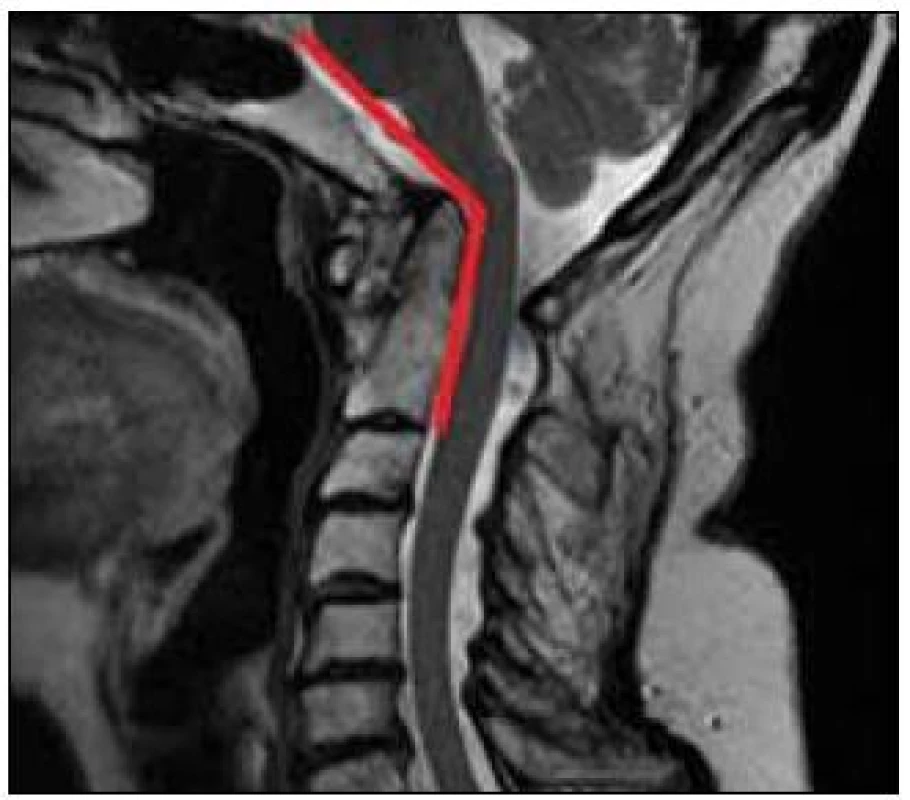
Image 5. Vyšetření atlantoaxiální dislokace v předklonu a v záklonu u nemocného s RA. 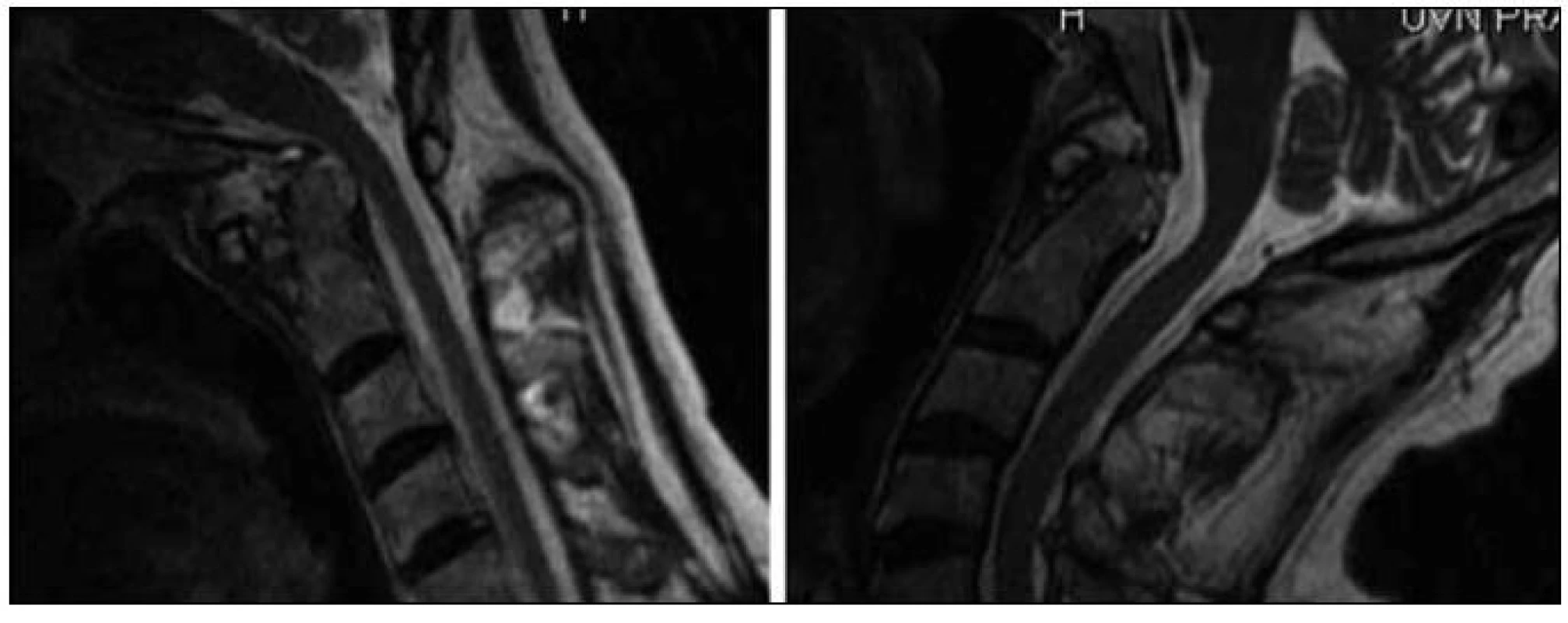
Počítačová tomografie (CT) se do vyšetřovacího algoritmu vřazuje při podezření na významnou destrukci kostěných struktur, u nemocných kontraindikovaných k provedení MR, ale vždy během plánování případné chirurgické intervence. Zde je CT výhodné k posouzení anatomických poměrů, obzvláště obratle C2 a průběhu vertebrálních arterií (VA) (obr. 6).Možností je i doplnění CT angiografie při nálezu atypického průběhu VA [45,46]. Analogickým parametrem k cervikomedulárnímu úhlu měřenému na MR je během vyšetření na CT určení úhlu kanál–klivus. CT rovněž umožňuje, v porovnání s nativními rentgenovými snímky, dokonalejší kontrolu pooperačního postavení ošetřeného úseku páteře a zavedené instrumentace. Může být využito také k exaktnímu posouzení kostního hojení, klasifikaci kostního spojení – fúze, během následného pooperačního sledování (obr. 7).
Image 6. Kraniální migrace zubu čepovce na sagitální rekonstrukci CT vyšetření. 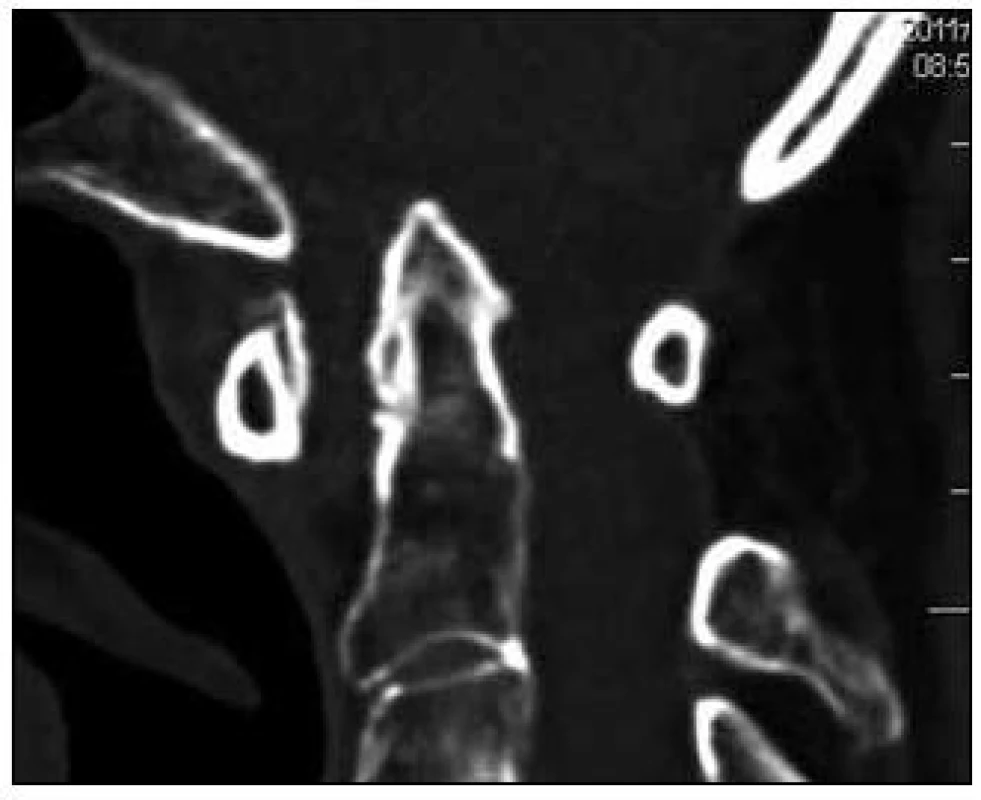
Image 7. Průběh kostního hojení zobrazený CT sagitální rekonstrukcí – stav po operaci a dokončená fúze oblouků C1/C2 rok po výkonu. 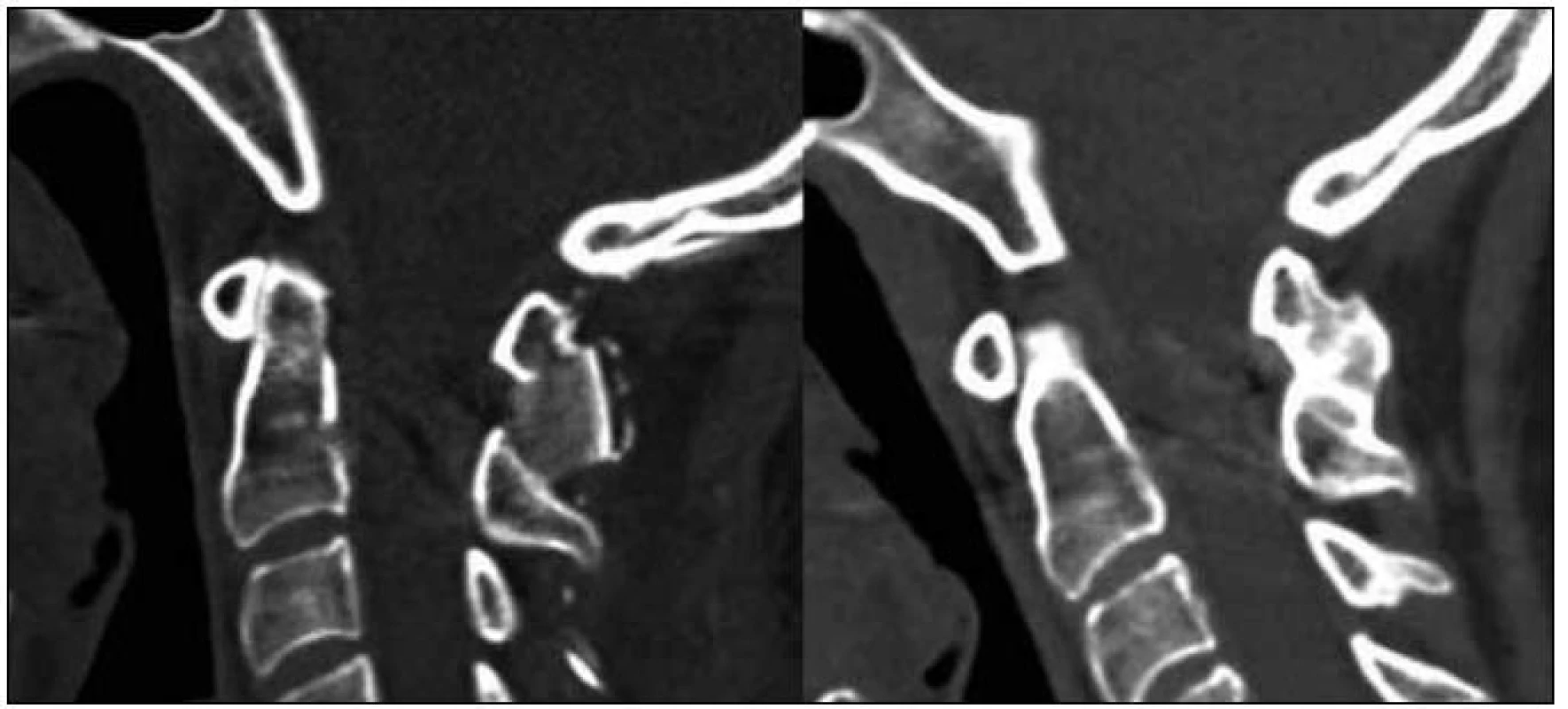
Elektrofyziologické vyšetření
Jak jsme se již zmínili, je objektivní neurologické vyšetření nemocných s RA velmi komplikované a zpožděné odhalení komprese neurologických struktur může mít pro nemocného závažné následky. Elektrofyziologie tedy představuje důležitý diagnostický nástroj pro odhalení a sledování myelopatie, ale také pro odlišení symptomatologie radikulární od postižení míšního [47]. Standardně jsou prováděny jak somatosenzorické (SSEP), tak motorické evokované potenciály (MEP) [48]. Při nálezu radiologické nestability v oblasti horní krční páteře by mělo být vyšetření opakováno nejméně jednou za půl roku, pokud je klinický obraz nemocného stabilní. Na našem pracovišti jsou tato měření prováděna kromě neutrální polohy také v předklonu a záklonu (obr. 8).
Image 8. Záznam změny průběhu MEP při předklonu a záklonu u nemocného s RA atlanto-axiálním dislokací 9 mm. 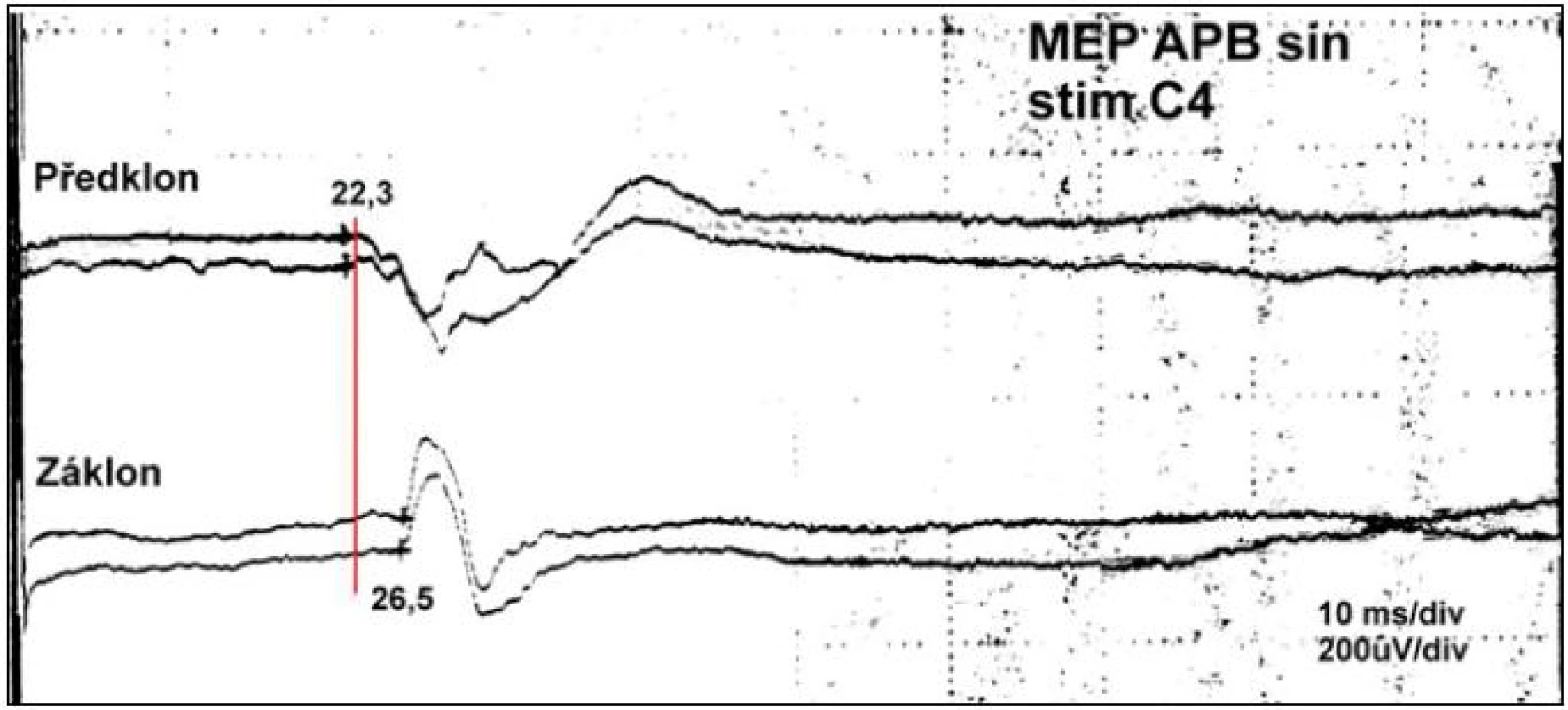
Chirurgická léčba
Stále se zdokonalující konzervativní terapie, včetně biologické léčby, významně zpomaluje průběh onemocnění, klesá výskyt postižení horní krční páteře. Počet nemocných indikovaných k chirurgické léčbě se snižuje. Nicméně zaznamená-li grafické vyšetření nález korespondující s revmatickou nestabilitu horní krční páteře, konzervativní terapie její progresi zabránit nedokáže [49,50]. Pokud je nemocný indikován ke stabilizační operaci, děje se tak v součinnosti s revmatology, kteří nemocného k výkonu připraví a přizpůsobí na dané období prováděnou terapii (přerušení či zastavení cytostatické nebo biologické terapie).
Bolest odpovídající instabilitě kraniocervikálního přechodu je považována za indikaci relativní, a to sice pokud ta dlouhodobě nereaguje na konzervativní terapii a významně nemocného limituje. Absolutní indikací ke stabilizační, případně dekompresivně stabilizační operaci je objevení se známek myelopatie u původně asymptomatického nemocného nebo progrese neurologického deficitu u vysoce interně rizikového nemocného dříve stabilního s pouze lehkou myelopatií [15,51]. Určitým indikačním problémem však jsou asymptomatičtí nemocní, ale s progredujícím grafickým nálezem odpovídajícím instabilitě v oblasti kraniocervikálního přechodu. V těchto případech je vhodné doporučit chirurgické řešení při nálezu PADI pod 14 mm, kombinovaném nálezu abnormální ADI a kraniální migrace dentu, stejně tak jako i při nálezu cervikomedulárního úhlu pod 135° [33,43,44].
Chirurgická léčba spočívá nejčastěji ze zadního přístupu provedené stabilizaci C1/C2 u izolované atlantoaxiální dislokace nebo okcipitocervikální dézy u komplexnějších nálezů [52]. Smyslem těchto výkonů je napravení anatomické situace s případnou dekompresí nervových struktur zároveň se zajištěním stabilní situace a vytvořením podmínek pro kostěné spojení C1/C2 nebo většího úseku mezi okciputem a horní krční páteří (C0–C2, event. dále dle rozsahu postižení), a to zavedením instrumentace a naložením autologních kostních štěpů.
Nejstaršími, ale dosud ne zcela opuštěnými, technikami jsou výkony založené na fixaci kostěných štěpů k obloukům obratlů pomocí drátěných kliček. Nejčastěji používanou technikou je stabilizace podle Gallieho. Ten vkládal autologní štěp z lopaty kosti kyčelní na dekortikovaný oblouk C1, opíral jej o trn a oblouk C2 s následnou fixací drátěnou kličkou vedenou pod oblouky C1,C2 [53]. Brooks et al se pokusili vylepšit stabilitu konstrukce tím, že využili štěpy dva a opět je fixovali drátěnými kličkami po straně trnu C2 [54]. Obdobnou technikou lze samozřejmě provést i rozsáhlejší stabilizaci zahrnující i okciput, např. pomocí naložení Ransfordovy kličky. Těmito operacemi lze dosáhnout kvalitního kostního spojení – fúze, v průměru u 70–80 % případů. Velikou nevýhodou ovšem je, že tyto konstrukce nevykazují okamžitou stabilitu. Může dojít k přetržení drátěných kliček nebo lanek. Při nízké kostní kvalitě pozorujeme tendenci k proříznutí oblouku a selhání konstrukce. Nemocný ošetřený touto technikou musí tedy být po výkonu několik týdnů jištěn protetickou pomůckou, jako halo vesta nebo sádrový korzet. Přičemž Loghters et al potvrdili, že halo fixace významně snižuje kvalitu života nemocných a její nasazení s sebou přináší komplikace až v 43 % případů [55]. Krční semirigidní límec není považován v této situaci za dostačující. S ohledem na možnosti současných instrumentarií pokládáme toto ošetření revmatika za obsolentní.
Další generaci stabilizačních systémů představují meziobloukové svorky typu Halifax, nicméně tento způsob nepřekročil stín svých předchůdců a platí pro ně to, co již bylo napsáno.
Naopak v roce 1979 zavedl Friedrich Magerl techniku, která posunula možnosti stabilizace C1/C2 zásadním způsobem vpřed [56]. Okamžité stability v segmentu dosáhl zavedením šroubů transartikulárně oběma klouby C1/C2. Pro dosažení kostního spojení vkládal kostní šupiny do intervertebrálních kloubů C1/C2. Jeho následovníci poté techniku zdokonalili o fixaci autologních štěpů kovovými kličkami a kabely k obloukům C1/C2 výše uvedenými technikami (obr. 9). Tímto způsobem je možno dosáhnout kvalitní fúze až v 99 % případů. Pokud je chirurg spokojený se zakotvením šroubů, není nezbytné pooperační nošení krčního límce nebo jiné ortotické pomůcky. Zároveň se ovšem jedná o řešení technicky náročnější a rizikovější v porovnání s technikami založenými na sublaminárních kličkách. Nejzávažnější uváděnou komplikací této techniky je poranění vertebrální arterie. Většina publikovaných souborů vyčísluje výskyt poranění vertebrální tepny maximálně do 2 % operovaných [57]. Určitou nevýhodou tohoto způsobu ošetření je to, že v momentě, kdy jsou zaváděny šrouby, musí již být segment v požadovaném pooperačním postavení. Jinými slovy – šrouby nelze využít k provedení repozice skluzu, ta již musí být nastolena před operací – polohováním na operačním stole, vytažením drátěnou kličkou zachycenou za oblouk C1 během výkonu či nasazením halotrakce během operace.
Image 9. Kontrola nemocného po stabilizaci C1/C2 dle Magerla rok po výkonu s dokončenou fúzí obloků C1/C2. 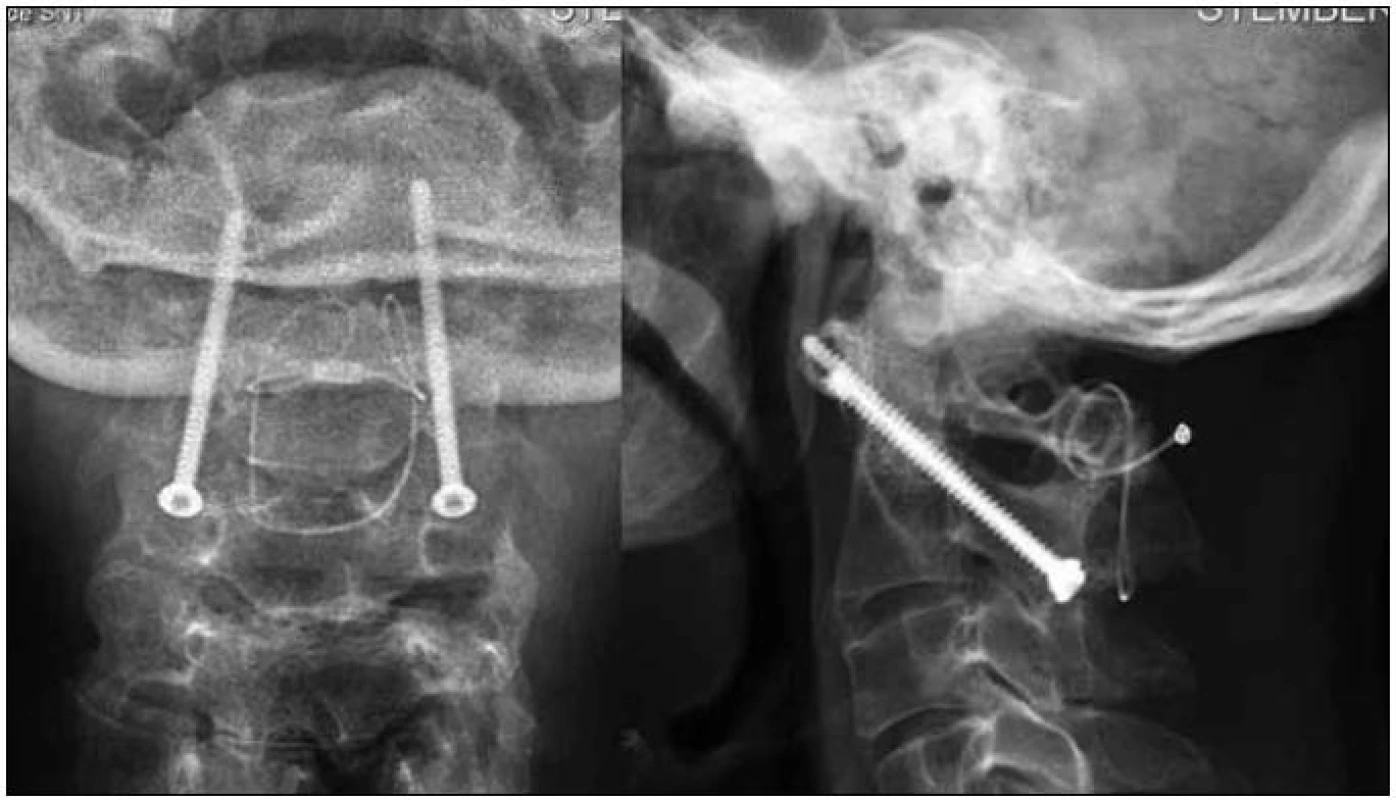
Harms et al v roce 2002 zdokonalili dříve publikovanou techniku Goelovu [58]. Ke stabilizaci C1/C2 využili sofistikovaný systém založený na polyaxiálních šroubech. Ty jsou v C1 oboustranně zavedeny do laterálních mas atlasu a transpedikulárně do C2 (obr. 10). Šrouby jsou následně spojeny tyčemi a poté je obdobně jako ve starších technikách fixován autologní štěp mezi oblouky C1 a C2. Riziko poranění vertebrální arterie je srovnatelné se jmenovanou technikou Magerlovou [59], ale na rozdíl od ní jsou šrouby zaváděny v příznivějších úhlech a je jich možno využít přímo k repozici a nastolení optimálních anatomických poměrů. V současné době na našem pracovišti využíváme pro řešení revmatických skluzů C1/C2 právě tuto techniku a výkon touto technikou jsme za poslední čtyři roky provedli u 25 nemocných.
Image 10. 3D CT rekonstrukce po stabilizaci C1/C2 technikou polyaxiálních šroubů a tyčí dle Harmse et al s naložením kostního štěpu mezi oblouky C1/C2, pooperační kontrola. 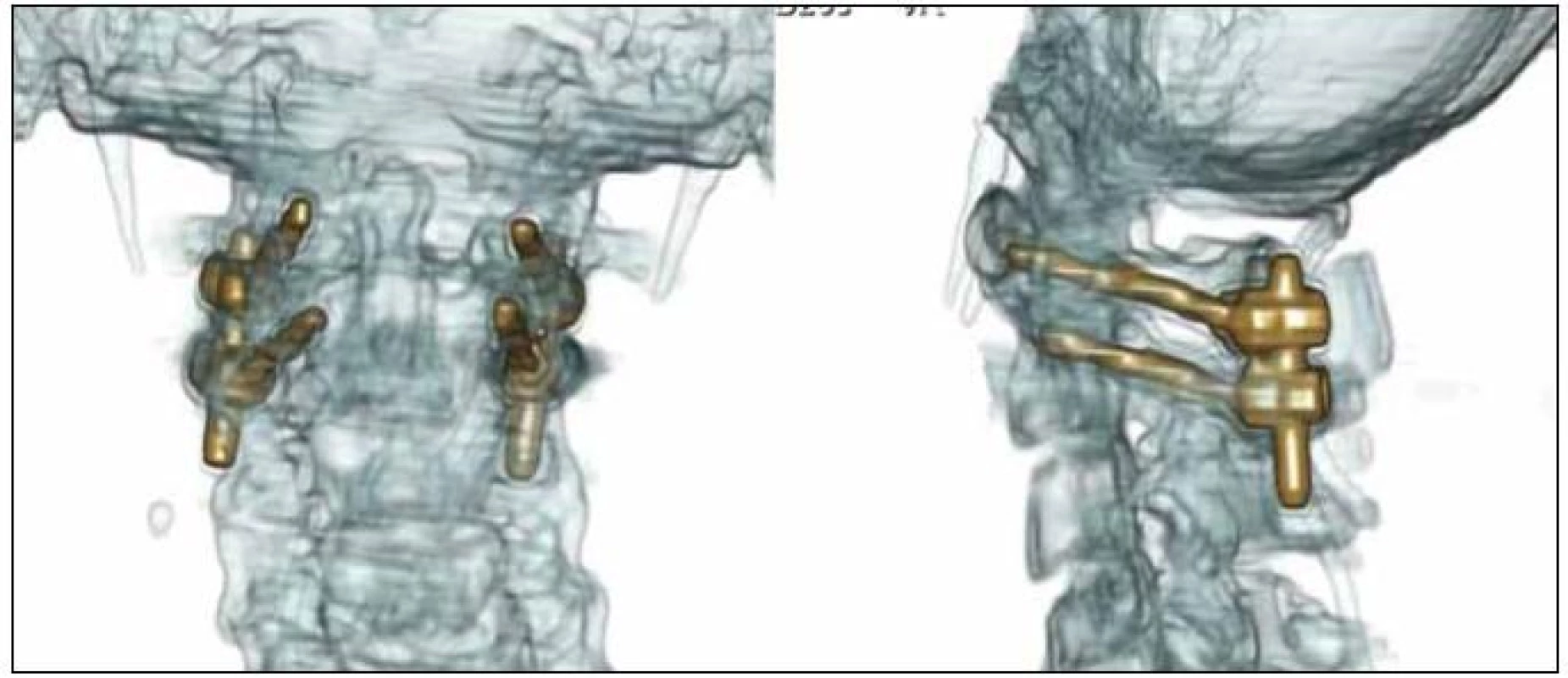
Dříve hojně využívaná transorální resekce části zubu čepovce spolu s revmatickým pannem je dnes rezervována pouze pro pacienty s nereponibilními posuny C1/C2 nebo kraniálními migracemi dentu. Dále při prokázané kompresi neurologických struktur, která se současně manifestuje progredujícím neurologickým deficitem [60,61]. Pokud je nemocný neurologicky intaktní či je zjištěna pouze incipientní myelopatie a komprese je způsobena dominantně pannem, lze většinou provést pouze stabilizaci. Repozicí při využití speciálních nástrojů instrumentárií se dá totiž většinou dosáhnout nepřímé dekomprese míchy a samotná stabilizace převážně vede i k regresi pannu (obr. 11,12) [62].
Image 11. Regrese revmatického panu v T1 váženém MR zobrazení – snímek před výkonem a kontrola rok po operaci. 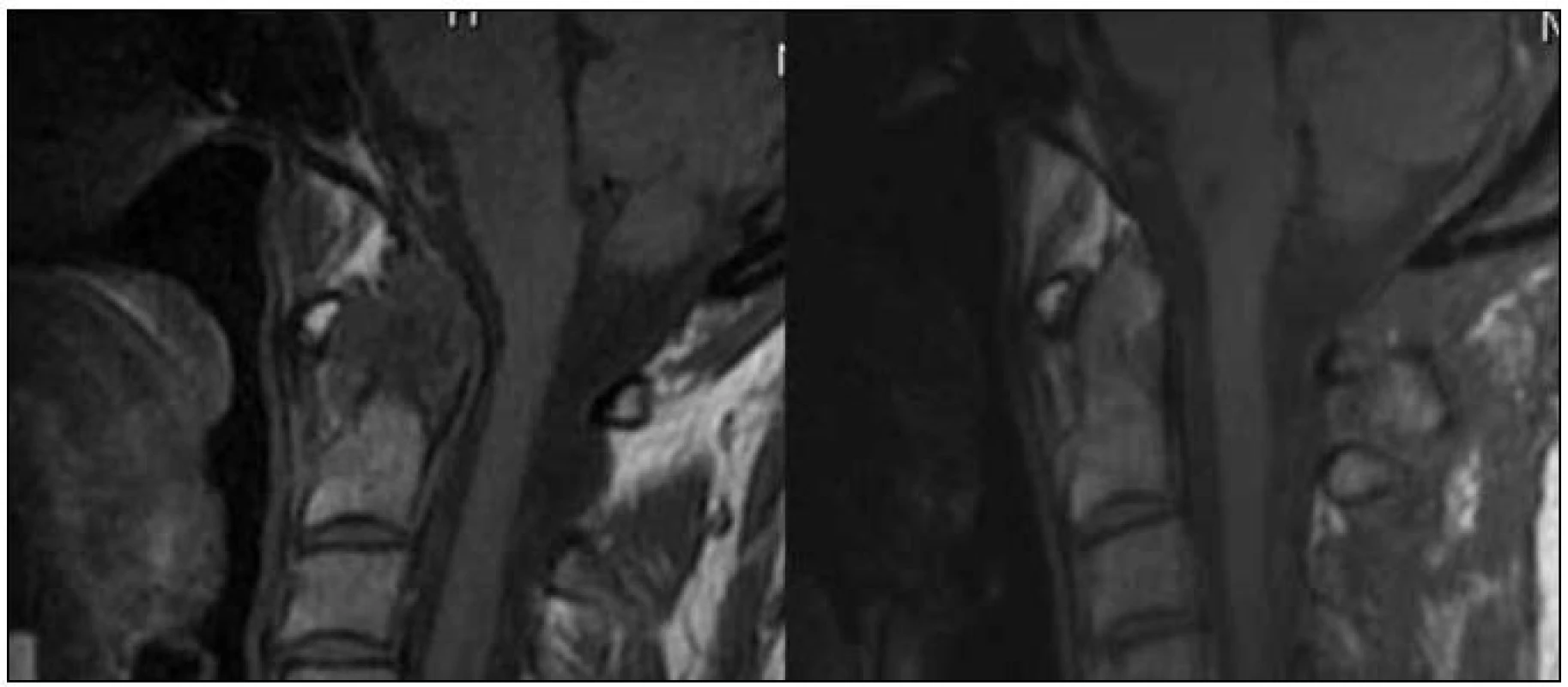
Image 12. 3D CT rekonstrukce provedené okcipitocervikální stabilizace (C0–C4) u revmatika – pooperační kontrola. Ve výřezech zobrazena nepřímá dekomprese prodloužené míchy změnou postavení v oblasti kraniocervikálního přechodu stejného nemocného v T2 váženém MR zobrazení – snímek před výkonem a pooperační kontrola. 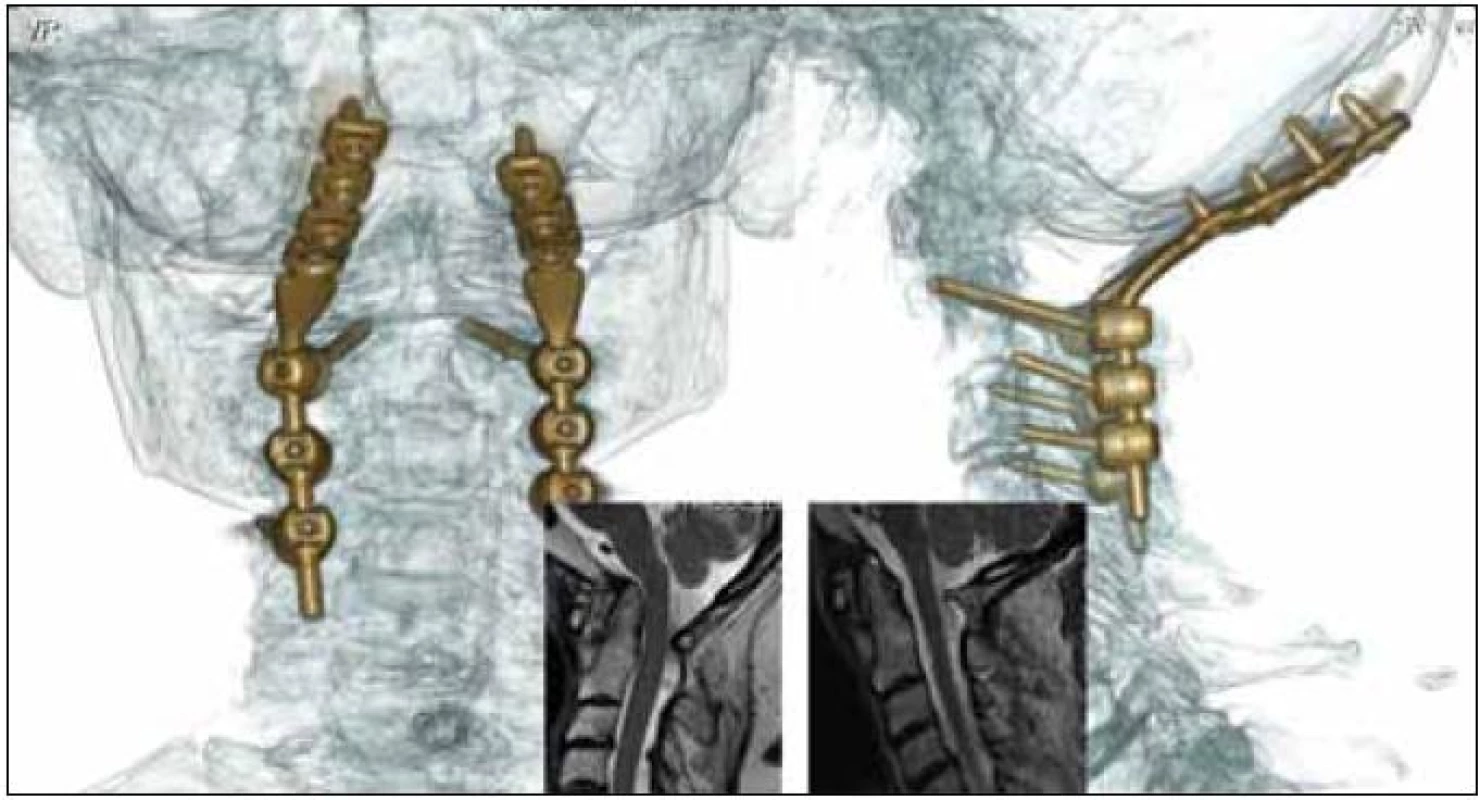
Operace jsou prováděny v celkové anestezii, pronační poloze na operačním stole. Hlava je zajištěna v Mayfieldově tříbodovém fixatéru nebo náplasťovou fixací v hlavové misce, ramena stažena rovněž náplastí. Kožní řez je veden nad trny ve střední čáře od okciputu po C4–C5. Svaly jsou subperiostálně disekovány od trnů a oblouků krčních obratlů, následně jsou nasazeny retraktory. Disekce je v oblasti C1a C2 vedena dostatečně laterálně za intervertebrální klouby. Je sondován průběh arteria vertebralis na C1, preparovány kořeny C1, C2 bilaterálně. Potom jsou standardním způsobem za kontroly sálovým rentgenovým zesilovačem v boční projekci zavedeny vruty do C1, C2. Následně je nasazena tyč, a pokud je třeba, je využito redukčních možností instrumentaria. Tyč je fixována matkami, které kromě fixace tyče zajistí zrušení polyaxiality šroubů. Následně je upraven tvar autologního štěpu, který byl odebrán z lopaty kosti kyčelní na počátku operace. Štěp je fixován mezi oblouky C1, C2 drátěnou kličkou nebo kostním stehem. Obdobně je prováděna okcipitocervikální stabilizace, samozřejmě se zavedením vrutů do týlní kosti a C2, poté dále dle případného postižení subaxiální krční páteře i do laterálních mas obratlů C3, C4 a níže, většinou s vynecháním obratle C1, následným naložením předtvarovaných tyčí zakončených okcipitální dlahou. Zásadní je volit takový rozsah stabilizace, aby dostatečně řešil patologii, nicméně nezbytnost fixace každého dalšího pohybového segmentu musí být bedlivě zvažována. Pro okcipitocervikální stabilizaci je zásadní i správné nastavení úhlu hlavy vůči páteři tak, aby byl po stabilizaci zajištěn horizontální pohled nemocného. Při nesprávné fixaci do předklonu může výkon kromě sociální mutilace zapříčinit nemocnému i polykací obtíže.
Na konci výkonu je do operační rány vložen drén aktivního sání. Sutura je provedena ve třech až čtyřech vrstvách.
Nemocní jsou vertikalizováni první pooperační den, je provedena pooperační grafická kontrola sestávající se z nativních rentgenových snímků v základní projekci a CT. Je-li postavení krční páteře a instrumentace vyhovující, není vyžadováno setrvání nemocného v krčním límci. Stehy jsou ponechány do desátého pooperačního dne a po jejich vynětí je možno započít se šetrnou rehabilitací paravertebrálních svalů.
Vzhledem k tomu, že oblast C1/C2 je odpovědná za cca 50 % rozsahu rotace a C0/C1 50 % flexe a extenze krční páteře, přinášejí tyto výkony významné omezení rozsahu pohybu krční páteře, které je následně alespoň částečně kompenzováno zbylými pohybovými segmenty krční páteře [63]. Stabilizace horní krční páteře nebo kraniocervikálního přechodu vede k přetížení subaxiální krční páteře. Kraus et al v roce 1991 publikovali výsledky své studie, která se zabývala významem rozsahu stabilizace v této oblasti vzhledem k progresi postižení subaxiální krční páteře. Zjistili, že u 36 % nemocných po stabilizaci C0–C2 se objeví nové subluxace na dolní krční páteři během 2,6 roku po operaci, zatímco stejný obraz nalezli jen u 5,5 % nemocných po stabilizaci C1/C2 během devíti let po výkonu. Je tedy zřejmé, že rozsah stabilizace musí být velmi pečlivě zvážen a krátká stabilizace C1/C2, pokud je dostačující pro řešení patologické situace, je dnes jasně preferovaným výkonem [64].
Jak vyplývá z předchozího textu, je chirurgie jediná léčebná modalita, která je schopna zabránit progresi neurologické léze způsobené revmatickou nestabilitou v oblasti kraniocervikálního přechodu [25,50,65–68]. Chirurgie však rovněž dokáže zajistit podmínky pro minimálně částečnou úpravu neurologického deficitu. Casey et al publikovali skupinu 134 nemocných s RA, kteří byli operováni pro symptomatické míšní komprese. Padesát osm procent nemocných, kteří byli před výkonem klasifikováni jako Ranawat IIIA, se po operaci zlepšilo na stupeň I či II, stejného výsledku však bylo dosaženo pouze u 20 % nemocných vstupně klasifikovaných jako Ranawat IIIB. Ve skupině IIIB byl zároveň zjištěn významně vyšší výskyt pooperačních komplikací a nemocní vyžadovali delší pooperační hospitalizaci [69]. Obdobné výsledky referovali ve své sestavě 90 nemocných Peppelmann et al, kteří zaznamenali zlepšení o nejméně jeden stupeň klasifikace u 86,7 % nemocných. Zajímavým zjištěním bylo, že pokud byla příčinou neurologické léze izolovaná atlantoaxiální dislokace, došlo k regresi neurologického deficitu v 94,8 % případů, zatímco stejný výsledek byl dosažen pouze u 76 % nemocných s kombinovaným nálezem atlantoaxiální dislokace a kraniální migrace čepovce [70].
Je tedy zřejmé, že předoperační přítomnost neurologického deficitu a nález komplexního postižení kraniocervikálního přechodu (atlantoaxiální dislokace a zároveň kraniální migrace zubu čepovce) představují faktory významně negativně ovlivňující výsledek chirurgické léčby.
Závěr
Revmatoidní artritida je systémové zánětlivé onemocnění neznámé etiologie, jehož základním projevem je infiltrace kloubního prostředí zánětlivými buňkami, hyperplazie synoviální tkáně a postupná destrukce chrupavky a přiléhající kosti. Klinicky se nejčastěji projevuje chronickou symetrickou polyartritidou s následným vznikem kloubních destrukcí a deformit. V oblasti páteře nejčastěji postihuje kraniocervikální přechod. Rozvolněním vazivových struktur vzniká až život ohrožující nestabilita, jejím projevem může být i náhlé úmrtí. Zahájení agresivní farmakoterapie, včetně cytostatické a biologické léčby, může zabránit či zpomalit progresi onemocnění. Kontrolní nativní rentgenové snímky krční páteře by měly být provedeny nejpozději do dvou let od počátku onemocnění a poté periodicky opakovány. V případě známek rozvoje radiologické nestability nebo neurologického deficitu je nutné doplnit vyšetření MR nebo CT. Chirurgická terapie by měla být indikována na podkladě grafických nálezů, a to ještě před rozvojem neurologické symptomatologie. Rozsah výkonu by měl být plánován tak, aby řešil patologickou situaci stabilizací co možná nejkratšího úseku krční páteře. Multidisciplinární přístup založený na spolupráci neurochirurga či ortopeda s revmatologem, neurologem a rehabilitačním lékařem je nezbytnou podmínkou úspěšné léčby revmatické nestability v oblasti kraniocervikálního přechodu.
Práce nebyla podpořena grantem, nebyl využit ani jiný zdroj prostředků.
MUDr. Petr Vaněk
1. LF UK a ÚVN Praha
U Vojenské nemocnice 1200
169 02 Praha 6
e-mail: petr.vanek@uvn.cz
Recenzenti:
prof. MUDr. Petr Suchomel, Ph.D.
doc. MUDr. Martin Sameš, Ph.D.
doc. MUDr. Lumír Hrabálek, Ph.D.Přijato k recenzi: 1. 4. 2012
Přijato do tisku: 18. 5. 2012MUDr. Petr Vaněk (1972)
Doktor Petr Vaněk se narodil 23. 10. 1972 v Mladé Boleslavi. V roce 1997 promoval na 3. LF UK v Praze. Klinickou praxi zahájil jako sekundární lékař na neurochirurgickém oddělení Masarykovy nemocnice v Ústí nad Labem. První atestaci, ze všeobecné chirurgie složil v roce 2000. Druhou atestaci, v oboru neurochirurgie složil v roce 2005. Od roku 2006 pracuje na Neurochirurgické klinice 1. LF UK a ÚVN Praha. Zde se podílel na založení spondylochirurgického oddělení v rámci kliniky. Spondylochirurgický program zde nabízí chirurgickou léčbu všech typů postižení páteře kromě komplexních deformit. Speciální pozornost je věnována miniinvazivním stabilizacím páteře a revmatochirurgii. Je prvním autorem 16 publikací s impakt faktorem, spoluautorem dvou monografií, přednesl více než 150 sdělení na odborných domácích i zahraničních sjezdech, podílel se na řešení pěti grantových projektů a provedl 14 instruktážních operací v zahraničí. Je členem České neurochirurgické společnosti a České spondylochirurgické společnosti ČLS JEP, Spine Society of Europe, AO Spine International.
Sources
1. Pavelka K. Revmatologie. 2nd ed. Praha: Galén 2010.
2. Wasserman BR, Moskovich R, Razi AE. Rheumatoid arthritis of the cervical spine – clinical consideration. Bull NYU Hosp Jt Dis 2011; 69(2): 136–148.
3. Garrod AE. A treatise on rheumatism and rheumatoid arthritis. London: Grifins Medical Series, Charles Grifin & Co 1890.
4. Davis FW jr, Markley HE. Rheumatoid arthritis with death from medullary compression. Ann Intern Med 1951; 35(2): 451–445.
5. Kornblum D, Clayton ML, Nash HH. Non-traumatic cervical dislocation in rheumatoid spondylitis. J Am Med Assoc 1952; 149(5): 431–435.
6. Bland JH. Rheumatoid arthritis of the cervical spine. Bull Rheum Dis 1967; 18(2): 471–476.
7. Fielding JW, Cochran GB, Lawsing JF jr, Hohl M. Tears of transverse ligament of the atlas. A clinical and biomechanical study. J Bone Joint Surg Am 1974; 56(8): 1683–1691.
8. Štulík J et al. Poranění krční páteře. 1st ed Praha: Galén 2010.
9. Moskovich R, Shott S, Yhang ZH. Does the cervical canal to body ratio predict spinal stenosis? Bull Hosp Jt Dis 1996; 55(2): 61–71.
10. Matthews JA. Atlanto-axial subluxtion in rheumatoid arthritis. A 5-year follow-up study. Ann Rheum Dis 1974; 33(6): 526–531.
11. Crockard HA. Surgical management of cervical rheumatoid problems. Spine 1995; 20(23): 2584–2590.
12. Weissman BN, Aliabadi P, Weinfel MS, Thomas WH, Sosman JL. Prognostic features of atlantoaxial subluxation in rheumatoid arthritis patient. Radiology 1982; 144(4): 745–751.
13. Agarwal AK, Peppelman WC, Kraus DR, Eisenbeis C. The cervical spine in rheumatoid arthritis. BMJ 1993; 306(6879): 79–80.
14. Halla JT, Hardin JG, Vitek J, Alarcón GS. Involvement of cervical spine in rheumatoid arthritis. Arthritis Rheum 1989; 32(5): 652–659.
15. Riise T, Jacobsen BK, Gran JT. High mortality in patients with rheumatoid arthritis and atlantoaxial subluxation. J Rheumatol 2001; 28(11): 2425–2429.
16. Sunahara N, Matsunaga S, Mori T, Ijiri K, Sakou T. Clinical course of conservatively managed rheumatoid arthritis patients with myelopathy. Spine 1997; 22(22): 2603–2607.
17. Yurube T, Sumi M, Nishida K, Takabatake M, Kohyama K, Matsubara T et al. Progression of cervical spine instabilities in rheumatoid arthritis. A prospective cohort study of outpatients over 5 years. Spine 2011; 36(8): 647–653.
18. Mikulowski P, Wollheim FA, Rotmil P, Olsen I. Sudden death in rheumatoid arthritis with atlanto-axila dislocation. Acta Med Scand 1975; 198(6): 445–451.
19. Paus AC, Steen H, Roislien J, Mowinckel P, Teigland J. High mortality rate in rheumatoid arthritis with subluxation of the cervical spine. A cohort study of operated and nonoperated patients. Spine 2008; 33(21): 2278–2283.
20. Boden SD, Dodge LD, Bohlman HH, Rechtine GR. Rheumatoid arthritis of the cervical spine. A long--term analysis with predictor of paralysis and recovery. J Bone Joint Surg Am 1993; 75(9): 1282–1297.
21. Marks JS, Sharp J. Rheumatoid cervical myelopathy. Q J Med 1981; 50(199): 307–319.
22. Rawlins BA, Girardi FP, Boachie-Adjei O. Rheumatoid arthritis of the cervical spine. Rheum Dis Clin North Am 1998; 24(1): 55–65.
23. Rana NA. Natural history of atlanto-axial subluxation in rheumatoid arthritis. Spine 1989; 14(10): 1054–1056.
24. Menezes AH, VanGilder JC, Clark CR, el-Khoury G. Odontoid upward migration in rheumatoid arthritis. An analysis of 45 patients with cranial settling. J Neurosurg 1985; 63(4): 500–509.
25. Rana NA, Hancock DO, Taylor AR, Hill AG. Upward translocation of the dens in rheumatoid arthritis. J Bone Joint Surg Br 1973 : 55(3): 471–477.
26. Ranawat CS, O’Leary P, Pellicci P, Tsairis P, Marchisello P, Dorr L. Cervical spine fusion in rheumatoid arthritis. J Bone Joint Surg Am 1979; 61(7): 1003–1010.
27. Steinbrocker O, Traeger CH, Batterman RC. Therapeutic criteria in rheumatoid arthritis. JAMA 1949; 140(8): 659–662.
28. Kwek TK, Lew TW, Thoo FL. The role of preoperative cervical spine X-rays in rheumatoid arthritis. Anaesth Intensive Care 1998; 26(6): 636–641.
29. Collins DN, Barnes CL, FitzRandolf RL. Cervical spine instability in rheumatoid patients having total hip or knee arthroplasty. Clin Orthop Relat Res 1991; 272 : 127–135.
30. Clark CR, Goetz DD, Menezes AH. Arthrodesis of the cervical spine in rheumatoid arthritis. J Bone Joint Surg Am 1989; 71(3): 381–392.
31. Casey AT, Crockard HA, Stevens J. Vertical translocation. Part II. Outcomes after surgical treatment of rheumatoid cervical myelopathy. J Neurosurg 1997; 87(6): 863–869.
32. Casey AT, Crockard HA, Geddes JF, Stevens J. Vertical translocation: the enigma of the disappearing atlantodens interval in patients with myelopathy and rheumatoid arthritis. Part I. Clinical, radiological, and neuropatological features. J Neurosurg 1997; 87(6): 856–862.
33. Boden SD. Rheumatoid arthritis of the cervical spine. Surgical decision making based on predictors of paralysis and recovery. Spine 1994; 19(20): 2275–2280.
34. McGreger M. The significance of certain measurements of the skull in the diagnosis of basilar impression. Br J Radiol 1948; 21(244): 171–181.
35. McRae DL, Barnum AS. Occipitalization of the atlas. Am J Roentgenol Radium Ther Micl Med 1953; 70(1): 23–46.
36. Chamberlain WE. Basilar impression (platybasia): a bizarre development of anomaly of the occipital bone upper cervical spine with striking and misleading neurologic manifestations. Yale J Biol Med 1939; 11(5): 487–496.
37. Redlund-Johnell I, Pettersson H. Radiographic measurements of the cranio-vertebral region. Designed for evaluation of abnormalities in rheumatoid arthritis. Acta Radiol Diagn 1984; 25(1): 23–28.
38. Riew KD, Hillibrand AS, Palumbo MA, Sethi N, Bohlman HH. Diagnosing basilar invagination in the rheumatoid patient. The reliability of radiographic criteria. J Bone Joint Surg Am 2001; 83A(2): 194–200.
39. Einig M, Higer HP, Meairs S, Faus-Tinnefeldt G, Kapp H. Magnetic resonance imaging of the craniocervical junction in rheumatoid arthritis: value, limitations, indications. Skeletal Radiol 1990; 19(5): 341–346.
40. Breedveld FC, Algra PR, Vielvoye CJ, Cats A. Magnetic resonance imaging in the evaluation of patients with rheumatoid arthritis and subluxation of the cervical spine. Arthritis Rheum 1987; 30(6): 624–629.
41. Petterson H, Larsson EM, Holtás S, Cronqvist S, Egund N, Zygmunt S et al. MR imaging of the cervical spine in rheumatoid arthritis. AJNR Am J Neuroradiol 1988; 9 : 573–577.
42. Bundschuh C, Modic MT, Kerney F, Morris R, Deal C. Rheumatoid arthritis of the cervical spine: surface coil MR imaging. AJR Am J Roentgeol 1988; 151(1): 181–187.
43. Reijnierse M, Breedveld FC, Kroon HM. Are magnetic resonance flexion views useful in evaluating the cervical spine of patients with rheumatoid arthritis? Skeletal radiol 2000; 29(2): 85–89.
44. Bell GR, Stearns KL. Flexion-extension MRI of the upper rheumatoid cervical spine. Orthopedics 1991; 14(9): 969–974.
45. Miyata M, Neo M, Ito H, Yoshida M, Miyaki K, Fujibayashi S et al. Is rheumatoid arthritis a risk factor for a high-riding vertebral artery? Spine 2008; 33(18): 2007–2011.
46. Miyata M, Neo M, Ito H, Yoshida M, Fujibayashi S, Nakamura T. Rheumatoid arthritis as a risk factor for a narrow C-2 pedicle: 3D analysis of the C2 pedicel screw trajectory. J Neurosurg Spine 2008; 9(1): 17–21.
47. Toolanen G, Knibestol M, Larsson SE, Landman K. Somatosensory evoked potentials (SSEPs) in rheumatoid cervical subluxation. Scand J Rheumatol 1987; 16(1): 17–25.
48. Dvorák J, Herdmann J, Janssen B. Motor-evoked potentials in patients with cervical spine disorders. Spine 1990; 15(10): 1013–1016.
49. Borenstein D. Inflammatory arthritides of the spine. Surgical versus nonsurgical treatment. Clin Orthop Rel Research 2006; 443 : 208–221.
50. Kaito T, Hosono N, Ohshima S, Ohwaki H, Takenaka S, Fujiwara H, Makino T, Yonenobu K. Effect of Biological Agents on Cervical Spine Lesions in Rheumatoid Arthritis. Spine. In press 2012.
51. Pellicci PM, Ranawat CS, Tsairis P, Bryan WJ. A prospective study of the progression of rheumatoid arthritis of the cervical spine. J Bone Joint Surg Am 1981; 63(3): 342–350.
52. Suchomel P, Choutka O. Reconstruction of Upper Cervical Spine and Craniovertebral Junction. 1st ed. Berlin: Springer Verlag 2011.
53. Gallie WE. Fracture and dislocations of the cervical spine. Amer J Surg 1939; 46 : 495–499.
54. Brooks AL, Jenkins EW. Atlanto-axial arthrodesis by the wedge compression method. J Bone Joint Surg 1975; 57 : 879–887.
55. Lögters T, Hoppe S, Linhart W, Habermann C, Windlof J, Rueger J et al. On the problem of halo vest treatment in the elderly. Results of a retrospective analysis. Unfallchirurg 2006; 109(4): 306–312.
56. Magerl F, Seemann PS. Stable posterior fusion of gthe atlas and axis by transarticular screw fixation. In: Kehr P, Weidner A (eds). Cervical spine. Wien: Springer 1987 : 322–327.
57. Gluf WM, Schmidt MH, Apfelbaum RI. Atlantoaxial transarticular screw fixation: a review of surgical indications, fusion rate, complications and lessons learned in 191 adult patients. J Neurosurg Spine 2005; 2(2): 155–163.
58. Harms J, Melcher PR. Posterior C1–2 fusion with polyaxial screw and rod fiaxation. Spine 2002; 26(22): 2467–2471.
59. Yoshida M, Neo M, Fujibayashi S, Nakamura T. Comparison of the anatomical risk for vertebral artery injury associated with the C2-pedicle screw and atlantoaxial transarticular screw. Spine 2006; 31(15): 513–517.
60. Johnston RA, Kelly IG. Surgery of the rheumatoid cervical spine. Ann Rheumatic Dis 1990; 49 (Suppl 2): 845–850.
51. Mouchaty H, Perrini P, Conti R, Di Lorenzo N. Craniovertebral juction lesions: our experience with transoral surgical approach. Eur Spine J 2009; 18 (Suppl 1): 13–19.
62. Grob D, Würsch R, Grauer W, Sturzenegger J, Dvorak J. Atlantoaxial fusion and retrodental pannus in rheumatoid arthritis. Spine 1997; 22(14): 1580–1583.
63. Sugimoto Y, Tanaka M, Nakanishi K, Misawa H, Takigawa T, Ozaki T. Assessing the range of cervical rotation in patients with rheumatoid arthritis after atlantoaxial screw fixation using axial CT. Spine 2007; 32(21): 2318–2321.
64. Kraus DR, Peppelman WC, Agarwal AK, DeLeeuw HW, Donaldson WF jr. Incidence of subaxial sbluxation in patients with generalized rheumatoid arthritis who have had previous occipital cervical fusions. Spine 1991; 16 (Suppl 10): S486–S489.
65. Meijers KA, Cats A, Kremer HP, Luyendijk W, Onvlee GJ, Thomeer RT. Cervical myelopathy in rheumatoid arthritis. Clin Exp Rheumatol 1984; 2(3): 239–245.
66. Stulik J, Vyskocil T, Sebesta P, Kryl J. Atlantoaxial fixation using the polyaxial screw-rod system. Eur Spine J 2007; 16(4): 479–484.
67. Suchomel P, Stulík J, Klézl Z, Chrobok J, Lukás R, Krbec M et al. Transarticular fixation of C1–C2: a multicenter retrospective study. Acta Chir Orthop Traumatol Cech 2004; 71(1): 6–12.
68. Krauss WE, Bledsoe JM, Clarke MJ, Nottmeier EW, Pichelmann MA. Rheumatoid Arthritis of the Craniovertebral Junction. Neurosurgery 2010; 66 (Suppl 3): 83–95.
69. Casey AT, Crockard HA, Bland JM, Stevens J, Moskovich R, Ransford AO. Surgery on the rheumatoid cervical spine for the non-ambulant myelopatic patient-too much, too late? Lancet 1996; 347(9007): 1004–1007.
70. Peppelman WC, Kraus DR, Donaldson WF, Argawal A. Cervical spine surgery in rheumatoid arthritis: improvement of neurologic deficit after cervical spine fusion. Spine 1993; 18(16): 2375–2379.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2012 Issue 3-
All articles in this issue
- Chirurgická léčba revmatického postižení kraniocervikálního přechodu
- Konformačně specifické protilátky a diagnostika prionových chorob
- Low back pain a deprese – vzájemný vztah
- Neurosyfilis
- Diagnostika a možnosti léčby Niemann-Pickovy choroby typ C
- Asociace polymorfizmů v genu pro matrix metalloproteinázu-2 a tkáňový inhibitor metalloproteinázy-2 s roztroušenou sklerózou
- Neurofyziologická diagnostika poškození loketního nervu v oblasti lokte
- Rozšířený transnazální endoskopický přístup k nádorům lebeční spodiny a očnice
- Stanovení mozečkové dominance podle asymetrie svalového tonu končetin
- Operační léčba syndromu tarzálního tunelu
- Zadní interhemisférický prekuneální/transspleniální přístup k intrinsickým mozkovým lézím
- Atypický paraneoplastický neurologický syndrom – kazuistika
- Oboustranná léze n. phrenicus manifestující se jako ortopnoe – kazuistiky tří případů
- Alzheimerova nemoc probíhající pod obrazem kortikobazální degenerace – kazuistika
- Adherence k léčbě u pacientů se schizofrenií
- Tau protein a anti-tau protilátky u pacientů s roztroušenou sklerózou
- Vzorec posturálnych zmien v súvislosti so symetrickou vibráciou krčných svalov
- Neurenterická cysta kraniocervikální junkce – kazuistika
- Rozsáhlý epidurální absces cervikotorakální páteře řešený kombinovaným přístupem – kazuistika
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Neurosyfilis
- Operační léčba syndromu tarzálního tunelu
- Oboustranná léze n. phrenicus manifestující se jako ortopnoe – kazuistiky tří případů
- Diagnostika a možnosti léčby Niemann-Pickovy choroby typ C
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


