-
Medical journals
- Career
Neurosyfilis
: D. Vaňousová 1; R. Černý 2; H. Zákoucká 3; P. Kožner 4; D. Jilich 5; J. Lisý 6; J. Hercogová 1; L. Machala 7
: Dermatovenerologická klinika 2. LF UK a Nemocnice Na Bulovce, Praha 1; Neurologická klinika dospělých 2. LF UK a FN v Motole, Praha 2; Národní referenční laboratoř pro syfilis, Státní zdravotní ústav, Praha 3; Oční oddělení, Nemocnice Na Bulovce, Praha 4; Klinika infekčních a tropických nemocí 1. LF UK a Nemocnice Na Bulovce, Praha 5; Klinika zobrazovacích metod 2. LF UK a FN v Motole, Praha 6; Klinika infekčních nemocí 3. LF UK a Nemocnice Na Bulovce, Praha 7
: Cesk Slov Neurol N 2012; 75/108(3): 297-302
: Review Article
Syfilis je staré onemocnění, jehož výskyt v rozvinutých zemích ve druhé polovině minulého století dočasně poklesl, ale které se opět vrací. V České republice byla minimální incidence v roce 1990, od té doby u nás vzrostl výskyt syfilis více než šestkrát. Zvláště ohroženi jsou homosexuální muži, zejména s HIV infekcí, a toxikomani. K postižení nervového systému může dojít během kteréhokoliv stadia syfilis; v současné době převládají časnější formy neurosyfilis, pozdní komplikace se vyskytují vzácně. Diagnóza syfilis je založena především na sérologických testech. Ve skríningu se používá kombinace metod nespecifických (netreponemových) a specifických (treponemových), pro konfirmaci se používají testy specifické. Klinický obraz neurosyfilis je velmi pestrý a v diagnostice má základní význam komplexní vyšetření likvoru včetně sérologických testů nespecifických a specifických. Diagnóza syfilis podléhá povinnému hlášení a rovněž léčba je ze zákona povinná. Základním lékem neurosyfilis je benzylpenicilin, ostatní antibiotika jsou méně účinná. Po ukončení léčby syfilis zůstávají všichni pacienti v dlouhodobé dispenzarizaci dermatovenerologa. Vzhledem ke složitosti klinické i laboratorní problematiky neurosyfilis je pro stanovení správné diagnózy a rozhodnutí o optimální terapii vždy nutná úzká spolupráce neurologa, dermatovenerologa a laboratorního specialisty.
Klíčová slova:
syfilis – neurosyfilis – diagnóza – terapieÚvod
Syfilis se u nás vyskytuje již více než 500 let a lékaři v minulosti toto onemocnění dobře znali, ovšem díky zavedení penicilinu se výskyt syfilis u nás výrazně snížil a znalost její problematiky postupně poklesla. V posledním desetiletí však počet případů syfilis u nás opět narůstá, a je proto nutné, aby zdravotníci toto onemocnění dobře znali a s jeho výskytem počítali.
Původcem syfilis je spirocheta Treponema pallidum subsp. pallidum (T.p.p). K přenosu dochází hlavně sexuálně (90 %) a také transplacentárně či během porodu [1].
Podle Světové zdravotnické organizace se každoročně nakazí asi 12 milionů lidí a syfilis je celosvětově zodpovědná přibližně za 0,3 % všech úmrtí [2,3].
Do konce 20. století byl výskyt syfilis ve vyspělých zemích nízký, od roku 2000 však v USA, Kanadě a Evropě, zvláště východní, výskyt syfilis trvale roste [4,5]. Zvýšený výskyt je mezi homosexuály, zejména HIV pozitivními, a toxikomany [6,7].
U nás se po druhé světové válce pohybovala roční incidence syfilis kolem 100/100 000, ale díky tzv. akci PN (pohlavní nemoci) její výskyt trvale klesal. Do roku 1990 klesla roční incidence na 1,6/100 000, pak však začala opět stoupat. V roce 2010 byla podle předběžných údajů incidence syfilis 10,3/100 000 (1 022 případů) a maximální výskyt byl zatím v roce 2001 (graf 1). Tento trend odráží rozsáhlé změny v naší společnosti a také imigrační vlny – např. v rekordním roce 2001 byl podíl cizinců 53,1 %. Nejčastěji je u nás syfilis diagnostikována u žen ve věku 25 let a u mužů ve věku 30 let [8–10].
1. Celkové počty diagnostikovaných případů syfilis v České republice. 
Patogeneze a klinický obraz neurosyfilis
V místě kontaktu vniká T.p.p rychle sliznicí či kožním traumatem a následuje diseminace po organizmu. V místě vstupu se za tři týdny (10–90 dní) vytvoří tvrdý vřed, který je základním projevem primárního stadia syfilis a představuje její nejinfekčnější formu. Spontánně se tvrdý vřed hojí obvykle za dva až osm týdnů.
Po přibližně devíti týdnech od nákazy se dostaví stadium sekundární. Klinické příznaky jsou velmi pestré, typické jsou různé kožní exantémy. Neléčené projevy sekundární syfilis se obyčejně během 3–12 týdnů spontánně vyhojí a následuje latentní stadium.
První dva roky od nákazy představují časnou syfilis, kdy je pacient infekční. Po dvou letech již jde o pozdní syfilis a pacient již je obvykle neinfekční.
Terciární stadium s pozdními následky neléčené infekce se rozvíjí na podkladě endarteriitidy a periarteriitidy malých a středních cév po řadě roků až desítek let. Mezi typické projevy patří postižení nervového a kardiovaskulárního systému a kůže.
Patogeneze postižení nervového systému zůstává dosud značně nejasná. Roli hraje jak neuroinvazivita infikujícího kmene T.p.p., tak i imunoreaktivita nakaženého jedince [11,12]. K rozvoji neurosyfilis může dojít kdykoliv během primárního či sekundárního stadia (časná neurosyfilis) nebo terciárního stadia (pozdní neurosyfilis) (tab. 1).
1. Klinická manifestace a laboratorní nálezy u neurosyfilis, upraveno podle [35]. ![Klinická manifestace a laboratorní nálezy u neurosyfilis, upraveno podle [35].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/f929bffa02c86567a8f20b042dfe78b2.png)
Do CNS jsou spirochety schopné pronikat už hodiny či dny po inokulaci a u více než 40 % pacientů se rozvíjí asymptomatická neurosyfilis. Ta je definována jako abnormální likvorový nález při absenci neurologických příznaků. V moku je lymfocytární pleocytóza se zvýšenou hladinou proteinů a/anebo pozitivita nespecifických i specifických sérologických reakcí [13].
Samotný průnik spirochet do CNS však nemusí znamenat další progresi onemocnění. Abnormální likvorový nález může být pouze přechodný a většinou se do dvou let spontánně normalizuje [14]. Do klinicky manifestní formy přechází jen asi 5 % případů neléčené asymptomatické neurosyfilis. Riziko progrese je výrazně vyšší u imunodeficitních pacientů, zvláště s infekcí HIV [15].
Nejčastěji dochází k invazi do CNS spojené se zánětlivým postižením mening během sekundárního stadia a v období časné latence, kdy vrcholí generalizace infekce.
Akutní syfilitická meningitida se projevuje meningeálními příznaky, často s poruchami mozkových nervů, horečka bývá jen vzácně. V krvi i likvoru jsou vysoké hladiny protilátek, které jsou reakcí na přítomnost virulentních spirochet. V likvoru je zvýšený tlak, lymfocytární pleocytóza, zvýšená hladina proteinů a až u 50 % pacientů bývá hypoglykorachie [13].
V pozdním stadiu syfilis, v období orgánových projevů, dochází k postižení mening, parenchymu CNS a cév, které se vyvíjí roky až desítky let po primární infekci. Klinicky manifestní neurosyfilis se v této fázi dělí na meningovaskulární a parenchymatózní, ovšem i v tomto období může být přítomen pouze abnormální likvorový nález bez klinické symptomatologie.
Meningovaskulární syfilis se rozvíjí za pět až sedm let po primární infekci a vzniká na podkladě zánětlivé obliterační endarteriitidy se vznikem trombóz, aneuryzmat a následných hemoragií, které vedou k ischemickým změnám CNS. Typickou manifestací je obraz cévní mozkové příhody u relativně mladé osoby s postižením v oblasti arteria cerebri media či arteria basilaris, méně často jsou postiženy cévy míšní. V moku je pravidelně proteocytologická asociace s pozitivitou nespecifických i specifických reakcí.
Parenchymatózní syfilis je považována již za projev terciárního stadia a dělí se na progresivní paralýzu a tabes dorsalis, vyskytnout se mohou i formy smíšené [16]. V současné době je výskyt těchto forem neurosyfilis v rozvinutých zemích vzácný [17].
Progresivní paralýza se obvykle rozvíjí za 10–20 let po infekci, možný je však i dřívější výskyt a postihuje kolem 5 % neléčených pacientů. Příčinou je chronická progresivní frontotemporální meningoencefalitida s kortikální atrofií a následným rozvojem demence. V klinickém obraze dominují psychopatologické projevy s plíživým rozvojem osobnostních změn, rozvrat intelektu a psychotické příznaky s bludy a halucinacemi [18]. S postupem onemocnění se objevuje bilaterální Argyll--Robertsonův příznak s malou a nepravidelnou zorničkou s reakcí na konvergenci, ale nikoli na světlo. V likvoru bývá proteocytologická asociace s pozitivitou nespecifických i specifických reakcí. Stav progreduje do obrazu terminální demence a onemocnění pak během 3–5 let končí fatálně [16].
Tabes dorsalis vzniká 10 až 15 let po infekci. Na podkladě autoimunitního procesu dochází k leptomeningeálnímu zánětu dorzálních nervových kořenů, atrofiím zadních míšních provazců s následnou ataxií, bolestmi; může být i atrofie optického nervu. Spirochety v ložiscích nejsou přítomny. Onemocnění začíná bolestmi vystřelujícími do dolních končetin, postupně vyhasínají reflexy dolních končetin a dochází ke ztrátě proprioreceptivního a vibračního čití a ataxii (pozitivní Rombergův příznak). U 50 % pacientů bývá pozitivní Argyll-Robertsonův příznak. Cytologický a biochemický nález v likvoru může být patologický, ale i normální. Sérologické testy jsou slabě pozitivní a v likvoru mohou být i negativní [16].
Kdykoliv po iniciální infekci se mohou v CNS objevit gumata. Guma je ostře ohraničené ložisko granulační tkáně se strukturou specifického granulomu s centrální kaseifikací [19]. Příznaky závisí na lokalizaci a odpovídají expanzivnímu procesu, gumata mohou ovšem být i klinicky němá [20].
Oční syfilis může vzniknout kdykoliv během časné i pozdní fáze infekce. Typickým projevem je Argyll-Robertsonova zornice, přítomná ovšem až v pozdních stadiích onemocnění. V časném stadiu se vyskytuje obvykle iridocyklitida nebo uveitida následkem depozice imunokomplexů, později se objevuje neuritida či atrofie optického nervu, většinou jednostranná. Oční syfilis je nutno považovat i bez jiných projevů postižení CNS za formu neurosyfilis a jako taková musí být adekvátně léčena [21].
Syfilis ucha je vzácnou formu neurosyfilis vyskytující se častěji u vrozené infekce. Projevuje se obvykle náhle vzniklou jednostrannou senzoneurální poruchou sluchu. Jediným projevem může být i tinitus a likvorový nález bývá obvykle normální [22].
Laboratorní diagnostika syfilis a neurosyfilis
Spolehlivé stanovení diagnózy neurosyfilis je komplikované a lze jej učinit pouze na základě komplexního zhodnocení anamnestických údajů, klinického nálezu a výsledků řady laboratorních vyšetření, především sérologického vyšetření krve a mozkomíšního moku. Nezbytnou součástí vyšetření likvoru je rovněž komplexní biochemická a cytologická analýza.
Základem diagnostiky syfilis je potvrzení nebo vyloučení přítomnosti infekce T.p.p. pomocí sérologických testů. Při vyhledávání syfilis se standardně používá kombinace dvou typů skríningových testů, které jsou představovány jednak nespecifickými reakcemi netreponemovými a jednak specifickými reakcemi treponemovými.
Testy netreponemové prokazují protilátky proti kardiolipinovým (fosfolipidovým) antigenům uvolňovaným z tkání vlivem zánětu při syfilis. Klasickým nespecifickým testem je Bordett-Wassermanova reakce (BWR), která byla nahrazena jednoduššími a přesnějšími reakcemi, jako je VDRL (Veneral Diseases Research Laboratories) či RRR (Rapid Reagin Reaction).
Pozitivita netreponemových testů nastupuje tři až čtyři týdny po nákaze a vrcholí během sekundárního stadia či v časné latenci. Titry korelují s aktivitou onemocnění, a proto se užívají k hodnocení úspěšnosti léčby či odhalení relapsu a reinfekce. Po úspěšné léčbě klesají netreponemové testy k negativitě do šesti měsíců až jednoho roku. Titry však klesají i u neléčených pacientů a přibližně u třetiny neléčených pacientů je VDRL po několika letech negativní. Negativní mohou být netreponemové testy také u HIV pozitivních pacientů či v důsledku tzv. zonálního fenoménu (paradoxní negativita antifosfolipidových protilátek u akutní aktivní syfilis), a proto je nutné kombinovat je s testy treponemovými. Falešně pozitivní mohou netreponemové testy být při některých akutních virových infekcích (varicela, příušnice, primoinfekce virem Epsteina-Barrové, hepatitidy), malárii, po infarktu myokardu či jiném poškození tkání (popálenina, crush syndrom), u toxikomanů a v graviditě [23].
Z treponemových metod se nejčastěji užívá test TPHA (Treponema Pallidum Haemagglutination Assay) nebo TP-PA (Treponema Pallidum Particle Agglutination); lze použít i průkaz protilátek pomocí metody ELISA či EIA, chemiluminiscenční nebo imunochromatografické [24].
K sérokonverzi specifických testů dochází u imunokompententních osob již 4–5 týdnů po infekci, ovšem na počátku primárního stadia mohou být i tyto testy ještě negativní.
Při pozitivitě skríningových testů se provádí potvrzení diagnózy testy konfirmačními. Mezi tyto testy patří FTA-ABS test IgM a IgG (Fluorescent Treponemal Antibody Absorption Test), 19S IgM SPHA (Solid Phase Haemagglutination Assay) a Western Blot (WB) IgM a IgG. Ve sporných případech je možné použít průkaz nukleové kyseliny T.p.p. polymerázovou řetězovou reakcí (PCR) [25].
V sekundárním stadiu jsou netreponemové i treponemové testy výrazně pozitivní. V dalším průběhu může pozitivita nespecifických testů vymizet, ale specifické IgG protilátky zůstávají vždy pozitivní do konce života. Falešná pozitivita specifických testů může být při borelióze, virových hepatitidách, malárii, autoimunitních chorobách, některých malignitách, u toxikomanů a také při nevenerických treponematózách [23,26].
V diagnostice neurosyfilis má klíčovou úlohu sérologické, cytologické a biochemické vyšetření mozkomíšního moku. K sérologickému vyšetření likvoru se podobně jako při vyšetření krve používají netreponemové i treponemové testy, v nejasných případech lze též použít PCR [27–29].
Pozitivita VDRL v likvoru spolu s pozitivitou testů treponemových (TPHA, FTA--ABS) velmi specificky svědčí pro postižení CNS; falešná pozitivita může být jen v případě kontaminace likvoru krví. Proto se současně s vyšetřením v likvoru provádí testy v krvi a titry se porovnávají. Negativita VDRL v séru či likvoru však diagnózu neurosyfilis nevylučuje. Vyšší senzitivitu než VDRL má v likvoru test FTA-ABS a jeho negativita v likvoru diagnózu neurosyfilis vylučuje [30].
Vzhledem k možnému pasivnímu přestupu antitreponemových protilátek přes hematoencefalickou bariéru je třeba stanovit jejich intratékální produkci. To je možné pomocí TPHA indexu, který se zjistí porovnáním titru TPHA v likvoru k albuminovému kvocientu (poměr albuminu v likvoru k albuminu v séru); při hodnotách indexu v rozmezí 70–500 je diagnóza neurosyfilis pravděpodobná, při indexu > 500 je vysoce pravděpodobná [31]. Další možností je stanovení hematoencefalické bariéry a intratékální syntézy dle Reibera et al [32].
Pro neurosyfilis svědčí likvorový nález s lymfocytární pleocytózou vyšší než 5 buněk/µl a elevací bílkovin v kombinaci s pozitivní likvorovou sérologií. Vyšetření likvoru má být vždy provedeno u séropozitivních pacientů s neurologickou či oční symptomatologií, u pacientů s aktivní terciární syfilis (aortitida, gumata), při selhání léčby a vždy také u HIV pozitivních pacientů s latentní syfilis. U ostatních pacientů s latentní syfilis či při nejasném stáří infekce má být vyšetření likvoru zváženo zvláště při titrech netreponemového testu vyšších než 1 : 32.
Při vyšetření zobrazovacími metodami se u pacientů s meningovaskulární formou neurosyfilis nalézají v CNS ischemické léze. Gumata CNS jsou na CT snímcích hypodenzní, při vyšetření MR jsou na T1 vážených snímcích hypointenzní až izointenzní a na T2 vážených snímcích hyperintenzní [20]. U pacientů s progresivní paralýzou jsou kortikální atrofie, zejména v temporálních a frontoparietálních oblastech (obr. 1) [33].
1. MR mozku: T2 turbo spin – echo sekvence. V transverzální rovině je patrná lehká kortikální atrofie fronto-parietální oblasti oboustranně. 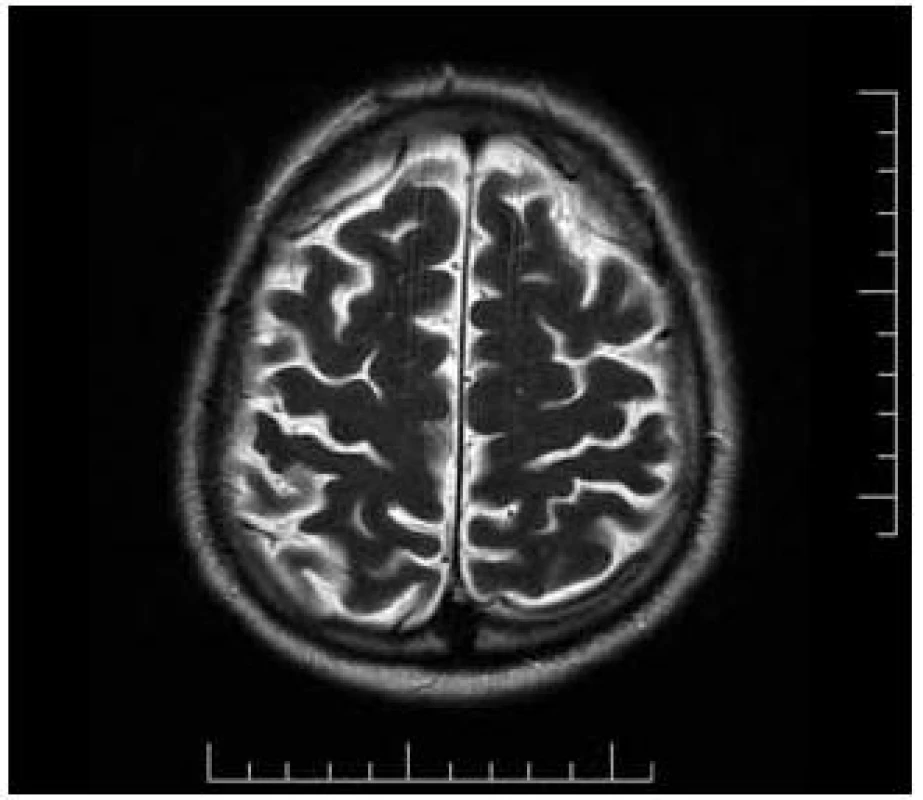
Součástí vyšetření pacientů se syfilis musí být vždy podrobné oftalmologické vyšetření zaměřené na zadní segment a u pozdní syfilis je před léčbou nutné echokardiograficky vyloučit postižení aorty.
Povinnost vyšetřovat na syfilis všechny dospělé hospitalizované pacienty byla zrušena a nyní je povinný skríning prováděn podle vyhlášky č. 195/2005 Sb. pouze u těhotných a novorozenců, dále u žen před umělým přerušením těhotenství a také u venerologických pacientů.
Potvrzení diagnózy syfilis podléhá zákonnému hlášení na formuláři Hlášení pohlavních chorob. Vzhledem k obdobné epidemiologii je dle platných zákonů nutné u všech pacientů s prokázanou syfilis provádět také skríning na infekci HIV a další pohlavně přenosné infekce, jako je kapavka a chlamydiová infekce; častý je u těchto pacientů také první záchyt hepatitidy B a C [34].
Léčba
Léčba syfilis je ze zákona povinná a během léčby se pacient musí zdržet pohlavního styku, což podepisuje při potvrzení diagnózy.
Lékem volby všech forem syfilis je penicilin, který byl sice do léčby syfilis zaveden již v roce 1943, ale T.p.p. na něj zůstává výborně citlivá. Léčba syfilis bez postižení CNS se provádí benzahin-benzylpenicilinen či prokain-benzylpenicilinem v různých schématech podle stadia onemocnění [36,37].
K léčbě neurosyfilis je jednoznačně doporučováno intravenózní podávání benzylpenicilinu v dávce 4–5 milionů IU každých 4 až 6 hodin (celková denní dávka 16–24 milionů IU) po dobu alespoň 14 dní [37,38]. Interval 4 hodiny je doporučen k zajištění konstantní treponemicidní koncentrace v likvoru [39]. Druhou možností je léčba prokain-benzylpenicilinem v celkové denní dávce 3 miliony IU i.m. podávaný současně s probenicidem 500 mg p.o. každých šest hodin po dobu minimálně 14 dní, probenecid ale u nás není registrován. Oba tyto režimy se doporučuje zakončit podáním třech dávek benzathin-benzylpenicilinu v dávce 2 × 1,5 milionů IU i.m. v intervalu jednoho týdne. Léčba samotným benzathin-benzylpenicilinem nezajišťuje spolehlivě dosažení potřebných hladin v likvoru [40].
Po zahájení léčby penicilinem se může u časné syfilis do 24 hod objevit Jarischova-Herxheimerova reakce. Jde o reakci na rozpadové produkty spirochet, jež se projevuje horečkou, myalgiemi, cefaleou, tachykardií a hypotenzí, a k jejímu tlumení lze bez přerušení podávání antibiotika použít salicyláty [41].
Penicilin je jednoznačně nejúčinnějším lékem všech forem neurosyfilis bez spolehlivě plnohodnotné alternativy. U pacientů alergických na penicilin je proto vhodné nejprve zkusit desenzibilizaci a teprve pak zvažovat podání jiného antibiotika [42]. U pacientů s nízkým rizikem zkřížené alergické reakce mezi peniciliny a cefalosporiny lze užít ceftriaxon v celkové denní dávce 2 g i.m. nebo i.v. po dobu 10–14 dní [37]. Problematičtější je volba při závažnější alergii na betalaktamy (peniciliny, cefalosporiny), kterou nelze odstranit desenzibilizací. S ne zcela jistým úspěchem lze užít doxycyklin v dávce dvakrát denně 200 mg p.o. po dobu 28 dní, případně ještě azitromycin, ovšem některé kmeny T.p.p. jsou již na azitromycin a jiné makrolidy rezistentní [43]. Přehled léčby neurosyfilis předkládáme v tab. 2.
2. Léčba neurosyfilis penicilinem a alternativní režimy. 
Po léčbě neurosyfilis se provádí sérologické kontroly krve za jeden až tři měsíce a dále dle výsledků. Kontrolní vyšetření likvoru se doporučuje uskutečnit v odstupu šesti měsíců po dobu tří let či do normalizace likvorového nálezu. V případě úspěšné léčby má pleocytóza vymizet během 12 měsíců a titr VDRL v likvoru poklesnout o dvě ředění nebo se negativizovat do dvou let. Vzestup titru VDRL v likvoru o více než dvě ředění a přetrvávání pleocytózy déle než jeden rok po léčbě se považuje za selhání terapie a vyžaduje novou léčbu [44].
Pacienti léčení pro kteroukoli formu syfilis zůstávají v trvalé dispenzární péči dermatovenerologa do konce života nebo alespoň do věku 65 let (vyhláška č. 39/2012 Sb.).
Závěr
Syfilis, stará pozapomenutá choroba se vrátila a její výskyt ve světě i u nás dále stoupá. Tento trend je zvláště patrný u rizikových skupin populace, jako jsou homosexuální muži a toxikomani. Zvyšuje se i výskyt neurologických komplikací syfilis, a je proto nutné, aby neurologové s jejím výskytem trvale počítali a syfilis zařadili do svých diferenciálně diagnostických rozvah. Protože však syfilis, a neurosyfilis zvláště, mají komplikovaný klinický i laboratorní obraz, je pro správné stanovení diagnózy a volbu optimální léčby naprosto nezbytná úzká spolupráce neurologa s dermatovenerologem a specialistou z diagnostické laboratoře.
doc. MUDr. Ladislav Machala, Ph.D
Klinika infekčních nemocí
3. LF UK a Nemocnice Na Bulovce
Budínova 2
180 81 Praha 8
e-mail: ladimachala@centrum.cz
Přijato k recenzi: 29. 8. 2011
Přijato do tisku: 21. 11. 2011
Sources
1. Hercogova J, Vanousova D. Syphilis and borreliosis during pregnancy. Dermatol Ther 2008; 21(3): 205–209.
2. Global prevalence and incidence of selected curable sexually transmitted infections. Geneva: WHO 2001.
3. The World Health Report 2004 – Changing history. Geneva: WHO 2004.
4. Centers for Disease Control and Prevention (CDC). Primary and secondary syphilis – United States, 2003–2004. MMWR Morb Mortal Wkly Rep 2006; 55(10): 269–273.
5. Uuskula A, Puur A, Toompere K, DeHovitz J. Trends in the epidemiology of bacterial sexually transmitted infections in eastern Europe, 1995–2005. Sex Transm Infect 2010; 86(1): 6–14.
6. Coyne KM, Banks A, Heggie C, Scott CJ, Grover D, Evans C et al. Sexual health of adults working in pornographic films. Int J STD AIDS 2009; 20(7): 508–509.
7. Savage EJ, Hughes G, Ison C, Lowndes CM. Syphilis and gonorrhoea in men who have sex with men: a European overview. Euro Surveill 2009; 14(47): Dostupné z URL: http://www.eurosurveillance.org/ViewArticle.aspx?ArticleId=19417.
8. Pohlavní nemoci 2009. Praha: Ústav zdravotnických informací a statistiky ČR 2010: Dostupné z URL: http://www.uzis.cz/publikace/pohlavni-nemoci-2009.
9. Rozehnalová Z, Hercogová J, Jilich D, Machala, Rozsypal H. Koinfekce syfilis a HIV. Čes-slov Derm 2009; 84(5): 278–283.
10. Zákoucká H, Polánecký V, Kaštánková V. Syphilis and gonorrhoea in the Czech Republic. Eurosurveillance 2004; 9(12): Dostupné z URL: http://www.eurosurveillance.org/ViewArticle.aspx?ArticleId=496.
11. Peeling RW, Hook EW jr. The pathogenesis of syphilis: the Great Mimicker, revisited. J Pathol 2006; 208(2): 224–232.
12. Tantalo LC, Lukehart SA, Marra CM. Treponema pallidum strain-specific differences in neuroinvasion and clinical phenotype in a rabbit model. J Infect Dis 2005; 191(1): 75–80.
13. Lukehart SA, Hook EW jr, Baker-Zander SA, Collier AC, Critchlow CW, Handsfield HH. Invasion of the central nervous system by Treponema pallidum: implications for diagnosis and treatment. Ann Intern Med 1988; 109(11): 855–862.
14. Marra CM, Castro CD, Kuller L, Dukes AC, Centurion-Lara A, Morton WR et al. Mechanisms of clearance of Treponema pallidum from the CSF in a nonhuman primate model. Neurology 1998; 51(4): 957–961.
15. Funnyé A, Akhtar A. Syphilis and human immunodeficiency virus co-infection. J Natl Med Assoc 2003; 95(5): 363–382.
16. Doutlík S. Infekce a nervová soustava. Praha: Avicenum 1987.
17. Golden M, Marra C, Holmes K. Update on syphilis: resurgence of an old problem. JAMA 2003; 290(11): 1510–1514.
18. Lukesova J, Triskova J. Dnešní problematika syfilis a neurosyfilis v psychiatrii. Česk Psychiatr 1982; 78(5): 326–331.
19. Hook EW, 3rd, Marra CM. Acquired syphilis in adults. N Engl J Med 1992; 326(16): 1060–1069.
20. Soares-Fernandes JP, Ribeiro M, Mare R, Magalhaes Z, Lourenco E, Rocha JF. Diffusion-weighted magnetic resonance imaging findings in a patient with cerebral syphilitic gumma. J Comput Assist Tomogr 2007; 31(4): 592–594.
21. Prokosch V, Thanos S. Emerging syphilitic optic neuropathy: critical review and recommendations. Restor Neurol Neurosci 2008; 26(4–5): 279–289.
22. Rothenberg R, Becker G, Wiet R. Syphilitic hearing loss. South Med J 1979; 72(2): 118–120.
23. Zákoucká H. Syfilis – tradiční choroba, současný problém II. Zprávy CEM (SZÚ, Praha) 2007; 16(10–11): 493–497.
24. Larsen S, Johnson R. Diagnostic Tests. In: Larsen S, Pope W, Johnson R (eds). Manual of Tests for Syphilis. Washington: American Public Health Association Publications 1999 : 1–52.
25. Norris S, Weinstock GM. Comparative genomics. In: Radolf J, Lukehart S (eds). Pathogenic Treponema: Molecular And Cellular Biology. Wymondham: Caister Academic Press 2006 : 19–38.
26. Jirouš J, Knappová M, Hercogova J. Možnosti zkřížené reakce v sérologii syfilidy a lymeské borreliózy. Čes-slov Derm 1991; 66(3): 183–188.
27. Woznicova V, Smajs D, Wechsler D, Matejkova P, Flasarova M. Detection of Treponema pallidum subsp. pallidum from skin lesions, serum, and cerebrospinal fluid in an infant with congenital syphilis after clindamycin treatment of the mother during pregnancy. J Clin Microbiol 2007; 45(2): 659–661.
28. Flasarova M, Smajs D, Matejkova P, Woznicova V, Heroldova-Dvorakova M, Votava M. Molekulární detekce a typizace Treponema pallidum subsp. pallidum v klinickém materiálu. Epidemiol Mikrobiol Imunol 2006; 55(3): 105–111.
29. Marra C, Tantalo L, Maxwell C, Dougherty K, Wood B. Alternative cerebrospinal tests to diagnose neurosyphilis in HIV-infected individuals. Neurology 2004; 63(1): 85–88.
30. Timmermans M, Carr J. Neurosyphilis in the modern era. J Neurol Neurosurg Psychiatry 2004; 75(12): 1727–1730.
31. Woznicová V. Neurosyfilis. Prakt Lék 2006; 86(12): 698–702.
32. Reiber H, Peter JB. Cerebrospinal fluid analysis: disease-related data patterns and evaluation programs. J Neurol Sci 2001; 184(2): 101–122.
33. Alam F, Yasutomi H, Fukuda H, Horiguchi J, Murakami Y, Ohshita T et al. Diffuse cerebral white matter T2-weighted hyperintensity: a new finding of general paresis. Acta Radiol 2006; 47(6): 609–611.
34. Branger J, van der Meer JT, van Ketel RJ, Jurriaans S, Prins JM. High incidence of asymptomatic syphilis in HIV-infected MSM justifies routine screening. Sex Transm Dis 2009; 36(2): 84–85.
35. O‘Donnell JA, Emery CL. Neurosyphilis: A Current Review. Curr Infect Dis Rep 2005; 7(4): 277–284.
36. Resl V. Doporučené postupy pro praktické lékaře. Sexuálně přenosné nemoci II. Praha 2002: MZ ČR a ČLS JEP.
37. Centers for Disease Control and Prevention. Sexually Transmitted Diseases Treatment Guidelines, 2010. MMWR 2010; 59(RR12): 1–110.
38. French P, Gomberg M, Janier M, Schmidt B, van Voorst Vader P, Young H. IUSTI: 2008 European Guidelines on the Management of Syphilis. Int J STD AIDS 2009; 20(5): 300–9.
39. Crowe G, Theodore C, Forster GE, Goh BT. Acceptability and compliance with daily injections of procaine penicillin in the outpatient treatment of syphilis-treponemal infection. Sex Transm Dis 1997; 24(3): 127–130.
40. Jorgensen J, Tikjob G, Weismann K. Neurosyphilis after treatment of latent syphilis with benzathine penicillin. Genitourin Med 1986; 62(2): 129–131.
41. Marinella MA. Jarisch-Herxheimer reaction. West J Med 1996; 165(3): 161–2.
42. Robinson JL, Hameed T, Carr S. Practical aspects of choosing an antibiotic for patients with a reported allergy to an antibiotic. Clin Infect Dis 2002; 35(1): 26–31.
43. Matejková P, Flasarová M, Zákoucká H, Borek M, Kremenová S, Arenberger P et al. Macrolide treatment failure in a case of secondary syphilis: a novel A2059G mutation in the 23S rRNA gene of Treponema pallidum subsp. pallidum. J Med Microbiol 2009; 58(6): 832–836.
44. Marra CM, Maxwell CL, Tantalo LC, Sahi SK, Lukehart SA. Normalization of serum rapid plasma reagin titer predicts normalization of cerebrospinal fluid and clinical abnormalities after treatment of neurosyphilis. Clin Infect Dis 2008; 47(7): 893–899.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2012 Issue 3-
All articles in this issue
- Surgical Treatment of Rheumatoid Lesion at Craniocervical Junction
- Conformation Specific Antibodies and Diagnosis of Prion Diseases
- Low Back Pain and Depression – Mutual Relationship
- Neurosyphilis
- Diagnosis and Treatment Options for Niemann-Pick Disease Type C
- An Association between Matrix Metalloproteinase-2 and TIMP-2 +853G/A Gene Polymorphisms and Multiple Sclerosis
- Neurophysiological Diagnosis of the Ulnar Nerve Damage at the Elbow
- Extended Transnasal Endoscopic Approach for Skull Base Tumors and Tumors of the Orbit
- Determination of Cerebellar Dominance from Muscle Tone of the Limbs
- Surgical Treatment of a Tarsal Tunnel Syndrome
- Posterior Interhemispheric Precuneal/Transplenial Approach to Intrinsic Brain Lesions
- Atypical Paraneoplastic Neurological Syndrome – a Case Report
- Bilateral Phrenic Nerve Lesion Manifesting as an Orthopnea – Three Case Reports
- Alzheimer’s Disease Manifesting as Corticobasal Degeneration – Case Report
- Treatment Adherence in Patients with Schizophrenia
- Tau Protein and Anti-Tau Antibodies in Patients with Multiple Sclerosis
- Pattern of Postural Changes after Symmetric Neck Muscle Vibration
- A Dorsal Neurenteric Cyst of the Craniocervical Junction – a Case Report
- An Extensive Epidural Abscess of Cervicothoracic Spine Resolved by a Combined Approach – a Case Report
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Neurosyphilis
- Surgical Treatment of a Tarsal Tunnel Syndrome
- Bilateral Phrenic Nerve Lesion Manifesting as an Orthopnea – Three Case Reports
- Diagnosis and Treatment Options for Niemann-Pick Disease Type C
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

