-
Medical journals
- Career
Katetrizační uzávěr foramen ovale patens u potápěčů
Authors: J. Honěk
Authors‘ workplace: Kardiologická klinika 2. LF UK a FN v Motole, Praha
Published in: Kardiol Rev Int Med 2015, 17(1): 25-27
Category: Cardiology Review
Overview
Foramen ovale patens (PFO) je asociováno se zvýšeným rizikem vzniku dekompresní choroby potápěčů (DCS). Mechanizmem je paradoxní embolizace dusíkových bublin z žilní krve do systémového oběhu skrze PFO. Recentně publikovaná data poukazují na možnou efektivitu jak katetrizačního uzávěru, tak konzervativních profilů ponoru v prevenci paradoxní embolizace bublin. Tento přehledový článek si klade za cíl uvést základní fyziologické a patofyziologické principy tvorby bublin a vzniku DCS a shrnout současné poznatky o vztahu PFO a DCS a možnostech léčby symptomatických potápěčů.
Klíčová slova:
foramen ovale patens – katetrizační uzávěr – dekompresní choroba
Potápěč je při pobytu pod vodní hladinou vystaven zvýšenému tlaku okolního prostředí. Tato okolnost je spojena s řadou fyziologických, ale i patofyziologických změn, a také se specifickými zdravotními riziky, zejména dekompresní chorobou potápěčů (DCS). V posledních letech byla intenzivně studována souvislost foramen ovale patens (PFO) s různými chorobnými stavy. U potápěčů je PFO spojeno se zvýšeným rizikem vzniku DCS [1]. I přes vysokou prevalenci PFO v dospělém věku (~27 %) [2] však zůstávají nezodpovězeny základní otázky screeningové strategie, rizikové stratifikace i léčby symptomatických potápěčů. Tento přehledový článek si klade za cíl uvést základní fyziologické a patofyziologické principy tvorby bublin a vzniku DCS a shrnout současné poznatky k tématu PFO a DCS včetně možnosti katetrizačního uzávěru PFO u symptomatických potápěčů.
Dekompresní choroba potápěčů – fyziologie a patofyziologie
Dýchací směs (vzduch, případně jiná směs obsahující kyslík) je potápěči dodávána z přístroje (SCUBA – self contained underwater breathing apparatus) pod okolním tlakem zvyšujícím se s hloubkou ponoru. Podle Henryho zákona jsou plyny rozpouštěny v tkáních v množství úměrném jejich parciálnímu tlaku. V hloubce tedy dochází k sycení tkání dusíkem, který se nezúčastní metabolizmu. Rychlost saturace se liší mezi tkáněmi a je závislá na jejich kapilaritě a chemickém složení [3]. Při výstupu potápěče k hladině se tlakový gradient obrací, dýchaná směs obsahuje nižší parciální tlak dusíku a ten je postupně vysycován z tkání a vydýcháván. Pokud okolní tlak poklesne příliš rychle, dojde k přesycení (supersaturaci) tkání a ke vzniku plynné fáze (bublin) [4].
Proces vzniku bublin je zkoumán již přes 100 let a stále zůstává mnoho aspektů nejasných. Předpokládá se apriorní přítomnost určité formy mikrojader, přestože jejich přesná povaha stále není známa [4]. Z praktického hlediska je významné, že rychlost saturace a desaturace je odlišná v různých tkáních. K popisu celotělové kinetiky dusíku se používají multikompartmentové matematické modely [5]. Na těchto modelech jsou založeny potápěčské tabulky a počítače používané při plánování a v průběhu ponoru. Pomocí správného plánování lze teoreticky předejít přesycení tkání a tvorbě bublin.
Dekompresní choroba je způsobena vznikem a růstem bublin v přesycených tkáních při výstupu na hladinu. Tyto bubliny mohou působit buď lokálně v místě vzniku, nebo embolizovat krevním řečištěm [6]. Malé množství bublin v žilní krvi lze sonograficky detekovat i po běžných ponorech [7,8] (obr. 1). Většina potápěčů však zůstává asymptomatická, protože bubliny jsou efektivně filtrovány v plicním řečišti. Symptomy mohou vzniknout buď při masivní embolizaci (plicní forma DCS při závažném porušení dekompresních pravidel – např. nekontrolovaný výstup k hladině), nebo při paradoxní embolizaci bublin do systémového oběhu u potápěče s permanentním či tranzientním pravo ‑ levým zkratem. U potápěčů s PFO způsobují arteriální plynové emboly (bubliny) obturací kapilár lokální ischemii. V periferii je navíc stále zvýšený parciální tlak dusíku, proto nedochází k rozpouštění bublin, ale naopak k jejich dalšímu růstu [6].
Image 1. Echokardiografický obraz dusíkových bublin v pravostranných srdečních oddílech. 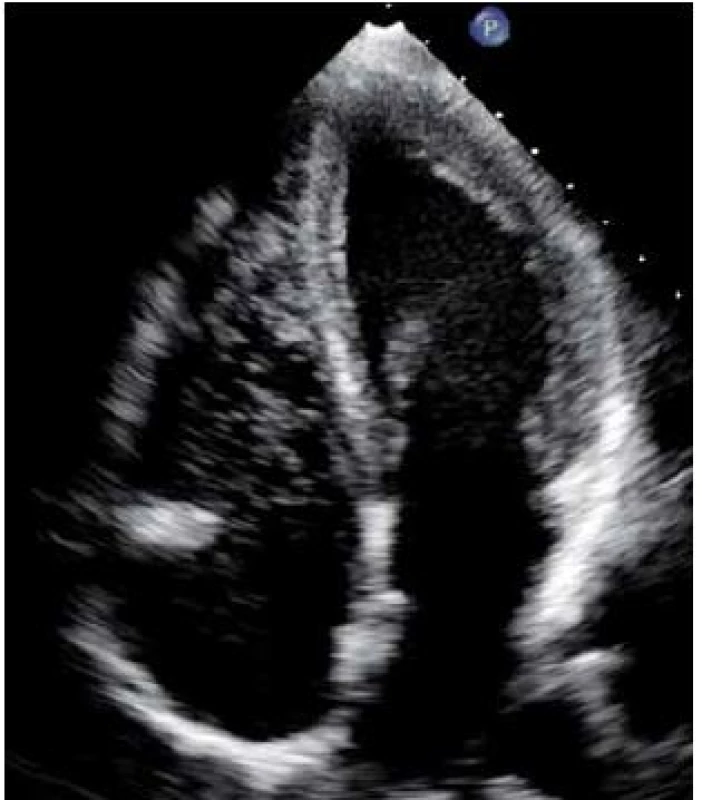
Klinický obraz DCS je velice heterogenní, odpovídá množství, velikosti a distribuci bublin. Podle symptomatologie rozlišujeme formu kožní, muskuloskeletální, neurologickou a plicní. Muskuloskeletální forma se projevuje krutou bolestí velkých kloubů a předpokládá se, že je způsobena lokální tvorbou bublin v avaskulární kloubní chrupavce [9]. Naopak PFO je spojováno zejména s formou neurologickou, ale i kožní. Zdá se, že paradoxní embolizace bublin skrze PFO by mohla hrát významnou roli u těchto forem DCS [5].
Dekompresní choroba potápěčů – role foramen ovale patens
Souvislost mezi PFO a DCS byla poprvé popsána v 80. letech 20. století [10,11]. Od té doby byla opakovaně zaznamenána vyšší prevalence PFO u potápěčů s neurologickou a kožní formou DCS [12 – 15]. Současně bylo dokumentováno, že riziko vzniku DCS roste s velikostí pravo ‑ levého zkratu [15]. Mimo tyto akutní projevy byly popsány také možné chronické následky opakovaných asymptomatických embolizací do centrálního nervového systému (CNS) v podobě mnohočetných lézí detekovatelných na magnetické rezonanci mozku [16].
Patofyziologickým podkladem vzniku DCS u potápěčů s PFO je paradoxní embolizace bublin. Při pobytu pod vodou dochází k nárůstu tlaku v pravé síni v důsledku redistribuce krve z periferie do hrudníku [17], potápěči navíc v průběhu ponoru často opakovaně provádějí Valsalvův manévr (k vyrovnání tlaku ve středouší), v důsledku toho může dojít k intermitentnímu pravo ‑ levému zkratu skrze PFO. Výskyt určitého množství žilních bublin je přitom častý i po běžném rekreačním ponoru [8]. Proto se můžeme setkat u potápěčů s PFO s projevy DCS i v případě, že nedošlo k porušení dekompresních pravidel [14]. Tuto nepredikovatelnou událost nazýváme nevyprovokovanou dekompresní příhodou. Potápěči s PFO navíc častěji trpí recidivující DCS [18].
Na druhou stranu je také diskutována možnost paradoxní embolizace transpulmonální cestou [19]. Vzhledem k nízké prevalenci významných plicních arteriovenózních malformací [20] a naopak k vysoké prevalenci PFO [2] a výše zmíněným klinickým studiím [12 – 16,18] se však zdá, že PFO hraje v paradoxní embolizaci bublin u potápěčů významnější roli. Přesto zůstává v péči o potápěče s PFO řada nezodpovězených otázek. U symptomatických potápěčů se nabízejí tři možnosti dalšího postupu – ukončení činnosti, konzervativní přístup k potápění a katetrizační uzávěr PFO.
Katetrizační uzávěr foramen ovale patens
Řada autorů již formulovala hypotézu, že katetrizační uzávěr PFO by mohl vést k prevenci paradoxní embolizace bublin u potápěčů a snížit riziko vzniku DCS [21 – 23]. K dispozici je však doposud pouze jediná studie, ve které bylo prokázáno, že katetrizační uzávěr vedl k eliminaci arteriálních bublin po ponoru [24]. V této studii byl sonograficky srovnán výskyt venózních a arteriálních bublin u potápěčů po katetrizačním uzávěru PFO (n = 20) a s PFO (n = 27). Intervence byly prováděny okludery Amplatzer septal occluder (AGA Medical Corporation, Golden Valley, USA) a Occlutech Figulla PFO Occluder N (Occlutech GmbH, Jena, Německo). Ve studii nebyly detekovány žádné arteriální bubliny u potápěčů po katetrizačním uzávěru PFO, současně se u žádného z těchto potápěčů nevyskytly symptomy DCS (tento trend nedosáhl statistické významnosti). Limitací studie je její experimentální charakter (ponory byly simulovány v hyperbarické komoře), nízký počet pacientů a absence klinického primárního cíle (primárním cílem byla sonograficky ověřená přítomnost arteriálních bublin). Přestože jsou tyto výsledky velice povzbudivé, definitivní odpověď na to, jakou úlohu bude mít katetrizační uzávěr PFO u potápěčů, by měly přinést zejména longitudinální klinické studie.
Konzervativní postup
Za konzervativní postup u potápěčů, kterým bylo zjištěno PFO, lze označit buď zákaz další činnosti, nebo doporučení konzervativního způsobu potápění. Tento soubor opatření má za cíl snížení rizika vzniku dusíkových bublin, a tím i výskytu DCS. Prevence vzniku bublin můžeme dosáhnout jak omezením saturace tkání (zkrácená expozice, mělčí ponor, snížený obsah dusíku v dýchané směsi), tak zpomalením jejich desaturace (pomalejší rychlost výstupu). Doposud je však málo důkazů o efektivitě těchto postupů u potápěčů s PFO [25,26]. Obecně lze také snížit riziko vzniku bublin správnou přípravou na ponor (preconditioning) pomocí hydratace a lehké fyzické zátěže bezprostředně před ponorem [27].
Závěr
Foramen ovale patens je spojeno se zvýšeným rizikem vzniku DCS u potápěčů. I přes vysokou prevalenci PFO však stále zůstává v této problematice řada otázek a chybí doporučené postupy. Některé recentní studie naznačují možnou efektivitu katetrizačního uzávěru PFO v prevenci DCS. Pokud bude tato hypotéza potvrzena v longitudinálních klinických studiích, mohl by být katetrizační uzávěr PFO efektivní metodou v sekundární prevenci DCS v situacích, kdy nelze dostatečně přizpůsobit potápěčskou praxi přítomnosti PFO, tedy zejména u profesionálních potápěčů.
Podpořeno MZ ČR – RVO, FN v Motole 00064203.
Doručeno do redakce: 4. 1. 2015
Přijato po recenzi: 15. 1. 2015
MU Dr. Jakub Honěk
www.fnmotol.cz
jakub.honek@gmail.com
Sources
1. Bove AA. The PFO gets blamed again…perhaps this time it is real. JACC Cardiovasc Interv 2014; 7 : 409 – 410. doi: 10.1016/ j.jcin.2014.01.152.
2. Hagen PT, Scholz DG, Edwards WD. Incidence and size of patent foramen ovale during the first 10 decades of life: an autopsy study of 965 normal hearts. Mayo Clin Proc 1984; 59 : 17 – 20.
3. Doolette DJ, Mitchell SJ. The physiological kinetics of nitrogen and the prevention of decompression sickness. Clin Pharmacokinet 2001; 40 : 1 – 14.
4. Papadopoulou V, Eckersley RJ, Balestra C et al. A critical review of physiological bubble formation in hyperbaric decompression. Adv Colloid Interface Sci 2013; 191 – 192 : 22 – 30. doi: 10.1016/ j.cis.2013.02.002.
5. Bove AA. Diving medicine. Am J Respir Crit Care Med 2014; 189 : 1479 – 1486. doi: 10.1164/ rccm.201309 ‑ 1662CI.
6. Vann RD, Butler FK, Mitchell SJ et al. Decompression Illness. Lancet 2011; 377 : 153 – 164. doi: 10.1016/ S0140 ‑ 6736(10)61085 ‑ 9.
7. Dunford RG, Vann RD, Gerth WA et al. The incidence of venous gas emboli in recreational diving. Undersea Hyperb Med 2002; 29 : 247 – 259.
8. Ljubkovic M, Dujic Z, Møllerløkken A et al. Venous and arterial bubbles at rest after no ‑ decompression air dives. Med Sci Sports Exerc 2011; 43 : 990 – 995. doi: 10.1249/ MSS.0b013e31820618d3.
9. Gempp E, Blatteau JE, Simon O et al. Musculoskeletal decompression sickness and risk of dysbaric osteonecrosis in recreational divers. Diving Hyperb Med 2009; 39 : 200 – 204.
10. Wilmshurst PT, Ellis PT, Jenkins BS. Paradoxical gas embolism in a scuba diver with an atrial septal defect. Br Med J 1986; 293 : 1277.
11. Moon RE, Camporesi EM, Kisslo JA. Patent foramen ovale and decompression sickness in divers. Lancet 1989; 1 : 513 – 514.
12. Cantais E, Louge P, Suppini A et al. Right ‑ to ‑ left shunt and risk of decompression illness with cochleovestibular and cerebral symptoms in divers: case control study in 101 consecutive dive accidents. Crit Care Med 2003; 31 : 84 – 88.
13. Wilmshurst PT, Pearson MJ, Walsh KP et al. Relationship between right ‑ to ‑ left shunts and cutaneous decompression illness. Clin Sci 2001; 100 : 539 – 542.
14. Germonpré P, Dendale P, Unger P et al. Patent foramen ovale and decompression sickness in sports divers. J Appl Physiol 1998; 84 : 1622 – 1626.
15. Torti SR, Billinger M, Schwerzmann M et al. Risk of decompression illness among 230 divers in relation to the presence and size of patent foramen ovale. Eur Heart J 2004; 25 : 1014 – 1020.
16. Knauth M, Ries S, Pohimann S et al. Cohort study of multiple brain lesions in sport divers: role of a patent foramen ovale. BMJ 1997; 314 : 701 – 705.
17. Marabotti C, Scalzini A, Menicucci D et al. Cardiovascular changes during SCUBA diving: an underwater Doppler echocardiographic study. Acta Physiol 2013. doi: 10.1111/ apha.12112.
18. Gempp E, Louge P, Blatteau JE et al. Risks factors for recurrent neurological decompression sickness in recreational divers: a case ‑ control study. J Sports Med Phys Fitness 2012; 52 : 530 – 536.
19. Ljubkovic M, Zanchi J, Breskovic T et al. Determinants of arterial gas embolism after scuba diving. J Appl Physiol 2012; 112 : 91 – 95. doi: 10.1152/ japplphysiol.00943.2011.
20. Cartin‑Ceba R, Swanson KL, Krowka MJ. Pulmonary arteriovenous malformations. Chest 2013; 144 : 1033 – 1044. doi: 10.1378/ chest.12 ‑ 0924.
21. Billinger M, Zbinden R, Mordasini R et al. Patent foramen ovale closure in recreational divers: effect on decompression illness and ischaemic brain lesions during long‑term follow‑up. Heart 2011; 97 : 1932 – 1937. doi: 10.1136/ heartjnl ‑ 2011 ‑ 300436.
22. Walsh KP, Wilmshurst PT, Morrison WL. Transcatheter closure of patent foramen ovale using the Amplatzer septal occluder to prevent recurrence of neurological decompression illness in divers. Heart 1999; 81 : 257 – 261.
23. Lairez O, Cournot M, Minville V et al. Risk of neurological decompression sickness in the diver with right ‑ to ‑ left shunt: literature review and meta‑analysis. Clin J Sport Med 2009; 19 : 231 – 235. doi: 10.1097/ JSM.0b013e31819b0fa2.
24. Honěk J, Šrámek M, Šefc L et al. Effect of catheter‑based patent foramen ovale closure on the occurrence of arterial bubbles in scuba divers. JACC Cardivasc Interv 2014; 7 : 403 – 408. doi: 10.1016/ j.jcin.2013.12.199.
25. Honěk J, Šrámek M, Šefc L et al. Effect of conservative dive profiles on the occurrence of venous and arterial bubbles in divers with a patent foramen ovale: a pilot study. Int J Cardiol 2014; 176 : 1001 – 1002. doi: 10.1016/ j.ijcard.2014.04.218.
26. Klingmann C, Rathmann N, Hausmann D et al. Lower risk of decompression sickness after recommendation of conservative decompression practices in divers with and without vascular right ‑ to ‑ left shunt. Diving Hyperb Med 2012; 42 : 146 – 150.
27. Gempp E, Blatteau JE. Preconditioning methods and mechanisms for preventing the risk of decompression sickness in scuba divers: a review. Res Sports Med 2010; 18 : 205 – 218. doi: 10.1080/ 15438627.2010.490189.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2015 Issue 1-
All articles in this issue
- Patofyziologie a diagnóza obstrukce u hypertrofické kardiomyopatie
- Vyšetření cerebrovaskulární rezervy u asymptomatických pacientů s významnou stenózou vnitřní karotické tepny
- Genetika kardiomyopatií
- Katetrizační léčba chronické stabilní ischemické choroby srdeční v současnosti
- Katetrizační uzávěr foramen ovale patens u potápěčů
- Katetrizační léčba fibrilace síní
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- Není perikarditida jako perikarditida – kazuistika
- Studie Pegasus – duální antiagregace (ASA + ticagrelor) dlouhodobě po infarktu myokardu
- TDM antibiotik v klinické praxi
- TDM digoxinu v klinické praxi
- Lékové interakce a současná klinická praxe
- Přímá perorální antikoagulancia – perspektivy terapeutického monitorování
- Klinická farmakologie antirevmatik
- Specifika klinických hodnocení léčiv časných fází I a II
- Význam TDM metotrexátu při terapii psoriázy
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- TDM digoxinu v klinické praxi
- Lékové interakce a současná klinická praxe
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- TDM antibiotik v klinické praxi
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

