-
Medical journals
- Career
Vorapaxar v klinických studiích
Authors: J. Špinar 1; J. Vítovec 2; L. Špinarová 2
Authors‘ workplace: Interní kardiologická klinika FN Brno, LF MU a ICRC, Brno 1; I. interní kardioangiologická klinika FN u sv. Anny, LF MU a ICRC, Brno 2
Published in: Kardiol Rev Int Med 2012, 14(2): 109-113
Category: Reports from Foreign countries
Overview
Dosavadní protidestičková strategie u akutních i chronických stavů má závažnou slabinu – tou je selhání léčby či snížení léčebné odpovědi u významného procenta léčených. Výsledkem je přetrvávání hyperaktivace trombocytů a riziko rozvoje trombotické komplikace. Schůdnou a logickou cestou je proto přechod na léčbu účinnějšími přípravky. Takovými přípravky jsou dnes již dostupný ireverzibilní inhibitor receptoru ADP, tj. prasugrel, či inhibitor reverzibilní, tj. ticagrelor. V tomto článku uvádíme výsledky klinického zkoušení s inhibitorem destičkových receptorů PAR 1 – vorapaxarem (SCH530348). Studie TRACER je mezinárodní klinická studie u 12 944 nemocných s akutním koronárním syndromem s ST elevacemi. Primární cíl byl složený z úmrtí na kardiovaskulární příčiny, infarktu myokardu, cévní mozkové příhody, hospitalizace pro ischemii nebo urgentní revaskularizace. Studie byla předčasně ukončena po vyhodnocení bezpečnosti podávané medikace. Přidání vorapaxaru ke standardní léčbě nesnížilo významně primární cíl, naopak zvýšilo krvácení, včetně intrakraniláního krvácení. Studie TRA-2P TIMI 50 byla multicentrická, dvojitě slepá studie. Zařazováni byli nemocní po infarktu myokardu nebo po cévní mozkové příhodě minimálně dva týdny, maximálně však 12 měsíců. Zařazeno bylo 26 449 nemocných. Ve třetím roku se primární cíl kardiovaskulární úmrtí, infarkt myokardu nebo cévní mozková příhoda vyskytl u 1 028 (9,3 %) nemocných léčených vorapaxarem a u 1 176 (10,5 %) nemocných léčených placebem, což bylo vysoce statisticky významné (p < 0,001). Studie TRA-2P TIMI 50 je jednou z nejúspěšnějších studií v historii a významnou měrou se na tom podílela Česká republika.
Klíčová slova:
antiagregační léčba – vorapaxar – infarkt myokardu – sekundární prevence
Primární hemostáza hraje klíčovou roli v rychlé reparaci poškozené cévní stěny. Trombocyty se však uplatňují i za patologických okolností při formaci trombů v procesu aterotrombózy. Aktivace destiček může být zprostředkována více podněty, nejdůležitějšími působky jsou adenozindifosfát (ADP), tromboxan A2 (TXA2) a trombin. Vlastní adheze je zprostředkována von Willebrandovým faktorem [1].
Dnes umíme úspěšně inhibovat všechny působky (obr. 1), problémem však je, že s mírou jejich inhibice sice klesá riziko trombotické komplikace, ale též zákonitě stoupá riziko krvácení. Proto vždy volíme strategii s posouzením konkrétní situace, tedy poměřujeme rizika trombózy na straně jedné a rizika krvácení na straně druhé. Například při akutním riziku uzavření věnčité tepny u nestabilní anginy pectoris neváháme s aplikací duální protidestičkové léčby (zpravidla blokádou adenozinové i tromboxanové cesty aktivace) spolu s terapií antikoagulační (zpravidla nízkomolekulárním či nefrakcionovaným heparinem). Krátkodobé zvýšení rizika krvácení je výrazně převýšeno snížením rizika vzniku infarktu myokardu. Naopak, je-li riziko nízké – například při stabilizované angině pectoris –, volíme strategii méně razantní s jedním protidestičkovým lékem – kyselinou acetylsalicylovou (ASA) nebo inhibicí aktivace cesty ADP, zpravidla podáním clopidogrelu.
Image 1. Místa působení antiagregačních léků. 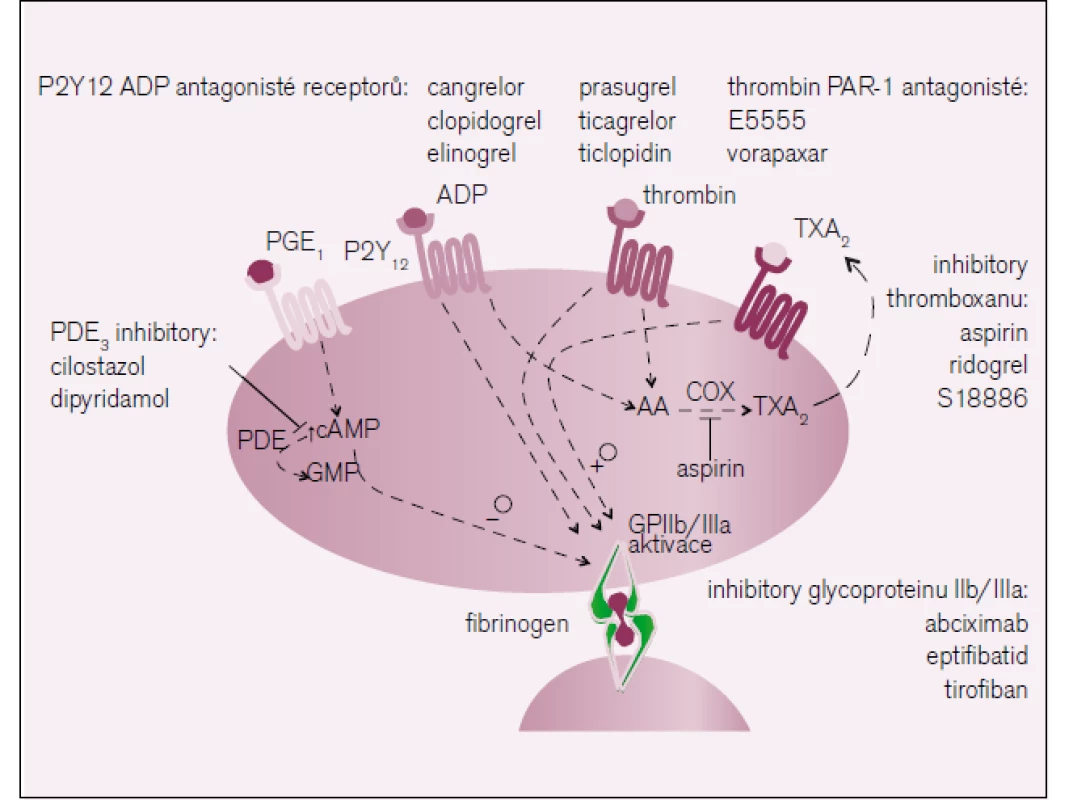
Dosavadní protidestičková strategie u akutních i chronických stavů má nicméně závažnou slabinu – tou je selhání léčby či snížení léčebné odpovědi u významného procenta léčených. U části nemocných, označovaných jako semirespondeři (event. hyporespondeři) či dokonce nonrespondeři, není odpověď na podanou medikaci – na kyselinu acetylsalicylovou či clopidogrel – dostatečně rychlá či má pouze slabý projev. Výsledkem je přetrvávání hyperaktivace trombocytů a riziko rozvoje trombotické komplikace.
Nejčastějšími příčinami rezistence na kyselinu acetylsalicylovou a clopidogrel jsou (kromě vysoké non-compliance ze strany pacienta) zejména variabilní absorpce, suboptimální podaná dávka, polymorfizmus systémů bioaktivace, zvýšený obrat trombocytů a jejich nadměrná aktivace (při trombocytóze, diabetu či kouření), komedikace interferující buď s vazbou kyseliny acetylsalicylové na aktivní místo cyklooxygenázy (zejména nesteroidními antiflogistiky, nejčastěji ibuprofenem), nebo s bioaktivací clopidogrelu (nejčastěji s inhibitory protonové pumpy).
Schůdnou a logickou cestou je proto přechod na léčbu účinnějšími přípravky se spolehlivějším účinkem, který nezávisí na bioaktivaci. Takovými přípravky jsou dnes již dostupný ireverzibilní inhibitor receptoru ADP, tj. prasugrel, či inhibitor reverzibilní, tj. ticagrelor. V tomto článku uvádíme výsledky klinického zkoušení s inhibitorem destičkových receptorů PAR-1 – vorapaxarem (SCH530348).
Studie TRACER byla prezentována na americkém kardiologickém kongrese v Orlandu na podzim 2011 a referovali jsme o ní v minulém čísle Kardiologické revue [2–3]. Proto jen stručně uvádíme:
TRACER – Thrombin-Receptor Antagonist Vorapaxar in Acute Coronary Syndromes
Studie TRACER je mezinárodní klinická studie u 12 944 nemocných s akutním koronárním syndromem s ST elevacemi. Primární cíl byl složený z úmrtí na kardiovaskulární příčiny, infarktu myokardu, cévní mozkové příhody, hospitalizace pro ischemii nebo urgentní revaskularizace.
Studie byla předčasně ukončena po vyhodnocení bezpečnosti podávané medikace. Průměrná doba sledování byla 502 dní (od 349 do 667) a primární cíl se vyskytl u 1 031 nemocných z 6 473 dostávajících vorapaxar oproti 1 102 nemocných z 6 471 dostávajících placebo (18,5 % vs 19,9 %) (obr. 2 a tab. 1).
Image 2. Primární cíl ve studii TRACER. 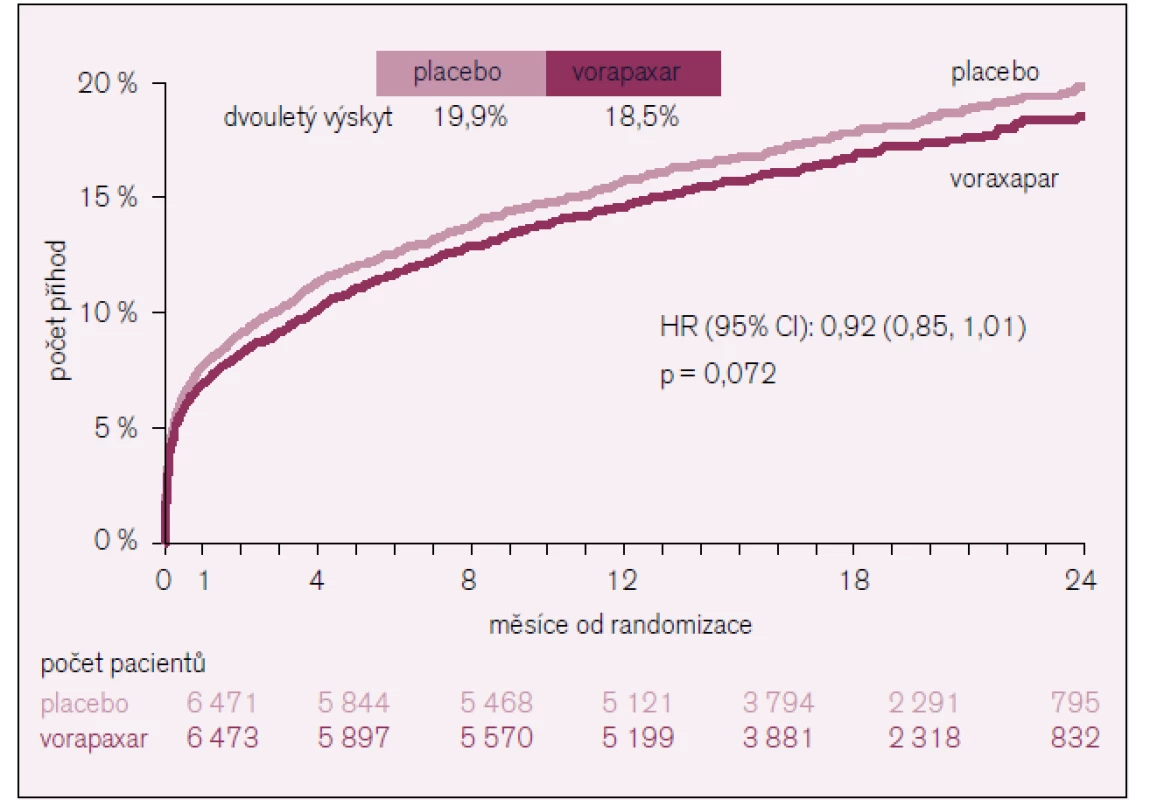
Table 1. Výsledky studie TRACER. 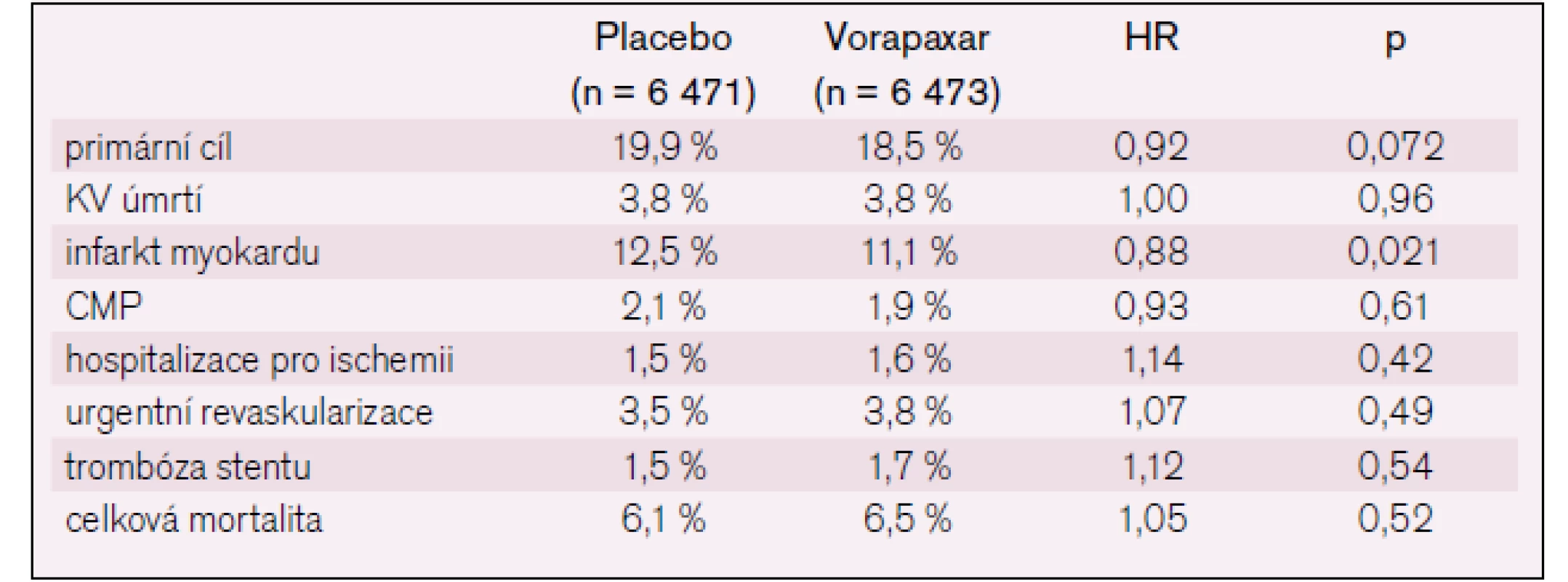
Smíšený cíl úmrtí, infarkt myokardu a cévní mozková příhoda byl u 822 nemocných na aktivní léčbě a u 910 nemocných na placebu (14,7 % vs 16,4 %, p = 0,02). Výskyt závažného krvácení byl 7,2 % na aktivní léčbě a 5,2 % na placebu (p < 0,01). Intrakraniální krvácení bylo 1,1 % vs 0,2 % (p < 0,001) (obr. 3). Výskyt nekrvácivých nežádoucích účinků byl v obou skupinách stejný.
Image 3. Krvácení ve studii TRACER. 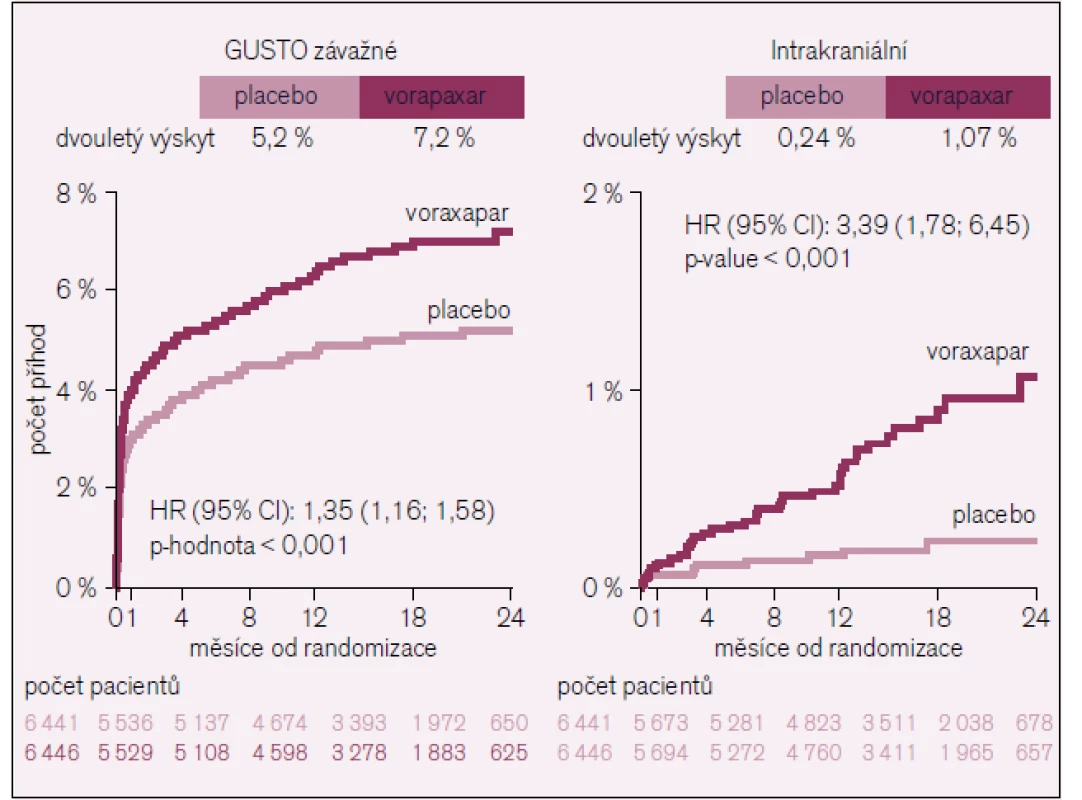
Závěr: Přidání vorapaxaru ke standardní léčbě nesnížilo významně primární cíl, naopak zvýšilo krvácení, včetně intrakraniláního krvácení.
Studie byla zklamáním, proto se s napětím čekalo na další velkou studii, tentokrát u chronické ischemické choroby srdeční, známé jako TRA-2P TIMI 50, jejíž výsledky byly prezentovány na 61. kongresu American College of Cardiology 24.–27. 3. 2012 v Chicagu [4].
TRA-2P TIMI 50 – Vorapaxar in the secondary prevention of atherothrombotic events
Studie TRA-2P TIMI 50 byla multicentrická, dvojitě slepá studie prováděná ve 32 zemích a 1 032 centrech. Největší centrum na světě byla Interní kardiologická klinika Fakultní nemocnice Brno, kdy na tomto pracovišti bylo randomizováno a do studie zařazeno 302 nemocných. Vedoucím centra byl prof. MUDr. Jindřich Špinar, CSc., a koordinátorem studie vedoucí koronární jednotky MUDr. Mgr. Jiří Pařenica, Ph.D.
Zařazováni byli nemocní po infarktu myokardu nebo po cévní mozkové příhodě minimálně dva týdny, maximálně však 12 měsíců. Nevhodní byli nemocní, kteří měli plánováno nějaké revaskularizační řešení – PTCA či CABG. Pacienti byli randomizováni na léčbu vorapaxarem či placebem v poměru 1 : 1 a veškerá doprovodná medikace včetně thienopyridinů byla povolena.
V lednu 2011 byl ukončen nábor a průměr sledování byl 24 měsíců. Na zasedání bezpečnostní komise byl zjištěn vyšší výskyt krvácení do mozku u nemocných, kteří měli v anamnéze cévní mozkovou příhodu, a tato větev byla zastavena.
Primární cíl studie byl kardiovaskulární mortalita, nefatální infarkt myokardu, cévní mozková příhoda a opakovaná ischemie vedoucí k revaskularizaci. Velmi pozorně byl sledován výskyt krvácení, které bylo klasifikováno jednak systémem GUSTO, jednak TIMI klasifikací pro krvácení.
Zařazeno bylo 26 449 nemocných od září 2007 do listopadu 2009, vorapaxar dostalo 13 225 nemocných, placebo 13 244 (tab. 2).
Table 2. Vstupní charakteristika souboru. 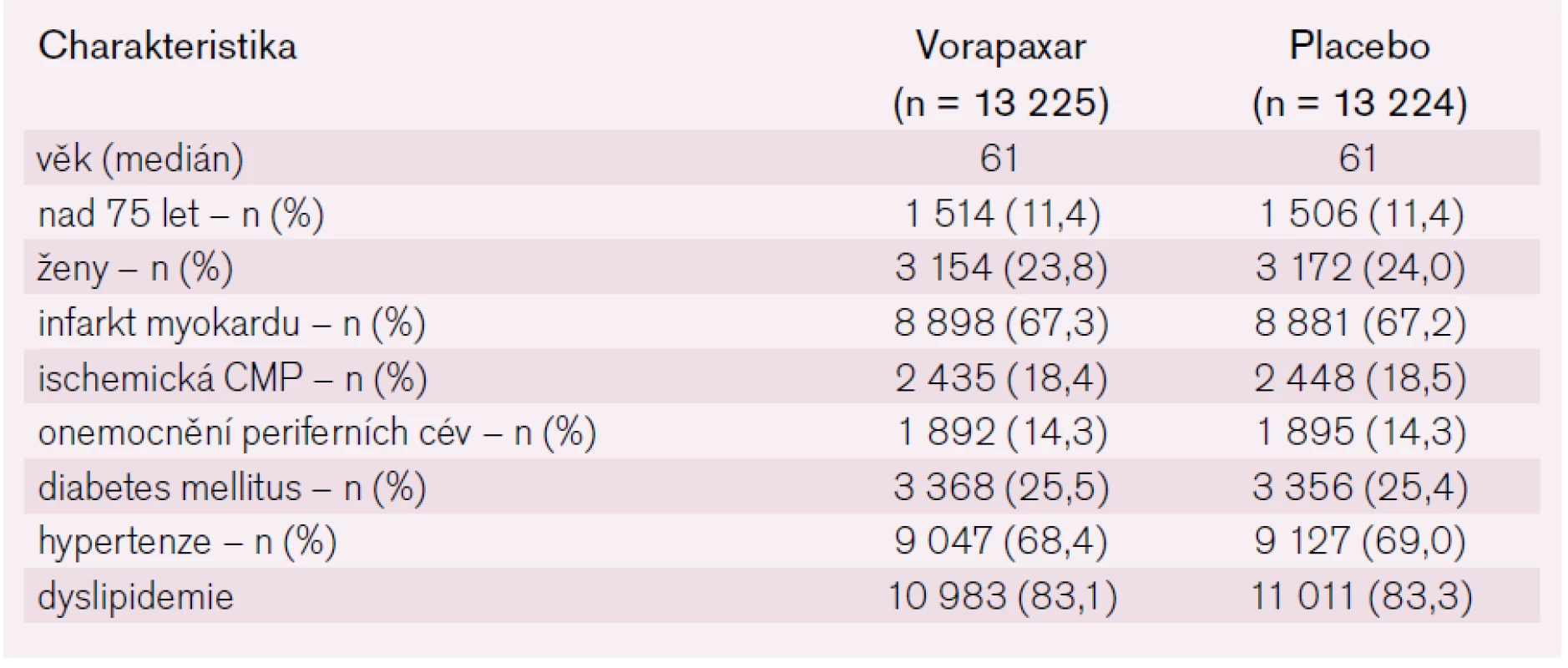
Nemocní po infarktu myokardu užívali v 98,1 % kyselinu acetylsalicylovou (ASA) v obou větvích a v 77,9 %, resp. 78,4 % thienopyridiny (většinou clopidogrel). Po cévní mozkové příhodě to bylo v případě ASA pouze 81,2 %, resp. 88,2 % a thienopyridin užívalo 36,8 % nemocných v obou větvích. Celkem užívalo ASA 94 % nemocných. Hypolipidemickou medikaci mělo 12 032 nemocných (91,0 %) ve větvi s vorapaxarem a 12 131 (91,7 %) v placebové větvi. Blokátor systému renin-angiotenzin-aldosteron 9 714 (73,5 %), resp. 9 871 (74,6 %) nemocných. Průměrná doba sledování byla 30 měsíců, nejdelší sledování bylo 49 měsíců. Studie byla ukončena v lednu 2012, poslední návštěvy probíhaly na podzim 2011.
Ve třetím roku se primární cíl kardiovaskulární úmrtí, infarkt myokardu nebo cévní mozková příhoda vyskytl u 1 028 (9,3 %) nemocných léčených vorapaxarem a u 1 176 (10,5 %) nemocných léčených placebem, což bylo vysoce statisticky významné (p < 0,001) (tab. 3, obr. 4, 5).
Image 4. Primární cíl ve studii TRA-2P TIMI 50. 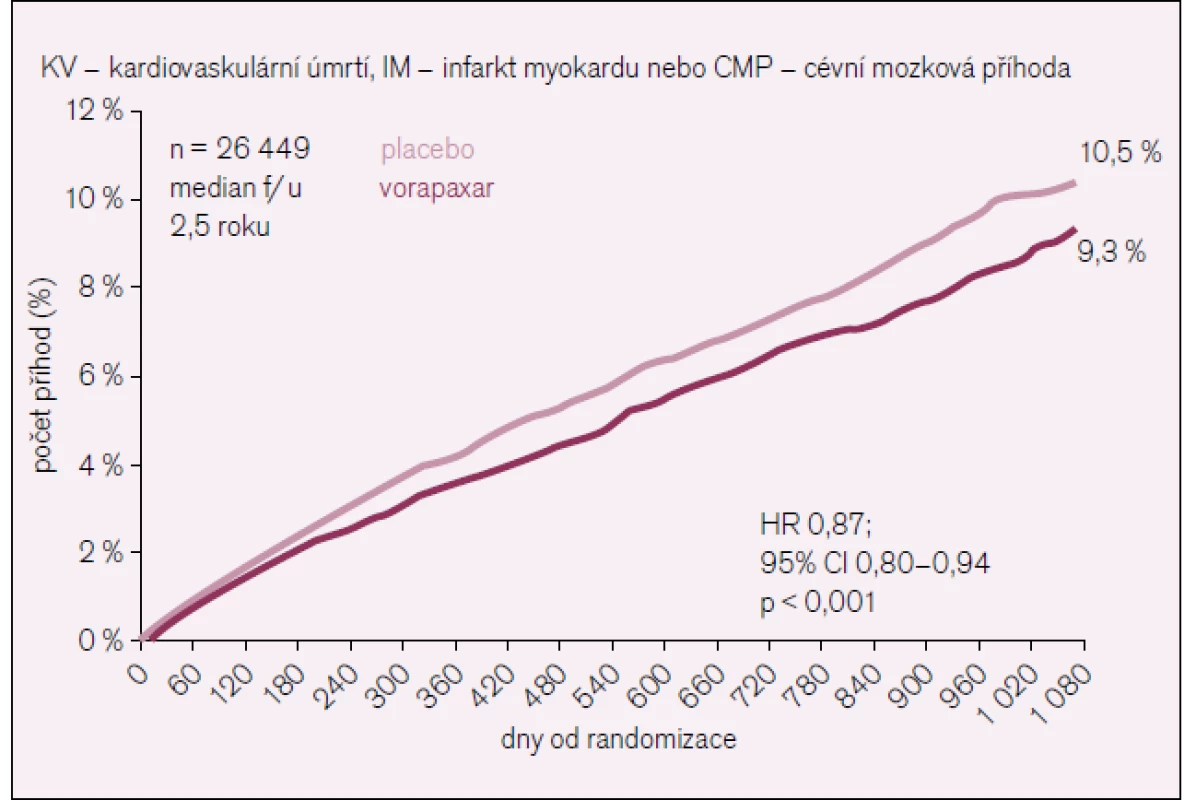
Image 5. Sekundární cíle ve studii TRA-2P TIMI 50. 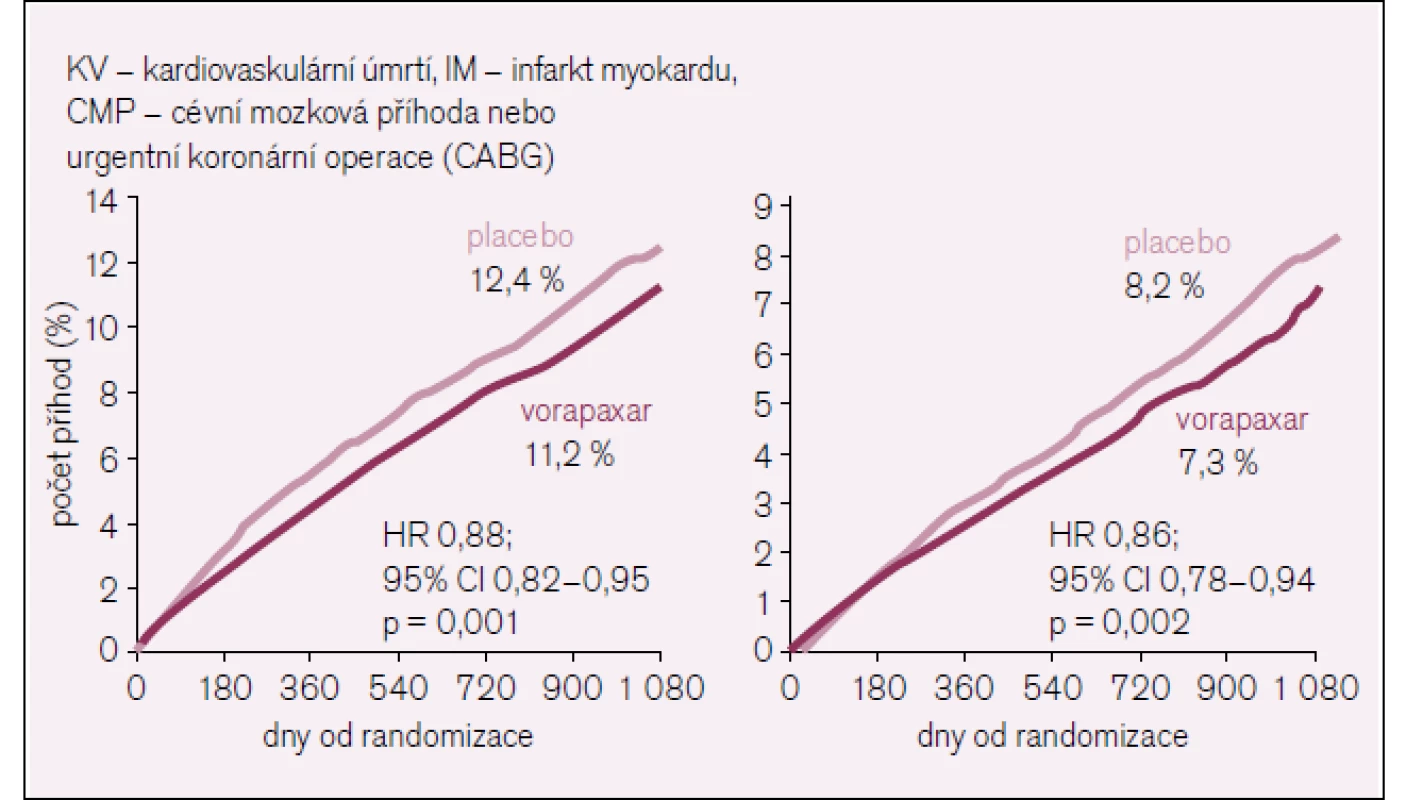
Table 3. Vstupní charakteristika souboru. 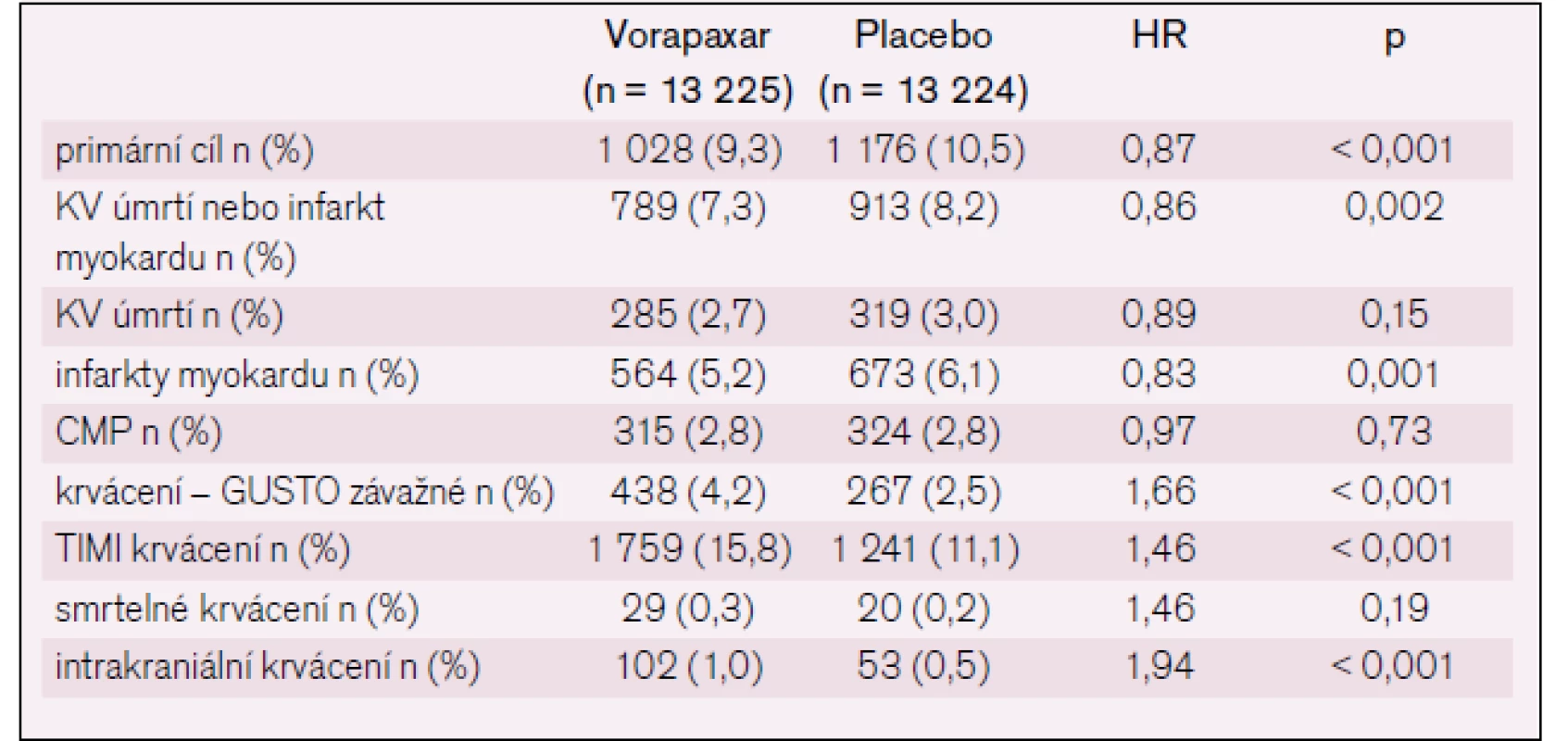
Tento vysoce pozitivní efekt byl vyvážen zvýšeným výskytem krvácení (tab. 3, obr. 6).
Image 6. Krvácení ve studii TRA-2P TIMI 50. 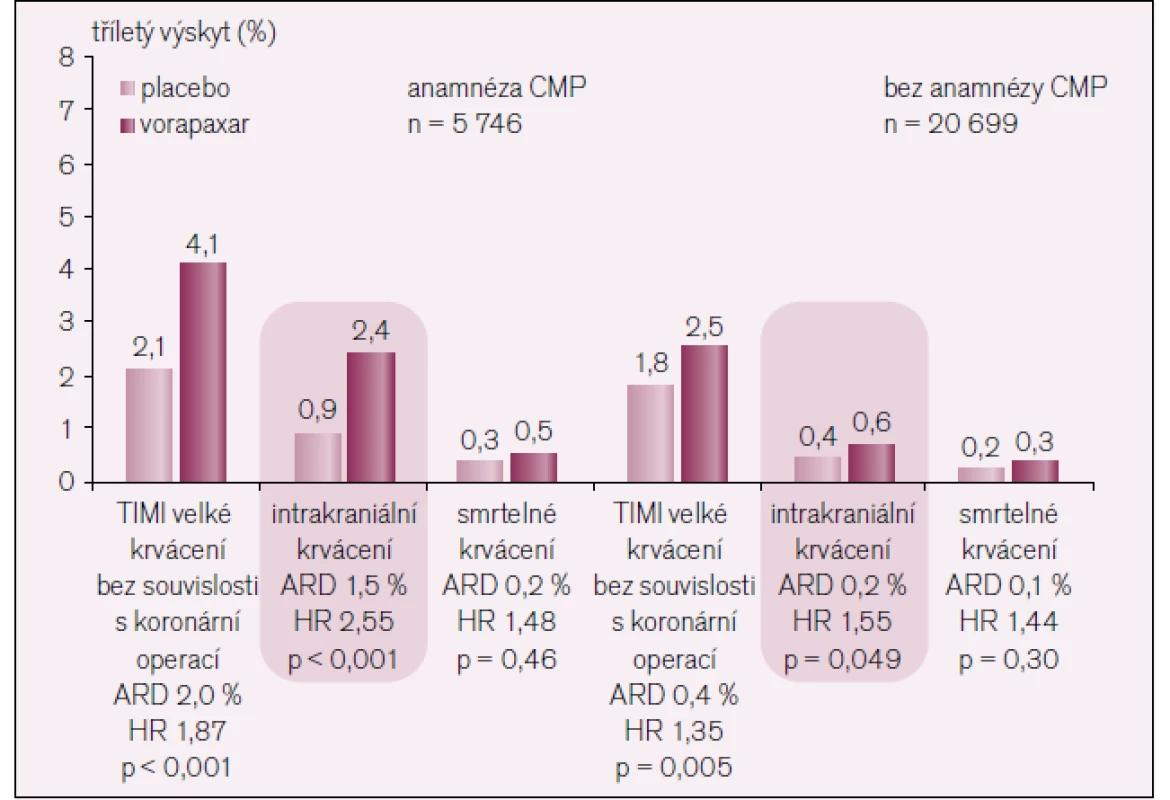
Předchozí klinické studie nedaly jasný výsledek, zda přidání dalšího antiagregačního léku ke kyselině acetylsalicylové a clopidogrelu přinese další prospěch pro nemocného. Klinická studie TRA-2P TIMI 50 toto jasně prokázala, tento klinický prospěch je ale vyvážen zvýšeným výskytem krvácení, ne však krvácení smrtelného, jehož výskyt byl v obou větvích stejný. Tento výsledek se objevil velmi časně a přetrvával po celou dobu studie.
Během studie bezpečnostní komise doporučila pozastavení větve nemocných s anamnézou cévní mozkové příhody. Proto byla provedena samostatná analýza nemocných bez anamnézy CMP a ta zjistila významný prospěch z léčby u těchto pacientů. U 3 846 nemocných byl navíc další infarkt myokardu v anamnéze a zde bylo snížení primárního cíle o 23 %! Nejzávažnější komplikací bylo intrakraniální krvácení, které bylo častější u nemocných léčených vorapaxarem. Při další analýze se zjistilo, že intrakranilání krvácení se vyskytlo pouze u 0,2 % nemocných bez anamnézy CMP a u 0,8 % nemocných s anamnézou CMP. Důležité je, že nebyl zvýšen výskyt smrtelného krvácení.
Obr. 7 shrnuje výsledky studie TRA-2P TIMI.
Image 7. Souhrn klinických výsledků a krvácení ve stuii TRA-2P TIMI 50. 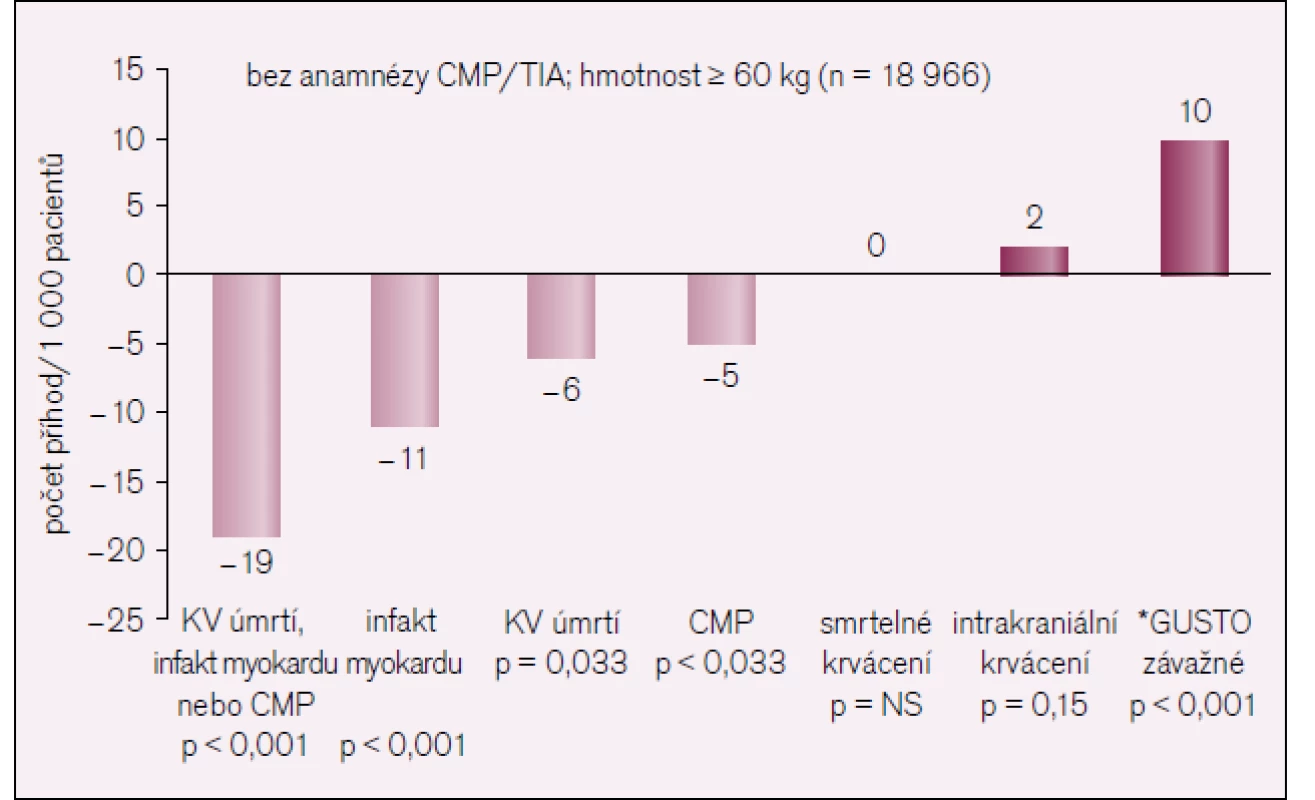
Závěr
Při léčbě 1 000 nemocných vorapaxarem, přidaným k standardní antiagregační léčbě se zabrání:
- 19 kardiovaskulárním příhodám, infarktu myokardu či cévní mozkové příhodě
- 11 infarktům myokardu
- 6 kardiovaskulárním úmrtím
- 5 cévním mozkovým příhodám
- nezvýší se smrtelné krvácení
- 2 nemocní budou mít navíc intrakraniální krvácení
- 10 nemocných bude mít navíc závažné krvácení
Studie TRA-2P TIMI 50 je jednou z nejúspěšnějších studií v historii a významnou měrou se na tom podílela Česká republika. V České republice bylo zařazeno 1 356 nemocných ve 23 centrech, to je 59 nemocných na jedno centrum, což znamenalo nejlepší nábor na světě. Národním koordinátorem byl prof. MUDr. Jindřich Špinar, CSc., který touto formou všem řešitelům v České republice moc děkuje a těší se na další spolupráci v rámci TIMI skupiny.
Doručeno do redakce 5. 4. 2012
Přijato po recenzi 24. 4. 2012
prof. MUDr. Jindřich Špinar, CSc., FESC1
prof. MUDr. Jiří Vítovec, CSc., FESC2
prof. MUDr. Lenka Špinarová, Ph.D., FESC2
1 Interní kardiologická klinika FN Brno, LF MU a ICRC, Brno
2 I. interní kardioangiologická klinika FN u sv. Anny, LF MU a ICRC, Brno
jspinar@fnbrno.cz
Sources
1. Karetová D. Aktuality v antiagregační léčbě. Medicína po promoci 2011; 12 : 45–46.
2. Špinar J, Vítovec J. Novinky z American Heart Association 2011. Kardiol Rev 2012; 14 : 49–51.
3. Tricoci P, Huang Z, Held C et al. TRACER Investigators. Thrombin-Receptor Antagonist Vorapaxar in Acute Coronary Syndromes. N Engl J Med 2012; 366 : 20–33.
4. Morrow DA, Braunwald E, Bonaca MP et al. TRA 2P–TIMI 50 Steering Committee and Investigators. Vorapaxar in the secondary prevention of atherotrombotic events. N Engl J Med 2012; 366 : 20–33.
5. Meadows TA, Bhatt DL. Clinical aspects of platelet inhibitors and thrombus formation. Circ Res 2007; 100 : 1261–1275.
6. Desai NR, Bhatt DL. The state of periprocedural antiplatelet therapy after recent trials. JACC Cardiovasc Interv 2010; 3 : 571–583.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2012 Issue 2-
All articles in this issue
- Antiagregační a antikoagulační léčba – základní principy
- Perorální protidestičková léčba u pacientů s akutním koronárním syndromem
- Současné doporučení k antiagregační léčbě v neurologii
- Antikoagulační terapie a fibrilace síní
- Nová perorální antitrombotika v prevenci a léčbě trombembolizmu
- Nová antitrombotika v prevenci pooperační tromboembolické nemoci
- Současné možnosti monitorování antitrombotické léčby – nová antitrombotika
- Kam se ubírá současný vývoj léků ovlivňujících krevní srážení?
- Vorapaxar v klinických studiích
- Čo je vernakalant a kde je jeho miesto v klinickej praxi?
- Eprosartan – duální blokátor AT1 receptorů
- Polypragmazie a oběhové selhání při maligních komorových arytmiích s postižením jaterních funkcí
- Pacientka po transplantaci srdce s plicní formou invazivní aspergilózy
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Antiagregační a antikoagulační léčba – základní principy
- Antikoagulační terapie a fibrilace síní
- Kam se ubírá současný vývoj léků ovlivňujících krevní srážení?
- Současné doporučení k antiagregační léčbě v neurologii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

