-
Medical journals
- Career
Antikoagulační terapie a fibrilace síní
: R. Lábrová; J. Špinar
: Interní kardiologická klinika LF MU a FN Brno
: Kardiol Rev Int Med 2012, 14(2): 79-86
Fibrilace síní je nejčastější supraventrikulární arytmií a je spojena se zvýšenou morbiditou a mortalitou. Všechny formy fibrilace síní jsou významným rizikovým faktorem vzniku cévní mozkové příhody a systémové embolizace. V léčbě a prevenci kardioembolizačních příhod u rizikových pacientů je indikováno podání antikoagulační terapie. Stratifikace pacientů k podání antikoagulační terapie se podle nových evropských doporučení pro diagnostiku a léčbu fibrilace síní z roku 2010 řídí stanovením rizika vzniku cévní mozkové příhody podle CHA2DS2-VASc skóre a rizika krvácení podle HAS-BLED skóre. Byla vyvinuta nová antikoagulancia, která působí na různých místech koagulační kaskády a mají oproti standardnímu podání antagonistů vitaminu K – warfarinu značné výhody. Jedná se o přímý inhibitor trombinu – dabigatran (studie RE-LY), inhibitory faktoru Xa – rivaroxaban (studie ROCKET-AF) a apixaban (studie AVERROES, ARISTOTLE), dále probíhá velká klinická studie s edoxabanem (studie ENGAGE).
Klíčová slova:
fibrilace síní – CHA2DS2-VASc skóre – warfarin – nová antikoagulancia – dabigatran – apixaban – rivaroxaban – edoxabanÚvod
Fibrilace síní (FS) je nejčastější srdeční arytmií, vyskytuje se u více než 1 % populace a dochází k jejímu trvalému nárůstu. Její prevalence roste exponenciálně s věkem a postihuje až 10 % populace starší 80 let. U neléčených pacientů s FS je mortalita dvojnásobně vyšší a tito pacienti mají pětinásobně vyšší riziko vzniku cévní mozkové příhody než u sinusového rytmu [1,2]. Nejčastější a nejzávažnější komplikací FS je tromboembolie, a to bez ohledu na to, o jakou formu FS se jedná, zda jde o FS paroxyzmální, perzistentní či permanentní. V 90 % tromboembolických příhod je postižen centrální nervový systém s obrazem ischemické mozkové příhody, méně jsou zastoupené systémové embolizace. FS je příčinou asi 1/6 všech cévních mozkových příhod (CMP).
V léčbě a prevenci kardioembolizačních příhod u rizikových pacientů je indikováno podání antikoagulační terapie. Stratifikace pacientů k podání antikoagulační terapie se podle nových evropských doporučení pro diagnostiku a léčbu fibrilace síní z roku 2010 a podle doporučení České kardiologické společnosti z roku 2011 řídí stanovením rizika vzniku CMP podle CHA2DS2-VASc skóre a rizika krvácení podle HAS-BLED skóre [3,4]. Standardní antikoagulační terapie je v současné době stále představována warfarinem – antagonistou vitaminu K a má značné nevýhody. Byla vyvinuta nová antikoagulancia, která působí na různých místech koagulační kaskády (obr. 1). Podle dávky léku jsou nová antikoagulancia v klinických studiích stejně účinná nebo lepší než warfarin a krvácivé projevy jsou srovnatelné nebo nižší než u warfarinu. Jedná se o přímý inhibitor trombinu – dabigatran (studie RE-LY), inhibitory faktoru Xa – rivaroxaban (studie ROCKET-AF) a apixaban (studie AVERROES, ARISTOTLE), dále probíhá velká klinická studie s edoxabanem (studie ENGAGE).
1. Působení antikoagulancií v koagulační kaskádě. Upraveno podle [17,18]. ![Působení antikoagulancií v koagulační kaskádě. Upraveno podle [17,18].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/fe04168d1e82ad3c97cfd136dfc44ca6.png)
Americká kardiologická společnost (AHA) zařadila v roce 2010 studie s novými antikoagulačními preparáty u fibrilace síní mezi deset nejdůležitějších objevů v oblasti kardiovaskulárních onemocnění. Jednalo se o studie RE-LY, ROCKET-AF a AVERROES. Studie RE-LY byla již publikována v Lancetu v roce 2009, studie ROCKET-AF byla prezentována na podzim 2010 na kongresu AHA, studie AVERROES na kongresu Evropské kardiologické společnosti v září 2010 současně s novými evropskými doporučeními pro diagnostiku a léčbu fibrilace síní a studie ARISTOTLE na posledním kongresu Evropské kardiologické společnosti v srpnu 2011.
V České republice byly v indikaci prevence tromboembolie u nevalvulární fibrilace síní schváleny dabigatran etexilát – Pradaxa, rivaroxaban – Xarelto, ale nevýhodou je jejich cena.
Farmakologická léčba fibrilace síní má čtyři základní okruhy:
- léčba a prevence onemocnění, která vedou k FS
- antikoagulační léčba – u pacientů s rizikem tromboembolie po stratifikaci rizika CMP a krvácení
- antiarytmická léčba – k obnovení a udržení sinusového rytmu (kontrola rytmu) nebo při FS udržet optimální frekvenci komor (kontrola frekvence)
- upstream léčba – jejím cílem je ovlivnit již vzniklou remodelaci síní nebo zabránit jejímu vzniku
Úspěšná invazivní nefarmakologická léčba FS, katetrová ablace, posouvá riziko tromboembolie na úroveň zdravého člověka.
Stratifikace rizika tromboembolie u FS
FS je významným rizikovým faktorem vzniku kardioembolizačních příhod, od tranzitorních ischemických atak (TIA) až po různě těžký stupeň CMP, které pacienta mohou trvale invalidizovat či mohou být příčinou smrti. Antikoagulace je velmi důležitá v léčbě, ale i prevenci tromboembolických komplikací FS. Doposud se podávaly převážně warfarin – antagonista vitaminu K nebo kyselina acetylsalicylová, v současné době je možnost podání přímého inhibitoru trombinu – dabigatranu a inhibitoru faktoru Xa – rivaroxabanu.
Podle metaanalýzy šesti studií u pacientů s FS došlo k 62% redukci relativního rizika tromboembolie při podání warfarinu proti placebu [5]. Ve všech studiích byl warfarin jednoznačně účinnější i ve srovnání s kyselinou acetylsalicylovou. Warfarin snížil relativní riziko tromboembolie o 39 %.
Nasazení antikoagulační léčby u fibrilace síní se řídí posouzením rizika vzniku CMP a rizika krvácení při nasazené antikoagulační léčbě. Lékař potom musí rozhodnout, které riziko u pacienta převažuje, a následně zvážit nasazení antikoagulační terapie. Pravděpodobnost rizika CMP můžeme vypočítat z tzv. CHADS2 skóre, kdy název je vytvořen z počátečních písmen rizikových faktorů. Ve skórovacím systému CHADS2 se přiděluje jeden bod za kongestivní srdeční selhání – C, hypertenzi – H, věk ≥ 75 let – A a diabetes mellitus – D a dva body za předchozí CMP – S, maximální počet je tedy šest bodů. Antikoagulační léčba warfarinem je doporučena při dvou a více bodech a cílové INR (mezinárodní normalizovaný poměr) by mělo být 2,0–3,0. Při jednom bodu je doporučena léčba antiagregační a při 0 bodech není třeba ani antikoagulace ani antiagregace. Pokud je CHADS2 = 1, mělo by se přejít na podrobnější stratifikaci rizika tromboembolie podle CHA2DS2-VASc skóre. V posledních klinických studiích byly sledovány další nové rizikové faktory FS a podle nich bylo vytvořeno modifikované tzv. CHA2DS2-VASc skóre, které má vyšší prediktivní hodnotu rizikové stratifikace tromboembolických příhod (tab. 1). Na rozdíl od CHADS2 je věk ≥ 75 let – A počítán za dva body, navíc je dalším rizikovým faktorem aterosklerotické cévní onemocnění – V (vascular disease), věk 65–74 let – A, ženské pohlaví – SC (sex category). Maximální skóre je 9 [6].
1. CHA2 DS2-VASc skóre. 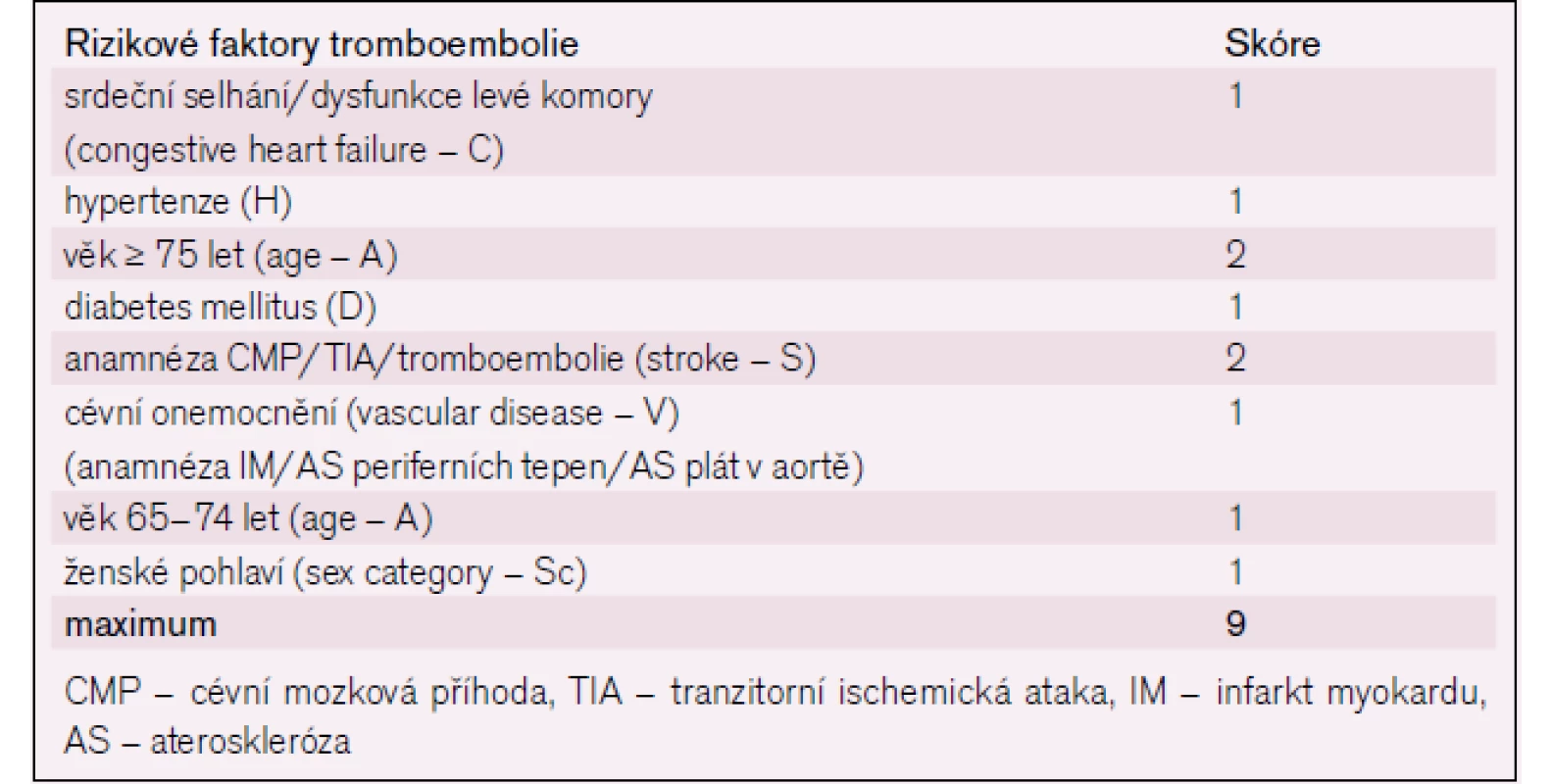
Riziková stratifikace tromboembolických příhod u pacientů s fibrilací síní bez přítomné chlopňové vady. Při 2 a více bodech hrozí vysoké riziko tromboembolie a je nutné zvážit antikoagulační terapii. Upraveno podle [3]. Pokud je skóre 0, je minimální riziko CMP či tromboembolie a není nutná žádná antitrombotická prevence. Podle zvážení lékaře je možné podání kyseliny acetylsalicylové v dávce 75–325 mg/den, ale preferuje se antitrombotickou terapii nepodávat.
Skóre 1 vymezuje pacienty se středním rizikem a je možné zvolit mezi antiagregační (kyselina acetylsalicylová v dávce 75–325 mg na den) a antikoagulační terapií, konečné rozhodnutí je ponecháno na rozvaze lékaře. Preferuje se léčba antikoagulační – warfarin (INR 2,0–3,0), případně dabigatran v dávce 2krát 150 mg, resp. 2krát 110 mg, pokud je nutná redukce dávky, rivaroxaban v dávce 20 mg jednou denně, v krátké době bude k dispozici apixaban, event. výhledově po ukončení studie ENGAGE koncem letošního roku další nové antikoagulancium – edoxaban.
Při skóre 2 a více jsou pacienti s vysokým rizikem CMP či tromboembolie a jsou jednoznačně indikovaní k antikoagulační terapii, ve stejné dávce jako u pacientů se středním rizikem.
Podle nových doporučení by při CHA2DS2-VASc skóre ≥ 1 měli mít všichni pacienti s FS antikoagulační terapii, což představuje asi 94 % pacientů s FS. Pouze u mužů i žen mladších 65 let bez přítomných rizikových faktorů se tedy může uvažovat o podání kyseliny acetylsalicylové.
Stratifikace rizika krvácení u antikoagulační terapie FS
Při nasazení antikoagulační terapie u FS je nutné také zvážit riziko krvácivých komplikací. Riziko krvácení se určuje podle tzv. HAS-BLED skóre, kdy název je opět vytvořen z počátečních písmen rizikových faktorů. Po jednom bodu se přičítá za hypertenzi – H, abnormální ledvinné funkce nebo abnormální jaterní funkce – A, CMP – S, předchozí krvácení – B, labilní INR – L, věk nad 65 let – E a pravidelné užívání alkoholu či léků zvyšujících krvácení – D (tab. 2). Maximální počet bodů je devět, kdy za vysoké riziko krvácení jsou považovány tři a více bodů [7]. U těchto nemocných není kontraindikovaná antikoagulační terapie, ale měla by být šetrnější titrace dávky warfarinu, přísnější a častější kontroly účinnosti antikoagulační terapie. K lepšímu nastavení antikoagulační terapie je možná monitorace INR pacientem, tzv. selfmonitoring pomocí přístroje na stanovení INR – CoaguChek, event. dle výsledku INR i úprava dávky warfarinu pacientem, nebo se musí zvážit nasazení nových alternativních antikoagulancií – dabigatranu, rivaroxabanu, event. výhledově po uvolnění této medikace pro indikaci pacientů s FS apixabanu, edoxabanu.
2. HAS-BLED skóre. 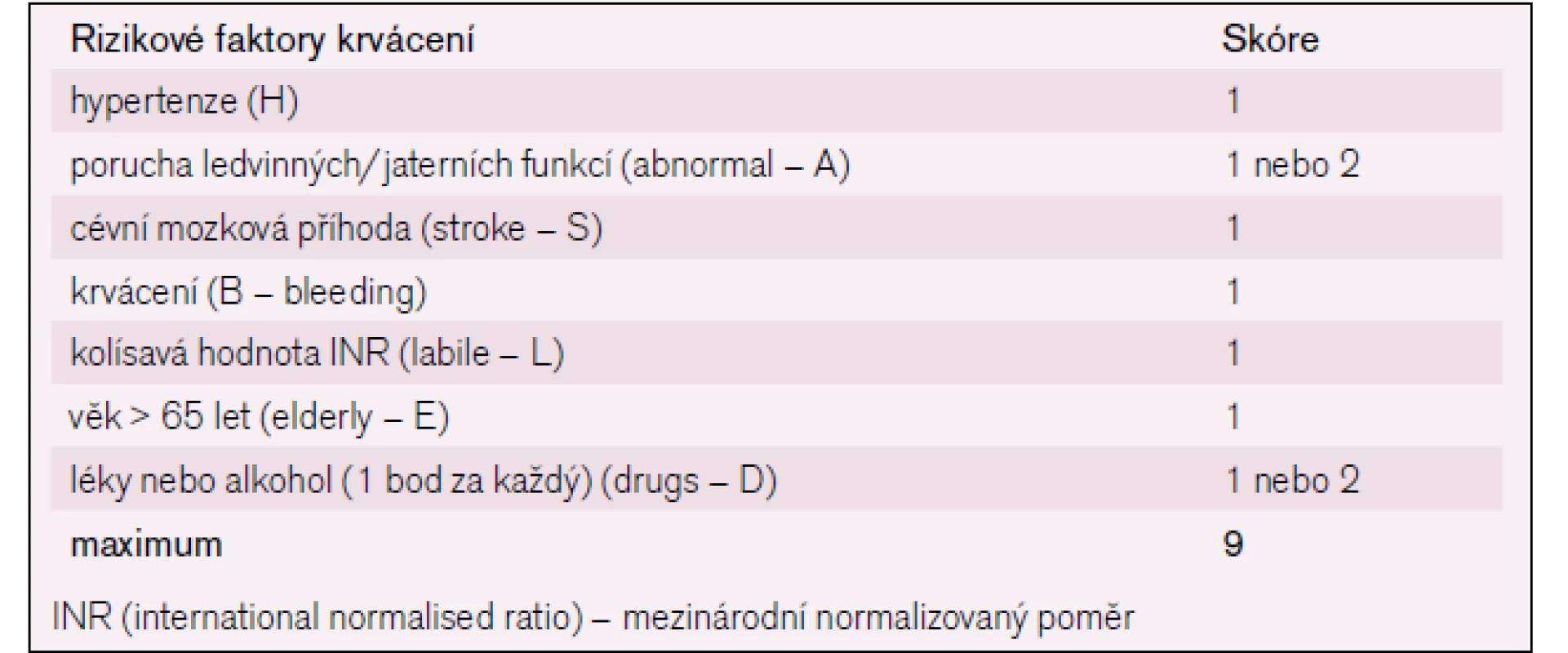
Riziková stratifikace krvácení. Při 3 a více bodech hrozí vysoké riziko krvácení. Upraveno podle [10]. Za nedostatek skórovacích systémů pro stratifikaci rizika tromboembolických komplikací a rizika krvácení u FS je možné považovat společné rizikové faktory, jako např. věk, hypertenzi a předchozí CMP, protože v obou případech zvyšují body rizika.
Antikoagulační vs antiagregační terapie u FS
V řadě studií u FS byl srovnáván účinek antagonistů vitaminu K – převážně warfarinu s kyselinou acetylsalicylovou. Ve všech studiích byl warfarin jednoznačně účinnější, snížil relativní riziko tromboembolie o 39 %. Pozitivní výsledek byl i u pacientů starších 75 let, kdy warfarin s cílovým INR 2–3 byl o 52 % účinnější než kyselina acetylsalicylová v dávce 75 mg ve snížení rizika fatálních nebo invalidizujících CMP, nitrolebního krvácení nebo významné tepenné embolie. Riziko krvácení se v obou skupinách nelišilo [8].
Ve studii ACTIVE A byla prokázána účinnější duální antiagregační terapie – clopidogrel a kyselina acetylsalicylová vs samotná kyselina acetylsalicylová u pacientů s FS [9]. Došlo k relativnímu snížení CMP o 28 %. Ale duální antiagregace měla častější velká krvácení. Pacienti, kteří nemohou užívat warfarin a nemají vysoké riziko krvácení, mohou být léčeni duální antiagregací. Ale v současné době by se jednoznačně preferovalo podání nových antikoagulancií – přímých inhibitorů trombinu nebo inhibitorů faktoru Xa než duální antiagregace.
Ve studii ACTIVE W se prokázalo, že u pacientů s paroxyzmální i permanentní FS s CHADS2 skóre ≥ 1 je antikoagulační terapie (warfarin) signifikantně účinnější než duální antiagregace (kyselina acetylsalicylová a clopidogrel) bez ohledu na formu FS [10]. Roční riziko tromboembolických příhod nebylo mezi oběma formami FS rozdílné, 2,0 % u paroxyzmální vs 2,2 % u permanentní FS. Krvácivé komplikace byly v obou skupinách podobné.
Pokud by došlo k tromboembolickým komplikacím při účinné warfarinizaci s INR 2–3, nepřidáváme léčbu antiagregační, protože hrozí velké riziko krvácení, ale udržujeme INR 3–3,5. Nyní se u těchto pacientů místo navýšení dávky warfarinu zváží podání alternativních antikoagulancií.
Alternativní antikoagulancia
Standardní antikoagulační terapie warfarinem má značné nevýhody. Má úzké terapeutické rozpětí s rizikem tromboembolie či krvácení. Má pomalý nástup a odeznění účinku, časté interakce s potravinami a léky. U některých pacientů nelze vytitrovat účinnou dávku warfarinu, např. vzhledem k přítomnosti genového polymorfizmu cílového enzymu a polymorfizmu biodegradace, a tito pacienti jsou ohrožení převážně krvácivými komplikacemi. Proto byla snaha vyvinout nová antikoagulancia, která působí na různých místech koagulační kaskády a mají oproti standardnímu podání warfarinu stabilní dávkování, bez nutnosti laboratorních kontrol, krátký biologický poločas s rychlým nástupem a odezněním účinku, dále mají minimální lékové interakce a nejsou nutná dietní opatření.
V poslední době byly ukončeny klinické studie fáze III se třemi novými antitrombotiky, které ukazují srovnatelnou nebo vyšší účinnost v prevenci tromboembolických komplikací u pacientů s nevalvulární FS ve srovnání s warfarinem a prokazují srovnatelný nebo nižší výskyt krvácení.
Mezinárodní multicentrická randomizovaná studie RE-LY (Randomized Evaluation of Long-term anticoagulant therapY) byla publikována již v roce 2009 a srovnávala dabigatran s warfarinem u nemocných s nevalvulární fibrilací síní a přítomným nejméně jedním rizikovým faktorem pro vznik CMP [11]. Dabigatran etexilát působí jako přímý reverzibilní inhibitor trombinu (faktor IIa) bez antitrombinové aktivity. Do studie bylo zařazeno18 113 nemocných s průměrným CHADS2 skóre 2,1. 2/3 nemocných ve všech větvích tvořili muži. Na léčbu dabigatranem 110 mg bylo randomizováno 6 015 nemocných, průměrného věku 71,4 let, na dabigatran 150 mg 6 076 nemocných průměrného věku 71,5 let a na warfarin 6 022 nemocných průměrného věku 71,6 let. Podle CHADS2 skóre měla jedna třetina bodové rozmezí 0–1, další třetina dosáhla skóre 2 a zbývající nejrizikovější třetina měla 3 a více bodů.
U pacientů léčených warfarinem se vyskytla CMP nebo systémová tromboembolie u 1,71 % pacientů za rok, ve skupině s redukovanou dávkou dabigatranu 2krát 110 mg u 1,54 % a při dávkování dabigatranu 2krát 150 mg u 1,11 % sledovaných za rok. Z výsledků studie můžeme shrnout, že dabigatran 2krát 110 mg má stejný výskyt CMP a systémové tromboembolie jako warfarin s výrazně nižším počtem velkých krvácení. Dabigatran 2krát 150 mg má výrazně nižší počet CMP a systémových tromboembolií než warfarin se stejným výskytem krvácení (obr. 2, 3). Obě dávky dabigatranu snižují výskyt závažného mozkového krvácení oproti warfarinu. Výsledky primárního cíle studie RE-LY a výskyt krvácení shrnují tab. 3 a 4. Obě dávky dabigatranu se neprojevily hepatotoxicitou či nefrotoxicitou, ale byl zaznamenán větší výskyt dyspepsií. Při vyšší dávce dabigatranu bývá častější krvácení do zažívacího traktu, většinou u pacientů starších 75 let. K prevenci je možné zvážit podání inhibitorů protonové pumpy. Vyšší výskyt infarktů byl nejspíš náhodný.
2. Výsledky studie RE-LY. 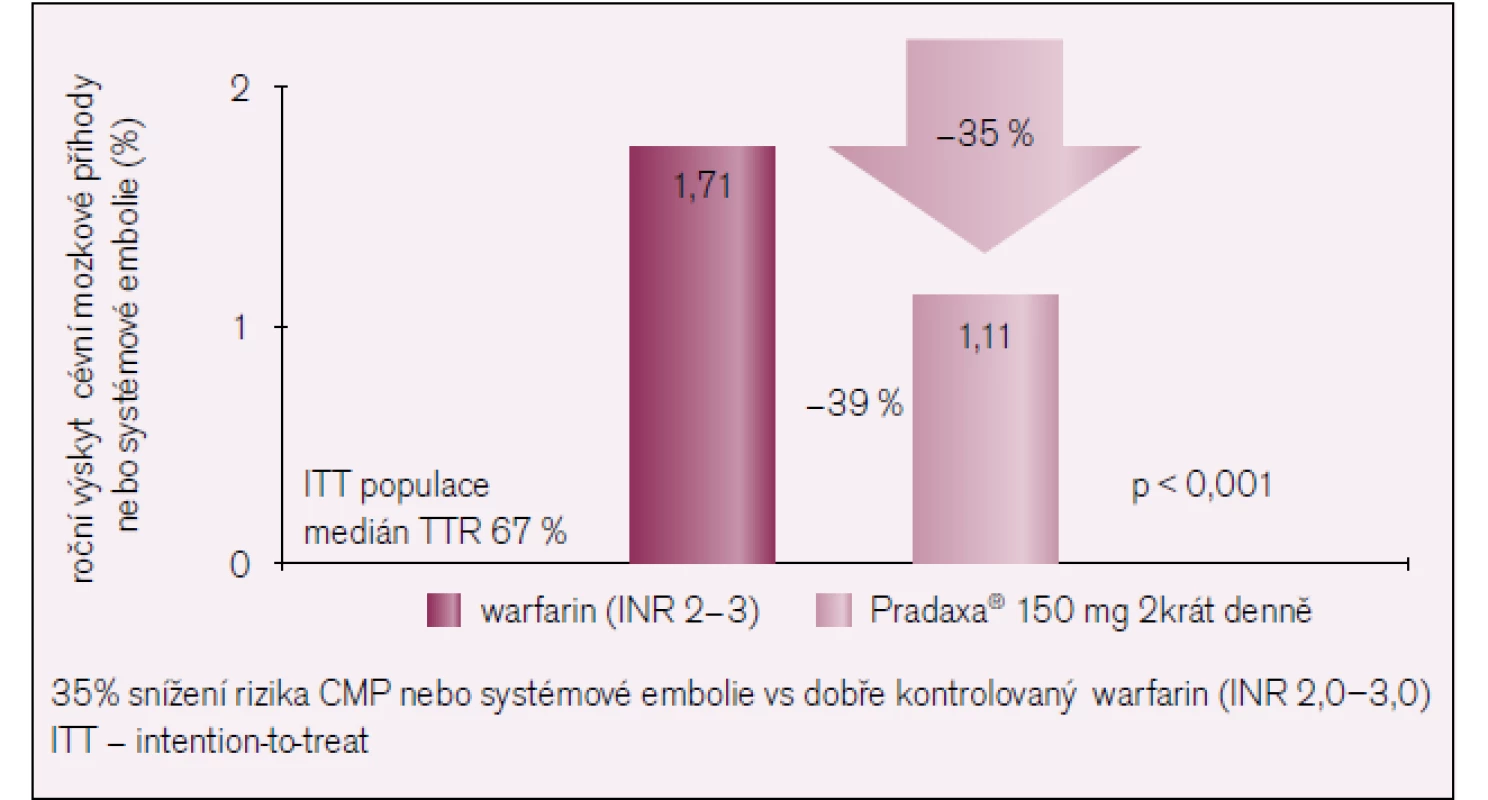
Dabigatran – Pradaxa je v dávce 2krát 150 mg účinnější v prevenci CMP a systémové embolie než warfarin. Dochází k 35% snížení rizika CMP nebo systémové embolie ve srovnání s dobře kontrolovaným podání warfarinu (INR 2,0–3,0). Upraveno podle [13,19]. 3. Výsledky studie RE-LY. 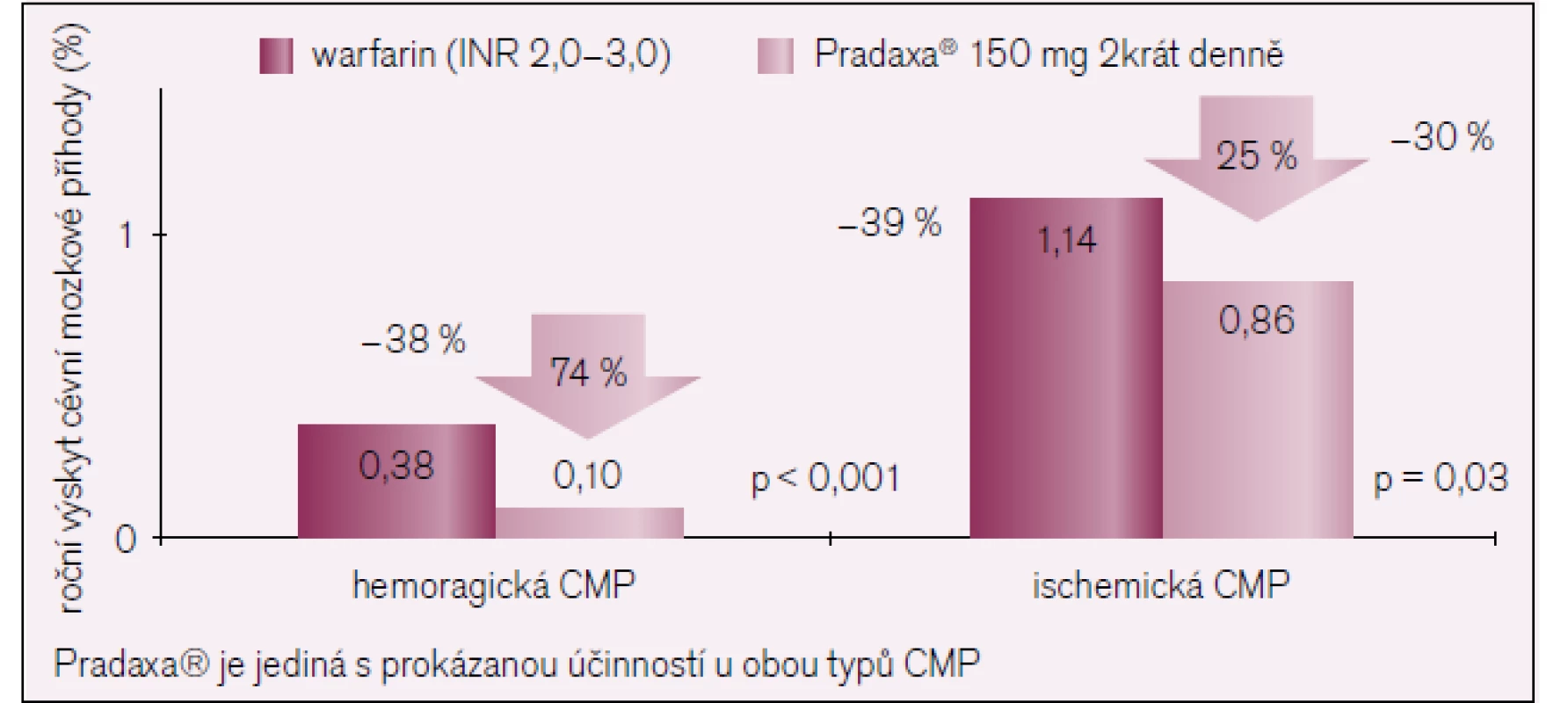
Dabigatran – Pradaxa v dávce 2krát 150 mg snižuje riziko ročního výskytu hemoragické CMP o 74 % a ischemické CMP o 25 % ve srovnání s warfarinem. Upraveno podle [12,19]. 3. Primární cíl ve studii RE-LY. Upraveno podle [11]. ![Primární cíl ve studii RE-LY. Upraveno podle [11].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/98c0da59ff34a19d124ef6683ee0376b.png)
4. Krvácení ve studii RE-LY. Upraveno podle [11]. ![Krvácení ve studii RE-LY. Upraveno podle [11].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/fd3fa3f3d3de7ec59b550c342f584e66.png)
Indikace dabigatranu
Na základě studie RE-LY byl dabigatran schválen FDA k preventivnímu podávání. V České republice je pod názvem Pradaxa (firmy Boehringer-Ingelheim, SRN) schválen již delší dobu k prevenci žilních tromboembolií u dospělých pacientů po elektivní náhradě kyčelního a kolenního kloubu. Jako první z nových antitrombotik je v České republice k dispozici v indikaci prevence CMP a systémové tromboembolie u nevalvulární FS s přítomným jedním nebo více rizikovými faktory – CMP, tranzitorní ischemická ataka nebo systémová embolie v anamnéze; ejekční frakce levé komory < 40 %; symptomatické srdeční selhání NYHA II a vyšší; věk ≥ 75 let; věk ≥ 65 let spojený s diabetes mellitus nebo ischemickou chorobou srdeční či hypertenzí.
Dávkování
U většiny pacientů je doporučovaná dávka 150 mg 2krát denně.
Dávku 2krát 110 mg je nutné zvážit u středně těžké poruchy funkce ledvin při kreatininové clearence 30–50 ml/min a vysokém riziku krvácení, u pacientů mezi 75–80 lety, u kterých převažuje riziko krvácení nad tromboembolií, dále u pacientů se zvýšeným rizikem krvácení, přítomnou gastritidou, ezofagitidou a gastroezofageálním refluxem.
Dávkou 2krát 110 mg musí být léčeni pacienti ve věku 80 let a více, z důvodu zvýšeného rizika krvácení a pacienti medikující verapamil.
Pokud se bude u pacienta přecházet z warfarinu na dabigatran, musí se podání antagonistů vitaminu K ukončit, a jakmile je hodnota INR < 2, lze dabigatran podat. Pokud se přechází z parenterální antikoagulační léčby na dabigatran, podá se dabigatran 0–2 hod před časem, na který připadá následující dávka nízkomolekulárního heparinu, nebo v době přerušení kontinuálního podání heparinu.
Zapomenutá dávka dabigatranu může být užita do 6 hod před podáním následující dávky. Pokud je čas do následující dávky kratší než 6 hod, je nutné zapomenutou dávku vynechat.
Kontraindikace
Kontraindikací podání dabigatranu je hypersenzitivita na účinnou nebo pomocnou látku přípravku, těžká porucha funkce ledvin, kdy je kreatininová clearence pod 30 ml/min, klinicky významné krvácení, organické léze spojené s rizikem krvácení, porucha hemostázy, porucha funkce jater nebo jaterní onemocnění ovlivňující přežití pacienta, souběžná léčba systémově podávaným ketokonazolem, cyklosporinem, itrakonazolem a takrolimem.
Monitorování účinku
Dabigatran dosahuje nejvyšší plazmatické hladiny asi 2 hod po podání. Vzhledem ke krátkému biologickému poločasu není nutné monitorovat účinek dabigatranu. Pokud chceme za určitých stavů, jako jsou předávkování, krvácení nebo akutní operace, znát jeho účinek, použijeme ke stanovení terapeutické hladiny trombinový čas, a pokud je aPTT (aktivovaný parciální tromboplastinový čas) > 80 s před podáním další dávky dabigatranu, je vysoké riziko krvácení. Ke stanovení hladiny dabigatranu v plazmě slouží specifický test – Hemoclot trombin inhibitors. Pokud je koncentrace dabigatranu před podáním další dávky větší než 200 ng/ml, je vysoké riziko krvácení.
Pokud je nutné rychle snížit hladinu dabigatranu, je možné podat aktivní uhlí, čerstvě mraženou plazmu, u těžších stavů koncentráty aktivovaného protrombinového komplexu (Prothromplex) nebo rekombinantní faktor VIIa (NovoSeven). Díky nízké vazbě na bílkoviny je dialyzovatelný, ale zatím jsou malé zkušenosti [12,13]. Z 80 % se vylučuje ledvinami. Specifické antidotum neexistuje.
Studie ROCKET-AF (Rivaroxaban Once--daily direct factor Xa ihibition Compared with vitamin K antagonism for prevention of stroke and Embolism Trial in Atrial Fibrillation) byla mezinárodní multicentrická dvojitě zaslepená studie, která porovnávala rivaroxaban s warfarinem u pacientů s nonvalvulární fibrilací síní a zvýšeným rizikem CMP či tromboembolie. Rivaroxaban je přímý reverzibilní inhibitor faktoru Xa. Tato blokáda faktoru Xa v porovnání s dabigatranem stojí o krok výše a inhibuje konverzi protrombinu na trombin. Do studie byli zařazeni vysoce rizikoví pacienti, 55 % pacientů bylo po prodělané CMP a 90 % pacientů se léčilo s hypertenzí. Průměrné CHADS2 skóre bylo 3,5. Jednalo se o pacienty s FS a vysokým rizikem vzniku CMP, kdy více než 90 % pacientů mělo CHADS2 skóre ≥ 3. Výsledky studie byly prezentovány na podzim 2010 v Chicagu na kongresu AHA. Do studie bylo zařazeno 14 246 pacientů s fibrilací síní a rivaroxaban byl podáván v dávce 20 mg 1krát denně po dobu 12–32 měsíců. Rivaroxaban byl stejně účinný v prevenci cévní mozkové příhody jako warfarin a nezvyšoval počet krvácení.
Počet CMP a embolizací byl u 1,71 % pacientů za rok při léčbě rivaroxabanem a při léčbě warfarinem u 2,16 % sledovaných za rok, což bylo pouze na hranici statistické významnosti (p < 0,001 pro noninferioritu a 0,018 pro superioritu) (obr. 4). Při podání rivaroxabanu bylo zaznamenáno 21% snížení výskytu CMP a systémové embolizace. Kromě toho došlo v rivaroxabanové skupině také k signifikantnímu poklesu hemoragických CMP (0,26 % vs 0,44 %, p = 0,024), infarktů myokardu (0,91 % vs 1,12 %, p = 0,12), úmrtí z jakýchkoli příčin (1,87 % vs 2,21 %, p = 0,073). Výskyt závažného krvácení a klinicky významného krvácení byl v obou skupinách podobný (14,91 % vs 14,52 %), ale u pacientů užívajících rivaroxaban bylo méně často zaznamenáno krvácení vedoucí k úmrtí (0,24 % vs 0,48 %, p = 0,003), kritické orgánové krvácení (0,82 % vs 1,18 %, p = 0,007) či intrakraniální hemoragie (0,49 % vs 0,74 %, p = 0,019) (obr. 5) [14].
4. Výsledky studie ROCKET-AF. 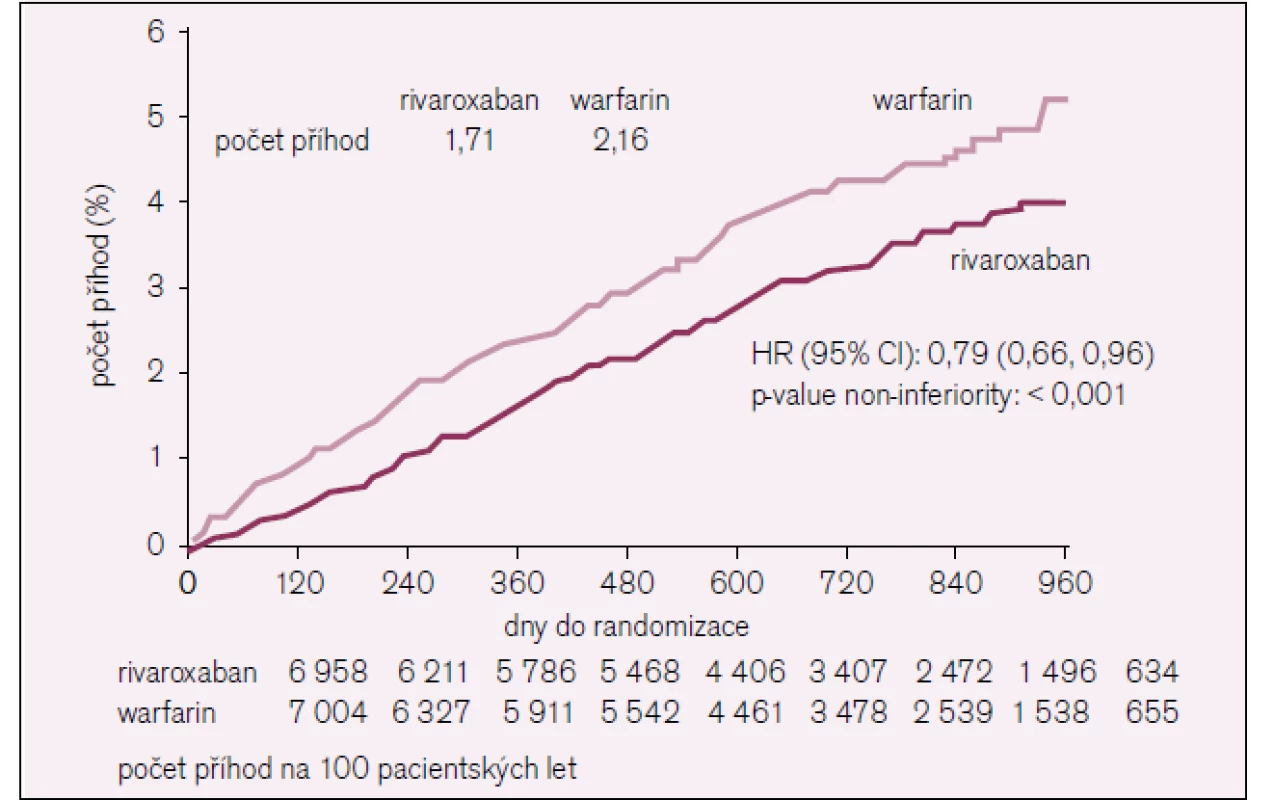
Při podání rivaroxabanu bylo zaznamenáno 21% snížení rizika výskytu CMP a systémové embolie ve srovnání s warfarinem. Upraveno podle [14]. 5. Výsledky studie ROCKET-AF. 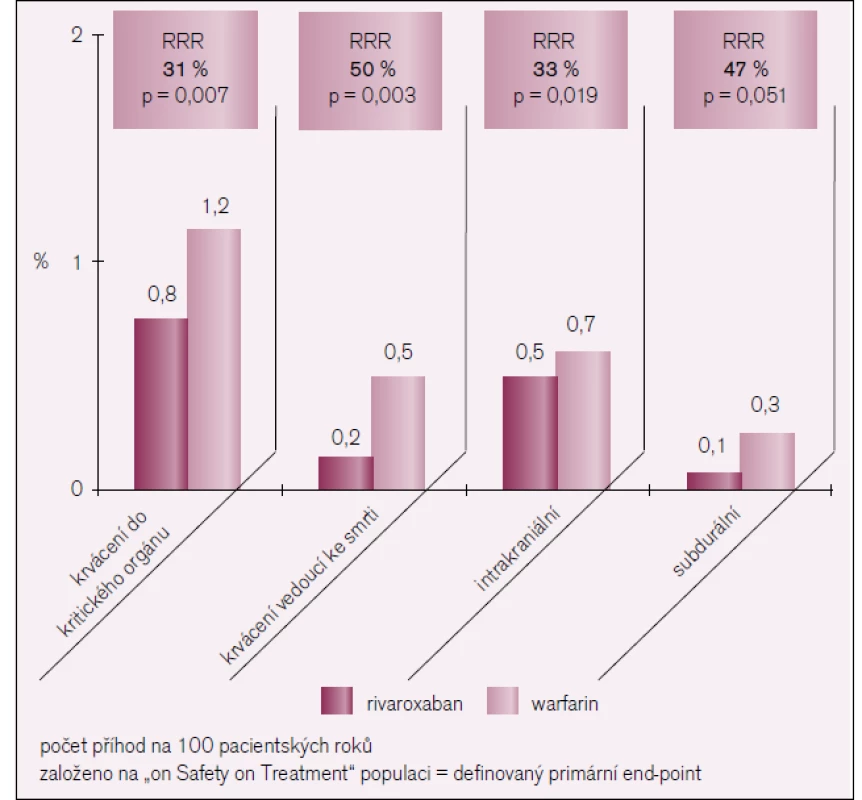
Při podání rivaroxabanu došlo ke snížení rizika krvácení do kritického orgánu o 31 %, rizika krvácení vedoucí ke smrti o 50 %, intrakraniálního krvácení o 33 %, subdurálního krvácení o 47 %. Upraveno podle [14]. V České republice je rivaroxaban k dispozici pod názvem Xarelto (firmy Bayer, SRN), ale zatím bez úhrady. Rivaroxaban je přímý inhibitor aktivovaného faktoru Xa, přímo kompetitivně obsazuje katalytické místo koagulačního faktoru. Jde o vysoce selektivní vazbu, která inhibuje faktor Xa v přímé závislosti na dávce. Rivaroxaban může inhibovat jak volný Xa, tak i vázaný v protrombinázovém komplexu. Inhibice přetrvává nejméně 12 hod. Maximální koncentrace je dosaženo za 2,5–4 hod od podání, biologický poločas je 5–11 hod. Eliminace je ze dvou třetin cestou renální a z jedné třetiny játry.
Indikace
Na základě výsledků studií byl rivaroxaban nejdříve podáván k prevenci žilních tromboembolií u dospělých pacientů po elektivní náhradě kyčelního a kolenního kloubu.
Dále je indikován k prevenci recidivující hluboké žilní trombózy a plicní embolie, ale i k léčbě hluboké žilní trombózy. Jako druhé z nových antitrombotik je v České republice k dispozici v indikaci prevence CMP a systémové tromboembolie u nevalvulární FS s jedním nebo více rizikovými faktory.
Dávkování
Doporučená dávka rivaroxabanu pro prevenci CMP a systémové tromboembolie u nevalvulární FS je 20 mg 1krát denně. Užívá se nejlépe s jídlem, které zvyšuje absorpci léku a zajišťuje vysokou biologickou dostupnost. Pokud je středně až těžce závažná renální insuficience, při clearence kreatininu 49 ml/min a méně, podává se redukovaná dávka 15 mg 1krát denně. Při poklesu clearence kreatininu pod 15 ml/min se podávání nedoporučuje.
Při vynechání dávky pacient užije lék co nejdříve a potom další dávku následující den. Dávka by se tentýž den neměla zdvojnásobit.
Pokud dojde k předávkování, lze zvážit podání aktivního uhlí ke snížení absorpce léku. Při život ohrožujících krváceních se podávají specifické prokoagulační látky, jako jsou koncentrát protrombinového komplexu (PCC), aktivovaný koncentrát protrombinového komplexu (APCC) nebo rekombinantní faktor VIIa (r-FVIIa).
Převod pacienta z warfarinu na rivaroxaban je možný při INR ≤ 3. Pokud se podává intravenózní nefrakcionovaný heparin, rivaroxaban se podá v okamžiku vysazení. Při léčbě nízkomolekulárním heparinem (LMWH) se zahájí podání 0–2 hod před další plánovanou aplikací LMWH.
Kontraindikace
Pacienti s ledvinovou nedostatečností při clearence kreatininu < 15 ml/min, jaterním selhání. Při současném užívání jiných přípravků – systémových azolových antimykotik jako ketokonazol, itrakonazol nebo inhibitorů proteáz HIV, např. Ritonavir, léků, které ovlivňují krevní srážlivost jako nesteroidní antiflogistika, kyselina acetylsalicylová inhibitory agregace trombocytů. Pacienti s jinými rizikovými faktory krvácení.
Monitorování účinku
Během léčby rivaroxabanem není nutné rutinně monitorovat parametry koagulace. Ze základních koagulačních testů jsou zvýšené protrombinový čas – PT, aktivovaný parciální tromboplastinový čas – aPTT. Pokud je klinická indikace, je možné hodnotit stav hemostázy testováním PT za použití Neoplastinu.
Vzhledem k vysoké vazbě na plazmatické proteiny se neočekává odstranění rivaroxabanu dialýzou. Specifické antidotum také neexistuje.
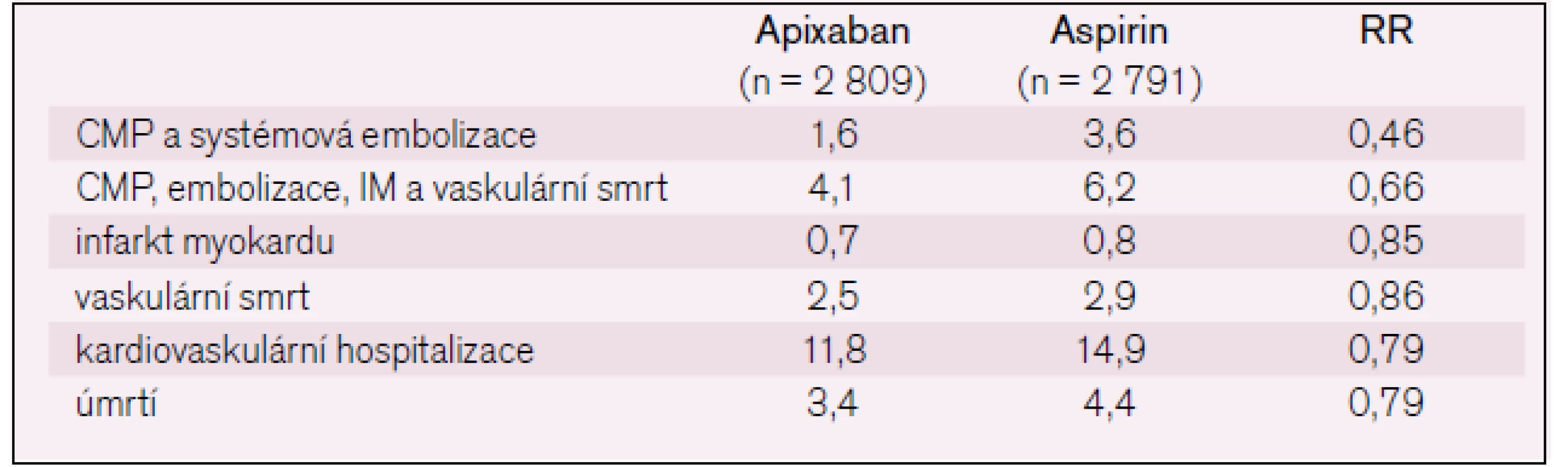
Třetí ze studií AVERROES byla předčasně ukončena pro jasný benefit z léčby apixabanem, což je inhibitor faktoru Xa, proti aspirinu u nemocných s fibrilací síní, u kterých nebylo možné užívat warfarin. Apixaban vede k signifikantnímu snížení CMP nebo systémovým tromboemboliím bez zvýšení rizika krvácení ve srovnání s kyselinou acetylsalicylovou (tab. 5, 6). Výsledky studie byly prezentovány na kongrese Evropské kardiologické společnosti v září 2010 ve Stockholmu [15].
6. Krvácení ve studii AVERROES. 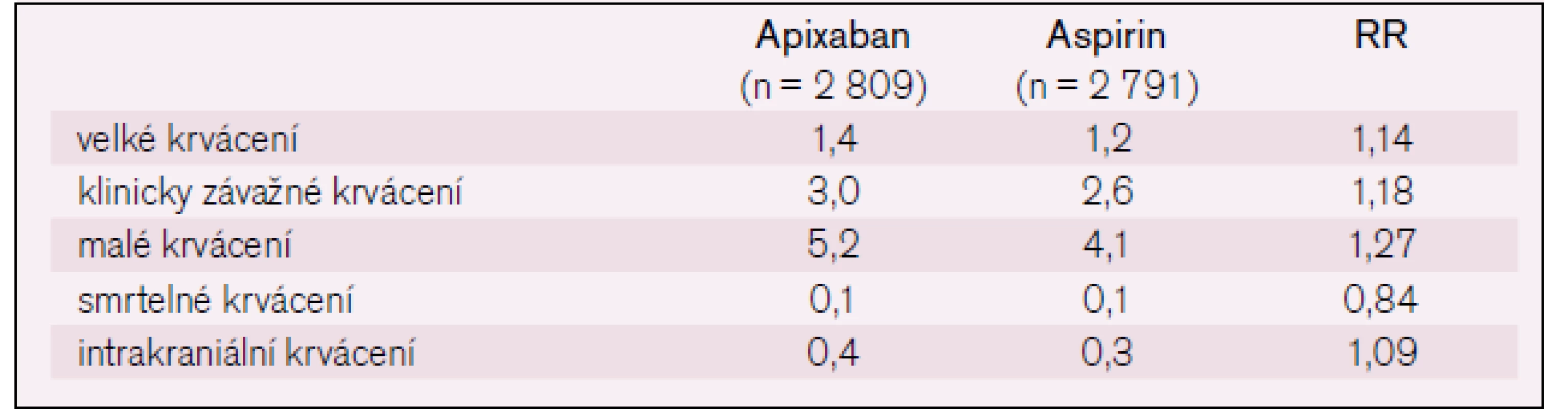
V srpnu 2011 na Evropském kardiologickém kongresu v Paříži byly prezentovány výsledky studie ARISTOTLE (Apixaban for Reduction of In STroke and Other ThromboemboLic Events in atrial fibrillation) [16]. Studie porovnávala apixaban, což je inhibitor faktoru Xa, v dávce 5 mg 2krát denně s warfarinem v prevenci CMP a systémových tromboembolických příhod u nemocných s fibrilací nebo flutterem síní a nejméně jedním rizikovým faktorem pro vznik CMP (věk ≥ 75 let, anamnéza CMP, systémová embolie či tranzitorní ischemická ataka, diabetes mellitus, hypertenze vyžadující léčbu a další). Pouze u pacientů splňujících dvě ze tří kritérií – věk nad 80 let, tělesná hmotnost pod 60 kg, koncentrace kreatininu nad 133 µmol/l se dávka apixabanu redukovala na 2,5 mg 2krát denně. Apixaban se vyznačuje rychlou absorpcí, plazmatický poločas je 12 hod, eliminace je převážně hepatální a renální představuje asi 25 %. Do studie bylo zařazeno celkem 18 201 pacientů, medián věku byl 70 let, pouze 35 % pacientů tvořily ženy, průměrné CHADS2 skóre bylo 2,1. Přibližně 20 % pacientů mělo v anamnéze CMP, tranzitorní ischemickou ataku nebo systémovou embolizaci.
Při podání warfarinu byl výskyt CMP a sysstémových embolizací u 1,6 % pacientů za rok, zatímco ve skupině léčené apixabanem u 1,27 % sledovaných za rok. Apixaban byl tedy účinnější než warfarin. Při léčbě apixabanem se převážně snížil výskyt hemoragických o 49 %, p < 0,001, ischemických a nespecifikovaných CMP o 8 %, p = 0,42. Také četnost úmrtí z jakýchkoli příčin byla nižší při podání apixabanu u 3,52 % pacientů za rok ve srovnání s 3,94 % sledovaných za rok u warfarinu. Při léčbě apixabanem se nesignifikantně snížil výskyt infarktů myokardu. Závažné krvácení se objevilo u 2,13 % pacientů za rok léčených apixabanem vs 3,09 % pacientů za rok léčených warfarinem, p < 0,001, přičemž signifikantní rozdíl byl zaznamenán především ve výskytu intrakraniálního krvácení – 0,33 % sledovaných za rok u apixabanu vs 0,80 % za rok u warfarinu, p < 0,001. Výskyt závažného krvácení při léčbě apixabanem byl nižší ve všech sledovaných podskupinách. Studie ARISTOTLE u pacientů s FS a flutterem síní a nejméně jedním rizikovým faktorem pro vznik CMP prokazuje superiotu apixabanu ve srovnání s warfarinem z hlediska snížení CMP, systémových tromboembolií a mortality z jakýchkoli příčin, přičemž při léčbě apixabanem signifikantně poklesl výskyt krvácení (obr. 6).
6. Výsledky studie ARISTOTLE. 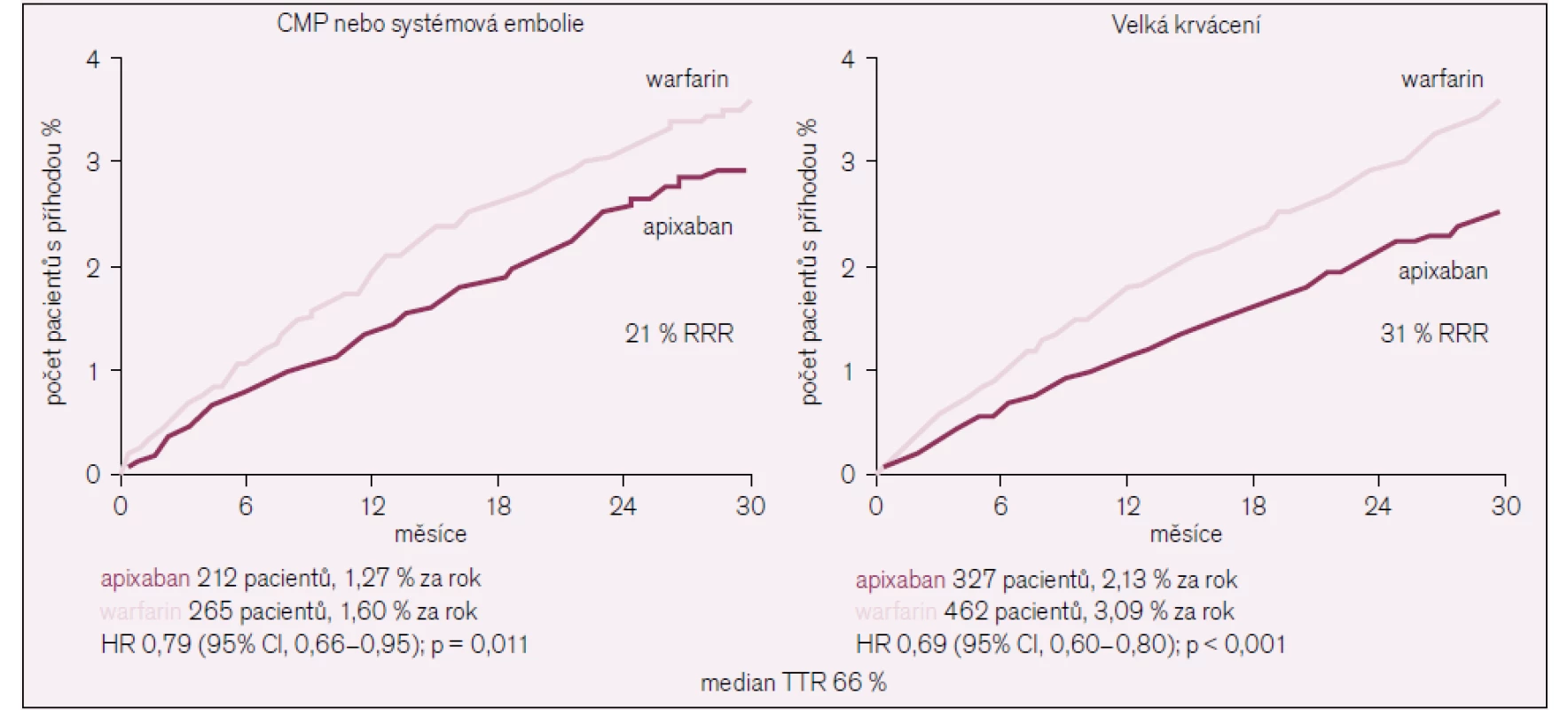
Při podání apixabanu došlo ke snížení rizika vzniku CMP a systémové embolie o 21 %, rizika velkého krvácení o 31 %. Upraveno podle [16]. V České republice je apixaban k dispozici pod názvem Eliquis (firmy BMS/Pfizer, Velká Británie), ale zatím v síle 2,5 mg.
Indikace podání apixabanu je nyní pouze k prevenci žilních tromboembolií u dospělých pacientů po elektivní náhradě kyčelního a kolenního kloubu v dávce 2,5 mg 2krát denně. Předpokládá se, že v nejbližší době se indikace podání apixabanu rozšíří i na prevenci CMP a systémových tromboembolií u pacientů s fibrilací síní podle výsledků studie ARISTOTLE.
Na závěr však musíme upozornit, že jiná studie s apixabanem u nemocných s akutním koronárním syndromem APPRAISE-2 byla předčasně ukončena pro zvýšený výskyt krvácení na aktivní léčbě.
Závěr
Nová antitrombotika působí na různých místech koagulační kaskády a byla vyvinuta z potřeby nahradit warfarin, který má řadu nevýhod, nežádoucích účinků a složité ambulantní sledování účinku léčby.
V současné době máme k dipozici výsledky velkých klinických studií se třemi novými antitrombotiky, jejichž účinek se srovnává s warfarinem u pacientů s fibrilací síní a rizikovými faktory pro vznik CMP. Jedná se o gatrany, přímé inhibitory trombinu – dabigatran (Pradaxa) a xabany, inhibitory faktoru Xa – rivaroxaban (Xarelto) a apixaban (Eliquis). U všech tří nových antitrombotik je většinou vyšší účinnost v prevenci CMP a systémových embolizací a nižší nebo srovnatelný výskyt krvácivých komplikací. V České republice jsou již dabigatran a rivaroxaban schválené pro prevenci CMP a systémové embolizace u nevalvulární FS s jedním nebo více rizikovými faktory vzniku CMP. V krátké době se předpokládá, že tuto indikaci bude mít schválenou i apixaban.
Limitací pro větší zavedení nových antitrombotik do klinické praxe je cena léků. Od 1. května 2012 je schválena úhrada zdravotními pojišťovnami pro dabigatran (Pradaxa). Doplatek pacientem na Pradaxu 60 tbl. po 150 mg je 130 Kč.
Nová antitrombotika mají řadu výhod ve srovnání s warfarinem. Jejich účinek rychle nastupuje i odeznívá, jejich dávkování je fixní bez nutnosti pravidelných laboratorních odběrů, nevyskytují se u nich závažné interakce s potravinami a mají nízký potenciál pro interakce s jinými léky. Předpokládá se vyšší účinnost s nižší frekvencí komplikací a zlepšením kvality života.
Na rozdíl od warfarinu není známo specifické antidotum. Nevýhodou je i obtížnější hodnocení účinku antitrombotik pomocí standardních koagulačních testů. Působí na různých místech koagulační kaskády, ale zatím nejsou důkazy, zda je lepší ovlivnit jeden nebo druhý faktor, protože srovnávací studie nových antitrombotik mezi sebou nemáme.
Data o možných alternativách léčby antagonisty vitaminu K – warfarinem jsou velmi povzbudivá a určitě pomohou překlenout některé významné limitace warfarinu. Přesto ale je antikoagulační léčba warfarinem stále nenahraditelná.
Na začátku 21. století vypadal velmi slibně ximelagatran, který se ve studiích SPORTF I–V zdál být dobrou alternativou warfarinu, nakonec však klinické uplatnění nenašel, protože docházelo k významnému vzestupu jaterních testů.
V současné době probíhá velká klinická studie ENGAGE u pacientů s fibrilací síní a rizikem vzniku CMP, kde se srovnává účinek edoxabanu, inhibitoru faktoru Xa s warfarinem. Ve studii je celkem 19 100 nemocných. Této studie se účastní i Česká republika. Její výsledky můžeme očekávat koncem letošního roku.
Doručeno do redakce 6. 4. 2012
Přijato po recenzi 16. 4. 2012
doc. MUDr. Růžena Lábrová, Ph.D.
Interní kardiologická klinika LF MU a FN Brno
labrova@seznam.cz
Sources
1. Go AS, Hylek EM, Phillips KA et al. Prevalence of diagnosed atrial fibrillation in adults. National implications for rhythm management and stroke prevention: The Anticoagulation and Risk Factors in Atrial Fibrillation (ATRIA) Study. JAMA 2001; 285 : 2370–2375.
2. Lábrová R. Epidemiologie fibrilace síní. Kardiofórum 2007; 5 : 6–10.
3. Camm AJ, Kirchhof P, Lip GY et al. European Heart Rhythm Association, European Association for Cardio-Thoracic Surgery. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010; 31 : 2369–2429.
4. Čihák R, Heinz P, Haman L et al. Fibrilace síní doporučený diagnostický a léčebný postup České kardiologické společnosti vypracovaný Pracovní skupinou arytmie a trvalé kardiostimulace. Cor Vasa 2011; 53 (Suppl 1): 27–52.
5. Hart RG, Benavente O, McBride R et al. Antithrombotic therapy to prevent stroke in patients with atrial fibrillation: a meta-analysis. Ann Intern Med 1999; 131 : 492–501.
6. Lip GY, Nieuwlaat R, Pisters R et al. Refining clinical risk stratification for predicting stroke and thrombembolism in atrial fibrillation using a novel risk factor-based approach: the Euro Heart Survey on atrial fibrillation. Chest 2010; 137 : 263–272.
7. Pisters R, Lane DA, Nieuwlaat R et al. A novel userfriendly score (HAS-BLED) to assess one-year risk of major bleeding in patients with atrial fibrillation: The Euro Heart Survey. Chest 2010; 138 : 1093–1100.
8. Nabauer M, Gerth A, Limbourg T et al. The Registry of the German Competence NETwork on Atrial Fibrillation: patient characteristics and initial management. Europace 2009; 11 : 423–434.
9. Conolly SJ, Pogue J, Hart RG et al. ACTIVE Investigators. Effect of clopidogrel added to aspirin in patients with atrial fibrillation. N Engl J Med 2009; 360 : 2066–2078.
10. Conolly SJ, Pogue J, Hart RG et al. ACTIVE Writing Group of the ACTIVE Investigators. Clopidogrel plus aspirin versus oral anticoagulation for atrial fibrillation in the Atrial fibrillation Clopidogrel Trial with Irbesartan for prevention of Vascular Events (ACTIVE W): a randomised controlled trial. Lancet 2006; 367 : 1903–1912.
11. Ezekowitz MD, Conolly S, Pareth A et al. Rationale and design of RE-LY: randomized evaluation of long-term anticoagulant therapy, warfarin, compared with dabigatran. Am Heart J 2009; 157 : 805–810.
12. SPC přípravku Pradaxa 110 a 150mg, SÚKL Praha, 2011.
13. Connolly SJ, Ezekowitz MD, Yusuf S et al. RE-LY Steering Committee and Investigators. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009; 361 : 1139–1151.
14. ROCKET AF Study Investigators. Rivaroxaban once daily, oral, direct factor Xa inhibition compared with vitamin K antagonism for prevention of stroke and Embolism Trial in Atrial Fibrillation: rationale and design of the ROCKET AF study. Am Heart J 2010; 159 : 340–347.
15. Eikelboom JW, O’Donnell M, Yusuf S et al. Rationale and design of AVERROES: apixaban versus acetylsalicylic acid to prevent stroke in atrial fibrillation patients who have failed or are unsuitable for vitamin K antagonist treatment. Am Heart J 2010; 159 : 348–353.
16. Granger CB, Alexander JH, McMurray JJ et al. ARISTOTLE Committees and Investigators. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2011; 365 : 981–992.
17. Weitz JI, Crowther MA. New anticoagulants: current status and future potential. Am J Cardiovasc Drugs 2003; 3 : 201–209.
18. Weitz JI, Hirsh J, Samama MM. American College of Chest Physicians. New antithrombotic drugs: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8th ed.). Chest 2008; 133 : 234S–256S.
19. Connolly SJ, Ezekowitz MD, Yusuf S et al. Randomized Evaluation of Long-Term Anticoagulation Therapy Investigators. Newly identified events in the RE-LY trial. N Engl J Med 2010; 363 : 1875–1876.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2012 Issue 2-
All articles in this issue
- Antiaggregating and anticoagulant therapy – basic principles
- Oral antiplatelet therapy in patients with acute coronary syndrome
- Current guidelines for antiplatelet therapy in neurology
- Anticoagulant therapy and atrial fibrillation
- New peroral antithrombotics in the prevention and treatment of tromboembolism
- New antithrombotic drugs in the prophylaxis of postoperative venous thromboembolism
- Current possibilities of monitoring of antithrombotic therapy – new antithrombotic drugs
- Where is a step in the current development of drugs that affect blood clotting?
- Vorapaxar in clinical studies
- What is vernakalant and what is its place in clinical practice?
- Eprosartan – dual blocker of AT1 receptors
- Multiple administration of medication and circulatory failure for malignant ventricular arrhythmias and impairment of liver function
- Heart Transplant Patient with Invasive Pulmonary Aspergillosis
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Antiaggregating and anticoagulant therapy – basic principles
- Anticoagulant therapy and atrial fibrillation
- Where is a step in the current development of drugs that affect blood clotting?
- Current guidelines for antiplatelet therapy in neurology
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career