-
Medical journals
- Career
Význam implantabilní monitorovací jednotky u pacientů s neobjasněnou synkopou
: R. Krausová
: Kardiol Rev Int Med 2007, 9(3): 177-181
Konvenční testy mají své známé limitace v diagnóze synkopy. Implantabilní monitorovací jednotka (ILR) kontinuálně monitoruje EKG po dobu několika měsíců s možností telemetrické aktivace po proběhlé synkopě a registrací záznamu během symptomů. Užití ILR představuje efektivní a bezpečnou metodu v diagnóze synkop neobjasněných konvenčními testy, zejména u nemocných s málo frekventní symptomatologií.
Klíčová slova:
dlouhodobá EKG-monitorace, neobjasněná synkopa, implantabilní monitor, bradyarytmie, tachyarytmieÚvod
Synkopa je náhlá, krátkodobá ztráta vědomí a posturálního tonu se spontánním zotavením způsobená přechodnou globální mozkovou hypoperfuzí. Odhadem postihuje 3 % mužů a 3,5 % žen; je příčinou 1–3 % akutních vyšetření a 6 % hospitalizací [1–3].
Synkopa jako symptom je projevem řady chorobných stavů od benigních až po potenciálně životu nebezpečné. Proto má její diferenciální diagnóza zásadní význam pro prognózu nemocných. Zásadním úkolem z hlediska prognózy je vyloučit kardiální, resp. arytmickou příčinu synkopy.
Zhruba u 60 % pacientů se pomocí podrobné anamnézy v kombinaci s fyzikálním vyšetřením a 12svodovým elektrokardiogramem (EKG) podaří příčinu synkopy objasnit, zbývajících 40 % zůstává nejasných i poté, co se pacient podrobí klinickému vyšetření [2,4].
Zlatým standardem pro diagnózu synkopy je dokumentace hemodynamických a elektrokardiografických nálezů. Vzhledem k charakteru synkopálních stavů, jež jsou většinou sporadické, málo frekventní a nepředvídatelné, je obtížné získat korelaci symptomů se srdečním rytmem.
Standardní ambulantní 24hodinová EKG monitorace (holterovská) je efektivní zejména u pacientů se současnými palpitacemi, její význam u pacientů se synkopou je podstatně nižší 3,5–8. Prodloužení doby monitorace nevede k podstatnému zvýšení výtěžnosti této metody. U pacientů s málo frekventní symptomatologií máme možnost použít malé externí nahrávače, tzv. event recorders, což jsou přístroje, které umožní získat až několikaminutový EKG záznam po aktivaci nemocným včetně retrográdního úseku před aktivací. Diagnostická výtěžnost však není o mnoho vyšší než u standardních monitorovacích technik [9,10].
U pacientů bez strukturálního srdečního postižení je vysoká pravděpodobnost synkopy neurokardiogenního původu. V těchto případech představuje jednoduché neinvazivní vyšetření tzv. head–up tilt test (HUT), který v mnoha případech dovoluje reprodukovat synkopu. Problémem je velký rozptyl senzitivity a specificity referovaný v jednotlivých studiích [11].
Elektrofyziologické vyšetření (EFV) má rovněž omezený přínos pro stanovení příčiny synkopy [12]. Je indikováno u nemocných s dokumentovaným strukturálním srdečním onemocněním a má větší výtěžnost při diagnóze synkop na podkladě tachyarytmií 13. Přítomnost strukturálního srdečního onemocnění se sníženou ejekční frakcí je významným prediktorem mortality a inducibility arytmií během EFV u pacientů se synkopou [9]. U pacientů bez organického srdečního postižení bývá EFV negativní [14]. Po provedení těchto konvenčních testů zůstává zhruba 10–26 % synkop nediagnostikovaných (tab.) [15–17].
1. Odhadovaná výtěžnost diagnostických metod pro objasnění původu synkopy. 
Implantabilní monitorovací jednotka(ILR)
V posledních letech byla do praxe zavedena implantabilnímonitorovací jednotka (Reveal Plus, Medtronic Inc., Minneapolis, MN, USA), která dlouhodobě monitoruje elektrickou srdeční aktivitu a umožňuje zaznamenat EKG–informace do paměti přístroje. EKG–data mohou být zaznamenána během symptomatických epizod a umožní tak korelaci rytmu se symptomy [17–22]. Implantabilní monitor je užitečný zejména u pacientů s málo frekventními symptomy, kdy dosud používané standardní krátkodobé monitorace selhávají.
ILR je malý implantabilní přístroj (obr. 1), který se všívá do podkoží na hrudníku a z hlediska kapacity baterie je možno ho ponechat implantovaný po dobu 14–18 měsíců. Kontinuálně monitoruje elektrickou srdeční aktivitu pomocí 2 elektrod umístěných na povrchu přístroje a umožňuje zaznamenat 1svodový EKG do paměti.
1. Implantabilní monitor (Reveal, ILR) je přístroj minimálních rozměrů 61 × 19 × 8 mm se 2 snímacími elektrodami 37 mm na povrchu přístroje. ILR má hmotnost 17 g a objem 8 ml, je tedy menší než standardní kardiostimulátor. 
Přístroj je možno aktivovat 2 způsoby. Manuální aktivace pomocí ručně přikládaného aktivátoru (obr. 2) je první způsob. Pacient nebo přítomná osoba přiloží aktivátor nad implantovaný přístroj bezprostředně po příhodě. Po přiložení aktivátoru (obr. 3) je možno získat až 42 minut EKG–záznamu včetně retrográdního záznamu. První generace ILR přístrojů umožňovala pouze manuální aktivaci. Zhruba 10 % pacientů nebylo schopno správně aktivovat přístroj v době obtíží.
2. Aktivátor zprostředkuje uložení EKG dat do paměti ILR. 
3. Přiložení aktivátoru nad ILR umožní zachycení EKG při potížích. 
Nová generace má navíc schopnost automatickéaktivace při asystolii, bradykardii či tachykardii, i když jsou tyto epizody asymptomatické. Klinický význam těchto asymptomatických epizod není zcela jasný, potvrzuje se, že má u mnoha pacientů vztah k příčině synkopy, zejména pokud se jedná o závažné arytmie.
Technika implantace se podstatněji neliší od implantace kardiostimulátoru, je prováděna v lokální anestezii s profylaktickým podáváním antibiotika. Optimální polohu přístroje z hlediska senzingu lze ověřit neinvazivně před implantací. Nejčastěji je umístěn do levé parasternální oblasti mezi 1. a 4. žebrem. Analýza a dokumentace EKG je jednoduchá a provádí se pomocí standardního programovacího zařízení používaného ke kontrole kardiostimulátorů Medtronic.
Před propuštěním z nemocnice je přístroj naprogramován (obr. 4) a pacient, případně rodinný příslušník, jsou poučeni o způsobu aktivace při každé epizodě synkopy. Po každé nahrané epizodě se pacient dostaví k ambulantní kontrole, která zahrnuje také interrogaci přístroje a výpis EKG z jednotlivých epizod. Explantaci indikujeme při stanovení diagnózy nebo po ukončení životnosti přístroje.
4. Nastavení záznamu EKG v přístroji Reveal. 
K recidivě synkopy a první aktivaci dochází nejčastěji 3–4 měsíce po implantaci. Na základě dokumentovaných arytmií je synkopa klasifikována jako arytmická – a následně je indikována adekvátní léčba, tj. implantace kardiostimulátoru v případě bradykardie, resp. asystolie (obr. 5), a radiofrekvenční ablace u dokumentovaných tachykardií (obr. 6). V případě dokumentace sinusového rytmu je synkopa diagnostikována jako nearytmická.
5. Příklad EKG-záznamu arytmické epizody (žena, 56 let, opakované synkopy, asystolie, řešena implantací kardiostimulátoru). 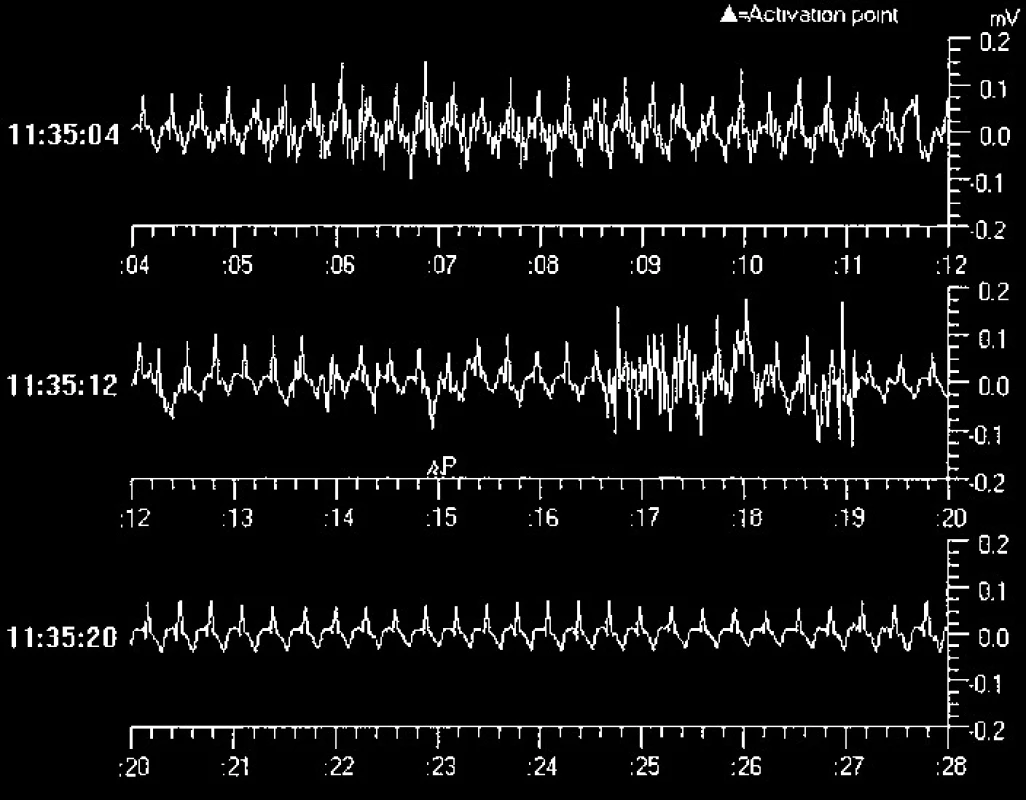
6. Příklad EKG-záznamu arytmické epizody (muž, 21 let, palpitace, presynkopy, supraventrikulární tachykardie typu AVNRT, následně řešená RF-ablací). 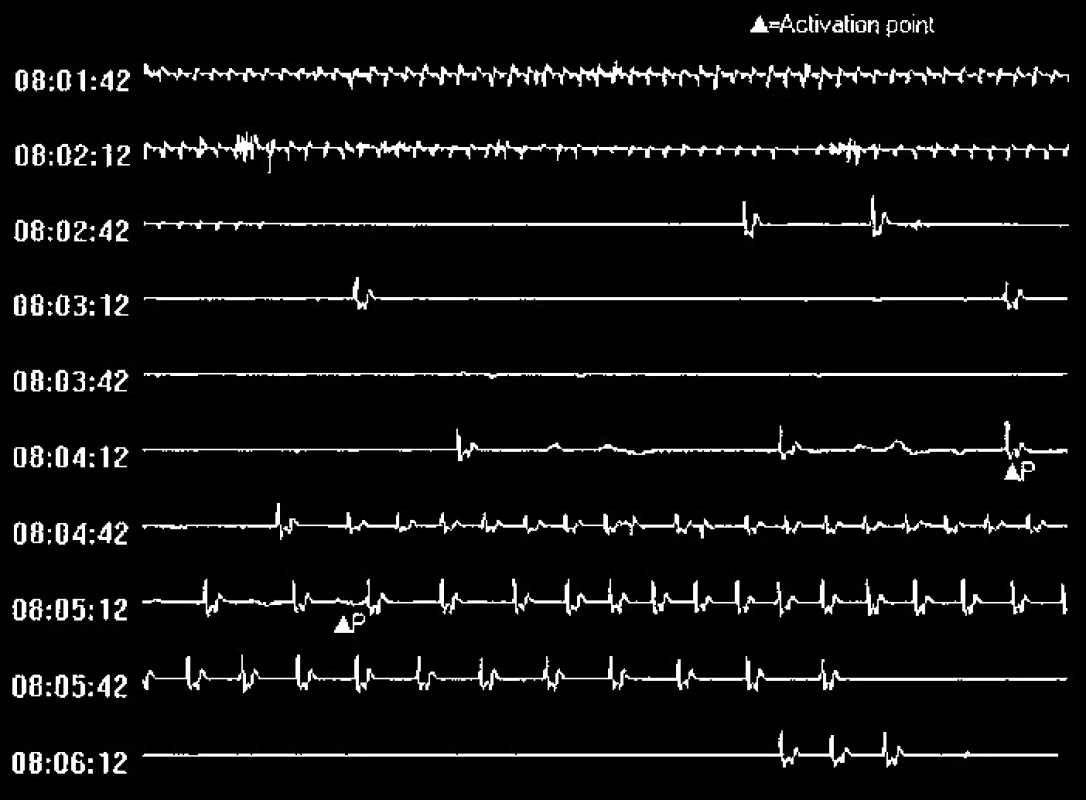
První zkušenosti v nerandomizovaných studiích ukazují přínos ILR k objasnění příčiny synkopy u 60–80 % případů v závislosti na délce sledování po implantaci přístroje [16, 18].
Pilotní kanadská studie publikovaná Krahnem et al [17] v 1998 zahrnovala 24 pacientů s neobjasněnou synkopou a implantace ILR vedla ke stanovení příčiny synkopy u 21 nemocných (88 % případů).
V roce 1998 a 1999 byly uveřejněny výsledky první multicentrické studie 19 zahrnující 85 pacientů s neobjasněnou synkopou, kterým byl implantován ILR. U 50 případů (68 %) s recidivou synkopy bylo dokumentováno 21 arytmických epizod (3krát tachykardie, 18krát bradykardie), u 29 pacientů nebyla navzdory potížím zachycena žádná arytmie. V posledních letech byly publikovány výsledky randomizovaných studií srovnávající přínos ILR s konvenčními testy v diagnostice neobjasněné synkopy, jež upřednostňují význam ILR [20–22].
Deharo [23] publikoval studii, která analyzovala srdeční rytmus během spontánních recidiv vazovagální synkopy u vysoce symptomatických pacientů dokumentovaný pomocí ILR. Rytmus byl během první spontánní synkopy identický s rytmem při jejích recidivách. Rytmus nekoreloval s výsledky při HUT. Tyto nálezy korespondují s výsledky ISSUE studie [24], kde byl výskyt spontánních asystolických synkop pozorován mnohem častěji, než by vyplynulo z výsledků HUT. Znalost srdečního rytmu během vazovagální synkopy významně přispívá k výběru terapie u těchto nemocných.
Pokud nedojde během sledování k recidivě synkopy, může jít o spontánní ústup potíží nebo o nedostatečně dlouhou dobu sledování. V prvém případě se jedná o přirozený průběh synkopy a je pravděpodobný i placebo efekt či vymizení obtíží po dosažení účelové implantace ILR [25–27].
Brignole [28] pomocí ILR ukázal, že u pacientů se synkopou, bifascikulární raménkovou blokádou a negativním EFV je při recidivě synkopy nejčastějším nálezem asystolická pauza na podkladě paroxysmální AV–blokády, zřídka na podkladě sinus arrest.
Někteří autoři uvádějí kazuistiky pacientů, u kterých byly pomocí ILR bez předchozího EFV diagnostikovány závažnější arytmie (supraventrikulární i komorové tachykardie), jež byly po řadu let příčinou synkopálních stavů [29]. S ohledem na výtěžnost konvenčních testů pro objasnění synkopy by pacienti bez organického srdečního postižení měli být indikovaní k implantaci ILR po provedení HUT s negativním výsledkem, zatímco při organickém postižení srdce je nezbytné provedení EFV.
ILR nepřispívá k objasnění epizod ztráty vědomí na podkladě poklesu krevního tlaku při ortostatické hypotenzi nebo vazodepresorickém typu vazovagální synkopy [30].
V poslední době se stále častěji používá kontinuální monitorace pomocí ILR u pacientů s fibrilací síní, zejména pro detekci asymptomatických epizod a bradykardického efektu léčby.
Využití ILR u pacientů s neobjasněnými palpitacemi demonstruje studie RUP (Recurrent Unexplained Palpitations) [31]. Výsledky ukazují diagnostický přínos ILR ve srovnání s konvenčními monitorovacími technikami a EFV u pacientů s málo frekventními palpitacemi bez závažného organického srdečního onemocnění.
Naše zkušenosti ukazují přínos ILR k objasnění příčin synkopy u 65–80 % případů. Komplikace související s implantací přístroje jsou zcela výjimečné, rovněž reimplantace při ztrátě senzingu. Při indikacích vycházíme z Guidelines ESC pro léčbu synkopy 32 z roku 2004. Provedená implantace i samotný přístroj jsou hrazeny pojišťovnou. Finanční náklady na opakované provádění konvenčních testů a implantaci ILR jsme neporovnávali, neboť finanční ohodnocení jednotlivých procedur (zejména EFV, implantace ILR) v podmínkách ČR nejsou srovnatelné s literárními údaji [33,34].
Z hlediska dlouhodobé prognózy ukazují údaje z poslední doby, že riziko rekurentní synkopy a primární arytmické smrti u pacientů s negativním nálezem z implantabilní monitorace je nízké. Z 26 pacientů během dlouhodobého sledování – follow up 27 + 16 měsíců 25 pacientů (96 %) nemělo recidivu synkopy [35].
Závěr
Problematika synkopy vyžaduje komplexní diagnostický přístup. Klíč ke stanovení příčiny synkopy spočívá v získání podrobné anamnézy a zhodnocení fyzikálního nálezu. Pro stanovení prognózy je rozhodující vyloučení organického srdečního onemocnění. U pacientů bez organického srdečního onemocnění je vysoká pravděpodobnost neurokardiogenní synkopy, kdy HUT představuje přínosné vyšetření s minimálními náklady a poměrně dostatečnou výtěžností. Vyšetření pacientů se synkopou při organickém srdečním onemocnění by mělo být vyhrazeno specializovaným pracovištím s možností případné následné nefarmakologické léčby (kardiochirurgický zákrok, katetrizační intervence a ablace arytmie, implantace kardiostimulátoru nebo defibrilátoru). Těmto pracovištím by také měla být vyhrazena indikace a implantace ILR.
- Implantace ILR je indikována u pacientů se synkopou neobjasněnou konvenčními vyšetřovacími metodami, zejména u pacientů s málo frekventními symptomy.
- EKG–data zaznamenaná během symptomatických epizod umožní korelaci rytmu se symptomy.
- Při recidivě synkopy a aktivaci ILR nám dokumentovaný EKG–záznam pomůže rozlišit mezi arytmickou a nearytmickou synkopou.
- Indikace a implantace ILR by měla být vyhrazena specializovaným kardiologickým pracovištím.
MUDr. Renata Krausová
Klinika kardiologie IKEM, Praha
Sources
1.Day SC, Cook EF, Funkenstein H et al. Evaluation and outcome of emergency room patients with transient loss of consciousness. Am J Med 1982; 73 : 15–23.
2.Kapoor WN, Karpf M, Weind S et al. A prospective evaluation and follow–up of patients with syncope. N Engl J Med 1983; 309 : 197–204.
3.Zimetbaum PJ, Josephson ME. The evolving role of ambulatory arrhythmia monitoring in general clinical practice. Ann Intern Med 1999; 130 : 848–856.
4.Kapoor WN. Evaluation and outcome of patients with syncope. Medicine 1990; 69 : 160–175.
5.Gibson TC, Heitzman MR. Diagnostic efficacy of 24–hour electrocardiographic monitoring for syncope. Am J Cardiol 1984; 53 : 1013–1017.
6.Clark PI, Glasser SO, Spoto E. Arrhythmias detected by ambulatory monitoring: Lack of correlation with symptoms of dizziness and syncope. Chest 1980; 77 : 722–725.
7.DiMarco JP, Philbrick JT. Use of ambulatory electrocardiografic (Holter) monitoring. Ann J Med 1990; 113 : 53–68.
8.Bass EB, Curtiss EI, Arena VC et al. The duration of holter monitoring in patients with syncope. Arch Intern Med 1990; 150 : 1073–1078.
9.Linzer M, Pritchett EL, Pontinen M et al. Incremental diagnostic yield of loop electrocardiographic recorders in unexplained syncope. Am J Cardiol 1990; 66 : 214–219.
10.Fogel RI, Evans JJ, Prystowsky EN. Utility and cost of event recorders in the diagnosis of palpitations, presyncope and syncope. Am J Cardiol 1997; 79 : 207–208.
11.Kapoor WN, Smith NA, Miller NL. Upright tilt testing in evaluating syncope: a comprehensive literature review. Am J Med 1994; 97 : 78–88.
12.Klein GJ, Gersh BJ, Yee R. Electrophysiological testing: the final court of appeal for diagnosis of syncope? Circulation 1995; 92 : 1332–1335.
13.Brignole M, Alboni P, Benditt D et al. Task Force on Syncope, European Society of Cardiology. Guidelines on management (diagnosis and treatment) of syncope. Eur Heart J 2001; 22 : 1256–1306.
14.Simantirakis EN, Chrysostomakis SI, Manios EG et al. Insertable loop recorder in unmasking the cause of syncope. Pacing Clin Electrophysiol 2000; 23 : 1573–1575.
15.Sra JS, Anderson AJ, Sheikh SH et al. Unexplained syncope evaluated by electrophysiologic studies and head–up tilt testing. Ann Intern Med 1991; 114 : 1013–1019.
16.Krahn AD, Klein GJ, Norris C at al. The etiology of syncope in patients with negative tilt table and electrophysiological testing. Circulation 1995; 92 : 1819–1824.
17.Krahn AD, Klein GJ, Yee R et al. The etiology of syncope in patients with negative noninvasive and invasive testing: final results from a pilot study with implantable loop recorder. Am J Cardiol 1998; 82 : 117–119.
18.Krahn AD, Klein G, Norris C et al. The etiology of syncope in patients with negative noninvasive testing: final results from a pilot study with an insertable lopp recorder. Pacing Clin Electrophysiol 1997; 20 : 1077.
19.Krahn AD, Klen GJ, Yee R. Use of an extended monitoring strategy in patients with problematic syncope. Reveal Investigators. Circulation 1999; 99 : 406–410.
20.Krahn AD, Klein GJ, Yee R. Recording that elusive rhythm. Can Med Assoc J 1999; 161 : 1424–1425.
21.Krahn AD, Klein GJ, Yee R et al. Randomized assesment of syncope trial: Conventional diagnostic testing versus a prolonged monitoring strategy. Circulation 2001; 104 : 46–51.
22.Seidl K, Breunung S, Rameken M et al. Initial experience with an implantable loop recorder in patients with unexplained syncope. Z Kardiol 2000; 89 : 43–50.
23.Deharo JC, Jego CH, LanteaumeA et al. An implantable loop recorde study og highly symptomatic vasovagal patients. J Am Coll Cardiol 2006; 47 : 587–593.
24.Moya A, Brignole M, Menozzi C et al. Mechanismus of syncope in patients with isolated syncope and in patients with tilt–positive syncope. Circulation 2001; 104 : 1261–1267.
25.Ashby DT, Cehic DA, Disney P et al. A retrospective case study to assess the value of the implantabile loop recorder for the investigation of undiagnosed syncope. Pacing Clin Electrophysiol 2002; 25 : 1200–1205.
26.Nierop PR, Van Mechelen R, Van Elsäcker A at al. Heart rhythm during syncope and presyncope: Results of implantable loop recorders. Pacing Clin Electrophysiol 2000; 23 : 1532–1538.
27.Krausová R. Dlouhodobá EKG monitorace pomocí implantabilních systémů. V. české sympozium o arytmiích a kardiostimulaci, 7.–9. října 1998, Olomouc (abstrakt).
28.Brignole M, Menozzi C, Moya A et al. Mechanismus of syncope in patients with bundle branch block and negative electrophysiological test. Circulation 2001; 104 : 2045–2050.
29.Muller U, Jochheim R, Knaup W et al. Implantable event recorder: a new aid for the diagnosis of arrhythmogenic syncope. Dtsch Med Wochenschr 1998; 123 : 1378–1382.
30.Vardas PE. From the Einthoven galvanometer to the implantable loop recorder: Revelations in store. Pacing Clin Electrophysiol 2000; 23 : 1453–1455.
31.Giada F,Gulizia M, Francese M. Recurrent Unexplained Palpitations (RUP) Study. J Am Coll Cardiol; 49 : 1951–1956.
32.Brignole M, Alboni P, Benditt DG et al. Guidelines on management (diagnosis and treatment) of syncope–update 2004. Europace 2004; 6 : 467–537.
33.Klein G, Yee R, Gonsales J et al. Cost effective analysis of diagnostic strategies in syncope of unknown etiology. Circulation 1998; 94(Suppl I): 3655.
34.Krahn AD, Klein GJ, Yee R, Manda V. The high cost of syncope: cost implications of a new insertable loop recorder in the investigation of reccurent syncope. Am Heart J 1999; 137 : 870–877.
35.Assar MD, Krahn AD, Klein GJ et al. Risk of reccurent syncope after negative implantable loop recorder monitoring: Long–term follow–up of 26 patients. Pacing Clin Electrophysiol 2002; 25 : 571 (abstrakt).
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2007 Issue 3-
All articles in this issue
- Pulmonary arterial hypertension
- The benefit of measurement of B-type natriuretic peptide for monitoring the treatment of chronic cardiac failure
- Importance of implantable loop recorder in patients with unexplaided syncope
- CURRENT MEDICAL LITERATURE LTD, LONDON 1998, 438S.
- Monitoring peroral anticoagulation therapy in outpatient practice
- Depression in patients with cardiovascular disease
- Nuclear medicine methods in the diagnosis of cardiovascular illnesses
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Monitoring peroral anticoagulation therapy in outpatient practice
- Importance of implantable loop recorder in patients with unexplaided syncope
- CURRENT MEDICAL LITERATURE LTD, LONDON 1998, 438S.
- Pulmonary arterial hypertension
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

