-
Medical journals
- Career
Familiární hypercholesterolemie: aktuality
Authors: Martina Vaclová; Michal Vrablík
Authors‘ workplace: Centrum preventivní kardiologie, III. interní klinika – endokrinologie a metabolismu 1. LF UK a VFN v Praze
Published in: AtheroRev 2021; 6(3): 163-167
Category:
Overview
Familiární hypercholesterolemie je metabolické onemocnění s rozsáhlými klinickými dopady na své nositele. Je zapříčiněna mutací v 1 ze 3 genů nezbytných pro metabolizmus LDL-cholesterolové částice. Podezření na familiární hypercholesterolemii bychom měli pojmout při hladině LDL-cholesterolu > 5 mmol/l bez výrazné elevace triglyceridů. Ke klinické diagnóze významně přispívá pozitivní rodinná anamnéza. Klinické známky familiární hypercholesterolemie jsou čím dále méně časté. V praxi se s úspěchem používají skórovací systémy, které umožňují kvantifikovat klinické podezření. Provedení molekulárně genetického vyšetření není k léčbě nezbytné, přesto může být pro pacienta přínosem. Léčba se neobejde bez diety a změn životního stylu, dále je zahajována léčba farmakologická. K dispozici máme statiny, ezetimib, eventuálně kombinace s jinými hypolipidemiky. Od roku 2018 můžeme u pacientů s familiární hypercholesterolemií indikovat léčbu PCSK9-inhibitory, tato léčba je v ČR organizována formou centrové léčby.
Klíčová slova:
familiární hypercholesterolemie – PCSK9-inhibitory – LDL-cholesterol – statiny – ezetimib – monakolin K
Úvod
Familiární hypercholesterolemie (FH) je nejčastějším monogenně dědičným metabolickým onemocněním člověka.
Biochemicky je charakterizována snížením katabolizmu LDL-cholesterolových částic, což vede k vysokým hladinám LDL-cholesterolu v plazmě a jeho dlouhodobému ukládání do stěn cév a jiných tkání. Nejdůležitějším klinickým důsledkem je předčasná manifestace aterosklerotického procesu v podobě infarktů myokardu, cévních mozkových příhod či aterosklerotického postižení tepen dolních končetin. Méně častou komplikací aterosklerózy mohou být stenóza aortální chlopně, ruptura aorty či viscerální ischemie.
FH je zapříčiněna mutací v 1 ze 3 genů potřebných při vazbě LDL-částice na LDL-receptor na povrchu hepatocytu. Mutace jsou přenášeny autosomálně dominantně (velmi vzácně i recesivně) [1]. Nejčastěji bývá příčinou mutace v genu pro LDL-receptor (přibližně u 90 % nemocných), na druhém místě v genu pro apolipoprotein B100 (přibližně u 5 % nemocných) a velmi vzácně je příčinou mutace v genu pro proprotein konvertázy subtilizin/kexin typu 9 – PCSK9 (< 1 % nemocných) [2]. Pro úplnost je nutno dodat, že u nemalé části klinicky jasných pacientů s FH není kauzální mutace odhalena nebo je nalezena mutace, jejíž přímý dopad není zcela objasněn.
Diagnostika FH
Diagnostika FH se odvíjí ve dvou rovinách. Nejdříve se jedná o diagnostiku klinickou, která je zásadní a opírá se o průkaz vysoké hladiny celkového (T-C) a LDL-cholesterolu (LDL-C) při normální či jen mírně elevované hladině triglyceridů (TG) spolu s pozitivní rodinnou anamnézou. Laboratorní testy by měly být provedeny za standardních podmínek, tedy po 10 hodinách lačnění v době, kdy se pacient cítí zdravý. Odběr by měl být potvrzen alespoň jedním kontrolním výsledkem s odstupem nejméně 6 týdnů a zároveň by měla být vyloučena možnost sekundární příčiny hypercholesterolemie (například gravidita, nefrotický syndrom, obstrukce žlučových cest, hypotyreóza, anorexie a vliv některých léků, jako jsou kortikosteroidy, pohlavní hormony včetně hormonální kontracepce). Pro rychlou orientaci si můžeme zapamatovat pouze několik čísel, u dospělého pojímáme podezření na FH vždy při hladinách LDL-C > 6 mmol/l nebo při hladině T-C > 8 mmol/l a současně LDL-C > 5 mmol/l (při hladině TG < 3 mmol/l), tab. 1. Pokud se jedná o dítě či adolescenta a/nebo pokud je pacient příbuzným již prokázaného pacienta s FH, pak je hladina potřebná k diagnostice FH nižší v závislosti na věku a stupni příbuznosti (u dětí bez FH příbuzných LDL-C > 4 mmol/l) [3]. Velký důraz se klade na kaskádový screening, který by měl být využit. U diagnostikovaného dítěte se vždy snažíme vyšetřit i jeho sourozence a rodiče, a naopak u dospělého pacienta s FH je vhodné vyšetřit jeho děti a sourozence, ev. rodiče, pokud je to možné (de facto se jedná o všechny prvostupňové příbuzné, u nichž je statistická pravděpodobnost výskytu onemocnění 50 %). Je velmi pravděpodobné, že kdyby se kaskádový screening striktně uplatňoval, odhalených pacientů s FH by bylo mnohem více.
Table 1. Podezření na FH u dospělých osob (nepříbuzných s FH) 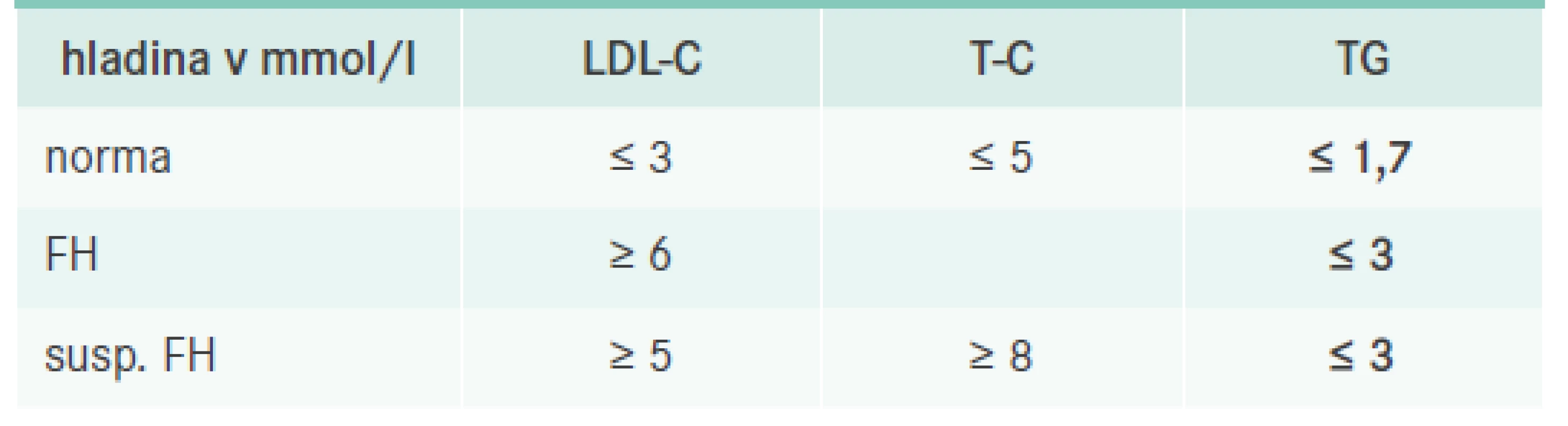
FH – familiární hypercholesterolemie LDL-C – LDL-cholesterol T-C – celkový cholesterol TG – triglyceridy Zároveň pátráme po pozitivní rodinné anamnéze. U velké části pacientů nacházíme nějakou formu předčasné manifestace kardiovaskulárních onemocnění (KVO). Za pozitivní se považuje výskyt KVO u prvostupňového příbuzného mužského pohlaví pod 55 let nebo u ženy pod 60 let věku. Přesto se stále častěji můžeme setkat i se situací, že je rodinná anamnéza buď zcela nebo částečně nevýtěžná (např. úmrtí rodiče v mladém věku na úraz či suicidiem, pacienti adoptovaní atd). V takovém případě bohužel přicházíme o cenný zdroj informací, který by nám v diagnostice FH pomohl. Ojedinělá není ani situace, kdy se nachází pozitivní rodinná anamnéza až u druhostupňových příbuzných a u prvostupňových nalezena není. Tento jev může být zapříčiněn, buď relativně nízkým věkem prvostupňových příbuzných (KVO nemají „zatím“) a/nebo jejich již delší dobu probíhající léčbou hypercholesterolemie, v takovém případě pak k manifestaci KVO nemusí dojít vůbec (což je skutečným cílem jejich léčby, na rozdíl od snížení hladiny cholesterolu, jak si mnozí pacienti bohužel myslí). Situaci s diagnostikou to však neulehčí.
Dalším ukazatelem, který může být nápomocný při stanovení diagnózy FH, jsou klinické příznaky. Klinické příznaky vyskytující se při déletrvající výrazné hypercholesterolemii nacházíme na víčcích očí v podobě xanthelasma palpebrarum, dále jako arcus lipoides corneae v podobě stříbřitě žlutavých kroužků nad okrajem duhovky oka (nemusí zabírat celý kruh) a také jako šlachové xantomy na šlachách především rukou a na šlachách Achillových. Příznaky hypercholesterolemie hledáme vždy u všech pacientů jak klinicky, tak i anamnesticky. V případě jejich nalezení je to velmi významná informace vedoucí nás k diagnostice familiární hypercholesterolemie. Prevalence klinických příznaků FH se stále snižuje. Vede k tomu běžně přístupná léčba hypercholesterolemie, z toho důvodu se klinické známky buď ani nevytvoří, nebo mohou s léčbou postupně vymizet dříve, než se pacient dostane do naší péče, v dnešní době je proto potřeba pátrat po klinických příznacích i anamnesticky, a to jak u rodiny, tak i u pacienta. Nezřídka se stává, že pacient podstoupí plastickou operaci víček, při které byla xanthelasmata odstraněna (někdy i opakovaně).
Jak vyplývá z výše uvedeného, klinická diagnostika FH není vždy zcela jednoduchá a jednoznačná. Z toho důvodu byly vyvinuty různé skórovací systémy, které mají za cíl diagnostiku usnadnit. Například se jedná o kritéria Simona Brooma nebo nizozemský systém Dutch Lipid Clinic Network Criteria (DLCN-kritéria) [4]. Obvykle se jedná o bodovací systém, ve kterém jsou body konkrétnímu pacientovi přiřazovány dle jeho rodinné a osobní anamnézy, fyzikálního vyšetření, dle nejvyšších výsledků hladiny LDL-cholesterolu v laboratorních výsledcích a ev. dle výsledků genetického vyšetření. V praxi se zdá nejkomplexnější systém DLCN-kritérií (tab. 2).
Table 2. Dutch Lipid Clinic Network Criteria pro diagnózu familiární hypercholesterolemie. Upraveno podle [4] ![Dutch Lipid Clinic Network Criteria pro diagnózu familiární hypercholesterolemie. Upraveno podle [4]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/7f9c07c46f78cd4f9ddd2d2ca8034eb3.png)
V každé z kategorií – rodinná a osobní anamnéza, fyzikální vyšetření, laboratorní vyšetření a analýza DNA je zvolena jen jedna – nejvyšší možná bodová hodnota.
Diagnóza FH je jistá při stavu skóre > 8 bodů, pravděpodobná při skóre 6–8 bodů a možná při skóre 3–5 bodů.
HDL-C– HDL-cholesterol ICHS – ischemická choroba srdeční LDL-C– LDL-cholesterol PCSK9 – proprotein konvertáza subtilizin/kexin typu 9
TG – triglyceridyDále můžeme, ale nemusíme, v diagnostice pokračovat genetickým vyšetřením, a to snahou o průkaz kauzální mutace. Genetické vyšetření přináší aspekty, se kterými je nutno počítat. Především jde o vyšetření, se kterým konkrétní pacient musí projevit písemný informovaný souhlas (bez souhlasu nelze k vyšetření přistoupit). Dále přináší nemalou finanční zátěž naštěstí jen jednorázovou. Případy, v nichž je genetické vyšetření potřeba opakovat, jsou velmi vzácné (v podstatě pouze při diskrepanci klinického a genetického vyšetření s podezřením na záměnu vzorků).
V neposlední řadě je potřeba zvážit, jakou informaci výsledek za vyšší cenu přinese a k jakému bude užitku. Z osobní praxe máme zkušenost, že kompliance k léčbě je u pacientů se známou mutací výrazně lepší než těch, kteří známou mutaci nemají a svou diagnózu familiární hypercholesterolemie často prezentují jako „vyšší cholesterol, který má dnes skoro každý“. Zároveň pacienti se známou mutací mají větší snahu a asi i argument pro vyšetření svých pokrevních příbuzných (především dětí a sourozenců). Do nedávné doby však genetické potvrzení klinické diagnózy familiární hypercholesterolemie nemělo přímý dopad na způsob a dostupnost léčby pro konkrétního pacienta. Léčba byla indikována zcela shodně, pokud pacient měl „pouze“ klinickou nebo i geneticky potvrzenou familiární hypercholesterolemii. Časy se však mění. V posledních 3 letech je k dispozici mimo jiné i biologická léčba hypercholesterolemie, konkrétně dva léky ze skupiny PCSK9-inhibitorů (alirokumab a evolokumab), která je indikována u pacientů s familiární hypercholesterolemií při nedostatečném snížení hladiny LDL-cholesterolu při maximální tolerované perorální léčbě (statinem, ev. v kombinaci s ezetimibem). V tomto případě lze s výhodou (naštěstí ne nezbytně) využít kritéria DLCN se zahrnutím genetické diagnózy familiární hypercholesterolemie.
Všeobjímající průnik technologií do našich životů můžeme také použít i při výpočtu bodových škál užívaných běžně k diagnóze familiární hypercholesterolemie (např. https://www.mdcalc.com/ nebo https://www.heartuk.org.uk).
Genetika
Jak bylo řečeno výše, výsledek molekulárně genetického vyšetření, ať již pozitivní či negativní, nemá přímý faktický vliv na léčbu pacienta.
Přednostně bychom měli uvažovat o genetickém vyšetření u pacientů, kteří mají velmi vysoké hodnoty LDL-C a je u nich podezření na homozygotní či smíšeně heterozygotní konstelaci mutací pro FH, dále pak u pacientů s těžkými nebo velmi časně se objevujícími klinickými známkami ze stejného důvodu. Stejně tak je výhodou, pokud je v jedné poradně léčeno více příbuzných, pak je možno otestovat jen jednoho z nich a ostatní pak testovat pouze na již odhalenou mutaci.
Genetické formy FH byly dříve děleny na FH heterozygotní a homozygotní dle průkazu 1 nebo obou mutovaných alel genu pro metabolizmus LDL-C (orientačně se jim přisuzovala i odpovídající hladina LDL-C). S přibývajícími poznatky v oboru molekulární biologie a přibývajícím množstvím geneticky vyšetřených pacientů s klinickou diagnózou FH však dochází k roztříštění tohoto zavedeného schématu. Geneticky se tedy může jednat o heterozygoty, homozygoty (s 1 totožnou mutovanou alelou) nebo o tzv. smíšené heterozygoty, kteří mají 2, avšak různé mutace alel stejného, či dokonce odlišného genu pro metabolizmus cholesterolu. Vzhledem k tomu, že sama přítomnost některé z mutací neříká nic o tíži klinického onemocnění ani o výši hladiny LDL-C v krvi, je nejlepší vyjadřovat výsledky genetického vyšetření pouze jako přítomnost dané mutované alely či alel s vysvětlením její klinické významnosti (pokud je známa) [5]. Není třeba se snažit je kategorizovat do jednotlivých podskupin. Je známo, že i jednotliví členové jedné rodiny nesoucí stejnou kauzální mutaci mohou mít různou tíži jak laboratorních, tak i klinických projevů. Závisí tedy jistě i na vlivu jiných genů a náš pohled na FH jako monogenně dědičné onemocnění se postupně, ale jistě mění na klinickou FH zapříčiněnou více či méně polygenně [6,7]. Podrobně se molekulárně genetickou diagnostikou u FH zabývá článek Mgr. Lukáše Tichého v tomto čísle AtheroReview.
Léčba: kdy, čím, jak?
Dietetická opatření a úprava životního stylu jsou nezpochybnitelným minimem, které pro svůj zdravotní stav může pacient udělat. Je potřeba si ale uvědomit, že zásadní je především trvání těchto opatření a pacientova celoživotní adherence k nim. Z toho důvodu preferujeme, ne imperativní, ale opakované vysvětlování vhodné diety se snahou o postupné zařazování změn, s tlakem na velmi dobrý životní styl po dobu běžného všedního života, ale s přípustným uvolněním diety ve dnech výjimečných a svátečních.
Naopak opatření k ukončení kouření by měla pro lékaře i pacienta být imperativem a zcela nezbytnou součástí léčby pacienta s familiární hypercholesterolemií, a to s využitím všech dostupných možností, vysvětlení, protikuřácké intervence, včetně konzultace v centru pro léčbu závislosti na tabáku, rozpisu nikotinových náhrad nebo eventuálního předpisu vareniklinu (např. www.bezcigaret.cz, www.slzt.cz).
Medikamentózní léčba FH je indikována u dospělých pacientů v okamžiku stanovení diagnózy. U většiny pacientů to nečiní obtíže, je nutno si uvědomit a zdůraznit jim, že vysoká hladina cholesterolu trvá od narození, a proto měl cholesterol již mnoho let možnost se jim „usazovat do cév“, ev. lze nastínit, že jejich „cévy jsou starší než zbytek jejich těla a kalendářní věk“ (pravděpodobně budou omezujícím faktorem jejich dožití).
U pacientů odhalených již v dětském věku zahajujeme léčbu nejpozději při dosažení dospělosti. V některých indikovaných případech dříve. Obvykle se v dětském věku zahajuje léčba pouze u homozygotů, u chlapců při obzvláště pozitivní rodinné anamnéze nebo při kumulaci významných rizikových faktorů. Nejčastěji je léčba zahájena ve věku 8–10 let u chlapců nebo později v adolescenci.
První volbou v léčbě familiární hypercholesterolemie jsou vysoce účinné statiny (atorvastatin a rosuvastatin) [8]. Dávku volíme individuálně, jak s přihlédnutím ke každému pacientovi, tak i k vlastní klinické zkušenosti. Lze začínat nižší dávkou 10 či 20 mg/den s úmyslem dávku navyšovat postupně až k dosažení cílové hodnoty LDL-C (tab. 3). Obzvláště vhodný je tento postup u starších pacientů, u pacientů s předchozí zkušeností s nežádoucími účinky či u pacientů s nižšími vstupními hodnotami, u kterých lze předpokládat dostatečnou účinnost i nižších a středních dávek léku. Naopak zahájení léčby maximálními dávkami léků lze doporučit u pacientů mladých, dosud bez zkušenosti s léčbou a nežádoucími účinky statinů či u pacientů s vysokými vstupními hladinami cholesterolu, u nichž lze předpokládat, že střední dávky statinů nebudou dostatečné. U obou postupů lze dosáhnout velmi dobrých výsledků za předpokladu, že s pacientem pracujeme citlivě, vysvětlujeme a respektujeme v něm partnera hodného spolupráce.
Table 3. Cílové hladiny LDL-C. Upraveno podle [3] ![Cílové hladiny LDL-C. Upraveno podle [3]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/987632f943c6f36875810e0cf8038399.png)
FH – familiární hypercholesterolemie KV – kardiovaskulární LDL-C – LDL cholesterol RF – rizikové faktory aterosklerózy Cílem léčby by mělo být vždy dosažení cílové hodnoty LDL-C, v první řadě využitím maximální potřebné či maximálně tolerované dávky vysoce účinného statinu. Pokud to není možné, snažíme se využít i ostatní dostupné statiny v nejvyšší možné tolerované dávce (simvastatin, fluvastatin, lovastatin). V uvedených případech přidáváme k maximální (tolerované) dávce statinu ezetimib, pokud nebylo dosaženo cílové hladiny LDL-C.
V případech nouze lze užívat i nestandardní dávkování statinů v kombinaci s ezetimibem, nebo i kombinaci s fibrátem (např. v případě přítomné hypertriglyceridemie nebo diabetu). Sekvestranty žlučových kyselin jsou v klinické praxi využívány opravdu minimálně, jak pro jejich horší dostupnost na trhu, tak i pro jejich četné gastrointestinální nežádoucí účinky a určité nepohodlí při užívání.
U některých pacientů lze s výhodou použít i monakolin K, volně prodejný potravinový doplněk získávaný přírodní cestou z plísně Monascuc purpureus, která barví substrát (nejčastěji rýži) na červeno. Extrakt získaný touto cestou obsahuje především monakolin K, který je chemicky identický s lovastatinem. Užívá se v dávce 10 mg/den a jeho účinek je slabší než účinek běžně užívaných statinů, avšak v kombinaci s ezetimibem může být snížení hladiny LDL-C uspokojivé (u některých pacientů se statinovou intolerancí nebo pacientů alternativně smýšlejících také bohužel jediné možné).
PCSK9-inhibitory
V posledních 3 letech máme možnost volby biologické léčby preparáty ze skupiny PCSK9-inhibitorů (alirokumab a evolokumab). Tuto léčbu je možno u familiární hypercholesterolemie indikovat z prostředků veřejného zdravotního pojištění při splnění úhradových podmínek [9] nebo formou samoplátcovství.
Odesílání do PCSK9 center
Do PCSK9 center by měli být odesíláni pacienti s FH diagnostikovanou jako pravděpodobná nebo jistá (dle kritérií DLCN nejméně 6 bodů) nedosahující při maximální statinové léčbě (rosuvastatin 40 mg/den nebo atorvastatin 80 mg/den) hodnot LDL-cholesterolu < 3,1 mmol/l, dále pak pacienti v sekundární prevenci KVO (s nebo i bez FH) při maximální statinové léčbě nedosahující hodnot LDL-C < 2,5 mmol/l.
Pokud má pacient parciální či úplnou intoleranci statinů, pak je nezbytně nutné, aby byly vyzkoušeny nejméně atorvastatin, rosuvastatin a ještě jeden jiný statin a tato skutečnost byla v dokumentaci precizně (včetně časových údajů a typu nežádoucích účinků) zaznamenána a dodána spolu s pacientem. V rámci provozu center ani vzhledem ke spolupráci s konkrétním pacientem není reálné ani etické v případě nedostatku informací opětovně všechny statiny zkoušet. V případě statinové intolerance se tedy k indikaci využívají hodnoty LDL-C při maximální tolerované statinové léčbě.
Ve všech případech může, ale nemusí být v kombinaci či monoterapii užit ezetimib. Pokud jsou dosažené výsledky alespoň o 20 % vyšší než hraniční hodnota, lze to komentovat tak, že by 20% snížení získané využitím ezetimibu nebylo dostatečné. Pak využití ezetimibu v medikaci není k úhradě PCSK9 podmínkou.
Dále považujeme za vhodné pacienta o zamýšlené léčbě injekčním preparátem před odesláním do centra informovat, situaci mu vysvětlit a uvážit, zda je aplikace schopen, i když jsou PCSK9-inhibitory vyráběny v předplněných perech a jejich aplikace je extrémně nenáročná a velmi dobře tolerovaná.
Závěr
Poznatky o FH, molekulárně genetická diagnostika i léčba postupují mílovými kroky kupředu. Přesto zůstává mnoho otazníků a FH je i nadále velmi zajímavým onemocněním, klinicky důležitým s rozsáhlými možnostmi jak na poli studia, diagnostiky tak i léčby. Pozitivní je, že informovanost laické populace i její zájem o vlastní zdraví výrazně narůstá. A tak je radostí s takovými pacienty pracovat.
MUDr. Martina Vaclová, PhD. | vaclova.martina@seznam.cz | www.int3.lf1.cuni.cz
Doručeno do redakce | Doručené do redakcie | Received 2. 7. 2021
Přijato po recenzi | Prijaté po recenzii | Accepted 21. 8. 2021
Sources
- Garcia CK, Wilund K, Arca M et al. Autosomal recessive hypercholesterolemia caused by mutations in a putative LDL receptor adaptor protein. Science 2001; 292(5520): 1394–1398. Dostupné z DOI: <http://dx.doi.org/10.1126/science.1060458>.
- Češka, R. Familiární hypercholesterolemie. Praha: Triton 2015. ISBN 978–80–7387–843–6.
- Vrablík M, Piťha J, Blaha V et al. Stanovisko výboru ČSAT k doporučením ESC/EAS pro diagnostiku a léčbu dyslipidemií z roku 2019. AtheroRev 2019; 4(3): 19–30.
- van Aalst-Cohen ES, Jansen AC, Tanck MW et al. Diagnosing familial hypercholesterolaemia: the relevance of genetic testing. Eur Heart J 2006; 27(18): 2240 – 2246. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehl113>.
- Brandts J, Dharmayat KI, Ray KK et al. Familial hypercholesterolemia: Is it time to separate monogenic from polygenic familial hypercholesterolemia? Curr Opin Lipidol 2020 Jun;31(3):111–118. Dostupné z DOI: <http://dx.doi.org/10.1097/MOL.0000000000000675>.
- Hubacek JA, Adamkova V, Lanska V et al. Polygenic hypercholesterolemia: examples of GWAS results and their replication in the Czech-Slavonic population. Physiol Res 2017; 66(Suppl 1): S101–S111. Dostupné z DOI: Dostupné z DOI: <http://dx.doi.org/10.33549/physiolres.933580>.
- Tada H, Kawashiri MA, Nomura A et al. Oligogenic familial hypercholesterolemia, LDL cholesterol, and coronary artery disease. J Clin Lipidol 2018; 12(6): 1436–1444. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacl.2018.08.006>.
- Mytilinaiou M, Kyrou I, Khan M et al. Familial hypercholesterolemia: New horizons for diagnosis and effective management. Front Pharmacol 2018 12; 9 : 707. Dostupné z DOI: <http://dx.doi.org/10.3389/fphar.2018.00707>.
- Informace dostupné z WWW: <https://www.sukl.cz/sukl/prehledy-cen-a-uhrad-leciv>.
Labels
Angiology Diabetology Internal medicine Cardiology General practitioner for adults
Article was published inAthero Review

2021 Issue 3-
All articles in this issue
- Editorialy
- Dopady pandemie COVID-19 na kardiovaskulární onemocnění a rizikové faktory
- Statiny a onemocnění COVID-19: Jsou si lhostejní?
- Kombinace statin a ezetimib: častěji v jedné tabletě a pro více pacientů
- Osa aterozla: játra – tepny – srdce
- NAFLD z pohledu hepatologa
- Nízký HDL-cholesterol: Jak to vlastně je?
- Srovnání profilu a léčby pacientů s nekontrolovanou arteriální hypertenzí a/nebo dyslipidemií v péči specialistů a v primární péči v Česku: srovnání výsledků studie LipitenCliDec 1 a LipitenCliDec 2
- Familiární hypercholesterolemie: aktuality
- Genetika familiární hypercholesterolemie: aktualizovaná kritéria pro interpretaci variant v genu LDLR
- Rešerše zajímavých článků ze zahraniční literatury
- Šobrův den 2021: XXXV. konference o hyperlipoproteinemiích tentokrát hybridní
- Athero Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nízký HDL-cholesterol: Jak to vlastně je?
- Familiární hypercholesterolemie: aktuality
- Kombinace statin a ezetimib: častěji v jedné tabletě a pro více pacientů
- Genetika familiární hypercholesterolemie: aktualizovaná kritéria pro interpretaci variant v genu LDLR
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

