-
Medical journals
- Career
Mechanismus vzniku hypotenze po i. v. paracetamolu u kriticky nemocných
Authors: Krajčová Adéla 1; Matoušek Vojtěch 1; Duška František 1,2
Authors‘ workplace: 3. lékařská fakulta Univerzity Karlovy, Praha 1; Klinika anesteziologie a resuscitace Fakultní nemocnice Královské Vinohrady, Praha 2; Ústav biochemie a molekulární biologie 3. LF UK, Praha 3
Published in: Anest. intenziv. Med., 22, 2011, č. 5, s. 266-271
Category: Intensive Care Medicine - Original Paper
Overview
Cíl studie:
Objasnit patofyziologii hypotenze po i. v. podání paracetamolu u kriticky nemocných.Typ studie:
Prospektivní observační cross-over studie.Název a sídlo pracoviště:
Klinika anesteziologie a resuscitace.Pacienti a metodika:
Subjekty byli ventilovaní kriticky nemocní, u kterých byl zároveň podáván paracetamol a monitorována hemodynamika metodou PiCCO, která umožňuje v reálném čase sledovat změny indexovaného srdečního výdeje (PCCI) i indexované systémové vaskulární rezistence (SVRI). Subjekt byl sledován po dobu 3 hodin po podání 1 g paracetamolu nebo negativní kontroly. Kontinuálně byly měřeny hemodynamické parametry, teplota jádra i periferie.Výsledky a diskuse:
Do studie bylo zařazeno celkem 6 subjektů, u kterých bylo provedeno 48 cyklů měření po i. v. paracetamolu a 35 po kontrolním léku. Před podáním léků se hemodynamické parametry nelišily (p = NS). Po podání kontrolního léku nedošlo k žádným významným změnám hemodynamiky. Po i. v. podání paracetamolu došlo k poklesu mediánu středního arteriálního tlaku o 7 % (p < 0,001), s maximem v 19. minutě po skončení infuze. Mechanismem je pokles jak srdečního výdeje, tak systémové vaskulární rezistence o 5 % (p < 0,001). Hemodynamická odpověď na paracetamol je interindividuálně variabilní a závislá na tělesné teplotě. Afebrilní pacienti reagují spíše poklesem SVRI v kontrastu s febrilními, kterým spíše klesal srdeční výdej (o 10 %, p = 0,01). Pokles gradientu mezi centrální a kožní teplotou, svědčící pro kožní vazodilataci, byl dokumentován u febrilních subjektů po podání paracetamolu, ale nebyl provázen významným poklesem SVRI.Závěr:
Hypotenze po paracetamolu vzniká u části kriticky nemocných díky kombinaci vazodilatace, která nesouvisí s termoregulací, a poklesu srdečního výdeje.Klíčová slova:
paracetamol – nežádoucí účinek – hypotenze – periferní cévní rezistence – srdeční výdejÚvod
Paracetamol byl do klinické praxe zaveden v roce 1956 a rozšířil se po průkazu asociace acetylsalicylové kyseliny se vznikem Reyova syndromu nejprve u pediatrických pacientů, později i u dospělých. Paracetamol je selektivní inhibitor cyklooxygenázy typu 2 a v porovnání s nesteroidními antirevmatiky má podobný mechanismus působení, ale podstatně méně nežádoucích účinků, především na gastrointestinání systém a krevní srážlivost. Tento poměrně výhodný profil a dostupnost parenterální formule jej předurčily pro poměrně široké využití v intenzivní péči i perioperační medicíně, zejména jako analgetikum (často v kombinaci s opiáty) a antipyretikum. Kromě známé a na dávce závislé hepatotoxicity je paracetamol často intuitivně považován za lék zcela nevinný a téměř prostý nežádoucích účinků.
Již v 80. letech minulého století byly zaznamenány případy závažných hypotenzí způsobených podáním perorálního paracetamolu [1]. Tento jev byl zprvu považován za součást anafylaktické či anafylaktoidní reakce u senzitivních jedinců, později ale bylo zjištěno, že se hypotenze po paracetamolu u kriticky nemocných pravidelně objevuje i bez jakýchkoli známek hypersenzitivní reakce [2, 3, 4]. Po perorálním podání paracetamolu došlo k poklesu systolického tlaku v průměru o 10 % (s maximem do 30 minut po podání) a středního arteriálního tlaku v průměru o 7 % (s maximem ve 30.–45. minutě) [3]. Podobné hypotenze byly zaznamenány i po intravenózním podání kriticky nemocným dospělým [5, 6, 7] i dětem [8]. S touto odpovědí se setkala každá zkušenější sestra u lůžka intenzivní péče a většinou se jedná o reakce nezávažné, které nevyžadují buď žádný léčebný zásah, nebo jen mírné zvýšení dávky vazopresorů. U hemodynamicky významně kompromitovaných pacientů však může být hypotenzivní působení paracetamolu nebezpečné [2, 9].
Dosud není známo, zdali paracetamol ovlivňuje krevní tlak snížením periferní vaskulární rezistence (vazodilatací) nebo snížením srdečního výdeje (negativně inotropním efektem) nebo kombinací obou jevů. Nabízí se hypotéza, že antipyretický efekt paracetamolu je provázen kožní vazodilatací (nutné k disipaci tepla), a tím dochází k poklesu periferní vaskulární rezistence a hypotenzi. Naše studie si kladla za cíl patofyziologii vzniku hypotenze po i. v. podání paracetamolu osvětlit.
Metody
Prospektivní observační cross-over studie byla prováděna na Klinice anesteziologie a resuscitace 3. LF UK a Fakultní nemocnice Královské Vinohrady. Kriticky nemocní na umělé plicní ventilaci, u kterých byl zároveň podáván paracetamol i monitorována hemodynamika metodou PiCCO, byli sledováni 3 hodiny po podání 1 g i. v. paracetamolu (který byl podáván v 6hodinových intervalech) nebo hemodynamicky indiferentního léku jako negativní kontroly. U každého ze subjektů byly opakovaně prováděny tříhodinové cykly měření střídavě po podání paracetamolu a kontrolního léku, a to tak dlouho, dokud byla invazivně monitorována hemodynamika i podáván paracetamol. Protokol studie i záznamový list pacienta byl schválen Etickou komisí FNKV a vzhledem k observačnímu charakteru studie, ve které není prováděna žádná intervence, byla studie povolena bez nutnosti získávat od subjektů informovaný souhlas (tzv. waiver).
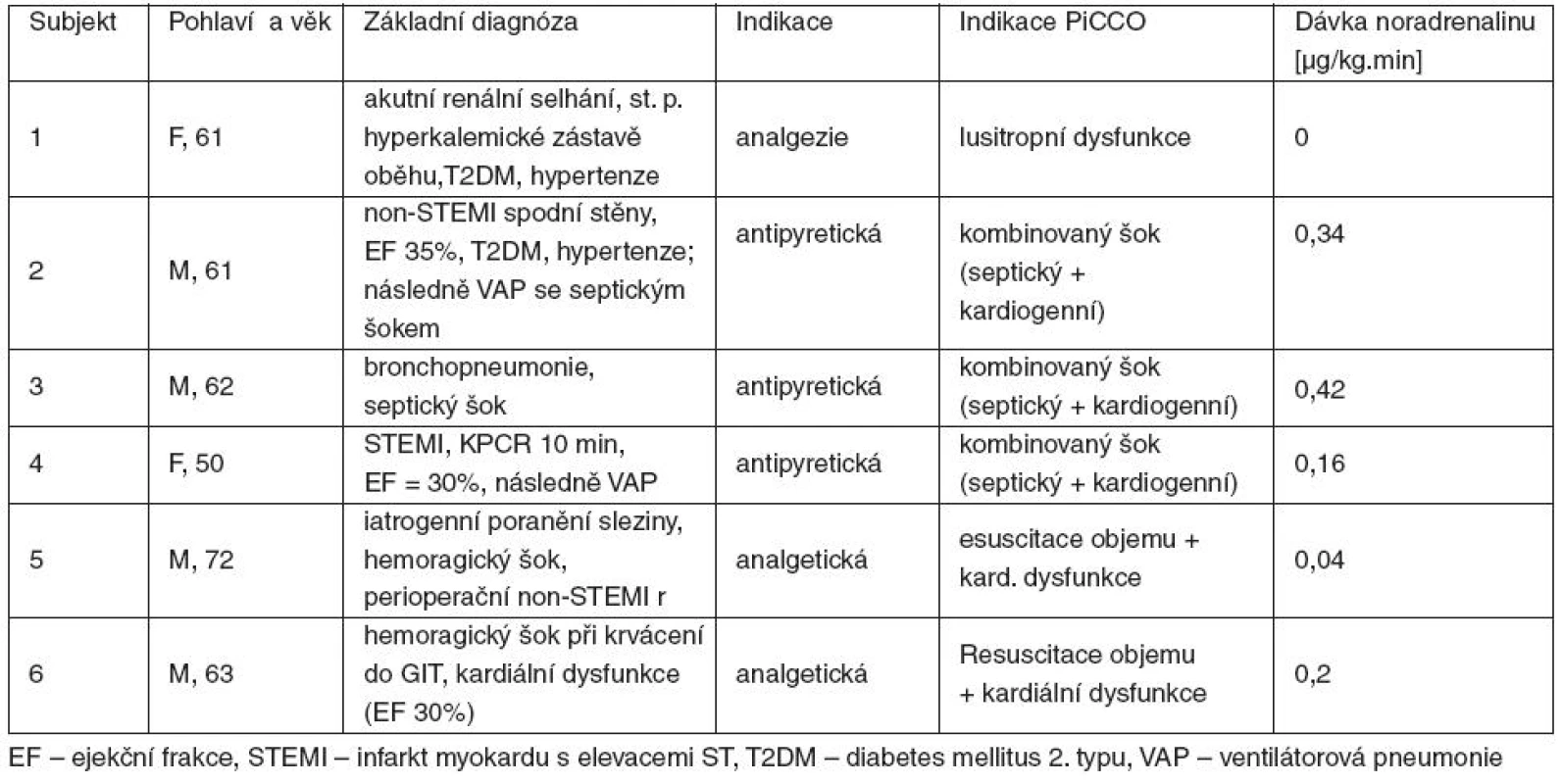
Subjekty studie byli ventilovaní kriticky nemocní nad 18 let, u kterých byl zároveň podáván i. v. paracetamol a prováděno hemodynamické monitorování metodou PiCCO. Vyloučeni byli nemocní, kteří byli hypovolemičtí (pozitivní test pasivního zvednutí končetin – vzestup PCCI > 10 %), moribudní nebo měli dávku katecholaminů nestabilní nebo vyšší než 0,5 μg/kg . min. Individuální charakteristika zařazených subjektů je uvedena v tabulce 1.
Podání medikace
Podle doporučení výrobce byl 1 g paracetamolu (Perfalgan, Bristol-Myers Squibb) v objemu 100 ml podán v 10minutové infuzi infuzní pumpou (BBraun). Kontrolní lék (Controloc – pantoprazol 40 mg/Quamatel – famotidin 20 mg/Ranital – ranitidin 50 mg) byl podáván stejným způsobem.
Hemodynamické monitorování
Metoda PiCCO (PiCCO2®, Pulsion Medical Systems, AG, USA) využívá matematické analýzy plochy pod křivkou arteriálního tlaku k výpočtu jednotlivých tepových objemů [10]. Z nich je potom vynásobením tepovou frekvencí vypočítán srdeční výdej (zobrazený jako indexovaný PCCI, přičemž PCCI = SV . HR/BSA). Indexovaná periferní (systémová) vaskulární rezistence (SVRI) je potom dopočítána vydělením tlakového gradientu ve velkém oběhu indexovaným srdečním výdejem.
SVRI = (MAP – CVP)/PCCI
Přístroj byl kalibrován podle doporučení výrobce technikou transpulmonální termodiluce před každým 3hodinovým cyklem měření. Arteriální PiCCO katétr byl zaveden do a. femoralis, žilní přístup byl cestou v. subclavia, oba invazivně měřené tlaky byly rovněž před každým cyklem překalibrovány. Na displeji přístroje se zobrazují hodnoty HR, MAP, PCCI a SVRI průměrované za 60 s. Všechny veličiny byly zaznamenávány v minutových intervalech v 0. až 30. minutě (0. minuta je baseline, 5.–15. minuta = infuze léku), v 5minutových intervalech ve 35.–60. minutě a následně po 30 minutách až do 180. minuty.
Měření gradientu centrální a periferní teploty
Centrální teplota byla měřena v břišní aortě termistorem katétru přístroje PiCCO. Periferní kožní teplota, jako měřítko kožní perfuze, byla měřena již popsanou technikou [11] elektronickým čidlem (Spacelabs Healthcare) umístěným na střed plantární plochy palce dolní končetiny, do které nebyl zaveden femorální katétr.
Statistika
Vzhledem k nenormální distribuci dat (podle Shapirova-Wilksova W testu) byly změny parametrů v čase testovány Friedmanovým testem (neparametrická varianta ANOVA pro opakovaná měření), párová data v rámci skupiny Wilcoxonovým testem a mezi skupinami Mannovým-Whitneyovým U testem. Vše v programu Statistica© ver. 8.0 (StatSoft, Inc. USA), data jsou prezentována jako medián (interkvartilový rozptyl) a hladiny významnosti p < 0,05 jsou považovány za významné.
Výsledky
Průběh studie
Do studie bylo zařazeno celkem 6 subjektů (viz tab. 1), u kterých bylo dohromady provedeno více než 250 hodin měření. Všichni pacienti byli v době měření sedováni kontinuálně podávaným fentanylem a midazolamem, s cílem dosažení stupně 2–3 Ramsayovy škály [12]. Vyloučeny byly ty cykly, kde měření nebylo možné provést (technické potíže, transport pacienta mimo jednotku), nebo pokud hemodynamické změny byly zkresleny jinými faktory (denní přerušení sedace, manipulace atp.). Celkem bylo analyzováno 48 cyklů měření po i. v. paracetamolu a 35 cyklů po kontrolním léku. Před podáním léků se hemodynamické parametry nelišily (p = NS), v 17, respektive 5 cyklech byli pacienti febrilní.
Změny hemodynamiky
Hemodynamické parametry před podáním paracetamolu a kontrolního léku se nelišily: MAP 87 (82–95), respektive 84 (79–92) torr; PCCI 3,13 (2,71–3,42), respektive 3,24 (2,92–3,72) l . min-1 . m-2; SVRI 1964 (1617–2278), respektive 1801 (1507–1946) dyn . cm-5 . m-2; centrální teplota 37,5 °C (37,1–38,1 °C), respektive 37,3 °C (37,0–37,8°C), kožní teplota 26,5 °C (25,2–31,3°C) respektive 28,7 °C (25,4–32,4°C), pro všechny p > 0,05 (Mannův-Whitneyův U test). Po paracetamolu došlo k poklesu krevního tlaku s maximem o 7 % (p < 0,001, Friedmanův test) v souvislosti s poklesem obou jeho determinant, tedy jak PCCI, tak SVRI o 5 % (p < 0,001, Friedmanův test). Po podání kontrolního léku nedošlo k žádným významným změnám hemodynamiky ani centrální, či periferní tělesné teploty (obr. 1).
Image 1. Hemodynamické změny po paracetamolu (A, B, C) a kontrolním léku (D, E, F) Křivky jsou mediány, vertikální úsečky označují interkvartilový rozptyl. Hodnoty na pravých osách grafu jsou označeny (R), na levých (L). MAP – střední arteriální tlak, SBP – systolický tlak, DBP – diastolický tlak, PCCI – srdeční index, HR – tepová frekvence, SV – tepový objem, SVRI – indexovaná systémová vaskulární rezistence, T<sub>core</sub> – teplota tělesného jádra, T<sub>periph</sub> – periferní kožní teplota 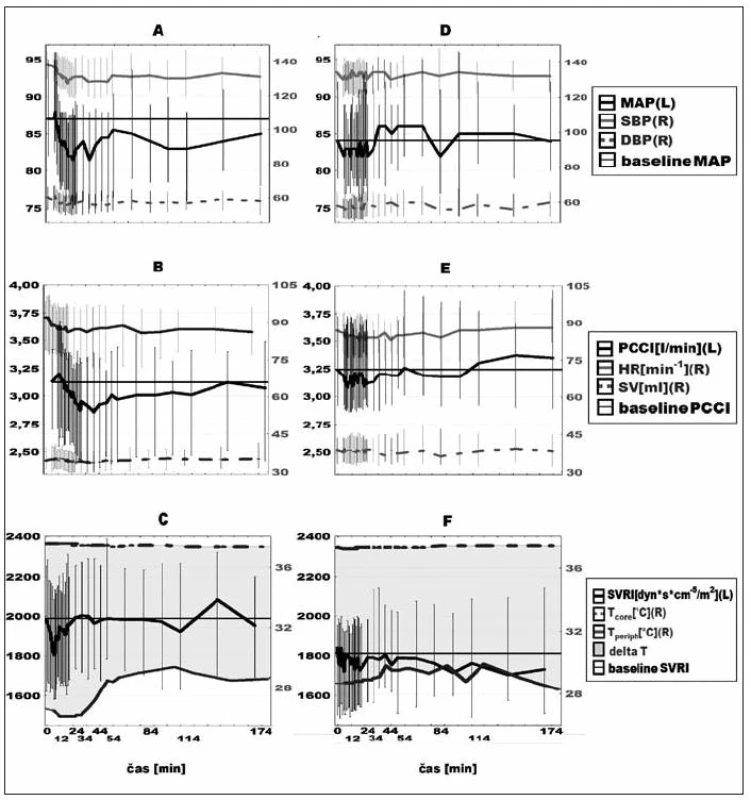
Za hranici klinické významnosti jsme si pracovně stanovili pokles o více než 15 % MAP. Pacienty, kteří takto reagovali, jsme označili jako „respondéry“ a dále analyzovali zvlášť.
Změny hemodynamiky u respondérů na paracetamol
Individuální analýza jednotlivých cyklů měření ukazuje, že zatímco u většiny pacientů nedošlo k žádným nebo jen nevýznamným změnám hemodynamiky, u 42 % cyklů po paracetamolu byl zaznamenán pokles MAP o > 15 %. U některých pacientů byly změny klinicky významné a vyžádaly si terapii – nejvyšší zaznamenaný pokles MAP po paracetamolu byl o 42 %, způsobený snížením SVRI o 51 %. Po rozdělení subjektů na předdefinované podskupiny afebrilních (centrální teplota < 37,5 °C) a febrilních (centrální teplota > 38 °C) respondérů (pokles MAP o více než 15 %), jsme analyzovali hemodynamické změny v čase maximálního poklesu MAP, který nastal v 19. minutě po začátku infuze paracetamolu.
Před začátkem infuze paracetamolu měli febrilní pacienti vyšší srdeční výdej (p = 0,01) díky vyšší tepové frekvenci (p = 0,03), ostatní hemodynamické parametry se nelišily. U afebrilních respondérů je po paracetamolu patrný pokles periferní vaskulární rezistence o 12 %, zatímco u febrilních je v baseline periferní vaskulární rezistence nevýznamně nižší než u afebrilních a po paracetamolu klesá jen o 5 %. Ani v jedné ze skupin tento rozdíl nedosáhl statistické významnosti. Srdeční výdej po paracetamolu klesá významně u febrilních pacientů díky poklesu tepového objemu a tepové frekvence. U afebrilních pacientů je patrný pokles tepové frekvence beze změny tepového objemu a nastal jen nevýznamný pokles srdečního výdeje (tab. 2).
Table 2. Hemodynamické změny po paracetamolu u febrilních a afebrilních respondérů 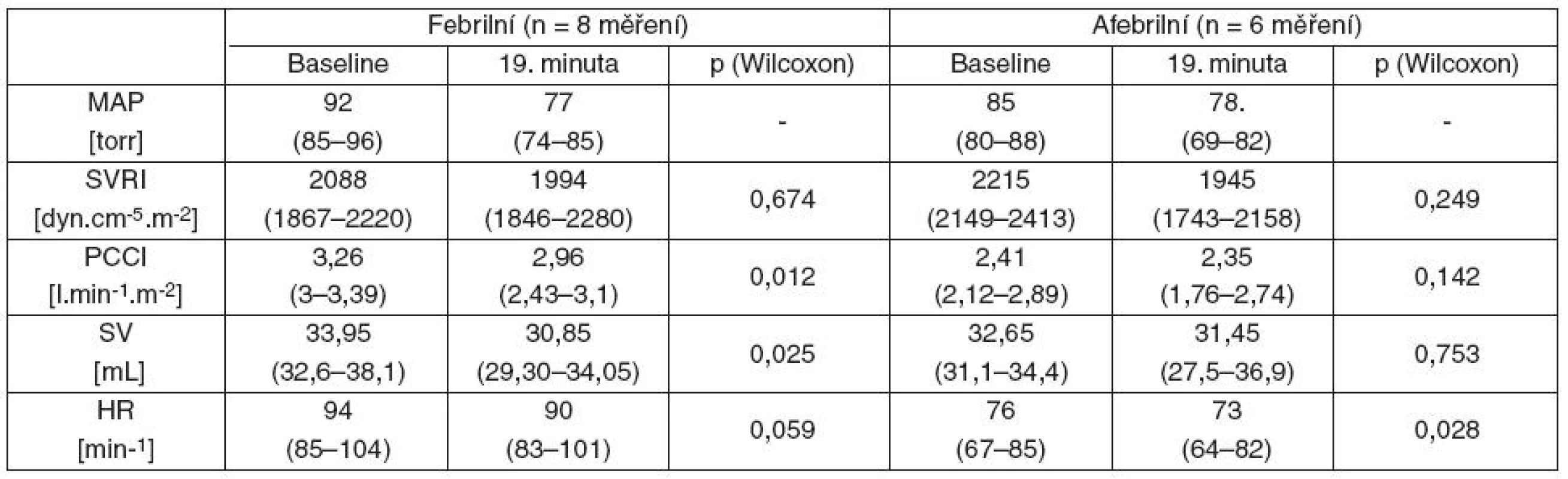
Změny tělesné teploty u respondérů na paracetamol
Největší změny tělesné teploty byly pozorovány v 69. minutě po začátku infuze paracetamolu. U febrilních subjektů poklesla centrální tělesná teplota z 38,1 °C (38,1–38,3 °C) na 37,8 °C (37,6–38,0 °C), p = 0,02; periferní kožní teplota zároveň stoupla z 25,4 °C (24,5–27,3 °C) na 28,9 °C (24,4–31,4 °C), p = 0,06. U afebrilních pacientů se centrální ani periferní teplota nezměnila: centrální teplota z 37,0 °C (36,8–37,2 °C) na 37,0 °C (36,6–37,4°C), p = 1,00; periferní kožní teplota z 25,1 °C (24,1–27,4°C) na 24,6 °C (24,6–24,8°C) p = 0,89.
Diskuse
Tato práce je první, která se zabývala změnami srdečního výdeje a periferní cévní rezistence po podání paracetamolu – dosavadní studie popisovaly změny krevního tlaku [1–6, 8] nebo souvislosti s předpokládanou imunopatologickou reakci [2, 3, 4]. Pouze v jedné observační studii byly u febrilních kriticky nemocných popsány změny kožní vodivosti, svědčící pro vzestup kožní perfuze, která časově korelovala s poklesem krevního tlaku [13].
Efekt paracetamolu na hemodynamické parametry
Analýza všech dat ze všech cyklů od našich subjektů ukazuje změny obou veličin determinujících krevní tlak – paracetamol snižoval srdeční výdej i periferní cévní rezistenci zhruba stejnou měrou, cca o 5 %. Po rozdělení na febrilní a afebrilní cykly (viz tab. 2) jsou patrny některé rozdíly. U afebrilních respondérů pozorujeme vazodilatační působení paracetamolu (pokles periferní vaskulární rezistence o 12 %), spolu se snížením tepové frekvence při nezměněném tepovém objemu. Naopak u febrilních pacientů, přestože je pozorováno snížení gradientu teploty mezi jádrem a kůží, kdy centrální teplota těla klesá a kožní teplota stoupá, periferní vaskulární rezistence zůstává téměř nezměněna, a naopak je patrný negativně inotropní efekt paracetamolu s poklesem tepového objemu i tepové frekvence. Srdeční výdej u febrilních respondérů po paracetamolu klesá o 10 %.
Příčiny negativně inotropního působení paracetamolu
Tepový objem je určen předtížením, dotížením a kontraktilitou. Ze studie byli vyloučeni hypovolemičtí, respektive volumresponzivní pacienti, přesto je možné, že paracetamol ovlivňuje předtížení, např. mechanismem venodilatace. Centrální žilní tlak však zůstal zcela beze změny 10 (9–13) vs. 10 (9–11) torr, p = 0,55, což svědčí proti změnám v žilním návratu způsobeným paracetamolem. Dotížení levé komory nemohlo být příčinou poklesu tepového objemu, neboť jeho determinanty (SVRI, MAP) se nezměnily, nebo spíše poklesly. Negativní ovlivnění kontraktility tedy zbývá jako jediný mechanismus snížení tepového objemu, i když z mechanismu účinku paracetamolu nijak nevyplývá. Je možné, že konstantní tepový objem u afebrilních respondérů je výsledkem současného negativně inotropního působení paracetamolu (s negativním vlivem na tepový objem), za současného poklesu dotížení při periferní vazodilataci (s pozitivním vlivem na tepový objem). V kontextu snížení tepové frekvence, které po paracetamolu u respondérů pravidelně následovalo, lze spekulovat o tom, že paracetamol snížil endogenní hladinu katecholaminů díky svému analgetickému působení nebo jiným mechanismem. Sám pokles teploty tělesného jádra může mít vztah k hemodynamickým změnám (např. může vysvětlit snížení tepové frekvence), ale zaznamenaný pokles teploty byl o pouhé 0,3 °C a dostavil se se zpožděním cca 50 minut po maximu hemodynamických změn.
Vztah mezi gradientem centrální a kožní teploty a systémovou vaskulární rezistencí
Kožní vazodilatace patří mezi mechanismy disipace tepla [14], ale podíl odporu kožních cév na celkové periferní vaskulární rezistenci není přesně znám [15]. U našich febrilních pacientů se vyšší perfuze kůže [13] neprojevila významnou změnou globální systémové vaskulární rezistence. Naopak k výraznějšímu poklesu periferní vaskulární rezistence došlo u afebrilních subjektů, u kterých se centrální ani kožní teplota neměnila. Maximum poklesu periferní vaskulární rezistence bylo v 19. minutě, zatímco maximum vzestupu kožní teploty (a poklesu centrální) bylo v 69. minutě. Z toho lze uzavřít, že změny systémové vaskulární rezistence po paracetamolu nijak nesouvisejí s kožní vazodilatací v rámci termoregulace.
Slabiny studie
Naše studie byla provedena na poměrně malém vzorku kriticky nemocných pacientů. Sama podmínka klinicky indikovaného invazivního monitorování před zařazením do studie vedla k tomu, že zařazené subjekty jsou podskupinou hemodynamicky problematických a kardiálně limitovaných pacientů resuscitačních oddělení a nemohou sloužit jako reprezentativní vzorek všech kriticky nemocných (tzv. selection bias). Použitá metodika kardiovaskulárního monitorování měla své limity – např. neumožnila posouzení změn preload pomocí měření plnicích tlaků levé komory. Každý nemocný sloužil jako vlastní kontrola, neboť cykly měření po i. v. paracetamolu byly střídány s cykly měření po kontrolním léku. Vzhledem k observačnímu charakteru studie nebylo možno použít podání placeba, protože tím by studie získala intervenční charakter.
Klinický význam
Je-li podáván i. v. paracetamol kriticky nemocnému pacientovi s kardiální limitací, je potřeba počítat cca u 40 % z nich s poklesem středního arteriálního tlaku, s maximem cca 20 minut po začátku infuze. U afebrilních pacientů je mechanismem zejména vazodilatace, zatímco u febrilních pacientů s již hyperkinetickou cirkulací je patrný negativně inotropní efekt, kdy je třeba počítat s poklesem srdečního výdeje cca o 10 %. U pacienta s hraničním srdečním výdejem může po podání paracetamolu dojít k orgánové hypoperfuzi. Pokud je nutná léčba paracetamolem navozené hypotenze, navrhujeme látky s betamimetickým, případně beta - i alfamimetickým působením (efedrin, metaraminol) spíše než noradrenalin.
Závěr
Intravenózní podávání paracetamolu ventilovaným kriticky nemocným pacientům s kardiální limitací vede u respondérů k hypotenzi, která vzniká kombinací periferní vazodilatace a poklesu srdečního výdeje. Pokles srdečního výdeje vzniká jak poklesem tepového objemu, tak tepové frekvence. U afebrilních pacientů je dominantní systémová vazodilatace, zatímco u febrilních převládá negativně inotropní efekt paracetamolu a k významnější vazodilataci již nedochází, přestože jsme po paracetamolu dokumentovali významné snížení gradientu mezi centrální a kožní teplotou.
Seznam zkratek:
BSA = povrch těla (body surface area)
FNKV = Fakultní nemocnice Královské Vinohrady
HR = tepová frekvence (heart rate)
MAP = střední arteriální tlak (mean arterial pressure)
PCCI = srdeční výdej přepočtený na m2 tělesného povrchu (pulse contour cardiac index)
SV = tepový objem (stroke volume)
SVRI = systémová vaskulární rezistence přepočtená na m2 tělesného povrchu (systemic vascular resistance index)
Došlo dne 23. 6. 2011.
Přijato dne 20. 9. 2011.
Adresa pro korespondenci:
MUDr. František Duška
AICU, Queens Medical Centre, Derby Road
NG7 2UH Nottingham, UK
e-mail: Frantisek.Duska@nuh.nhs.uk
Sources
1. Stricker, B. H. et al. Acute hypersensitivity reactions to paracetamol. Brit. Med. J. (Clinical Research Ed.), 1985, 145, p. 938–939.
2. Brown, G. Acetaminophen-induced hypotension. Heart & Lung, 1996, 25, p. 137–140.
3. Boyle, M. et al. Paracetamol administration is associated with hypotension in the critically ill. Australian Critical Care, 1997, 10, p. 120–122.
4. Mrozek, S. et al. Acetaminophene-induced hypotension in intensive care unit: a prospective study. Annales Françaises d’Anesthésie et de Réanimation, 2009, 28, p. 448–453.
5. Hersch, M. et al. Intravenous paracetamol (prodafalgan) causes hypotension in critically ill patiens. Critical Care, 2004, 8, p. 244.
6. de Maat, M. et al. Paracetamol for intravenous use in medium - and intensive care patients: pharmacokinetics and tolerance. Eur. J. Clin. Pharm., 2010, 42, p. 713–719.
7. Danguy, M. et al. Acetaminophen-induced hypotension after intravenous and oral administration. Annales Françaises d’Anesthésie et de Réanimation, 2010, 29, p. 313–314.
8. Allegaert, K. et al. Haemodynamics of intravenous paracetamol in neonates. Eur. J. Clin. Pharm., 2010, 42, p. 855–858.
9. Bendjelid, K. et al. Systemic arterial hypotension induced by paracetamol adminitration: nurse’s anecdotes or facts from intensive care unit? Annales Françaises d’Anesthésie et de Réanimation, 2000, 19, p. 499.
10. Uživatelská příručka PiCCO2 [online] 10-2008 [cit. 2011-05-31] Dostupné na WWW: <http://www.pulsion.com/fileadmin/ pulsion_share/Products_Flyer/PiCCO2_US_ALL/PiCCO2_Booklet_E_MPI851105_US_R01_091008_low.pdf>
11. Joly, H. R., Weil, M. H. Temperature of the great toe as an indication of the severity of shock. Circulation, 1969, 19, p. 131–138.
12. Ramsay, M. A. et al. Controlled sedation with alphaxalone-alphadolone. Brit. Med. J., 1974, 134, p. 656–659.
13. Boyle, M. et al. Paracetamol induced skin blood flow and blood pressure changes in febrile intensive care patients: An observational study. Australian Critical Care, 2010, 23, p. 208–214.
14. Johnson, J. M., Kellogg, D. L. jr. Thermoregulatory and thermal control in human cutaneous circulation. Frontiers in Bioscience, 2001, 6, p. 825–853.
15. Holowatz, L. A. et al. The human cutaneous circulation as a model of generalized microvascular function. Journal of Applied Physiology, 2008, 50, p. 370–372.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care Medicine
Article was published inAnaesthesiology and Intensive Care Medicine

2011 Issue 5-
All articles in this issue
- Ultrazvukem naváděný mediální cervikální blok
- Fibrinolýza v kardiochirurgii v postaprotinínovej ére
- Mechanismus vzniku hypotenze po i. v. paracetamolu u kriticky nemocných
- Je rozdiel v prežívaní pacientov s kraniocerebrálnym poranením s meraným a nemeraným intrakraniálnym tlakom?
- Vliv teploty na výsledky tromboelastografie – prospektivní studie
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Ultrazvukem naváděný mediální cervikální blok
- Je rozdiel v prežívaní pacientov s kraniocerebrálnym poranením s meraným a nemeraným intrakraniálnym tlakom?
- Mechanismus vzniku hypotenze po i. v. paracetamolu u kriticky nemocných
- Fibrinolýza v kardiochirurgii v postaprotinínovej ére
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career