-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
18FDG-PET/CT diagnostika adenokarcinomu pankreatu
18FDG-PET/CT diagnostics of pancreatic adenocarcinoma
Nowadays, high-resolution scanners are used for 18FDG-PET/CT examination, reaching adiagnostic accuracy of 90% to 95%, to diagnose pancreatic cancer. The advantage of the method is the whole-body examination range, which enables reliable detection of remote bodies of disease generalisation thanks to the high sensitivity of metabolic information. Therefore, 18FDG-PET/CT examination should be included in the pre-surgery consideration as it can lead to higher relative savings of funds despite its higher price, as well as improve post-surgery outcomesby excluding from radical treatment those patients whose disease is generalised at the time of the diagnose.
Key words:
pancreatic cancer – positron emission tomography and computed tomography
The author declares he has no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
27. 10. 2012Accepted:
5. 12. 2012
Autoři: P. Fencl
Působiště autorů: ONM-PET centrum, Nemocnice Na Homolce, Praha
Vyšlo v časopise: Gastroent Hepatol 2013; 67(1): 45-48
Kategorie: Gastrointestinální onkologie: přehledová práce
Souhrn
18FDG-PET/CT vyšetření se v současnosti provádí na scanerech s vysokým rozlišením, s diagnostickou spolehlivostí v průkazu karcinomu pankreatu mezi 90 a 95 %. Předností metody je celotělový charakter vyšetření, který díky citlivosti metabolické informace umožní zobrazit spolehlivě vzdálená ložiska generalizace choroby. 18FDG-PET/CT vyšetření by proto mělo být součástí předoperační rozvahy, kdy může i přes svou vyšší cenu vyprodukovat vyšší relativní úsporu vložených prostředků a zlepšit pooperační výsledky tím, že vyřadí z radikální léčby nemocné, u kterých je nemoc již v okamžiku diagnózy generalizovaná.
Klíčová slova:
karcinom pankreatu – 18FDG-PET/CT
18FDG-PET/CT diagnostika se v České republice provádí v pěti městech na osmi scanerech, v roce 2011 bylo provedeno přes 23 000 vyšetření. Převažující indikací jsou zhoubná onemocnění, přičemž tuto metodu nejvíce využívají kliničtí onkologové. To se zdá být logické, ale není tomu tak úplně. 18FDG-PET/CT diagnostika má své místo i na začátku vyšetřovacího algoritmu, když se hledá optimální léčebná strategie a nemocný je na klinickém lůžkovém oddělení nebo je vyšetřován ambulantně. V tomto stadiu jsou nemocní s karcinomem pankreatu vyšetřováni jen málo. Je tomu tak proto, že v okamžiku průkazu nemoci standardními vyšetřovacími postupy se zdá 18FDG-PET/CT diagnostika již jako nadbytečná, zdržující a příliš drahá. Toto paradigma má kořeny v minulosti, i když není z hlediska poskytovatelů zdravotní péče zcela racionální. Cílem článku je informovat o možnostech 18FDG-PET/CT diagnostiky v předoperační diagnostice adenokarcinomu pankreatu.
Diagnostika adenokarcinomu pankreatu pomocí 18FDG
Karcinom pankreatu patří spolu s ostatními zhoubnými novotvary gastrointestinálního traktu mezi glukózoavidní tumory, tedy nádory s vysokou konzumpcí glukózy i jejího analogu 18FDG (18F-2-fluoro-2-deoxy-D-glukózy). Po aplikaci 18FDG proto vzniká dostatečný kontrast mezi akumulací radiofarmaka v tumoru a na pozadí umožňující takové ložisko hypermetabolizmu glukózy detekovat. Diagnostické obtíže při průkazu adenokarcinom pankreatu však zpočátku působila horší rozlišovací schopnost starších typů PET scanerů a nedostatek anatomické informace. Dnes, když už je možné registrovat PET data ve vysokém rozlišení, zhoršuje kvalitu zobrazení u obézních pacientů anatomická poloha žlázy hluboko v retroperitoneu a subcentimetrová ložiska v iniciálních stadiích choroby, která mají z kurativního hlediska největší význam, tak nemusí být vždy zachycena.
Přes zvyšující se citlivost PET kamer zůstávala spolehlivost diagnostiky dlouho suboptimální, protože absence anatomických informací v PET obraze neumožnila zobrazená ložiska hypermetabolizmu glukózy spolehlivě lokalizovat do pankreatu. První zlepšení přinesla off-line fúze PET obrazu s CT daty. Off-line fúze označuje proces, při kterém se softwarově sloučí dvě na sobě časově i místně nezávisle zhotovená vyšetření. Citlivost v průkazu karcinomu pankreatu se zvýšila, jak referovali Lemke et al [1], na 89,9 % při off-line fúzi obou obrazů, zatímco izolované hodnocení CT vykázalo citlivost 76,6 % a PET vyšetření 84,4 %.
Zásadní pokrok v diagnostické spolehlivosti přinesla hybridní PET/CT zařízení, která umožňují v jednom přístroji v průběhu jednoho vyšetření registrovat CT i PET data. K vysokému rozlišení obrazu přispěla instalace modernějších PET detektorů, které v praxi detekují nádorová ložiska od 0,5 cm, a montáž víceřadých CT scanerů, které registrují dostatek dat pro izotropické zobrazení tkání. Casneuf et al [2] prokázali na moderních hybridních scanerech diagnostickou správnost průkazu karcinomu pankreatu 82,3 % při hodnocení PET vyšetření, 88,2 % při hodnocení CT vyšetření, zatímco hodnocení hybridního PET/CT obrazu přineslo spolehlivost 91,2 %. Při průkazu lokoregionální recidivy byla diagnostická správnost 91,6 % a převýšila obě samostatné komponenty. Obdobné výsledky byly zaznamenány nezávisle na sobě na více pracovištích [3–5]. Kysučan et al [6] z olomouckého pracoviště publikovali soubor 81 operovaných nemocných; v souboru byla v průkazu přítomnosti nádoru v pankreatu dosažena citlivost 92,2 % a přesnost 90,5 %. Vysoká spolehlivost byla potvrzena i v průkazu vzdálených metastáz s citlivostí 82,8 % a přesností 97,8 %, oproti tomu byl průkaz uzlinového postižení málo efektivní s citlivostí a správností málo přesahujících 50 %. Výsledky vyšetření však vedly v 15,6 % k upuštění od radikálního chirurgického řešení se všemi zdravotními i ekonomickými důsledky.
Více prací shodně konstatovalo, že diagnostickou spolehlivost metody zvýší použití nitrožilní jodové kontrastní látky pro CT část vyšetření. Buchs et al [7] například nalezli spolehlivost průkazu karcinomu pankreatu u PET/CT s podáním jodové kontrastní látky 90,3 %, zatímco bez této aplikace klesla na 64 %; obdobný rozdíl nalezli Kitajima et al [8] při průkazu recidivy karcinomu pankreatu po kurativní léčbě, spolehlivost CT diagnostiky po podání kontrastní látky nitrožilně byla 75,6 %, 18FDG-PET/CT vyšetření bez podání kontrastní látky vykazovala diagnostickou spolehlivost 86,7 %, po podání kontrastní látky se spolehlivost zvýšila na 93,3 %.
Diagnostická spolehlivost 18FDG vyšetření karcinomu pankreatu dle Evidence Based Medicine (EBM)
Již v roce 2000 se touto otázkou zabývala konference pod vedením Reskeho [9]. Pro potřeby odlišení zánětu pankreatu od karcinomu pankreatu byla míra evidence 18FDG vyšetření stanovena na stupni 1a (tj. klinické využití je prokázané) za předpokladu, že je hladina CRP u nemocného v normálních hodnotách; konsenzuální rozhodnutí bylo podloženo studií na 304 nemocných [10], ve které byl nalezen statisticky významný rozdíl (p = 0,01) v diagnostické spolehlivosti mezi nemocnými se zvýšenou a nezvýšenou hladinou CRP. Pro PET průkaz recidivy karcinomu pankreatu po kurativní léčbě byla stanovena míra evidence na stupni 1b EBM kritérií (tj. klinické užití je pravděpodobné).
Za EBM měřítko diagnostické správnosti lze počítat i ochotu plátců léčebné péče hradit ten který konkrétní diagnostický výkon z prostředků, které plátce spravuje [11]. Názorným příkladem je úhrada 18FDG PET výkonů z prostředků Medicare v USA: zatímco v roce 1998 byla hrazena jen diagnostika solitárních plicních nodulů, od roku 2003 byla úhrada rozšířena mimo jiné indikace i na diagnostiku karcinomu pankreatu za předpokladu, že je pracoviště vybaveno PET kamerou s definovanými minimálními technickými i softwarovými parametry. Stejným rozhodnutím byla zrušena úhrada výkonů zhotovených na koincidenčních kamerách [12]. Tento konsenzus byl podložen analýzou nashromážděných poznatků o diagnostické spolehlivosti metody [13–16].
Porovnání 18FDG-PET/CT diagnostiky adenokarcinomu pankreatu s ostatními diagnostickými možnostmi
Porovnání 18FDG-PET/CT vyšetření vůči 18FDG-PET diagnostice a endoskopické ultrasonografii (EUS) provedl například Tang et al [17] v metaanalýze zahrnující 51 originálních publikací referujících o 3 857 nemocných. 18FDG-PET/CT vyšetření se ukázalo jako vysoce citlivá metoda (90,1 %), převyšující 18FDG-PET (88,4 %) i EUS (81,2 %), zatímco přesnost byla v opačném pořadí, 93,2 % pro EUS, 83,1 % pro 18FDG-PET a 80,1 % pro 18FDG-PET/CT. Spolehlivost 18FDG-PET/CT vyšetření převýšila EUS při rozlišení chronické pankreatitidy a karcinomu pankreatu. Schick et al [18] nalezli srovnatelnou spolehlivost pro všechny použité metody, tedy 18FDG-PET/CT, EUS a ERCP s tím, že nálezy 18FDG-PET/CT přinesly dodatečné informace zprostředkované celotělovým charakterem vyšetření.
Velký zájem byl věnován porovnání 18FDG-PET/CT diagnostice a zobrazení karcinomu pankreatu pomocí magnetické rezonance (MRI). V práci Kauhanena et al [19] byla nalezena vyšší citlivost hybridního zobrazení 18FDG-PET/CT oproti konvenčním metodám CT a MRI. Obdobný výsledek nalezla metaanlýza Wu et al [20] porovnávající difuzně vážené časy MRI (DWI) [21] a 18FDG-PET/CT. Analýza zahrnula 16 studií s 804 nemocnými a ukázala, že 18FDG-PET/CT je v průkazu karcinomu pankreatu citlivější metodou než DWI (0,87 oproti 0,85), zatímco DWI vykazovala vyšší správnost (0,91 oproti 0,83). Práce Tanimoto et al [22] analyzovala spolehlivost 18FDG-PET/CT diagnostiky a informaci o nádorové celularitě zprostředkované MRI zobrazením tkáně tumoru. V průkazu karcinomu pankreatu nalezl shodnou spolehlivost tří metod: stanovení absolutní výšky akumulace 18FDG v tkáni tumoru pomocí SUV (Standardized Upake Value), stanovení relativní hodnoty SUV v porovnání s referenční tkání a zobrazení ADC (Apperent Diffuse Coeficient) [21] na MRI; a to ve výši 0,855, 0,875 a 0,83, respektive. Tyto tři postupy převýšily MRI zobrazení T2W časem i pomocí protonové hustoty (proton denzity).
Poměr cena-efekt 18FDG-PET/CT diagnostiky karcinomu pankreatu
18FDG-PET/CT diagnostika patří mezi drahé diagnostické výkony, a to jak pro cenu hybridního přístroje, tak pro vysoké provozní náklady spojené s nákupem radiofarmaka. Předmětem zájmu je proto nejen diagnostická efektivita metody, ale i její efektivita ekonomická [23]. Mírně zvýšená diagnostická spolehlivost v průkazu karcinomu pankreatu v porovnání se standardními diagnostickými postupy vysoký rozdíl v ceně jistě nevyváží. Předností metody je ale celotělový charakter 18FDG-PET/CT vyšetření, který spolu s vysokou citlivostí metabolické informace dokáže zobrazit vzdálená ložiska generalizace choroby. Strobel et al [4] nalezl mezi 50 nemocnými indikovanými k operaci 27 (54 %) osob s pokročilou chorobou vylučující radikální výkon, 18FDG-PET/CT určila toto stadium s 96% citlivostí a 88% správností. V práci Barber et al [24] změnila informace 18FDG-PET/CT diagnostiky léčebnou strategii v 41 %, když prokázala generalizaci choroby, a éčba byla změněna z kurativní na paliativní. Podrobný ekonomický rozbor provedli Heinrich et al [25]. V jejich práci bylo pět z 59 nemocných (8,4 %) na základě 18FDG-PET/CT průkazu generalizace choroby vyloučeno z plánované resekce pankreatu. Při nákladech na resekci pankreatu u těchto pěti nemocných 188 500 $ (USD) a ceně 59 vyšetření 18FDG-PET/CT ve výši 125 588 $ (včetně biopsie pod CT kontrolou) nemuselo být vydáno $ 62 912, což představuje úsporu 1 066 $ na jednoho neoperovaného nemocného. Při vyšším počtu neoperovaných nemocných, jak referují ostatní autoři [4,6,18], by byla i relativní úspora vyšší. Studie sice zcela neodráží poměry v našem zdravotnictví, ale dokládá, že informace z 18FDG-PET/CT diagnostiky má ekonomicky nejvyšší přínos na počátku léčebné rozvahy před tím, než se zahájí nákladná radikální léčba se všemi zdravotními i ekonomickými náklady a riziky (obr. 1). Stejně vysokou diagnostickou spolehlivost má 18FDG-PET/CT diagnostika i v průkazu recidivy choroby po radikálním výkonu; v této indikaci se ovšem při pozitivním průkazu recidivy nedá ekonomický či zdravotní prospěch očekávat, úsporu by ale mohlo přinést upuštění od paliativní chemoterapie na základě progrese 18FDG-PET/CT nálezu.
Obr. 1. Axiální projekce hlavy pankreatu na CT vyšetření po podání kontrastní látky nitrožilně (vlevo), fúze téhož obrazu s <sup>18</sup>FDG-PET vyšetřením (vpravo). Karcinom hlavy pankreatu o průměru více než 2 cm, drobná metastáza v 6. segmentu pravého laloku jater. Rozsah choroby nelze na CT spolehlivě rozlišit. Fig. 1. Axial projection of head of pancreas on CT scan after IV administration of contrast agent (left), fusion of the same image with <sup>18</sup>FDG-PET scan (right). Carcinoma of head of pancreas with the diameter of over 2 cm, small metastasis in the sixth segment of the right hepatic lobe. The extent of the disease cannot be reliably distinguished on CT scan. 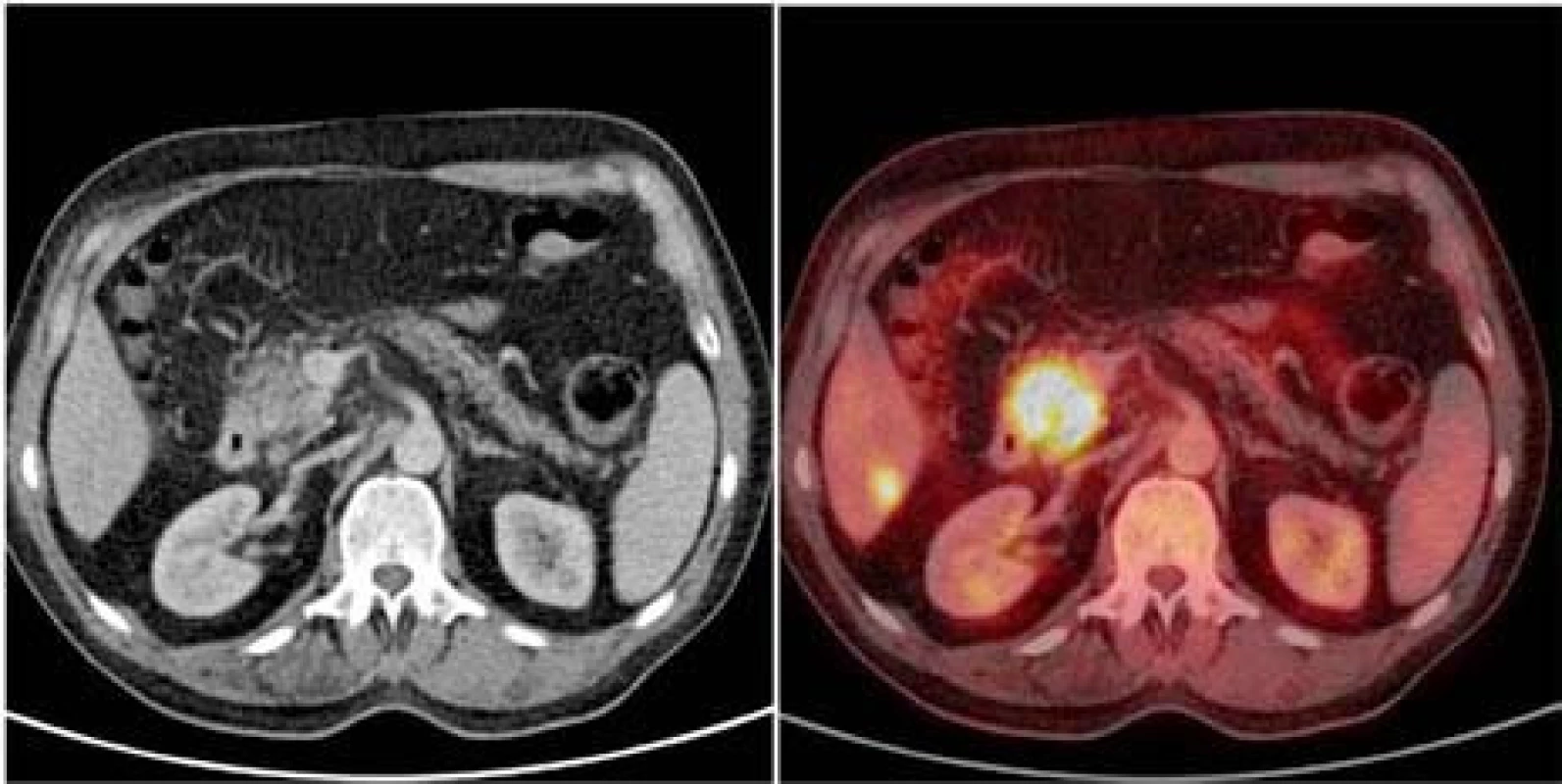
Závěr
V roce 2008 definovali Delbeke a Martin [26] pro chirurgickou obec indikační kritéria pro užití 18FDG-PET diagnostiky v průkazu adenokarcinomu pankreatu a v předoperačním stanovení rozsahu choroby (staging). Doporučení bylo opřeno o zkušenosti nashromážděné do roku 2006, tedy v době, kdy byla vyšetření prováděna převážně na PET přístrojích s horším prostorovým rozlišením. Delbeke a Martin konstatovali, že je 18FDG diagnostika přínosná v případě, když je CT vyšetření nediagnostické, nebo je výsledek biopsie nejednoznačný; když je třeba odlišit chronickou pankreatitidu, nebo je třeba určit povahu cystické léze v žláze. V předoperačním stagingu [27] upozornili, že 18FDG diagnostika nedosahuje spolehlivost srovnatelnou se standardními diagnostickými postupy v určení cT stadia ani v určení cN stadia, ale vysoce převyšuje ostatní metody v určení cM stadia.
V současnosti se diagnostika provádí převážně na 18FDG-PET/CT scanerech s vysokým rozlišením a spolehlivost diagnostiky se zvýšila; přesto však není třeba na závěrech publikovaných v roce 2008 nic měnit, jenom jsme schopni informace o přítomnosti či nepřítomnosti karcinomu pankreatu a o rozsahu choroby získat s vyšší věrohodností. 18FDG-PET/CT vyšetření je u nás dostupné, a mělo by se proto racionálně využívat. V diagnostice karcinomu pankreatu to znamená indikovat tuto modalitu v předoperačním stagingu, kdy může vyšetření i přes svou cenu vyprodukovat vyšší relativní úsporu vložených prostředků a zlepšit pooperační výsledky tím, že vyřadí z éčby nemocné, u kterých je nemoc již v okamžiku diagnózy generalizovaná.
Autor deklaruje, že v souvislosti s předmětem studie nemá žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 27. 10. 2012
Přijato: 5. 12. 2012
MUDr. Pavel Fencl, CSc.
ONM-PET centrum
Nemocnice Na Homolce
Roentgenova 2, 150 30 Praha 5
pavel.fencl@homolka.cz
Zdroje
1. Lemke AJ, Niehues SM, Hosten N et al. Retrospective digital image fusion of multidetector CT and 18F-FDG PET: clinical value in pancreatic lesions – a prospective study with 104 patients. J Nucl Med 2004; 45(8): 1279–1286.
2. Casneuf V, Delrue L, Kelles A et al. Is combined 18F-fluorodeoxyglucose-positron emission tomography/computed tomography superior to positron emission tomography or computed tomography alone for diagnosis, staging and restaging of pancreatic lesions? Acta Gastroenterol Belg 2007; 70(4): 331–338.
3. Buchs NC, Bühler L, Bucher P et al. Value of contrast-enhanced 18F-fluorodeoxyglucose positron emission tomography/computed tomography in detection and presurgical assessment of pancreatic cancer: a prospective study. J Gastroenterol Hepatol 2011; 26(4): 657–662.
4. Strobel K, Heinrich S, Bhure U et al. Contrast-enhanced 18F-FDG PET/CT: 1-stop-shop imaging for assessing the resectability of pancreatic cancer. J Nucl Med 2008; 49(9): 1408–1413.
5. Sahani DV, Shah ZK, Catalano OA et al. Radiology of pancreatic adenocarcinoma: Current status of paging. J Gastroenterol Hepatol 2008; 23(1): 23–33.
6. Kysučan J, Loveček M, Klos D et al. Přínos PET/CT k předoperačnímu staging karciniomu pankreatu. Rozhl Chir 2010; 89(7): 433–440.
7. Buchs NC, Bühler L, Bucher P et al. Value of contrast-enhanced 18F-fluorodeoxyglucose positron emission tomography/computed tomography in detection and presurgical assessment of pancreatic cancer: a prospective study. J Gastroenterol Hepatol 2011; 26(4): 657–662.
8. Kitajima K, Murakami K, Yamasaki E et al. Performance of integrated FDG-PET//contrast-enhanced CT in the diagnosis of recurrent pancreatic cancer: comparison with integrated FDG-PET/non-contrast--enhanced CT and enhanced CT. Mol Imaging Biol 2010; 12(4): 452–459.
9. Reske SN, Kotzerke J. FDG-PET for clinical use. Results of the 3rd German Interdisciplinary Consensus Conference, “Onko-PET III”, 21 July and 19 September 2000. Eur J Nucl Med 2001; 28(11): 1707–1723.
10. Diederichs CG, Staib L, Glasbrenner B et al. F-18 Fluorodeoxyglucose (FDG) and C-Reactive Protein (CRP). Clin Positron Imaging 1999; 2(3): 131–136.
11. Johnson GC. Assessment and approval of medical devices used in diagnostic imaging in the United States. Isr J Med Sci 1986; 22(7–8): 505–518.
12. Bietendorf J. FDG PET reimbursement. J Nucl Med Technol 2004; 32(1): 33–38.
13. Berberat P, Friess H, Kashiwagi M et al. Diagnosis and staging of pancreatic cancer by positron emission tomography. World J Surg 1999; 23(9): 882–887.
14. Zimny M, Bares R, Fass J et al. Fluorine-18 fluorodeoxyglucose positron emission tomography in the differential diagnosis pf pancreatic carcinoma: a report of 106 cases. Eur J Nucl Med 1997; 24(6): 678–682.
15. Delbeke D, Rose DM, Chapman WC et al. Optimal interpretation of FDG PET in the diagnosis, staging and mangement of pancreatic carcinoma. J Nucl Med 1999; 40(11): 1784–1791.
16. Zimny M, Schlumpelick V. Fluordeoxyglucose positron emission tomography (FDG-PET) in the differential diagnosis of pancreatic lesions. Chirurg 2001; 72(9): 989–994.
17. Tang S, Huang G, Liu J et al. Usefulness of 18F-FDG PET, combined FDG-PET/CT and EUS in diagnosing primary pancreatic carcinoma: A meta-analysis. Eur J Radiol 2011; 78(1): 142–150.
18. Schick V, Franzius C, Beyna T et al. Diagnostic impact of 18F-FDG PET-CT evaluating solid pancreatic lesions versusendosonography, endoscopic retrograde cholangio-pancreatography with intraductalultrasonography and abdominal ultrasound. Eur J Nucl Med Mol Imaging 2008; 35(10): 1775–1785.
19. Kauhanen SP, Komar G, Seppänen MP et al. A Prospective Diagnostic Accuracy Study of 18F-Fluorodeoxyglucose Positron Emission Tomography/Computed Tomography, Multidetector Row Computed Tomography, and Magnetic Resonance Imaging in Primary Diagnosis and Staging of Pancreatic Cancer. Ann Surg 2009; 250(6): 957–963.
20. Wu LM, Hu JN, Hua J et al. Diagnostic value of diffusion-weighted magnetic resonance imaging (DWI) compared to FDG PET/CT for pancreatic malignancy: a meta-analysis using a hierarchical regression model. J Gastroenterol Hepatol 2012; 27(6): 1027–1035.
21. http://en.wikipedia.org/wiki/Diffusion_MRI.
22. Tanimoto K, Yoshikawa K, Obata T et al. Role of glucose metabolism and cellularity for tumor malignancy evaluation using FDG-PET/CT and MRI. Nucl Med Commun 2010; 31(6): 604–609.
23. Buck AK, Herrmann K, Stargardt T et al. Economic evaluation of PET and PET/CT in oncology: evidence and methodologic approaches. J Nucl Med Technol 2010; 38(1): 6–17.
24. Barber TW, Kalff V, Cherk MH et al. 18F-FDG PET/CT influences management in patients with known or suspected pancreatic cancer. Intern Med J 2011; 41(11): 776–783.
25. Heinrich S, Goerres GW, Schäfer M et al. Positron Emission Tomography/Computed Tomography Influences on the Management of Resectable Pancreatic Cancer and Its Cost-Effectiveness. Ann Surg 2005; 242(2): 235–243.
26. Delbeke D, Martin WH. PET and PET/CT for pancreatic malignancies. Surg Oncol Clin N Am 2010; 19(2): 235–254.
27. Sobin LH, Gospadorowicz MK, Wittekind C. TNM classification of malignant tumours. Chichester: John Wiley & Sons 2009.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2013 Číslo 1- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Sérové protilátky proti zymogenovému glykoproteinu 2 (anti-GP2) u nemocných s idiopatickými střevními záněty
- Recidivující subileózní stavy na tenkém střevě mohou skýtat překvapení
- Hodnocení slizničního hojení v průběhu biologické léčby Crohnovy choroby tenkého střeva pomocí kapslové endoskopie: prospektivní observační studie
- Mesalazin u Crohnovy nemoci: obsolentní nebo neprávem opomíjená léčba?
- Současný pohled na léčbu perianálních píštělí u nemocných s Crohnovou chorobou
- Akutní krvácení do GIT a změny v lipidovém spektru – pilotní projekt
- Perforující gangrenózní cholecystitida
- Dysfunkce horní části trávicího traktu u kriticky nemocných: současný pohled a perspektiva
- 18FDG-PET/CT diagnostika adenokarcinomu pankreatu
- Stenty v liečbe zhubných nádorov kolorekta – prehľad a vlastné skúsenosti
- Metastáza maligního melanomu v bulbu duodena jako vzácná příčina obstrukce výtokového traktu žaludku
- Segmentálna portálna hypertenzia
- Plány a představy redakční rady na rok 2013
-
Imunosupresivní a biologická léčba u CN „šitá na míru“.
Komentář ke studii STORI - Aminosalicyláty v liečbe aktívnej Crohnovej choroby – kedy a prečo nie
- Komentář: Perforující gangrenózní cholecystitida
- UEGW Amsterdam 2012 – pohled z jiné strany
- Gastrofórum – Pankreatofórum v januári 2013
- Správná odpověď na kvíz
- Leading change in IBD
- Pangrol 20000
- Za vším hledej peníze (... a nebo ženu)
- Autodidaktický test: idiopatické střevní záněty
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Segmentálna portálna hypertenzia
- Současný pohled na léčbu perianálních píštělí u nemocných s Crohnovou chorobou
- Perforující gangrenózní cholecystitida
- Recidivující subileózní stavy na tenkém střevě mohou skýtat překvapení
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



