-
Medical journals
- Career
Chronická pánevní bolest (CPPS): anatomické parametry, patofyziologické mechanizmy, nejednoznačné onemocnění, fenomén chronického onemocnění. Syndrom bolestivého močového měchýře
Authors: J. J. Wyndale
Authors‘ workplace: University Antwerp and Antwerp University Hospital ; Professor of Urology
Published in: Urol List 2010; 8(3): 6-12
Overview
Díky mezinárodní spolupráci a vzniku nových výzkumných skupin v Evropě i USA došlo k významnému pokroku v porozumění i léčbě urologických bolestivých stavů. Bylo prokázáno, že chronickou pánevní bolest je třeba posuzovat jako obecnější stav, jenž může mít důsledky v lokální, centrální i obecné rovině. Toto onemocnění má s největší pravděpodobností řadu různých klinických manifestací a obvykle se vyskytuje ve spojitosti s dalšími chorobami. Dopad chronické pánevní bolesti na kvalitu života pacienta není nezanedbatelný. Pro syndrom chronické bolesti v oblasti močového měchýře je charakteristická určitá konstelace různých symptomů. Při diagnostice se využívají nejrůznější klinická a technická vyšetření, pro diferenciaci onemocnění je nutné provedení cystoskopie a biopsie. Před stanovením definitivní diagnózy je nutné vyloučit přítomnost ostatních nejednoznačných onemocnění. Léčba zahrnuje behaviorální terapie, medikamentózní i intravezikální léčbu. V některých případech může být indikována i operační léčba. Ta však v každém případě vyžaduje rovněž psychickou podporu pacienta. Výsledek terapie je často nejistý, v mnoha případech je ale možné dosáhnout zmírnění symptomů.
Klíčová slova:
močový měchýř, pánevní bolest, syndrom bolestivého močového měchýře, intersticiální cystitidaÚVOD
ICS ve své poslední zprávě týkající se terminologie z roku 2002 [1] uvádí logické a pochopitelné definice.
„Bolest, dyskomfort i pocit tlaku představují abnormální vjemy. Nejvíce pacienta ovlivňuje pocit bolesti, který může být spojen s plněním a vyprazdňováním močového měchýře, může se vyskytovat po močení nebo může být přítomen neustále. Bolest lze klasifikovat na základě typu, frekvence, trvání, vyvolávajících faktorů vedoucích k úlevě bolesti a lokalizace. Pacienti obvykle pociťují bolest v močovém měchýři v suprapubické nebo retropubické oblasti a její intenzita se obvykle stupňuje v plnicí fázi. Bolest může přetrvávat i po močení. Do této skupiny spadá rovněž bolest v oblasti močové trubice, vulvy, vaginy, skrota a perinea.
Syndromy bolesti v oblasti močopohlavního ústrojí zahrnují ustálenou konstelaci symptomů a jejich různé kombinace, nelze je však užít pro stanovení přesné diagnózy. O syndrom se jedná pouze v případě, že je přítomen přinejmenším jeden další symptom k popisu syndromu. Termínem bolestivé syndromy se nejčastěji označují funkční abnormality, u nichž neznáme přesnou příčinu vzniku, v případě, kdy běžná vyšetření vyloučila přítomnost zjevných lokálních patologií, jako jsou například infekce, tumor, metabolické nebo hormonální příčiny. Je zřejmé, že spolu s rozšiřujícími se znalostmi a vědomostmi se z řady „syndromů“ stanou „onemocnění“.
Vnitřní orgány dutiny břišní jsou poměrně necitlivé na mechanické podněty. Silná distenze a spasmodické kontrakce však mohou vyvolat bolest, zejména pokud jsou spojeny s ischemií. Bolest může být rovněž vyvolána přímým traumatem v důsledku incize, koagulace nebo silné elektrické stimulace. Další příčinou bolesti může být penetrace cizorodého materiálu do stěny močového měchýře, infekce, zánět nebo přímé podráždění aferentních nervů (např. prorůstajícím tumorem). Z výše uvedených informací je zřejmé, že problematika pánevní bolesti je poměrně komplikovaná.
Jak správně uvádějí EAU Guidelines pro léčbu chronické pánevní bolesti, problematiku znesnadňuje neschopnost stanovit přesnou patofyziologickou příčinu jednotlivých typů bolesti. Tento typ bolesti bývá obvykle označován termíny „intersticiální cystitida“ (IC) nebo „chronická prostatitida“ (CP). Obě označení jsou klinickým výkladem symptomů, jež uvádí sám pacient. Podvědomě považujeme (vzhledem k symptomům) za hlavní příčinu bolesti zánět. Jestliže máme důvěru v odhalení skutečného důkazu pro příčinu onemocnění, zdá se užití přípony „titida“ logické.
Díky mezinárodní spolupráci a vzniku výzkumných skupin v Evropě, USA i Asii došlo k významnému pokroku v porozumění i léčbě urologických bolestivých stavů. Tento článek odráží výsledky práce těchto skupin.
ANATOMICKÉ PARAMETRY
V pánevní oblasti jsou umístěny vnitřní orgány dutiny břišní, pánev dále zahrnuje svalovinu (hladkou i příčně pruhovanou), fascie, nervy, žíly, arterie a lymfatické struktury, které zajišťují významné funkce, jako jsou mikce, kontinence, defekace, rozmnožování a sex. Tyto struktury zajišťují podpůrnou roli při pohybu, zažívání, dýchání a dalších činnostech.
Všechny tyto orgány jsou díky svému stejnému embryologickému původu, blízkosti uložení a společnému nervovému zásobení a svalovině vzájemně propojeny. Jejich senzorické funkce spolu vzájemně souvisí a působí na psychosociální faktory. Vzhledem k tomu, že patologie a symptomy přítomné v jednom orgánu mohou ovlivňovat i ostatní orgány, je stále obtížnější je vnímat odděleně.
Je zřejmé, že na CPPS se mohou podílet všechny nervy v pánevní oblasti. Senzorický signál je přenášen míchou přes nervové synapse až do senzorické části mozkové kůry. Na tyto nervové dráhy mohou mít vliv další okolní struktury, jako například jádro ve střední čáře a ventrobazální komplex v talamu.
PATOFYZIOLOGICKÉ MECHANIZMY
Řada mechanizmů podílejících se na vzniku CPPS je snadno pochopitelná [3]. Vznik bolesti v důsledku stimulace nociceptivních nervů při zánětu, infekci, traumatu, nadměrném naplnění močového měchýře nebo v důsledku přítomnosti tumoru je jednoznačně přijímán.
Problém však vyvstává u stavů, kdy není žádná z výše uvedených příčin odhalena. U bolestivých „idiopatických“ stavů je nutné zvolit odlišný přístup. Doposud rovněž nebylo prokázáno, zda lze změnu mastocytů nebo dysfunkci GAG vrstvy považovat za příčinu nebo spíše za důsledek patologie obecnějšího rázu. Významný pokrok v porozumění funkci močového měchýře přispěl k objasnění skutečných faktorů. V současné době probíhá výzkum látek, jako jsou ATP, NO, P2X3, VPN, jež umožní vyvinout nové léčebné modality. Další rozvíjející se oblastí je výzkum purinergních signálních drah. U pacientů s PBS prokazují psychofyzikální důkazy hypersenzitivitu na tlak a ischemii a bylo prokázáno narušení centrálního zpracování senzorických vjemů z močového měchýře.
Na základě psychologických testů (např. „stress life model“) bylo zjištěno, že psychologické faktory hrají u pacientů s PBS významnější roli než u pacientů v kontrolní skupině. U těchto pacientů byla zjištěna významnější souvislost mezi stresem a symptomy PBS, jež se dále prohlubuje spolu se závažností onemocnění. PBS bývá spojována s úzkostí a depresí, kdy za potenciální mediátor bývá považován faktor uvolňující kortikotropin.
U pacientů s PBS byla dále studována změna hladiny kortizolu během dne. Výsledky prokázaly spojitost mezi ranní hladinou kortizolu a komorbidními stavy zapříčiněnými hypotalamo-hypofyzární-adrenální osou, jako jsou například fibromyalgie, chronická únava a revmatoidní artritida.
Další výzvu představuje neuroplasticita vznikající v důsledku zvýšené tvorby neurotrofických faktorů v močovém měchýři.
Významnou roli v této problematice hraje rovněž svalovina pánevního dna. Hypertonicita a nedostatečná relaxace pánevního dna byly prokázány již před desítkami let. Mezitím došlo k významnému pokroku v oblasti našich znalostí funkce svaloviny pánevního dna, což nám otvírá celou řadu možností pro léčbu. Je nutné si uvědomit aspekty charakterizující viscerální bolest: špatná lokalizace, zvýšený tonus kosterní svaloviny spolu s emocionální a autonomní reakcí projektující se na kožní povrch, což má za následek zvýšenou citlivost kůže a pravděpodobně také trofické změny stěny tělní.
NEJEDNOZNAČNÁ ONEMOCNĚNÍ
Bolest v pánevní oblasti může vznikat v celé řadě různých orgánů a může mít celou řadu příčin. PBS a další bolestivé syndromy urologického systému lze diagnostikovat pouze na základě vyloučení přítomnosti ostatních onemocnění. ESSIC vytvořila návod pro postup při diagnostice onemocnění (www.essicoffice.org) (tab. 1) [4,5].
Table 1. Aktualizovaný seznam relevantních nejednoznačných onemocnění a postup pro jejich vyloučení nebo diagnostikování [1]. ![Aktualizovaný seznam relevantních nejednoznačných onemocnění a postup pro jejich vyloučení nebo diagnostikování [1].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/a64f7d7a112f08444ddac14a79360ba9.png)
Z tohoto návodu jednoznačně vyplývá, že nás na stopu může přivést již odebrání klinické anamnézy, provedení klinického vyšetření a laboratorních testů. V případě podezření na přítomnost patologického stavu nám může ke stanovení konečné diagnózy pomoci technické vyšetření.
FENOMÉN CHRONICKÉ BOLESTI
Chronickou bolest nelze považovat za pouhé pokračování akutní bolesti. Chronická bolest vyvolává změny, které mají dopad jak na diagnostiku, tak na léčbu bolesti. Vzhledem k tomu, že bolestivé stimuly přetrvávající celé roky mohou vyvolat celou řadu nejrůznějších změn v senzorických signálních drahách a mozkovém zpracování, mohou ovlivňovat kvalitu života, emocionální stav a vést ke změnám v ostatních orgánech a strukturách, je jasné, že diagnostika v tomto případě často probíhá na principu pokus – omyl, a léčba by tedy neměla být příliš cílená na jedinou strukturu. Údaje z dalších studií nám jistě pomohou při hledání nejvhodnějšího postupu.
SYNDROM BOLESTIVÉHO MOČOVÉHO MĚCHÝŘE/IC (TERMINOLOGIE NAVRŽENÁ ESSIC)
BPS/IC představuje extrémně bolestivý a stresující stav diagnostikovaný na základě chronické pánevní bolesti, pocitu tlaku nebo dyskomfortu v oblasti močového měchýře a doprovázený alespoň jedním dalším močovým symptomem, jako je například přetrvávající urgence nebo močová frekvence [5].
Frekvence močení je v tomto případě výrazně zvýšená, není však přítomna inkontinence. Symptomy přetrvávají i během noci, a narušují tak spánek pacienta. Onemocnění narušuje všechny stránky normálního života pacienta: 60 % pacientů se v důsledku svých symptomů vyhýbá pohlavnímu životu, onemocnění dokonce zdvojnásobuje míru výskytu sebevražd.
Pro vysvětlení vzniku BPS byla dosud navrhována celá řada mechanizmů, přesná etiologie však doposud nebyla odhalena.
Důkazy nasvědčují tomu, že zasažení neurobiologických faktorů narušuje inervaci močového měchýře. Ve tkáni močového měchýře u pacientů trpících BPS byla ve srovnání s kontrolní skupinou prokázána zvýšená hladina tyrosin hydroxylázy (enzym omezující rychlost syntézy katecholaminu). Nejvýznamnější zvýšení bylo pozorováno u pacientů s klasickou formou onemocnění [6]. Tyto změny odpovídají zvýšené stimulaci sympatiku. Dále se předpokládá, že na patogenezi BPS se může podílet narušená propustnost epiteliální bariéry tvořené vrstvou GAG (glykosaminoglykanů). Submukózní vrstva (včetně intramurálních nervových vláken) je tak vystavena škodlivým látkám obsaženým v moči [7].
Pro klasický BPS je charakteristická zánětlivá složka přenášená mastocyty, která by mohla vysvětlovat řadu ze symptomů tohoto onemocnění [8].
Předpokládá se, že změna v metabolizmu oxidu dusnatého (NO) souvisí s imunologickou reakcí u BPS. Orální aplikace L-argininu (substrát pro vznik NO) zvyšuje u pacientů s BPS koncentraci enzymů souvisejících s NO a metabolitů v moči a zmírňuje symptomy onemocnění.
Důkazy nasvědčující tomu, že etiologie BPS zahrnuje složitou neuroimunoendokrinní dráhu, pocházejí ze studií, které prokázaly, že aktivita mastocytů lokalizovaných v blízkosti nervových zakončení je ovlivněna estradiolem a faktorem uvolňujícím kortikotropin a že aktivitu mastocytů ovlivňují tři různé neutrofické faktory. Navzdory stále se zvyšujícímu množství důkazů, které nasvědčují multifaktoriální příčině BPS, je nutné teprve stanovit konkrétní detaily [9]. Ať už je však mechanizmus jakýkoli, je jisté, že u pacientů s BPS dochází k závažnému narušení senzorické inervace močového měchýře.
Intersticiální cystitida je heterogenní onemocnění, které se obvykle dělí do dvou kategorií – klasická a neulcerózní (non-Hunnerovy) léze [4]. Oba dva typy se vyznačují téměř identickými symptomy, liší se však několika významnými aspekty. Hlavní rozdíl spočívá ve skutečnosti, že u neulcerózního onemocnění se známky zánětu vyskytují pouze velmi vzácně. Tento typ onemocnění pravděpodobně souvisí s dalšími autonomními dysfunkcemi, jako je například syndrom dráždivého střeva a dalšími stavy jako např. Sjögren. Neurobiologická studie (zkoumající marker axonu S-100) srovnávající vzorky biopsie odebrané u pacientů s klasickou a neulcerózní IC a kontrolních subjektů zjistila rozdíly v hladině proteinu S-100. U pacientů s neulcerózní IC byla pozorována nižší hladina tohoto proteinu, což by nasvědčovalo potenciální neurogenní etiologii u tohoto podtypu IC.
DIAGNOSTIKA
Hlavní cíl spočívá v získání co největšího množství přesných informací, a to takovým způsobem, který bude přijatelný pro pacienta. Doporučuje se užívání různých diagnostických technik, jako jsou například endoskopické vyšetření, test propustnosti sliznice močového měchýře a urodynamické vyšetření [10].
ESSIC vytvořila standardizované schéma umožňující diferenciaci mezi jednotlivými typy BPS [5] a doporučení pro detekci nejednoznačného onemocnění.
ESSIC uvádí, že pro diagnostikování BPS je nutné mezi celou řadou možností nejednoznačných onemocnění identifikovat to správné jedním z následujících způsobů: rozpoznáním specifických kombinací znaků onemocnění nebo vyloučením přítomnosti ostatních nejednoznačných onemocnění [4] (souhrn v tab. 2). Lze užít obě dvě metody, protože:
- výskyt ostatních nejednoznačných onemocnění je častější než výskyt BPS. Vzhledem k tomu, že řadu z nich lze léčit, je správná identifikace nezbytná.
- neschopnost diagnostikovat jiné nejednoznačné onemocnění by automaticky nesprávně znamenalo diagnózu BPS
- u pacienta může být zároveň přítomno nejednoznačné onemocnění i BPS
Table 2. Souhrn pro postup při diagnostice. 
Diagnóza podtypu BPS by měla být stanovena na základě pacientem udávané bolesti v souvislosti s plněním močového měchýře doprovázené dalšími močovými symptomy, jako jsou denní a noční frekvence. Nezbytné je vyloučit přítomnost jiného nejednoznačného onemocnění. Pro první tři typy BPS (tab. 3) je indikována cystoskopie s hydrodistenzí a biopsie. V případě, že nebyla provedena cystoskopie s hydrodistenzí ani biopsie, je BPS považována za neklasifikovanou (BPS typ X). Typ 1 a 3 ESSIC dále subklasifikujeme na základě toho, zda byla provedena biopsie, a pokud ano, tak na základě nálezu (tab. 3).
Table 3. Klasifikace BPS podle návrhu ESSIC. 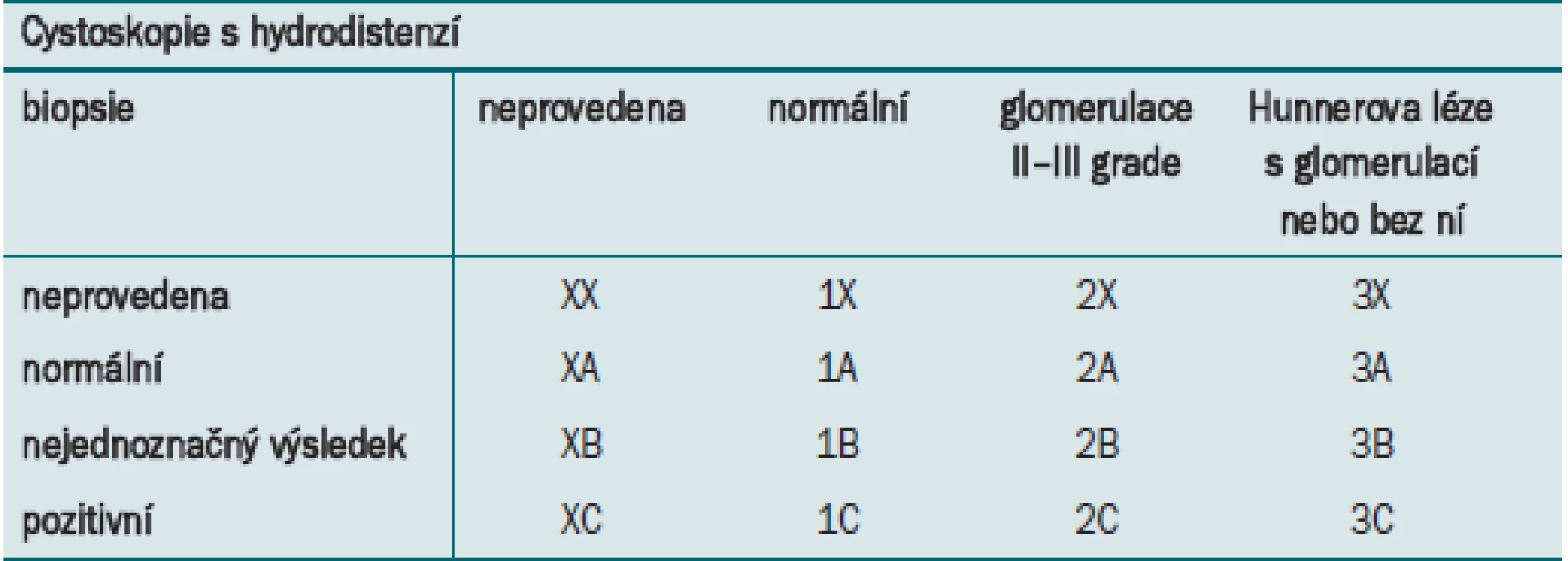
Pozitivní biopsie = histologické vyšetření prokáže zánětlivé infiltráty a/nebo mastocytózu detruzoru a/nebo granulační tkáň a/nebo intrafascikulární fibrózu. ESSIC klasifikace jednotlivých typů BPS (syndromu bolestivého močového měchýře)
Definice typu (tab. 2)
Typ X nebo neklasifikováno
Nebyla provedena cystoskopie s hydrodistenzí ani biopsie
1. normální cystoskopie s hydrodistenzí
- a) nebyla provedena biopsie
- b) normální biopsie
2. normální cystoskopie s hydrodistenzí, ale plus pozitivní histologické změny1
3. pozitivní nález při cystoskopii s hydrodistenzí2
- a)
glomerulace
X biopsie neprovedena nebo nejednoznačný výsledek
- žádné histologické změny
- pozitivní histologické změny1
- b)
Hunnerova léze
X biopsie neprovedena nebo nejednoznačný výsledek
- žádné histologické změny
- pozitivní histologické změny1
1histologické vyšetření prokáže zánětlivé infiltráty a/nebo mastocytózu detruzoru a/nebo granulační tkáň a/nebo intrafascikulární fibrózu
2cystoskopie: glomerulace 2–3 grade a/nebo Hunnerova léze
typ X a typ 1 v minulosti označován jako PBS
typ 2 a typ 3 v minulosti označovány jako ICKlasifikace podle ESSIC
ESSIC uvádí, že pro dokumentaci pozitivních znaků při diagnostice BPS je v rámci cystoskopie nezbytné provedení hydrodistenze. V případě, že je indikována, by měla být provedena biopsie (k dokumentaci histologických detailů BPS). Za pozitivní znaky BPS identifikované při cystoskopii se považují: glomerulace II–III grade a/nebo Hunnerovy léze. Za pozitivní znaky BPS identifikované při biopsii se považují: zánětlivé infliltráty a/nebo granulační tkáň a/nebo mastocytóza (> 28 buněk/mm2 a/nebo intrafascikulární fibróza). Některé údaje však nasvědčují tomu, že (pravděpodobně zvýšený) počet mastocytů je třeba prozkoumat v dalších studiích [11].
Hunnerova léze
Hunnerova léze se obvykle manifestuje jako ohraničená zarudlá oblast sliznice s malými cévami vyzařujícími směrem k centrálně lokalizovanému zjizvení, s vrstvou fibrinu nebo připojeným koagulem. Spolu se zvětšující se distenzí močového měchýře dochází k ruptuře této oblasti se známkami petechiálního krvácení z léze a okrajů sliznice v podobě vodopádu. Po distenzi dochází ke vzniku typického bulózního otoku, který se může rozšiřovat směrem k periferii. Poslední zkušenosti nasvědčují tomu, že Hunnerova léze je často přehlížena.
Bolest jako základní předpoklad
Pro BPS je charakteristická bolest v močovém měchýři. Nejnovější studie však prokazují, že korelace mezi stupněm obtížnosti bolesti v IC indexu (pálení, dyskomfort, bolest nebo tlak) a přítomností bolesti v IC symptom indexu činí pouze 0,7. Toto zjištění podtrhuje skutečnost, že řada pacientů uvádějící pocit tlaku nebo dyskomfortu v močovém měchýři/pánvi popisuje tento vjem spíše jako urgenci, a nikoli bolest. IASP (International Association for the Study of Pain, www.iasp-pain.org) uvádí následující definici bolesti: „Nepříjemný senzorický a emoční vjem spojený se skutečným nebo potenciálním poškozením tkáně, nebo popisovaný v rámci tohoto poškození“. Podle definice se jedná o bolest, ovšem pacient tento pocit jako bolest neoznačuje. Bolest nebo ekvivalentní pocit tlaku či dyskomfortu související s močovým měchýřem byl tedy považován za základní předpoklad pro popis symptomů, na jejichž základě by měl pacient podstoupit další vyšetření na BPS. Zvýšení intenzity bolesti při plnění močového měchýře nemusí být přítomno u všech pacientů.
Urgence nebyla zahrnuta do popisu pacientů, kteří vyžadují další vyšetření BPS
ICS definuje urgenci jako náhlé nutkání močit, které je obtížné vydržet [1]. BPS je často zaměňováno s OAB (hyperaktivní močový měchýř) vzhledem k tomu, že termín urgence se užívá pro popis symptomů obou poruch. Zatímco některé ženy popisují urgenci jako intenzivní potřebu běžet na toaletu, aby předešly pomočení, jiné ženy urgenci popisují jako potřebu močit pro zabránění intenzivní bolesti, pocitu tlaku nebo dyskomfortu. První skupina žen bude mít pravděpodobně OAB, zatímco u druhé skupiny žen lze očekávat přítomnost BPS.
Do popisu pacientů, kteří vyžadují další vyšetření BPS, ESSIC nezahrnula močovou urgenci, a to z několika následujících důvodů: urgence představuje hlavní symptom OAB – onemocnění, které je nejčastěji zaměňováno s BPS a jehož incidence je desetkrát častější než výskyt BPS. Klinické aspekty urgence jsou velmi složité. Jedním z návrhů, jak zabránit záměně BPS s OAB, je užívání termínu perzistentní nutkání (persistent urge) místo urgence (P. Hanno 2007, osobní komunikace). Vzhledem k tomu, že řada pacientů považuje silné, nepříjemné nutkání močit za nejvýraznější a nejvíce omezující ze všech symptomů, jsou pacienti (i lékaři) často zmatení, neboť se současnou terminologií nemohou pro popis svých obtíží používat výraz nutkání. V angličtině je nutkání (urge) definováno jako „silná tužba“, zatímco pro urgenci se užívá definice „vyžadující rychlé rozhodnutí nebo akci“. Termíny urgence a nutkání tedy velmi přesně vystihují rozdíl v pocitech, které pociťují pacienti s OAB a BPS. Perzistentní nutkání je tedy zařazeno mezi typické symptomy, jako je například frekvence. Přítomnost těchto symptomů tedy není nezbytná pro suspekci nebo diagnózu BPS.
Je nutné vyloučit přítomnost ostatních onemocnění, která mohou být zaměňována s BPS
V medicíně založené na důkazech (evidence-based) je diagnóza stanovena na základě klinické anamnézy, fyzikálního vyšetření a vhodného klinického vyšetření, která umožní eliminovat další onemocnění ze seznamu diferenciálních diagnóz a potvrdit konečnou diagnózu. BPS se může vyskytovat v kombinaci s dalšími onemocněními, jako jsou chronická nebo recidivující infekce močových cest nebo endometrióza. Zdá se tedy logické vyloučit z terapeutických studií pacienty s nejednoznačným onemocněním vzhledem k tomu, že symptomy a znaky mohou být vyvolány jak BPS, tak dalším onemocněním, nebo případně oběma. Do studií zkoumajících prevalenci BPS je však naopak vhodné zahrnout všechny případy BPS, tedy i pacienty s dalšími nejednoznačnými onemocněními. Tento přístup eliminuje potřebu stanovit samostatná diagnostická kritéria pro klinickou praxi a vědecké studie.
LÉČBA
U většiny pacientů lze kromě agresivnějšího přístupu indikovat rovněž konzervativní léčbu. Karsenty et al přiřadili jednotlivým možnostem léčby úrovně důkazu a stupně doporučení [12].
Behaviorální terapie spočívá v poskytnutí informací týkajících se osobní hygieny, způsobů, jak předcházet zácpě, stravy bez nápojů a potravin, které mohou zhoršovat bolest (alkohol, citrusy/rajčata, káva, koření, kyselina citronová a perlivé nápoje) a naopak konzumaci produktů, které mohou bolest zmírňovat (vláknina a mastné kyseliny udržující rovnováhu prostgladinů). Jako užitečné se dále uvádí rady týkající se tělesného pohodlí (volné oblečení, masáže, výhřevné podložky, horké koupele) a psychologická péče.
Medikamentózní léčba BPS
Je třeba si uvědomit, že odpověď na různé druhy léčby se liší v závislosti na podtypu onemocnění. K dispozici máme několik terapeutických modalit (tab. 4).
Table 4. Léčebné modality se stupněm doporučení (12 a další). 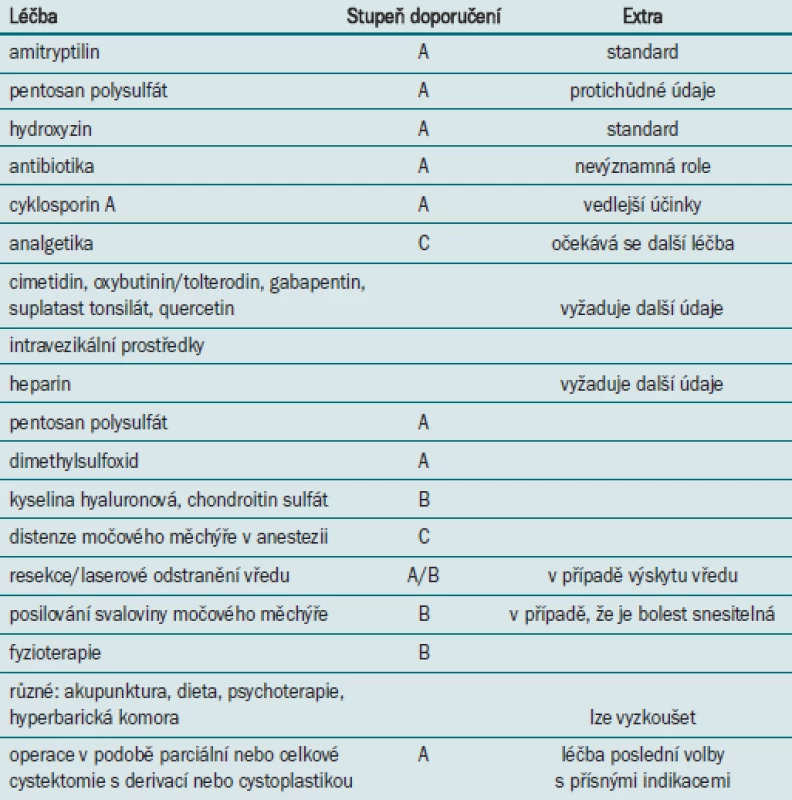
Perorální léčba
V povětšinou malých studiích byla testována různá agens:
- Amitriptylin [13], 25–100 mg, úroveň důkazu: 1, stupeň doporučení: B. Princip účinku tohoto agens je několikanásobný: jako 5-HT inhibitor zpětného vychytávání Na zvyšuje inhibici v dorzálním rohu. Jako antagonista NMDA (N-methyl-D-aspartát) působí proti centrální senzitizaci. Rovněž periferně moduluje Na-kanály a uplatňuje systém endogenních opioidů.
- O účinku syntetického GAG, pentosanpolysulfátu sodného (Elmiron®) existují v literatuře protichůdné údaje, aplikace tohoto agens však může přinášet benefit [14–16].
- Mezi další perorální agens patří Nifedipin [17], antihistaminika [18–19], různé léky proti bolesti.
Instilační terapie
- Heparin (polysacharid sulfát) se aplikuje v dávce 10 000–40 000 jednotek jednou denně po dobu několika týdnů. Účinek se nedostavuje okamžitě, ale po jednom až třech měsících. Dosavadní zkušenosti ukazují, že léčbu nelze přerušit.
- Dimethyl sulfoxid (DMSO) v dávce 50 ml/ 50 %, 30 % nebo 20 % má protizánětlivé, analgetické vlastnosti a rovněž působí jako svalový relaxans. Instilace probíhá od několika do 30 minut, jednou týdně, po dobu dvou měsíců. Tento preparát je schválen FDA (Úřadem pro kontrolu potravin a léčiv) a může být aplikován 3–4 týdny po odebrání biopsie. 24–48 hodin po aplikaci vyvolává zápach a pachuť česneku. V případě nedostatečné odpovědi lze přidat 100 mg hydrokortizonu.
- Mezi další preparáty patří chondroitin, quercitin, clorpactin 0,4% v anestezii, botulin toxin, capsaicien-resinoferatoxin.
Nemedikamentózní léčba
- fyzioterapie s manuální terapií, relaxace a TENS [20–22]
- posilování močového měchýře v případě, že to bolest umožňuje
- neuromodulace [24,25]
Operační léčba
- konzervativní operace: déletrvající hydrodistenze [26]
- rozsáhlejší operační výkony jako např. derivace moči, enterocystoplastika [27]
Centra pro léčbu bolesti
PSYCHOLOGICKÝ ASPEKT BOLESTIVÉHO MOČOVÉHO MĚCHÝŘE
Je zřejmé, že oblast perinea zahrnující dolní cesty močové představuje „citlivou“ zónu. Není tedy překvapující, že v případě, kdy se pacient příliš koncentruje na tuto oblast, může být pociťovaný vjem ještě posílen. Problematickým se jeví vliv „skutečné“ bolesti na psychický stav pacienta. Dostáváme se zde k tradiční otázce: „Co bylo dříve, vejce, nebo slepice?“ Ve většině případů se jedná o neřešitelný problém.
Klinický obraz bolestivého močového měchýře lze pouze výjimečně snadno interpretovat. U mnoha pacientů trvá stanovení správné diagnózy delší dobu a v řadě případů je diagnóza stanovena až na základě vyloučení přítomnosti ostatních onemocnění. Pacient tak navštíví několik lékařů a pravděpodobně podstoupí v rámci diagnostiky a léčby onemocnění řadu nepříjemných vyšetření. Vzhledem k tomu, že BPS není ve všech případech odhalen, existuje zde riziko, že lékař bude pacientovy potíže související s dolními cestami močovými mylně přisuzovat psychiatrickému onemocnění. Webster uvádí, že u více než 45 % žen bylo mylně diagnostikováno gynekologické onemocnění a dalším 43 % ženám byl přisuzován psychiatrický problém [28]. Důsledky tohoto omylu jsou skutečné: absence strategie umožňující pacientovi předcházet symptomům, sebeobviňování, nedostatečné prostředky pro zvládání onemocnění, negativní posuzování vlastní síly a kompetence. Negativní dopad symptomů na běžný život pacienta, jeho zaměstnání, spánek, sexuální život i celkovou kondici je evidentní.
V naší společnosti, která si cení fyzickou sílu a dokonalost, bude oslabující zdravotní stav, jakým je bolestivý močový měchýř při BPS nebo jiném onemocnění, vyvolávat pocit studu a hanby. K tomu přispívá obraz lékaře, jehož hlavním úkolem je léčit pacienty s akutním onemocněním, u nichž léčba přinese rychlou úlevu. Léčba pacientů s chronickým onemocněním je obvykle velmi frustrující, protože i navzdory nejlepší péči nemusí přinášet úlevu. Ne všichni lékaři se budou chtít do léčby těchto pacientů pouštět. Z tohoto důvodu byla vytvořena specializovaná centra, kde je pacientům vedle fyzické léčby poskytována rovněž časově náročná psychologická podpora [29,30].
SLEDOVÁNÍ
Pacienti trpící BPS/CPPS vyžadují dlouhodobou péči, která vyžaduje pravidelná vyšetření a modifikaci terapeutického přístupu. Vzhledem k tomu, že úplné vyléčení onemocnění je výjimečné, a dokonce nepravděpodobné, hlavní cíl terapie spočívá ve zmírnění bolesti a s ní spojeného utrpení. Tito pacienti tedy vyžadují sledování a podporu.
Wyndaele Jean Jacques
MD DSci PhD FEBU FISCOS
Professor of Urology
University Antwerp and Antwerp University Hospital
10 Wilrijkstraat
B 2650 Edegem
Belgium
Jean-Jacques.wyndaele@ua.ac.be
Sources
1. Abrams P, Cardozo L, Fall M et al. The standardisation of terminology of lower urinary tract function: report from the Standardisation Sub-committee of the International Continence Society. Neurourol Urodyn 2002; 21(2): 167–178.
2. Fall M, Baranowski AP, Elneil S et al. EAU guidelines on chronic pelvic pain. Eur Urol 2010; 57(1): 35–48.
3. Wyndaele JJ, De Wachter S. The basics behind bladder pain: a review of data on lower urinary tract sensations. Int J Urol 2003; 10 Suppl: S49–55.
4. van de Merwe JP, Nordling J, Bouchelouche P et al. Diagnostic Criteria, Classification, and Nomenclature for Painful Bladder Syndrome/Interstitial Cystitis: An ESSIC Proposal. Eur Urol 2008; 53(1): 60–67.
5. Nordling J, Anjum FH, Bade JJ et al. Primary evaluation of patients suspected of having interstitial cystitis (IC). Eur Urol 2004; 45(5): 662–669.
6. Peeker R, Aldenborg F, Dahlström A et al. Increased tyrosine hydroxylase immunoreactivity in bladder tissue from patients with classic and nonulcer interstitial cystitis. J Urol 2000; 163(4): 1112–1115.
7. Russell AL. Glycoaminoglycan (GAG) deficiency in protective barrier as an underlying, primary cause of ulcerative colitis, Crohn's disease interstitial cystitis and possibly Reiter's syndrome. Med Hypotheses 1999; 52(4): 297–301.
8. Lundeberg T, Liedberg H, Nordling L et al. Interstitial cystitis: correlation with nerve fibres, mast cells and histamine. Br J Urol 1993; 71(4): 427–429.
9. Johansson SL, Ogawa K, Fall M. The pathology of IC.in Interstitial cystitis edited by Grannum R Sant, Lippincott-Raven. Philadelphia 1997,Chapter 18 : 143–151.
10. Wyndaele JJ. Evaluation of patients with Painful Bladder Syndrome/interstitial cystitis. ScientificWorldJournal 2005; 5 : 942–949.
11. Wyndaele JJ, Van Dyck J, Toussaint N. Cystoscopy and bladder biopsies in patients with bladder pain syndrome carried out following ESSIC guidelines. Scand J Urol Nephrol 2009; 43(6): 471–475.
12. Karsenty G, AlTaweel W, Hajebrahimi S et al. EAU-EBU Update Series 2006; 4 : 47–61.
13. Hanno PM. Amitriptyline in the treatment of interstitial cystitis. Urol Clin North Am 1994; 21(1): 89–92.
14. Dimitrakov J, Kroenke K, Steers WD et al. Pharmacologic management of painful bladder syndrome/ interstitial cystitis: a systematic review. Arch Intern Med 2007; 167(18): 1922–1929.
15. Parsons CL, Benson G, Childs SJ et al. A quantitatively controlled method to study prospectively interstitial cystitis and demonstrate the efficacy of pentosanpolysulfate. J Urol 1993; 150(3): 845–848.
16. Fritjofsson A, Fall M, Juhlin R et al. Treatment of ulcer and nonulcer interstitial cystitis with sodium pentosanpolysulfate: a multicenter trial. J Urol 1987; 138(3): 508–512.
17. Fleischmann JD, Huntley HN, Shingleton WB et al. Clinical and immunological response to nifedipine for the treatment of interstitial cystitis. J Urol 1991; 146(5): 1235–1239.
18. Simmons JL. Interstitial cystitis: an explanation for the beneficial effect of an antihistamine. J Urol 1961; 85 : 149–155.
19. Seshadri P, Emerson L, Morales A. Cimetidine in the treatment of interstitial cystitis. Urology 1994; 44(4): 614–616.
20. Weiss JM. Pelvic floor myofascial trigger points: manual therapy for interstitial cystitis and the urgency-frequency syndrome. J Urol 2001; 166(6): 2226–2231.
21. Fall M, Carlsson CA, Erlandson BE. Electrical stimulation in interstitial cystitis. J Urol 1980; 123(2): 192–195.
22. Fall M, Lindstrom S. Transcutaneous electrical nerve stimulation in classic and nonulcer interstitial cystitis. Urol Clin North Am 1994; 21(1): 131–139.
23. Barbanti G, Maggi CA, Beneforti P et al. Relief of pain following intravesical capsaicin in patients with hypersensitive disorders of the lower urinary tract. Brit J Urol 1993; 71(6): 686.
24. MaherCF, Carey MP, Dwyer PL et al. Percutaneous sacral nerve root neuromodulation for intractable interstitial cystitis. J Urol 2001; 165(3): 884–886.
25. Payne CK, Whitmore KE, Diokno AC et al. Sacral neuromodulation in patients with interstitial cystitis: a multi-center clinical trial. Neurourol Urodyn 2001; 20 : 554–555.
26. Aihara K, Hirayama A, Tanaka N et al. Hydrodistension under local anesthesia for patients with suspected painful bladder syndrome/interstitial cystitis: safety, diagnostic potential and therapeutic efficacy. Int J Urol 2009; 16(12): 947–952.
27. Rössberger J, Fall M, Jonsson O et al. Long-term results of reconstructive surgery in patients with bladder pain syndrome/interstitial cystitis: subtyping is imperative. Urology 2007; 70(4): 638–642.
28. Webster D. Interstitial cystitis: women at risk for psychiatric misdiagnosis. AWHONNS Clin Issues Perinat Women Health Nurs 1993; 4(2): 236–243.
29. Draucker CB. Coping with a difficult to diagnose illness: The example of interstitial cystitis. Health Care women Int 1991; 12(2): 191–198.
30. Frewen WK. The significance of psychosomatic factor in urge incontinence. Br J Urol 1984; 56(3): 330.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2010 Issue 3-
All articles in this issue
- Role sakrální neuromodulace v urologické praxi
- Guidelines EAU pro léčbu chronické pánevní bolesti
- Změny v řešení chronické prostatitidy/syndromu chronické pánevní bolesti
- Chronická pánevní bolest (CPPS): anatomické parametry, patofyziologické mechanizmy, nejednoznačné onemocnění, fenomén chronického onemocnění. Syndrom bolestivého močového měchýře
- Syndrom chronické pánevní bolesti a současné možnosti léčby
- Bladder pain syndrome – současná terminologie, diagnostika a léčba
- Hyperaktivní močový měchýř u dětí a dospělých
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Syndrom chronické pánevní bolesti a současné možnosti léčby
- Změny v řešení chronické prostatitidy/syndromu chronické pánevní bolesti
- Hyperaktivní močový měchýř u dětí a dospělých
- Chronická pánevní bolest (CPPS): anatomické parametry, patofyziologické mechanizmy, nejednoznačné onemocnění, fenomén chronického onemocnění. Syndrom bolestivého močového měchýře
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career
