-
Medical journals
- Career
Symptomatický myeloidný sarkóm uteru v čase diagnózy akútnej myeloblastovej leukémie – kazuistika
Authors: Martišová M.ihash2ihash4ihash6ihash8ihash10 1 1 1 2 3 1
Authors‘ workplace: Klinika hematológie a transfuziológie SZU, LFUK a UNB Bratislava, Ústav patologickej anatómie a konzultačné centrum bioptickej diagnostiky ochorení krvotvorby JLFUK a MFN Martin, Gynekologicko-pôrodnícke oddelenie Považská Bystrica 1
Published in: Transfuze Hematol. dnes,17, 2011, No. 3, p. 144-148.
Category: Comprehensive Reports, Original Papers, Case Reports
Overview
Extramedulárna leukemická infiltrácia v podobe myeloidného sarkómu je veľmi zriedkavá, vo väčšine prípadov klinicky nemá a často preto zostáva nediagnostikovaná. Symptomatický myeloidný sarkóm sa môže manifestovať v čase diagnózy a relapsu akútnej myeloblastovej leukémie, ojedinele však s rôznym časovým odstupom predchádza prejavom základného ochorenia v kostnej dreni. Jeho manifestácia v oblasti ženského genitálneho traktu je raritná, najčastejšie popisovaná v ováriách, extrémne zriedkavý je však v cervixe a cavum uteri.
Kľúčové slová:
myeloidný sarkóm, akútna myeloblastová leukémia, ženský genitálny traktÚvod
Myeloidný sarkóm (granulocytový sarkóm, chloróm, chloromyelóm, chloromyelosarkóm, granulocytový leukosarkóm, myeloblastóm, myelocytóm, myelosarkóm) je raritná forma extramedulárnej leukemickej infiltrácie; solídny tumor pozostávajúci z nedostatočne diferencovaných buniek myeloidnej línie (1, 2).
Prvýkrát bol popísaný anglickým lekárom A. Burnsom v roku 1811, hoci pojem „chloróm“ sa objavil až v roku 1853 a odvodzuje sa z gréckeho základu slova chloros (zelený). Zelená farba je vďaka vysokému podielu myeloperoxidázy v bunkových lyzozómoch dominantnou farbou tohto tumoru. Avšak v dôsledku skutočnosti, že viac ako 30 % z nich sa prezentuje aj farbou bielou, šedou, či hnedou, zaviedol Rappaport v roku 1967 pojem myeloidný sarkóm (MS).
V súčasnosti sa v prípade akejkoľvek extramedulárnej manifestácie akútnej myeloblastovej leukémie (AML) preferuje označenie MS, s výnimkou dvoch špecifických lokalizácii:
- leukemia cutis – infiltrácia kože leukemickými bunkami
- meningeálna leukémia – infiltrácia meningov/ subarachnoidálneho priestoru leukemickými bunkami (častejšia ako solídny tumor).
Súvislosť medzi MS a akútnou leukémiou bola prvýkrát popísaná v roku 1902 Dockom a Warthinom.
MS sa najčastejšie vyskytuje ako systémová manifestácia klinicky známej AML (3), signalizuje jej relaps po chemoterapii (4), či transplantácii periférnych krvotvorných buniek (PKB) (5), môže však byť aj súčasťou blastovej transformácie chronickej myelocytovej leukémie (CML) (3), či myelodysplastického syndrómu (MDS) alebo myeloproliferatívnej neoplázie (MPN) do AML (6). Zriedka býva iniciálnym prejavom základného ochorenia v čase diagnózy (3, 7–11), kedy sa jeho vývoj pripisuje masívnej proliferácii leukemických buniek a len celkom raritne sa prezentuje ako tumor bez predchádzajúcej evidencie AML (tzv. primárny chloróm) (12–14). MS bez preexistujúcej či konkomitantnej AML, MDS či MPN takmer vždy AML predchádza a je iniciálnou manifestáciou systémového, nie ohraničeného malígneho procesu. Časový medián od diagnózy MS po dôkaz leukemickej infiltrácie kostnej drene varíruje od 5 týždňov do 3 rokov (12, 15). Rovnako sa aj solitárna manifestácia MS po úspešnej liečbe AML považuje za predzvesť systémového relapsu.
Súhrn rizikových faktorov výskytu MS pri akútnej myeloblastovej leukémii:
- AML FAB podtyp M2 (6), M4 (16,17), M5 (16,17),
- cytogenetické abnormality (t(8;21) (6,18), t(16;16), inv (16) (6)),
- expresia T-bunkových povrchových diferenciačných antigénov (napr. CD13, CD14, CD56) na myeloblastoch,
- hyperleukocytóza v čase diagnózy.
Napriek uvedeným rizikovým faktorom je výskyt MS zriedkavou komplikáciou AML.
MS býva často klinicky nemý, prípadne je jeho symptomatológia len málo významná, často nešpecifická, závislá od lokalizácie. Z viscerálnych orgánov postihuje najčastejšie obličky, kde v dokumentovaných prípadoch viedol až k renálnemu zlyhaniu, popísal sa aj v pečeni, slezine, ostatných častiach GIT, lymfatických uzlinách, gingívach, CNS, pľúcach a testes. Zriedkavejšie bol zaznamenaný v koži, močovom mechúre, pankrease, peritoneálnej dutine, pleure, štítnej žľaze, thyme, prsníku či orbite.
Symptomatické postihnutie ženského genitálneho traktu je veľmi zriedkavé (7). Častejšie sú asymptomatické formy, s predominantným postihnutím ovárií (cca 11–36 %). Infiltrácia uteru je raritná (19) a existuje len limitovaný počet kazuistík symptomatického MS postihujúceho cavum (5, 7–11) a cervix uteri (1, 11, 12). Najčastejšími symptómami sú nebolestivé vaginálne alebo postkoitálne krvácanie (81 %), dyspareunia a abdominálna bolesť (13 %) a systémové príznaky (6 %) (2).
V diagnostike MS zohráva najvýznamnejšiu úlohu bioptické vyšetrenie. Keďže morfológia buniek pripomína veľkobunkový lymfóm, z historických údajov je známe, že bioptické obrazy boli často chybne interpretované predovšetkým tam, kde sa MS vyvinul pred manifestáciou AML v kostnej dreni (20). Vývoj nových diagnostických techník, imunohistochémie, monoklonových protilátok a prietokovej cytometrie viedol k zvýšeniu spoľahlivosti a spresneniu diagnostiky MS.
Podľa literárnych údajov sa v minulosti liečba ojedinelých prípadov MS uteru realizovala kombináciou chirurgickej intervencie, chemoterapie a rádioterapie (5, 7–11).
Chorlton (12) a Seo (1) publikovali 2 a 1 prípad MS cervixu uteri, ktoré sa prezentovali vaginálnym krvácaním a tumorom. V počiatočných štádiách týchto prípadov nič nenaznačovalo, že by mohlo ísť o prejav systémovej choroby, avšak leukémia sa potvrdila neskôr v pooperačnom období. Na základe týchto sledovaní bol vyslovený názor o možnosti akcelerácie priebehu ochorenia pri samostatne chirurgickom riešení. Následne aj Imrie (21) publikoval výsledky analýzy skupiny 90 prípadov solitárnych MS, ktoré predchádzali dôkazu AML. Podanie chemoterapie (CHT) v čase diagnózy MS oneskorilo progresiu do AML s mediánom 36 mesiacov oproti 6 mesiacom bez CHT a súviselo s lepším prežívaním. Najlepšie výsledky sa teda dosahujú v prípade, keď sa systémová liečba podá v čase diagnózy MS (6).
Tieto pozorovania poukazujú na to, že napriek zdanlivo lokalizovanej chorobe je MS indikátorom systémovej choroby, ktorá vyžaduje systémovú terapiu (23).
Názory na prognostický význam MS sú rozporuplné. Časť odborníkov sa prikláňa k názoru, že MS je známkou horšej prognózy pre slabšiu odpoveď na liečbu a skrátené prežívanie (24). Iní argumentujú, že MS sa ako biologický marker asociuje s ďalšími negatívnymi prognostickými faktormi a nemá preto nezávislú prognostickú signifikantnosť (17).
Dvojročné prežívanie pacientov s MS je iba 6 % a ani jeden chorý neprežíva dlhšie ako 5 rokov (3). Navyše žiadny pacient s MS, ktorý sa objavil pri relapse AML, neprežíva dlhšie ako 2 roky (3).
Kazuistika
58ročná pacientka bez závažnejšieho predchorobia, bola 26. 9. 2008 odoslaná na Oddelenie urgentnej medicíny Nemocnice Sv. Cyrila a Metoda, Antolská 11, Bratislava, pre 4dňovú menometrorágiu po 3ročnej menopauzálnej pauze, s anamnézou takmer 2 mesiace trvajúcich febrilít, progresívnej slabosti, artralgií, profúzneho nočného potenia a anorexie s úbytkom hmotnosti. Objektívne vyšetrenie nepreukázalo lymfadenopatiu (LAP), abdomen bol bez peritoneálnej iritácie, fyzikálne aj USG vyšetrením bola zistená hepatomegália, lien zväčšený nebol. V hemograme bola leukocytóza (Le 60 x 109/l) s 87,5 % blastov, anémia ľahkého stupňa (Hb 113 g/l), trombocyty v norme (Tr 148 x 109/l), fyziologický koagulogram, biochemické parametre s hyperurikémiou a hraničným kreatinínom, ostatný nález bol v norme. V nátere periférnej krvi 46 % blastov vykazovalo POX pozitivitu. Cytologické vyšetrenie kostnej drene potvrdilo 75% infiltráciu blastami so 45% POX pozitivitou, cytogenetické vyšetrenie kostnej drene bolo pozitívne na dôkaz zvýšenej hodnoty wt1 proliferačného markera (NCN 6,04; fyziologická hodnota v KD je 0,01–0,04), prietokovou cytometriou sa dokázal imunofenotyp blastov CD34, CD33, CD65, CD117 (pozn. marker CD56 nevyšetrený). Na základe uvedených vyšetrení bola stanovená diagnóza AML podtyp M2 (FAB).
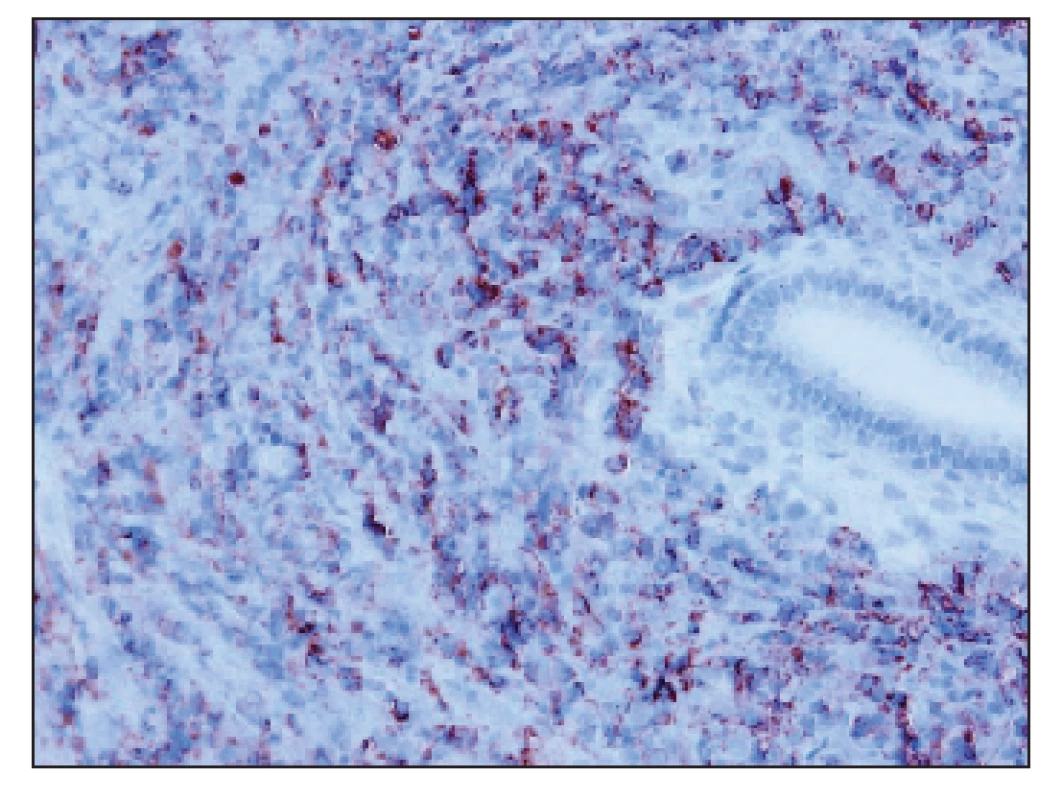
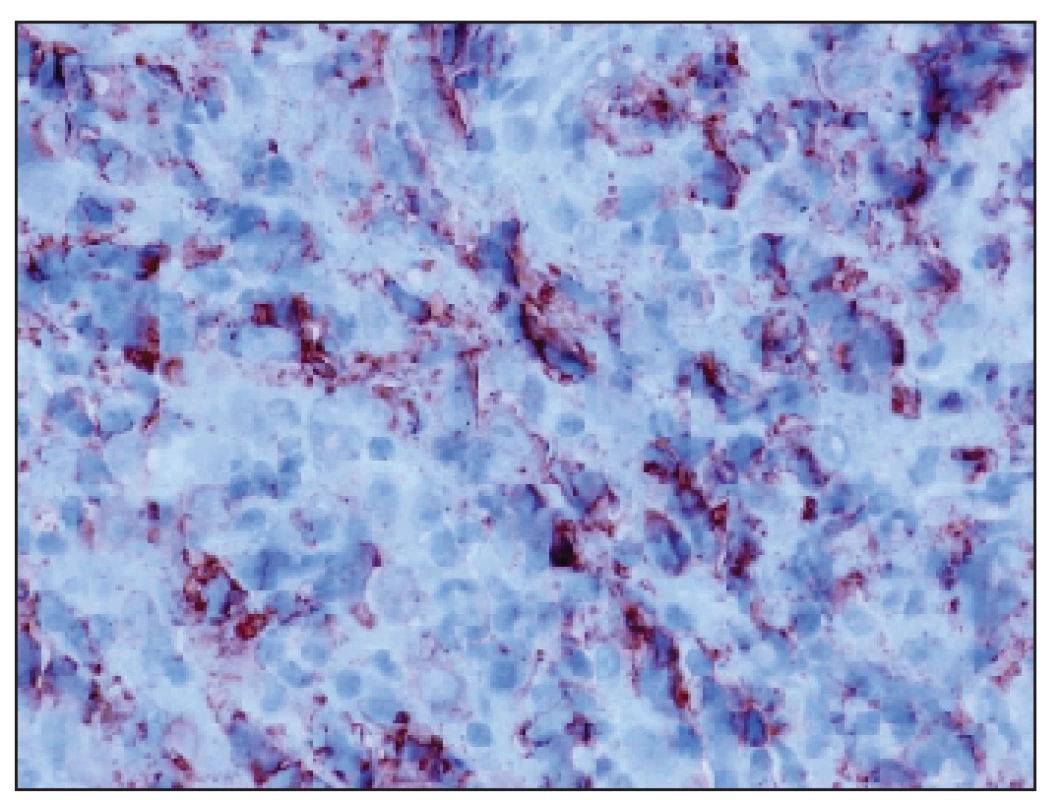
U pacientky sme začali cytoredukčnú liečbu hydroxyureou a pre pretrvávajúcu menometrorágiu bez jednoznačného hematologického pandantu sme podali methylergometrín (MEM). Napriek terapii MEM a doplnenej hemostyptickej liečbe krvácanie naďalej pokračovalo. Pre pozitívnu rodinnú anamnézu v zmysle gynekologických malignít, sa suponovala duálna malignita. CT vyšetrenie brucha a malej panvy s kontrastom však nepotvrdilo jednoznačné známky malígneho neoplastického procesu a LAP v malej panve, uterus bol primeranej veľkosti, bez ložiskových zmien. V rámci riešenia hemorágie sa vykonala frakcionovaná kyretáž, ktorou sa z cervixu získalo malé, z cavum uteri hojnejšie množstvo belavého materiálu. V histologickom obraze zaslanej vzorky bola rozsiahla lymfocytárna infiltrácia strómy B-bunkovými agregátmi a výrazná prímes T-lymfocytov, v zhlukoch a pruhoch bola prítomná prímes blastických elementov CD34, CHAE čiastočne a MPO pozit., čo zodpovedalo infiltrácii klinicky známou AML M2 (obr. 1–6). Po cytoredukčnej liečbe dostala pacientka indukčnú chemoterapiu podľa protokolu EORTC AML-12, ktorá navodila 3. 11. 2008 prvú kompletnú hematologickú remisiu (KHR).
Image 1. Nenápadné blasty medzi žľazami (HE 20x). 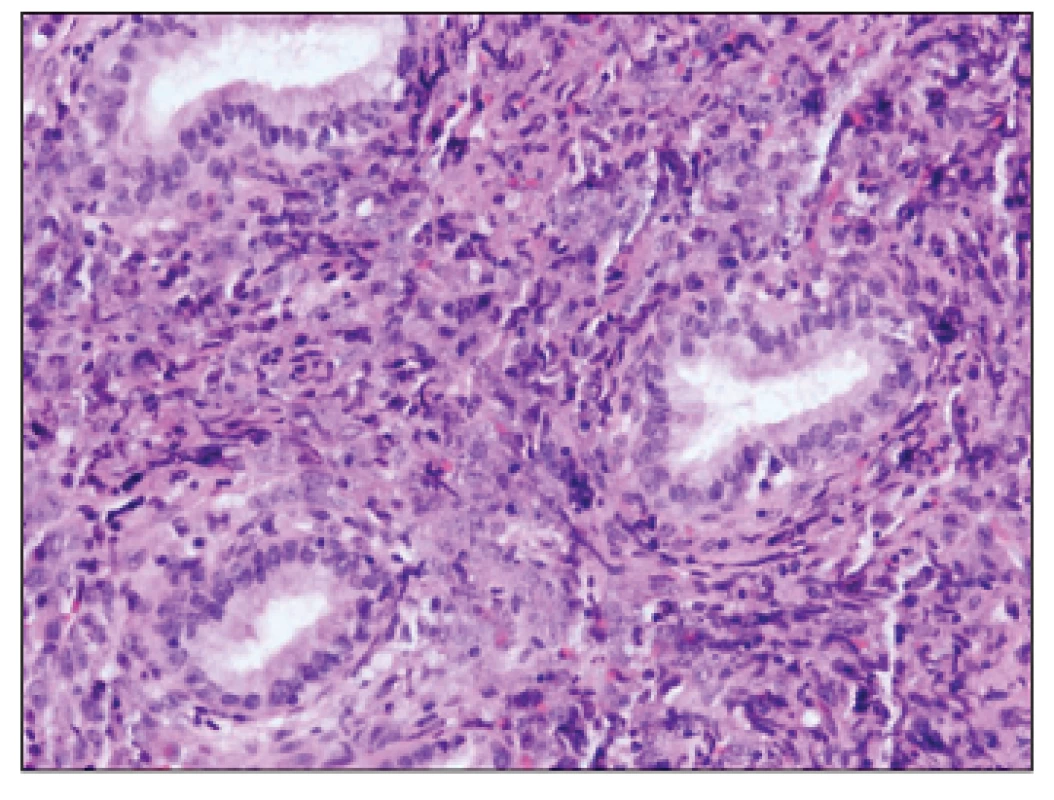
Image 2. Žľaza a blasty (HE 20x). 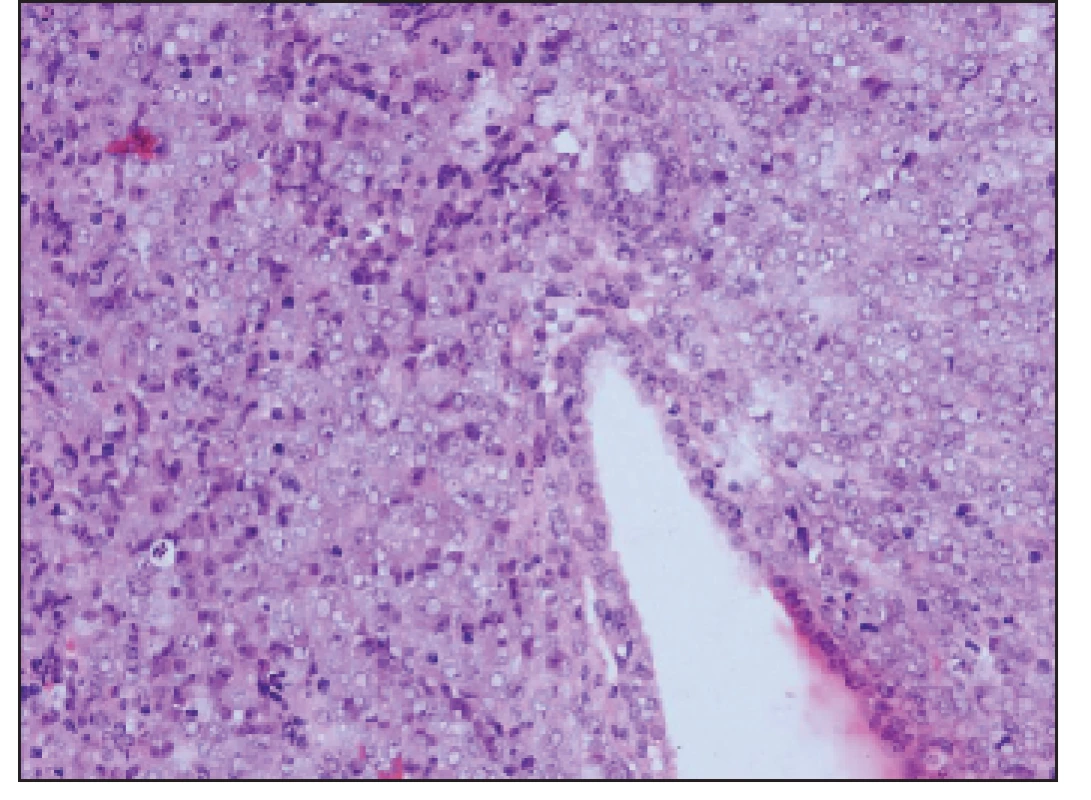
Image 3. Detail – blasty (HE 40x). 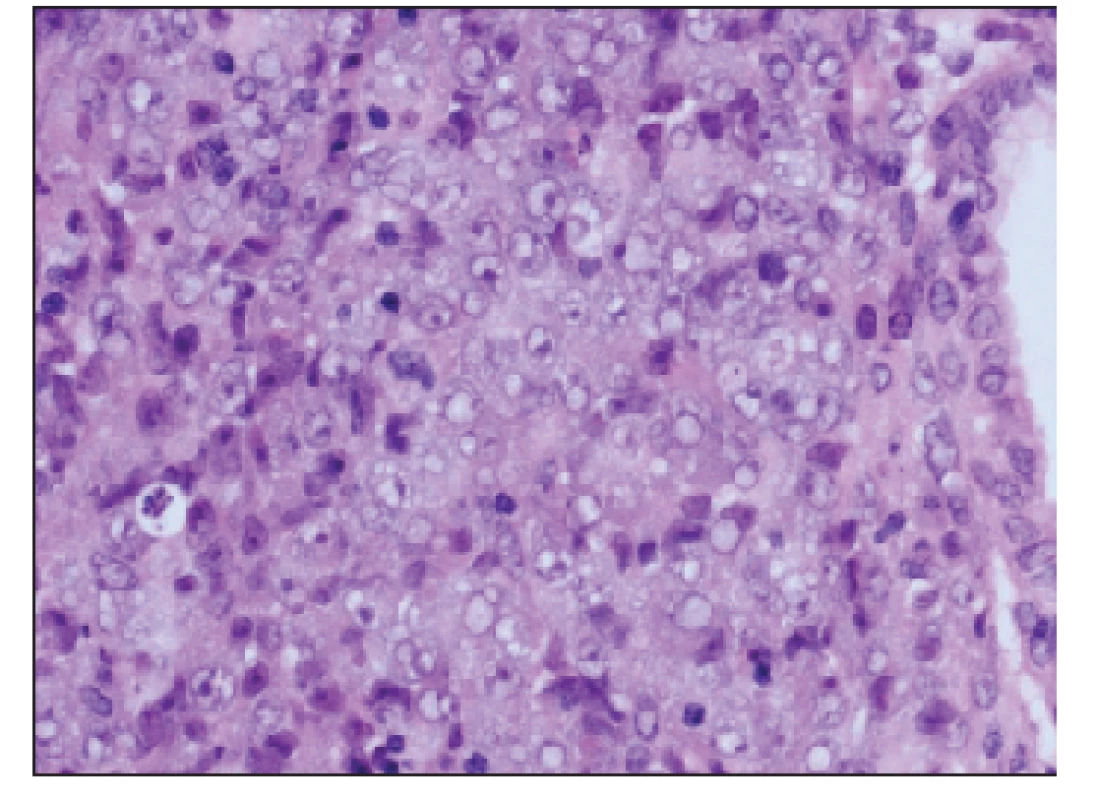
Image 4. CHAE pozitivita ojedinelých buniek (CHAE 40x). 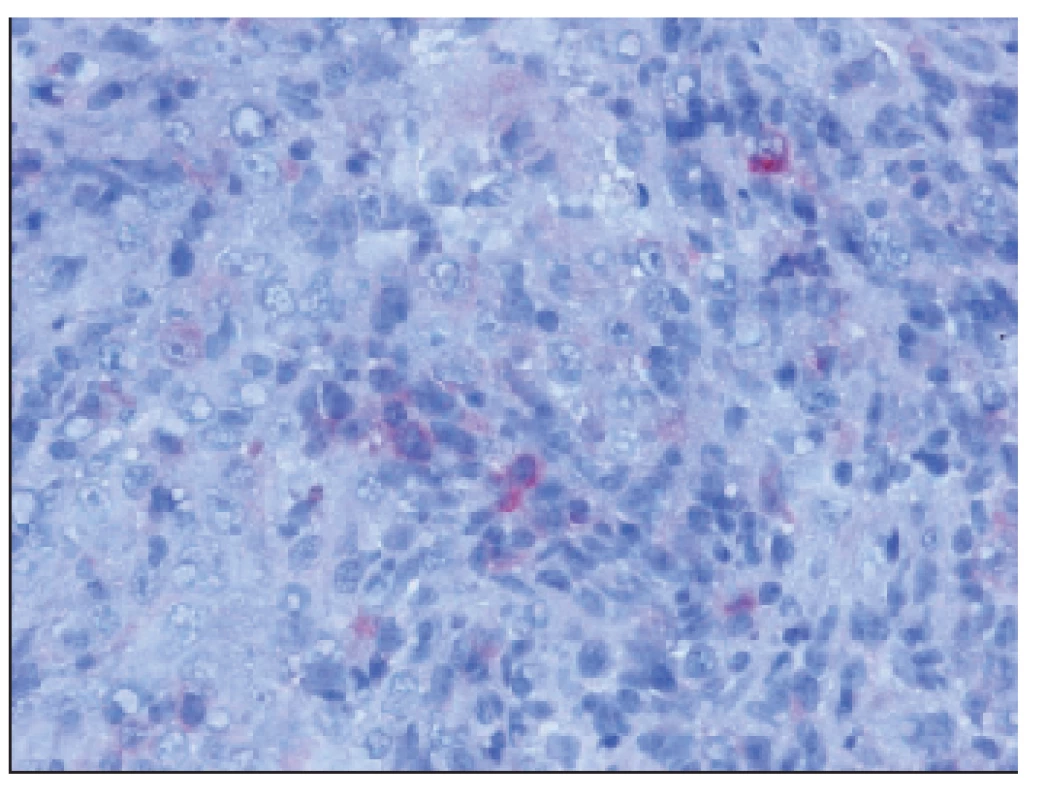
U pacientky sa počas následnej liečby ani pri 2 ďalších relapsoch leukémie už neobjavila gynekologická symptomatológia či relaps MS uteru ani v inej lokalizácii. Pacientka exitovala v 2. relapse AML, 13 mesiacov od stanovenia diagnózy.
Diskusia
Extramedulárna manifestácia AML je častejšia pri hyperleukocytóze v čase diagnózy, monocytových variantoch AML, niektorých cytogenetických abnormalitách a imunofenotypovej pozitivite CD56 (22, 25, 26). Incidencia klinicky manifestných MS komplikujúcich základné ochorenie je menej ako 1 % (2).
Medián vekového výskytu MS ženského genitálneho traktu je 47 rokov (rozsah 26–75 rokov) a u väčšiny pacientiek sa prezentuje vaginálnym krvácaním, niekedy abdominálnou bolesťou alebo nešpecifickými systémovými príznakmi. Nie je známy špecifický morfologický, povrchový marker, cytogenetický či molekulový podtyp AML, ktorý by mal jednoznačnú afinitu k uterinnému tkanivu. Mechanizmus infiltrácie endometria ostáva nevysvetlený a je predmetom ďalšieho výskumu. Sliznica maternice je infiltrovaná CD56 pozitívnymi NK bunkami, ktorých počet sa zvyšuje predovšetkým v čase implantácie oplodneného vajíčka v skorých štádiách gravidity. CD 56 pozitívne NK bunky sú pravdepodobne zapojené do procesu trofoblastovej migrácie a formovania placenty (27). Keďže CD56 predstavuje adhezívnu molekulu, predpokladá sa, že by mohla zohrať aktívnu úlohu v preferenčnom usmernení NK buniek do uterinného tkaniva a zapríčiniť akumuláciu leukemických buniek s CD56 pozitívnym markerom v tejto lokalizácii (16).
Záver
V uvedenej kazuistike prezentujeme vo všeobecnosti zriedkavý MS, ktorý sa vyznačuje ďalšími dvomi raritami; zriedkavou lokalizáciou (cervix a cavum uteri), ako aj málokedy prítomnou klinickou symptomatológiou (vaginálne krvácanie).
Dostupnosť informácií o problematike MS je obmedzená, v literatúre limitovaná na nepočetné kazuistiky a analýzy skupín publikovaných prípadov. Problematika je však očividne multidisciplinárna, závislá na vzájomnej kooperácii viacerých špecialistov. Keďže prognóza základného ochorenia je všeobecne nepriaznivá, stáva sa pre pacientku kruciálnym včasné zahájenie systémovej liečby. Zvažovať MS ženského genitálneho traktu v rámci diferenciálnej diagnostiky, interdisciplinárny prístup, adekvátna a komplexná diagnostika vedúca k skorému zahájeniu liečby, by tak mohla viesť k zlepšeniu prežívania pacientiek s takouto formou MS. Pacientky s abnormálnym uterinným krvácaním a nejednoznačnou endometriálnou biopsiou by mali byť dôsledne vyšetrené, sledované a podrobené ďalšej diferenciálnej diagnostike.
Zoznam použitých skratiek:
AML – akútna myeloblastová leukémia
CD – „cluster of differentiation“, diferenciačný antigén
CNS – centrálny nervový systém
CML – chronická myelocytová leukémia
CT – computer tomography, počítačová tomografia
EORTC – European Organisation for Research and Treatment of Cancer, Európska organizácia pre výskum a liečbu rakoviny
FAB – francúzsko-americko-britská klasifikácia AML
GIT – gastro-intestinálny trakt
CHT – chemoterapia
KD – kostná dreň
KHR – kompletná hematologická remisia
LAP – lymfadenopatia
MDS – myelodysplastický syndróm
MEM – methylergometrín
MPO – myeloperoxidáza
MPN – myeloprofileratívna neoplázia
MS – myeloidný sarkóm
NCN – normalizovaný počet kópií
PKB – periférne krvotvorné bunky
POX – peroxidáza
USG – ultrasonografia
MUDr. Michaela Martišová
Klinika hematológie a transfuziológie LFUK, SZU a UNB
Nemocnica sv. Cyrila a Metoda
Antolská 11
851 07 Bratislava
Slovensko
Doručeno do redakce: 19. 4. 2011
Přijato po recenzi: 16. 5. 2011
Sources
1. Seo IS, Hull MT, Pak HY. Granulocytic sarcoma of the cervix as a primary manifestation. Case without overt leukemic features for 26 months. Cancer 1977; 40 : 3030.
2. Delaflor-Weiss E, Zauber NP, Kintiroglou M, Bermon EL, Malcynski D. Acute myelogenous leukemia relapsing as granulocytic sarcoma of the cervix. Acta Cytol 1999; 43 : 1124-1130.
3. Pathak B, Bruchim I, Brisson ML, Hammouda W, Bloom C, Gotlieb WH. Granulocytic sarcoma presenting as tumors of the cervix. Gynecol Oncol 2005; 98 : 493-497.
4. Shiga Y, Schichishima T, Aikawa K, et al. A case of acute nonlymphocytic leukaemia with leukaemic cell infiltration to the uterus followed by bone marrow relapse. Rinsho Ketsueki 1994; 35 : 501-505.
5. Maeng H, Cheong JW, Lee TS, Yang WI, Hahn JS, Ko YW. Isolated extramedullary relapse of acute myelogenous leukemia as uterine granulocytic sarcoma in an allogeneic hematopoietic stem cell transplantation recipient. Yonsei Med J 2004; 45 : 330-333.
6. Braekeleer M. Isolated granulocytic sarcoma followed by acute myelogenous leukemia type FAB-M2 associated with inversion 16 and trisomes 9 and 22. Leukemia 2002; 16 : 2458-2459.
7. Tripathi R, Sharma B, Chaturvedi KU, Khurana N, Mala YM. Granulocytic sarcoma of the female genital tract: report of a case with an unusual presentation. Gynecol Obstet Invest 2005; 59 : 184-186.
8. Kamble R, Kochupillai V, Sharma A, Kumar L, Thulkar S, Sharma MC. Granulocytic sarcoma of uterine cervix as presentation of acute myeloid leukemia: a case report and review of literature. J Obstet Gynaecol Res 1997; 23 : 261-266.
9. Huter O, Brezinka C, Nachbaur D, Schwaighofer H, Lang A, Neideswieser D. Successful treatment of primary extramedullary leukemia (EML) of the uterus with radical surgery, chemotherapy, autologous bone marrow transplantation (BMT) and prophylactic local irradiation. Bone Marrow Transplant 1996; 18 : 663-664.
10. Cassi E, Tossi A, De Paoli A, Turri C, Fortunato A, Assi A. Granulocytic sarcoma without evidence of acute leukemia: 2 cases with unusual localization (uterus and breast) and 1 case with bone localization. Haematologica 1984; 69 : 464-496.
11. Kapadia SB, Krause JR, Kanbour AI, Hartsock RJ. Granulocytic sarcoma of the uterus. Cancer 1978; 41 : 687-691.
12. Chorlton I, Norris HJ, King FM. Malignant reticuloendothelial disease involving ovary as a primary manifestation: A series of 19 lymphomas and 1 granulocytic sarcoma. Cancer 1974; 34 : 397.
13. Mwanda WO, Rajab JA. Granulocytic sarcoma: report of three cases. East Afr Med J 1999; 76 : 594-596.
14. Neiman RS, Barkos M, Bererd C, Bonner H, Mann R, Rydell RE. Granulocytic sarcoma: a clinicopathologic study of 61 biopsied cases. Cancer 1981; 48 : 1426-1437.
15. Mason TE, Demaree RS, Margolis CI. Granulocytic sarcoma (chloroma) two years preceding myelogenous leukemia. Cancer 1973; 31 : 423.
16. Matthes T, Collao C, Samii K, Chapuis B, Girardet CH, Diebold-Berger S. Uterine infiltration as first sign of acute myeloid leukemia. Am J Hematol 1999; 60 : 253-254.
17. Bischop MM, Revesz T, Bierings M, et al. Extramedullary infiltrates at diagnosis have no prognostic significance in children with acute myeloid leukemia. Leukemia 2001; 15 : 46-49.
18. Schwyzer R, Sherman GG, Cohn RJ, et al. Granulocytic sarcoma in children with acute myeloblastic leukemia and t(8;21). Med Pediatr Oncol 1998; 31 : 144-149.
19. Oliva E, Ferry JA, Young RH, Prat J, Srigley JR, Scully RE. Granulocytic sarcoma of the female genital tract: a clinicopathologic study of 11 cases. Am J Surg Pathol 1997; 21 : 1156-1165.
20. Yamauchi K, Yasuda M. Comparison in treatments of nonleukemic granulocytic sarcoma: report of 2 cases and a review of 72 cases in the literature. Cancer 2002; 94 : 1739-1746.
21. Imrie KR, Kovacs MJ, Selby D, et al. Isolated chloroma, the efect of early antileukemic therapy. Ann Intern Med 1995; 123 : 351-353.
22. Swirsky DM, Li YS, Matthews JG, Flemens RJ, Rees JK, Hayhoe FG. 8;12 translocation in acute granulocytic leukemia: cytological, cytochemical and clinic features. Br J Haematol 1984; 56 : 199-213.
23. Pitz MW, Maslyak O, Morales C, Seftel MD. Myeloid sarcoma of the uterus presenting as vaginal bleeding. Intern Med J 2006; 36 : 669-671.
24. Byrd JC, Weiss RB, Arthur DC, et al. Extramedullary leukemia adversely affects hematologic complete remission rate and overall survival in patients with t(8;21)(q22;q22): Results from Cancer and Leukemia Group B 8461. J Clin Oncol 1997; 15 : 466-475.
25. Chang H, Brandwein J, Yi QL, Chun K, Patterson B, Brien B. Extramedullary infiltrates of AML are associated with CD56 expression, 11q23 abnormatlities and inferior outcome. Leuk Res 2004; 28 : 1007-1011.
26. Holmes R, Keating MJ, Cork A, et al. A unique pattern of central nervous system leukemia in acute myelomonocytic leukemia associated wth inv(16) (p13q22). Blood 1985; 65 : 1071-1078.
27. King A, Burrows T, Loke YW. Human uterine natural killer cells. Nat Immun 1996-97; 15 : 41-52.
Labels
Haematology Internal medicine Clinical oncology
Article was published inTransfusion and Haematology Today

2011 Issue 3-
All articles in this issue
- Léčebná studie Relapsed AML 2001/01, 02 pro děti s relapsem akutní myeloidní leukemie nebo primárně rezistentní nemocí zlepšila jejich naději na vyléčení
- Úloha alogenní transplantace buněk krvetvorby v léčbě získané aplastické anémie u dětí – zkušenost v České republice v letech 1991–2007
- Nežádoucí reakce při odběru hemopoetických kmenových buněk u nepříbuzných dárců – desetiletá zkušenost Českého národního registru dárců dřeně (ČNRDD)
- Transformace folikulárního lymfomu – výjimka nebo pravidlo? Přehledný článek a vlastní výsledky
- Symptomatický myeloidný sarkóm uteru v čase diagnózy akútnej myeloblastovej leukémie – kazuistika
- Kazuistika závažné pancytopenie s dominující megaloblastovou anémií malnutriční etiologie
- Transfusion and Haematology Today
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nežádoucí reakce při odběru hemopoetických kmenových buněk u nepříbuzných dárců – desetiletá zkušenost Českého národního registru dárců dřeně (ČNRDD)
- Kazuistika závažné pancytopenie s dominující megaloblastovou anémií malnutriční etiologie
- Transformace folikulárního lymfomu – výjimka nebo pravidlo? Přehledný článek a vlastní výsledky
- Symptomatický myeloidný sarkóm uteru v čase diagnózy akútnej myeloblastovej leukémie – kazuistika
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career