-
Medical journals
- Career
Výhodné vlastnosti gestodenu a jejich využití v kombinované hormonální antikoncepci
: Tomáš Fait
: Gynekologicko-porodnická klinika 1. LF UK a VFN Praha, přednosta prof. MUDr. Alois Martan, DrSc.
: Prakt Gyn 2014; 18(2): 110-113
: Gynecology and Obstetrics: Review Article
Gestoden je derivát 19-nortestosteronu a gonanu s nulovou reziduální androgenní aktivitou. Je řazen do 3. generace progestinů. Monofázická kombinace 20 µg EE a 75 µg GSD je v klinické praxi vyzkoušenou antikoncepcí s vysokou účinností a vysokou kompliancí pacientek. Ta je dána studiemi ověřenou metabolickou neutrálností, minimálním rizikem změn tělesné hmotnosti, nulovými změnami krevního tlaku, dostatečným antiandrogenním efektem a výbornou kontrolou pseudomenstruačního cyklu.
Klíčová slova:
gestoden – kombinovaná perorální antikoncepceÚvod
Kombinovaná hormonální antikoncepce (combinated hormonal contraception – CHC) je chemicky směs estrogenu a progestinu, proto se také používá výraz estrogen-gestagenní antikoncepce.
Mechanizmus jejího účinku je kombinovaný. Dominantní je inhibice ovulace ovlivněním zpětných vazeb v ose hypotalamus – hypofýza – ovarium, přidává se vliv progestinu na motilitu vejcovodů, trofiku sliznice a cervikální hlen.
Pearlův index CHC je udáván mezi 0,0 a 0,4 při bezchybném užívání, které však není samozřejmostí.
Cílená volba dávky etinylestradiolu a gestagenní složky je základem pro možnost úplného využití antikoncepčního a neantikoncepčního potenciálu CHC u dané pacientky.
Každý nový preparát s sebou přináší prohloubení možnosti individuálního výběru antikoncepční metody. Při hodnocení relativních kontraindikací je vždy nutno kalkulovat s možností nežádoucího otěhotnění, které je, odhlédneme-li od etické stránky věci, svými hormonálními změnami výrazně nebezpečnější než u kteréhokoli ze soudobých antikoncepčních preparátů [1].
Gestoden
Progestiny v CHC lze označit jako reziduálně androgenní (noretisteron, lynestrenol, levonorgestrel), slabě androgenní až s téměř nulovou reziduální androgenní aktivitou (desogestrel, gestoden, norgestimát) a antiandrogenní (cyproteronacetát, chlormadinonacetát, dienogest, drospirenon).
Na základě chemické struktury lze progestiny dělit na deriváty 17α-hydroxyprogesteronu (cyproteronacetát a chlormadinonacetát) a 19-nortestosteronu, které se dělí na estrany (noretisteron, lynestrenol, dienogest) a gonany (levonorgestrel, gestoden, desogestrel, norgestimát). Gestoden, desogestrel a norgestimát jsou pro svoji minimální androgenicitu řazeny mezi tak zvané progestiny 3. generace.
Osobně považuji za rozumné hovořit o jednotlivých progestinech dle jejich vlastností (tab. 1) a nikoli o generacích.
1. Vlastnosti progestinů 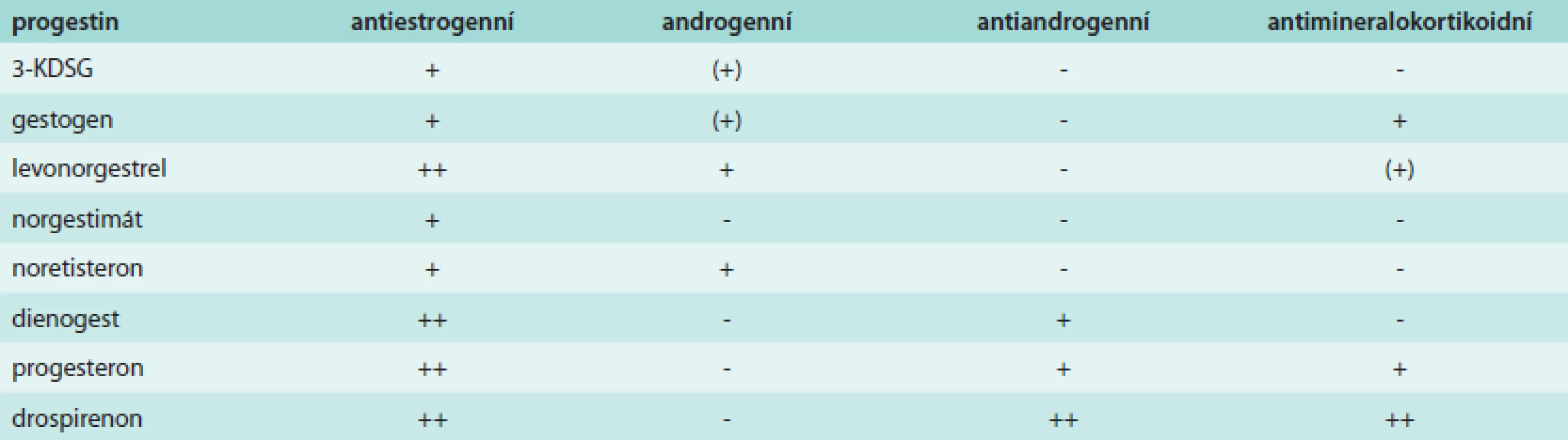
3-KDSG – 3-ketodesogestrel Gestoden (GSD) má 100% biologickou dostupnost. Z užívaných progestinů má nejvyšší gestagenní aktivitu a nulový estrogenní účinek. Má rovněž antimineralokortikoidní aktivitu, která se pohybuje na úrovni 20 % spironolaktonu. To je v klinické praxi důležité pro stabilitu hmotnosti uživatelek, neb víme, že většinou nárůst hmotnosti při užívání antikoncepce připadá na retenci tekutiny aktivací systému renin-angiotenzin. Stejně tak je této retenci tekutin přičítán vliv na projevy premenstruačního syndromu.
Gestoden nesnižuje etinylestradiolem indukovanou hladinu sexual hormone binding globulinu (SHBG). Vazba na SHBG je 65–75 %, na albumin 24–34 %. Hladiny SHBG jsou základem společného antiandrogenního působení veškeré CHC.
Maximální koncentrace (Cmax) je v plazmě dosaženo za 30 minut po perorálním podání. Biologický poločas gestodenu je 17 hodin, v kombinaci s etinylestradiolem se prodlužuje na 20 hod, což je podstatné pro zachování antikoncepčního účinku při chybě uživatelky [2].
Studie s antikoncepcí obsahující gestoden
Dominantním estrogenem CHC je stále etinylestradiol (EE). Má významné metabolické ztráty ve sliznici střeva a v játrech, a tak je biologická dostupnost při perorálním podání 38–48%. EE má silný antigonadotropní efekt a inhibuje vlastní 17β-hydroxylaci. Metabolizuje se v játrech pomocí cytochromu P450. Vylučován je ve formě glukuronidů a sulfátů. V plazmě se váže na albumin a jen 1 % cirkuluje volně. V kombinaci s gestodenem vzájemně příznivě ovlivňují svůj metabolizmus [3].
Příznivý vliv kombinace EE + GSD na hyperandrogenní stavy prokázala studie 33 žen ve věku 15–25 let, které po 13 cyklů užívaly trifázickou CHC s tímto progestinem. Došlo k 78% redukci počtu lézí u akné. Subjektivně vnímalo zlepšení 90 % žen. Hladina SHBG byla zvýšena o 229 % a hladina celkového testosteronu snížena o 40 %, volného pak o 90 % [4].
Užívání monofázické kombinace EE 20 µg + 75 µg GSD (Lindynette® tbl) hodnotil po 6 měsících užívání v souboru 302 žen průměrného věku 22,6 ± 6,8 Nikolov [5]. Nezaznamenal žádný vliv na krevní tlak (na začátku 106,6/67,9; po 3 měsících 106,8/68,0; po 6 měsících 106,4/68,5). Minimální vliv na tělesnou hmotnost (zvýšení o ≥ 2 kg ve 4,65 %, snížení o ≥ 2 kg v 6,31 %). Vedlejšími účinky byly nejčastěji bolesti hlavy (14 % uživatelek), nevolnost (3 %), napětí prsů (7 %) a emoční nestabilita (6 %). Celkovou snášenlivost hodnotilo 81 % žen jako skvělou a 17,5 % jako velmi dobrou.
Vysokou míru snášenlivosti a neutralitu k tělesné hmotnosti prokázal ve své studii srovnávající kombinaci 75 µg GSD s 20 µg a 30 µg EE Endrikat, který doporučuje vždy začínat s nižší dávkou EE a teprve při potížích s kontrolou menstruačního cyklu dávku navýšit [6]. Pro nežádoucí účinky včetně nepravidelností cyklu ukončilo předčasně studii pouze 9,8 % žen ze skupiny s 20 µg a 7,2 % ve skupině s 30 µg.
Vysokou komplianci k podávání potvrdila také polská [7] 6měsíční studie, kterou dokončilo 95,7 % žen bez jediného selhání a bez závažných vedlejších účinků.
Asi největší studie s 20 µg EE a 75 µg gestodenu byla koncipována jako otevřená a multicentrická. Po 36 měsíců sledovala soubor 670 žen ve věku 18–45 let, tedy vyhodnotila 19 095 cyklů. Dosáhla Pearlova indexu 0,07. Preparát byl obecně dobře tolerován. Nedošlo k významné změně hmotnosti ani krevního tlaku. Vysoce byla uživatelkami hodnocena dobrá kontrola cyklu [8].
Endrikat nadesignoval rovněž 2 studie, které srovnávaly kombinaci 20 µg EE + 75 µg gestodenu s kombinací 20 µg EE + 150 µg desogestrelu [9,10].
Roční studie publikovaná v roce 1995 [9] zahrnovala 469 žen (4 991cyklů). Prokázala nižší incidenci špinění a krvácení z průniku o 3,5 % v prvních 3 cyklech a o 7,6 % v prvních 6 cyklech ve prospěch gestodenu a stejně tak nižší incidenci dysmenorey (p = 0,001). Stejná byla incidence bolestí hlavy, napětí prsů a nauzey vedoucí v obou skupinách k přerušení užívání u 19 žen.
Novější opět roční studie hodnotila 1 476 žen (14 700 cyklů). Prokázala shodný pokles špinění z 35,1 % resp. 37,5 % na 10 % ve 4. cyklu. Zcela bez špinění bylo 84,7 % cyklů s gestodenem, resp. 82,5 % cyklů s desogestrelem. Amenoreu udávalo 2,7 %, resp. 2,9 % žen. Hmotnostní přírůstek < 2 kg udávalo shodně 83 % žen [10].
Bezpečnostní aspekty
Jediné významné riziko, které s sebou CHC přináší, jsou kardiovaskulární příhody.
Tromboembolická nemoc (TEN) se v populaci vyskytuje s incidencí 1 : 1 000 žen a rok, ve věku do 45 let jen 1 : 10 000 žen ročně. Kombinovaná hormonální antikoncepce je jedním z nejčastějších získaných rizikových faktorů. Příčina je vždy multifaktoriální. Nejčastěji musíme myslet na riziko TEN u uživatelek CHC při znehybnění po operaci či při dlouhé imobilitě a v kombinaci s dalšími rizikovými faktory.
Relativní riziko tromboembolické nemoci u uživatelek CHC je 2–4. Je nutno toto riziko brát v úvahu přesto, že pouze 1–2 % těchto příhod končí fatálně.
Jednou z cest jak snížit riziko TEN při užívání CHC je snižování dávky EE. Dávky nižší než 50 µg nesou nižší riziko než v 70. letech používané vyšší dávky. Většina studií neprokázala již další snižování rizika při poklesu dávky EE pod 35 µg (nízkodávkovaná CHC).
Riziko TEN je ovlivněno i užitým progestinem. Diskuse na toto téma jsou stále živé. V roce 1995 byly publikovány 3 studie prokazující vyšší riziko při užití progestinů 3. generace oproti generaci 2. Jick prokázal kohortovou analýzou RR 1,9, analýzou případů a kontrol 2,3 pro progestiny 3. generace oproti 2. generaci. V roce 2001 EMEA uzavírá diskusi reanalýzou, z které vyplývá, že riziko u 3. generace je 1,5–2krát vyšší, tedy incidence se zvýší z 20/100 000 na 30–40/100 000 [1]. A tedy ani recentní „Přímé sdělení pro pracovníky ve zdravotnictví“, které na příkaz SÚKL rozeslali držitelé rozhodnutí o registraci CHC, nepřináší novější informaci.
Relativní riziko infarktu myokardu pro uživatelky CHC je 2–3,2. Prakticky není zvýšeno u žen do 35 let věku. Nicméně v kombinaci s kouřením se situace razantně mění, u kuřaček pod 35 let věku je relativní riziko 10, nad 35 let věku 120. Zavedení progestinů 3. generace do praxe vedlo k rozšíření preskripce CHC i do rizikových skupin žen díky snížení rizika infarktu myokardu. Hypertenze a kouření jsou nejvýznamnějšími rizikovými faktory, které podání CHC násobí [1]. Podkladem pro vyšší bezpečnost progestinů 3. generace je to, že potencují zvýšení HDL-cholesterolu indukované etinyestradiolem.
Holistický přístup
Při výběru antikoncepce pro konkrétní ženu musíme samozřejmě zvažovat její zdravotní profil, profil přípravku a její osobní očekávání.
Ženy berou jako samozřejmost, že CHC bude účinná a bezpečná. Očekávají také co nejvíce z neantikoncepčních přínosů kombinované hormonální antikoncepce (tab. 2).
2. Neantikoncepční přínosy CHC 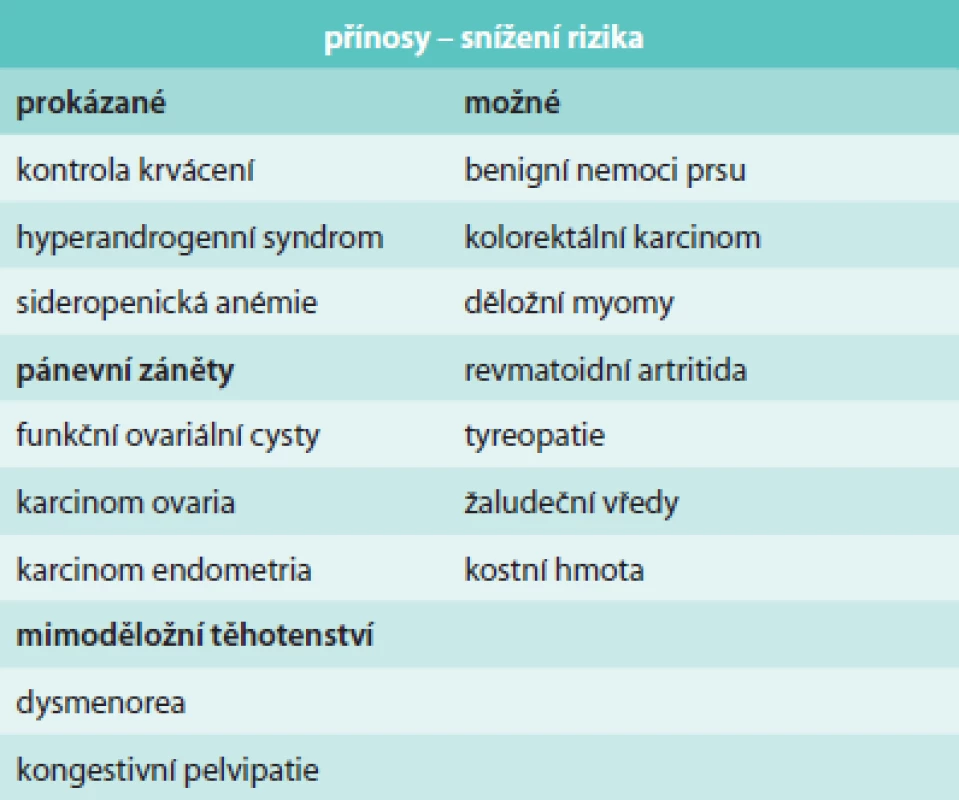
Monofázické přípravky umožňují kontinuální, nejčastěji 3–6 měsíční podávání, které má své indikace.
Indikace ke kontinuálnímu užívání CHC
- endometrióza
- premenstruační syndrom
- hyperandrogenní syndrom
- dysmenorea, hypermenorea, dysfunkční krvácení
- hematologické nemoci (krvácivé poruchy, anémie)
- katemeniální epilepsie a další neurologické potíže vázané na menstruační cyklus
- mentální postižení
- ochrana gonád při chemoterapii
- přání pacientky
Závěr
Gestoden je derivát 19-nortestosteronu a gonanu s nulovou reziduální androgenní aktivitou. Je řazen do 3. generace progestinů.
Monofázická kombinace 20 µg EE a 75 µg GSD je v klinické praxi vyzkoušenou antikoncepcí s vysokou účinností a vysokou kompliancí pacientek. Ta je dána studiemi ověřenou metabolickou neutrálností, minimálním rizikem změn tělesné hmotnosti, nulovými změnami krevního tlaku, dostatečným antiandrogenním efektem a výbornou kontrolou pseudomenstruačního cyklu.
Doručeno do redakce dne 19. 2. 2014
Přijato po recenzi dne 11. 4. 2014
doc. MUDr. Tomáš Fait, Ph.D.
tfait@seznam.cz
Gynekologicko-porodnická klinika 1. LF UK a VFN, Praha
www.vfn.cz
Sources
1. Fait T. Antikoncepce. 2. vydání. Maxdorf: Praha 2012. ISBN 978–80–7345–280–3.
2. Kuhl H. Comparative pharmacology of newer progestogens. Drugs 1996; 51(2): 188–215.
3. Jung-Hoffmann C, Kuhl H. Interaction with the pharmacokinetics of ethinyelstradiol and progestogens contained in oral contraceptives. Contraception 1989; 40(3): 299–312.
4. Pierard-Franchimont G, Gaspard U, Lacante P et al. A quantitative biometrological assessment of acne and hormonal evaluation in young women using a triphasic low-dose oral contraceptive containing gestodene. Eur J Contracept Reprod Health Care 2000; 5(4): 275–286.
5. Nikolov A. Influence of the very low dose oral contraception on the blood presure, body weight, and general condition of the patients. Akush Ginekol (Sofia) 2009; 48(4): 11–16.
6. Endrikat J, Müller U, Düsterberg B. A twelve-month comparative clinical investigation of two low-dose oral contraceptives containing 20 micrograms ethinylestradiol/75 micrograms gestodene and 30 micrograms ethinylestradiol/75 micrograms gestodene, with respect to efficacy, cycle control, and tolerance. Contraception 1997; 55(3): 131–137.
7. Lech MM, Swiatek EJ. The effectiveness and acceptability of oral contraceptives (Logest), containing 20 micrograms ethinylestradiol and 75 micrograms gestodene. Ginekol Pol 2004, 75(3): 209–214.
8. Dusterberg B, Ellman H, Müller U et at. A three-year clinical investigation into efficacy, cycle control and tolerability of a new low-dose monophasic oral contraceptive containing gestodene. Gynecol Endocrinol 1996; 10(1): 33–39.
9. Endrikat J, Jaques MA, Mayerhofer M et al. A twelve-month comparative clinical investigation of two low-dose oral contraceptives containing 20 micrograms ethinylestradiol/75 micrograms gestodene and 20 micrograms ethinylestradiol/150 micrograms desogestrel, with respect to efficacy, cycle control and tolerance. Contraception 1995; 52(4): 229–235.
10. Endrikat J, Dusterberg B, Ruebig A et al. Comparison of efficacy, cycle control, and tolerability of two low-dose oral contraceptives in a multicenter clinical study. Contraception 1999; 60(5): 269–274.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inPractical Gynecology

2014 Issue 2-
All articles in this issue
- Interview with associated professor Michael J. Halaška, MD, PhD, about the role and the benefit of the ENYGO
- Advantageous properties of gestodene and its use in combined hormonal contraception
- Management of a pregnant woman with diabetes
- Role of ultrasound diagnostics in monitoring the pregnancy complicated by diabetes of a pregnant woman
- New laboratory diagnostic techniques and prediction of preeclampsia
- Jsou vaginálně aplikované izoflavony vhodnou náhradou estrogenů?
- Smoking cessation in pregnancy
- Smoking pregnant woman
- Sexuality in pregnancy
- Atypical findings in the diagnostics of precancer and cancer of cervix: case reports
- Partnership and sexual life in women with cancer
- Expert´s witness opinion in pediatric gynecology
- Burn-out syndrome – a critical view
- International Menopause Society – 14th World Congress on the Menopause
- Practical Gynecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Advantageous properties of gestodene and its use in combined hormonal contraception
- Atypical findings in the diagnostics of precancer and cancer of cervix: case reports
- Jsou vaginálně aplikované izoflavony vhodnou náhradou estrogenů?
- Smoking cessation in pregnancy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

