-
Medical journals
- Career
Plicní arteriovenózní malformace řešená videoasistovanou torakoskopickou lobektomií
Authors: I. Hanke 1; L. Maršík 1; V. Chovanec 2; M. Slanina 2; V. Koblížek 3
Authors‘ workplace: Kardiochirurgická klinika Lékařské fakulty Univerzity Karlovy v Hradci Králové a Fakultní nemocnice Hradec Králové 1; Radiologická klinika Lékařské fakulty Univerzity Karlovy v Hradci Králové a Fakultní nemocnice Hradec Králové 2; Plicní klinika Lékařské fakulty Univerzity Karlovy v Hradci Králové a Fakultní nemocnice Hradec Králové 3
Published in: Rozhl. Chir., 2020, roč. 99, č. 10, s. 467-471.
Category: Case Report
Overview
Plicní arteriovenózní malformace (PAVM) jsou tvořeny abnormálními spojkami mezi plicními tepnami a žílami, které obcházejí plicní kapilární řečiště a dopravují neokysličenou krev plicními žilami do levého srdce. To způsobuje nedostatečné okysličení krve v plicích. Postižení je dlouho bezpříznakové. Nejčastějšími symptomy jsou námahová dušnost, krvácení z nosu, zvýšená únavnost a postupně i cyanóza. Závažná komplikace je paradoxní embolizace do mozku projevující se jako cévní mozková příhoda nebo mozkový absces. Léčba onemocnění spočívá v embolizaci cévních spojek, chirurgické resekci postiženého plicního parenchymu a řešení dalších průvodních projevů postižení. Většina PAVM vzniká v důsledku autozomálně dominantně dědičné poruchy nazvané hereditární hemorhagická teleangiektázie.
Kazuistika: V našem sdělení chceme dokumentovat diagnostický a léčebný postup u mladého pacienta, kde byla PAVM diagnostikována po pádu z kola. Po komplexním vyšetření byla zjištěna AV malformace se 40% zkratem plicního řečiště. Vzhledem k typu a rozsahu postižení nebyla angiografická intervence vhodná. Proto byla indikována resekce postiženého plicního laloku videoasistovaně.
Závěr: Nález PAVM je raritní. U všech nemocných s projevy hereditární hemorhagické telengiektázie (HHT) na sliznici úst by měla být vyloučena PAVM. Metodou volby diagnostiky je sonografie srdce s kontrastem a CT hrudníku s kontrastem. Konzervativní nebo medikamentózní léčba nezlepšuje stav nemocného. Zpravidla je řešitelný embolizací. Pokud je PAVM většího rozsahu nebo difuzní, a tak nevhodný k endovaskulárnímu řešení, je dobře řešitelný endoskopickou resekcí v rozsahu postižení.
Klíčová slova:
pulmonary arteriovenous malformation – VATS lobectomy – embolization
Úvod
Plicní arteriovenózní malformace (PAVM) je tvořena abnormálním cévním spojením mezi plicní tepnou a žilou obvykle na subsegmentální úrovni. Neokysličená krev se tak plicním pravo-levým zkratem dostává přes levé srdce do systémové cirkulace. Tato anomálie byla poprvé popsána v roce 1897 [1]. Pacienti bývají zpočátku asymptomatičtí, ale s postupujícím věkem se pomalu zvětšuje velikost pravo-levého zkratu a objevují se první klinické obtíže. Nejčastěji jde o námahovou dušnost, epistaxi a postupně se prohlubující cyanózu [2].
Závažnou komplikací je cévní mozková příhoda nebo mozkový absces. U AV malformaci totiž dochází při absenci fyziologického filtru plicního kapilárního řečiště k paradoxní embolizaci trombů a bakterií do systémového řečiště [3].
85 % PAVM je na podkladě autozomálně dominantně dědičné vady – hereditární hemorhagické telengiektázie (HHT) [4]. PAVM mohou být i získané. Setkáváme se s nimi u pacientů s onemocněním jater (hlavně jaterní cirhózou), aktinomykózou, traumaty hrudníku nebo metastazující rakovinou štítné žlázy. Mohou se také vyskytovat u některých vrozených srdečních vad nebo vznikat jako důsledek jejich chirurgické korekce [5].
Historicky léčba spočívala v chirurgické resekci postiženého plicního parenchymu či u izolovaných píštělí v podvazu přívodné cévy z torakotomie. Po publikaci Porstmannem v roce 1977 [6] endovaskulární léčba pomocí embolizace metalickými spirálami postupně nahradila chirurgický přístup.
Kazuistika
Dvacetiletý muž se dostavil na chirurgickou ambulanci spádové nemocnice pro bolesti pohmožděného hrudníku po pádu z kola. Při vstupním vyšetření byl bez dušnosti, orientovaný, spolupracující, oběhově stabilní, se symetrickým dýcháním. Měl palpační bolestivost v levé polovině hrudníku, exkoriace na hrudníku a břiše, bez krepitace či hematomu v popsané oblasti. Vyšetřující lékař si všiml promodralých konečků prstů, které byly paličkové. Nativní skiagram hrudníku byl bez patologie. Pacientovi byla změřena saturace periferní krve a zjištěna hodnota 65 %. V laboratoři v krevním obraze změřeno erytrocytů 6,23 10 na12/l, hemoglobin 183 g/l, hematokrit 0,534. Stanoveny krevní plyny v kapilární krvi s nálezem pH 7,472, pO2 4,94 kPa, pCO2 3,80 kPa, BE -2,1. Při podrobnějším pátrání v anamnéze bylo pacientem upřesněno, že již od dětství měl namodralé zabarvení pokožky při fyzické aktivitě. Doma ani u dětského lékaře to nikdo neřešil. Pacient kouřil deset cigaret denně od 13 let, od 15 let věku ještě i marihuanu.
Provedené CT s kontrastem (Obr. 1, 2) zobrazilo rozvinuté plíce, bez pneumothoraxu či fluidothoraxu a žádné traumatické změny na skeletu hrudníku. Zřetelně viditelné byly atypické, rozšířené, mnohočetné cévní struktury pravého dolního laloku. Bylo vysloveno podezření na cévní anomálii s možnými AV zkraty.
Image 1. CT plic − transverzální řez v plicním okně: prokazuje atypické, rozšířené, mnohočetné cévní struktury pravého dolního laloku
Fig. 1: CT scan of the lungs, transverse cut in the pulmonary window: atypical, enlarged, multiple vascular structures of the lower right lobe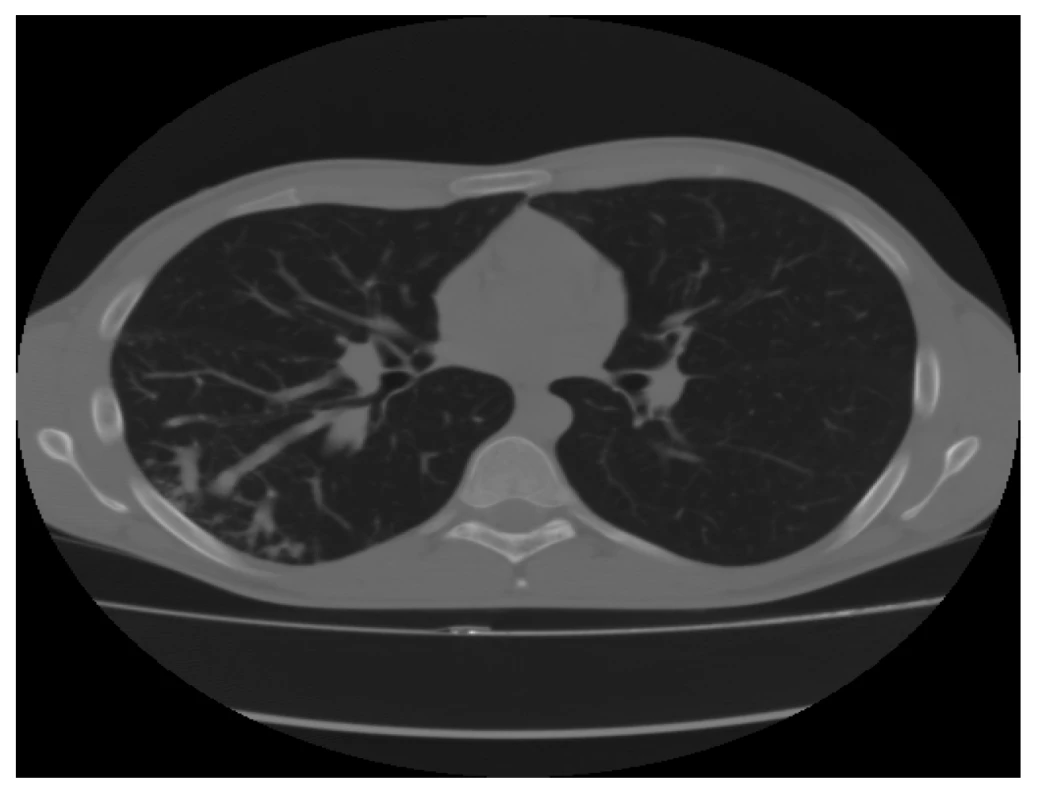
Image 2. CT plic − koronální rekonstrukce v plicním okně: dilatované plicní řečiště pravého dolního laloku
Fig. 2: CT scan of the lungs, coronal reconstruction in the pulmonary window: dilated pulmonary vasculature of the right lower lobe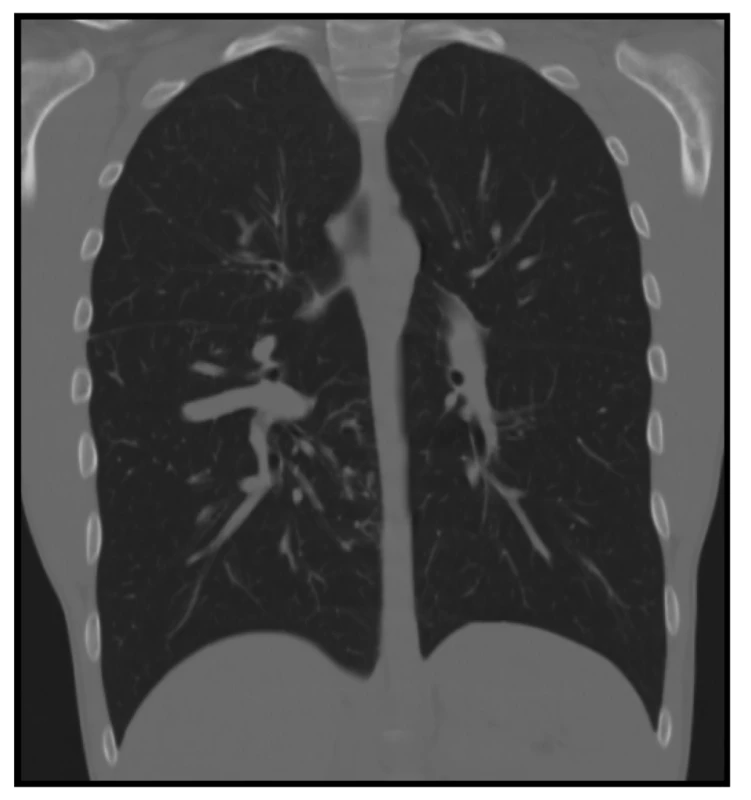
Pacient byl přeložen na plicní oddělení krajské nemocnice. ECHO srdce neprokázalo patologii, na EKG v klidu byla popsána sinusová tachykardie 112 za minutu.
Pro hematokrit 0,534 a hladinu hemoglobinu 183 g/l byla, po konzultaci s hematologem, provedena venepunkce 250 ml žilní krve.
V klidu s 5 litry O2 se saturace krve upravila na 92 %. Byla stanovena diagnóza respirační insuficience 1. typu. Nemocný byl přeložen k došetření AV píštělí v pravém dolním laloku do fakultní nemocnice.
Po překladu podstoupil plicní angiografii. Ta prokázala difuzní cévní postižení v oblasti dolního plicního laloku vpravo s mnohočetnými převážně drobnými AV zkraty − primárně nevhodnými k embolizační léčbě (Obr. 3).
Image 3. Plicní angiografie zobrazující difúzní postižení dolního plicního laloku vpravo s mnohočetnými převážně drobnými AV zkraty
Fig. 3: Pulmonary angiography: diffuse involvement of the right lower lobe with multiple, predominantly minor AV shunts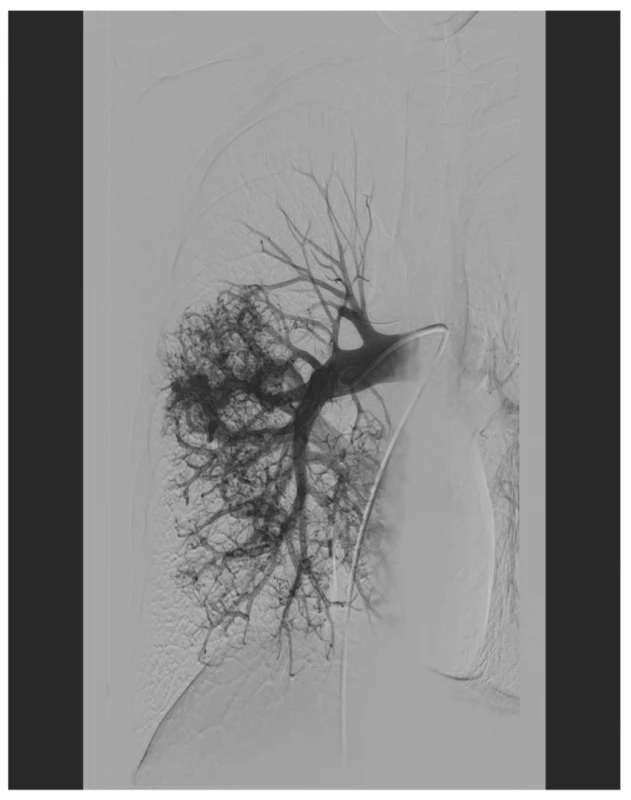
Ke kvantifikaci významnosti pravo-levého zkratu byla provedena celotělová scintigrafie s 99mTc-MAA: s nálezem významného P-L zkratu ve 40,5 % (u zdravých osob je okolo 5 %).
Funkční vyšetření plic neprokázalo obstrukční ani restrikční ventilační poruchu. Byla prokázána lehká plicní hyperinflace (RV 157 %, RV/TLC 35 %). Transfer faktor a transfer koeficient byly středně těžce omezeny (TLco 40 %, Kco 49 %). Index plicní hypertenze (VCmax%/TLco% = 2,17) byl zvýšený.
Byla provedena jícnová echokardiografie s podáním echokontrastu − 2×20 ml Gelaspanu. S latencí 5–7 sekund kontrast masivně pronikal do levostranných oddílů. Šlo o jasný průkaz pravo-levého zkratu. Perzistující foramen ovale či jiný intrakardiální zkrat byl při vyšetření vyloučen.
Vzhledem k nevhodnosti embolizační léčby (mnohočetné postižení celého laloku), námahou se prohlubující hypoxemii, minimální odezvě na kyslíkovou terapii s přihlédnutím k lokalizaci PAVM změn omezených na jeden plicní lalok bylo na mezioborovém indikačním semináři rozhodnuto o provedení VATS dolní lobektomie. Operace byla provedena v celkové narkóze kombinované s epidurální anestezií při selektivní intubaci a separované ventilaci plic. Na dolním laloku bylo vidět patologickou vaskularizaci a girlandovitě zmnoženou vaskulaturu s maximem v šestém segmentu. S pomocí harmonického skalpelu a staplerů byla provedena dolní lobektomie. Saturace krve O2 se ihned upravila na 98 %. Peroperační krevní ztráta byla 200 ml. Během operace trvající 155 minut nedošlo k žádným komplikacím.
Na jednotce intenzivní péče byla analgezie u dlouhodobého uživatele marihuany vedena cestou epidurálního katétru. Drobný únik vzduchu z hrudního drénu postupně ustal. Pro nespolupráci pacienta dochází opakovaně k dislokaci drénu, proto hospitalizace prodloužena na 2 týdny.
Na ambulantní kontrole po osmi dnech se pacient cítil dobře. Na nativním skiagramu hrudníku byla plíce s reziduálním drobným PNO v apexu pravého hemitoraxu. Na kontrolním CT plic (Obr. 4) provedeném po dvou měsících byla zobrazená plíce zcela rozvinuta, bez známek přetrvávajících viditelných AV píštělí či abnormalit v cévním utváření zbylého plicního parenchymu.
Image 4. CT plic nativní, koronální rekonstrukce v plicním okně po operaci: zobrazující plíce zcela rozvinuté bez patologického rozšíření cévních struktur, bez známek přetrvávajících viditelných AV píštělí či abnormalit v cévním řečišti zbylého plicního parenchymu
Fig. 4: Native CT scan of the lungs, coronal reconstruction in the pulmonary window after surgery: lungs completely expanded without any pathological dilation of the vascular structures, without any signs of persistent visible AV fistulas or abnormalities of the remaining pulmonary parenchyma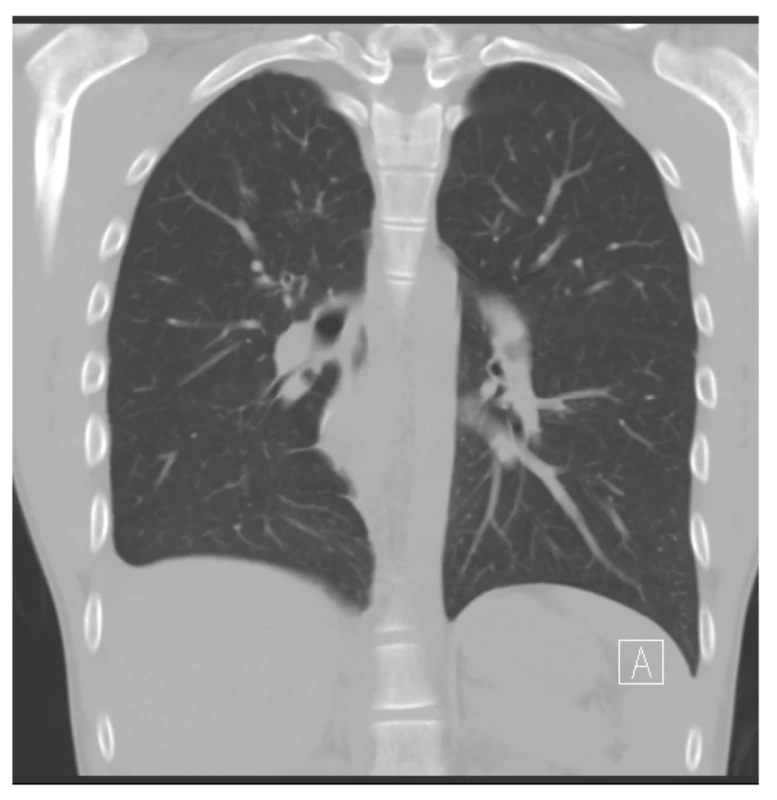
Patolog popsal fokální známky čerstvého i staršího alveolárního krvácení ve formě kumulace siderofágů. V parenchymu zastiženy drobné uzliny bez patologického mikroskopického nálezu. Nález je kompatibilní s klinickým údajem cévní malformace (výrazně dilatované plicní žíly).
Diskuze
PAVM byla poprvé popsána na pitvě Churtonem v roce 1897 [1]. Přibližně 80–90 % všech PAVMs je asociováno se syndromem Rendu-Osler-Weber neboli hereditární hemorhagickou teleangiektázií (HHT), přičemž okolo 15–35 % nemocných s HHT má prokázanou PAVM [5]. Jedná se o fibrovaskulární dysplazii s autozomálně dominantní dědičností a prevalencí přibližně 1 : 5000 v celosvětovém měřítku [4]. HHT je charakterizována přítomností teleangiektázií a arteriovenózních malformací kůže, sliznic a vnitřních orgánů s familiárně vázaným výskytem. Pro stanovení diagnózy HHT byla v roce 2000 přijata mezinárodní klinická kritéria, která zahrnují pozitivní rodinnou anamnézu, opakované epizody epistaxí, výskyt mnohočetných teleangiektázií a viscerální příznaky (teleangiektázie v gastrointestinální trubici, arteriovenózní malformace v oblasti jater, mozku a míchy). Přítomnost 3 a více příznaků činí diagnózu jednoznačnou. Pokud jsou přítomna jen 2 kritéria, je diagnóza pravděpodobná [3].
Podle anatomické charakteristiky uvedené v práci Meek, et al. jsou PAVMs klasifikovány následovně [7]:
jednoduché – nejčastěji zastoupené, s jedinou arterií zásobující malformaci;
komplexní – jsou zásobeny několika arteriemi;
difuzní – vzácné, charakterizovány stovkami malformací, s kombinací jednoduchých i komplexních.
Přibližně 15 % nemocných s PAVM nesplňuje kritéria HHT a nemá ani jinou systémovou nemoc. Mohou se vyskytnout následkem traumatu a u nemocných s jaterním postižením. Nemocní s kongenitální srdeční vadou, kdy systémový žilní návrat nezahrnuje žilní návrat z jaterních žil, mohou také vytvořit PAVM. Mohou vzniknout i v důsledku chronických infekcí jako schistosomóza, aktinomykóza, tuberkulóza a u metastazujícího karcinomu štítné žlázy [2]. Tyto PAVM mohou vzniknout jako komunikace mezi bronchiální arterií a plicní žilou − tyto vzácné formy, na rozdíl od klasických PAVM, mohou mít výraznou tendenci k hemoptýzám.
Incidence PAVM je nízká 2−3 na 100 000 obyvatel. Pokud se projeví příznaky, je důležité zahájit nezbytnou léčbu, aby se předešlo potenciálně katastrofickým neurologickým komplikacím. Klinické důsledky případné PAVM závisí na tíži pravo-levého zkratu. Pacienti mohou být zpočátku asymptomatičtí, ale s postupujícím časem se zvyšuje velikost pravo-levého zkratu a mohou se objevit první klinické obtíže (obvykle okolo 3.–4. dekády). Větší podíl neokysličené krve proudící skrz PAVM se může prezentovat jako hypoxemie, dyspnoe a cyanóza (obvykle u pacientů s rozsáhlými či vícečetnými PAVMs) [2]. V případě vzniku paradoxní embolizace nebo vzniku trombu in situ může dojít ke vzniku tranzitorní ischemické ataky, ischemického iktu či mozkového abscesu. Celkem 46 % všech pacientů s ojedinělou PAVM, 59 % s vícečetnými a skoro 70 % pacientů s difuzními PAVMs v minulosti prodělalo CMP nebo bylo léčeno pro mozkový absces [8].
Indikační kritéria k embolizační léčbě jsou symptomatické PAVM, neurologické komplikace a symptomatické léze s přívodnou cévou v průměru větším než 3 mm. Tento přístup má nižší morbiditu než tradiční chirurgický. Pokud dojde k progresi onemocnění, je možné endovaskulární intervenci opakovat [9]. Zavedení VATS operací opět oživilo chirurgický postup v léčbě PAVM. Uplatňuje se především při těžké alergii na kontrastní látku a u centrálně uložené PAVM. V případech, kde jde o mnohočetné léze a není endovaskulární přístup možný, je chirurgická resekce postižené oblasti metodou volby [10].
Chirurgicky je možné řešit průvodní komplikace endovaskulární léčby a i rekurence PAVM po provedené embolizaci. Pro pokles morbidity při VATS resekcích, a protože nabízí definitivní řešení, může být indikována u izolovaných periferních lézí i časně.
Ve shodě s kanadskými autory máme zkušenost, že u mladých nemocných dlouhodobě užívajících marihuanu se v perioperačním období často vyskytnou potíže při tlumení bolesti a současně nespavost. Proto se snažíme minimalizovat intravenózní podání opiátů a k analgetizaci volíme cestu epidurální anestezie katétrem, i když jde o minimálně invazivní výkon [11].
V naší nemocnici je v současnosti sledováno 20 nemocných s PAVM (4/5 postižených jsou ženy). U všech byla efektivní embolizační léčba, u třetiny bylo nutno ji opakovat pro progresi PAVM v jiné lokalitě. Kromě pacienta uvedeného v této kazuistice nebyl nikdo léčen operačně. Nejzávažnější, potenciálně fatální komplikace PAVM jsou v našem souboru způsobeny postižením mozku. Všechny takto nemocné je pro vysoké riziko rekurence choroby nezbytné trvale dispenzarizovat.
Závěr
Nález PAVM je raritní. U všech nemocných s projevy HHT na sliznici úst by měla být vyloučena PAVM. Metodou volby diagnostiky je sonografie srdce s kontrastem a CT hrudníku s kontrastem. Konzervativní nebo medikamentózní léčba nezlepšuje stav nemocného. Zpravidla je řešitelný embolizací. Pokud je PAVM většího rozsahu nebo difuzní, a tak nevhodný k endovaskulárnímu řešení, je dobře řešitelný endoskopickou resekcí v rozsahu postižení.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Ivo Hanke, PhD.
Kardiochirurgická klinika FN HK
e-mail: ivo.hanke@fnhk.cz
Sources
- Churton T. Multiple aneurysm of pulmonary artery. Br Med J. (Clin Res Ed). 1897;1 : 1223.
- Shovlin CL. Pulmonary arteriovenous malformations. Am J Respir Crit Care Med. 2014;190(11):1217−1228.
- Love BA. Pulmonary arteriovenous fistulae. Medscape Reference 2015. http://emedicine.medscape.com/article/900681-overview.
- Pulmonary arteriovenous fistula. MedlinePlus. 2014; https://www.nlm.nih.gov/medlineplus/ency/article/001090.htm.
- Porstmann W. Therapeutic embolization of arteriovenous pulmonary fistula by catheter technique. In: Kelop O, editor. Current concepts in pediatric radiology. Berlin, Springer 1977 : 23−31.
- Trakal L, Malý P, Marušincová I, et al. Plicní arteriovenózní malformace jako vzácná příčina ischemické cévní mozkové příhody. Ces Slov Neurol N. 2019;82(5): 571−573.
- Adla T, Pádr R, Polovinčák M, et al. Plicní arteriovenózní malformace Ces radiol. 2019; 73 (1):62.
- Bakhos CT, Wang SC, Rosen JM. Contemporary role of minimally invasive thoracic surgery in the management of pulmonary arteriovenous malformations: report of two cases and review of the literature. J Thorac Dis. 2016;8(1):195−197.
- Meek ME, Meek JC, Beheshti MV. Management of pulmonary arteriovenous malformations. Semin Intervent Radiol. 2011;28(1):24–31. doi: 10.1055/s-0031-1273937.
- Krajina A, Koblizek V, Keller FS. Endovaskulární léčba plicních arteriovenózních zkratů. In: Krajina A, Peregrin JH. Intervenční radiologie – miniinvazivní terapie. Hradec Králové 2005 : 535−541.
- Liu CH W, Bhatia A, Buzon-Tan A, et al. Weeding out the problem: The impact of preoperative cannabinoid use on pain in the perioperative period. Anesth Analg. 2019;129 : 874–81.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2020 Issue 10-
All articles in this issue
- Využití mimotělních podpor v hrudní chirurgii
- Pooperační chylothorax − souhrnné sdělení
- Léčba insuficience hrudní anastomózy po Ivor Lewis ezofagektomii
- Maligní onemocnění po transplantaci plic
- Hypertermická peroperační intrapleurální chemoterapie a chirurgická cytoredukce jako součást multimodální léčby maligního mezoteliomu pleury – kazuistika
- Problematika plicních metastáz při pseudomyxomu peritonea – kazuistika a přehled literatury
- Plicní arteriovenózní malformace řešená videoasistovanou torakoskopickou lobektomií
- Minimalizace a maximalizace v hrudní chirurgii
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Pooperační chylothorax − souhrnné sdělení
- Hypertermická peroperační intrapleurální chemoterapie a chirurgická cytoredukce jako součást multimodální léčby maligního mezoteliomu pleury – kazuistika
- Maligní onemocnění po transplantaci plic
- Využití mimotělních podpor v hrudní chirurgii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

