-
Medical journals
- Career
Komplikace u pacientů po operaci pro plicní malignitu
Authors: L. Mitáš; T. Horváth; M. Sobotka; B. Garajová; I. Hanke; Z. Kala; I. Penka; J. Ivičič; J. Vomela
Authors‘ workplace: Chirurgická klinika FN Brno a LF MU, přednosta: prof. MUDr. Zdeněk Kala, CSc.
Published in: Rozhl. Chir., 2010, roč. 89, č. 2, s. 113-117.
Category: Monothematic special - Original
Overview
Cíl:
Rozbor příčin a četností komplikací klasických plicních resekcí pro malignitu.Metody:
Retrospektivní rozbor dokumentace 189 pacientů (128 mužů, 61 žen) s mediánem věku u mužů 61 let (rozpětí 21–78 let), u žen 64 let (rozpětí 33–80 let), kteří v období (2003–2007) podstoupili otevřený resekční zákrok plic pro malignitu. Data byla statisticky zhodnocena programem Statistica pomocí parametrů odds ratio a χ2 testu.Výsledky:
Komplikace byly rozděleny do 5 skupin. První skupinu tvoří 3 komplikace v perioperačním období (1,5 %): dysfunkce endotracheální kanyly, těžká srdeční arytmie, závažné krvácení. Druhá skupina zahrnuje komplikace v období 7 dnů po operaci: prodloužený únik vzduchu (PAL > 7dnů) 7,4 %, bronchopneumonie 6,9 %, lehká forma srdeční arytmie 6,9 %, pooperační delirium 4,2 %, atelektáza 2,6 %, infekce rány 1,1 %, krvácení 1,1 % a chylotorax 0,5 %. Ve třetí skupině jsme shromáždili osoby s následky pneumochirurgické intervence v období od 8. do 30. pooperačního dne: hrudní empyém 2,1 %, dysfonie 2,1 %, omalgie 1,1 %, infekce zažívacího traktu 0,5 % a insuficience sutury bronchu 0,5 %. Ve čtvrté skupině figurují 2 pacienti se závažnými příhodami vedoucími k úmrtí během 30 dnů od operace: ischemický iktus 0,5 % a plicní embolie 0,5 %. Pátá skupina představuje nemocné bez komplikací (60,5 %).Závěr:
Hlavními rizikovými faktory pro vznik komplikací v pooperačním průběhu po plicní resekci pro primární či sekundární plicní malignitu v našem souboru jsou CHOPN, kortikoterapie, délka operace nad 3 hodiny, BMI nad 25, levostranná lokalizace nádoru a operační výkon s bronchoplastikou. Pro vznik srdečních arytmií se jeví být rizikovými provedení pneumonektomie a předchozí neoadjuvantní radiochemoterapie.Klíčová slova:
chirurgické komplikace – pneumoonkochirurgie – plicní nádorÚVOD
Plicní resekce jsou standardní terapeutickou možností u většiny pacientů s časnými stadii nemalobuněčného plicního karcinomu, solitárních metastatických ložisek i benigních pulmonálních lézí. Resekce plic jsou řazeny mezi operace s vyšším rizikem pooperačních komplikací, které vedou ke zvýšení mortality [1]. Mortalita plicních resekcí se pohybuje v rozmezí 2–12 %, navzdory pokrokům v chirurgické technice, anestezii i perioperační péči [2]. Pneumonektomie pro maligní onemocnění je spojena se signifikantně zvýšenou morbiditou a mortalitou [3]. Mezi rizikové faktory plicních resekcí prokázané četnými studiemi patří věk, zhoršené ventilační funkce, kardiovaskulární komorbidity, tabakismus [3, 4]. Jeden z hlavních rizikových faktorů morbidity u pacientů s plicní resekcí jsou pooperační záněty. Bronchopneumonie, infekce rány a hrudní empyém jsou odpovědny za 11 až 46 % pooperačních infekčních komplikací u pacientů, kteří podstoupili operaci plic [5].
V současnosti i v oboru hrudní onkochirurgie nabývají na významu miniinvazivní přístupy reprezentované videoasistovanými a torakoskopickými operačními zákroky, které jsou spojeny se snížením inflamatorní odpovědi na operační inzult, nižším procentem komplikací, zkrácením doby hospitalizace, nižší spotřebou analgetik, lepším kosmetickým efektem, čili nižší zátěží pro pacienta [6, 7]. Další miniinvazivní metodou hlásící se ke slovu je robotická chirurgie, relevantních dat z této problematiky je však zatím málo [8].
MATERIÁL A METODA
Retrospektivní studium údajů pacientů operovaných pro primární či sekundární plicní malignitu na Chirurgické klinice FN Brno od 1. 1. 2003 do 31. 12. 2007.
Diagnóza byla stanovena podle RTG snímku – v rámci preventivní nebo dispenzární prohlídky, v některých případech jako náhodný nález. U symptomatických pacientů s dušností, kašlem, bolestmi na hrudi, pleurálním výpotkem, recidivujícími infekty dýchacích cest či s hemoptýzou během došetřování příčiny stavu.
Následně byl stav verifikován pomocí výpočetní tomografie hrudníku (CT), pozitronové emisní tomografie (PET), odběrem vzorku na histologické nebo cytologické vyšetření při bronchoskopii, eventuálně biopsií pod CT kontrolou.
Operace byly provedeny čtyřmi hrudními chirurgy, přístupem do hrudníku byla standardně anterolaterální torakotomie. Podle peroperačního nálezu a možnosti rozsahu resekce podle funkčního vyšetření byla provedena onkologicky radikální resekce s mediastinální lymfadenektomií. Po operaci byly založeny 1 či 2 hrudní drény v závislosti na peroperačním nálezu a zvyklostech operatéra. S výjimkou pneumonektomie byly hrudní drény po převozu pacienta na jednotku intenzivní péče (JIP) napojeny na aktivní sání standardně o intenzitě 20 cm vodního sloupce. U více než dvou třetin pacientů (69 %) byl na sále v rámci předoperační přípravy zaveden epidurální katétr k tlumení pooperační bolesti a urychlení aktivní rehabilitace. Jakmile byl zřejmý pokles úniku vzduchu z operované plíce, byl hrudní drén sveden na spádovou drenáž. V případě, že sekrece měla serózní charakter bez sanguinolentní příměsi a množství kleslo pod 100–150 ml/24 h byl drén vytažen.
Předoperačně byla u všech pacientů v rámci antibiotické profylaxe použita antibiotika ze skupiny cefalosporinů 2. generace v jedné dávce (single shot), která byla podána půl hodiny před operací v rámci anesteziologické přípravy. U pacientů byly sledovány následující parametry: věk, pohlaví, typ operace, lokalizace postižení, histologický nález, délka trvání hrudní drenáže, komplikace v pooperačním období, použití stapleru k resekci, nutnost rozrušování adhezí mezi viscerální a parietální pleurou, antibiotická terapie, délka hospitalizace, přidružená onemocnění, kouření v anamnéze.
Do zkoumaného souboru byli zařazeni pouze pacienti, u nichž měla operace kurativní záměr.
Data byla statisticky zhodnocena programem Statistica pomocí parametrů odds ratio (OR) a chí kvadrát testur (χ2).
VÝSLEDKY
Celkem 189 pacientů operovaných pro primární nebo sekundární plicní malignitu na Chirurgické klinice FN Brno v letech 2003–2007 představuje 128 mužů s mediánem věku 61 let (rozmezí 21–78 let) a 61 žen s mediánem 64 let (rozmezí 33–80 let). V distribuci výkonů figuruje 96 lobektomií, 21 bilobektomií, 18 pneumonektomií, 8 rozšířených pneumonektomií, 36 klínovitých resekcí a 10 segmentektomií.
Histologie shledala 56 spinocelulárních karcinomů, 45 adenokarcinomů, 10 velkobuněčných karcinomů, 6 karcinoidů, 44 plicních metastáz a 28 nálezů bylo zařazeno do skupiny ostatní. Metastatická onemocnění reprezentují adenokarcinom ledvin, prsu, gastrointestinálního traktu – GIT, prostaty, Ewingův sarkom, hemangiopericytom, maligní melanom, teratom varlat, cholangiocelulární karcinom a karcinom močového měchýře. Do skupiny ostatní byly zařazeny karcinomy s nižší četností výskytu: pleomorfní, brochioloalveolární, adenoskvamózní, bazaloidní, nediferencovaný, kulatobuněčný liposarkom, folikulární lymfom a několik případů malobuněčného karcinomu.
Anamnesticky bylo v době operace 39 mužů a 16 žen aktivními kuřáky. 54 mužů a 12 žen zanechalo kouření déle než 8 týdnů před operací a 35 mužů a 33 žen byli nekuřáci.
Table 1. Výskyt komplikací u jednotlivých typů operací Tab. 1. Complication rates in individual types of surgery 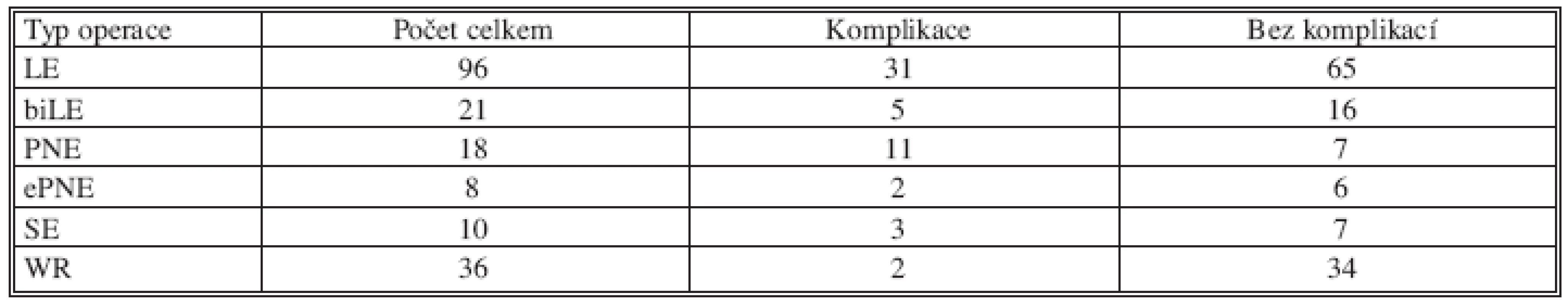
LE – lobektomie, biLE – bilobektomie, PNE – pneumonektomie, ePNE – rozšířená pneumonektomie, SE – segmentektomie, WR – klínovitá resekce Table 2. Výskyt jednotlivých rizikových faktorů ve skupině s komplikacemi a bez komplikací Tab. 2. Risk factors in a group with complications and in a group without complications 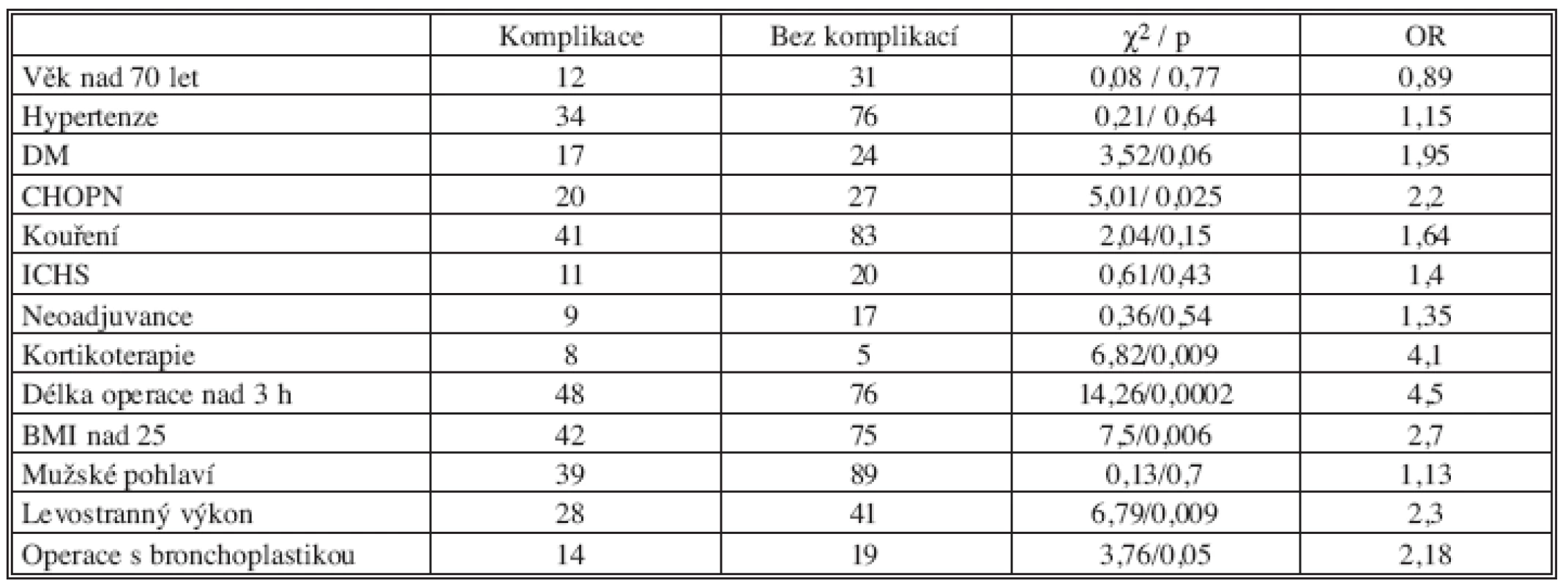
DM – diabetes mellitus, CHOPN – chronická obstrukční plicní nemoc, ICHS – ischemická choroba srdeční, BMI – body mass index, OR – odds ratio Komplikace byly rozděleny do 5 skupin:
První skupinu tvoří tři závažné peroperační komplikace (1,5 %) s přímým ohrožením života nemocných. Prvním případem byla náhlá dysfunkce endotracheální kanyly s poruchou ventilace levé plíce ve fázi částečného ošetření vaskulatury pravého horního plicního laloku. Dále těžká srdeční arytmie vyprovokovaná mechanickým útlakem srdce při obtížném, rozsáhlou levostrannou retetorakoplastikou vynuceném sternotomickém přístupu k centrální metastáze sarkomu měkkých tkání stěny hrudní do levé plíce. Třetí událostí v této skupině bylo proříznutí ligatury kmene arteria pulmonalis po levostranné pneumonektomii ještě na operačním sále krátce po uzavření torakotomie.
Druhá skupina zahrnuje komplikace v období 7 dnů po operaci, kam řadíme: prodloužený únik vzduchu (PAL > 7 dnů) 7,4 %, bronchopneumonii 6,9 %, lehké formy srdeční arytmie 6,9 %, pooperační delirium 4,2 %, atelektázu 2,6 %, infekce rány 1,1 %, krvácení 1,1 % a chylotorax 0,5 %. Ve třetí skupině jsme shromáždili osoby s událostmi diagnostikovanými v období od 8. do 30. pooperačního dne: hrudní empyém 2,1 %, přechodná dysfonie 2,1 %, bolesti ramene 1,1 %, infekce trávicího traktu 0,5 % a insuficience sutury bronchu 0,5 %.
Ve čtvrté skupině figurují 2 pacienti se závažnými příhodami vedoucími k úmrtí během 30 dnů od operace: ischemický iktus 0,5 % a plicní embolie 0,5 %.
Pátá skupina představuje nemocné bez komplikací (60,5 %).
Komplikace můžeme z hlediska závažnosti rozdělit do 2 skupin: velké (tzn. ohrožující pacienta na životě) a malé.
Do skupiny velkých komplikací (16,2 %) řadíme bronchopneumonii, atelektázu, krvácení, chylotorax, hrudní empyém, insuficienci sutury bronchu, úmrtí na ischemický iktus a plicní embolizaci. Zbývajících 23,3 % řadíme do skupiny malých komplikací.
Celkem 70 případů komplikací se vyskytlo u 54 pacientů (tzn. 28,6 % z celkového počtu), více než jedna komplikace se vyskytla u 12 pacientů (6,3 % z celkové počtu operovaných osob).
Z rizikových faktorů byly sledovány věk, kouření v anamnéze, neoadjuvantní radio - či chemoterapie, kortikoterapie, délka operace, operace s bronchoplastikou, absence epidurální analgezie nebo její ukončení v průběhu 0. či 1. pooperačního dne pro dysfunkci, BMI (Body Mass Index), komorbidity (ischemická choroba srdeční – ICHS, arteriální hypertenze, diabetes mellitus či porucha glukózové tolerance).
V tabulce 2 je statistické zhodnocení výskytu jednotlivých rizikových faktorů ve skupině s komplikacemi a bez komplikací v perioperačním nebo pooperačním průběhu.
DISKUSE
Komplikace v pooperačním období jsou obávanou příhodou v každém chirurgickém oboru. Některé z těchto komplikací jsou natolik závažné, že ohrožují pacienta na životě. Plicní primární a sekundární malignity se obvykle vyskytují u pacientů ve vyšším věku s četnými komorbiditami, proto je u těchto pacientů v případě komplikovaného pooperačního průběhu prognóza závažná.
Komplikace u polymorbidních pacientů lze v pooperačním průběhu očekávat. Proto klademe důraz na důslednou předoperační přípravu, operační techniku i pooperační zajištění pacienta. I přesto někdy dochází k nepředvídatelným komplikacím deklarovaným v první skupině.
U nich pak záleží na zkušenostech a sehranosti operačního týmu, anesteziologa a technickém vybavení.
Jednou z nejvýznamnějších skupin komplikací po operaci plicní malignity jsou komplikace plicní: bronchopneumonie, PAL, atelektáza, plicní embolizace, dále ARDS – syndrom dechové tísně dospělých, pneumotorax, bronchospazmus a aspirační pneumonie.
V práci Patela a spol. představují plicní komplikace 25 % všech případů s mortalitou 7,5 %. Jako nezávislé rizikové faktory jsou prezentovány hodnoty ASA (klasifikace Americké společnosti anesteziologie) ≥ 3, délka operace nad 80 minut a nutnost pooperační umělé plicní ventilace delší než 48 minut [4]. Četnost plicních komplikací v našem souboru je 17,4 % s mortalitou 1 % (2 případy). Příčinou prvního úmrtí byla plicní embolizace u staršího pacienta po pneumonektomii, ve druhém případě se jednalo o abscedující bronchopneumonii u kortikodependentní pacientky.
K faktorům nepříznivě ovlivňujícím pooperační průběh z hlediska výskytu možných komplikací jsou řazeny preexistující plicní onemocnění, resekční výkon s bronchoplastikou, FEV1 (usilovně vydechnutý objem za první sekundu) < 80 %, rozšířené resekce, typ plicní resekce, výskyt komorbidit a neoadjuvantní chemoterapie [9]. V našem souboru bylo provedeno celkem 33 výkonů s bronchoplastikou, z nichž 14 případů bylo ve skupině komplikovaných pacientů (25,9 % z provedených operací v této skupině) a 19 ve skupině pacientů bez komplikací v pooperačním průběhu (14,1 % z celkového počtu operovaných pacientů bez komplikací).
Mortalita resekčních zákroků pro malignitu plic se v 30denním intervalu pohybuje kolem 4,4 %. Mužské pohlaví, vyšší věk (70–79 let), nádor na pravé straně a rozsáhlé výkony (pneumonektomie) byly identifikovány jako rizikové faktory mortality v pooperačním období [10].
Třicetidenní mortalita našeho souboru pacientů dosáhla 1 % (2 pacienti), v obou případech se jednalo o muže. U jednoho byla provedena lobektomie, u druhého pneumonektomie, v obou případech pro spinocelulární karcinom. Příčinou úmrtí v prvním případě byla ischemická cévní mozková příhoda, ve druhém pak masivní plicní embolizace po proběhlé pneumonektomii.
V souboru 30denní mortality nefiguruje kortikodependentní pacientka po operaci mozkové metastázy plicního karcinomu, která byla následně operována na naší klinice pro plicní origo. Pooperační průběh byl komplikován oboustrannou abscedující bronchopneumonií, na kterou pacientka zemřela 46. den po operaci. Na nízké mortalitě našeho souboru má podíl profesní dovednost intenzivistů na chirurgické JIP a spolupráce s lékaři Kliniky anesteziologie, resuscitační a intenzivní medicíny (KARIM) naší nemocnice.
V práci Duguea se četnost časných pooperačních komplikací pohybuje kolem 32,4 %. Vyšší morbidita byla pozorována u pacientů s preexistujícím cévním onemocněním, inzulin dependentním diabetem a u pacientů po pneumonektomii. Mortalita v tomto souboru pacientů byla 6,6 % a byla vyšší u pacientů s preexistujícím vaskulárním onemocněním a po podstoupené pneumonektomii [11]. V našem souboru bylo provedeno 26 pneumonektomií (z toho 8 rozšířených) přičemž mortalita u této operace byla 3,6 %. Některé publikované práce uvádějí mortalitu u pneumonektomií 6,8 % [12], jiná prezentuje 30denní mortalitu tohoto výkonu dosahující 9,3 % [13].
Prodloužený únik vzduchu po plicní resekci zůstává častou komplikací, která může vést ke vzniku závažných stavů např. hrudnímu empyému, a vede k prodloužení nutné délky hrudní drenáže a pooperační hospitalizace [14].
Provedli jsme celkem 117 lobektomií – LE (z toho 21 bilobektomií). PAL se vyskytl celkem u 14 pacientů z toho u 12 osob po LE, což odpovídá 10,25 % z provedených LE. Brunelli se spoluautory uvádí četnost PAL 15,6 % po provedené lobektomii. Nezávislými rizikovými faktory pro vznik PAL jsou v této práci prezentovány snížená předpovídaná pooperační FEV1, přítomnost pleurálních adhezí a horní resekce [14].
Schussler se spolupracovníky studovali příčiny vzniku pooperační bronchopneumonie u pacientů po resekci plic a z výsledků vyplývají jako hlavní rizikové faktory mužské pohlaví, CHOPN (chronická obstrukční plicní nemoc) II. stupně, provedená lobektomie nebo bilobektomie a bronchiální kolonizace patogeny z peroperačně odebraného stěru [15]. V našem souboru pacientů s bronchopneumonií bylo 69 % mužů, CHOPN se vyskytoval u 30,7 % pacientů a ze 13 provedených operačních zákroků bylo provedeno 9 lobektomií, 2 bilobektomie a po 1 pneumonektomii a klínovité resekci.
Kortikoterapie podle výsledků naší práce patří mezi statisticky významné rizikové faktory pro vznik komplikací, a to především infekčních. Souvislosti této skutečnosti jsou multifaktoriální, jistě však na nich participuje imunosupresivní účinek této medikace.
Podle našich výsledků je levostranný výkon statisticky významným rizikovým faktorem. Významnost této skutečnosti bude muset být ověřena rozšířením souboru či dalšími pracemi. Z citovaných prací je pravostranný výkon nezávislým rizikovým faktorem mortality v 30denním intervalu pneumoonkochirurgických intervencí [10].
Vliv hodnoty BMI na perioperační komplikace v hrudní chirurgii byl sledován například japonskými autory [16]. Ve skupině obézních pacientů (BMI ≥ 30) byl signifikantně vyšší výskyt kardiovaskulárních komorbidit (hypertenze, ICHS), ve skupině s podváhou (BMI < 18) byl naproti tomu zvýšen výskyt plicního emfyzému a onemocnění ledvin. Ve skupině obézních pacientů byla signifikantně prodloužena doba extubace po operaci, délka hospitalizace a byl vyšší výskyt srdečních arytmií. Ve skupině s podváhou pak vyšší výskyt PAL. Mezi skupinami s podváhou, normální hodnotou BMI (18,5–24,9), nadváhou (BMI 25–29,9) a obézními nebyl shledán rozdíl v mortalitě, skupiny s podváhou a obézní pacienti však měli zvýšené riziko perioperačních komplikací.
Naproti tomu Smith a spol. nezjistili, že by přítomnost obezity zvyšovala incidenci perioperačních komplikací, mortalitu nebo délku hospitalizace po anatomické plicní resekci pro nemalobuněčný plicní karcinom [17].
V naší práci se hodnota BMI nad 25 stala statisticky významným faktorem pro komplikovaný pooperační průběh.
S narůstající délkou operačního zákroku stoupá riziko vyplývající z nežádoucích účinků celkové anestezie, dále riziko kontaminace operačního pole, kolonizace dýchacích cest patogeny a rizika plynoucí ze selektivní intubace. Aoki a kolektiv zabývající se plicními komplikacemi po chirurgické intervenci pro malignitu u pacientů starších 80 let prokázali delší operační čas jako jeden z rizikových faktorů pro vznik komplikací u této věkové skupiny [18]. V naší práci byla délka operace nad 3 hodiny vyhodnocena jako riziková se statistickou významností.
ZÁVĚR
Hlavními rizikovými faktory pro vznik komplikací v pooperačním průběhu po plicní resekci pro primární a sekundární plicní malignitu v našem souboru jsou CHOPN, kortikoterapie, délka operačního výkonu nad 3 hodiny, hodnota BMI nad 25, operační výkon s bronchoplastikou a levostranná lokalizace malignity. Pro vznik srdečních arytmií predisponuje provedení pneumonektomie a předchozí neoadjuvantní radiochemoterapie, která se vyskytovala u 46 % pacientů se srdeční arytmii v pooperačním období. Naopak věk nad 70 let, ICHS, mužské pohlaví a absence epidurální analgezie se nejeví být rizikovými pro vznik komplikací. Výskyt pooperačních komplikací můžeme snížit na nejnižší možnou míru nejen kvalitní operační technikou, při níž je kromě šetrnosti k plicnímu parenchymu kladen důraz na dokonalou aero - a hemostázu, ale také důslednou předoperační přípravou, včetně rehabilitační přípravy, sanací stávající infekce dýchacích cest, stabilizací vnitřního prostředí a kvalitní pooperační péčí. Toho lze dosáhnout pouze kvalitní interdisciplinární spoluprací.
Zkratky:
- ASA – klasifikace Americké anesteziologické společnosti
- ARDS – syndrom dechové tísně dospělých
- biLE – bilobektomie
- BMI – Body Mass Index
- CT – výpočetní tomografie
- DM – diabetes mellitus
- ePNE – rozšířená pneumonektomie
- FEV1 – usilovně vydechnutý objem za první sekundu
- GIT – gastrointestinální trakt
- CHOPN – chronická obstrukční plicní nemoc
- ICHS – ischemická choroba srdeční
- JIP – jednotka intenzivní péče
- KARIM – Klinika anesteziologie resuscitace a intenzivní medicíny
- LE – lobektomie
- OR – odds ratio
- PAL – prodloužený únik vzduchu
- PET – pozitronová emisní tomografie
- PNE – pneumonektomie
- SE – segmentektomie
- WR – klínovitá resekce
MUDr. Ladislav Mitáš
Pekařská 37
602 00 Brno
e-mail: ladislav.mitas@centrum.cz
Sources
1. Stolz, A., Schützner, J., Simonek, J., Lischke, R., Pafko, P.: Comparison of postoperative complications of 60 - and 70-year-old patients after lung surgery. Interactive Cardiovascular and Thoracic Surgery, 2003; 2 : 620–623.
2. Wada, H., Nakamura, T., Nakomoto, K., Maeda, M., Watanabe, Y. Thirty-day operative mortality for thoracotomy in lung cancer. J. Thorac. Cardiovasc. Surg., 1998; 115 : 70–73.
3. Ferguson, M. K. Assessment of operative risk for pneumonectomy. Chest Surg. Clin. N. Am., 1999; 9 : 339–351.
4. Patel, R. L., Townsend, E. R., Fountain, S. W. Elective pneumonectomy: factors associated with morbidity and operative mortality. Ann. Thorac. Surg., 1992; 54 : 84–88.
5. Stephan, F., Boucheseiche, S., Hollande, J., et. al. Pulmonary complications following lung resection: a comprehensive analysis of incidence and possible risk factors. Chest, 2000; 118 : 1263–1270.
6. Demmy, T. L., Curtis, J. J. Minimally invasive lobectomy directed toward frail and high-risk patients: a case-control study. Ann. Thorac. Surg., 1999; 68 : 194–200.
7. Hoksch, B., Ablassmaier, B., Walter, M., Müller, J. M. Complication rate after thoracoscopic and conventional lobectomy. Zentralbl. Chir., 2003; 128 : 106–110.
8. Park, B. J., Flores, R. M., Rush, V. W. Robotic assistance for video-assisted thoracic surgical lobectomy: Technique and initial results. J. Thorac. Cardiovasc. Surg., 2006; 131 : 54–59.
9. Bernard, A., Ferrand, L., Hagry, O., Benoit, L., Cheynel, N., Favre, J. P. Identification of prognostic factors determining risk groups for lung resection. Ann. Thorac. Surg., 2000; 70 : 1161–1167.
10. Strand, T. E., Rostad, H., Damhuis, R. A. M., Norstein, J. Risk factors for 30-day mortality after resection of lung cancer and prediction of their magnitude. Thorax., 2007; 62 : 991–997.
11. Duque, J. L., Ramos, G., Castrodeza, J., Cerezal, J., Castanedo, M., Yuste, M. G., Heras, F. Early Complications in Surgical Treatment of Lung Cancer: A Prospective, Multicenter Study. Ann. Thorac. Surg., 1997; 63 : 944–950.
12. Alexiou, Ch., Beggs, D., Rogers, M. L., Beggs, L., Asopa, S., Salama, F. D. Pneumonectomy for non-small cell lung cancer: predictors of operative mortality and survival. Eur. J. Cardiothorac. Surg., 2001; 20 : 476–480.
13. Licker, M., Spiliopoulos, A., Frey, J. G., Robert, J., Höhn, L., Perrot, M., Tschopp, J. M. Risk Factors for Early Mortality and Major Complications Following Pneumonectomy for Non-small Cell Carcinoma of the Lung. Chest, 2002; 121 : 1890–1897.
14. Brunelli, A., Monteverde, M., Borri, A., Salati, M., Marasco, R.D., Fianchini, A. Predictors of prolonged air leak after pulmonary lobectomy. Ann. Thorac. Surg., 2004; 77 : 1205–1210.
15. Schussler, O., Alifano, M., Dermine, H., Strano, S., Casetta, A., Sepulveda, S., Chafik, A., Coignard, S., Rabbat, A. and Regnard, J. F. Postoperative Pneumonia after Major Lung Resection. Am. J. Respir. and Crit. Care Med., 2006; 173 : 1161–1169.
16. Suemitsu, R., Sakoguchi, T., Morikawa, K., Yamaguchi, M., Tanaka, H., Takeo, S. Effect of Body Mass Index on Perioperative Complications in Thoracic Surgery. Asian Cardiovasc. Thorac. Ann., 2008; 16 : 463–467.
17. Smith, P. W., Wang, H.,Gazoni, L. M., Shen, K. R., Daniel, T. M., Jones, D. R. Obesity does not increase complications after anatomic resection for non-small cell lung cancer. Ann. Thorac. Surg., 2007; 84 : 1098–1105; discussion 1105–1106.
18. Aoki, T., Yamato, Y., Tsuchida, M., Watanabe, T., Hayashi, J., Hirono, T. Pulmonary complications after surgical treatment of lung cancer in octogenarians. Eur. J. Cardiothorac. Surg., 2000; 18 : 662–665.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2010 Issue 2-
All articles in this issue
- Axiloskopie – alternativa v disekci axilárních lymfatických uzlin při karcinomu mammy
- Hemoragické komplikace léčby warfarinem
- Opakované chirurgické výkony jako zásadní součást léčby recidivujícího kolorektálního karcinomu – kazuistika
- Minimální reziduální choroba u karcinomu pankreatu – naše prvotní zkušenosti
- Cysta choledochu II. typu alebo nadpočetný žlčník?
- Subperiostálna direktná zlomenina lopatky u dieťaťa
- Zarastený prsteň na prste u pacientky závislej na alkohole
- Chirurgická léčba jaterních metastáz kolorektálního původu v České republice: současný celostátní survey
- Osteoplastická dekompresivní kraniotomie – indikace a operační technika
- Komplikace u pacientů po operaci pro plicní malignitu
- PCCP – metoda volby v léčení trochanterických zlomenin na našem pracovišti
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Osteoplastická dekompresivní kraniotomie – indikace a operační technika
- Komplikace u pacientů po operaci pro plicní malignitu
- PCCP – metoda volby v léčení trochanterických zlomenin na našem pracovišti
- Cysta choledochu II. typu alebo nadpočetný žlčník?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

