-
Medical journals
- Career
Tolerance akcelerované pooperační rehabilitace po střevních resekčních výkonech
Authors: Z. Šerclová 1,3; P. Dytrych 1; J. Marvan 1; K. Nová 4; Z. Hankeová 4; O. Ryska 1; Z. Šlégrová 5; L. Burešová 5; L. Trávníková 1; F. Antoš 2,3
Authors‘ workplace: Chirurgická klinika, Fakultní nemocnice Na Bulovce, Praha 1; Institut postgraduálního vzdělávání, Praha 2; 1. lékařská fakulta, Univerzita Karlova, Praha 3; Anesteziologické oddělení, Fakultní nemocnice Na Bulovce, Praha 4; Institut biostatistiky a analýzy, Masarykova univerzitní nemocnice, Brno 5
Published in: Rozhl. Chir., 2009, roč. 88, č. 4, s. 178-184.
Category: Monothematic special - Original
Overview
Úvod:
Moderní postupy v perioperační péči vycházející z principů medicíny založené na důkazech zlepšují pooperační výsledky. Jejich osvojení však není běžnou klinickou praxí na většině chirurgických pracovišť.Cíl:
Cílem naší studie bylo vypracování protokolu a jeho zavedení do praxe. Předmětem sdělení je tolerance protokolu v našich podmínkách.Pacienti a metoda:
Do prospektivní randomizované studie byli zařazeni nemocní operovaní (otevřená střevní resekce) na chirurgické klinice 4/2005–12/2007 a randomizováni do fast track skupiny (n = 53) a non-fast track skupiny (n = 52). Ve fast track skupině (FTS) bylo postupováno podle protokolu akcelerované rehabilitace, v non-fast track skupině (non-FTS) tradičním způsobem. Výsledky byly statisticky zhodnoceny. Dva nemocní z FTS byli vyřazeni z hodnocení pro časné porušení protokolu personálem. Protokol i informovaný souhlas pacienta byly schváleny etickou komisí nemocnice.Výsledky:
Skupiny se nelišily věkem, diagnózou a délkou operace. Analgezie byla významně lépe kontrolovaná ve FTS, podobně tolerance perorálního příjmu byla v této skupině vyšší (operační den – průměrně 634 ml, proti 304 ml). Návrat střevní pasáže byl ve sledované skupině rychlejší (průměrně 2,1 proti 3,9 dnů). Frekvence pooperačních komplikací byla nižší, délka hospitalizace byla kratší (medián 7,0, proti 9,0 dne, p < 0,001).Závěr:
Vypracovaný protokol fast track pooperační rehabilitace bylo možné v rámci studie zavést do klinické praxe. Tolerance nemocnými byla velmi dobrá. Uplatnění postupů akcelerované rehabilitace je v našich podmínkách možné, znamená to však překonat horší toleranci ošetřujícího personálu.Studie byla podporována grantem IGA MZ ČR NR84-20-3.
Klíčová slova:
fast track – otevřená střevní chirurgie – toleranceÚVOD
Pooperační hojení je ovlivněno předoperačním stavem nemocného, rozsahem a kvalitou chirurgického výkonu, ale i kvalitou pooperační péče. Od devadesátých let 20. století je v perioperačním průběhu uplatňována metoda akcelerované pooperační rehabilitace, nazývané též fast track či ERAS (Enhanced recovery after surgery) [1–5]. Jedná se o komplex postupů, které vycházejí z medicíny založené na důkazech a ne pouze z tradice, a jejichž cílem je redukce pooperačního stresu a tedy i pooperačních komplikací. Při těchto postupech je nutná koordinace kolemoperační péče, které se účastní anesteziolog, chirurg, dietetolog a fyzioterapeut. Přesto se na většině pracovišť v České republice i v Evropě uplatňuje způsob pooperační péče, který na důkazech založený není a vychází pouze ze zvyklostí [9].
V letech 2005–2007 byla na našem pracovišti provedena za podpory grantu IGA MZČR prospektivní randomizovaná studie, jejímž cílem bylo zavedení vlastního protokolu, který vycházel z dostupné literatury [1, 5–8], zabývající se problematikou a který byl přizpůsoben podmínkám pracoviště. Předmětem sdělení je část výsledků studie, týkající se zejména tolerance nemocných k fast track protokolu.
PACIENTI A METODA
Do prospektivní randomizované studie byli zařazeni nemocní operovaní na Chirurgické klinice FN Na Bulovce od dubna 2005 do prosince 2007, u nichž byla plánována otevřená střevní resekce bez/se stomií. Kvůli lepší spolupráci a snazšímu zavedení metody byli randomizováni pouze nemocní s nižší morbiditou (ASA I-II), dalším kritériem byl věk 18–70 let. Randomizováni nebyli nemocní s vyšší morbiditou – ASA III-IV, nemocní po radiaci, nemocní s generalizací nádoru, nemocní, u kterých se předpokládala multiorgánová resekce a těhotné ženy. Pacienti, kteří splnili zařazovací kritéria a podepsali informovaný souhlas, byli randomizováni do intervenční fast track skupiny (53 nemocných) a kontrolní non-fast track skupiny (52 nemocných). Nemocní ve fast track skupině (FTS) byli předoperačně široce informováni o vlastním průběhu pooperační péče. Anesteziolog nemocného poučil o způsobu analgezie a jejím hodnocení pomocí vizuální analogové škály (VAS – 1–10 bodů), dále o použití analgetické pumpy, umožňující bolusové přidávání analgetik samotným pacientem (PCA – pacientem kontrolovaná analgezie). Podobně byla s nemocným předoperačně rozebrána dieta, rehabilitace a chirurgická pooperační péče. Pacienti ve FTS v den před operací absolvovali přípravu střeva ortográdní laváží pouze pokud je čekala resekce rekta, jinak bylo střevo ponecháno bez přípravy. V den před operací jim byl doporučen zvýšený příjem tekutin a večer popíjeli sacharidový koktejl (400–800 ml, Nutricia PreOp, Nutricia Ltd). Příjem tekutin byl ukončen 2–4 hodiny před operací, tedy ještě ráno v den operace popíjeli. Při celkové anestezii byly použity metody, omezující pooperační paralytický ileus a umožňující časnou pooperační spolupráci s nemocným (desfluran, vynechání N2O...). Pooperační analgezie byla zajištěna epidurálně (Th 10-12), pomocí kombinace sufentanylu s ropivacainem a byla aplikována PCA pumpou tak, aby si mohli nemocní ke kontinuální dávce přidávat bolus směsi. V případě potřeby byla doplněna intravenózním podáním paracetamolu a metamizolu. Nazogastrická sonda byla zavedena pouze na přání chirurga či anesteziologa, např. při dlouhotrvající operaci. Permanentní močový katétr byl zaveden pouze při operaci v malé pánvi, či na speciální přání. Pokud byly zavedeny nitrobřišní drény, byly první pooperační den odstraněny, jestliže se nejednalo o operaci v malé pánvi. Pooperačně, hned po oběhové stabilizaci, byli nemocní vybízeni k intenzivní rehabilitaci, včetně chůze, a k perorálnímu příjmu. Perorální příjem a rehabilitace byly zvyšovány v dalších pooperačních dnech. Pacienti byli propuštěni z lůžka na základě splnění kritérií: pacient má perorální příjem přes 2 000 ml, nejeví známky infekce, perorální analgezie dostačuje, střevní funkce jsou obnoveny, pacient souhlasí s propuštěním.
Pacienti v kontrolní non-FTS měli tradiční přípravu ortográdní laváží, hladověli od půlnoci před operací. O pooperačním průběhu byli informováni standardně, tedy pouze zběžně. Anestezie i analgezie byla závislá na volbě anesteziologa. Analgezie byla většinou zajištěna epidurálně v nižších etážích – lumbálně, či morfinem subkutánně. Nebyla používána PCA pumpa. Nemocným se rutinně zaváděly: nazogastrická sonda, močový katétr a drény. Pooperační perorální příjem a rehabilitace probíhaly též běžným způsobem. Pacienti byli propuštěni bez zvláštních kritérií. Nemocní z obou skupin byli sledováni do 30. dne po propuštění. Porovnání postupů v obou skupinách je shrnuto v tabulce 1.
Table 1. Hlavní body protokolu a srovnání se standardní péčí Tab. 1. Principal points of the protocol and comparison with a standard 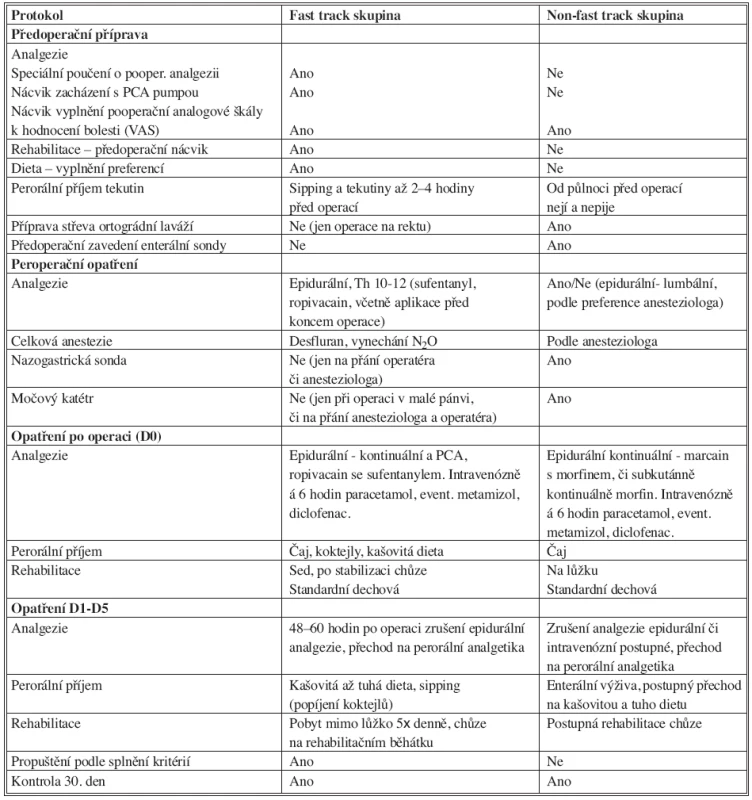
PCA – pacientem kontrolovaná analgezie, VAS – vizuální analogová škála PCA – patient-controlled analgesia, VAS – visual analogue scale STATISTIKA
Statisticky zhodnoceno bylo 51 pacientů ve FTS, 2 nemocní byli vyřazeni pro časné porušení protokolu (1x během anestezie, 1x pooperačně pro nemožnost použít PCA pumpu) a 52 nemocných v non-FTS. Pro spojité proměnné byla spočítána popisná statistika: průměr, směrodatná odchylka, medián, 95% interval spolehlivosti, minimum a maximum. Pro porovnání dvou spojitých proměnných mezi skupinami FT a non-FT byl při splnění normality dat použit t-test. Pokud byla porušena normalita dat, byl použit neparametrický Mannův-Whitneyův test. Pro kategoriální proměnné byly spočítány absolutní a relativní četnosti. Pro testování kontingenčních tabulek byl použit Fischerův exaktní test (tabulky 2x2), pro větší tabulky byl spočítán M-L Chi square test. Pro spojité proměnné měřené v čase byly vykresleny krabicové grafy a pro porovnání průběhu křivek mezi FTS a non-FTS byla spočítána Repeated measures ANOVA. Etická komise nemocnice schválila protokol a informovaný souhlas, projekt byl podpořen grantem IGA MZČR NR 84-20-3.
VÝSLEDKY
Pacienti v obou skupinách se lišili pouze četností pohlaví. Věk, diagnóza a délka operace byly v obou skupinách srovnatelné (Tab. 2, 3). Pooperační analgezie byla významně lépe kontrolovaná ve FTS (Graf 1) v pooperačních dnech 0–5 (D0–5). Průměrná denní hodnota v D0 (operační den) byla ve FTS průměrně 1,6 bodů VAS (medián 1,6 bodů, min-max – 0,0–5,5 bodů) oproti 3,3 bodů VAS (medián 3,4 bodů, min-max – 0,8–6,2 bodů). Zaznamenané maximální hodnoty VAS bodů byly též významně nižší ve FTS (Graf 2).
Table 2. Věk, pohlaví, diagnóza Tab. 2. Age, gender, diagnosis 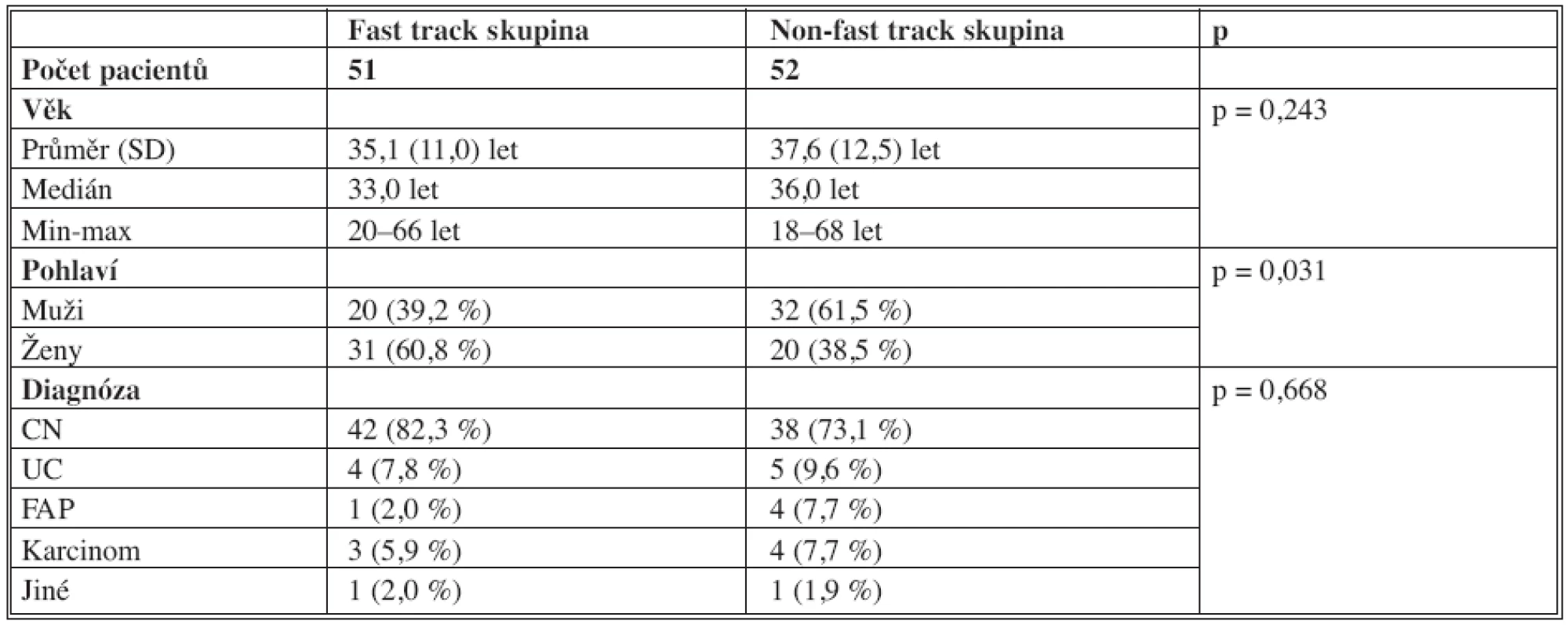
CN = Crohnova nemoc, UC = ulcerózní kolitida, FAP = familiální adenomatózní polypóza CN = Crohn’s disease, UC = ulcerative colitis, FAP = familial adenomatous polyposis Table 3. Charakteristika operace Tab 3. Characteristics of the procedure 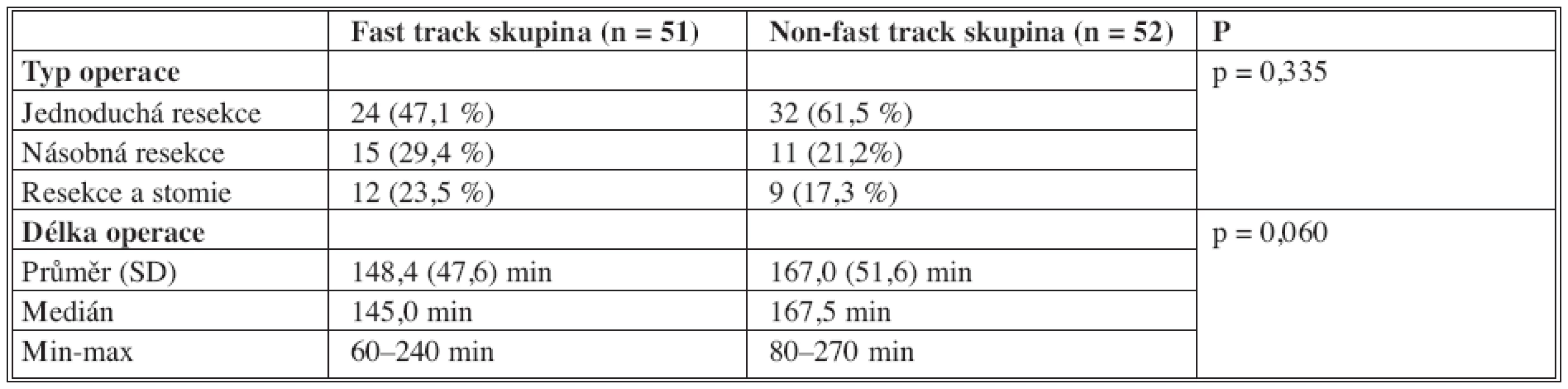
Graph 1. Hodnocení průměrné pooperační bolesti pomocí VAS (vizuální analogová škála, 0–10 bodů, 0 = žádná bolest, 10 = maximální bolest) Graph 1. Assessment of average postoperatove pain using VAS (visual analogue scale, 0–10 points, 0 = no paine, 10 = maximum pain) Průměrné denní hodnoty ode dne operace (D0) až 5. pooperační den (D5) VAS bylo měřeno á 1 hodina prvních 24 hodin, pak á 4 hodiny 
Graph 2. Hodnocení maximální pooperační bolesti pomocí VAS (vizuální analogová škála, 0–10 bodů, 0 = žádná bolest, 10 = maximální bolest) Graph 2. Assessment of the maximum postoperatove pain using VAS (visual analogue scale, 0–10 points, 0 = no paine, 10 = maximum pain) Maximální denní hodnota ve dnech 0–5 po operaci (D0–D5) 
Pacienti ve FTS tolerovali statisticky významně vyšší objem perorálního příjmu (Graf 3), v D0 průměrně 634 ml (medián 600 ml, max-min: 0–2000 ml), v non-FTS 304 ml (medián 300 ml, min-max: -350–900 ml). V D5 přijímali perorálně nemocní ve FTS průměrně 1934 ml (medián 2000 ml, min-max: 0–5750 ml). Dosažení 2000 ml bylo jedním z kritérií propuštění. Průměrný příjem v non-FTS byl významně nižší. Pátý pooperační den přijímali tito nemocní průměrně pouze 951 ml (medián 800 ml, min-max: 0–2150 ml). I přes vyšší perorální příjem jsme nezaznamenali vyšší počet pacientů s pooperačním zvracením ve FTS (Graf 4). Počet pacientů, kteří pooperačně zvraceli byl ve dnech D0, D2–5 nižší ve FTS, v D2 dokonce statisticky významně (1 nemocný proti 9 v non-FTS, p = 0,016), v D2 byl vomitus zaznamenám nevýznamně častěji ve FTS (8 versus 6 nemocných). Obnovení střevních funkcí bylo měřeno nejen tolerancí perorálního příjmu, ale též zaznamenáním odchodu plynů a stolice. K odchodu první stolice došlo průměrně za 2,1 dnů (medián 2,0 dne, min-max: 0–5 dní) ve FTS a průměrně za 3,9 dne v non-FTS (medián 4,0 dny, min-max: 1–7 dní), tedy vysoce významně pomaleji (p < 0,001). Během pooperačního sledování do 30. dne po operaci nikdo nezemřel, 2 nemocní byli vyřazeni z hodnocení pro porušení fast track protokolu do 24 hodin zdravotnickým personálem (1x byl nedodržen protokol během anestezie, 1x během pooperační péče sestrou).
Graph 3. Perorální příjem ve dnech 0–5 po operaci Graph 3. Postoperative oral intake, days 0–5 
Graph 4. Vomitus v pooperačních dnech 0–5 Graph 4. Postoperative vomiting, days 0–5 Procento nemocných, kteří během D0–5 zvraceli 
Pooperační hojení a komplikace si u nikoho nevyžádaly znovupřijetí do nemocnice do 30 dnů. Sledovány byly všechny komplikace, infekční i neinfekční. Nejzávažnějšími pooperačními komplikacemi byly 3 reoperace v časném pooperačním období (1x ve FTS, 2x v non-FTS). Celkem byly pooperační komplikace do 30 dnů od operace významně nižší v FTS (Tab. 4). U nemocných jsme měřili též ztrátu hmotnosti po operaci (váha před operací – váha při propuštění) a její změnu 30. den po operaci. Během hospitalizace nemocní ve FTS ztratili průměrně 2,1 kg své tělesné hmotnosti (medián 2,0 kg). Nemocní v non-FTS ubyli na váze významně více (průměr 4,0 kg, medián 3,5 kg), jak je patrné z grafu 5. Za měsíc po operaci nemocní přibyli průměrně 2,1 kg (medián 2 kg) ve FTS a u nemocných v non FTS byl stále ještě zaznamenán váhový úbytek průměrně 0,7 kg, medián 1,0 kg (Graf 6).
Table 4. Pooperační komplikace Tab 4. Postoperative complications 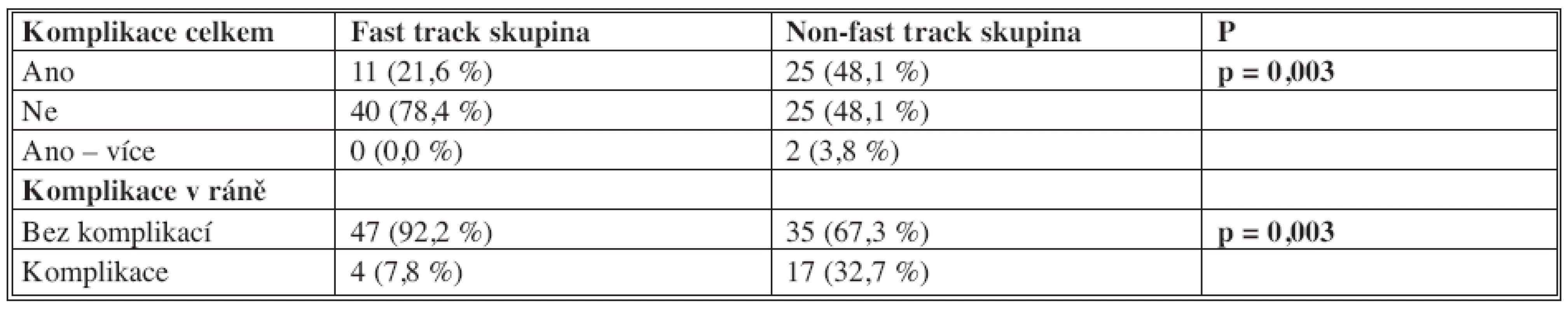
Komplikace do 30 dnů od operace (zaznamenány všechny komplikace, infekční i neinfekční) Complications within 30 days of the procedure (all complications, including infectious and non-infectious ones were recorded) Graph 5. Ztráta na váze během hospitalizace Graph 5. Weight loss during hospitalization Pooperační ztráta na váze (kg) (Váha při propuštění - váha před operací) 
Graph 6. Váhový přírůstek 1 měsíc po operaci Graph 6. Weight gain 1 month after the procedure (Váha 1 měsíc po operaci - váha při propuštění v kg) 
Pacienti ve FTS byli hospitalizováni průměrně 7,4 dne (medián 7,0 dní, min-max: 5–11 dní, 95 % IS 7,0–7,7 dne), délka hospitalizace v non-FTS byla vysoce významně delší, průměrně 10,4 dne (medián 9,0 dne, min-max: 7–22 dní, 95% IS 9,5–11,3 dne) (p < 0,001). Souborné výsledky práce byly odeslány do časopisu Clinical Nutrition.
DISKUSE
Z výše uvedených výsledků vyplývá, že vytvořený fast track protokol byl nemocnými dobře tolerován, žádný z nemocných nebyl vyřazen ze studie na vlastní přání. Protokol nebyl dodržen ve 2 případech ošetřujícím personálem. Za kriticky důležité jsme považovali intenzivní edukaci nemocných v pooperační péči, což jistě mělo vliv na jejich velmi pozitivní vnímání postupu. Bez aktivního zapojení nemocných není metoda uskutečnitelná.
Mezioborová koordinace je poměrně náročná. Před začátkem studie jsme u našich nemocných nejdříve uplatňovali jednotlivé části hlavních principů. Fyzioterapeutky nacvičovaly s nemocnými rehabilitaci chůze v den operace, v rehabilitaci byly edukovány i zdravotní sestry, protože celodenní rehabilitace vyžaduje jejich spolupráci. Pro principy analgezie a anestezie byl nutný konsensus a zaujetí anesteziologů. Pro význam perioperačního perorálního příjmu a zkrácení doby hladovění svědčí řada důkazů [10, 11], potvrzujících, že tímto způsobem lze účinně redukovat pooperační stres. Nicméně příjem tekutin ještě 2–4 hodiny před operací a perorální příjem hned po operaci znamenal změnit způsob myšlení anesteziologů, chirurgů i dalšího ošetřujícího personálu.
Z možných metod jsme zvolili analgezii metodou PCA epidurální cestou, při které byl katétr zaváděn v dolní hrudní oblasti, jehož užití je podle některých názorů kontroverzní [15]. Nicméně naše výsledky spíše podporují pozitivní vliv tohoto typu analgezie na pooperační rehabilitaci a zvládnutí pooperačního ileu [12–14]. Závažnou komplikaci epidurální analgezie ve FTS jsme nezaznamenali, ani k obávané významné hypotenzi nedošlo, což mohlo být způsobeno důrazem na předoperační hydrataci nemocných s nižší předoperační morbiditou a tím, že většina nemocných sledované skupiny nebyla připravována ortográdní laváží. Nejčastější komplikací bylo selhání funkce epidurální analgezie (7 nemocných, 13 %); u těchto pacientů pak byla užita kontinuální subkutánní analgezie.
Nemocní, kteří nemají nazogastrické sondy, močové katétry a drény, zvládají pooperační průběh komfortněji a jejich rehabilitace je snazší. Omezení artificiálních vstupů mohlo být příčinou nižší frekvence infekčních komplikací. Ve většině studií, zabývajících se akcelerovanou rehabilitací, bývá popisována vyšší frekvence zvracení u těchto pacientů. U našich nemocných však nebyl významný rozdíl ve frekvenci zvracení se sondou či bez, což podporuje důkazy proti rutinnímu zavádění nazogastrické sondy u gastrointestinálních operací [16].
Délka hospitalizace byla významně kratší u FTS než u non-FTS, nicméně medián 7,0 dní je poněkud delší, než v některých studiích, zejména severoamerických. Důvodem byla pravděpodobně tradičně delší hospitalizace v náší republice a též skutečnost, že většina nemocných byla operována pro diagnózu nespecifických zánětů střevních. Jednalo se obvykle o mimopražské nemocné a časné pooperační kontroly byly pro ně obtížné. Na druhé straně nikdo z našich nemocných nebyl rehospitalizován do 30 dnů, což není běžné při kratší primární hospitalizaci [17].
Tolerance fast track protokolu byla ze strany nemocných výborná ve všech jeho oblastech – analgezie, rehabilitace, perorální příjem, časné propuštění. Nikdo z nemocných nebyl ztracen ze sledování do 30 dnů od operace, nikdo ze studie neodstoupil. Tolerance zdravotnického personálu byla mnohem komplikovanější, vyžadovala dvouletý nácvik před zahájením studie, nicméně zavedení protokolu a nutnost jeho dodržení v rámci studie ke změnám v myšlení velmi přispěla.
ZÁVĚR
Vypracovaný protokol fast track pooperační rehabilitace bylo možné v rámci studie zavést do klinické praxe. Tolerance nemocnými byla velmi dobrá, pacienti ve sledované skupině byli hospitalizováni významně kratší počet dní, měli významně méně pooperačních komplikací, tolerovali časněji větší objem perorálního příjmu a jejich střevní funkce se obnovily rychleji. Měli nižší váhový úbytek během pooperačního období a rychlejší návrat k původní váze. Uplatnění postupů akcelerované rehabilitace je v našich podmínkách možné, znamená to však překonat horší toleranci ošetřujícího personálu.
Seznam zkratek:
FTS – fast track skupina
Non-FTS – non-fast track skupina
VAS – vizuální analogová škála
PCA – pacientem kontrolovaná analgezie
D0 – den operace
D1–5 – pooperační den 1–5
As. MUDr. Z. Šerclová
Chirurgická klinika FN Na Bulovce
Budínova 2
180 81 Praha 8
e-mail: sercl@seznam.cz
Sources
1. Kehlet, H. Fast-track colonic surgery: status and perspectives. Recent Results Cancer Res., 2005; 165 : 8–13. Review.
2. Soop, M., Nygren, J., Ljungqvist, O. Optimizing perioperative management of patients undergoing colorectal surgery: what is new? Curr. Opin. Crit. Care, 2006; Apr; 12(2): 166–170. Review.
3. Schwenk, W., Neudecker, J., Raue, W., et al. „Fast-track“ rehabilitation after rectal cancer resection. Int. J. Colorectal. Dis., 2006, Sep; 21(6): 547–553.
4. Kariv, Y., Delaney, C. P., Senagore, A. J., at al. Clinical outcomes and cost analysis of a „fast track“ postoperative care pathway for ileal pouch-anal anastomosis: a case control study. Dis. Colon Rectum, 2007, Feb; 50(2): 137–146.
5. Scharfenberg, M., Raue, W., Junghans, T., at al. „Fast-track“ rehabilitation after colonic surgery in elderly patients – is it feasible? Int. J. Colorectal Dis., 2007, Dec; 22(12): 1469–1474.
6. Zutshi, M., Delaney, C. P., Senagore, A. J., at al. Randomized controlled trial comparing the controlled rehabilitation with early ambulation and diet pathway versus the controlled rehabilitation with early ambulation and diet with preemptive epidural anesthesia/analgesia afiter laparotomy and intestinal resection. Am. J. Surg., 2005, Mar; 189(3): 268–272.
7. Fearon, K. C., Ljungqvist, O., von Meyenfeldt, M., et al. Enhanced recovery after surgery: a consensus review of clinical care for patients undergoing colonic resection. Clin. Nutr., 2005, Jun; 24(3): 466–477.
8. Khoo, C. K., Vickery, C. J., Forsyth, N., et al. A prospective randomized controlled trial of multimodal perioperative management protocol in patients undergoing elective colorectal resection for cancer. Ann. Surg., 2007, Jun; 245(6): 867–872.
9. Lassen, K., Dejong, C. H., Ljungqvist, O., et al. Nutritional support and oral intake after gastric resection in five northern European countries. Dig. Surg., 2005; 22(5): 346–352; discussion 352. 2005; 22(5): 346–352; discussion 352.
10. Hausel, J., Nygren, J., Lagerkranser, M. et al. A carbohydrate-rich drink reduces preoperative discomfort in elective surgery patients. Anesth. Analg., 2001, Nov; 93(5): 1344–1350.
11. Weimann, A., Braga, M., Harsanyi, L., et al. ESPEN Guidelines on Enteral Nutrition: Surgery including organ transplantation. Surgery including organ transplantation. Clin. Nutr., 2006, Apr; 25(2): 224–244.
12. Liu, S. S., Wu, C. L. Effect of postoperative analgesia on major postoperative complications: and systematic update of the evidence. Anesth. Analg., 2007, Mar; 104(3): 689–702.
13. Carli, F., Mayo, N., Klubien, K., et al. Epidural analgesia enhances functional exercise capacity and health-related quality of life after colonic surgery: results of a randomized trial. Anestesiology, 2002, Sep; 97(3): 540–549.
14. Clemente, A., Carli, F. The physiological effects of thoracic epidural anesthesia and analgesia on the cardiovascular, respiratory and gastrointestinal systems. Minerva Anestesiologica, 2008, Oct; 74(10): 549–563.
15. Low, J., Johnston, N., Morris, C. Epidural analgesia: first do no harm. Anaesthesia, 2008, Jan; 63(1): 1–3. Erratum in: Anaesthesia, 2008, Oct; 63(10): 1157. Anaesthesia, 2008, Sep; 63(9): 1037.
16. Nelson, R., Tse, B., Edwards, S. Systematic review of prophylactic nasogastric decompression after abdominal operations. Br. J. Surg., 2005, Jun; 92(6): 673–680.
17. Andersen, J., Hjort-Jakobsen, D., Christiansen, P. S., et al. Readmission rates after a planned hospital stay of 2 versus 3 days in fast-track colonic surgery. Br. J. Surg., 2007, Jul; 94(7): 890–893.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2009 Issue 4-
All articles in this issue
- Antitrombotická profylaxe v chirurgických oborech – doporučení American College of Chest Physicians 2008
- Tolerance akcelerované pooperační rehabilitace po střevních resekčních výkonech
- Úloha chirurgického výkonu v liečbe Crohnovej choroby
- Náhodný nález maligního onemocnění při operačním řešení nezvyklé příčiny střevní obstrukce u pacientky po transplantaci ledviny
- Stenóza truncus coeliacus při duodenopankreatektomii
- Nádorový trombus dolní duté žíly u karcinomu ledviny
- Giardiosa, jako málo frekventní onemocnění v diferenciální diagnostice bolestí břicha
- Poranění femorálních cév u trochanterických zlomenin
- Antimikrobní léčba u komplikované nitrobřišní infekce – současný stav
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Stenóza truncus coeliacus při duodenopankreatektomii
- Nádorový trombus dolní duté žíly u karcinomu ledviny
- Antimikrobní léčba u komplikované nitrobřišní infekce – současný stav
- Úloha chirurgického výkonu v liečbe Crohnovej choroby
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

