-
Medical journals
- Career
Hereditární hemoragická teleanginektazie – naše zkušenosti
Authors: Z. Knížek 1; J. Vodička 1,2; O. Vincent 3; K. Šnorová 4
Authors‘ workplace: Klinika otorinolaryngologie a chirurgie hlavy a krku, NPK Pardubická nemocnice 1; Fakulta zdravotnických studií, Univerzita Pardubice 2; Radiodiagnostické oddělení, NPK Pardubická nemocnice 3; Oddělení klinické hematologie, NPK Pardubická nemocnice 4
Published in: Otorinolaryngol Foniatr, 69, 2020, No. 4, pp. 166-171.
Category: Original Article
Overview
Úvod: Hereditární hemoragická teleangiektazie (HHT) je vzácné autozomálně dominantně dědičné vaskulární onemocnění, které se klinicky manifestuje spontánními rekurentními epistaxemi, mukokutánními teleangiektaziemi a arteriovenózními malformacemi (AVM) v různých orgánových systémech. Cílem našeho sdělení je poukázat nejen na terapeutické možnosti epistaxe u těchto pacientů, ale také podat přehled o péči o pacienty s HHT na našem pracovišti, která probíhá podle mezinárodního doporučení.
Metodika: Pacienty s HHT pravidelně sledujeme a zajišťujeme management podle mezinárodního doporučení od roku 2015. Pacienty na kontrolách necháváme vyplnit Epistaxis severity score (ESS), dotazník k určení tíže onemocnění, podle kterého následně volíme terapeutický postup.
Výsledky: Od roku 2015 pravidelně dispenzarizujeme 6 pacientů s HHT. U dvou pacientů byly odhaleny plicní AVM, 3 pacienti měli na základě našeho doporučení provedenu gastroskopii s ošetřením žaludečních či duodenálních teleangiektazií. Po jednotlivých intervencích pro rekurentní epistaxe bylo dosaženo lehkého průběhu epistaxí u 4 pacientů a středního průběhu epistaxí u 2 pacientů, přičemž u všech pacientů došlo ke zlepšení. Průměrné vstupní skóre podle ESS bylo 6,13, průměrné skóre po intervencích bylo 3,28.
Závěr: V ČR chybí centralizovaná péče o pacienty s HHT. Vzhledem k tomu, že nejčastějším příznakem bývá rekurentní epistaxe, dostává se pacient jako první k ORL lékaři, který by tedy měl zahájit alespoň bazální screening a péči o tyto pacienty. Léčba epistaxe u těchto pacientů se výrazněji vymyká standardním způsobům ošetření, na což by měl být každý ORL lékař připraven. Podle našeho pozorování je navíc patrné, že každý z pacientů reaguje na jednotlivé léčebné modality k zamezení rekurence epistaxí individuálně.
Klíčová slova:
hereditární hemoragická teleangiektazie – epistaxe – arteriovenózní malformace – KTP-laser – operace pole Younga – bevacizumab
ÚVOD
Hereditární hemoragická teleangiektazie (HHT), známá též pod názvem Weberova-Oslerova-Renduova nemoc je autozomálně dominantně dědičné vaskulární onemocnění. Vyskytuje se s prevalencí asi 1 : 5 000 až 1 : 9 000 podle geografického rozložení (8). Onemocnění se projevuje obvykle v adolescenci, ale může se projevit i výrazně později, popisovány jsou případy manifestace nemoci až v 70 letech věku (8). Klinicky se u pacientů objevují spontánní rekurentní epistaxe (93–98 % pacientů) (5, 1), mukokutánní teleangiektazie (75–90 %) (3) a arteriovenózní malformace (AVM) v různých orgánových systémech.
Přestože se jedná o systémové onemocnění a od roku 2011 jsou k dispozici guidelines k diagnostice a managementu pacientů s HHT (2), v praxi se ukazuje, že často tito pacienti nejsou pravidelně dispenzarizováni u žádné odbornosti. Vzhledem k tomu, že z jednotlivých příznaků je nejčastější epistaxe, lékařem prvního kontaktu bývá ORL specialista. Cílem našeho sdělení je poukázat nejen na terapeutické možnosti epistaxe u těchto pacientů, ale také podat přehled o péči o pacienty s HHT na našem pracovišti, která probíhá podle mezinárodního doporučení (2).
METODIKA
Pacienty s HHT pravidelně sledujeme a zajišťujeme management podle International Guidelines for the Diagnosis and Management of Hereditary Haemorrhagic Telangiectasia (2) od roku 2015.
Diagnostika a léčba pacientů
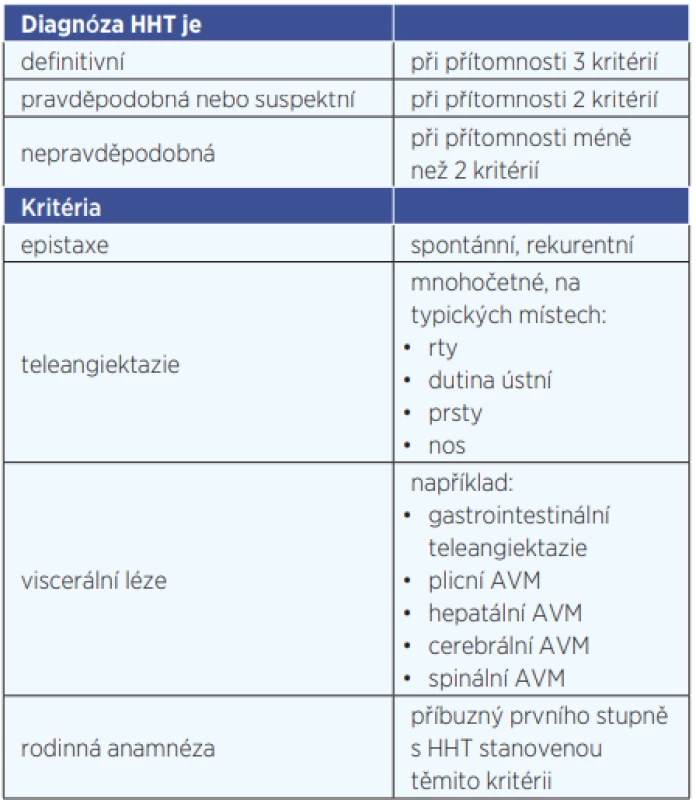
Diagnostika onemocnění je na základě doporučení stanovena podle Curaçao kritérií (tab. 1) (9) – při splnění alespoň 3 kritérií má pacient definitivní onemocnění. Možné onemocnění má pacient, který splňuje pouze 2 kritéria. V takovém případě je ke zvážení provedení genetického vyšetření.
Standardní management zahrnuje screening a léčbu AVM a řešení akutní epistaxe a prevence rekurence epistaxí.
Arteriovenózní malformace
Podle doporučení jsme zjišťovali, zda byla v minulosti u pacienta provedena vyšetření k odhalení AVM. Pakliže nebyla provedena, tato vyšetření jsme indikovali.
Podle dokumentu je doporučeno pátrat po plicních AVM (pAVM) u všech pacientů vzhledem k vysokému riziku paradoxní embolizace s následnou cévní mozkovou příhodou a smrtí. Pokud nebylo doposud u pacienta provedeno, tak jsme jako vyšetřovací metodu volili postkontrastní CT hrudníku (obr. 1).
Image 1. Axiální snímek postkontrastního CT plic – v plíci vpravo ventrálně je patrná plicní arteriovenózní malformace indikovaná k řešení na pracovišti intervenční radiologie 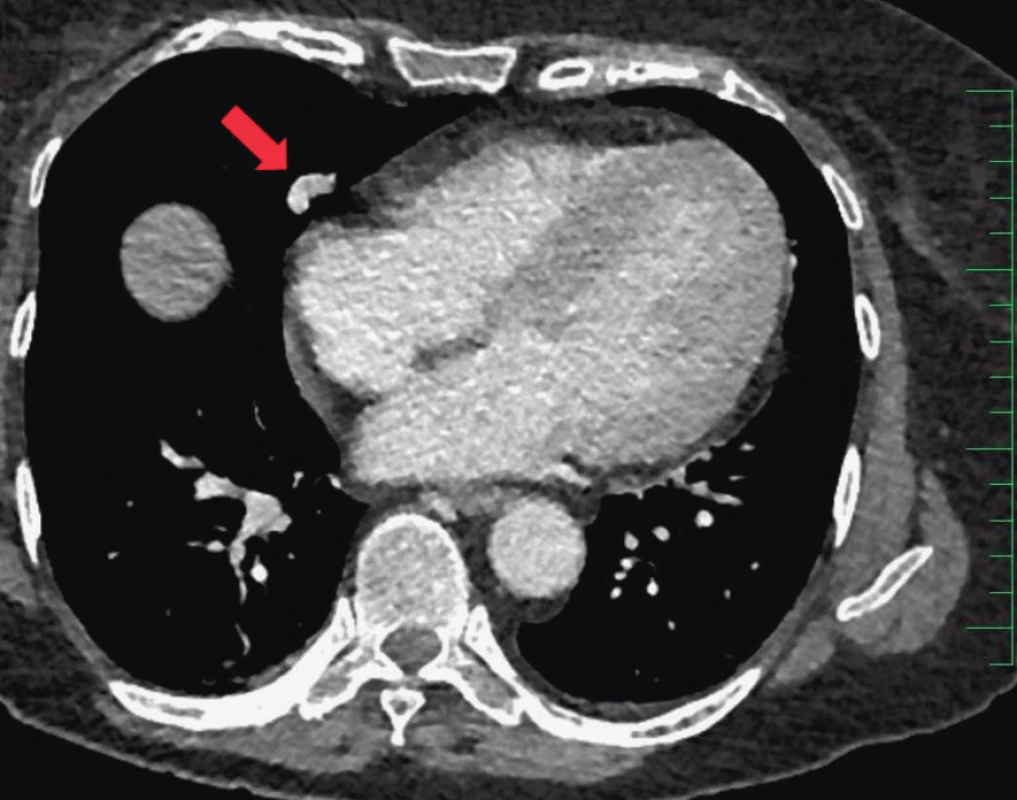
Je rovněž doporučeno pátrat po cerebrálních AVM (cAVM), ale vzhledem k vysoké rizikovosti případné terapie těchto malformací je potřeba vždy zvažovat benefit a riziko takového výkonu. Proto jsme volili jako vyšetřovací metodu MR mozku pouze u pacientů s neurologickou symptomatologií.
Screenovat hepatální AVM (hAVM) se doporučuje pouze při příznacích, které by mohly souviset s postižením jater (tedy zvýšené jaterní testy, srdeční selhávání, portální hypertenze či ischemické poškození žlučovodu). Screeningovou zobrazovací metodou volby je UZ jater.
Gastrointestinální teleangiektazie se mohou u pacientů vyskytovat často, ale screening je doporučen pouze u pacientů, kteří mají sekundární sideropenickou anémii nevysvětlitelnou opakovanými epistaxemi. V takovém případě jsme konzultovali gastroenterologa ke zvážení provedení gastroskopie a případně ošetření lézí argon plazma koagulací (obr. 2).
Image 2. Ošetřování žaludečních teleangiektazií argon plazma koagulací při gastroskopickém vyšetření 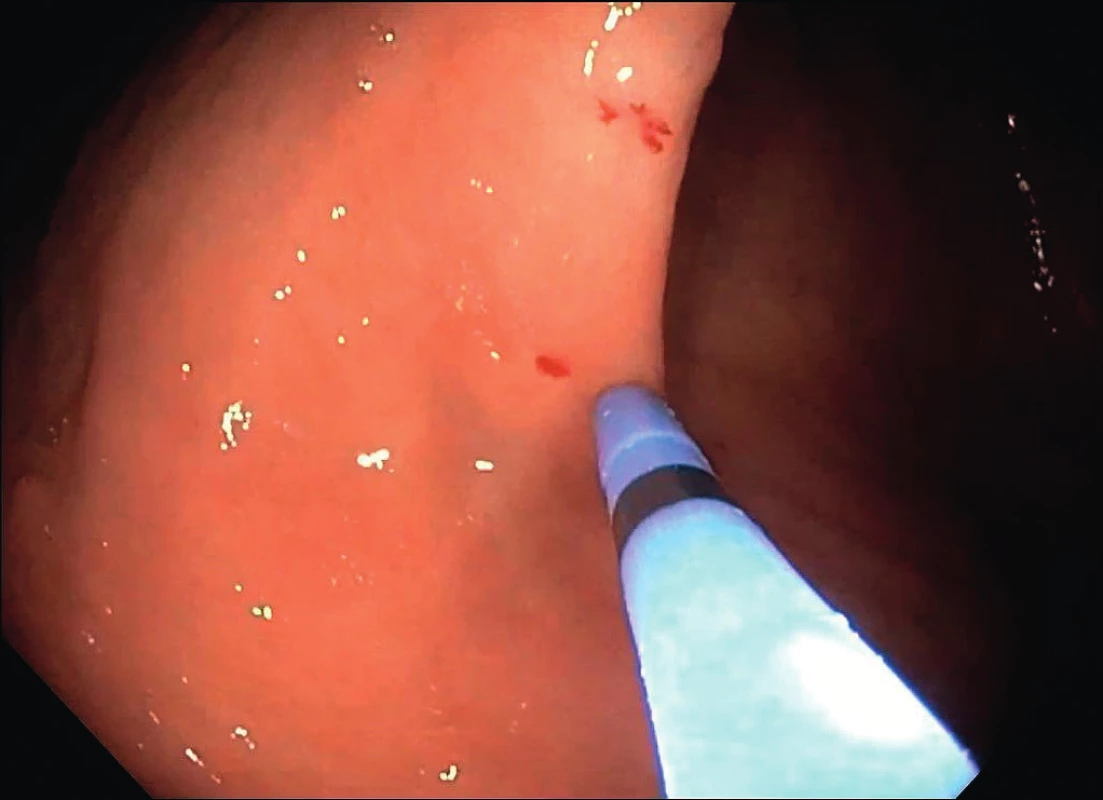
Akutní epistaxe
Epistaxe u pacientů s HHT má svá specifika, proto vždy doporučujeme, v souhlase s guidelines, vyhledat při závažnější epizodě pomoc ORL lékaře, který má zkušenosti s tímto onemocněním.
Krvácení nestavíme cílenou endonazální koagulací. Tato kontaktní metoda může v budoucnosti vést ke zhoršení průběhu epistaxí a nelze opomenout ani riziko vzniku perforace septa, která pak dále přispívá ke zhoršování obtíží nemocného (7). Nevstřebatelnou tamponádu se doporučuje standardně neužívat, nicméně lze využít nízkotlakou tamponádu – například karboxymetylcelulózu na balónu (RapidRhino, Smith & Nephew, Londýn, Velká Británie).
Metodou první volby na našem pracovišti je užití vstřebatelného materiálu (želatiny – Gelaspon, Bausch & Lomb, Rochester, NY, USA), na který je aplikováno 10 ml (1 000 mg) kyseliny tranexamové (obr. 3). Při nedostatečném efektu zvažujeme možnost ošetření na intervenční radiologii se všemi riziky, která s sebou tato intervence přináší (slepota, ischemická cévní mozková příhoda).
Image 3. Bloček želatiny napuštěný kyselinou tranexamovou připravený k vložení do nosní dutiny 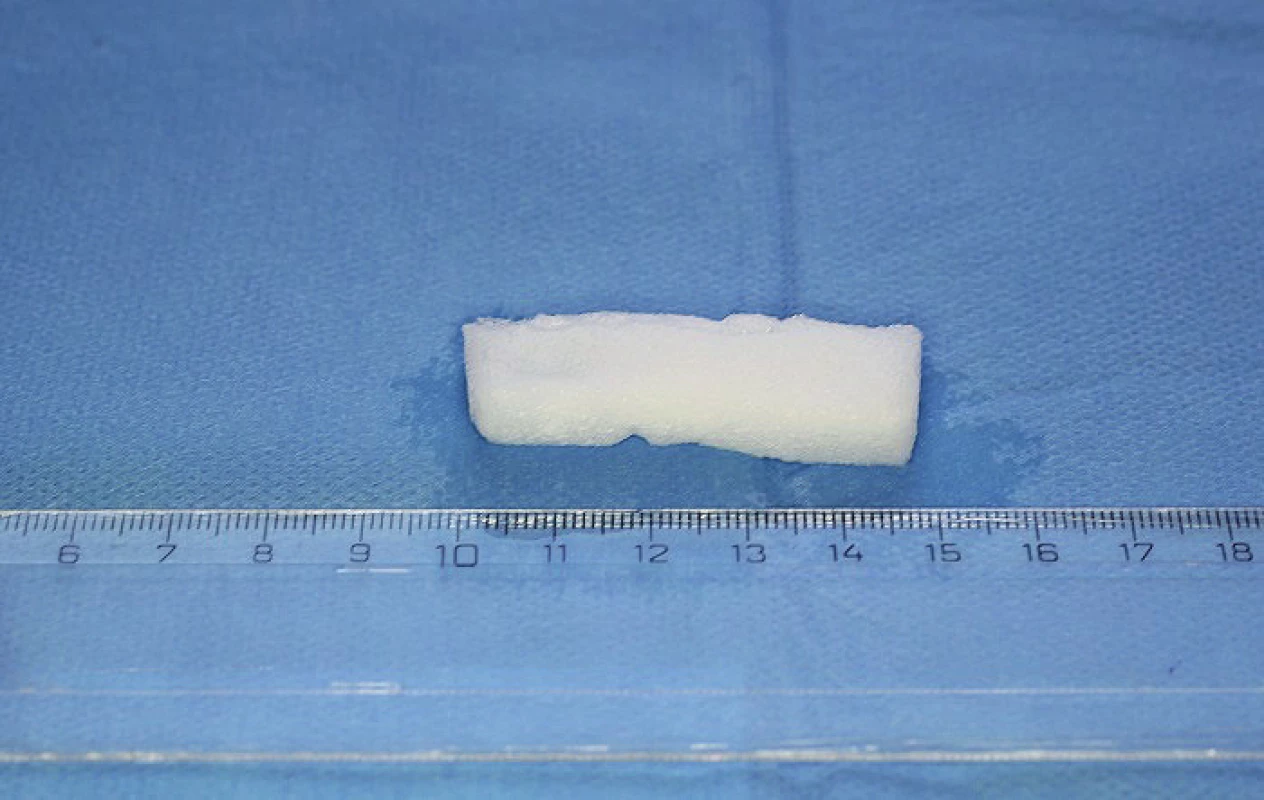
Prevence rekurence epistaxí
Z konzervativních postupů všem pacientům doporučujeme užívání estriolové masti (Ovestin) 2× denně lokálně do nosní dutiny a důsledně doporučujeme vyhýbat se jakékoliv traumatizaci nosu.
Z chirurgických postupů u pacientů s lehčím typem onemocnění a při neúspěchu konzervativní terapie nabízíme ošetření teleangiektazií nosní dutiny endonazálně endoskopicky KTP laserem (obr. 4). U těžších případů nabízíme možnost aplikace bevacizumabu intralezionálně či septodermoplastiku. U nejtěžších případů potom zvažujeme jednostranné či oboustranné uzavření nosního vchodu podle Younga modifikovanou podle Lundové (7) (obr. 5).
Image 4. Ošetření teleangiektazií nosní dutiny KTP laserem 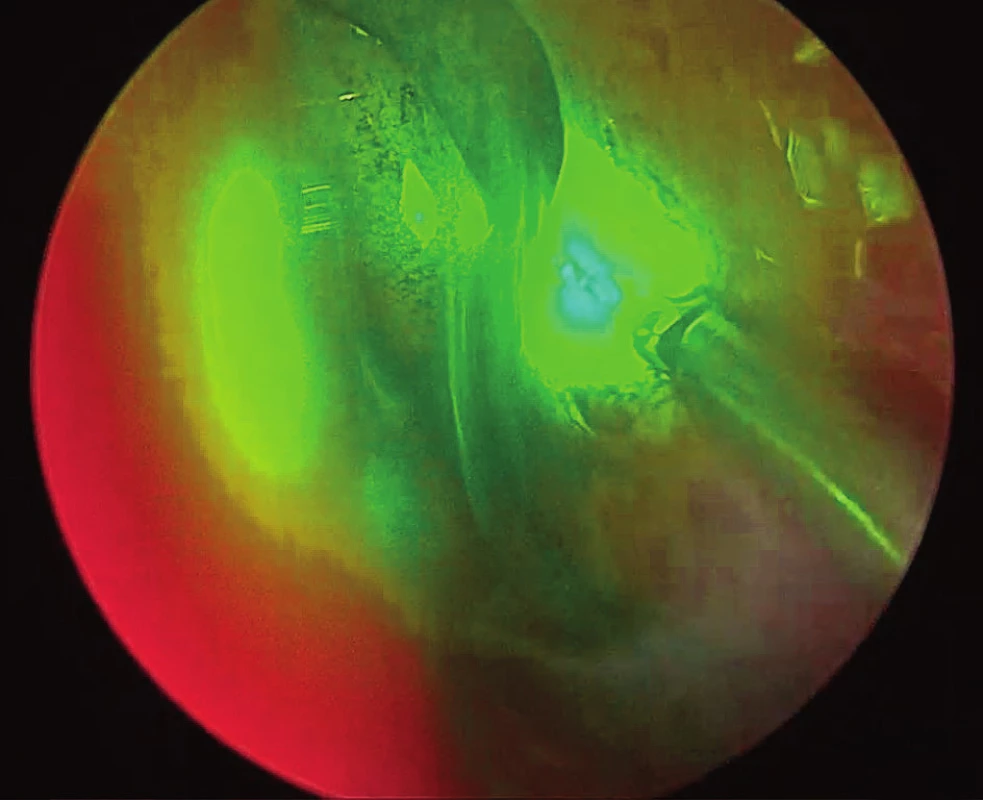
Image 5. Operace podle Younga modifikovaná Lundovou na levé straně 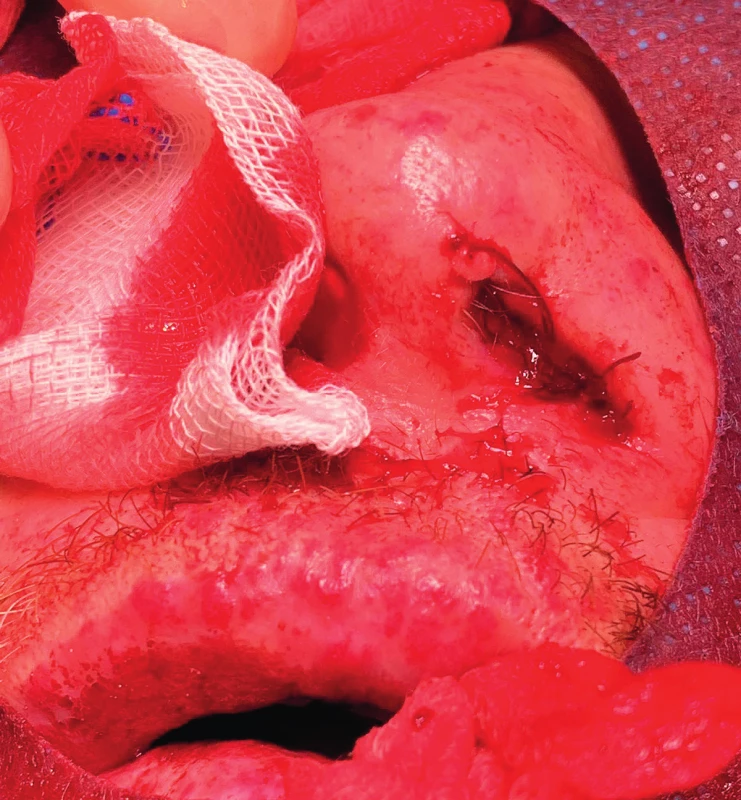
Soubor pacientů
Na začátku dispenzarizace jsme u pacientů potvrdili diagnózu HHT na základě Curaçao kritérií. Dále jsme všechny pacienty nechali vyplnit Epistaxis Severity Score (ESS), dotazník (4) přeložený do češtiny k určení tíže onemocnění (a následně tak oklasifikovali na lehký, střední či těžký průběh epistaxí) (obr. 6). Následně jsme volili terapeutický postup, který se odvíjel od tíže onemocnění a přání nemocného po zvážení benefitu a možných rizik. Po každém terapeutickém postupu s časovým odstupem minimálně 2 měsíců pacienti opět vyplnili ESS dotazník a podle výsledků bylo rozhodnuto o případné další intervenci.
Image 6. Epistaxis Severity Score (ESS), dotazník přeložený do češtiny. Podle vzorečku navrženého autorem dotazníku je dopočítáno tzv. hrubé ESS skóre, které je po dosazení do dalšího vzorečku použito z vypočteného tzv. normalizovaného ESS skóre. 
VÝSLEDKY
Celkem jsme na našem pracovišti od roku 2015 podle doporučení guidelines začali pravidelně dispenzarizovat 7 pacientů, z toho 5 žen a 2 muže. Jeden muž se na další kontroly po iniciálním screeningu a zahájení léčby nedostavoval, zařazeno do sledování tedy bylo pouze 6 pacientů. Průměrný věk začátku dispenzarizace byl 58 let. Všichni pacienti měli splněna alespoň 3 Curaçao kritéria, tedy definitivní onemocnění. Pozitivní rodinná anamnéza byla zjištěna u 5 pacientů (tab. 2).
Table 2. Soubor pacientů sledovaných na našem oddělení. Všichni pacienti měli splněna alespoň 3 Curaçao kritéria, přičemž 3 pacienti měli splněna všechna Curaçao kritéria. U 2 pacientů byly odhaleny plicní AVM na základě postkontrastního CT. U 3 pacientů byla doporučena gastroskopie pro susp. na krvácení z gastrointestinálních teleangiekazií (GIT). Jiné AVM nebyly u žádného z pacientů zaznamenány. 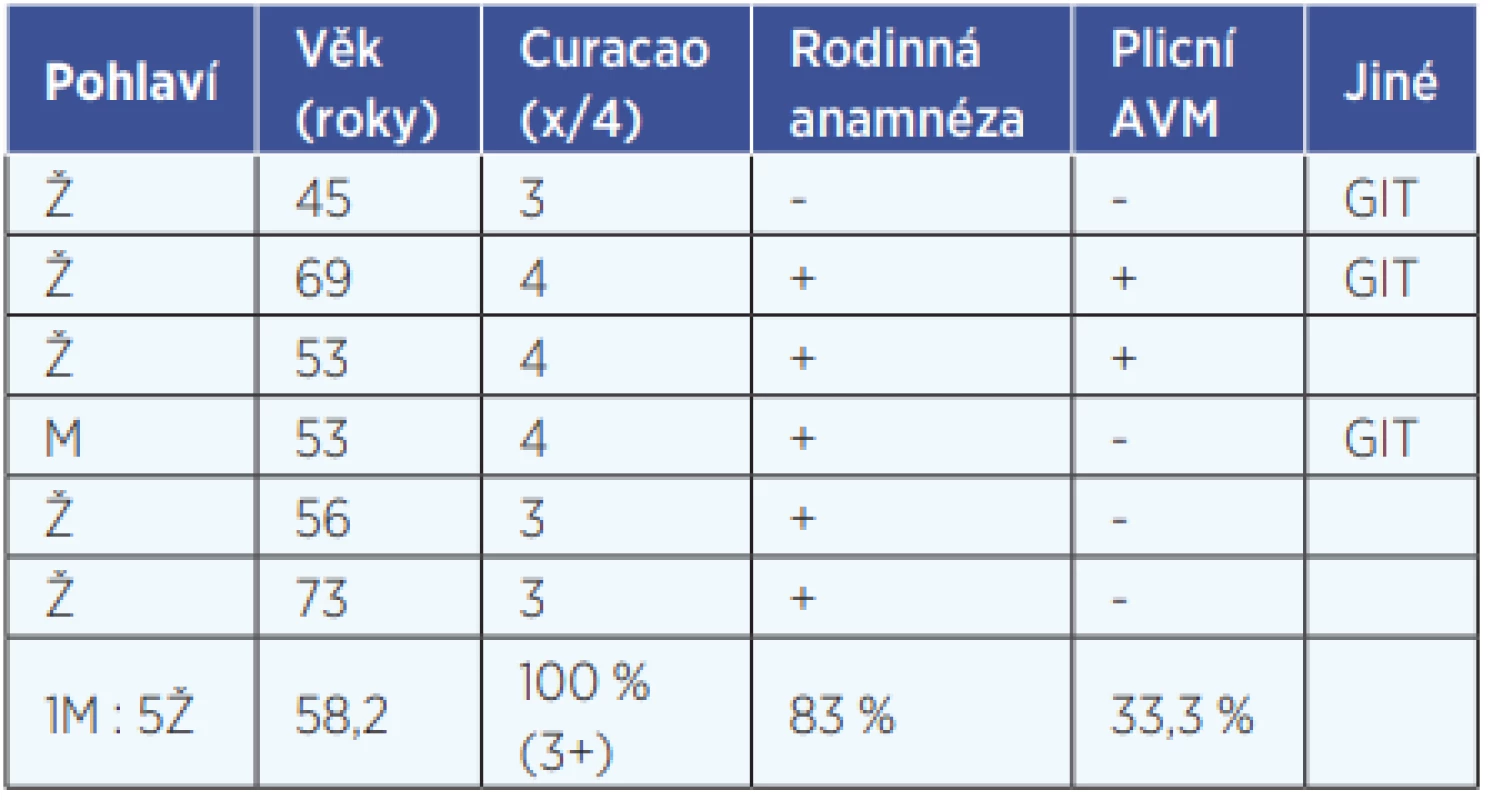
Všichni pacienti měli provedeno postkontrastní CT plic (3 indikované námi a 3 pacienti měli CT provedeno již dříve). U dvou pacientů byly odhaleny plicní AVM a bylo doporučeno provedení jejich ošetření na pracovišti intervenční radiologie. Tři pacienti měli na základě našeho doporučení provedenu gastroskopii s ošetřením žaludečních či duodenálních teleangiektazií pro pokles hemoglobinu nevysvětlitelný rekurentními epistaxemi.
Při zahájení dispenzarizace před zahájením jakékoliv intervence měli 4 pacienti střední průběh epistaxí a 2 pacienti těžký průběh epistaxí. Všichni pacienti byli léčeni estriolovou mastí, 4× bylo indikováno ošetření venektazií KTP laserem či argon plazma koagulací. U jednoho pacienta jsme indikovali intralezionálně aplikovaný bevacizumab. U dvou pacientů jsme provedli Youngovu operaci (u jednoho z nich jednostranně a u jednoho oboustranně). Po jednotlivých intervencích (tab. 3) bylo dosaženo lehkého průběhu epistaxí u 4 pacientů a středního průběhu epistaxí u 2 pacientů, přičemž u všech pacientů došlo ke zlepšení. Průměrné vstupní skóre podle ESS bylo 6,13, průměrné skóre po intervencích bylo 3,28 (průměrný pokles tedy o 2,85).
Table 3. Výsledky Epistaxis Severity Score (ESS), dotazníku u jednotlivých pacientů
ESS1 – ESS skóre při první návštěvě při zahájení pravidelné dispenzarizace, ESS2, ESS3 – ESS skóre při kontrolních návštěvách, ESS4 – ESS skóre po jednotlivých léčebných modalitách, ESS1-4 – pokles ESS skóre oproti první návštěvě, estriol – zahájení léčby estriolovou mastí, APC – ošetření nosních teleangiektazií argon plazma koagulací, KTP – ošetření nosních teleangiektazií KTP laserem, bevacizumab – aplikace bevacizumabu intralezionálně, Young – operace pole Younga Iniciály ESS 1 Léčba 1 ESS 2 Léčba 2 E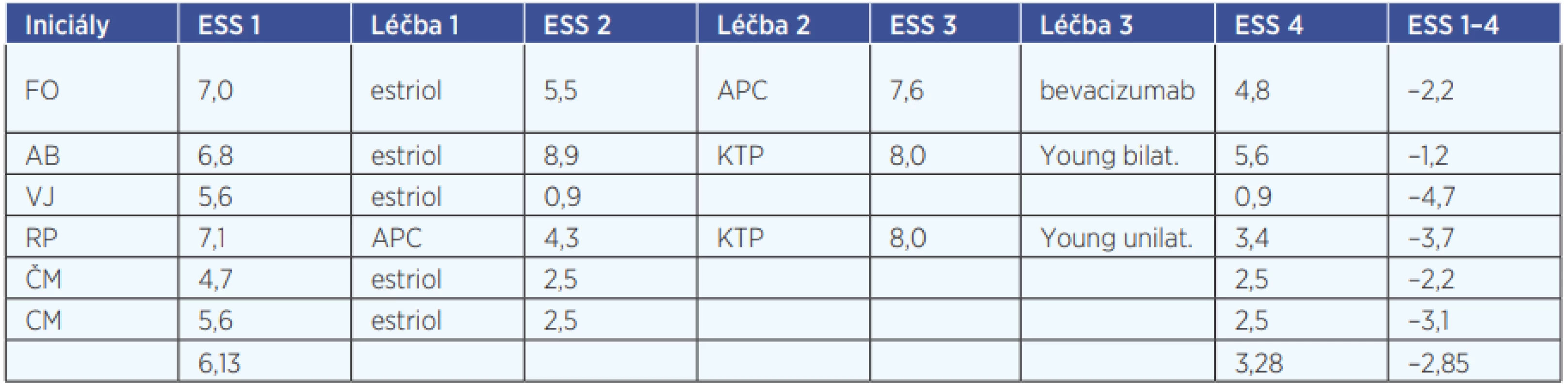
DISKUSE
Od roku 2011 jsou k dispozici kvalitní guidelines v péči o pacienty s HHT (2). Přestože je dokumentu vyčítáno, že je sestaven na základě názoru expertů a není podložen dostatečnými randomizovanými klinickými pokusy (3), jedná se v tuto chvíli o nejucelenější přehled o diagnostice a managementu onemocnění.
V guidelines je zmíněno, že se jedná o systémové onemocnění a hlavní dispenzarizace by měla připadat praktickému lékaři. Z naší zkušenosti se však v praxi ukazuje, že tomu tak často není. V České republice neexistují centra, která by se o pacienty s HHT starala. Vzhledem k tomu, že nejčastějším a obvykle prvním příznakem u těchto pacientů je rekurentní epistaxe, je ORL specialista často lékařem prvního kontaktu.
Onemocnění přitom s sebou nese rizika komplikací AVM v některých orgánových soustavách, čehož si klinici často nemusí být vědomi. Zejména se jedná o plicní AVM, které mohou způsobit paradoxní embolizaci a cévní mozkovou příhodu s následnou smrtí.
Ze sdělení Garga et al. (3) vyplývá, že základ managementu u tohoto typu onemocnění je časná diagnóza na základě klinických kritérií, léčba orgán specifických symptomů, screening a management AVM a edukace pacienta a jeho rodinných příslušníků.
Časná diagnóza
Diagnóza onemocnění se opírá o klinická kritéria – Curaçao kritéria (9). Všichni naši pacienti mají splněna alespoň 3 kritéria, tedy definitivní onemocnění. Tři pacienti potom splňovali všechna 4 kritéria. Genetické testování je doporučeno u pacientů, kde je diagnóza pravděpodobná (tedy splněna 2 Curaçao kritéria) (3), což nebylo u žádného z našich pacientů. Genetické testování lze rovněž využít k odhalení specifické mutace pro danou rodinu, a tak časně odhalit onemocnění již v dětském věku či adolescenci (3).
Až 80 % pacientů s HHT má identifikovatelnou mutaci v genu ENG na chromozomu 9 (HHT typ 1) či genu ACVRL1 na chromozomu 12 (HHT typ 2) (8). V současnosti je známo celkem 5 podtypů HHT rozdělených na základě genetického testování; jednotlivé podtypy se pak od sebe odlišují rozdílným procentuálním zastoupením jednotlivých AVM a příznaků (6). Asi 3–5 % pacientů má mutaci v genu MADH4 a současně s HHT trpí na juvenilní polypózu; asi ve 20 % se mutace v rodině nenajde (8).
Léčba orgán specifických symptomů
Vzhledem k faktu, že více než 90 % pacientů trpí rekurentními epistaxemi (5, 1), bývá krvácení z nosu prvním příznakem, který pacienta přivádí k lékaři. Je tedy vysoká pravděpodobnost, že ORL lékař bude prvním specialistou, který může onemocnění rozpoznat.
Management epistaxe u pacientů s HHT je rozdílný proti standardnímu ošetřování krvácení z nosu. ORL lékař při podezření na HHT si musí být vědom následujících skutečností, aby byl schopen zajistit časný záchyt a následnou kvalitní péči: 1. krvácení probíhá z teleangiektazií, 2. krvácení se objevuje spontánně, 3. krvácení probíhá v různé tíží – od minimálně obtěžujícího až po život ohrožující (5). Ošetření je nutné provést co nejšetrnější a ideálně bezkontaktní metodou, neboť jakákoliv traumatizace sliznice vede ke stimulaci neoangiogeneze a zmnožení teleangiektazií s následným zhoršením epistaxe; nezanedbatelné je i riziko perforace přepážky, rovněž zhoršující průběh budoucích epistaxí (8).
K zastavení akutní epistaxe je proto vhodné užít materiál vstřebatelný (želatina, polyuretan), napuštěný v adrenalinu či kyselině tranexamové, případně i novější typy nevstřebatelných tamponád (karboxymetylcelulóza) (8). Na našem pracovišti standardně jako první linii léčby užíváme želatinu s kyselinou tranexamovou. Vzácně je nutno tamponádu doplnit o embolizaci na intervenční radiologii. Postup je nutno zvážit velmi pečlivě vzhledem k riziku slepoty a ischemické cévní mozkové příhody a také skutečnosti, že účinek je pouze krátkodobý (8). Na našem pracovišti jsme za sledované období neindikovali ošetření embolizací pro akutní epistaxi u pacienta s HHT.
K zamezení rekurence epistaxí je jedinou účinnou metodou uzávěr nosního vchodu, ostatní metody pouze snižují rekurenci či závažnost krvácení (8). Postupů byla popsána celá řada, vždy je nutné vzít v potaz závažnost epistaxí a přání nemocného. Z konzervativních postupů lze užít betablokátorové kapky, kyselinu tranexamovou lokálně či systémově, estriolovou mast či bevacizumab (intralezionálně nebo systémově); z chirurgických postupů potom ošetření nosních teleangiektazií laserem (např. KTP) či argon plazma koagulací, septodermoplastiku nebo již dříve zmíněný uzávěr nosního vchodu (8). Uzávěr nosního vchodu byl popsán Youngem k řešení atrofické rinitidy, k řešení epistaxí u HHT byla poté popsána modifikace podle Lundové v roce 1995, kdy místo dvoulalokového uzávěru byl použit uzávěr třílalokový (7).
Na našem pracovišti volíme rovněž terapeutické modality podle tíže epistaxí a přání nemocného, a to obvykle stupňovitě (blíže tab. 3). Z našich výsledků vyplývá, že k zamezení rekurence epistaxí u některých pacientů dostačuje již pouhá aplikace estriolové masti intranazálně. V našem sledování jsme byli s tímto postupem úspěšní u 3 pacientů. U jednoho pacienta po aplikaci bevacizumabu do strany nosní dutiny s horším průběhem epistaxí došlo také k výraznějšímu zlepšení obtíží. U jiných pacientů naopak estriolová mast nepřináší výraznější zlepšení, a to dokonce ani po doplnění o ošetření lézí KTP laserem. U některých pacientů pak ani uzávěr nosního vchodu nemusí vést ke kompletní rezoluci příznaků. U jednoho pacienta jsme provedli uzávěr pouze jednostranně (vzhledem k přání nemocného), u druhého pak byl uzávěr proveden oboustranně, nicméně u něj došlo k dehiscenci na jedné straně. Dalším krokem u tohoto pacienta byl zvažovaný uzávěr nosního vchodu nazolabiálním lalokem, ale pacient byl spokojený se stávajícím průběhem epistaxí a další intervenci si nepřál. V našem souboru nebyl vhodný kandidát k provedení septodermoplastiky (bylo zvažováno u pacienta se středně těžkým průběhem epistaxí – průběh epistaxí již byl příliš těžký, byla přítomna perforace nosní přepážky nebo si pacient tento výkon nepřál).
Screening a management AVM
Guidelines z roku 2011 se podrobně vyjadřují k otázce screeningu a managementu AVM. Vzhledem k faktu, že v ČR nejsou dostupná centra zajišťující péči o tyto pacienty a ORL lékař bývá prvním klinikem, se kterým se pacient dostává do kontaktu, je vhodné zajistit alespoň screening a řešení potenciálně fatálních AVM, tedy plicní AVM (2). Všichni naši pacienti měli provedené zobrazovací vyšetření k odhalení této malformace, a ta byla odhalena u 2 pacientů. Oba pacienti měli pAVM řešenou intervenčním radiologem.
Vzhledem k rizikovosti a nejistému benefitu řešení cerebrálních AVM neprovádíme na našem pracovišti standardně screening cAVM.
U žádného z pacientů jsme neindikovali zobrazovací metodu k odhalení hAVM, byť jeden z pacientů trpěl na příznaky srdečního selhávání, které bylo řešeno na kardiologickém a interním oddělení. V minulosti již totiž bylo u pacienta provedeno vyšetření magnetickou rezonancí se zaměřením na játra bez patrných AVM; příčinou selhávání byla hypervolemie po opakovaném podávání transfuzí při chlopenní vadě.
U 2 pacientů jsme doporučili gastroskopické vyšetření pro výraznější pokles hemoglobinu a přítomnost meleny. U obou pacientů byly nalezeny opakovaně vícečetné teleangiektazie v žaludku, které pak byly ošetřeny argon plazma koagulací.
Edukace
Efektivní edukace pacientů s možným či definitivním onemocněním je důležitá nejen z hlediska managementu, ale i k odhalení onemocnění v časných stadiích u rodinných příslušníků. U jednoho z našich pacientů bylo doporučeno na základě anamnézy vyšetření dcery, u které následně bylo onemocnění potvrzeno na základě klinických kritérií a došlo ke standardnímu screeningu a stanovení léčebné modality epistaxe.
ZÁVĚR
V ČR chybí centralizovaná péče o pacienty s HHT. Vzhledem k tomu, že nejčastějším příznakem bývá rekurentní epistaxe, dostává se pacient jako první k ORL lékaři, který by tedy měl zahájit alespoň bazální screening a péči o tyto pacienty. Léčba epistaxe u těchto pacientů se výrazněji vymyká standardním způsobům ošetření, na což by měl být každý ORL lékař připraven. Podle našeho pozorování je navíc patrné, že každý z pacientů reaguje na jednotlivé léčebné modality k zamezení rekurence epistaxí individuálně.
Prohlášení o střetu zájmů
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Do redakce došlo dne: 1. 3. 2020
Přijato k publikaci dne: 14. 4. 2020
Adresa ke korespondenci:
MUDr. Zdeněk Knížek
Klinika otorinolaryngologie a chirurgie hlavy a krku
NPK Pardubická nemocnice
Kyjevská 44
532 03 Pardubice
e-mail: knizekz@seznam.cz
Sources
1. Assar, O. S., Friedman, C. M., White, R. I., jr.: The natural history of epistaxis in hereditary hemorrhagic telangiectasia. Laryngoscope, 101, 1991, 9, s. 977–980.
2. Faughnan, M. E., Palda, V. A., Garcia-Tsao, G., et al.: International guidelines for the diagnosis and management of hereditary haemorrhagic telangiectasia. J Med Genet, 48, 2011, 2, s. 73–87.
3. Garg, N., Khunger, M., Gupta, A., et al.: Optimal management of hereditary hemorrhagic telangiectasia. J Blood Med, 15, 2014, 10, s. 191–206.
4. Hoag, J., Reh, D., Mitchell, S., et al.: Development of a hereditary hemorrhagic telangiectasia epistaxis severity scoring (HHT--ESS) system. Haematol Meet Rep, 3, 2009, s. 27–28.
5. Chin, Ch. J., Rotenberg, B. W., Witterick, I. J.: Epistaxis in hereditary hemorrhagic telangiectasia: an evidence based review of surgical management. J Otolaryngol Head Neck Surg, 45, 2016, s. 3.
6. Koenighofer, M., Parzefall, T., Frohne, A., et al.: Spectrum of novel hereditary hemorrhagic telangiectasia variants in an austrian patient cohort. Clin Exp Otorhinolaryngol, 12, 2019, 11, s. 405–411.
7. Lund, V. J., Darby, Y., Rimmer, J., et al.: Nasal closure for severe hereditary haemorrhagic telangiectasia in 100 patients. The Lund modification of the Young’s procedure: a 22-year experience. Rhinology, 55, 2017, s. 135–141.
8. Rimmer, J., Lund, V. J.: Hereditary haemorrhagic telangiectasia. Rhinology, 53, 2015, 9, s. 195–203.
9. Shovlin, C. L., Guttmacher, A. E., Buscarini, E., et al.: Diagnostic criteria for hereditary hemorrhagic telangiectasia (Rendu-Osler-Weber syndrome). Am J Med Genet, 91, 2000, 3, s. 66–67.
Labels
Audiology Paediatric ENT ENT (Otorhinolaryngology)
Article was published inOtorhinolaryngology and Phoniatrics

2020 Issue 4-
All articles in this issue
- Biologické chování adenoidně cystického karcinomu velkých slinných žláz
- Přínos spánkové endoskopie v chirurgické léčbě syndromu obstrukční spánkové apnoe
- Hereditární hemoragická teleanginektazie – naše zkušenosti
- Současná klasifikace a staging cholesteatomu
- Granulomatóza s polyangiitidou nosní sliznice diagnostikovaná de novo v graviditě
- Otický hydrocefalus: vzácná komplikace akutního hnisavého středoušního zánětu
- Nazolabiální cysta – popis dvou případů a přehled literatury
- Laureáti Kutvirtovy ceny 2019
- Kutvirtova cena 2019
- Cena časopisu Otorinolaryngologie a foniatrie 2019
- Kutvirtova cena 2020 – podmínky soutěže
- Cena časopisu Otorinolaryngologie a foniatrie 2020 – podmínky soutěže
- Odešel doc. MUDr. Aleš Hahn, CSc., Dr. Med.
- K životnímu jubileu prof. MUDr. Josefa Syky, DrSc.
- Otorhinolaryngology and Phoniatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nazolabiální cysta – popis dvou případů a přehled literatury
- Současná klasifikace a staging cholesteatomu
- Otický hydrocefalus: vzácná komplikace akutního hnisavého středoušního zánětu
- Biologické chování adenoidně cystického karcinomu velkých slinných žláz
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career