-
Medical journals
- Career
Možnosti diagnostiky jaterní steatózy
Authors: Karel Dvořák
Authors‘ workplace: Oddělení gastroenterologie a hepatologie, Krajská nemocnice Liberec, a. s.
Published in: Čas. Lék. čes. 2022; 161: 57-60
Category: Review Article
Overview
Nemoci asociované s jaterní steatózou představují nejčastější chronické jaterní choroby současnosti, proto má diagnostika steatózy prvořadý význam. Nejčastěji používaným zobrazovacím vyšetřením jater v běžné klinické praxi je ultrasonografie, která je dostupná, má dobrou výpovědní hodnotu, ale také u mírné steatózy a pacientů s výraznější obezitou limitace v nižší senzitivitě. Sonograficky se steatóza projevuje zejména zvýšením echogenity jaterního parenchymu a dorsálním oslabením akustického signálu. Existují i pokročilejší metody umožňující semikvantitativní a kvantitativní hodnocení množství tuku v játrech. Jedná se zejména o metody založené na hodnocení atenuace akustického signálu. Nejpoužívanější je funkce CAP (controlled attenuation parameter) integrovaná do přístrojů FibroScan, umožňující hodnocení steatózy bez sonografického vyšetření. Další modalitou jsou specifické metody založené na magnetické rezonanci – MR spektroskopie a PDFF (protein density fat fraction), které s vysokou přesností kvantifikují množství tuku v játrech a mohou sloužit jako referenční standard.
Klíčová slova:
diagnostika – magnetická rezonance – sonografie – steatóza jater – kvantifikace
ÚVOD
Tuk se v játrech vyskytuje fyziologicky, jeho nadměrná akumulace se nazývá steatóza. Ta je histologicky definována přítomností tukových vezikul (obsahující triacylglyceroly) ve více než 5 % hepatocytů. Steatóza patří mezi jednu z obecných odpovědí jaterní tkáně na inzult; chorob asociovaných se steatózou je tak celá řada. Mezi nejvýznamnější zahrnujeme steatózu při metabolickém syndromu (NAFLD – non-alcoholic fatty liver disease) a steatózu při poškození jater alkoholem (ALD – alcoholic liver disease). NAFLD je považována za nejčastější chronickou jaterní chorobu současnosti postihující 25 % populace. Alkohol samotný je příčinou minimálně poloviny případů jaterní cirhózy v Česku, přičemž se může spolupodílet na jaterním poškození i při jiných chronických jaterních chorobách. Dalšími chorobami, které jsou asociované s jaterní steatózou, jsou chronická infekce HCV (genotypem 3), celiakie, Wilsonova nemoc, polékové poškození, dlouhodobá parenterální výživa nebo poruchy metabolismu lipidů.
HISTOLOGICKÉ HODNOCENÍ A KVANTIFIKACE JATERNÍ STEATÓZY
Podle velikosti tukových inkluzí rozlišujeme steatózu mikrovezikulární, makrovezikulární a smíšenou. Stupeň steatózy hodnotíme podle zastoupení hepatocytů s tukovými vakuolami v cytoplazmě jako mírný (≤ 25 %), střední (≤ 50 %), pokročilý (≤ 75 %) a těžký (> 75 %). Pro NAFLD bývá používána pouze třístupňová škála – grade 1 (≤ 33 %), grade 2 (≤ 66 %) grade 3 (> 66 %) (1). Tyto údaje je možné získat od patologa při hodnocení jaterní biopsie. Informaci o přítomnosti tuku v játrech poskytují také zobrazovací metody.
ULTRASONOGRAFIE
Nejčastěji používaným zobrazovacím vyšetřením jater je sonografie. Sonografické vyšetření jater zahrnuje hodnocení morfologie jater, jejich povrchu (nejlépe lineární sondou), hodnocení jaterního parenchymu – jeho echogenity a přítomnosti dorsálního oslabení akustického signálu, vizualizaci a hodnocení intrahepatálních cév.
Echogenita normálního jaterního parenchymu je obdobná jako u parenchymu přiléhající pravé ledviny. Steatóza se projevuje vyšší echogenitou jater – játra jsou světlejší (obr. 1). Ne vždy je však takový rozdíl dobře patrný, takto lze dobře diagnostikovat steatózu středního a vyššího stupně. Můžeme použít i další sonografické známky steatózy, jako je přítomnost fokálního neztukovatění (zobrazuje se jako mapovitý okrsek nižší echogenity), typicky se vyskytující v blízkosti žlučníku nebo v jaterním hilu. Při pečlivém vyšetření u pacienta se steatózou je alespoň drobný okrsek neztukovatění u žlučníku patrný prakticky vždycky. Tento sonografický znak nám často pomůže odpovědět na otázku na přítomnost steatózy.
Image 1. Sonografický nález normálních jater (A) a jater se steatózou (B) 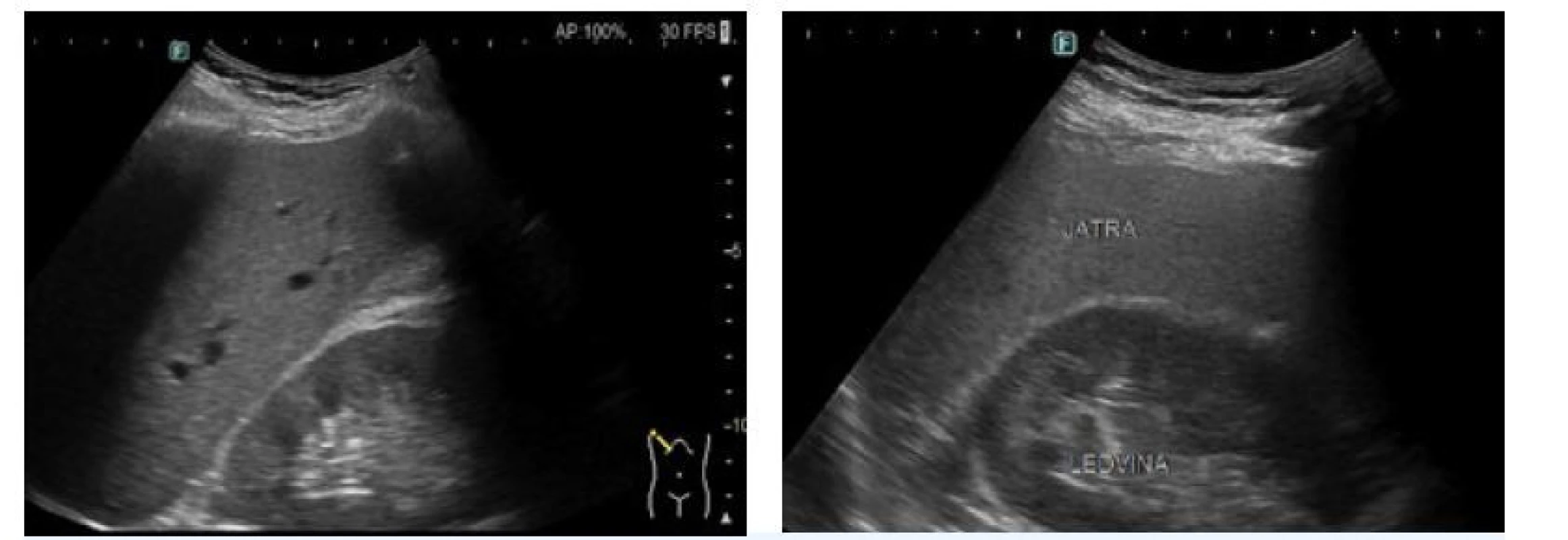
Senzitivita sonografie pro detekci steatózy je kolem 85 % pro alespoň středně pokročilou steatózu, specificita pak 93 % (2). Pro mírnou steatózu je senzitivita nižší, více zatížena subjektivitou hodnocení se senzitivitou 60–65 % pro steatózu grade 1 (3). Paradoxně u pacientů s BMI nad 35 je senzitivita sonografie opět podstatně nižší – 50–60 % (4). Pokud je steatóza sonograficky patrná, je tuk přítomen alespoň ve 20 % hepatocytů. CT vyšetření má menší diagnostický přínos než ultrasonografie (zejména kvůli nižší senzitivitě pro nižší stupně steatózy a variabilitě mezi přístroji) (5).
Další sonografickou známkou steatózy je přítomnost dorsálního oslabení (atenuace) akustického signálu. Tukové inkluze v hepatocytech fungují jako akustická rozhraní a vedou ke zpětnému odrazu, rozptylu a nižší penetraci akustického signálu, což přispívá k neostrosti kontur velkých jaterních cév a samo o sobě snižuje kvalitu zobrazení částí jater vzdálenějších od ultrazvukové sondy a zhoršuje tak vyšetřitelnost pacienta. Můžeme toho však využít k semikvantifikaci přítomné steatózy. Přítomnost výrazného dorsálního oslabení, kdy jsou neostré kontury velkých cév a není patrná bránice, odpovídá pokročilé steatóze grade 3 (obr. 2).
Image 2. Sonografické nálezy různě pokročilé steatózy grade 1, 2 a 3 – jasně patrný rozdíl v intenzitě dorzálního oslabení akustického signálu 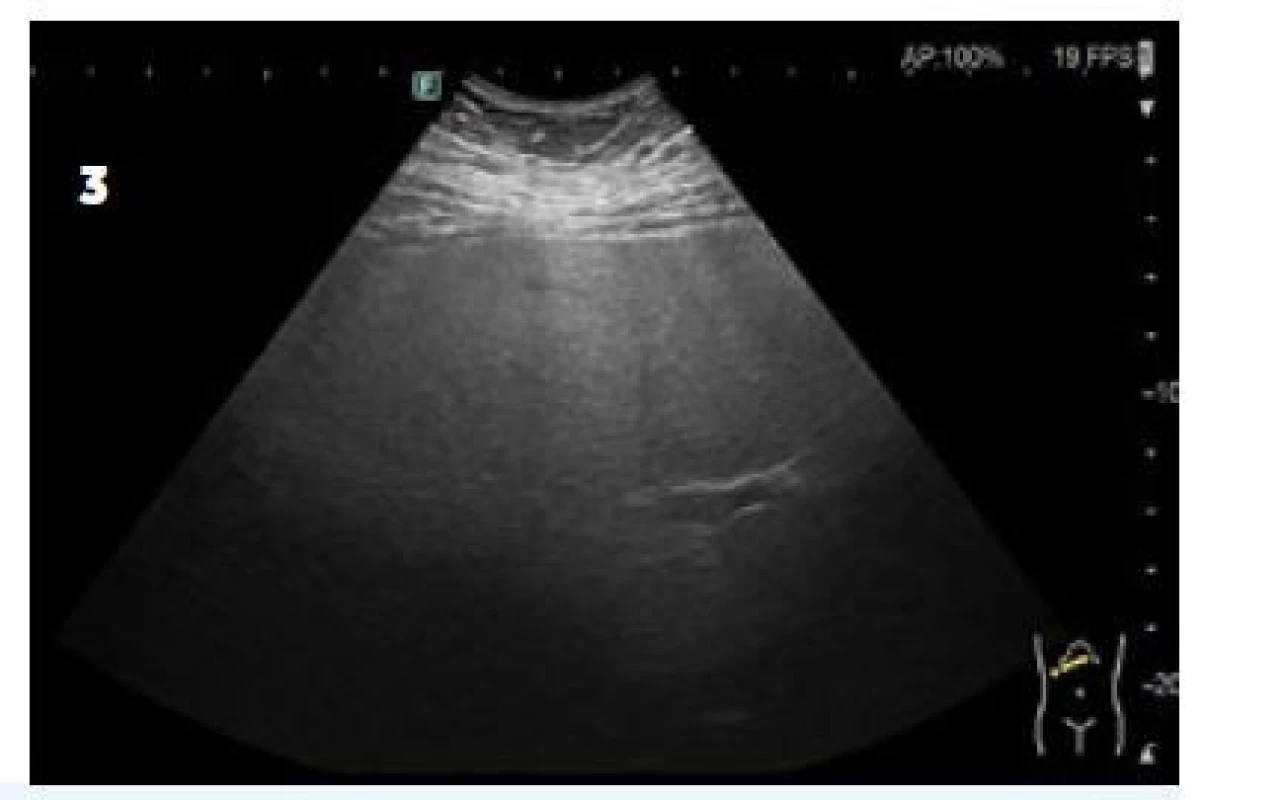
Další možností semikvantitativního hodnocení je počítačová analýza hepatorenálního indexu (HRI – hepatorenal index), tedy hodnocení rozdílů echogenity jater a pravé ledviny pomocí pokročilých algoritmů. Tato modalita bývá v současnosti standardně implementována do moderních ultrazvukových přístrojů. Podle některých literárních údajů funguje stejně přesně jako PDFF (protein density fat fraction) (6) nebo CAP (controlled attenuation parameter), viz níže. Hodnota HRI > 1,22 vykazovala při použití histologie jako referenčního standardu AUROC 0,90 a senzitivitu 76 % a specificitu 93 % pro steatózu ≥ grade 1 (7). HRI je lepší možností k potvrzení než k vyloučení steatózy, k rozlišování vyšších stupňů steatózy se však nehodí. Vzhledem ke snadnosti a rychlosti měření může mít do budoucna místo ve screeningu steatózy u rizikových skupin pacientů.
Kvantitativní sonografické metody
V posledních letech byly vyvinuty a do praxe zavedeny pokročilejší metody založené na hodnocení změn akustického signálu při průchodu jaterní tkání. Z klinického hlediska jde zejména o metody založené na výpočtu atenuačního koeficientu. Tyto techniky vypočítávají pomocí analýzy radiofrekvenčních ech detekovaných ultrazvukovou sondou atenuaci ultrazvukového signálu v tkáni. Takovou funkci dnes nabízí prakticky každý renomovaný výrobce ultrasonografických přístrojů.
Od roku 2010 je k dispozici na přístrojích FibroScan firmy Echosens modalita CAP (controlled attenuation parameter), která byla první komerčně dostupnou metodou sonografické kvantifikace steatózy. Od té doby byly publikovány stovky prací s jeho použitím. Měření je během měření tuhosti jaterní tkáně prováděno automaticky (a ve stejném objemu). Měřena je atenuace ultrazvukového signálu po průchodu jaterní tkání a výsledek je udáván v dB/m. Hodnoty se pohybují od 100 do 400 dB/m (obr. 3). Hodnota pro diagnózu steatózy není dosud jednoznačně určena. Např. 248 dB/m vykazovalo podle jedné metaanalýzy AUROC (plocha pod ROC křivkou) 0,82 a senzitivitu a specificitu 69 %, respektive 82 % (8). Z pozdějších literárních údajů vyplývá, že jeho optimální hodnota je nejspíše vyšší, kolem 290 dB/m (9, 10).
Image 3. Měření CAP přístrojem FibroScan – normální játra (A) a těžká steatóza grade 3 (B) 
Podle metaanalýzy 1270 biopticky ověřených pacientů s NAFLD vyšla senzitivita a specificita CAP pro mírnou steatózu (grade 1) 87 %, respektive 91 %, lepších výsledků bylo dosaženo pro mírnou než pro pokročilou steatózu (11). Pro výrazný překryv naměřených hodnot u jednotlivých stupňů pokročilosti jaterní steatózy se tato metoda zatím nehodí k longitudinálnímu sledování změn množství tuku v játrech. V tomto směru by v budoucnu bylo potřeba na základě histologických nálezů definovat klinicky významnou míru poklesu hodnoty CAP. Z tohoto důvodu je potřeba CAP zatím vnímat spíše jako nástroj k diagnostice jaterní steatózy bez nutnosti provádění klasické sonografie.
Další kvantitativní metodou je ATT (fatty liver attenuation index, Fujifilm), která stanovuje atenuační koeficient na základě rozdílů v atenuaci zachycených radiofrekvenčních signálů různých frekvencí. Měření probíhá v hloubce 4–10 cm, což napomáhá eliminovat vliv tloušťky podkožního tuku. Měření je spolu s elastografickým měřením prováděno v pravém jaterním laloku (obr. 4). Normální hodnota dosahuje 0,5–0,6 dB/cm/MHz, navržené hodnoty pro jednotlivé stupně jaterní steatózy pak ≥ S1/ ≥ S2/ ≥ S3 jsou 0,62/0,67/0,73 dB/cm/MHz se senzitivitou/specificitou 72 % / 82 %; 87 % / 72 %; 82 % / 89 % (12). Při použití cut-off hodnoty ≥ 0,66 dB/cm/MHz byla pro diagnózu steatózy grade 2/3 s AUROC 0,91 senzitivita 100 % a specificita 90 % (13). Další metody kvantifikace pracují s technikami spektrální analýzy akustického signálu, obálkové (envelope) statistiky hodnocení akustického rozptylu nebo pomocí analýzy rychlosti šíření zvuku, která je se stoupajícím množstvím tuku v tkáni nižší (3).
Image 4. ATT měření jater pacienta se středně pokročilou jaterní steatózou grade 2 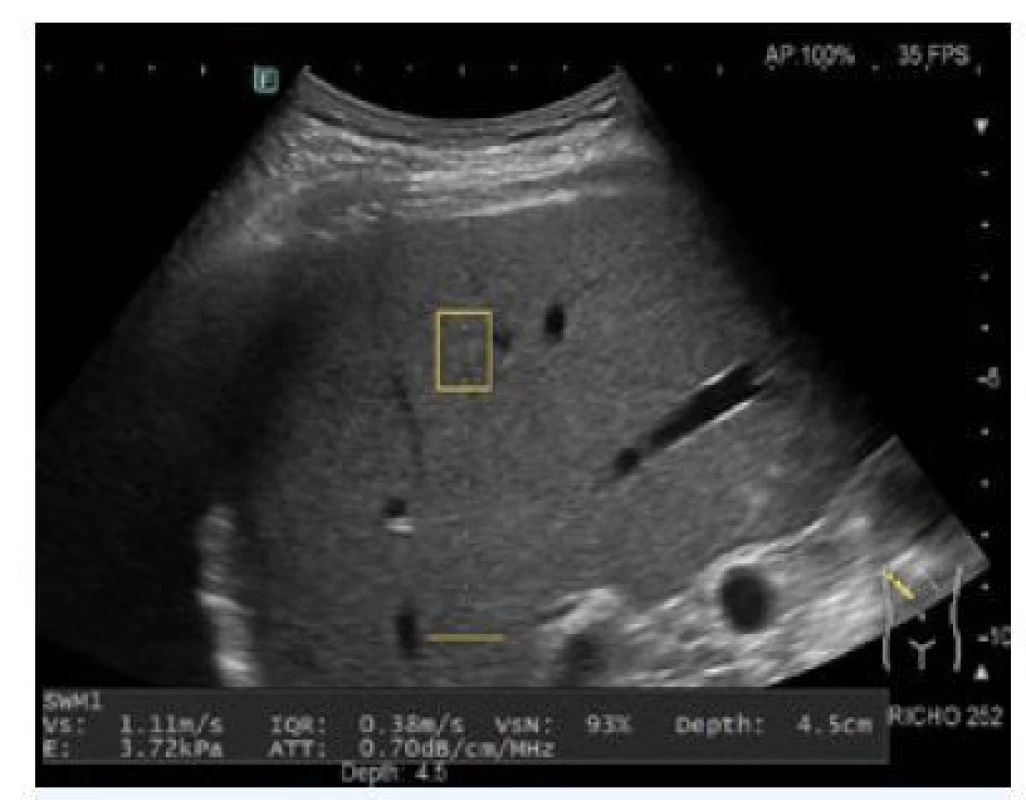
METODY ZALOŽENÉ NA MAGNETICKÉ REZONANCI
Běžné zobrazení jater magnetickou rezonancí se k diagnostice steatózy nehodí, a to zejména pro nízkou specificitu. V posledních letech ale byly vyvinuty speciální metody s vysokou diagnostickou hodnotou. V současnosti jsou používány zejména 2 metody – protonová (1H) MRI spektroskopie (MRS) a PDFF (proton density fat fraction).
MRI spektroskopie funguje na principu vizualizace protonů obsažených ve vodě (jeden peak je v oblasti 4,7 ppm, miliontin rezonančního kmitočtu) a protonů obsažených v tuku (vícečetné peaky). Frakce tuku v játrech je pak vypočítána jako poměr intenzity signálu protonů v tuku ku součtu intenzit signálu z tuku a vody. Ačkoliv princip MRS pro kvantifikaci jaterní steatózy je poměrně přímočarý, mohou vznikat určitá zkreslení. Hodnocení je prováděno v objemu jaterní tkáně o velikosti 8–27 cm3, což může být vzhledem k nehomogenní distribuci patologických změn v játrech limitující. Metoda PDFF funguje na principu zobrazování chemického posunu (CSI – chemical shift imaging). Využívá rozdílu ve frekvenci rezonance protonů obsažených ve vodě a v tuku. Za nejpřesnější je považována PDFF získaná pomocí T1-nezávislé, T2*-vážené multi-echo CSI, která umožňuje zhodnotit celá játra i s nerovnoměrnou distribucí tuku. Obě zmíněné MRI metody spolu navíc výborně korelují (14) a poskytují velmi dobré výsledky umožňující neinvazivní kvantifikaci jaterní steatózy. Jsou tak v současnosti považovány za referenční standard. Jejich zásadní nevýhodou je velmi nízká dostupnost v klinické praxi.
ZÁVĚR
Nemoci asociované s jaterní steatózou, tedy zejména nealkoholová a alkoholová jaterní choroby, představují nejčastější chronické jaterní onemocnění současnosti, proto má diagnostika steatózy prvořadý význam. V běžné klinické praxi je metodou první volby sonografické vyšetření. Má obecně dobrou vypovídací hodnotu, ale při mírném stupni steatózy horší senzitivitu a u výrazně obézních pacientů. Steatóza se projevuje vyšší echogenitou jaterního parenchymu; hodnocení dalších sonografických známek, jako jsou dorsální oslabení akustického signálu a přítomnost fokálního neztukovatění, umožňuje přesnější diagnostiku například u pokročilejší steatózy a při diagnostických nejasnostech. Totéž platí pro semikvantitativní hodnocení pomocí hepatorenálního indexu. Kvantitativní sonografické metody jsou dalším nástrojem, nejvíce dat bylo publikováno o metodě CAP. Ta může být v budoucnu screeningovým nástrojem u rizikových skupin pacientů. Metody založené na magnetické rezonanci – MR spektroskopie a PDFF umožňují přesnou neinvazivní kvantifikaci množství tuku v játrech.
Čestné prohlášení
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Seznam použitých zkratek
ALD alkoholová jaterní choroba
ATT Fatty Liver Attenuation Index
AUROC area under receiver operating characteristic (matematická metoda k hodnocení kvality testu)
BMI body mass index
CAP controlled attenuation parameter
CSI chemical shift imaging
HRI hepatorenální index
MRS magnetickorezonanční spektroskopie
MRI magnetická rezonance
NAFLD nealkoholová jaterní choroba při metabolickém syndromu
PDFF protein density fat fraction
Adresa pro korespondenci:
MUDr. Karel Dvořák, Ph.D.
Oddělení gastroenterologie a hepatologie
Krajská nemocnice Liberec, a. s.
Husova 357/10, 460 63 Liberec
Tel.: 485 312 678
e-mail: karel.dvorak@nemlib.cz
Sources
1. Kleiner DE, Brunt EM, Van Natta M et al. Design and validation of a histological scoring system for nonalcoholic fatty liver disease. Hepatology 2005; 41(6): 1313–1321.
2. Hernaez R, Lazo M, Bonekamp S et al. Diagnostic accuracy and reliability of ultrasonography for the detection of fatty liver: a meta-analysis. Hepatology 2011; 54(3): 1082–1090.
3. Ferraioli G, Berzigotti A, Barr RG et al. Quantification of liver fat content with ultrasound: a WFUMB position paper. Ultrasound Med Biol 2021; 47(10): 2803–2820.
4. de Moura Almeida A, Cotrim HP, Barbosa DB et al. Fatty liver disease in severe obese patients: diagnostic value of abdominal ultrasound. World J Gastroenterol 2008; 14(9): 1415–1418.
5. Dietrich CF, Shi L, Lowe A et al. Conventional ultrasound for diagnosis of hepatic steatosis is better than believed. Z Gastroenterol 2021, doi: 10.1055/a-1491-1771.
6. Marshall RH, Eissa M, Bluth EI, Gulotta PM, Davis NK. Hepatorenal index as an accurate, simple, and effective tool in screening for steatosis. Am J Roentgenol 2012; 199(5): 997–1002.
7. Moret A, Boursier J, Houssel Debry P et al. Evaluation of the hepatorenal B-mode ratio and the "controlled attenuation parameter" for the detection and grading of steatosis. Ultraschall Med 2020, doi: 10.1055/a-1233-2290.
8. Karlas T, Petroff D, Sasso M et al. Individual patient data meta-analysis of controlled attenuation parameter (CAP) technology for assessing steatosis. J Hepatol 2017; 66(5): 1022–1030.
9. Caussy C, Alquiraish MH, Nguyen P et al. Optimal threshold of controlled attenuation parameter with MRI-PDFF as the gold standard for the detection of hepatic steatosis. Hepatology 2018; 67(4): 1348–1359.
10. Petroff D, Blank V, Newsome PN et al. Assessment of hepatic steatosis by controlled attenuation parameter using the M and XL probes: an individual patient data meta-analysis. Lancet Gastroenterol Hepatol 2021; 6(3): 185–198.
11. Pu K, Wang Y, Bai S et al. Diagnostic accuracy of controlled attenuation parameter (CAP) as a non-invasive test for steatosis in suspected non-alcoholic fatty liver disease: a systematic review and meta-analysis. BMC Gastroenterol 2019; 19(1): 51.
12. Tamaki N, Koizumi Y, Hirooka M et al. Novel quantitative assessment system of liver steatosis using a newly developed attenuation measurement method. Hepatol Res 2018; 48(10): 821–828.
13. Cerit M, Sendur HN, Cindil E et al. Quantification of liver fat content with ultrasonographic attenuation measurement function: correlation with unenhanced multidimensional computerized tomography. Clin Imaging 2020; 65 : 85–93.
14. Noureddin M, Lam J, Peterson MR et al. Utility of magnetic resonance imaging versus histology for quantifying changes in liver fat in nonalcoholic fatty liver disease trials. Hepatology 2013; 58(6): 1930–1940.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

2022 Issue 2-
All articles in this issue
- ÚVODEM
- EDITORIAL
- Liver tests
- Diagnostic methods of fatty liver diseases
- Liver elastography
- Metabolic dysfunction-associated fatty liver disease (MAFLD) as a more accurate name for NAFLD – common aspects of pathogenesis
- Diagnosis of non-alcoholic fatty liver disease and its active screening in risk groups
- An overview of current therapy options of non-alcoholic fatty liver disease
- Statins and liver
- Alcohol-related liver disease in medical practice
- Current hepatitis C therapy
- Klinická obezitologie – nejen Základy
- Dietary habits in students from the medical faculties
- Za profesorem Peterem Krištúfkem, čestným prezidentem SLS
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


