-
Medical journals
- Career
Poruchy vodního a elektrolytového metabolismu a změny acidobazické rovnováhy u pacientů s ascitickou cirhózou jater
Authors: Halima Gottfriedová 1; Miroslava Horáčková 2; Milena Čáslavská 3; Julius Špičák 4; Otto Schück 5
Authors‘ workplace: Klinika hepatogastroenterologie TC IKEM 1; Interní klinika 2. LF UK a FN Motol 2; Klinika nefrologie TC IKEM 3; Klinika hepatogastroenterologie TC IKEM 4; Interní klinika 2. LF UK a FN Motol 5
Published in: Čas. Lék. čes. 2017; 156: 150-152
Category: Review Article
Overview
U pacientů s pokročilou jaterní cirhózou s ascitem jsou často přítomny poruchy metabolismu elektrolytů a vody, které jsou spojeny se změnami v acidobazické rovnováze. Tyto poruchy mohou být velmi komplikované, jejich diagnóza i léčba svízelné. Nejčastější poruchou je diluční hyponatremie. Hyponatremie je u cirhotiků spojena se zvýšenou morbiditou a mortalitou před i po transplantaci jater. Mezi další časté poruchy patří hyperchloremická acidóza, hypokalemie, metabolická alkalóza, laktátová acidóza a respirační alkalóza. Pokud se přidruží porucha funkce ledvin (například hepatorenální syndrom), může dojít k rozvoji metabolické acidózy a retenci kyselých metabolitů.
V patogenezi těchto stavů se uplatňují především změny hemodynamické. Aktivace renin-angiotenzin-aldosteronového systému a neosmotická stimulace antidiuretického hormonu spouštějí závažné změny ve vodním a natrio-chloridovém metabolismu. Klinicky se tato aktivace projevuje otoky, ascitem, hydrothoraxem, nízkou až nulovou koncentrací natria v moči a zvýšenou močovou osmolalitou, která je vyšší než sérová osmolalita. V praxi může být hodnocení významně modifikováno současně probíhající diuretickou léčbou. Podrobnější sledování změn vodního a elektrolytového metabolismu společně se změnami acidobazické rovnováhy u pacientů s ascitickou cirhózou jater je nezbytné nejen z hlediska diagnostického, ale především terapeutického.Klíčová slova:
ascitická cirhóza jater, diluční hyponatremie, retence bezsolutové vody, acidobazická rovnováha, diuretická léčba
U pacientů s ascitickou cirhózou jater (ACJ) se často setkáváme se závažnými poruchami vodního a elektrolytového metabolismu, které jsou spojeny se změnami acidobazické rovnováhy (ABR). Současné znalosti nasvědčují tomu, že tyto změny jsou obvykle komplikované, protože bývá souběžně vyjádřeno několik metabolických odchylek, které se také mohou kombinovat s odchylkami respiračními (1). U pacientů s ACJ se relativně často setkáváme s diluční hyponatremií (1–3, 5), diluční a hyperchloremickou acidózou (3, 4), laktátovou acidózou (3), metabolickou alkalózou (4), hypokalemií (4) a respirační hypokapnickou alkalózou (6).
Metabolické odchylky se mohou dále komplikovat při současném postižení ledvin (hepatorenální syndrom, nefropatie při chronických onemocněních jater) rozvojem metabolické acidózy spojené s retencí kyselých katabolitů a projevující se rozšířením aniontové mezery (anion gap). K výše zmíněným poruchám se mohou přidružit metabolické změny způsobené terapií, především diuretiky. Poruchy ve vodním, elektrolytovém a acidobazickém metabolismu se mohou výrazně podílet na morbiditě a mortalitě pacientů s ACJ před i po transplantaci jater (1).
Rozpoznání, zda a jak se jednotlivé metabolické odchylky uplatňují u jednotlivého pacienta, často nebývá jednoduché. Řada studií z posledních let podporuje předpoklad, že diference a poměr sérové koncentrace natria a chloridů (SNa+ − SCl− a SNa+/SCl−) mohou pomoci při hodnocení změn expanze tělesných tekutin a změn ABR (7–9). V tomto stručném přehledu se pokoušíme vytvořit (pokud možno) jednoduchý přehled patofyziologických procesů, které sledované poruchy podmiňují, a nastínit klinické možnosti jejich rozpoznání, což umožňuje zvolit správný terapeutický postup.
Image 1. Modifikované a doplněné schéma podle Ginese a Cardenase (1) 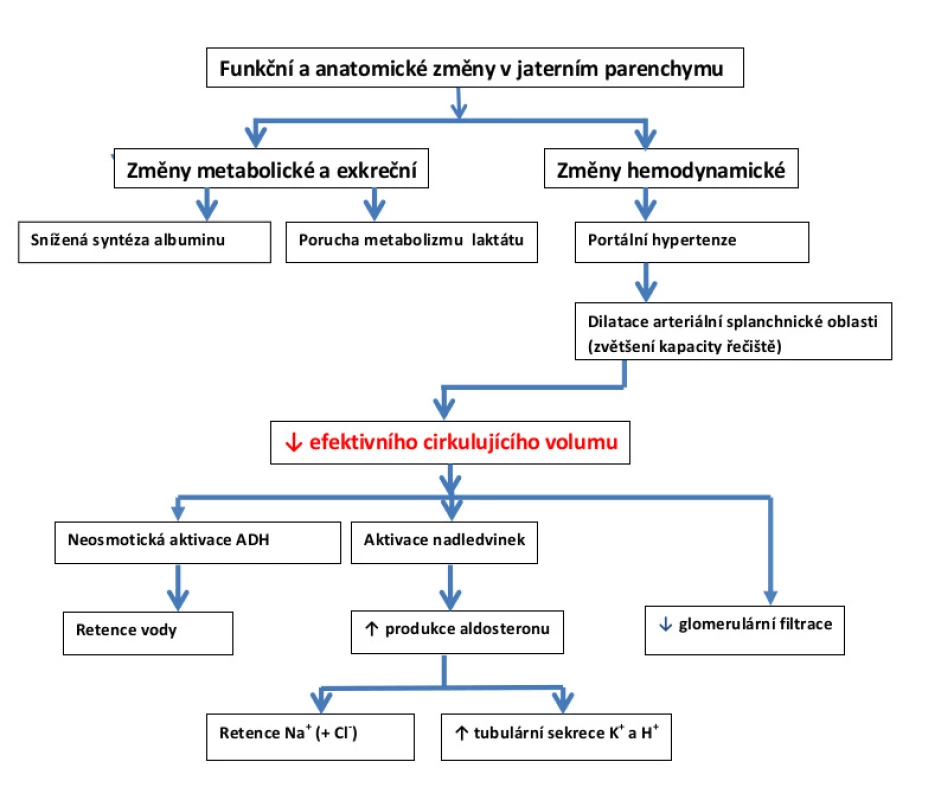
Obr. 1 zachycuje základní patofyziologické procesy, jež jsou podkladem pro sledované metabolické změny. Je z něj zjevné, že v rozvoji poruchy metabolismu vody, elektrolytů a ABR hrají u pacientů s ACJ významnou roli změny hemodynamické, které jsou indukovány snížením efektivního cirkulujícího volumu. V důsledku těchto hemodynamických změn, jež „mylně“ signalizují zmenšení objemu tělesných tekutin, dochází ke zvýšení produkce antidiuretického hormonu (ADH) a aldosteronu. Zvýšení produkce těchto hormonů působí závažné změny ve vodním a natrio-chloridovém metabolismu, které jsou provázeny změnami v ABR.
S hemodynamickými změnami souvisí též rozvoj kolaterál, které umožňují průnik substancí ze střeva do systémové cirkulace, aniž by byly podrobeny detoxikační kontrole jater. Další důležité metabolické změny v játrech nejsou ve schématu podrobněji rozebírány, protože nemusejí být provázeny poruchami v metabolismu vody, elektrolytů a ABR. Tyto změny se mohou projevit snížením metabolismu laktátu, zvýšením jeho sérové koncentrace a sníženou syntézou albuminu. Retence vody je spojena s diluční hyponatremií a společně s retencí natria (Na+) a chloridů (Cl−) s rozvojem hyperchloremické metabolické acidózy. Diluce vnitřního prostředí bezsolutovou vodou a následná hyponatremie je provázena poklesem sérové osmolality (Sosm).
Snížení efektivní osmotické koncentrace (tonicity) je asociováno s přesunem vody z extracelulární tekutiny do buněk. Tato osmotická ekvilibrace může podmínit edém mozku a významně se podílet na jaterní encefalopatii (2). Jak je uvedeno na obr. 1, tyto změny v metabolismu vody jsou podmíněny zvýšenou produkcí ADH. Při biochemickém vyšetření nemůžeme stanovit koncentraci ADH, ale jeho zvýšenou produkci můžeme posoudit podle vlivu na tubulární resorpci bezsolutové vody. V tomto případě se vytváří hypertonická moč i za podmínek hyponatremie a snížené tonicity extracelulární tekutiny. V klinické praxi tedy můžeme posoudit neadekvátní produkci ADH podle toho, že se při snížení Sosm (pod 275 mOsm/kg) vytváří moč, jejíž osmotická koncentrace (Uosm) je relativně vysoká, u pacientů s ACJ převyšuje Sosm a nikoliv vzácně dosahuje maximálních hodnot 800–1000 mOsm/kg (10).
Jak již bylo uvedeno, retence bezsolutové vody u pacientů s ACJ je provázena též retencí Na+. Pokles Sosm závisí na tom, v jakém poměru je retence bezsolutové vody a Na+. U pacientů s ACJ obvykle retence vody převyšuje retenci Na+ (s ohledem na normální poměr ve vnitřním prostředí). Retence vody a Na+ je důsledkem nejen jejich sníženého renálního vylučování, ale také velikosti jejich příjmu (zevní bilance). Sodík přijímaný v potravě je dán především příjmem soli (NaCl), ve které jsou Na+ a Cl− v ekvimolárním poměru 1 : 1. V extracelulární tekutině se tento poměr pohybuje okolo 1,4 : 1,0. Jestliže nemocný není schopen přijaté množství soli vyloučit, je retence Cl− relativně vyšší než retence Na+. Hodnota SCl− se za těchto podmínek snižuje méně než SNa+, ale nemusí se snižovat vůbec, dokonce se může i zvyšovat.
Hyperchloremie při současné hyponatremii se při běžném klinickém vyšetřování může projevit tím, že pokud korigujeme zjištěnou hodnotu SNa+ na normální hodnotu SNa+ (140 mmol/l), zjistíme, že SCl− převyšuje horní hranici normy 108 mmol/l. Za těchto podmínek se zvyšuje poměr SNa+/SCl− nad horní hranici normy, která v našich měřeních činí 1,37 (9). Současné stanovení diference SNa+ − SCl− rovněž umožňuje posoudit velikost expanze tělových tekutin. Normální hodnota SNa+ − SCl− se v našich měřeních pohybuje v rozmezí 32–38 mmol/l (9). Za podmínek diluce dochází ke snižování této diference pod dolní hranici normy. Proto je při klinickém hodnocení SNa+ u pacientů s ACJ důležité hodnotit též SCl−. Hyperchloremická acidóza při diluční hyponatremii se nemusí projevit v absolutní hodnotě SCl−, ale vztahem k SNa+. K rozvoji hyperchloremické acidózy u pacientů s ACJ může v některých případech přispět ještě zvýšené vylučování HCO3− v důsledku renální tubulární acidózy (RTA). Dále se na rozvoji metabolické acidózy může podílet zvýšení sérové koncentrace laktátu v souvislosti s jeho sníženým metabolismem v játrech. Zvýšení sérové koncentrace laktátu se může podílet i na hodnotě anion gap (AG).
Obr. 2 pak zachycuje, jak dalece se uvedené patofyziologické procesy projevují při biochemickém vyšetření odchylek vnitřního prostředí. Za účelem zjednodušení jsou na obrázku probírané metabolické změny ve vnitřním prostředí rozděleny z hlediska změn ABR na acidifikační a alkalizační.
Image 2. Vliv acidifikačních a alkalizačních procesů na biochemické změny ve vnitřním prostředí u pacientů s ACJ 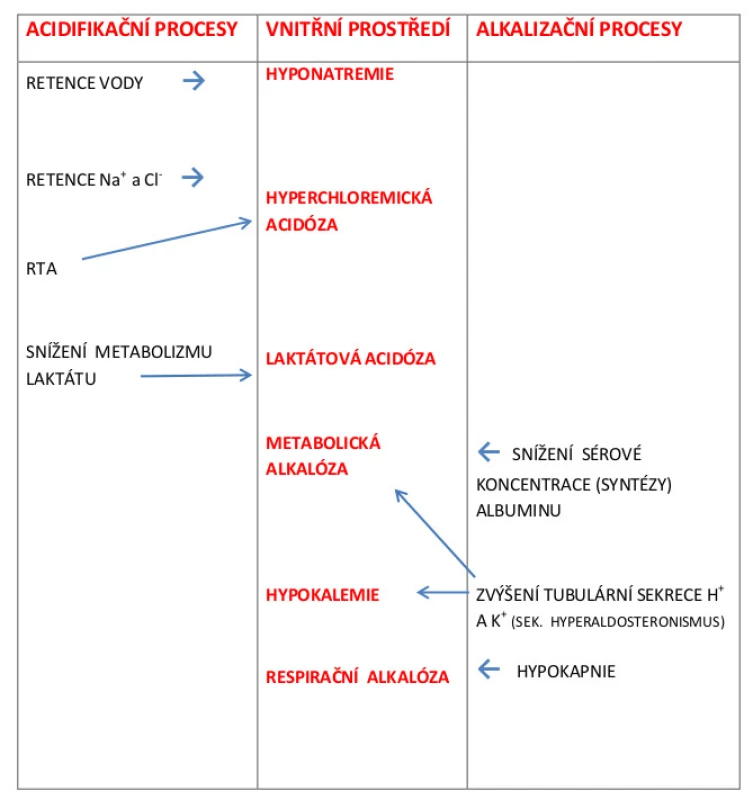
Jak je patrno z obr. 2, na stavu ABR se mohou významně podílet i procesy alkalizační. U pacientů s ACJ se z tohoto hlediska významně uplatňuje snížení sérové koncentrace albuminu (Salb). Z těchto důvodů musíme hodnotu AG korigovat na normální hodnotu Salb (obvykle 40 mmol/l). Užívá se korekce, která předpokládá, že snížení Salb o 10 mmol/l je spojeno se zvýšením AG o 2,5 mmol/l (11). Na rozvoji metabolické alkalózy se u pacientů s ACJ podílí sekundární hyperaldosteronismus tím, že zvyšuje tubulární sekreci H+ a K+. Tyto změny v tubulárním transportu se mohou podílet na rozvoji hypokalemie, která je u pacientů s ACJ závažnou komplikací. Pozoruhodný je nález, že u pacientů s ACJ dochází relativně často k rozvoji respirační alkalózy (12). Při biochemickém vyšetření se tato porucha projevuje snížením pCO2 (hypokapnií). Příčina respirační alkalózy u cirhotiků dosud není uspokojivě vysvětlena (12). Renální kompenzace respirační alkalózy spočívá ve zvýšené retenci Cl− a zvýšeném vylučování HCO3−.
Kombinace uvedených změn v ABR se nutně nemusí projevit na změně pH vnitřního prostředí, které může zůstávat v mezích normy i při závažných metabolických poruchách díky kombinaci acidifikačních a alkalizačních procesů (3).
Změny vnitřního prostředí a elektrolytového metabolismu u pacientů s ACJ mohou být významně ovlivněny terapií diuretiky. U těchto nemocných je diuretikem volby antagonista aldosteronu. V praxi se nejčastěji užívá spironolakton, který působí v distálním úseku nefronu. Jeho působením dochází ke snížení tubulární resorpce Na+ a snížení tubulární sekrece K+ a H+ (13). Tyto změny se mohou podílet na rozvoji metabolické alkalózy a hyperkalemie (zvláště u pacientů s výrazně sníženou glomerulární filtrací). Jako další diuretikum se často užívá furosemid, obvykle v kombinaci se spironolaktonem. Furosemid působí v ascendentním raménku Henleovy kličky, snižuje resorpci Na+, K+, Cl− a bezsolutové vody. Při intenzivnějším působení furosemidu může docházet k rozvoji metabolické alkalózy a k hypokalemii. Tyto změny se mohou projevit zvyšováním SNa+ − SCl− a SNa+/SCl−. Malé dávky furosemidu mohou přispět k normalizaci SNa+ a snížení hyperchloremické acidózy, proto je u pacientů s ACJ doporučováno pouze nízké dávkování (1). Větší dávky naopak mohou podmínit prohloubení hyponatremie v důsledku deplece Na+ a Cl−. Thiazidová diuretika se u pacientů s ACJ nedoporučují, protože vedle zvýšeného vylučování Na+ a Cl− v distálním tubulu podmiňují také aktivaci ADH a zadržují vodu (14).
Dávkování diuretik u pacientů s ACJ a jejich vliv na změny vnitřního prostředí jsou častým terapeutickým problémem. Podrobnější sledování změn acidobazické rovnováhy u pacientů s ACJ léčených diuretiky je důležité nejen z hlediska diagnostického, ale zejména terapeutického.
Prohlašuji, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsem ve střetu zájmů. Vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů článku.
Seznam použitých zkratek
ABR acidobazická rovnováha
ACJ ascitická cirhóza jater
ADH antidiuretický hormon
RTA renální tubulární acidóz
Adresa pro korespondenci:
MUDr. Halima Gottfriedová, CSc.
Klinika hepatogastroenterologie
Transplantcentrum IKEM
Vídeňská 1958/9
140 21 Praha 4
Tel.: 603 869 905
e-mail: Halima.Gottfriedova@ikem.cz
Sources
1. Ginès P, Cárdenas A. The management of ascites and hyponatremia in cirrhosis. Semin Liv Dis 2008; 28 : 43–58.
2. Restuccia T, Gómez-Ansón B, Guevara M et al. Effects of dilutional hyponatremia on brain organic osmolytes and water content in patients with cirrhosis. Hepatology 2004; 39 : 1613–1622.
3. Funk GC, Doberer D, Osterreicher C et al. Equilibrium of acidifying and alkalinizing metabolic acid-base disorders in liver cirrhosis. Liver Int 2005; 25 : 505–512.
4. Oster JR, Perez GO. Acid-base disturbances in liver disesase. J Hepatol 1986; 2 : 299–306.
5. John S, Thuluvath PJ. Hyponatremia in cirrhosis: pathophysiology and management. World J Gastroenterol 2015; 21 : 3197–3205.
6. Ahya SN, José Soler M, Levitsky J, Batlle D. Acid-base and potassium disorders in liver disease. Semin Nephrol 2006; 26 : 466–470.
7. Nagaoka D, Nessar Junior AP, Maciel AT et al. The use of sodium-chloride difference and chloride-sodium ratio as strong ion difference surrogates in the evaluation of metabolic acidosis in critically ill patients. J Crit Care 2010; 25 : 525–531.
8. Kurt A, Ecevit A, Ozkiraz S et al. The use of chloride-sodium ratio in the evaluation of metabolic acidosis in critically ill neonates. Eur J Pediatr 2012; 171 : 963–969.
9. Schück O, Horáčková M. Diference a poměr sérových koncentrací natria a chloridů u pacientů s hyponatremií. Vnitřní lékařství 2016; 62 : 629–634.
10. Schück O, Hoenig V, Šmahelová R. Liver cirrhosis and the elaboration of hypertonic urine. Rev Czech Med 1960; 6 : 112–117.
11. Jabor A. Vnitřní prostředí. Grada Publishing, Praha, 2008.
12. Stanley NN, Salisbury BG, McHenry LC Jr, Cherniack NS. Effect of liver failure on the response on ventilation and cerebral circulation to carbon dioxide in man and in the goat. Clin Sci Mol Med 1975; 49 : 157–169.
13. Greger R, Heidland A. Action and clinical use of diuretics. In Davison AM et al. Oxford Textbook of Clinical Nephrology, 2nd ed. Oxford University Press: Oxford, New York, Tokyo, 1998 : 2679–2706.
14. Rosner MH. Severe hyponatremia associated with the combined use of thiazide diuretics and selective serotonin reuptake inhibitors. Am J Med Sci 2004; 327 : 109–111.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

-
All articles in this issue
- Bazaliom a možnosti jeho terapie
- Lymphogranuloma venereum (lymphogranuloma inquinale, morbus Nicolas-Favre-Durand)
- Komorbidity psoriázy
- Chronická kopřivka – nové pohledy na diagnostiku a léčbu onemocnění
- Hidradenitis suppurativa – symptomy, diagnostika a léčba
- Hirsutismus – etiopatogeneze, diagnostika a léčba
- Choroby postihující kůži kštice
- Androgenní alopecie žen
- Mezoterapie v trichologii
- Psychologie ztráty vlasů
- Poruchy vodního a elektrolytového metabolismu a změny acidobazické rovnováhy u pacientů s ascitickou cirhózou jater
- Povinnosti a oprávnění poskytovatele zdravotních služeb v souvislosti s podáváním stížností
- Posvátné okrsky boha lékařství Asklépia ve starověkých Athénách
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Bazaliom a možnosti jeho terapie
- Choroby postihující kůži kštice
- Hirsutismus – etiopatogeneze, diagnostika a léčba
- Androgenní alopecie žen
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

