-
Medical journals
- Career
Jaká jsou specifika syndromu diabetické nohy a proč potřebujeme mezioborová doporučení pro jeho diagnostiku a léčbu?
Authors: Alexandra Jirkovská 1; Vladimíra Fejfarová 1; Michal Dubský 1; Veronika Wosková 1; Jiří Jarkovský 2,3; Klára Benešová 2,3; Tomáš Pavlík 2,3
Authors‘ workplace: Centrum diabetologie Institutu klinické a experimentální medicíny, Praha 1; Ústav zdravotnických informací a statistiky ČR, Praha 2; Institut biostatistiky a analýz, Lékařská fakulta Masarykovy univerzity, Brno 3
Published in: Vnitř Lék 2021; 67(8): 489-494
Category:
Overview
Péče o pacienty se syndromem diabetické nohy (SDN) vyžaduje mezioborovou spolupráci, a proto jsou na místě i mezioborová doporučení zaměřená na diagnostiku i léčbu a prevenci SDN. Tato doporučení potřebujeme také proto, že SDN má svá specifika, která ovlivňují jeho diagnostiku, terapii, ale i prognózu pacientů. Patří mezi ně např. odlišný průběh infekce a ICHDK u pacientů s diabetem, diagnostika neuropatické Charcotovy osteoartropatie i častá asociace s pokročilým onemocněním ledvin, které zhoršuje průběh SDN a zvyšuje jeho riziko. V neposlední řadě patří mezi specifika SDN problematika amputací s výrazně horší prognózou než u osob bez diabetu. Vytvoření interdisciplinárního týmu v podiatrických ambulancích, zajišťujícího komplexní péči o pacienty se SDN podle zásad uvedených v doporučeném postupu, je spojeno se zlepšením prognózy pacientů se SDN, zejména snížením amputací.
Klíčová slova:
syndrom diabetické nohy – infekce – amputace – ICHDK – Charcotova osteoartropatie
Úvod
Cílem článku je v rámci rubriky „Dobrá rada“ odpovědět na danou otázku a poskytnout rychlou a praktickou radu. Na úvodní otázku „Proč potřebujeme mezioborová doporučení pro syndrom diabetické nohy (SDN)“ bychom mohli jednoduše odpovědět stručně: tato doporučení potřebujeme proto, že SDN má svá specifika, která ovlivňují jeho diagnostiku, terapii, ale i prognózu pacientů. V následujícím textu se pokusíme některá specifika SDN objasnit.
Hned úvodem je nutné zdůraznit, že péče o pacienty se SDN je typickým příkladem mezioborové spolupráce, a proto jsou na místě i mezioborová doporučení. Studie po celém světě ukázaly, že vytvoření interdisciplinárního podiatrického týmu, zajišťujícího komplexní péči o pacienty se SDN podle zásad uvedených v doporučeném postupu, je spojeno se snížením amputací (1, 2), což je hlavním cílem doporučených postupů. Pokud není možné vytvořit hned od počátku komplexní podiatrický tým, doporučuje se zaměřit se na jeho sestavování „krok po kroku“, s postupným zapojením různých odborníků. Např. diabetolog v rámci předatestační přípravy získá praxi na podiatrické ambulanci, podobně i chirurg a protetik se mohou specializovat na podiatrii a získat praxi na podiatrické ambulanci, zdravotní sestra může absolvovat certifikovaný kurz pro všeobecné sestry v podiatrii. Tento tým pak může vytvořit podiatrickou ambulanci na základě pravidel uvedených v Doporučených postupech České diabetologické společnosti (3). Konziliární spolupráce je nutná také s dalšími odborníky – intervenčními radiology, angiology, infekcionisty, internisty, praktickými lékaři, dermatology, plastickými chirurgy, domácí péčí, psychology, sociálními pracovnicemi, fyzioterapeuty apod. Samozřejmě je nutné péči o pacienta se SDN koordinovat tak, aby jednotliví odborníci pracovali podle obdobných pravidel a aby nedocházelo k polypragmazii. Soustředění péče o pacienta se SDN do podiatrické ambulance umožňuje pacientovi lépe dodržovat léčebná opatření a končetinu nadměrně nezatěžovat. Vlastní diagnostika a hojení SDN je závislé na řadě faktorů na kvalitní komplexní podiatrické péči zejména v podiatrických ambulancích, ale i na péči interní (4) a na péči dalších lékařů, zejména praktických lékařů v první linii a ambulantních specialistů.
Která jsou podle našich zkušeností hlavní specifika SDN?
SDN (Obr. 1) je definován jako infekce, ulcerace nebo destrukce tkání nohy spojené s neuropatií a/nebo ICHDK u pacientů s diabetem (1).
A právě klinické I laboratorní charakteristiky hlavních patogenetických faktorů, tj. infekce, ICHDK a neuropatie dolních končetin, mají u diabetiků svá specifika a budeme se jim věnovat v následujícím textu.
Pozornost zasluhuje také neuropatická Charcotova osteoartropatie (CNO), která má svá specifika a pacienti bývají poměrně často nesprávně diagnostikováni a léčeni pod jinými diagnózami (5, 6). Proto se CNO budeme také dále věnovat.
Dalším specifikem v diagnostice a léčbě SDN je častá kombinace s pokročilým stadiem onemocnění ledvin, které má vliv nejen na vysoké riziko SDN, ale i na jeho průběh a prognózu (7–9).
Svá specifika má i hojení diabetických ulcerací na nohou, které je komplikováno výraznou tkáňovou ischemií při postižení makrocirkulace i mikrocirkulace, infekcí I neuropatií, imunodeficitem i dekompenzací diabetu. Řada metabolických pochodů je v rámci hojení ran vlivem dlouhodobého diabetu postižena. Tato problematika přesahuje rozsah článku, a proto se jí podrobněji nevěnujeme a odkazujeme příslušné přehledové články (10–12).
Hlavním problémem, se kterým se podiatricky zaměření lékaři potýkají, je velký sklon pacientů k rekurencím diabetických ulcerací (do 3 let téměř v 60 %) a k rekurenci infekcí nohou (do 3 let např. v 25 %). Dalším problémem, který musíme v podiatrických ambulancích řešit, je také reaktivace CNO se vznikem deformit, k níž by při dobré dispenzarizaci a edukaci pacientů docházet nemuselo (5, 6, 13, 14). V neposlední řadě je pro diabetiky se SDN specifické riziko amputací spojené s vysokou mortalitou, převážně na kardiovaskulární onemocnění (1, 15). Některým z uvedených specifických faktorů se budeme věnovat podrobněji v následujícím textu.
Specifika infekce u SDN (1, 3, 4, 16)
Infekce syndromu diabetické nohy (SDN) je nejčastější příčinou hospitalizace pro komplikace diabetu a nejčastější příčinou amputací:
Infikované ulcerace se do roka zhojily pouze ve 46 %, 15 % pacientů zemřelo a 17 % potřebovalo amputaci a 22 % zůstalo nezhojeno (17).
Příznaky infekce SDN jsou mitigovány neuropatií, ICHDK a imunodeficiencí diabetiků.
Chronická hyperglykemie může potencovat infekci SDN a akutní hyperglykemie může být známkou progrese infekce.
Z hlediska rozpoznání akutního stadia SDN je nejdůležitější včas rozpoznat infekci. U diabetiků mohou být známky a příznaky infekce maskovány přítomností periferní neuropatie, ischemické choroby dolních končetin nebo imunitní dysfunkcí. Zánětlivá odpověď vyvolaná infekcí může způsobit tlak v kompartmentu, který, pokud překročí kapilární tlak, vede k nekróze ischemické tkáně a k rychlé progresi infekce. Anatomická predispozice šlach a jejich obalů uvnitř kompartmentů usnadňuje proximální šíření infekce, z oblasti s vyšším tlakem do oblasti s nižším tlakem. Faktory bakteriální virulence a oslabené imunitní odpovědi u diabetiků s neuropatií nebo se špatnou kompenzací diabetu mohou také hrát roli.
Systémové příznaky infekce (např. horečka, zimnice), výrazná leukocytóza nebo závažné metabolické poruch, jsou u diabetiků s infekcí SDN méně časté, tím spíše jejich přítomnost svědčí pro závažnou, končetinu ohrožující (nebo dokonce život ohrožující) infekci. Zkušený lékař s podiatrickou erudicí by tedy měl optimálně zhodnotit pacienta se závažnější infekcí SDN do 24 hodin. Hnisavá sekrece, zejména pokud je pod tlakem nebo pokud je spojená s nekrózou, vyžaduje okamžitou (obvykle do 24 hodin) dekompresi a drenáž. Přestože při léčbě osteomyelitidy je často nutná resekce kosti (nejlépe malá), může být velmi závažná i infekce měkkých tkání bez osteomyelitidy (např. flegmóna) a vyžaduje urgentně antimikrobiální terapii i chirurgický zákrok (např. discisii, drenáž apod.).
U diabetika se suspektní infekcí, u kterého je klinické vyšetření sporné, doplňte vždy vyšetření sérových biomarkerů zánětu, například C‑reaktivního proteinu, sedimentace erytrocytů (FW) a v některých případech i prokalcitoninu. Ve srovnání s FW mají hladiny CRP tendenci rychleji stoupat s rozvojem infekce a rychleji klesat při jejím ústupu. Hodnoty FW mohou být ovlivněny různými komorbiditami (např. anémií, uremií), nemusí být také zvýšeny u akutních infekcí v důsledku relativně pomalé odezvy tohoto biomarkeru, ale vysoce zvýšená FW (≥ 70 mm/h) je suspektní z postižení osteomyelitidou. Pokud přetrvává podezření na osteomyelitidu, pro které ale nesvědčí jednoznačně rtg či jiné morfologické vyšetření (CT, MR), nebo pokud neustupují známky infekce a je vhodné změnit antibiotickou léčbu, doporučuje se provedení kostní biopsie a mikrobiologické vyšetření kostního vzorku.
Specifika ischemické choroby dolních končetin (ICHDK) (3, 18, 19)
Hlavní odlišností průběhu ICHDK u pacientů s diabetem je chybění typických známek ICHDK, které vídáme u osob bez diabetu, a to:
klaudikací,
šelestů nad femorálními arteriemi,
nehmatných periferních pulzací.
Navíc nelze často využít v diagnostice neinvazivní vyšetření ICHDK, jako např. vyšetření dopplerovského indexu kotník/paže (ABI), a to pro jeho zkreslení mediokalcinózou. Toto vyšetření nám pomáhá především při stanovení rizika SDN u pacientů bez závažnějšího postižení neuropatií a ulceracemi. ABI < 0,9 je užitečným testem pro detekci ICHDK prakticky u všech vyšetřovaných diabetiků; avšak ABI > 0,9 plně nevylučuje ICHDK, zejména u těch s mediokalcinózou a těžší neuropatií. Můžeme využít další vyšetření, např. měření palcových tlaků a indexů, které jsou méně ovlivněny mediokalcinózou, nebo ultrazvukové vyšetření tepen, které se díky zkušenostem vyšetřujících a kvalitě přístrojů dostává do popředí. V neposlední řadě doporučujeme u pacientů se SDN vyšetřit tkáňovou tenzi kyslíku TcPO2, která nám velmi dobře, pokud jsou zachována všechna doporučení pro správné měření, predikuje prognózu hojení, určí vhodnou indikaci pro revaskularizaci i posoudí efekt revaskularizace či restenózu, případně pomůže určit optimální úroveň amputace.
Pro pacienty s již rozvinutou neuroischemickou nebo nehojící se ulcerací se přístup k cévnímu vyšetření liší od vyšetření preventivního. Měli bychom posoudit arteriální řečiště na dolních končetinách s cílem indikovat revaskularizaci, a to co nejdříve. Pokud je dostupné, je vhodné zvolit vyšetření magnetickou rezonancí (MR angiografii) Kvalitními přístroji lze dobře zobrazit i podkolenní řečiště a tepny nohy, a to i při mediokalcinóze. Limitací je schopnost pacienta podstoupit déle trvající vyšetření, nebo i větší obezita nebo kontraindikace MR vyšetření. CT angiografie má u diabetiků více limitací, mezi něž patří zejména obtížné zobrazení bércového řečiště při mediokalcinóze a riziko kontrastové nefropatie při ambulantním výkonu, při němž není zajištěna dostatečná hydratace ani kontrola renálních funkcí (nejlépe za 2–3 dny po výkonu) a množství kontrastu může být vyšší než při samotném jednostranném zobrazení tepen při digitální subtrakční angiografiii. Vyšetření tepenného řešiště je možné provést akutně i pomocí již zmíněného ultrazvuku nebo verifikovat tkáňovou ischemii pomocí transkutánní tenze kyslíku. Digitální subtrakční angiografii indikujeme vždy, pokud zvažujeme revaskularizaci. Nejlépe ji provádíme po vyloučení stenóz v oblasti pánevního řečiště a třísla ultrazvukem tak, aby bylo možné provést současně s diagnostickou angiografií i PTA a pacient nebyl zatěžován dvakrát kontrastem i riziky tohoto vyšetření.
Charcotova neuropatická osteoarthropatie (5, 6)
CNO je onemocnění postihující kosti, klouby i měkké tkáně nohy a kotníku, které je v časné fázi charakterizováno neinfekčním zánětem. Souhrn příznaků CNO tvoří „Syndrom Charcotovy nohy“. Vzniká především následkem diabetické neuropatie, a to jak senzomotorické, tak autonomní.
V patogenezi tohoto onemocnění se uplatňují vedle neuropatie a diabetu také trauma a metabolické změny, v podstatě se jedná o mikrofraktury neuropatické kosti, které stimulují zánětlivé cytokiny a osteolýzu v akutním stadiu a mohou vést k deformitám při nedostatečné léčbě (Obr. 1). S jakými specifiky a problémy se u CNO setkáváme?
Velmi často se na něj nemyslí a pacient je chybně léčen pod jinými diagnózami.
I při správné diagnostice se často otálí s úplným odlehčením a znehybněním postižené končetiny obdobně jako při léčbě fraktury.
Celková doba léčby se podcení, po ukončení odlehčení není kontrolována aktivita tohoto onemocnění porovnáním kožní teploty (cave bilaterální postižení) na obou končetinách a s odstupem i pomocí MR nebo SPECT‑CT.
Pacienti nejsou po zklidnění aktivní fáze dostatečně edukováni a dispenzarizováni.
Je pouze málo ortopedů či podiatrických chirurgů, kteří se věnují chirurgické léčbě tohoto onemocnění, především u nestabilních forem CNO a korekci deformit.
Pacient s CNO má být vyšetřen i z hlediska možného současného výskytu osteomyelitidy (především sledování zánětlivých parametrů, v případě ulcerací také mikrobiologické kultivace ze tkání).
Je nutné posoudit i cévní řečiště, pokud se ulcerace u pacienta s CNO nehojí. Není vyloučena koincidence s ICHDK.
Je nutné zvážit, že každá infekce, chirurgický zákrok, další trauma, revaskularizace apod. mohou opět CNO znovu aktivovat a pacient musí nohu ihned odlehčit.
Nejsou často k dispozici vhodné odlehčovací techniky a zdravotnické prostředky: např. speciální sádrové fixace či dlahy, speciální sériové či individuální ortézy typu Sarmiento, zevní fixatéry či kvalitní vnitřní fixace, vhodná obuv v chronickém stadiu apod..
V neposlední řadě je nutné pamatovat na to, že neuropatické postižení končetin je oboustranné a že je druhá končetina rovněž ohrožena CNO, zejména pokud ji pacient více zatěžuje při odlehčení druhé končetiny a aktivním CNO nebo s ulcerací. CNO se může vyskytovat i v jiných lokalizacích než na noze.
Image 1. Typický syndrom diabetické nohy: kombinace Charcotovy osteoarthropatie, deformit, ulcerací a infekce 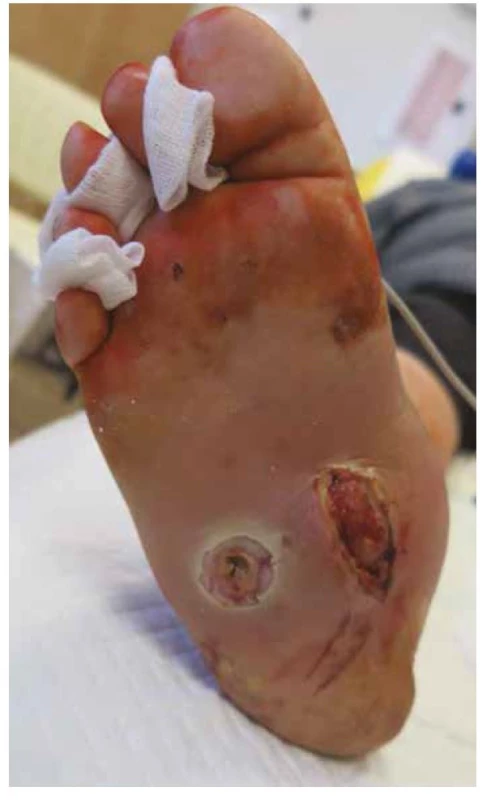
Pro správnou diagnostiku CNO je nutné při otoku nohou, často jednostranném nebo asymetrickém, u diabetika, a to i bez deformit nebo s deformitami, vyšetřit neuropatii, změřit oboustranně kožní teplotu (při rozdílu více než 1 °C již zvažovat patologický proces nohy), udělat rentgen nohy či jiné vyšetření, které ukáže změny časněji (např. MR nebo SPECT CT, případně třífázová scintigrafie) a nabrat zánětlivé parametry a případně i parametry kostní remodelace (např. CRP, ALP, kolagenní fragmenty).
V diferenciální diagnóze zvažujeme především:
osteomyelitidu a/nebo flegmónu (pozor, mohou se vyskytovat simultánně nebo na sebe navazovat),
prosté fraktury kostí nohy,
poúrazové stavy – hematomy,
flebotrombózu,
infekční artritidu (např. i borreliózu), případně jiný typ artritidy (dnavou, revmatickou apod.),
erysipel (doporučujeme doplnit ASLO, dochází často k záměně s flegmónou s jinými mikrobiálními agens).
Asociace SDN s onemocněním ledvin u diabetiků (7–9)
Specifika SDN u diabetiků se současným závažnějším postižením ledvin spatřujeme především v tom, že mají vyšší riziko SDN, a to jak ulcerací, tak CNO, z následujících důvodů:
mají těžší neuropatii kombinované etiologie (diabetická i uremická),
mají proto i větší riziko Charcotovy osteoartropatie, protože se těžší neuropatie kombinuje s multifaktoriálním kostním postižením,
častěji bývá postižena makro - i mikrocirkulace a mediokalcinóza,
větší sklon k infekci je dán sníženou imunitou, obtížné hojení infekce je podmíněno sklonem k rezistenci na antibiotika (20) a větší riziko osteomyelitidy souvisí se zhoršeným průnikem antibiotik do tkání nohy,
dialyzační terapie je potenciálně nezávislý rizikový faktor SDN, což je dáno např. snížením oxygenace tkání při hypotenzi, imobilizací pacientů a jejich rizikem dekubitů pat během dialýz. V neposlední řadě mají pacienti na hemodialýze problémy s odlehčením končetin při dojíždění na hemodialýzu, roli hraje i psychosociální zátěž vedoucí ke snížené adherenci s léčbou.
Amputace u syndromu diabetické nohy, problematika rekurence SDN (1–3)
Mezi možné příčiny vysokých amputací u diabetiků patří v dnešní době především:
pozdní hospitalizace pacientů – s hlubokým defektem nebo flegmónou, mnohdy až ve stadiu sepse,
pozdní diagnostika i léčba Charcotovy osteoartropatie,
nedostatečně léčená infekce, zvláště osteomyelitida a flegmóna,
těžká ischemie dolních končetin u pacientů s diabetem, kterou již není možné léčit revaskularizací,
dlouhodobě špatně kompenzovaný diabetes,
kouření a další rizikové faktory aterosklerózy,
vrůstající počet pacientů s renální insuficiencí.
Diabetik by měl být indikován k vysoké amputaci až po vyčerpání všech možností konzervativní léčby včetně chirurgických zákroků na noze, které zachovávají funkční končetinu (např. parciální nízké amputace, resekce postižených kloubů, odstranění infikovaných kostí). Do komplexní léčby patří vždy kontrola důsledného odlehčení končetiny např. speciální kontaktní dlahou či fixací nebo vhodnou ortézou, včasná a dostatečně účinná léčba infekce apod. Diabetici mají po vysokých amputacích podstatně horší prognózu než lidé bez diabetu – jejich pětiletá mortalita dosahuje 70 %, a pokud jsou dialyzováni, tak mají mortalitu až 74 % již za dva roky od amputace (21).
Příčin horší prognózy diabetiků po vysokých amputacích je hned několik, např.:
vysoký výskyt rizikových faktorů aterosklerózy a jejich akcelerace po amputacích (při stresu, snížené pohyblivosti a recidivujících infekcích) a následně vyšší výskyt kardiovaskulárních onemocnění
přetrvávající neuropatie, která vede ke komplikacím na pahýlu amputované končetiny (zejména otlakům, ulceracím, infekci) a komplikuje používání protéz,
přetížení druhostranné končetiny, která je rovněž postižena neuropatií a snadno na ní také vznikají ulcerace či Charcotova osteoartropatie a deformity a nezřídka je nutná i druhostranná amputace,
zhoršení kompenzace diabetu při váhovém přírůstku a častých infekcích i při stresu,
nezvládnutelné nároky na fyzickou zdatnost při používání protéz,
progrese pozdních komplikací diabetu, zejména renální insuficience.
Rekurence ulcerací je jedním z hlavních problémů současné podiatrie. Sami jsme zjistili rekurenci SDN do tří let od zhojení téměř u 60 % pacientů (14). Proto je nezbytná důsledná dispenzarizace pacientů po zhojení syndromu diabetické nohy a jejich časté kontroly a ošetření preulcerózních lézí.
K prokazatelně účinným opatřením pro prevenci reulcerací patří podle nedávné metaanalýzy i současného mezinárodního konsenzu (1, 13):
dispenzarizace rizikových pacientů na specializovaných pracovištích (podiatrické ambulance) včetně ošetření preulcerozních lézí (odborných pedikúr),
samostatná kontrola pacientů zahrnující nejen prohlížení nohou, ale i vhodnou rehabilitaci,
vhodná obuv včetně stélek, která je ale nošena alespoň 60–70 % času,
preventivní chirurgické odstranění deformit.
Klíčovým faktorem rekurence zůstává non‑adherence k preventivním doporučením a k léčbě, která je častá, a proto je nutné se snažit analyzovat a odstraňovat její příčiny.
Šíře problému syndromu diabetické nohy ve světě i v ČR – epidemiologická charakteristika
SDN je nejen hlavní příčinou hospitalizace diabetiků a neúrazových amputací dolních končetin, také často vede k dlouhodobé pracovní neschopnosti a invaliditě. Počet pacientů se syndromem diabetické nohy mírně stoupá (představují 5,6 % diabetiků), riziko syndromu diabetické nohy má ale 15–25 % pacientů s diabetem.
V České republice je od roku 2016 pokrokem možnost sledování některých komplikací diabetu pomocí Národního diabetologického registru, který využívá data Národního registru hrazených zdravotnických služeb (NRHZS), jak lze nalézt na stránkách ÚZIS. Z nich můžeme např. vyčíst, že mezi léty 2010–2020 nám mírně poklesl počet diabetiků se syndromem diabetické nohy ze 75 553 na 67 665 osob a poklesl i relativní počet amputací, a to jak všech amputací (Graf 1 A), tak vysokých amputací (Graf 1 B).
Graph 1. A. Relativní incidence všech amputací u léčených diabetiků v letech 2010–2020 v ČR (zdroj: NRHZS 2010–2020, IS LPZ 2010–2020) 
Graf 1B. Relativní incidence vysokých amputací u léčených diabetiků v letech 2010–2020 v ČR (zdroj: NRHZS 2010–2020, IS LPZ 2010–2020) 
Absolutní počet diabetiků po amputaci (prevalence) mezi léty 2015 a 2020 mírně vzrostl, především na úkor nízkých amputací (Tab. 1).
Table 1. Prevalence diabetických amputací; zdroj: NRHZS 2010–2020, IS LPZ 2010–2020 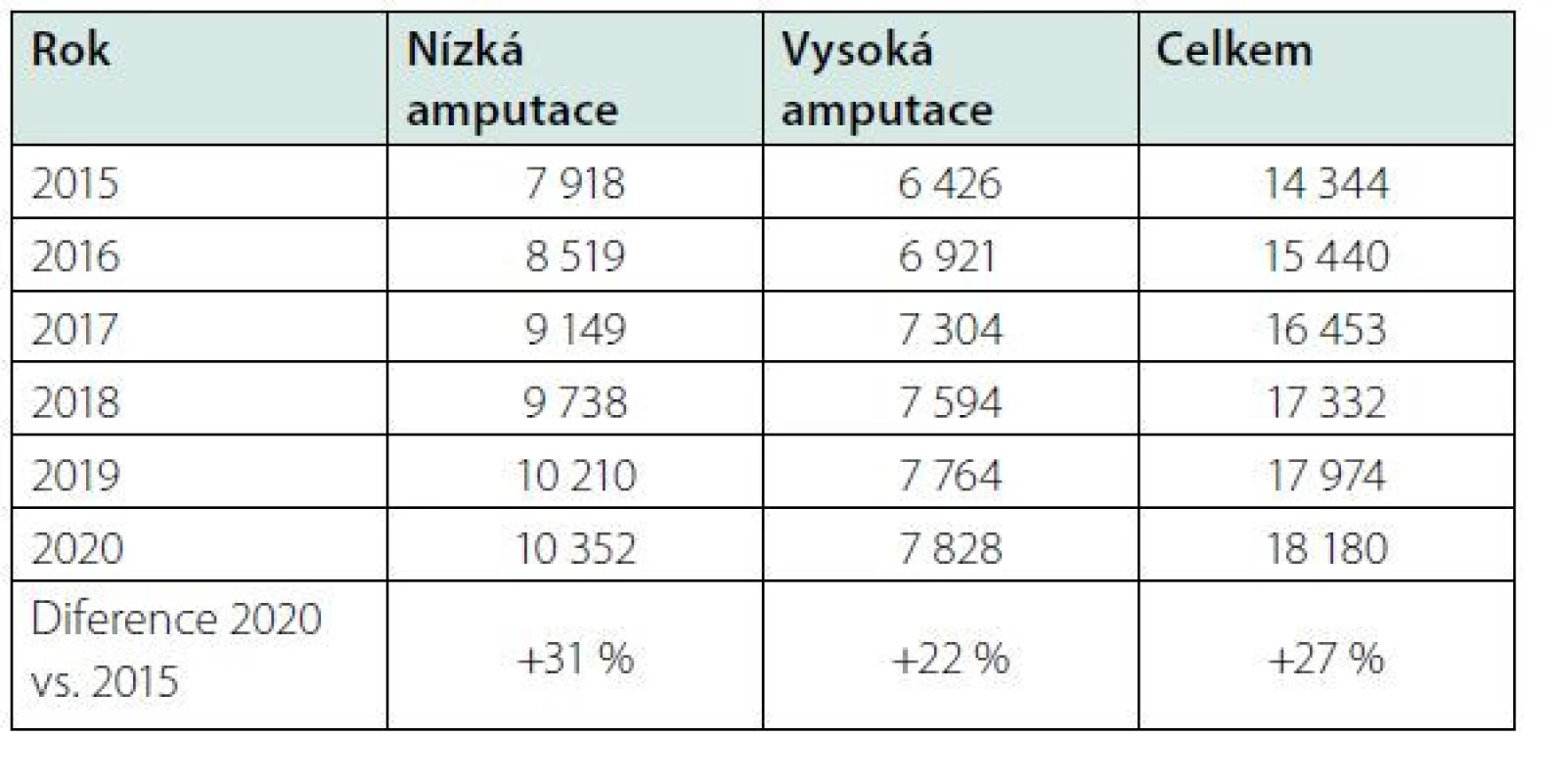
Poznámka k metodice zjišťování prevalence amputací: Je uveden počet osob s diabetes mellitus, které byly naživu v daném roce a měly v daném roce nebo někdy v minulosti (od roku 2010) vykázaný výkon o provedení nízké nebo vysoké amputace. V případě vykázání nízké i vysoké amputace je u pacienta započtena pouze vysoká. Data jsou prezentována od roku 2015 z důvodu minimalizace vlivu pacientů incidentních před rokem 2010.
Z těchto údajů vidíme, že se počet amputovaných osob zvyšuje, a to nejen kvůli vyššímu počtu diabetiků, ale pravděpodobně i kvůli delšímu přežívání amputovaných pacientů, a v neposlední řadě i kvůli mírně vzrůstající incidenci absolutního počtu vyšších amputací a výrazněji stoupajícího počtu nízkých amputací.
Závěr
Základním východiskem pro tvorbu mezioborových Klinických doporučených postupů (KDP) pro SDN je potřeba zajištění kvalitní podiatrické péče o diabetiky s ohledem na specifika tohoto onemocnění a prevence amputací. Prevalence pacientů se SDN i amputací stále stoupá, především v důsledku stoupajícího počtu diabetiků. Mezi hlavní specifika SDN, na něž se naše i mezinárodní doporučené postupy zaměřují, patří adekvátní diagnostika i terapie infekce SDN, odlišný průběh ICHDK, včasná diagnostika Charcotovy osteoartropatie, velmi rizikové skupiny diabetiků, a to nejen s aktivním SDN nebo s jeho anamnézou, ale také pacienti s pokročilým onemocněním ledvin. Porozumění specifickému průběhu SDN pomáhá specialistům z různých oborů efektivně navzájem spolupracovat. V nejbližší době by měl být k dispozici Klinický doporučený postup (KDP) pro syndrom diabetické nohy, který je založen na adaptaci mezinárodních doporučení, a to na stránkách Národního portálu klinických doporučených postupů (https//kdp.uzis.cz) i v dalších formách implementace do praxe.
Poděkování
Poděkování za obětavou práci při adaptaci IWGDF Guidelines patří všem kolegům z týmu pověřeném zpracováním KDP SDN:
MUDr. Michal Dubský, Ph. D.; MUDr. Vladimíra Fejfarová, Ph. D.; MUDr. Jarmila Jirkovská; MUDr. Miroslav Koliba, MBA; MUDr. Petr Krawczyk, PhD; MUDr. Dušan Kučera, Ph. D., MBA; MUDr. Bedřich Sixta; MUDr. Veronika Wosková; PhDr. Zuzana Fialová
Metodici: adj. Assoc. Prof. PhDr. Miloslav Klugar, Ph. D.; Ing. Mgr. Tereza Vrbová, Ph.D.
Podpořeno MZ ČR – RVO („Institut klinické a experimentální medicíny – IKEM, IČ 00023001“)
KORESPONDENČNÍ ADRESA AUTORA:
prof. MUDr. Alexandra Jirkovská, CSc.
Centrum diabetologie IKEM Vídeňská 1958/9, 14021 Praha 4 – Krč
Cit. zkr: Vnitř Lék 2021; 67(8): 489–494
Článek přijat redakcí: 15. 10. 2021
Článek přijat po recenzích: 12. 11. 2021
Sources
1. Schaper NC, van Netten JJ, Apelqvist J et al. IWGDF Guidelines on the prevention and management of diabetic foot disease: IWGDF; 2019 [updated; cited 2020 01-30]. Available from: https://iwgdfguidelines.org/wp‑content/ uploads/2019/05/IWGDF‑Guidelines - 2019.pdf
2. Paisey RB, Abbott A, Levenson R et al. Diabetes‑related major lower limb amputation incidence is strongly related to diabetic foot service provision and improves with enhancement of services: peer review of the South‑West of England. Diabet Med. 2018; 35(1): 53–62.
3. Jirkovská A, Lacigová S, Rušavý Z, Bém R. Doporučený postup pro prevenci, diagnostiku a terapii syndromu diabetické nohy: 2016 Dostupné na https://www.diab.cz/dokumenty/ standard_diab_noha.pdf
4. Jirkovská A. Syndrom diabetické nohy z pohledu internisty‑podiatra. Vnitr Lek. 2016; 62(Suppl. 4): 42–47.
5. Rogers L, Frygberg R, Armstrong D et al. The Charcot foot in diabetes. Diabetes Care 2011; 34 : 2123–2129.
6. Marmolejo V, Arnold J, Ponticello M et al. Charcot foot. Clinical clues, diagnostic strategies, and treatment principles. Am Fam Physician 2018; 97 (9): 594–599.
7. Lavery LA, Hunt NA, Ndip A et al. Impact of Chronic Kidney Disease on survival after amputation in individuals with diabetes. Diabetes Care 2010; 33(11): 2365–2369.
8. Otte J, van Netten JJ, Woittiez AJJ. The association of chronic kidney disease and dialysis treatment with foot ulceration and major amputation. J Vasc Surg. 2015; 62(2): 406-411.
9.Game FL, Chipchase SY, Hubbard R et al. Temporal association between the incidence of foot ulceration and the start of dialysis in diabetes mellitus. Nephrol Dial Transplant. 2006; 21(11): 3207–3210.
10. Rayman G, Vas P, Dhatariya K et al. on behalf of the International Working Group on the Diabetic Foot. Guidelines on use of interventions to enhance healing of chronic foot ulcers in diabetes (IWGDF 2019 update). Diabetes Metab Res Rev. 2020; 36(Suppl 1): e3283.1
11. Vas P, Rayman G, Dhatariya K et al. Effectiveness of interventions to enhance healing of chronic foot ulcers in diabetes: a systematic review. Diabetes Metab Res Rev. 2020; 36(Suppl 1): e3284.
12. Lefrancois T, Mehta K, Sullivan VS et al. Evidence based review of literature on detriments to healing of diabetic foot ulcers. Foot Ankle Surg. 2017; 23(4): 215–224
13. Armstrong DG, Boulton AJM, Bus SA. Diabetic Foot Ulcers and Their Recurrence. N England J Med. 2017; 376(24): 2367–2375.
14.Dubsky M, Jirkovska A, Bem R et al. Risk factors for recurrence of diabetic foot ulcers: prospective follow‑up analysis in the Eurodiale subgroup. Int Wound J. 2013; 10(5): 555-561.
15. Apelqvist J. Epidemiology of diabetic foot disease and etiology of ulceration. In: Hinchliffe RJ, Schaper N, Thompson M et al., eds. The diabetic foot. 1st ed. London: JP Medical Publishers; 2014 : 3–9.
16. Lipsky BA, Aragón‑Sánchez J, Diggle M et al. IWGDF guidance on the diagnosis and management of foot infections in persons with diabetes. Diabetes Metab Res Rev. 2016; 32 Suppl 1 : 45–74.
17. Ndosi M, Wright‑Hughes A, Brown S et al. Prognosis of the infected diabetic foot ulcer: a 12-month prospective observational study. Diabet Med. 2018; 35(1): 78–88.
18. Hinchliffe RJ, Forsythe RO, Apelqvist J et al. on behalf of the International Working Group on the Diabetic Foot. Guidelines on diagnosis, prognosis, and management of peripheral artery disease in patients with foot ulcers and diabetes (IWGDF 2019 update). Diabetes Metab Res Rev. 2020; 36(Suppl 1): e3276.
19. Frank U, Nicol S, Belch J + PAD writing group. ESVMB Guideline on peripheral arterial disease.VASA European Journal of Vascular Medicine 2019; 48, Suppl. 102.
20. Fejfarová V, Jirkovská A, Petkov V et al. Comparison of microbial findings and resistance to antibiotics between transplant patients, patients on hemodialysis, and other patients with the diabetic foot. J Diabetes Complications 2004; 18(2): 108–112.
21. Armstrong DG, Lavery LA, American Diabetes Association. Clinical care of the diabetic foot. 3rd edition. ed. Alexandria, Virginia: American Diabetes Association; 2016.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2021 Issue 8-
All articles in this issue
- Problematika antibiotické léčby u pacientů s covidem-19
- Aktivní vyhledávání a časná diagnostika HCV infikovaných osob
- Optimální hladina kalia u pacientů se srdečním selháním
- Lokalizovaná (unicentrická) forma Castlemanovy nemoci. Klinické projevy, diagnostika a léčba
- Glifloziny – nové léky pro pacienty se srdečním selháním?
- Renoparenchymatózní hypertenze – aktuality v diagnostice a léčbě
- Oboustranné vícečetné pneumatokély jako vzácná pozdní komplikace pneumonie covid-19
- Jaká jsou specifika syndromu diabetické nohy a proč potřebujeme mezioborová doporučení pro jeho diagnostiku a léčbu?
- Expertní konsenzus k významu deficitu železa a možnosti jeho korekce u pacientů se srdečním selháním
- Memorandum z jednání zástupců ČIS a ČPFS dne 6. 5. 2021 v Lékařském domě ČLS JEP v Praze
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Renoparenchymatózní hypertenze – aktuality v diagnostice a léčbě
- Glifloziny – nové léky pro pacienty se srdečním selháním?
- Optimální hladina kalia u pacientů se srdečním selháním
- Problematika antibiotické léčby u pacientů s covidem-19
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

