-
Medical journals
- Career
Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
Authors: Lenka Nosáková; Martin Schnierer; Peter Bánovčin; Katarína Stašková; Martin Uríček; Rudolf Hyrdel
Authors‘ workplace: Interná klinika – gastroenterologická JLF UK a UN Martin, Slovenská republika
Published in: Vnitř Lék 2020; 66(6): 53-57
Category: Case Report
Overview
Sharpov syndróm (mixed connective tissue diseases – MCTD) je veľmi zriedkavé autoimunitné ochorenie spájajúce klinické príznaky systémového lupusu, systémovej sklerózy, polymyozitídy a reumatoidnej artritídy. Klinické prejavy sú veľmi rôznorodé. U niektorých pacientov býva postihnutý tráviaci trakt v rôznom rozsahu. Najčastejšie býva postihnutý pažerák a pacienti sa sťažujú na dysfágiu. Morfologicky je toto postihnutie podobné postihnutiu pažeráka pri systémovej sklerodermii. V tejto kazuistike popisujeme jedinečný prípad ťažkého tráviaceho traktu manifestujúceho sa poruchami motility pažeráka, kachektizáciou, ascitom a opakovanými ileóznymi stavmi.
Klíčová slova:
Ascites – kachexia – poruchy motility pažeráka – Sharpov syndróm
Úvod
Sharpov syndróm (mixed connective tissue diseases – MCTD) je veľmi zriedkavé autoimunitné ochorenie spájajúce klinické príznaky systémového lupusu, systémovej sklerózy, polymyozitídy a reumatoidnej artritídy. Prvýkrát bol tento syndróm popísaný pred zhruba 40 rokmi, napriek tomu dodnes neexistuje jednoznačný konsenzus v zmysle definície, klasifikácie a liečby tohto ochorenia (1–4). Prevalencia sa udáva zhruba 1–9 prípadov na 100 000 obyvateľov. Obyčajne postihuje mladších ľudí vo veku od 15–35 rokov, častejšie sú postihnuté ženy. Klinické prejavy sú veľmi rôznorodé, od nešpecifických symptómov, ako je únava a subfebrility po vysoko špecifické symptómy pre autoimunitné choroby, ako sú Raynaudov fenomén, artralgie, artritídy, myozitídy, periunguálne hemorágie a sklerodaktýlia. U niektorých pacientov sú prítomné poruchy motility pažeráka, pleuritída, perikarditída, pľúcna hypertenzia. Etiológia MCTD je nejasná. Diagnostika je zložitá, väčšina pacientov máva vysoké titre anti-U1-ribounkleoproteínu (RNP) a anti-U1-70 protilátok. Liečba je podobná ako u iných autoimunitných chorobách, zahŕňa podávanie NSAID, imunosupresív alebo nízkych dávok kortikoidov. V prípadoch ťažkého systémového postihnutia viscerálnych orgánov sa v liečbe využívajú imunosupresíva. Prognóza je zvyčajne dobrá, až 80 % pacientov prežíva 10 rokov. Vo všeobecnosti však prognóza závisí od viscerálného postihnutia. Pacienti s klinickými prejavmi systémovej sklerodermie, s prítomnou pľúcnou hypertenziou mávajú horšiu prognózu.
Postihnutie tráviaceho systému pri tomto ochorení je relatívne časté a býva prítomné v rozmedzí od 66–74 % (5). Z gastrointestinálneho traktu býva najčastejšie postihnutý pažerák. Pacienti sa sťažujú na dysfágiu, manometrické vyšetrenie pažeráku odhalí prítomnosť ťažej poruchy motility, podobne ako pri systémovej sklerodermii (6–8). Z iných príznakov môže byť prítomná tzv. protein-losing enteropathia, akútna pankreatitída, perforácia čreva a. i.
Kazuistika
Náš pacient bol 53-ročný muž bez závažnejšieho interného predchorobia, bez chronickej medikácie. V apríli roku 2017 navštívil spádového gastroenterológa pre dyspeptický syndróm s vomitom, pyrózou a hnačkami. Podstúpil EGD, bioptické vzorky z duodena preukázali prítomnosť intraepiteliálnych lymfocytov, bez atrofie klkov. Ďalším nálezom bola infekcia Helicobycter pylori (HP).Bola započatá eradikačná terapia. Ťažkosti pacienta však neustupovali, následne v tom istom mesiaci bol hospitalizovaný na internom oddelení pre úporný vomitus, GERD a nemožnosť per os príjmu. Počas hospitalizácie bola realizovaná RTG pasáž ezofágu s nálezom stagnácie kontrastnej látky nad kardiou. Po stabilizovaní klinického stavu a preliečení HP infekcie bol prepustený. Následne sa u neho objavili opuchy nôh, rozvoj ascitu a progresívne chudnutie. V júli roku 2017 bol pacient hospitalizovaný pre mechanický ileus tenkého čreva. Ako príčina bola stanovená obštrukcia tuhou stolicou, s nutnosťou operačného riešenia. Nasledovalo obdobie opakovaných hospitalizácií pre subileózne stavy, ktoré nevyžadovali operačné riešenie, boli zvládnuté konzervatívne. Pre opuchy dolných končatín bolo doplnené vyšetrenie nefrológom, ktorý stav zhodnotil ako nefrotický syndróm nejasnej etiológie. Pacient absolvoval aj reumatologické vyšetrenie, kde bolo vyslovené podozrenie na MCTD a bolo doporučené doplniť vyšetrenie špecifických protilátok. V decembri roku 2017 bol opäť hospitalizovaný pre subileus, ascites, edémy a hypoproteinémiu. Za účelom diferenciálnej diagnostiky ascitu, hnačiek, kachexie a progresívneho úbytku hmotnosti (celkovo 42 kg za 9 mesiacov) bol pacient preložený na naše oddelenie Internej kliniky gastroenterologickej. Pri príjme na naše oddelenie bol pacient kachektický, boli prítomné edémy dolných končatín, ascites, výrazná hypotrofia svalstva, Raynaudov fenomén na prstoch horných a dolných končatín (Obr. 1 a 2). Pri výške 185 cm bola pacientova hmotnosť 50 kg. Laboratórne bola prítomná ťažká hypoproteinémia, sideropénia a elevácia CRP (výsledky niektorých laboratórnych vyšetrení uvádza tab. 1). V prvom kroku realizujeme diagnostickú punkciu ascitu. Získaná vzorka bola biochemicky a mikrobiologicky vyšetrená, ascites vykazoval charakter transudátu, cytologické vyšetrenie preukázalo prítomnosť lymfocytárno-histiocitárneho infiltrátu bez prejavov akútneho zápalu alebo malígnej proliferácie. Dopĺňame odporúčané vyšetrenie autoprotilátok, ktoré poukazuje na pozitivitu anti Ro-52 a anti-RNP. V rámci pátrania po príčine tráviacich ťažkostí pacienta dopĺňame sériu špecifických vyšetrení. EGD zobrazuje dilatáciu pažeráku, bez prítomnej peristaltiky a peptické zápalové zmeny. Kolonoskopické vyšetrenie okrem hemoroidov a mierne dilatovaného ptotického čreva nepreukázalo vážnejšiu patológiu. Realizujeme kontrastné vyšetrenie pasáže celým tráviacim traktom s nálezom suspektnej achalázie kardie. Prítomné sú zápalové resp. pozápalove zmeny od céka po colon sigmoideum. Bolo vyslovené podozrenia na entero-enterálnu fistulu v oblasti jejuna (Obr. 3). Dopĺňame scintigrafické vyšetrenie gastrointestinálneho traktu s nálezom normálnej evakuácie žalúdka, prítomný je však výrazne rozšírený pažerák so spomalenou pasážou a aberantný obraz tenkého čreva v laterálnej časti brušnej dutiny vľavo so záverom, že sa môže sa jednať o atypicky rozšírenú kľučku pred parciálne obštruovanou distálnejšou časťou tenkého čreva, event. o funkčný slepý pahýľ. Realizovaná MR enterografia nález entero-enterálnej fistuly nepotvrdzuje. V rámci diferenciálnej diagnostiky dysfágie a achalázie realizujeme HR manometriu pažeráka. Táto poukazuje na prítomnosť ťažkej poruchy motility pažeráka v zmysle aperistaltiky dľa Chicagskej klasifikácie (Obr. 4), bez prítomnosti propulzívnej peristaltiky, nie sú však prítomné panezofageálne presurizácie a oblasť dolného pažerákového zvierača relaxuje dostatočne. Kontrolné reumatologické vyšetrenie suponuje diagnózu MCTD s ťažkým difúznym postihnutím tráviaceho traktu, prítomnosťou Raynaudovho syndrómu, prítomnosťou periunguálnych hemorágií s pozitívnym kapilaroskopickým nálezom, serozitídou a nefrotickým syndrómom. Realizujeme PET CT vyšetrenie, ktoré vylučuje malignitu. Bola zahájená vysoko nutričná parenterálna terapia, liečba hypoproteinémie a liečba kortikosteroidmi. Vzhľadom k závažnosti stavu je zvažovaná aj liečba imunosupresívami. Na tejto liečbe však dochádza k zlepšeniu klinického stavu, prírastku na váhe (Obr. 5), preto od liečby imunosupresívami upúšťame. Ako príčina pacientových gastrointestinálnych ťažkostí bola stanovená základná diagnóza Sharpov syndróm s postihnutím tráviaceho traktu.
Image 1. Pacient pri príjme na oddelenie Internej kliniky gastroenterologickej UN Martin 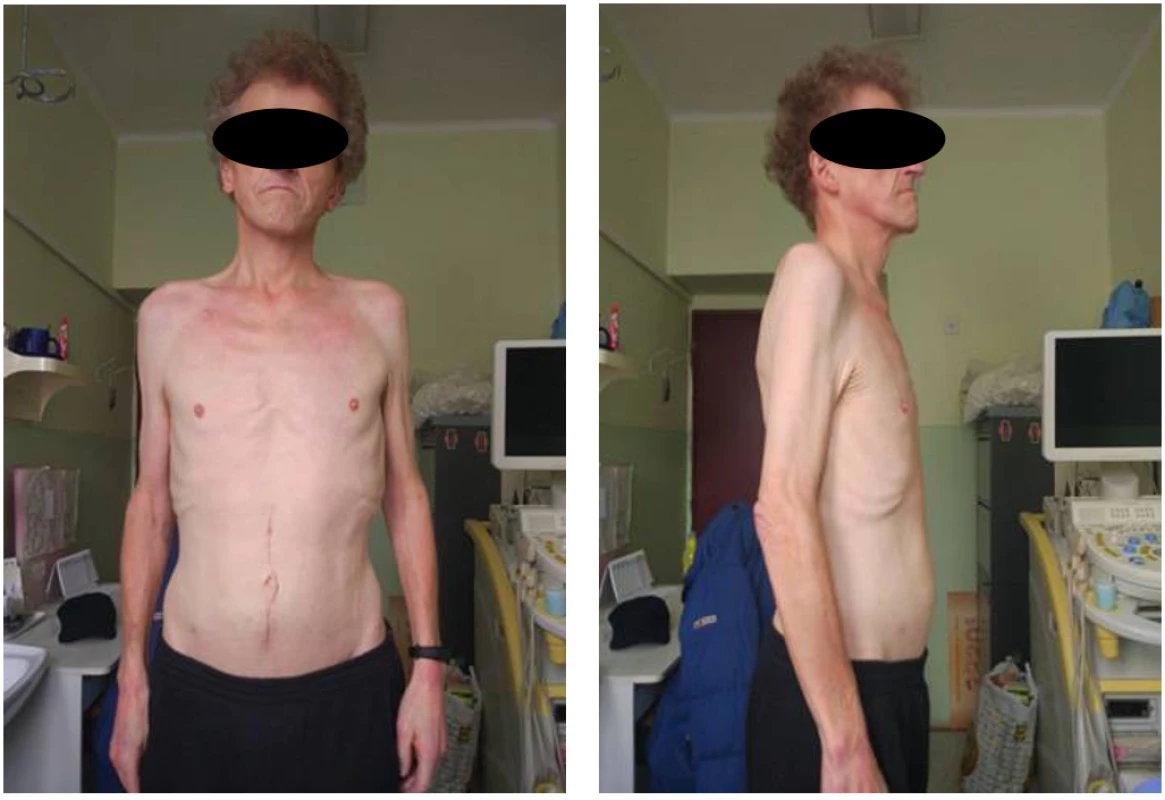
Image 2. Raynaudov syndróm a periunguálne hemorágie 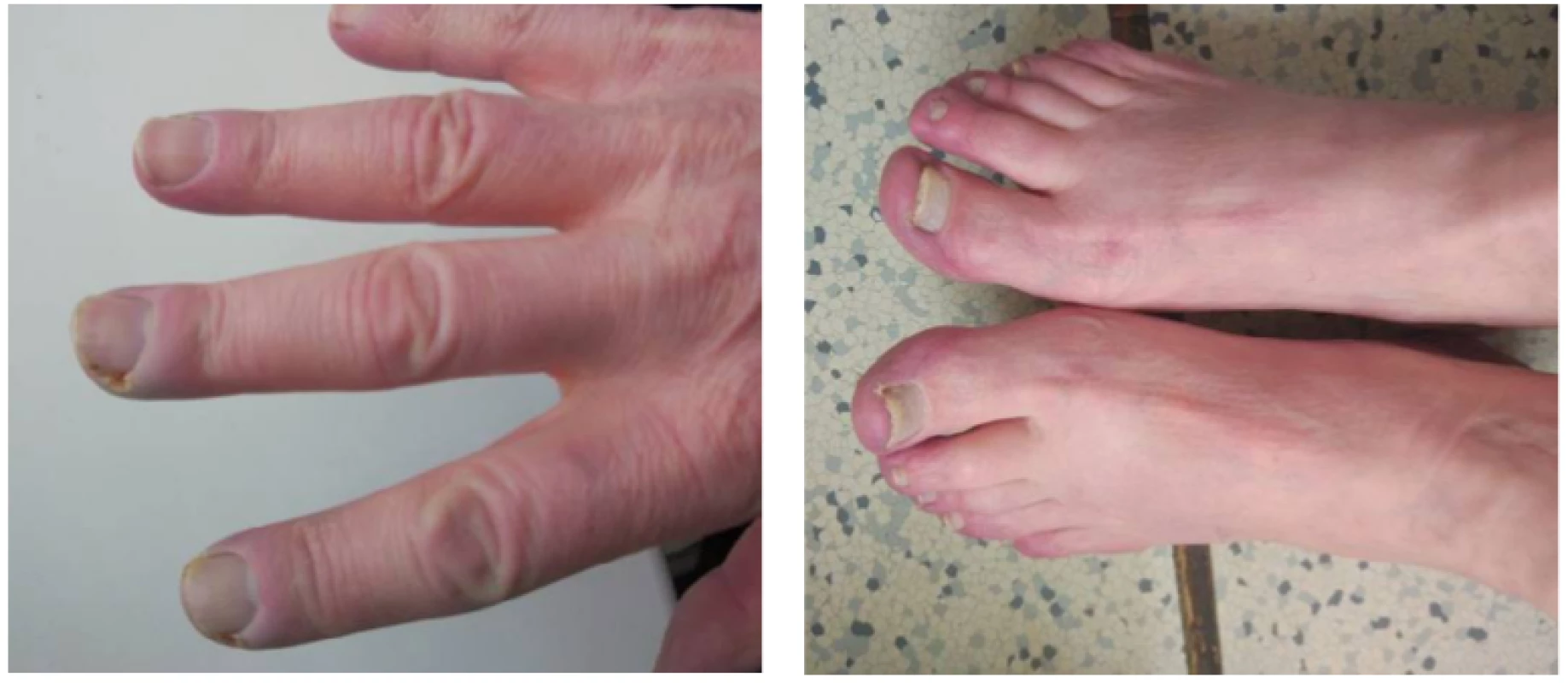
Image 3. RTG pasáž tráviacim traktom – vpravo pozápalové zmeny hrubého čreva, vľavo obraz dilatácie pažeráka so zúžením v oblasti kardie a stagnáciou kontrastnej látky 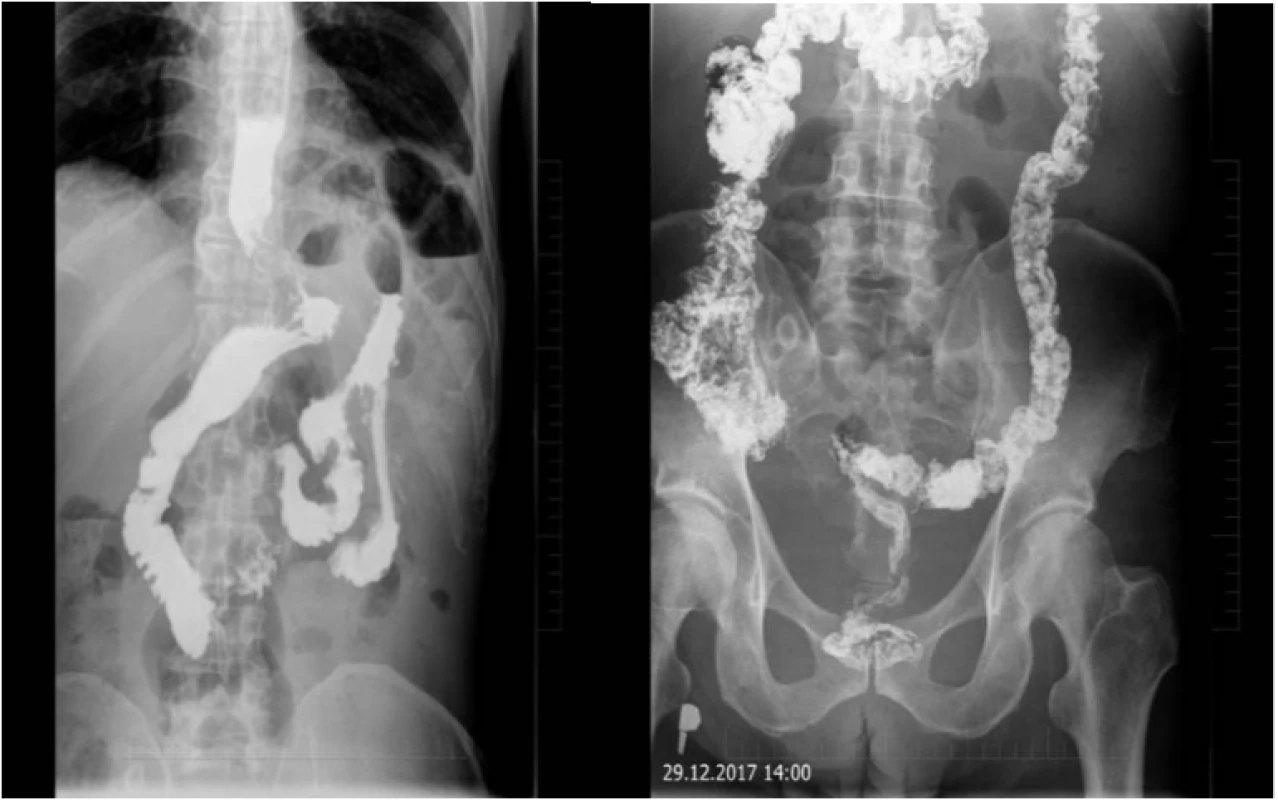
Image 4. HR manometria pažeráka – obraz ťažkej poruchy motility, bez prítomnosti propulzívnej peristaltiky, oblasť dolného ezofageálneho zvierača relaxuje dostatočne 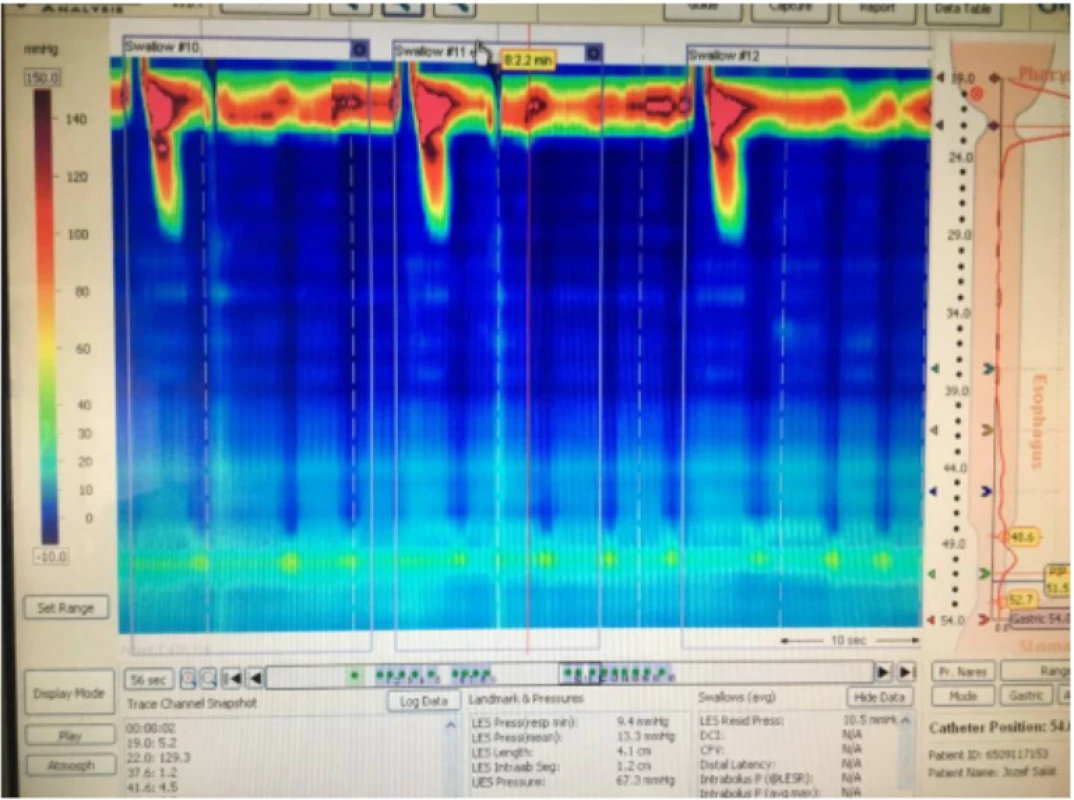
Image 5. Obraz pacienta pri demitácií z oddelenia 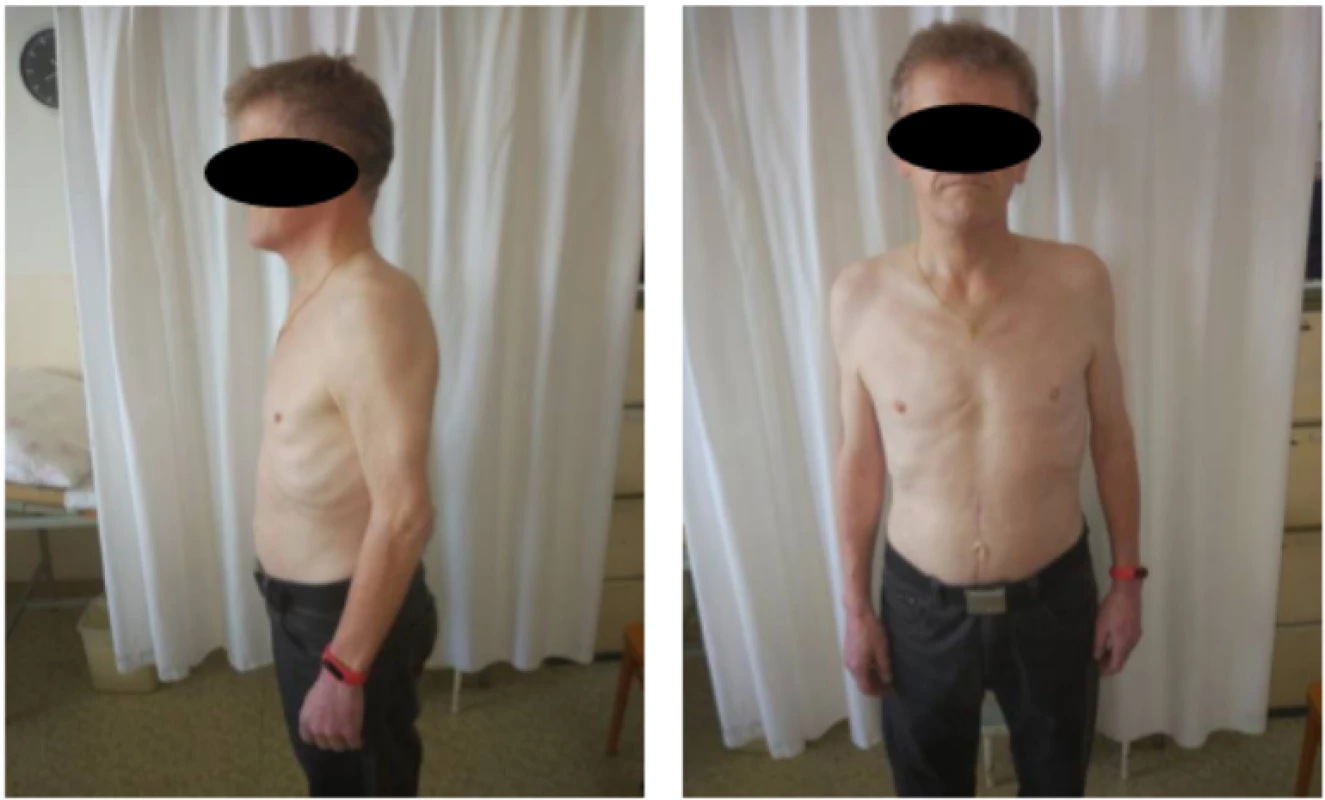
Table 1. Prehl´ad niektorých výsledkov laboratorných vyšetrení u pacienta. 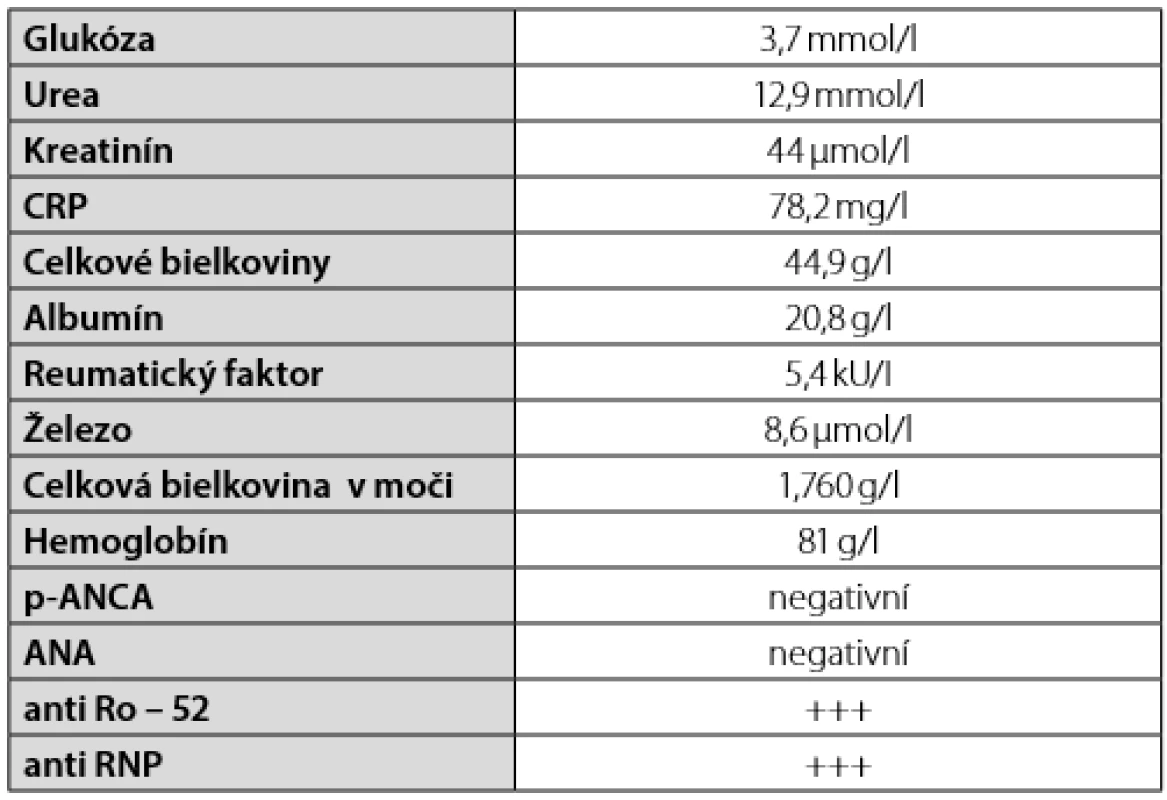
Diskusia
Sharpov syndróm je veľmi zriedkavé autoimunitné ochorenie spojiva. Čo sa diagnostiky autoimunitných ochorení týka, najdôležitejšie je na ne myslieť. Ťažké postihnutie viscerálnych orgánov je zriedkavé, vo všeobecnosti má toto ochorenie dobrú prognózu. Klinický obraz tohto ochorenia je veľmi variabilný a zahŕňa široké spektrum symptómov v závislosti od toho, ktorý konkrétny systém je postihnutí. Postihnutie tráviaceho systému býva časté a prítomné je až u 70 % pacientov s MCTD (5). Najčastejšie býva postihnutý pažerák, ako tomu bolo aj u nášho pacienta. V literatúre sú popisované ako najčastejšie klinické prejavy pálenie záhy a dysfágia. Až 1/3 pacientov však môže byť úplne asymptomatických (9, 10). Vyšetrenie pažeráku HR manometriou odhalí vo väčšine prípadov ťažkú poruchu motility v zmysle aperistaltiky (11, 12). Obraz je nápadne podobný postihnutiu pažeráka pri systémovej sklerodermii, väčšinou však nemá taký závažný charakter (7, 9). U nášho pacienta však bola prítomná závažná porucha motility
celého tráviaceho traktu. Poruchy motility sa však môžu objaviť v ktorejkoľvek časti gastrointestinálneho traktu, aj keď je to zriedkavé. Čo sa tyká patofyziologického mechanizmu spôsobujúceho tieto poruchy, ten nie je presne známy. Niektorí autori zastávajú názor, že poškodenie spôsobujú autoprotilátky napádajúce hladkú svalovinu tráviaceho traktu, gangliónové bunky Auerbachového plexu, stenu ciev a svalových vlákien, čo vedie k dysfágií (13). Z jednej štúdie realizovanej postmortem u pacientov s MCTD boli prítomné histopatologické zmeny vnútornej cirkulárnej vrstvy svaloviny, predominantne v dolných 2/3 pažeráku (14).Čo sa týka postihnutie obličiek, vo všeobecnosti sa považovalo za zriedkavé. Podľa dostupných zdrojov je renálne poškodenie prítomné u 10–50 % pacientov s MCTD (15–17). Poškodenie obličiek ma zvyčajne histopatologický charakter membranóznej glomerulonefritídy, nefrotický syndróm býva prítomný až u 75 % týchto pacientov s poškodením obličiek (16).
Pri závažnom poškodení orgánov je štandardne doporučovaná liečba kortikosteroidmi, niekedy v kombinácií s imunosupresívami (18). Z literatúry je zaujímavý fakt, že títo pacienti väčšinou dobre reagujú na liečbu kortikosteroidmi, s postupnou úpravou klinického stavu, napriek tomu, že morfologické zmeny na postihnutých orgánoch pretrvávajú (16–18).
Záver
Sharpov syndróm je zriedkavé autoimunitné ochorenie náročné na diagnostiku pre svoj rozmanitý obraz. V tejto kazuistike popisujeme jedinečný prípad ťažkého postihnutia tráviaceho traktu a obličiek pri tomto syndróme s progresívnou kachektizáciou, poruchou motility pažeráka a rozvojom ascitu. Pre správny manažment takéhoto pacienta je potrebná intenzívna terapia, prechodne parenterálna nutričná podpora a mutlitidisciplnárny prístup. Základom liečby je podávanie kortikosteroidov. V prípade nedostatočného efektu a ťažkého orgánového postihnutia je možné do liečby pridať imunosupresíva.
Táto publikácia vznikla vďaka podpore v rámci operačného programu Výskum a vývoj pre projekt: Meranie kinetiky cílií respiračného traktu, ITMS kód projektu: 26220220019, spolufinancovaný zo zdrojov Európskeho fondu regionálneho rozvoja.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Martin Schnierer,
Interná klinika gastroenterologická JLF UK a UN
Kollárová 2,
036 01 Martin
Cit. zkr: Vnitř Lék 2020; 66(6): e53–e57
Článek přijat redakcí: 16. 10. 2019
Článek přijat po recenzích k publikaci: 4. 1. 2020
Sources
1. Gunnarsson R, Hetlevik SO, Lilleby V, et al. Mixed connective tissue disease. Best Pract Res Clin Rheumatol 2016; 30 : 95–111.
2. Aringer M, Steiner G, Smolen JS. Does mixed connective tissue disease exist? Yes. Rheum Dis Clin North Am 2005; 31 : 411–420.
3. Swanton J, Isenberg D. Mixed connective tissue disease: still crazy after all these years. Rheum Dis Clin North Am 2005; 31 : 421–436.
4. Sharp GC MCTD: a concept which stood the test of time. Lupus 2002; 11 : 333–339.
5. Marshall JB, Kretschmar JM, Gerhardt DC, et al. Gastrointestinal manifestations of mixed connective tissue disease. Gastroenterology 1990; 98 : 1232–1238.
6. Gutierrez F, Valenzuela JE, Ehresmann GR, et al. Esophageal dysfunction in patients with mixed connective tissue diseases and systemic lupus erythematosus. Digestive Diseases and Sciences 1982; 27 : 592–597.
7. Doria A, Bonavina L, Anselmino M, et al. Esophageal involvement in mixed connective tissue disease. Journal of Rheumatology 1991; 18 : 685–690.
8. Fagundes MN, Caleiro MT, Navarro-Rodriguez T, et al. Esophageal involvement and interstitial lung disease in mixed connective tissue disease. Respiratory Medicine 2009; 103 : 854–860.
9. Schneider HA, Yonker RA, Longley S, et al. Scleroderma esophagus: a nonspecific entity. Ann Intern Med 1984; 100 : 848–850.
10. Nica AE, Alexa LM, Ionescu AO, et al. Esophageal disordes in mixed connective tissue diseases. J Med Life 2016; 9 : 141–143.
11. Hyrdel R, Bánovčin P, Ďuríček M. Poruchy motility pažeráka – Chicagska klasifikácia, v 3.0. Gastroent Hepatol 2015; 69 : 130–138.
12. Kroupa R, Dolina J, Hep A, et al. pH-metrie a manometrie jícnu. Současné postavení diagnostických metód. Čes a Slov Gastroent a Hepatol 2006; 60 : 149–156.
13. Reichlin M. Problem in differentiating SLE and mixed connective-tissue disease. N Engl J Med 1976; 295 : 1194–1195.
14. Kamataki A, Uzuki M, Sawai T. Histopathological Change of Esophagus related to Dysphagia in Mixed Connective Tissue Disease, Seminars in Dysphagia Renne Speyer and Hans Bogaardt, IntechOpen, DOI: 10.5772/60509. Available from: https: //www.intechopen.com/books/seminars-in-dysphagia/histopathological-change-of-esophagus-related-to-dysfagia-in-mixed-connective-tissue-disease.
15. Bennett RM, Spargo BH. Immune complex nephropathy in mixed connective tissue disease. Am J Med 1977; 63 : 534–541.
16. Kitridou RC, Akmal M, Turkel SB, et al. Renal involvement in MCTD: a longitudinal clinicopathologic study. Semin Arthritis Rheum 1986; 16 : 135–145.
17. Kobayashi S, Nagase M, Kimura M, et al. Renal involvement in mixed connective tissue disease. Am J Nephrol 1985; 5 : 282–289.
18. Prakash MD, Luthra HS, Divertie MB. Intrathoracic manifestations in MCTD. Mayo Clin Proc 1985; 60 : 813–821.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2020 Issue 6-
All articles in this issue
- Anafylaxe – akutní a dlouhodobý management
- Potravinová alergie a intolerance
- Poruchy v komplementovém systému
- Imunosenescence – západ slunce nad imunitním systémem
- Chřipka a její komplikace
- Familiární plicní fibróza – doporučení pro diagnostiku a léčbu
- Nové dělení krystalopatií z pohledu nefrologa
- Infarkt myokardu nebo syndrom zlomeného srdce?
- Dieulafoy lézia jejuna ako zdroj život ohrozujúceho krvácania
- Co nového internistům přinášejí doporučené postupy pro diagnostiku a léčbu plicní embolie z roku 2019?
- Perkutánní okluze ouška levé síně
- Současné postavení dietních opatření u pacientů s pokročilým stupněm chronického onemocnění ledvin
- Dysfunkčný dialyzačný cievny prístup a jeho endovaskulárna liečba
- Histiocytózy a neoplazie odvozené od makrofágů a dendritických buněk. Srovnání WHO klasifikace z roku 2017 a klasifikace Histiocyte society z roku 2016
- Glykovaný hemoglobín ako marker zvýšenia LDL a TAG – kohortná štúdia
- Deriváty sulfonylurey a riziko hypoglykemie u diabetiků 2. typu
- Endoskopická diagnostika a terapie pankreatobiliárních onemocnění u osob po resekci žaludku podle Billrotha I
- Nozokomiální methemoglobinemie
- Alergie a imunopatologie – hlavní téma
- Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Infarkt myokardu nebo syndrom zlomeného srdce?
- Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
- Potravinová alergie a intolerance
- Poruchy v komplementovém systému
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

