-
Medical journals
- Career
Dieulafoy lézia jejuna ako zdroj život ohrozujúceho krvácania
Authors: Lenka Dvorská 1; Jiří Janoušek 1; Ilja Tachecí 2; Tomáš Rozkoš 3
Authors‘ workplace: Interní oddělení Oblastní nemocnice Trutnov, a. s. 1; II. interní gastroenterologická klinika LF UK a FN Hradec Králové 2; Fingerlandův ústav patologie LF UK a FN Hradec Králové 3
Published in: Vnitř Lék 2020; 66(6): 381-385
Category: Case Report
Overview
Dieulafoy lézia je vzácna príčina krvácania do tráviaceho traktu z minimálneho defektu erodovanej submukóznej artérie. Najčastejšie býva lokalizovaná v žalúdku u starších polymorbídnych mužov, môže sa však vyskytovať v celom tráviacom trakte, u obidvoch pohlaví a v každom veku. Malo by sa na ňu myslieť, ako na jednu z možných príčin krvácania z neurčeného zdroja. Krvácanie je často masívne, vyžadujúce rýchlu diagnostiku, liečbu a mutidisciplinárny prístup. Kazuistika popisuje prípad pacienta s recidivujúcim hemodynamicky významným krvácaním z jejuna. Poukazuje na kombinovaný diagnostický postup s využitím endoskopie a vazografie. Po neúspešných angiografických a endoskopických pokusoch sa pre hemodynamickú instabilitu pacienta pristúpilo ku chirurgickej resekcii. Definitívna diagnóza Dieulafoy lézie jejuna sa stanovila až histologicky. Voľba diagnostickej a terapeutickej metódy by mala byť individuálna s prihliadnutím na pacientov stav a možnosti daného pracoviska. Chirurgická intervencia zostáva metódou voľby pri hemodynamickej instabilite pacienta alebo po zlyhaní endoskopických a angiografických metód.
Klíčová slova:
akútne krvácanie do tráviaceho traktu – Dielafoy lézia – Jejunum – krvácanie z neurčeného zdroja
Úvod
Dieulafoy lézia (DL) je relatívne vzácna, ale potenciálne život ohrozujúca príčina krvácania do tráviaceho traktu (GIT), ktoré často recidivuje. Pre jej malý rozmer, intermitentné, ale často masívne krvácanie predstavuje výzvu vzhľadom k obtiažnej diagnostike a liečbe. Je nazvaná po francúzskom chirurgovi G. Dieulafoy, ktorý ju vo svojej práci z roku 1898 označil ako „exulceratio simplex“ (1, 2). Predstavuje 1–2 % akútnych krvácaní do GIT (2). Podkladom lézie je abnormálne dilatovaná veľkokalibrová artéria v submukóze, ktorá pravdepodobne svojou pulzáciou eroduje priliehajúcu sliznicu (1). Presná patogenéza však nie je jasná. Približne 70 % lézií sa vyskytuje v žalúdku pozdĺž malej kurvatúry, ďalšie časté lokality zahrňujú duodenum (15 %), ezofagus (8 %), menej často hrubé črevo (2 %), apendix, rektum (2 %), jejunum – ileum (1 %), a análny kanál (2, 3). Môžu sa však vyskytovať aj mimo tráviaceho traktu ako napr. v bronchu prezentujúc sa hemoptýzou (4). V oblasti žalúdku sú muži postihnutí 2× častejšie ako ženy, v ostatných lokalitách GIT je zastúpenie pohlaví vyrovnané (5).
Najčastejšie sa DL prezentuje v priemernom veku asi 65 rokov, avšak výskyt DL je popisovaný v celom vekovom spektre vrátane detí a novorodencov (1–3, 6, 7). Frekventované komorbidity, popisované spolu s DL, sú najmä kardiopulmonálne a renálne ochorenia. Z liekov je to užívanie nesteroidných antireumatik, kyseliny acetylsalicylovej, warfarínu alebo inej antikoagulačnej či antitrombotickej terapie (1–3, 5, 8). Pacienti s DL sú typicky asymptomatickí, než sa lézia manifestuje. Najčastejším prejavom je akútne krvácanie do GIT formou hematemézy (28–30 %), melény (18–44 %) a enterorágie (6 %) (2, 3, 5). Približne v polovici prípadov sa hemateméza a meléna vyskytujú súčasne (3). Len v 1 % sa DL prezentuje sideropenickou anémiou (2). Charakteristické pre DL je absencia bolesti a iných dyspeptických symptómov. Rozvoj známok hemodynamickej instability ako hypotenzia, tachykardia, ortostáza závisia na závažnosti krvácania do GIT. Diagnostické metódy pre DL zahrňujú endoskopiu, angiografiu a scintigrafiu. Vzhľadom k relatívne raritnému výskytu ochorenia zatiaľ pre DL neexistuje univerzálny odporúčaný liečebný postup. Medzi terapeutické možnosti patria endoskopické metódy (s termálnym, mechanickým a regionálneinjekčným hemostatickým pôsobením), selektívna angiografia s embolizáciou a v neposlednom rade chirurgická revízia. S rozvojom endoskopických techník klesla mortalita z 80 % na terajších 9–13 % (3) a nutnosť chirurgickej intervencie zo 100 % na 3–5 % (2, 5).
Naša kazuistika popisuje prípad pacienta s recidivujúcim, hemodynamicky významným krvácaním do GIT z neurčeného zdroja, u ktorého zlyhala endoskopická i vazografická terapia. Diagnóza DL jejuna sa potvrdila až histologicky z chirurgického resekátu.
Cieľom tejto práce je zvýšiť povedomie o DL ako o možnej príčine krvácania do GIT z neurčeného zdroja a poukázať na nutnosť individuálneho prístupu pri voľbe diagnostického i terapeutického postupu.
Popis prípadu
41‑ročný pacient, nefajčiar, s astma bronchiale v detstve v osobnej anamnéze, inak zdravý, bol v máji roku 2018 privezený na naše oddelenie pre recidivujúce synkopy a melénu. Pri prevzatí bol pacient pri vedomí, okrem pretrvávajúcej slabosti po vertikalizácii sa na nič konkrétne nesťažoval. Neudával tráviace problémy ani bolesti brucha. Akékoľvek krvácavé prejavy negoval. Okrem symptomatickej hypotenzie (tlak krvi – TK 80/50 mm Hg) a melénoznej stolice v rekte bol fyzikálny nález normálny. Pacienta sme prijali na jednotku intezívnej starostlivosti (JIS) nášho oddelenia a začali intenzívnu parenterálnu liečbu krvácania do tráviaceho traktu, ktorá zahrňovala i.v. somatostatín, inhibítory protónovej pumpy (PPI) a infúznu terapiu. Vstupný krvný obraz (KO) bol s miernou normocytárnou normochrómnou anémiou 122 g/l hemoglobínu, s leukocytózou 11,1 × 10⁹/l, 3,95 × 10¹²/l červených krviniek, 187 × 10⁹/l krvných doštičiek, orientačné koagulačné parametre protrombínový a aktivovaný parciálny tromboplastínový čas neboli predĺžené, biochemické vyšetrenie (urea, kreatinín, minerály, glykémia, bilirubín, ALT, AST, GMT, CRP) taktiež v norme. Po stabilizácii pacienta sme doplnili gastroskopiu s nálezom erytematóznej antrálnej gastropatie, bez známok krvácania. Helicobacter pylori bol negatívny. Za hospitalizácie pacient absolvoval skiagram hrudníku, ultrazvuk brucha a totálnu kolonoskopiu až po terminálne ileum, všetko bez patologického nálezu. Behom hospitalizácie sa pacient na nič nesťažoval, krvácanie sa neopakovalo i po zaťažení stravou. Po 6 dňoch sme pacienta dimitovali na perorálnej terapii PPI. Vzhľadom k tomu, že sa nenašiel zdroj krvácania, objednali sme pacientovi ambulantne kapslovú endoskopiu vo FN Hradec Králové (FNHK) na jún roku 2018.
Za 5 dní bol však pacient znovu privezený pre recidívu synkopy so symptomatickou posturálnou hypotenziou a opätovne prijatý na JIS. Pri prijatí vo fyzikálnom náleze dominoval anemický kolorit pacienta a hypotenzia. KO bol s významnou normocytárnou anémiou s hemoglobínom 85 g/l, bez leukocytózy, rýchlo sa rozvinula meléna. Následovala intenzívna liečba krvácania do zažívacieho traktu (i.v. somatostatín, PPI), infúzna terapia kryštalickými roztokmi, transfúzie erymasami (celkovo 4×). Akútna gastroskopia nepreukázala zdroj krvácania. Pacient ďalej absolvoval počítačovú tomografiu (CT) brucha s enterografiou, ktorá bola bez detekovatelného zdroja krvácania, bez známok Meckelova divertiklu, karcinoidu či inej príčiny krvácania. Vzhľadom k vyčerpaniu našich diagnostických možností sa pacient po stabilizácii stavu ešte v deň prijatia preložil k dovyšetreniu na JIS III. internej gerontometabolickej kliniky FNHK.
Tu sa doplnila plánovaná kapslová endoskopia s nálezom krvácajúceho submukózneho tumoru jejuna o veľkosti asi 10 mm. V diferenciálnej rozvahe sa zvažoval gastrointersticiálny stromálny tumor (GIST) alebo cievna malformácia. Stav pacienta bol následne komplikovaný recidívou krvácania s rozvojom hemoragického šoku. Akútna CT angiografia brucha odhalila významný arteriálny extravazát kontrastnej látky v lumen orálneho jejuna, riešený vazograficky embolizáciou pomocou histoacrylu (Obr. 1). Efekt bol však len prechodný. V ďalšom priebehu pacient absolvoval dvojbalónovú enteroskopiu. Popisovaný malý submukózny tumor jejuna z kapslovej endoskopie bol s koagulom a viditelným aktívnym krvácaním (Obr. 2). Snaha o zastavenie krvácania opichom adrenalínu nebola úspešná. Vzhľadom k charakteru lézie a hemodynamickej instabilite pacienta sa endoskopisti o ďalšiu intervenciu nepokúšali a pacient bol indikovaný k urgentnému chirurgickému riešeniu. Miesto krvácania označili Spotom, vďaka ktorému sa krvácajúce ložisko našlo asi 200 cm za Treitzovým väzom. Laparotomicky sa zresekovalo asi 10 cm proximálneho jejuna s malým krvácajúcim tumorom a zároveň bol odstránený i náhodne nájdený nekrvácajúci Meckelov divertikel. Podľa výsledku histologického vyšetrenia (ktoré sme mali k dispozícii až po dimisii pacienta) bola príčinou krvácania Dieulafoy lézia. Makroskopicky sa v resekáte popisovalo prekrvácané ložisko o priemere 15 mm s 2 mm ulceráciou, v lumen čreva sa nachádzalo krvné koagulum. Mikroskopický popis ložiska obsahoval povrchovo exulcerovanú sliznicu tenkého čreva, v submukóze bola zastihnutá tepna muskulárneho typu (priemer 8 mm) s ruptúrou, výpadky elastiky, s trombom a akútnym krvácaním (Obr. 3 a 4). Meckelov divertikel bol s heterotopickou sliznicou tela žalúdku bez pozoruhodností.
Image 1. CT angiografia: leak kontrastnej látky do oblasti proximálneho jejuna 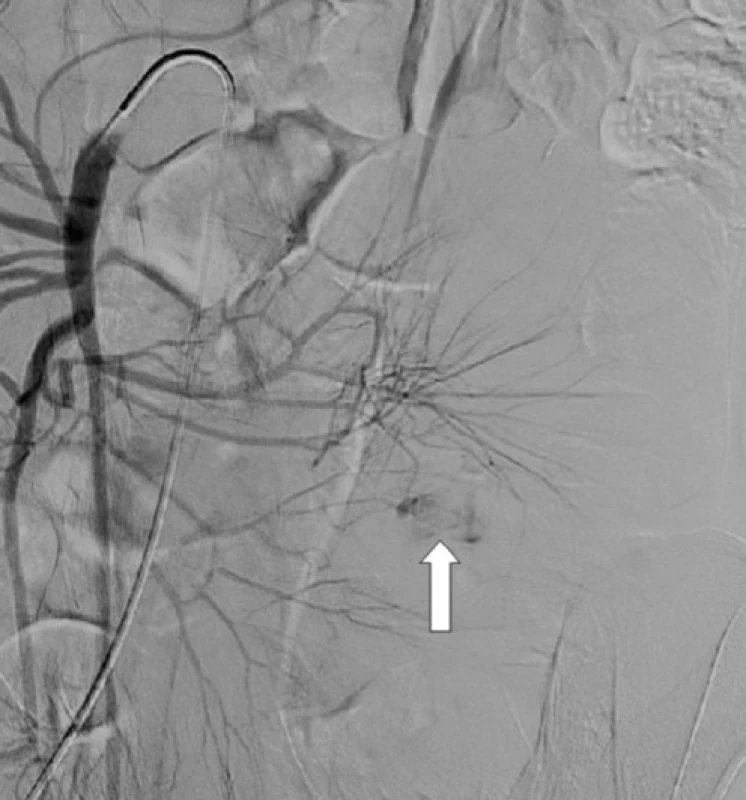
Image 2. Dieulafoy lézia jejúna – dvojbalónová endoskopia 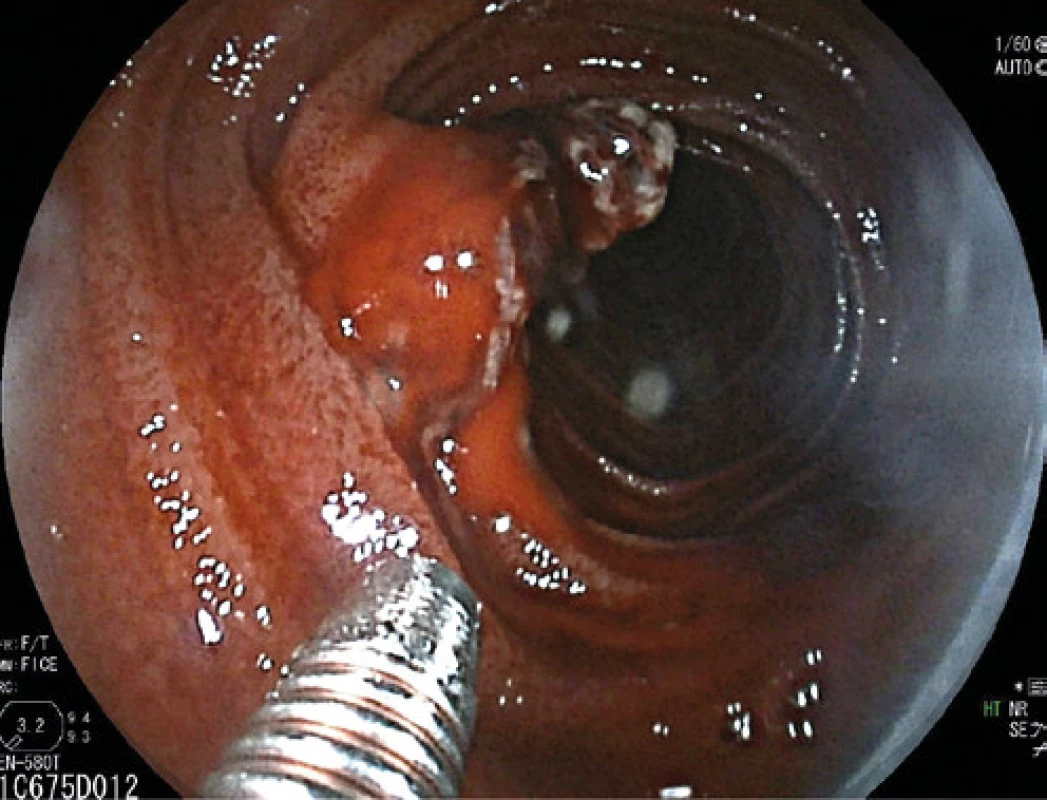
Image 3. Dieulafoy lézia jejúna, hematoxylin‑eozin, 10× 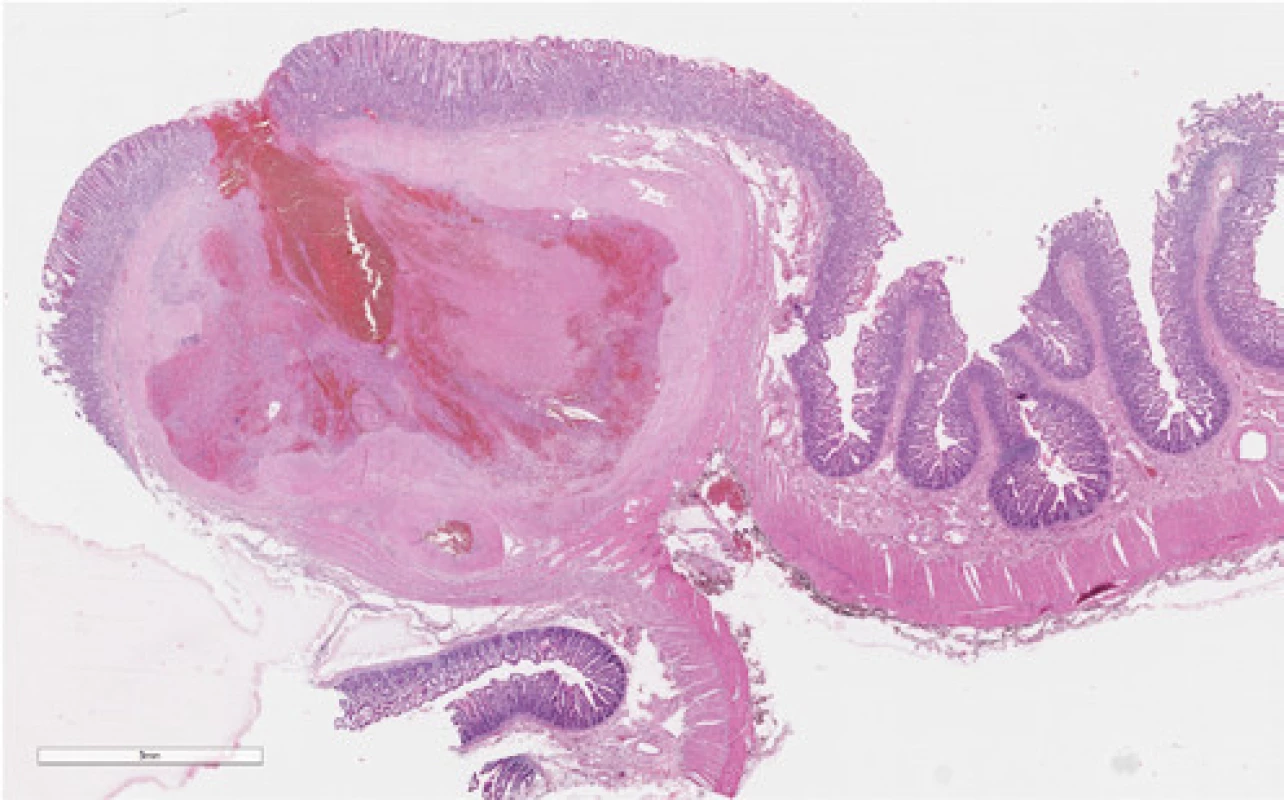
Image 4. Dieulafoy lézia jejuna, farbenie na elastiku (čierne vlákna) 35× 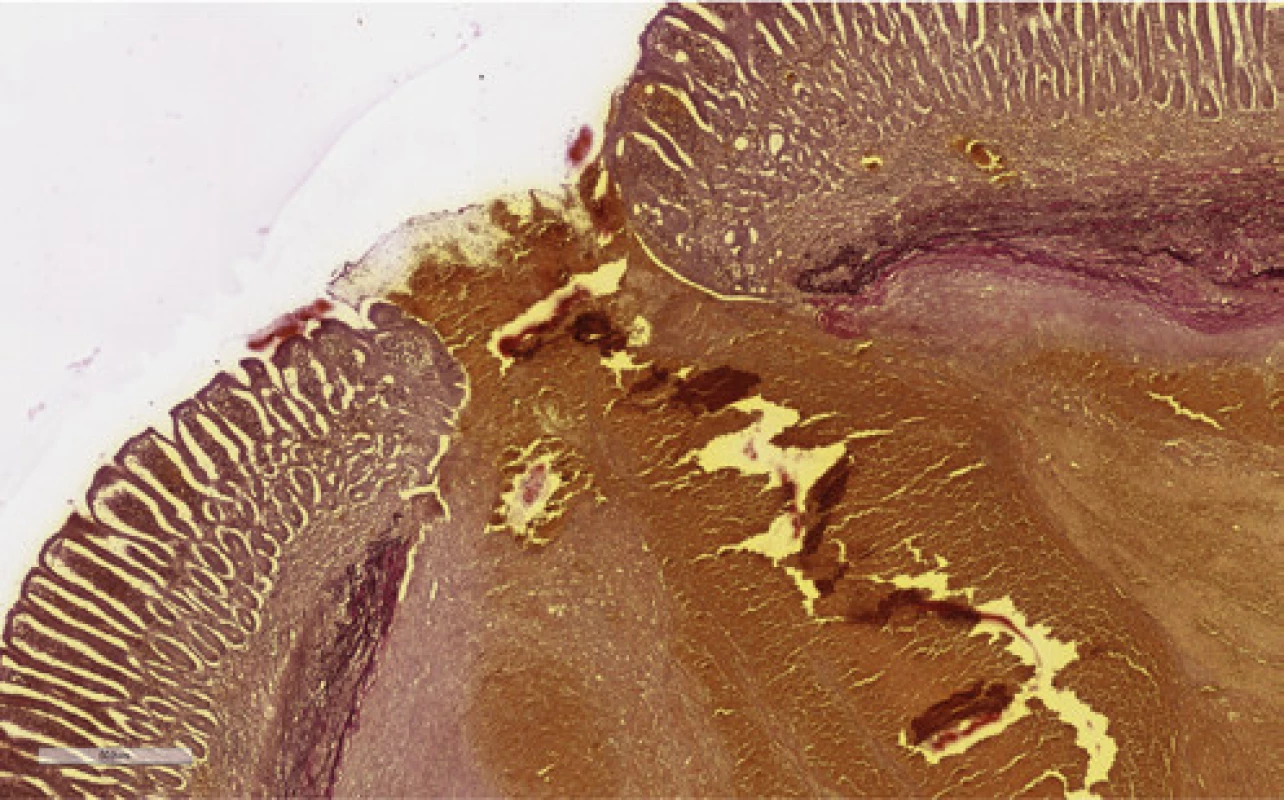
Pooperačný priebeh a rekonvalescencia sa obišli bez komplikácií. Po 8 dňoch hospitalizácie sa pacient preložil k doliečeniu a rehabilitácii na naše štandardné oddelenie. I po zaťažení stravou bol naďalej bez ťažkostí, bez recidívy krvácania a po 3 dňovej hospitalizácii sa následne prepustil do domáceho ošetrovania. V januári roka 2019 na plánovanej kontrole bol naďalej bez problémov a recidívy krvácania.
Diskusia
Krvácaním do GIT z neurčeného zdroja (v anglickej literatúre „obscure bleeding“) sa označuje recidivujúce či pretrvávajúce, nápadné alebo okultné krvácanie, pokiaľ sú vstupné štandardné endoskopické vyšetrenia (gastroskopia a kolonoskopia) negatívne (9). 75 % krvácaní z nejasného zdroja je lokalizovaných na tenkom čreve, zvyšok tvoria lézie prehliadnuté v dosahu štandardných endoskopických metód (9–11). Najčastejším zdrojom krvácania z neurčeného zdroja sú cievne malformácie (40 %), ďalej nádory tenkého čreva, vredy tenkého čreva, Crohnova choroba, ulcerácie ektopickej žalúdočnej sliznice v Meckelovom divertikli, varixy tenkého čreva, postradiačná enteropatia a iné (9). Dieulafoy lézia je jedna z možných príčin krvácania do GIT z nejasného zdroja. Krvácanie je často intermitentné, lokalita môže byť relatívne nedostupná pre konvekčnú endoskopiu hlavne v prípade jejuna a ilea a lézie sú malé, nenápadné a veľakrát nepostrehnuté i v prípade opakovania diagnostických metód (3). DL by sa mala endoskopicky odlíšiť od iných patológií s podobným klinickým prejavom a endoskopickým vzhľadom ako sú arteriovenózne malformácie, hereditárna hemoragická teleangiektázia alebo vaskulárne tumory. Predovšetkým gastrointestinálne stromálne tumory (GIST), ktoré stáli na prvom mieste v diferenciálnej diagnostike u nášho pacienta, môžu imitovať DL (12). Na rozdiel od hereditárnej hemoragickej teleangiektázie, žiadne genetické mutácie neboli asociované s DL. Angiodyspláziu možno odlíšiť od DL jej charakteristickým angiografickým obrazom ako je skoré venózne plnenie. Je veľmi dôležité rozlíšiť DL od adenomatózneho polypu, aby sa predišlo masívnemu krvácaniu z „polypektómie“ DL (3). Scitigraficky 99mTc značeným pertechnetátom po podaní pentagastrínu a H2‑blokátorov môžeme potvrdiť ektopickú žalúdočnú sliznicu v Meckelovom divertikli hlavne u mladších pacientov (9).
V minulosti sa diagnostika DL opierala skoro výlučne o histologické vyšetrenie po chirurgickej intervencii. V dnešnej dobe je DL diagnostikovaná skôr endoskopicky než histologicky. Endoskopické diagnostické kritériá pre DL zahrňujú niekoľko parametrov:
- aktívne arteriálne striekanie alebo mikropulzatívne krvácanie z minimálneho slizničného defektu (< 3 mm) alebo z normálnej okolitej sliznice;
- viditelná protrudujúca cievka s alebo bez aktívneho krvácania z minimálneho slizničného defektu alebo z normálnej okolitej sliznice;
- čerstvé, hutné priliehajúce koagulum s úzkym bodom prichytenia k minimálnemu slizničnému defektu alebo k normálne vyzerajúcej sliznici (2, 5).
Histologicky sa jedná o normálnu muskulárnu arteriolu bez výdutí, aterosklerotických zmien a bez známok vaskulitídy. Má abnormálne široký priemer, zachovávajúc si konštantnú šírku 1–3 mm. Prebieha vinuto pozdĺž submukózy a typicky protruduje cez drobný 2–5 mm slizničný defekt s fibrinoidnou nekrózou na jeho bázi (2, 5). Okolitá sliznica je normálna (5).
Jejunálna DL zahŕňa len 3,5 % všetkých krvácaní z tenkého čreva. V literatúre je popisovaných menej ako 50 prípadov jejunálnej DL (5). Pri negativite vstupných štandardných endoskopických vyšetrení krvácaní z nejasného zdroja a po vylúčení významnej striktúry čreva, je diagnostickou metódou voľby kapslová endoskopia (9–11). Výhodou je nízka invazivita, vysoká diagnostická výťažnosť (61 %) hlavne v intrahemoragickej fáze (do 48 hod) a vysoká pravdepodobnosť vyšetrenia celého tenkého čreva (84 %) (9). Nevýhodou je absencia terapeutického potenciálu (2, 3). Pri hemodynamickej nestabilite pacienta volíme diagnostické metódy s terapeutickým potenciálom ako angiografia alebo hlboká enteroskopia (jednobalónová alebo dvojbalónová). Lipka et al stanovil prevládajúcu lokalitu DL v proximálnom jejune (13) a Dulic ‑Lakovic et al ukázal, že priemerná vzdialenosť jejunálnej DL od pyloru bola 132 ± 115 cm (14), čo splňoval i náš pacient. Angiografické vyšetrenie je prínosné predovšetkým u pokračujúceho krvácania s intenzitou minimálne 0,5–1 ml/min (9, 15). Neexistuje špecifický radiologický obraz pre DL, ale nález extravazácie kontrastu z normálne vyzerajúcej veľkokalibrovej vinutej erodovanej artérie môže túto diagnózu naznačovať (3, 5). Tiež sa v literatúre popisuje prípad pacienta, u ktorého sa DL jejuna prezentovala krátkou striktúrou na CT a enteroklýze (16). CT angiografia bola prínosná v diagnostike miesta krvácania v 79,2 % (19/24) (17). Jednobalónová alebo dvojbalónová enteroskopia je podľa recentných štúdií preferovanou metódou liečby krvácania v strednej časti GIT (medzi Vaterovou papilou a Bauhinovou chlopňou), a teda aj jejunálnej DL (5). Poskytuje diagnostickú výťažnosť porovnatelnú s kapslovou enteroskopiou (57 %), ale aj možnosť odberu vzoriek k histologickému vyšetreniu a terapeutické možnosti u 43–84 % pacientov. Hlavnou nevýhodou je vyššia invazivita, nižšia dostupnosť, riziko komplikácií a relatívne nízka pravdepodobnosť vyšetrenia celého tenkého čreva v jednom sedení (29 %) (9). Malá veľkosť DL, masívne krvácanie alebo tvorba koagul v lumen tenkého čreva môže výrazne zťažiť diagnostiku, preto je často nutné endoskopiu opakovať (8). Scintigrafia s technéciom 99 značenými erytrocytmi môže byť nápomocná pri diagnostike krvácania z DL po nediagnostických endoskopiách. Je vysoko senzitívna (zachytí krvácanie až 0,1 ml/min), ale málo špecifická. Lokalizácia nie je presná, určí len orientačnú časť brušnej dutiny, kde sa zdroj krvácania nachádza, preto sa indikuje len výnimočne (3, 15). Podporné metódy ako endoskopický ultrazvuk a vyprovokovanie krvácania pomocou intravenózneho podania heparínu môže pomôcť zlepšiť diagnostickú úspešnosť DL (3).
Pacienti s DL sa obyčajne prezentujú masívnym krvácaním do GIT, preto stojí na prvom mieste v terapii všeobecný prístup pri krvácaní do GIT, ktorý zahrňuje tekutinovú resuscitáciu, krvné transfúzie a podrobnú monitoráciu vitálnych funkcií. Hlavný faktor určujúci, ktorá liečebná metóda je pre pacienta vhodná, je pacientov hemodynamický status (5). I keď neexistujú konkrétne odporúčané postupy pre terapiu DL, v posledných rokoch sú výrazne uprednostňované endoskopické a angiografické terapeutické postupy pred chirurgiou (3). Endoskopické terapeutické metódy sú liečbou voľby u ľahko dostupných lézií s úspešnosťou cez 90 % a nízkym rizikom recidívy krvácania pod 10 % (2, 3). Niektoré štúdie naznačujú, že mechanické hemostatické metódy sú v porovnaní s injekčnými a termokoagulačnými účinnejšie. Taktiež kombinácia endoskopických metód má nižší výskyt recidív krvácania než monoterapie (2, 3). Dulic ‑Lakovic et al popisoval recidívu krvácania u 3 z 10 pacientov po ošetrení DL balón‑asistovanou enteroskopiou (BAE), z toho 2 z 10 pacientov finálne vyžadovalo chirurgickú intervenciu (13, 14). Lipka et al zas preukázal 87,5 % (7 z 8) úspešnosť iniciálnej hemostázy pomocou jednobalónovej enteroskopie. Ani jeden pacient následne nevyžadoval chirurgickú intervenciu (13). V oboch štúdiách kombinovali hlavne termokoaguláciu, argonplazmakoaguláciu, adrenalínové injekcie a klipovanie. Selektívna angiografia s embolizáciou môže byť liečba voľby pre pacientov:
- u ktorých zlyhala endoskopická terapia,
- akútne krvácajú z dolného GIT alebo krvácanie je mimo dosah terapeutickej endoskopie,
- nie sú vhodnými kandidátmi pre chirurgické riešenie (8, 17).
Embolizácia nesie riziko ischémie čreva zásobovaného postihnutou artériou (2, 3). V literatúre popisované výsledky terapeutickej angiografie DL sú nekonštantné (17). Yilmaz et al. popisoval v zhrnutí 6 prípadov s jejunálnou DL, u ktorých terapeutická angiografia zlyhala podobne ako v našom prípade (5). Chirurgická revízia je nutná u pacientov, u ktorých zlyhala endoskopická alebo angiografická terapia alebo s hemodynamickou instabilitou, ako to bolo i v našom prípade. Laparoskopická minimálne invazívna intervencia je atraktívna varianta, vyžaduje ale preoperatívnu lokalizáciu miesta krvácania, na čo slúži intraoperatívna endoskopia (5, 8). Segmentálna resekcia a anastomóza je preferovaný chirurgický postup pri jejunálnej DL. Po chirurgickom ošetrení DL sa v literatúre nepopisuje žiadna recidiva krvácania (5). Kozan et al referoval podobný prípad končiaci urgentnou chirurgickou intervenciou ako v našej kazuistike, s rozdielom využitia intraoperatívnej enterotomie a endoskopie (8).Záver
Naša kazuistika potvrdzuje fakt, že DL jejuna patrí medzi významné príčiny krvácania do GIT a nemalo by sa na ňu zabúdať v diferenciálnej diagnostike krvácania z neurčeného zdroja. Jej diagnostika a liečba vyžaduje multidisciplinárny prístup, môže spôsobiť značné problémy, časové prestoje a patrí na pracoviská vyššieho typu s dostupným personálnym a technickým vybavením. I keď sú v dnešnej dobe preferované endoskopické a minimálne invazívne terapeutické postupy pri liečbe DL, chirurgická intervencia s preoperatívnou alebo perioperatívnou lokalizáciou zdroja krvácania je stále metódou voľby hlavne pri hemodynamickej nestabilite pacienta alebo po zlyhaní terapeutických endoskopických a angiografických metód. Pri voľbe diagnostickej a liečebnej metódy je potrebné pristupovať individuálne a podľa možností daného pracoviska.
Sources
1. Lukáš K, Hoch J, et al. Nemoci střev. Praha: Grada 2018, 292 s.
2. Baxter M, Aly EH. Dieulafoy’s lesion: Current trends in diagnosis and management. Ann R Coll Surg Engl 2010; 92 : 548–554.
3. Nojkov B, Cappel MS. Gastrointestinal bleeding from Dielafoy’s lesion: Clinical presentation, endoscopic findings, and endoscopic therapy. World J Gastrointest Endosc 2015; 7 : 295–307.
4. Parrot A, Antoine M, Khalil A, et al. Aproach to diagnosis and pathological examination in bronchial Dieulafoy disease: a case series. Resp Res 2008; 9 : 58.
5. Yilmaz T, Kozan R. Duodenal and jejunal Dieulafoy’s lesions: optimal managment. Clinical and Experimental Gastroenterology 2017; 10 : 275–283.
6. Zavras N, et al. Succesful diagnosis and treatment of Dieulafoy’s lesion with endoscopy and termocoagulation in full‑term neonate: Report of a case and literature review. J Ped Surg Case Reports 2014; 2 : 250–253.
7. Chao H, et al. Jejunal Dieulafoy lesion detected by intraoperative endoscopy in a child. Iran J Pediatr 2016; 26: e7727.
8. Kozan R, Gulen M, Yilmaz TU, et al. Massive lower gastrointestinal bleeding from a jejunal Dieulafoy lesion. Ulus Cerrahi Derg 2014; 30 : 225–227.
9. http://www.endoskopiste.cz/wp ‑content/uploads/2016/06/komentar ‑ke ‑guidelines‑asge ‑krvaceni ‑z‑neurceneho ‑zdroje.pdf
10. Tacheci I, Devière J, Kopacova M, et al. The importance of upper gastrointestinal lesions detected with capsule endoscopy in patients with obscure digestive bleeding. Acta Gastroenterol Belg 2011; 74 : 395–399.
11. Pennazio M, et al. Small ‑bowel capsule endoscopy and device ‑assisted enteroscopy for diagnosis and treatment of small ‑bowel disorders: European Society of Gastro ‑ intestinal Endoscopy (ESGE) Clinical Guideline 2015; 47 : 352–376.
12. Aomatsu N, et al. A case of emergency resection of a giant gastrointestinal stromal tumor of the stomach associated with hemorrhagic shock. Gan To Kagaku Ryoho 2013; 40 : 2185–2187.
13. Lipka S, Rabbanifard R, Kumar A, et al. A single ‑center United States experience with bleeding Dieulafoy lesions of the small bowel: diagnosis and treatment with single ‑balloon enteroscopy. Endosc Int Open 2015; 3 : 339–345.
14. Dulic ‑Lakovic E, et al. Bleeding Dieulafoy lesions of the small bowel: a systematic study on the epidemiology and efficacy of enteroskopic treatment. Gastrointest Endosc 2011; 74 : 573–580.
15. Adamová Z, Slováček R. Diagnostika a léčba krvácení do dolní části zažívacího traktu. Med praxi 2013; 10 : 380–382.
16. Kim JK, Jo BJ, Lee KM, et al. Dieulafoy’s lesion of jejunum: presenting small bowel mass and stricture. Yonsei Med J 2005; 46 : 445–447.
17. Alshumrani G, Almuaikeel M. Angiographic findings and endovascular embolization in Dieulafoy disease: a case report and literature review. Diagn Interv Radiol 2006; 12 : 151–154.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2020 Issue 6-
All articles in this issue
- Anafylaxe – akutní a dlouhodobý management
- Potravinová alergie a intolerance
- Poruchy v komplementovém systému
- Imunosenescence – západ slunce nad imunitním systémem
- Chřipka a její komplikace
- Familiární plicní fibróza – doporučení pro diagnostiku a léčbu
- Nové dělení krystalopatií z pohledu nefrologa
- Infarkt myokardu nebo syndrom zlomeného srdce?
- Dieulafoy lézia jejuna ako zdroj život ohrozujúceho krvácania
- Co nového internistům přinášejí doporučené postupy pro diagnostiku a léčbu plicní embolie z roku 2019?
- Perkutánní okluze ouška levé síně
- Současné postavení dietních opatření u pacientů s pokročilým stupněm chronického onemocnění ledvin
- Dysfunkčný dialyzačný cievny prístup a jeho endovaskulárna liečba
- Histiocytózy a neoplazie odvozené od makrofágů a dendritických buněk. Srovnání WHO klasifikace z roku 2017 a klasifikace Histiocyte society z roku 2016
- Glykovaný hemoglobín ako marker zvýšenia LDL a TAG – kohortná štúdia
- Deriváty sulfonylurey a riziko hypoglykemie u diabetiků 2. typu
- Endoskopická diagnostika a terapie pankreatobiliárních onemocnění u osob po resekci žaludku podle Billrotha I
- Nozokomiální methemoglobinemie
- Alergie a imunopatologie – hlavní téma
- Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Infarkt myokardu nebo syndrom zlomeného srdce?
- Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
- Potravinová alergie a intolerance
- Poruchy v komplementovém systému
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

