-
Medical journals
- Career
Klinická štúdia FOURIER
Authors: Ján Murín
Authors‘ workplace: I. interná klinika LF UK a UNB, Nemocnica Staré mesto, Bratislava, Slovenská republika
Published in: Vnitř Lék 2017; 63(6): 411-414
Category: Reviews
Overview
Dnes sa do klinickej praxe dostáva nová skupina hypolipidemických látok, tzv. inhibítory proteínu PCSK9, nakoľko aj u liečených statínmi ostáva naďalej vysoké kardiovaskulárne reziduálne riziko. Štúdia FOURIER (Further cardiovascular OUtcomes Research with PCSK9 Inhibition subjects with Elevated Risk) je prvou „príhodovou“ štúdiou, ktorá preukázala, že evolokumab (protilátka voči proteínu PCSK9) významne ďalej redukuje sérový LDL-cholesterol a následne aj kardiovaskulárnu morbiditu a mortalitu: (a) kompozitný primárny cieľ (kardiovaskulárnu mortalitu, výskyt infarktov, cievnych mozgových príhod, hospitalizácií pre nestabilnú anginu pectoris, koronárnych revaskularizácií) o 15 % (p < 0,001), (b) druhotný cieľ (kardiovaskulárnu mortalitu, výskyt infarktov a mozgových cievnych príhod) o 20 % (p < 0,001), (c) efekt liečby narastal s dĺžkou trvania liečby a (d) liečba bola bezpečná. Teda štúdia potvrdila, že ďalšia redukcia sérového LDL-cholesterolu pomocou evolokumabu významne redukuje výskyt kardiovaskulárnych príhod u rizikových chorých. Túto liečbu potrebujú hlavne tí kardiovaskulárne najrizikovejší.
Kľúčové slová:
ateroskleróza – evolokumab – kardiovaskulárne ochorenia – LDL-cholesterol – PCSK9 inhibítoryÚvod
LDL-cholesterol (LDL-C) je známym a modifikovateľným rizikovým faktorom kardiovaskulárneho (KV) ochorenia. Monoklonálne protilátky, inhibujúce proprotein konvertázu subtilizín – kexin typ 9 (PCSK9), sú novou triedou liekov, ktoré vynikajúco redukujú sérové hladiny LDL-C [1]. Evolokumab, jeden zo zástupcov tejto novej triedy liekov, je plnou humánnou monoklonálnou protilátkou a redukuje sérový LDL-C asi o 60 % [2,3].
Genetické práce [4,5] preukázali, že nositelia mutovaného génu PCSK9 „so stratou funkcie jeho alel“ mávajú nižšie sérové hladiny LDL-C a spolu s tým mávajú redukované aj riziko vzniku infarktu myokardu. Údaje z klinických štúdií vo fázach 2 a 3 s PCSK9 inhibítormi preukázali, že ak sa predĺžilo sledovanie chorých, tak u týchto pacientov zaznamenali významnú redukciu výskytu KV príhod [6,7], avšak príhod bolo málo (celkovo < 100 príhod).
Preto naplánovali a zahájili dlhodobú „prípadovú štúdiu“ FOURIER (Further cardiovascular OUtcomes Research with PCSK9 Inhibition subjects with Elevated Risk), ktorá analyzovala klinickú účinnosť a bezpečnosť evolokumabu pri jeho pridaní k statínovej liečbe (statín s vysokou alebo stredne silnou intenzitou pôsobenia) u chorých, ktorí trpeli zrejmým aterosklerotickým KV-ochorením [8].
Dizajn štúdie
FOURIER štúdia [8] je randomizovaná, dvojito zaslepená, placebom kontrolovaná a počtom zaradených pacientov aj veľká (1 242 centier, 49 krajín) štúdia. Sponzor (Amgen) zodpovedal za zber údajov, tie sa posunuli pracovnej skupine TIMI (the Thrombolysis In Myocardial Infarction) v Bostone, ktorej členovia vykonali analýzu štúdie a jej údajov.
Pacienti: vek 40–85 rokov, klinicky zrejmá prítomnosť aterosklerotického KV ochorenia, t. j. prekonaný infarkt myokardu, prekonaná nonhemoragická mozgová príhoda či prítomné symptomatické periférne arteriálne ochorenie, ale potrebné pre zaradenie chorého boli i ďalšie charakteristiky chorých, aby išlo o osoby s vyšším KV rizikom. Nasledovalo vyšetrenie séra nalačno s preukázaním LDL-C ≥ 1,8 mmol/l či non-HDL-C ≥ 2,6 mmol/l pri dobrej/optimálnej hypolipidemickej liečbe (obvykle statín vysokej intenzity – aspoň atorvastatín v dávke 20 mg denne či jeho ekvivalent) s (ne)pridaním ezetimibu podľa rozhodnutia ošetrujúceho lekára. Chorí boli potom randomizovaní v pomere 1 : 1 k liečbe evolokumabom (buď 140 mg každé 2 týždne alebo 420 mg raz mesačne subkutánne, pričom pacient si mohol vybrať) alebo placebom (ale títo chorí užívali dobrú dávku silného statínu).
Analyzované klinické príhody (end-pointy):
- a) primárny endpoint (kompozitný): KV úmrtie, myokardiálny infarkt, cievna mozgová príhoda, hospitalizácia pre nestabilnú anginu pectoris, koronárna revaskularizácia
- b) hlavný sekundárny endpoint (kompozitný): KV úmrtie, myokardiálny infarkt a mozgová cievna príhoda
Bezpečnosť liečby sa hodnotila zbieraním nežiaducich účinkov liečby a laboratórnym sledovaním istých parametrov v krvi. Endpointy hodnotila komisia expertov (bez znalosti o skúmanej liečbe chorých).
Štatistická analýza: Ako je obvyklé v podobných štúdiách, analyzovali výskyt príhod v oboch ramenách liečby (potrebný bol výskyt 1 630 príhod, aby sa s 90% štatistickou silou mohla preukázať efektivita liečby evolokumabom, t. j. 15% relatívna redukcia rizika výskytu príhod oproti ich výskytu v placebovom rameni liečby), použili tzv. Coxov model (Cox proportional hazards model so stratifikačnými kovariatnými faktormi) a hodnoty P boli kalkulované použitím log-rank testov.
Výsledky štúdie FOURNIER
Štúdia začala náborom pacientov vo februári roku 2013 a skončila ho v júni roku 2015, pričom sa nazbieralo spolu 27 564 pacientov: v ramene evolokumabovom bolo 13 784 pacientov a v placebovom ramene bolo 13 780 pacientov. Vstupné charakteristiky chorých boli podobné v oboch ramenách liečby (tab. 1). Predčasné vyradenie chorých zo štúdie sa dotýkalo 12,5 % pacientov (5,7 %/rok), odobratie informovaného súhlasu sa dotklo 0,7 % (0,3 %/rok) chorých a „stratených pacientov“ bolo < 0,1 % (0,03 %/rok), a to podobne v oboch ramenách štúdie. Medián trvania štúdie bol 26 mesiacov, čo znamenalo 59 865 paciento-rokov sledovania. Overenie primárneho endpointu bolo skompletizované u 99,5 % potenciálnych paciento-rokov sledovania.
Table 1. Vstupné charakteristiky chorých 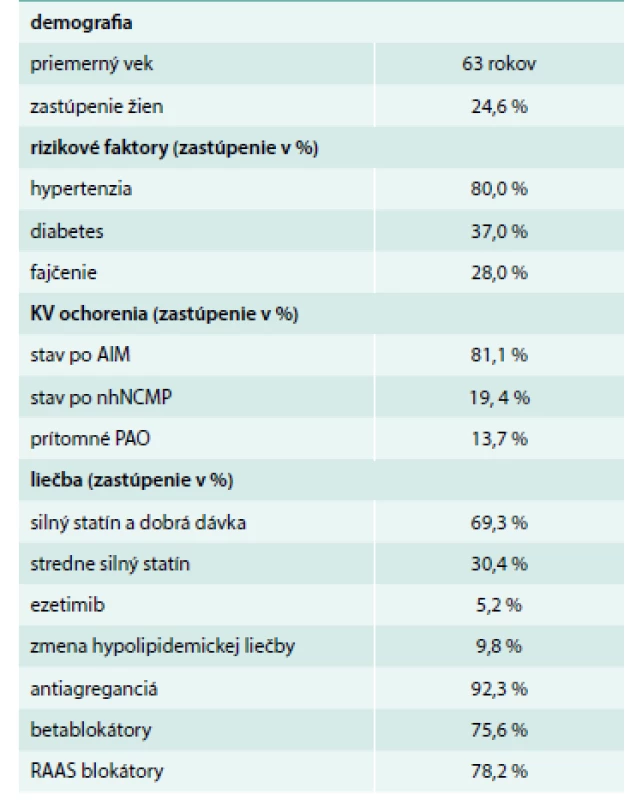
r – roky KV – kardiovaskulárny AIM – akútny infarkt myokardu nhNCMP – nehemoragická náhla cievna mozgová príhoda PAO – symptomatické periférne artériové ochorenie RAAS – renín-angiotenzín-aldosterónový systém Údaje o sérových lipidoch
Medián hodnoty sérového LDL-C vstupne bol 2,4 mmol/l. V 48. týždni štúdie bola prítomná redukcia sérového LDL-C v ramene liečby evolokumabom (oproti liečbe placebom) o 59 % výraznejšie (výsledok bol štatistický významný s p < 0,001), stredná absolútna redukcia LDL-C bola 1,45 mmol/l a medián LDL-C v evolokumabovom ramene bol 0,78 mmol/l. Dôležitým zistením bolo, že sa táto LDL-C redukcia udržala po celý čas štúdie. Na 48. týždeň liečby sa v ramene evolokumabovom dostalo pod hodnotu sérového LDL-C < 1,8 mmol až 87 % pacientov (v placebovom ramene len 18 % pacientov), pod hodnotu LDL-C < 1,0 mmol/l až 67 % pacientov (v placebovom ramene len 0,5 % pacientov) a pod hodnotu < 0,65 mmol/l až 42 % pacientov (v placebovom ramene menej ako 0,1 % pacientov), všetko štatisticky významné rozdiely v liečbe. Evolokumab v porovnaní s placebom významne redukoval v 48. týždni liečby aj non-HDL-C o 52 % a apolipoproteín B o 49 %, opäť štatisticky významne s p < 0,001.
Ovplyvnenie KV príhod
Evolokumab významne redukoval riziko výskytu primárneho endpointu (KV mortality, výskytu infarktu myokardu a cievnej mozgovej príhody, hospitalizácií pre nestabilnú anginu pectoris, koronárnych revaskularizácií): v tomto ramene sa tieto príhody vyskytli u 1 344 pacientov (9,8 %) oproti ich výskytu u 1 563 pacientov (11,3 %) v placebovom ramene liečby s relatívnym rizikom (hazard ratio) 0,85 (p < 0,001). Podobne bol úspešne liečbou evolakumabom redukovaný aj kľúčový sekundárny endpoint (KV mortalita, infarkt myokardu, mozgová cievna príhoda), prítomný u 816 pacientov (5,9 %) v ramene liečby evolokumabom vs u 1 013 pacientov (7,4 %) v placebovom ramene liečby, s relatívnym rizikom 0,80 (p < 0,001). Dôležitou skutočnosťou je však aj pozorovanie, že redukcia rizika KV príhod liečbou evolokumabom stúpala u primárneho endpointu v čase – z 12 % v 1. roku liečby na 19 % v neskorších rokoch liečby a sledovania. Podobne tomu bolo aj s kľúčovým sekundárnym endpointom – relatívne riziko redukcie bolo v 1. roku 16 %, ale v ďalších rokoch už 25 %.
Iné príhody
Evolokumab nemal efekt na KV mortalitu, redukoval však riziko výskytu infarktu myokardu (o 27 %, významne s p < 0,001), výskytu mozgových cievnych príhod (o 21 %, s p < 0,001) – dominantne ischemických príhod (o 25 %) a výskyt revaskularizácií tiež poklesol významne (o 22 %, p < 0,001). Evolokumab ale neovplyvnil výskyt hospitalizácií pre nestabilnú anginu pectoris, neovplyvnil hospitalizáciu pre zhoršenie srdcového zlyhávania a ani celkovú mortalitu. Spomínané benefity evolokumabu pri primárnom endpointe i pri kľúčovom sekundárnom endpointe boli prítomné aj v hlavných (veľkých) podskupinách pacientov – pri zohľadnení veku, pohlavia a aj typu KV ochorenia. Benefit bol pri každej úrovni vstupného sérového LDL-C, t. j. v hornom kvartile pacientov, v ktorom bol vstupne LDL-C 3,3 mmol/l, ale aj v dolnom kvartile, v ktorom bol vstupne LDL-C len 1,9 mmol/l. Intenzita statínovej liečby benefit neovplyvnila, ten bol prítomný vo všetkých skupinách statínovej liečby (teda bez ohľadu na intenzitu statínovej liečby). Obe dávky evolokumabu boli podobne úspešné.
Bezpečnosť liečby
Neboli preukázané významné rozdiely vo výskyte nežiaducich účinkov liečby medzi oboma spôsobmi liečby (ani vážne nežiaduce účinky, ani prerušenia liečby pre nežiaduce účinky). Medzi oboma ramenami liečby neboli rozdiely vo výskyte myalgií či myopatií, vo výskyte katarakt, vo výskyte porúch kognície ani vo výskyte hemoragických mozgových príhod. Výskyt kožných reakcií v mieste vpichov bol veľmi nízky, ale častejší v ramene liečby evolokumabovom (2,1 % vs 1,6 %), pričom > 90 % týchto reakcií bola hodnotená ako mierna (len 0,1 % pacientov v každom ramene liečby túto liečbu ukončilo z tohto dôvodu). Liečba evolokumabom nezvýšila výskyt diabetu (RR: 1,05, NS), výskyt alergických reakcií bol podobný (3,1 % evolokumab vs 2,9 % placebo). Výskyt nových protilátok voči evolokumabu sa dotkol 43 pacientov (0,3 %) a išlo o viažuce sa protilátky, a nie o blokujúce protilátky.
Čo štúdia FOURIER priniesla a čo nám pre klinickú prax odkazuje?
Evolokumab, pridaný k statínovej liečbe, redukuje sérový LDL-C o 59 % z jeho bazálnej (vstupnej) hodnoty (z mediánu LDL-C 2,4 mmol/na medián LDL-C 0,78 mmol/l) – toto je ohromný benefit a tento stav bol trvalý v priebehu štúdie. Z hľadiska výskytu KV príhod došlo práve preto liečbou evolokumabom k 15% redukcii výskytu primárneho endpointu (KV mortality, výskytu infarktov myokardu a cievnych mozgových príhod, hospitalizácií pre nestabilnú anginu pectoris a koronárnych revaskularizácií) a k 20% redukcii hlavného sekundárneho endopointu (KV mortality, infarktov myokardu a cievnych mozgových príhod).
V priebehu 26 mesiacov sledovania chorých (medián) neboli prítomné v ramene liečby evolokumabom žiadne nežiaduce účinky s výnimkou lokálnych kožných reakcií v mieste podávania lieku.
Novou skutočnosťou štúdie FOURIER je, že evolokumab redukoval priemerné hodnoty sérového LDL-C o mnoho viac než bola schopná preukázať iná hypolipidemická liečba. Predošlé štúdie, napr. štúdia PROVE IT-TIMI 22 a štúdia TNT štúdia, preukázali tiež vyššiu redukciu výskytu KV príhod v ramene liečby, v ktorej sa dosiahla väčšia redukcia sérového LDL-C [9,10] – obvykle silnejším statínom vs slabším statínom alebo použitím vyššej a nižšej dávky v daných ramenách liečby – porovnaním ramena liečby s dosiahnutím LDL-C v sére 2,6 mmol/l vs 1,8 mmol/l. Nedávno túto istú skutočnosť potvrdila aj štúdia IMPROVE-IT (rameno liečby s LDL-C 1,8 mmol/l vs s LDL-C 1,4 mmol/l, v druhom ramene bolo menej KV príhod) [11]. A tento koncept, t. j. „mať nižšiu sérovú hladinu LDL-C je lepšie (nakoľko to redukuje aj výskyt KV príhod)“, potvrdila elegantne a jasne i štúdia FOURIER. Výsledky štúdie FOURIER dobre ladia aj so štúdiou GLAGOV, ktorá preukázala, že pri nízkej hladine sérového LDL-C nastáva regresia koronárnej aterosklerózy (teda regresia veľkosti/objemov plakov, hodnotená metódou intrakoronárneho ultrazvuku – IVUS) [12]. Ukazuje sa, že benefit nízkej sérovej hladiny LDL-C je prítomný i pri veľmi nízkej jeho sérovej hladine, t. j. v úrovni až 0,52–0,65 mmol/l [13,14].
Aj v štúdii FOURIER sa potvrdili skúsenosti s inými hypolipidemickými prístupmi (statíny, ezetimib, kombinácie), že efekt KV protekcie sa časom zlepšuje, napr. v prípade kľúčového sekundárneho endpointu (výskyt KV mortality, výskyt infarktov myokardu a mozgových príhod) bol redukovaný v 1. roku liečby o 16 %, ale v 2. roku a ďalšom období to už bolo o 25 % (ohromné, však!). Aj tu sa potvrdilo (ako v predošlých štúdiách s i inými liekmi), že ďalšia redukcia sérového LDL-C neovplyvnila KV mortalitu [15]. Ohromne dobrá liečba, nielen evolokumabom, pomohla redukovať výskyt KV príhod v štúdii FOURIER na len tretinu výskytu týchto príhod v známej a dávnej štúdii 4S [16].
Štúdia FOURIER znova potvrdila, že redukcia KV príhod nastáva dlhodobou a výraznou redukciou sérového LDL-C, zvykne sa to prepočítavať na pokles LDL-C o 1,0 mmol/l, pri ktorom redukcia KV príhod býva okolo 21–22 % [17].
Liečba evolokumabom bola i bezpečná, a aj lokálne „vpichové“ problémy sú ľahko znesiteľné pri ohromnom KV benefite. Výskyt diabetu liečbou nestúpol. Neurokognitívne nežiaduce účinky, i pri nízkych hladinách sérového LDL-C, sa neobjavili. Výskyt protilátok voči evolokumabu bol nízky a tieto protilátky neblokovali efekt liečby.
Ako jedinú limitáciu štúdie niektorí pokladajú „krátke trvanie štúdie“, keďže štúdie s inými hypolipidemikami trvali oveľa dlhšie, až okolo 5 rokov. Tu sa plánovalo trvanie štúdie na 4 roky, ale výskyt príhod dovolil štúdiu ukončiť oveľa skôr.
Odkaz štúdie je teda celkom jasný. Bude treba uvažovať, ktorým pacientom túto liečbu dať. Bude to kompromis medzi hľadaním týchto rizikových osôb a finančnou náročnosťou liečby. Treba sa však s tým zapodievať. Benefit je totiž ohromný.
Záver
Štúdia FOURIER potvrdila platnosť konceptu, že „nižšia sérová hladina LDL-C u KV chorého redukuje výskyt KV príhod“, a tento benefit narastá s trvaním liečby. Liečbou evolokumabom sa tiež dosiahla výraznejšia redukcia sérového LDL-C ako liečbou len statínmi, čo pridalo KV benefit. Liečba bola bezpečná. Treba ju odporúčať najrizikovejším chorým.
prof. MUDr. Ján Murín, CSc.
jan.murin@gmail.com
I. interná klinika LF UK a UNB,
Nemocnica Staré Mesto,
Bratislava,
Slovenská republika
www.unb.sk
Doručeno do redakce redakce 26. 4. 2017
Přijato po recenzi 1. 6. 2017
Sources
1. Giugliano RP, Sabatine MS. Are PCSK9 inhibitors the next breakthrough in the cardiovascular field? J Am Coll Cardiol 2015; 65(24): 2636–2651. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2015.05.006>.
2. Blom DJ, Hala T, Bolognese M et al. A 52-week placebo-controlled trial of evolocumab in hyperlipidemia. N Engl J Med 2014; 370(19): 1809–1819. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1316222>.
3. Robinson JG, Nedergaard BS, Rogers WJ et al. Effect of evolocumab or ezetimibe added to moderate - or high-intensity statin therapy on LDL-C lowering in patients with hypercholesterolemia: the LAPLACE-2 randomized clinical trial. JAMA 2014; 311(18): 1870–1882. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2014.4030>.
4. Cohen JC, Boerwinkle E, Mosley TH Jr et al. Sequence variations in PCSK9, low LDL, and protection against coronary heart disease. N Engl J Med 2006; 354(12): 1264–1272. . Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa054013>.
5. Karhiresan S. [Myocardial Infarction Genetics Consortium]. A PCSK9 missense variant associated with a reduced risk of early-onset myocardial infarction. N Engl J Med 2008; 358(21): 2299–2300. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMc0707445>
6. Sabatine MS, Giugliano RP, Wiviott SD et al. Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med 2015; 372(16): 1500–1509. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1500858>.
7. Robinson JG, Farnier M, Krempf M et al. [ODYSSEY LONG TERM Investigators]. Efficacy and safety of alirocumab in reducing lipids and cardiovascular events. N Engl J Med 2015; 372(16): 1489–1499. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1501031>.
8. Sabatine MS, Giugliano RP, Keech AC et al. Evolocumab and clinical outcomes in patients with cardiovascular disease. N Engl J Med 2017; 376(18):1713–1722. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1615664>.
9. Cannon CP, Braunwald E, McCabe Ch et al. Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med 2004; 350(15): 1495–1504. Erratum in N Engl J Med. 2006; 354(7): 778. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa040583>.
10. LaRosa JC, Grundy SM, Waters DD et al. Intensive lipid lowering with atorvastatin in patients with stable coronary disease. N Engl J Med 2005; 352(14): 1425–1435. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa050461>.
11. Cannon CP, Blazing MA, Giugliano RP et al. Ezetimibe added to statin therapy after acute coronary syndromes. N Engl J Med 2015; 372(25): 2387–2397. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1410489>.
12. Nicholls SJ, Puri R, Anderson T et al. Effect of evolocumab on progression of coronary disease in statin-treated patients: the GLAGOV randomized clinical trial. JAMA 2016; 316(22): 2373–2384. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2016.16951>.
13. Loyd-Jones DM, Morris PB, Ballantyne CM et al. 2016 ACC expert consensus decision pathway on the role of nonstatin therapies for LDL-cholesterol lowering in the management of atherosclerotic cardiovascular disease risk: a report of the American College of Cardiology Task Force on Clinical Expert Consensus Documents. J Am Coll Cardiol 2016; 68(1): 92–125. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2016.03.519>.
14. Landmesser U, Chapman JM, Farnier M et al. European Society of Cardiology/European Atherosclerosis Society Task Force consensus statement on proprotein convertase subtilisin/kexin type 9 inhibitors: practical guidance for use in patients at very high cardiovascular risk. Eur Heart J 2016. pii: ehw480. Dostupné z DOI: <http://dx.doi.org/10.1093/eurheartj/ehw480>.
15. Baigent C, Blackwell L, Emberson J et al. [Cholesterol Treatment Trialists’ Collaboration]. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170 000 participants in 26 randomised trials. Lancet 2010; 376(9753): 1670–1681. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(10)61350–5>.
16. [Scandinavian Simvastatin Survival Study Group]. Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). Lancet 1994; 344(8934): 1383–1389. Dostupné z DOI: <http://dx.doi.org/10.1016/S0140–6736(94)90566–5>.
17. Silverman MG, Ference BA, Im K et al. Association between lowering LDL-C and cardiovascular risk reduction among different therapeutic review and meta-analysis. JAMA 2016; 316(12): 1289–1297. Dostupné z DOI: <http://dx.doi.org/10.1001/jama.2016.13985>.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2017 Issue 6-
All articles in this issue
- Rizikové faktory kardiovaskulárních onemocnění u potomků nemocných po časném infarktu myokardu
- Úskalia stanovenia vitamínu D
- Klinická štúdia FOURIER
- Primární testikulární lymfomy
- Rivaroxaban u rizikových pacientů
- Dva pohľady na venózny tromboembolizmus u onkologických pacientov
- Inzulinová pumpa u diabetu 2. typu: léčba zaměřená na B-buňku
- Prediktory kvality života u českých pacientek po léčbě karcinomu prsu se zaměřením na dovednosti zvládání zátěže
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Primární testikulární lymfomy
- Inzulinová pumpa u diabetu 2. typu: léčba zaměřená na B-buňku
- Úskalia stanovenia vitamínu D
- Dva pohľady na venózny tromboembolizmus u onkologických pacientov
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

