-
Medical journals
- Career
Feochromocytom – proč je jeho časná diagnóza pro pacienta důležitá?
Authors: Tomáš Zelinka; Jiří Widimský Jr
Authors‘ workplace: Centrum pro výzkum, diagnostiku a léčbu hypertenze III. interní kliniky – kliniky endokrinologie a metabolizmu 1. LF UK a VFN Praha, přednosta prof. MUDr. Štěpán Svačina, DrSc., MBA
Published in: Vnitř Lék 2015; 61(5): 487-491
Category: Reviews
Overview
Feochromocytom se může projevit různými příznaky, symptomy na podkladě setrvalého nebo paroxyzmálního uvolňování katecholaminů. Arteriální hypertenze může být trvalá nebo záchvatovitá a palpitace jsou většinou projevem sinusové tachykardie. V některých případech, dokonce jako první projev feochromocytomu, se mohou vyskytnout závažné kardiovaskulární komplikace, jako je hypertenzní emergentní situace, ischemie myokardu, kardiomyopatie a srdeční selhání, multisystémová krize nebo šok. Vylučování katecholaminů může být doprovázeno i arytmiemi – tachykardiemi (supraventrikulárními a komorovými) a méně často i bradykardiemi (AV blokem nebo junkčními). Vliv katecholaminů není omezen jen na myokard, ale může také vést k postižení centrální nervové soustavy, jako je tranzientní ischemická ataka nebo cévní mozková příhoda. Protože většina z těchto komplikací může být i život ohrožující, jedinou prevencí je včasná diagnóza a správná léčba, především ve specializovaných centrech.
Klíčová slova:
feochromocytom – hypertenze – ischemie myokardu – katecholaminy – ortostatická hypotenze – poruchy srdečního rytmu – postižení centrálního nervového systémuÚvod
Jako feochromocytom označujeme ty nádory, které vycházejí z dřeně nadledvin a většinou produkují a také vylučují katecholaminy. Nádory vycházející z chromafinní tkáně mimo dřeň nadledviny označujeme jako paragangliomy a typicky se vyskytují v oblasti hlavy a krku a dále hrudníku, břicha i malé pánve. Nádory hlavy a krku většinou bývají sekrečně němé, ostatní mohou také vylučovat katecholaminy, a pak je označujeme jako funkční paragangliomy [1]. V našem přehledu budeme používat termín feochromocytom (FEO) pro funkční nádory. První popis FEO pochází z roku 1886, kdy byla Fränkelem popsána mladá pacientka s bilaterálním tumorem nadledviny, která umřela na maligní hypertenzi [2]. Výraz paragangliom byl zaveden v roce 1908 Aleziasem a Peyronem za účelem popisu extraadrenálních chromafinních tumorů vycházejících z paraganglií a termín feochromocytom (nádor hnědé barvy) byl použit poprvé Pickem v roce 1912. V roce 1922 byly popsány L‘Abbém et al paroxyzmální hypertenzní krize u mladé pacientky, která měla zjištěn FEO při pitvě. První úspěšná operace FEO v Evropě byla provedena v roce 1926 Rouxem ve Švýcarsku a následující rok pak také C. H. Mayoem v USA [3].
Feochromocytom a paragangliom jsou velmi zvláštní nádory, které zajímají nejen patology (dosud nejsou stanovena žádná jednoznačná prognostická data stran predikce případné malignity, a tak zůstává jediným kritériem malignity u FEO přítomnost metastáz, tedy přítomnost chromafinní tkáně v místech, kde se normálně nenacházejí – nejčastěji se jedná o lymfatické uzliny, kosti, játra a plíce), ale také genetiky (do dnešní doby bylo popsáno celkem 18 genů [4], jejichž mutace může být spojena se vznikem feochromocytomu nebo paragangliomu – mezi ty nejtypičtější patří syndrom mnohočetné endokrinní neoplazie 2. typu, syndrom von Hippelův-Lindauův nebo syndromy mnohočetné paragangliomatózy), biochemiky (v poslední době byl udělán velký pokrok v diagnostice FEO, u nějž je základní metodou pro diagnózu těchto nádorů stanovení metanefrinů, především plazmatických; ukázala se pak i korelace mezi nádorovým biochemickým fenotypem [druhem vylučovaných katecholaminů nebo metanefrinů] a typem genetické mutace [5]). Pro kliniky může být FEO zajímavý především svojí klinickou prezentací, která je ve velké většině případů dána sekrecí katecholaminů (výjimkou může být např. útlak tumorem) a může být velmi variabilní (často bývají projevy velmi nenápadné, a tak je dnes asi 30 % FEO diagnostikováno při vyšetřeních provedených z jiného důvodu [6]). Smyslem tohoto přehledu je právě upozornit na tuto klinickou variabilitu – především na kardiovaskulární projevy, a to včetně těch život ohrožujících. Ty byly dříve také příčinou častých úmrtí na FEO [7] a i dnes mohou být vysvětlením úmrtí u pacientů, u kterých byl FEO diagnostikován až při pitvě [8].
Arteriální hypertenze a ortostatická hypotenze
Arteriální hypertenze se vyskytuje asi u 80–90 % pacientů s FEO. Může se jednat o hypertenzi setrvalou nebo o záchvatovitou, a to i v kombinaci. Zvýšení hladiny noradrenalinu je spojeno se zvýšením periferní cévní rezistence a sníženým srdečním indexem, což vede ke zvýšení systolického i diastolického krevního tlaku. Naopak adrenalin působí i na β2-adrenergní receptory, a tedy většinou nevede ke zvýšení diastolického krevního tlaku, ale jen k vzestupu systolického krevního tlaku a srdeční frekvence. Náhlá sekrece adrenalinu je spojena i s typickými záchvatovitými projevy, jako jsou palpitace, bolesti hlavy a pocení. Dnes už se málokdy setkáváme s projevy maligní hypertenze, jako je neuroretinopatie. Přesto jsme se nedávno setkali s pacientem, u něhož se FEO projevil náhle vzniklou poruchou vízu následkem těžké hypertenze a s následnou úplnou úpravou zraku po adrenalektomii. Frekvence záchvatů může být různá – od velmi častých obtíží, které má pacient několikrát denně, až po obtíže, které se vyskytují velmi zřídka, tedy i déle než za měsíc. Záchvaty mohou trvat velmi krátce (tedy několik minut), zřídka pak i několik hodin a mohou být vyprovokovány různými podněty (cvičením, močením, příjmem určité potraviny, manipulací s tumorem nebo i určitými léky – máme nedávnou zkušenost s mladou pacientkou, u níž došlo k vyvolání život ohrožujícího FEO záchvatu podáním pervitinu). Vnímavost adrenergních receptorů k vysokým hladinám katecholaminů je u každého pacienta jiná, a tak vlastní hladina katecholaminů nekoreluje se stupněm arteriální hypertenze a přítomností dalších obtíží. U jednotlivého pacienta je však vzestup hladiny katecholaminů spojen s následným vzestupem hodnot krevního tlaku [9].
Pro FEO je ale typický také výskyt ortostatické hypotenze, která se může vyskytnout až u 10–50 % pacientů s FEO [10]. Kombinace arteriální hypertenze a ortostatické hypotenze je pro FEO typická. Pravděpodobným vysvětlením by mohla být hypovolemie a desenzitizace α-adrenergních receptorů.
Pokud u pacienta s FEO provedeme 24hodinové monitorování krevního tlaku, můžeme u těchto pacientů očekávat zvýšenou variabilitu a také absenci (nebo často i vzestup) nočního poklesu krevního tlaku [11,12]. Jedním z možných vysvětlení může být kromě opakovaných vzestupů krevního tlaku také již zmiňovaný sklon k ortostatické hypotenzi (obr. 1) [12].
Image 1. Záznam 24hodinového monitorování krevního tlaku u pacienta s mnohočetnými funkčními paragangliomy (krk, mediastinum) s opakovanými náhlými vzestupy a poklesy krevního tlaku, které jsou doprovázeny vzestupem srdeční frekvence 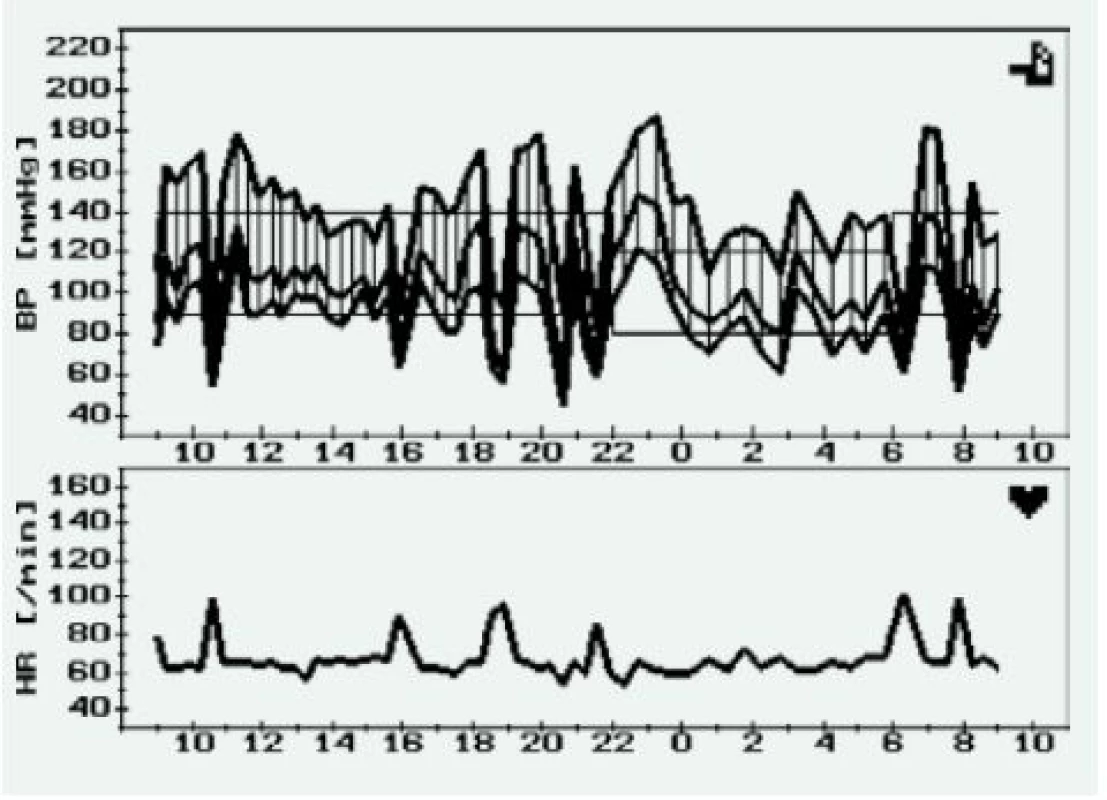
Arytmie
Stimulace β-receptorů katecholaminy je doprovázena palpitacemi nejméně u 50–70 % pacientů. Sinusová tachykardie se vyskytuje nejčastěji, ale setkat se můžeme i se supraventrikulárními (i fibrilace síní) i komorovými arytmiemi včetně komorové tachykardie (pro FEO je typické i prodloužení QT intervalu, takže se můžeme setkat i s polymorfní komorovou tachykardií). U FEO se však může vyskytnout i reflexní bradykardie nebo dokonce i AV blok vyššího stupně. Zajímavostí je, že se oba typy arytmií (bradykardie a tachykardie) mohou vyskytovat u jednoho pacienta (sami máme zkušenost se 2 takovými pacienty).
Ischemie myokardu
Bolesti na hrudi (doprovázející ostatní záchvatovité obtíže) patří také k typickým obtížím pacientů s FEO. Často bývají tito pacienti podrobováni i invazivnímu vyšetření, jehož výsledek neukáže významnější koronární aterosklerózu. Zavedení troponinů do rutinní klinické praxe pak výrazně zvýšilo i výskyt infarktu myokardu (v tomto případě většinou 2. typu) u těchto nemocných. Vysoké hladiny katecholaminů vedou ke zvýšené spotřebě kyslíku myokardu, vazokonstrikci a vazospazmům, zvýšené agregaci trombocytů nebo i k toxickým účinkům, jako je buněčná smrt nebo fibróza [13]. Často se setkáváme se změnami na EKG – sami jsme se setkali s elevacemi ST úseku, které napodobovaly STEMI, dále inverzí T vlny nebo depresemi ST úseku (obr. 2A). Tyto odchylky se upraví po ústupu klinických obtíží nebo až po úspěšném odstranění tumoru (obr. 2B). Dříve jsme se však mohli setkat u neléčených pacientů s častým uzávěrem koronární tepny jako příčinou úmrtí [7].
Image 2. EKG u pacientky s feochromocytomem před operací (A) ukazující na difuzní změny ST úseku a 5. pooperační den (B), kde tyto změny již nejsou patrné 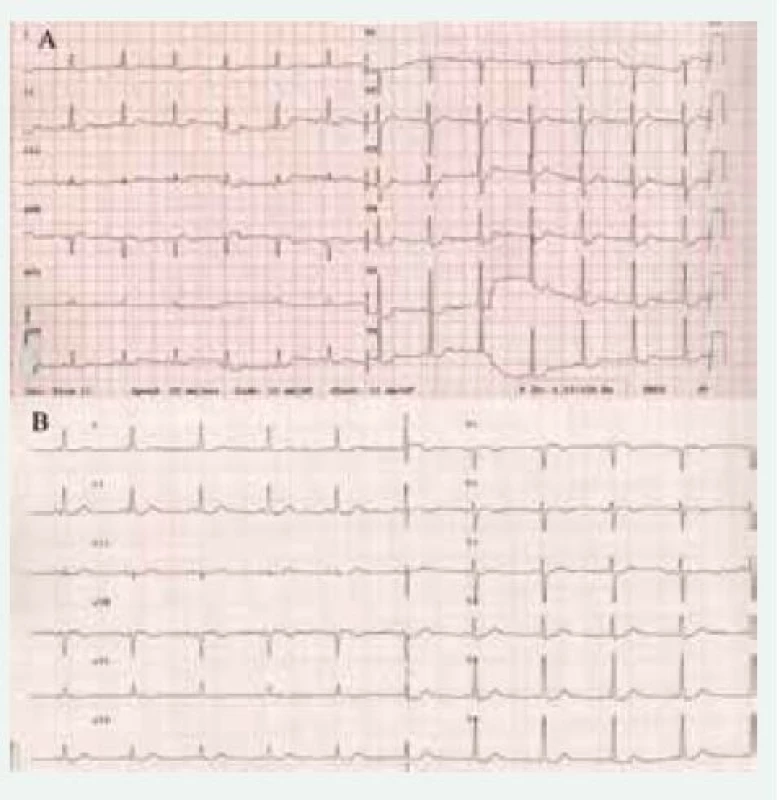
Hypertrofie myokardu, (takotsubo) kardiomoypatie a srdeční selhání
Katecholaminy mohou vést různými způsoby k akutnímu i chronickému postižení myokardu. K již výše zmíněným mechanizmům vedoucích k ischemii myokardu se přidává i zvýšená mobilita lipidů, přetížení vápníkem, zvýšená tvorba volných radikálů nebo zvýšená permeabilita sarkolem. Občasný výskyt hypertrofie myokardu u FEO (někdy až v podobě hypertrofické kardiomyopatie) pak většinou nesouvisí s výší krevního tlaku, ale s katecholaminy indukovanou produkcí proteinů [13]. Pokud jsou pacienti pečlivě vyšetřováni, výskyt systolické dysfunkce levé komory nebo akutní katecholaminové kardiomyopatie nemusí být vzácný – v některých případech až 11–20 % [14,15]. Zřídka může být FEO doprovázen kardiomyopatií, často dilatovanou, dnes pak v podobě tzv. takotsubo kardiomyopatie (tento výraz budeme používat i u pacientů s FEO, byť z definice vyplývá, že pro diagnózu takotsubo kardiomyopatie je nutno vyloučit FEO [16]), která je typickým následkem vysokých hladin katecholaminů. Dnes se ukazuje, že takotsubo kardiomyopatie (jak typická s akinézou hrotových oblastí nebo naopak invertovaná s akinézou bazálních částí myokardu) je velmi často komplikací FEO a má horší průběh (a může se i zopakovat) než u pacientů, u kterých byl FEO vyloučen [17]. Co je ale důležité, takotsubo kardiomyopatie může být první manifestací FEO. Častý výskyt ischemických postižení vedoucí až k obrazu ischemické kardiomyopatie na podkladě nediagnostikovaného FEO je jedním z možných vysvětlení smrti bývalého prezidenta USA D. Eisenhowera [18].
Feochromocytomová krize s šokem
Feochromocytomová krize by měla být brána v úvahu u všech pacientů s jinak nevysvětlitelným šokem, srdečním selháním, multiorgánovým selháním nebo s nevysvětlitelnou laktátovou acidózou s horečkami. Ve velké většině se jedná o život ohrožující stavy, často vyžadující i přístrojové podpory oběhu a dýchání. V některých případech může být stav komplikován i současnou nadprodukcí dalších působků, jako je např. interleukin 6. Tento druh život ohrožujících komplikací je typický především pro pacienty s nadprodukcí adrenalinu [19]. Za poslední rok jsme se setkali se 2 pacienty, u kterých byl FEO komplikován multisystémovou krizí – v jednom případě po aplikaci pervitinu a ve druhém případě se jednalo o pacientku, u níž se FEO nejdříve manifestoval v podobě NSTEMI a následně došlo k rozvoji obrazu septického šoku. Obě pacientky jsou nyní po adrenalektomii bez obtíží.
Cerebrovaskulární komplikace
Katecholaminy působí nejen na myokard, ale také na centrální nervovou soustavu v podobě katecholaminy indukované vazokonstrikce nebo vazospazmu vedoucí jen k tranzientní ischemické atace nebo až k dokonané cévní mozkové příhodě [20]. Opakované FEO záchvaty pak mohou vést k opakovaným drobným cévním inzultům s odpovídajícími ischemickými změnami v bílé hmotě a k neurologickému postižení. Cerebrovaskulární komplikace patřily dříve také k častým příčinám úmrtí u pacientů s FEO [7], dnes jsou však popisovány mnohem méně než srdeční komplikace [21]. Hemoragické postižení je také možné – např. krvácení ze subarachnoidálního aneuryzmatu u predisponovaných jedinců.
Jaké jsou naše zkušenosti s feochromocytomem na našem pracovišti?
Relativně nedávno jsme publikovali studii, která byla zaměřená právě na výskyt kardiovaskulárních komplikací u pacientů s FEO, kteří byli vyšetřeni na našem pracovišti. V souboru 145 pacientů jsme identifikovali celkem 28 pacientů (19,3 %), u nichž se vyskytla jedna nebo i více kardiovaskulárních komplikací (tab) [22]. S ohledem na to, že se jednalo o soubor pacientů vyšetřených během delšího časového úseku, dá se považovat toto číslo jako spíše nižší s ohledem na zavedení troponinů, akutního echokardiografického vyšetření nebo dokonce i akutní koronarografie do rutinní klinické praxe teprve v nedávné době. Pacienti s kardiovaskulárními komplikacemi měli spíše menší tumory a o trochu více u nich byla přítomna nadprodukce adrenalinu ve srovnání s pacienty bez komplikací. Tento rozdíl ale nedosáhl statistické významnosti. Efekt katecholaminů je zřejmý také nejen na cévní stěnu (rozšíření komplexu intima media karotického řečiště) [23], ale také i v urychlení rychlosti pulzní vlny [24].
Table 1. Kardiovaskulární komplikace u 28 pacientů s feochromocytomem 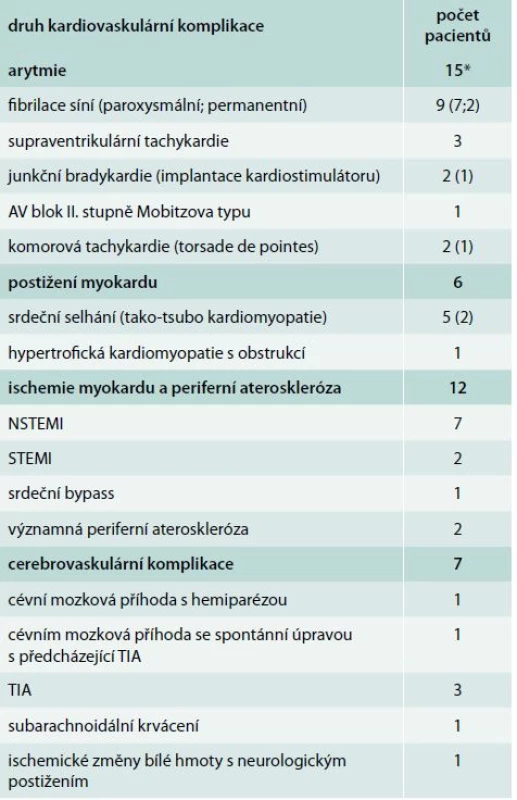
Léčba kardiovaskulárních komplikací
Základním léčebným opatřením je na diagnózu FEO vůbec pomyslet. Je velmi pravděpodobné, že časný záchyt těchto nádorů ještě v podobě náhodně zjištěného tumoru nadledviny (případně retroperitonea) je jednou ze základních prevencí těchto komplikací. Je jím také identifikace pacientů s obtížemi, které jsou kompatibilní s diagnózou FEO (např. mladší hubenější diabetici se záchvatovitými obtížemi, kteří jsou léčeni v diabetologických ambulancích pro diabetes mellitus 2. typu). Bohužel existuje ale velké množství pacientů, u kterých se FEO může projevit až v podobě život ohrožující komplikace. Kromě obecných opatření u jednotlivých kardiovaskulárních komplikací (především těch život ohrožujících) je základním opatřením terapie α-blokátory – v naší zemi nejspíše doxazosinem, a pokud je potřeba, tak i betablokátorem [25]. Akutní operace mívá většinou mnohem horší výsledky než stabilizace pacienta a následné odstranění tumoru až s odstupem po adekvátní medikamentózní přípravě [26]. Důležité je také soustředění těchto pacientů do center, která mají dostatečnou zkušenost s léčbou tohoto onemocnění – nejedná se jen o internisty (kardiology, endokrinology), ale také o chirurgy, anesteziology a případně i patology nebo odborníky v nukleární medicíně.
Závěr
Kardiovaskulární komplikace u FEO jsou velmi časté a mohou být i život ohrožující. Jejich nejlepší prevencí je vůbec na tuto diagnózu pomyslet: někdy je FEO označován jako velký imitátor (great mimic nebo masquerader) [27], bylo popsáno více než 80 různých klinických stavů spojených s tímto nádorem. Správná léčba pak může následky těchto komplikací zmírnit nebo dokonce jim i předejít.
Podpořeno výzkumnými projekty Univerzity Karlovy P25/LF1/2 a P27/LF1/1.
doc. MUDr. Tomáš Zelinka, CSc.
tzeli@lf1.cuni.cz
III. interní klinika - klinika endokrinologie a metabolizmu 1. LF UK a VFN Praha
www.vfn.cz, int3.lf1.cuni.cz
Doručeno do redakce 18. 2. 2015
Přijato po recenzi 8. 4. 2015
Sources
1. Zelinka T, Eisenhofer G, Pacák K. Pheochromocytoma as a catecholamine producing tumor: implications for clinical practice. Stress 2007; 10(2): 195–203.
2. Neumann HP, Vortmeyer A, Schmidt D et al. Evidence of MEN-2 in the original description of classic pheochromocytoma. N Engl J Med 2007; 357(13): 1311–1315.
3. Pacák K. Feochromocytom. Galén: Praha 2008. ISBN 978–80–7262–519–2.
4. Jochmanová I, Zelinka T, Widimský J jr et al. HIF signaling pathway in pheochromocytoma and other neuroendocrine tumors. Phys Res 2014; 63(Suppl 2): S251-S262.
5. Eisenhofer G, Peitzsch M. Laboratory Evaluation of Pheochromocytoma and Paraganglioma. Clin Chem 2014; 60(12): 1486–1499.
6. Kopetschke R, Slisko M, Kilisli A et al. Frequent incidental discovery of phaeochromocytoma: data from a German cohort of 201 phaeochromocytoma. Eur J Endocrinol 2009; 161(2): 355–361.
7. Graham JB. Pheochromocytoma and hypertension; an analysis of 207 cases. Int Abstr Surg 1951; 92(2): 105–121.
8. McNeil AR, Blok BH, Koelmeyer TD et al. Phaeochromocytomas discovered during coronial autopsies in Sydney, Melbourne and Auckland. Aust NZ J Med 2000; 30(6): 648–652.
9. Zelinka T, Pacák K, Widimský J Jr. Characteristics of blood pressure in pheochromocytoma. Ann NY Acad Sci 2006; 1073 : 86–93.
10. Streeten DH, Anderson GH Jr. Mechanisms of orthostatic hypotension and tachycardia in patients with pheochromocytoma. Am J Hypertens 1996; 9(8): 760–769.
11. Zelinka T, Widimský J, Weisserová J. Diminished circadian blood pressure rhythm in patients with asymptomatic normotensive pheochromocytoma. Phys Res 2001; 50(6): 631–634.
12. Zelinka T, Štrauch B, Petrák O et al. Increased blood pressure variability in pheochromocytoma compared to essential hypertension patients. J Hypertens 2005; 23(11): 2033–2039.
13. Prejbisz A, Lenders JW, Eisenhofer G et al. Cardiovascular manifestations of phaeochromocytoma. J Hypertens 2011; 29(11): 2049–2060.
14. Agarwal G, Sadacharan D, Kapoor A et al. Cardiovascular dysfunction and catecholamine cardiomyopathy in pheochromocytoma patients and their reversal following surgical cure: Results of a prospective case-control study. Surgery 2011; 150(6): 1202–1211.
15. Giavarini A, Chedid A, Bobrie G et al. Acute catecholamine cardiomyopathy in patients with phaeochromocytoma or functional paraganglioma. Heart 2013; 99(19): 1438–1444.
16. Yoshikawa T. Takotsubo cardiomyopathy, a new concept of cardiomyopathy: Clinical features and pathophysiology. Int J Cardiol 2014; 182 : 297–303. Dostupné z DOI: <http://dx.doi.org/10.1016/j.ijcard.2014.12.116>.
17. Agarwal V, Kant G, Hans N et al. Takotsubo-like cardiomyopathy in pheochromocytoma. Int J Cardiol 2011; 153(3): 241–248.
18. Messerli FH, Loughlin KR, Messerli AW et al. The president and the pheochromocytoma. Am J Cardiol 2007; 99(9): 1325–1329.
19. Whitelaw BC, Prague JK, Mustafa OG et al. Phaeochromocytoma [corrected] crisis. Clin Endocrinol (Oxf) 2014; 80(1): 13–22.
20. Majic T, Aiyagari V. Cerebrovascular manifestations of pheochromocytoma and the implications of a missed diagnosis. Neurocrit Care 2008; 9(3): 378–381.
21. Stolk RF, Bakx C, Mulder J et al. Is the excess cardiovascular morbidity in pheochromocytoma related to blood pressure or to catecholamines? J Clin Endocrinol Metab 2013; 98(3): 1100–1106.
22. Zelinka T, Petrák O, Turková H et al. High incidence of cardiovascular complications in pheochromocytoma. Horm Metab Res 2012; 44(5): 379–384.
23. Holaj R, Zelinka T, Wichterle D et al. Increased carotid intima-media thickness in patients with pheochromocytoma in comparison to essential hypertension. J Hum Hypertens 2009; 23(5): 350–358.
24. Petrák O, Štrauch B, Zelinka T et al. Factors influencing arterial stiffness in pheochromocytoma and effect of adrenalectomy. Hypertens Res 2010; 33(5): 454–459.
25. Pacák K. Preoperative management of the pheochromocytoma patient. J Clin Endocrinol Metab 2007; 92(11): 4069–4079.
26. Scholten A, Cisco RM, Vriens MR et al. Pheochromocytoma crisis is not a surgical emergency. J Clin Endocrinol Metab 2013; 98(2): 581–591.
27. Manger WM. An overview of pheochromocytoma: history, current concepts, vagaries, and diagnostic challenges. Ann N Y Acad Sci 2006; 1073 : 1–20.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2015 Issue 5-
All articles in this issue
- Vliv spironolaktonu u pacientů se srdečním selháním a zachovalou funkcí levé komory – studie TOPCAT
- Nová verze klasifikace plicní hypertenze
- Hypertenze u žen
- Vplyv pridania fytosterolu ku hypolipidemickej liečbe statínom na veľkosť lipoproteínových partikúl u pacientov s veľmi vysokým kardiovaskulárnym rizikom
- Hypertenze bílého pláště a maskovaná hypertenze
- Personalizovaná farmakoterapie digoxinem
- Kontroverze kolem betablokátorů
- Je potřeba léčit agresivně fibrilaci síní?
- Význam kyseliny močové a terapie alopurinolem v ovlivnění kardiovaskulárních onemocnění
- Ambulantní léčba žilní plicní embolie
- Současný stav a budoucnost péče o nemocné s vrozeným srdečními vadami
- Inhibice systému renin-angiotenzin-aldosteron u srdečního selhání aneb od obecného souhlasu (CONSENSUS) po vzorec myšlení (PARADIGM-HF)
- Hemokoagulace – nové pohledy na starou kaskádu
- Primární hyperaldosteronizmus: problémy diagnostických přístupů
- Neurokardiologie nebo kardioneurologie – nová specializace budoucnosti?
- Feochromocytom – proč je jeho časná diagnóza pro pacienta důležitá?
- Nakolik jsme schopni dosáhnout současně platných cílových hodnot LDL-cholesterolu v sekundární prevenci ischemické choroby srdeční
- Čo môže zapríčiniť diabetes
- Hyperosmolární hyperglykemický stav
- Kombinační léčba hypertenze 2015
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hyperosmolární hyperglykemický stav
- Hemokoagulace – nové pohledy na starou kaskádu
- Význam kyseliny močové a terapie alopurinolem v ovlivnění kardiovaskulárních onemocnění
- Hypertenze u žen
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

