-
Medical journals
- Career
Myelodysplastický syndrom – pokrok v léčbě v 21. století
Authors: A. Jonášová
Authors‘ workplace: I. interní klinika – klinika hematologie 1. lékařské fakulty UK a VFN Praha, přednosta prof. MU Dr. Marek Trněný, CSc.
Published in: Vnitř Lék 2013; 59(7): 635-640
Category:
Overview
Myelodysplastický syndrom je jedno z nejčastějších hematologických onemocnění ve věku nad 60 let. Donedávna byla terapie tohoto onemocnění velice svízelná a často končící jenom podpůrnou léčbou. V poslední době se objevily nové nadějné preparáty, které znamenají velký průlom nejen v terapii MDS, ale i v zájmu o patogenezi tohoto onemocnění. V naší práci se věnujeme vývoji v terapii MDS a zvláště pak novým preparátům a jejich přínosu.
Klíčová slova:
myelodysplastický syndrom – klasifikace – prognóza – terapieMyelodysplastický syndrom (MDS) představuje heterogenní skupinu klonálních chorob hemopoetické kmenové buňky charakterizovaných inefektivní hemopoézou, periferní cytopenií, morfologickou dysplazií a nebezpečím transformace do akutní myeloidní leukemie (AML). MDS, zvláště v raných fázích, je vlastně premaligním (preleukemickým) onemocněním.
MDS bylo jako přesněji definovaný soubor klinických podjednotek charakterizováno a pojmenováno v roce 1982 FAB (French ‑ American ‑ British) skupinou autorů. Odtud také název první FAB klasifikace jednotlivých podskupin MDS [1]. Od té doby se postupně rozšiřoval zájem o toto relativně „mladé“ onemocnění mezi hematologickou komunitou. Hromadily se nové informace a blíže se specifikovaly jednotlivé podskupiny onemocnění s přesnějším určením prognózy a návrhu správné terapie. Tak vznikaly nové klasifikace WHO 2001, WHO 2008, která je dnes užívána nejčastěji (tab. 1, obr. 1) a skórovací systémy IPSS (international prognostic scoring system) (tab. 2), WPSS (WHO prognostic scoring system) a poslední revidovaný skórovací systém R ‑ IPSS [2 – 5]. Klasifikace a skórovací systémy dělí tuto chorobu do četných podskupin s velmi rozdílným průběhem a prognózou. Nejdůležitějšími prognostickými faktory jsou: hloubka cytopenie, procento myeloblastů ve dřeni a cytogenetický nález.
Table 1. WHO klasifikace 2008 (Wardiman et al. Blood 2009; 114: 937–951). 
Image 1. Vývoj klasifikace MDS. 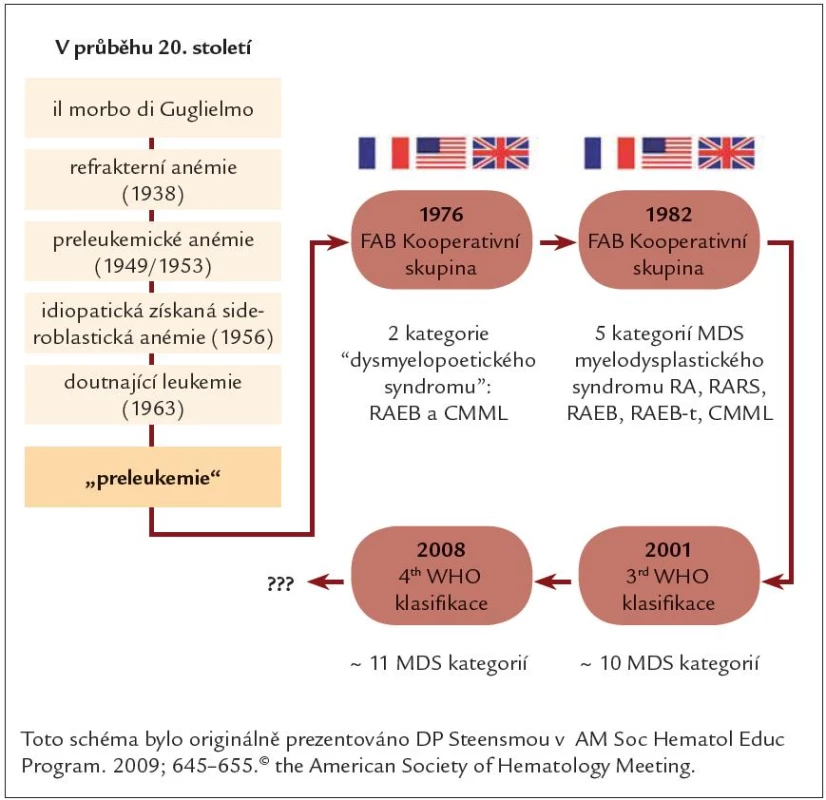
Se vzrůstajícím zájmem o MDS a lepší diagnostiku nemocných s nejasnými cytopeniemi se relativně zvyšovala také incidence onemocnění. U osob nad 60 let dosahuje 30 – 40// 100 000 (některá literární americká data uvádějí incidenci u populace nad 65 let až 75/ 100 000), což činí z MDS jednu z nejčastějších hematologických malignit v této věkové kategorii. MDS se s malou převahou vyskytuje častěji u mužů. Navzdory intenzivnímu výzkumu není etiologie onemocnění dosud objasněna. To se týká asi 80 % nemocných a onemocnění pak nazýváme primární MDS. U části nemocných je známa expozice toxickým látkám z prostředí, popřípadě onemocnění vzniká po předchozí chemoterapii či radioterapii pro jinou primární malignitu. Často se např. vyskytuje u nemocných, kteří podstoupili autologní transplantaci kmenových buněk. Tuto skupinu nazýváme sekundárním MDS. Charakteristickým znakem MDS jsou různé cytopenie, event. jejich kombinace a z nich plynoucí klinické komplikace. Většina, přes 90 % nemocných, má anémii, část nemocných má trombocytopenii a projevy krvácení, část neutropenii s možným rozvojem nejčastěji mykotických a bakteriálních infekcí. Hlavním znakem je dysplastická, většinou bohatá dřeň, která je právě v kontrastu s periferní cytopenií. Častý je výskyt početních chromozomálních aberací [5]. Příčinou úmrtí je asi u 30 – 40 % transformace do AML, u 40 % komplikace cytopenie a zbytek nemocných umírá na komorbidity, většinou též akcelerované přítomnou cytopenií.
I přes stálý intenzivní výzkum je MDS jednou z nejobtížněji řešitelných hematologických malignit. MDS je velice heterogenní choroba, u některých typů nemocní žijí dlouho a jejich prognóza je dobrá, v jiných případech se ale onemocnění může stát velmi zákeřným s rychlou progresí s pouze několikaměsíčním přežíváním. Proto i terapeutické přístupy musejí být orientované na jednotlivé podskupiny MDS. S ohledem na terapii nemocné dělíme na nižší a vyšší rizikové skupiny, pomáhá nám při tom skórovací systém IPSS (viz výše). Základní terapeutické možnosti jsou shrnuty v obr. 2. Hlavním cílem terapie nízce rizikových nemocných, t.j. nemocných s předpokládaným delším přežitím, lepší prognózou a menším rizikem transformace do AML, je zlepšení kvality život a prodloužení přežívání. Nemusíme usilovat, zvláště u starších nemocných, o eradikaci onemocnění. Zásadním problémem nízce rizikových nemocných je různě pokročilá cytopenie jedné či více hemopoetických řad a z ní plynoucí komplikace. Tímto směrem je též orientována léčba nízce rizikových nemocných.
Image 2. Základní terapeutické možnosti MDS – vývoj. 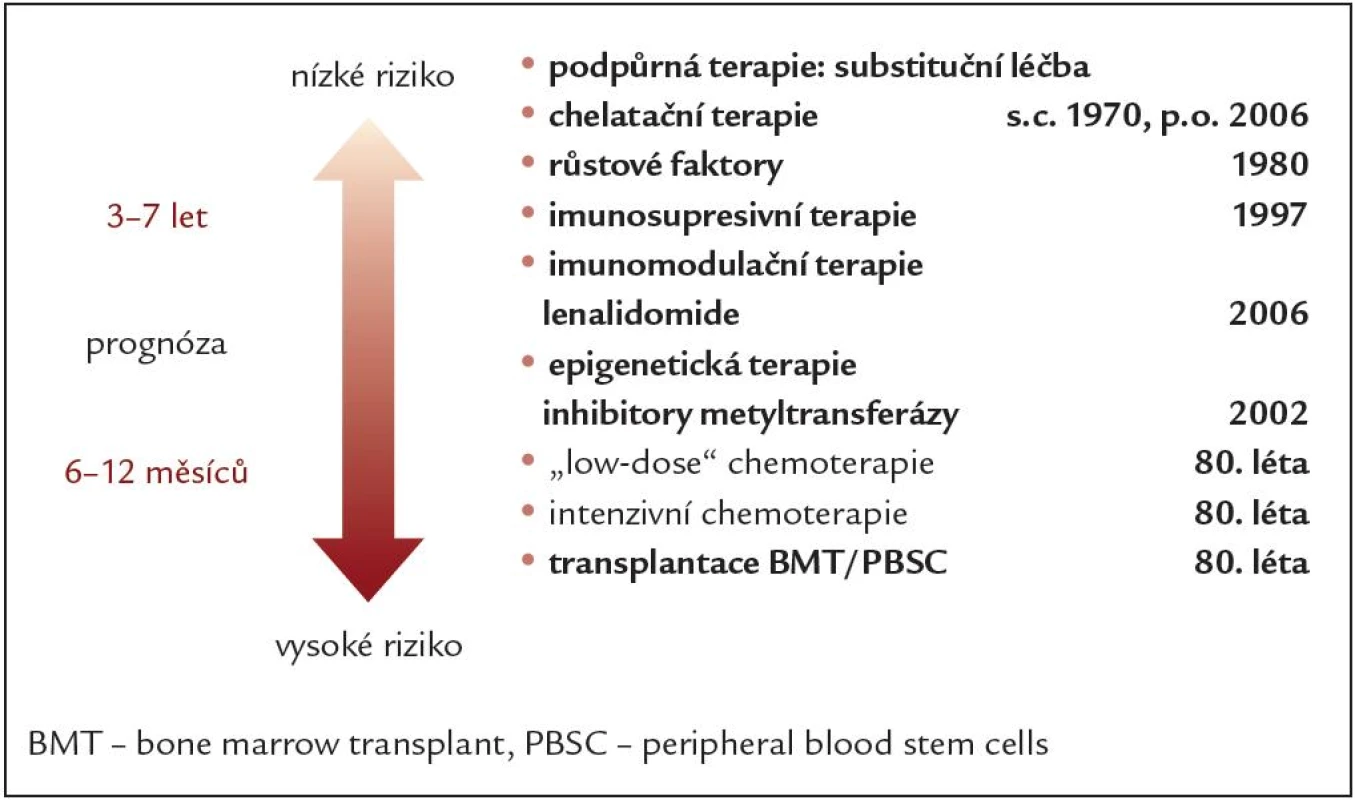
Vysoce rizikoví nemocní jsou ti, u kterých se objevila leukemická populace blastů. Terapie je proto vedle léčby cytopenií orientována na eradikaci patologického klonu buněk a prevenci transformace do AML. Našim hlavním cílem zvláště u mladších nemocných s MDS je dosažení kompletní remise.
Až do začátku 21. století byla terapie MDS na rozdíl od jiných hematologických chorob dosti frustrující, bez jediné terapie dosahující alespoň 50% odpovědi. U nízce rizikových nemocných vévodila podpůrná léčba. Ta samozřejmě stále hraje důležitou roli u cytopenických nemocných a sama o sobě znamenala oproti 80. letům minulého století, kdy bylo onemocnění definováno, velký pokrok. Dnes máme k dispozici velmi kvalitně připravované krevní preparáty a s vývojem nových účinných antibiotik a zvláště pak antimykotik můžeme lépe předcházet a léčit infekční komplikace. Asi 90 % nemocných má anémii a kolem 80 % dostává v průběhu svého onemocnění transfuze. Anémie je základním rysem onemocnění a bohužel většina nemocných se v průběhu svého onemocnění stane závislými na krevních převodech. Tito nemocní jsou ohroženi sekundární siderózou. Nadbytečné intracelulární Fe vede k tvorbě vysoce reaktivních hydroxylových radikálů, které mohou způsobit oxidativní poškození lipidů, proteinů, molekul DNA a vést až ke smrti buňky. Fe se hromadí v orgánech (srdce, játra, endokrinní orgány) s jejich následným poškozením vedoucím v některých případech až k selhání jejich funkcí. Přetížení Fe vede u MDS nemocných nejen ke snížení celkového přežití, ale i ke zhoršení výsledků u alogenních transplantací se zvýšenou peritransplantační mortalitou [6 – 8]. Přetížení železem brání chelatační terapie. Správnými kandidáty chelatační terapie jsou proto nemocní s nízkým rizikem, s ferritinem > 1 000 – 2 000 ng/ ml a event. kandidáti transplantace. Dlouhá léta byl k dispozici parenterální chelátor deferoxamin (Desferal), podával se v kontinuální subkutánní infuzi, vyžadující velkou trpělivost a spolupráci nemocného. V posledních letech se objevily nové a stejně účinné perorální chelátory. V ČR jsou k dispozici deferipron (Ferriprox) a deferasirox (Exjade). Nejčastěji je v současné době používán Exjade. Od 80. let minulého století patří k terapii nízce rizikových nemocných léčba růstovými faktory. Běžně používané jsou u nemocných se symptomatickou anémií erytropoézu stimulující látky. Sem patří především rekombinantní humánní erytropoetiny (Neorecornom, Eprex), pegylovaný erytropoetin s dlouhodobým efektem darbepoetin (Aranesp). Začátky používání erytropoetinů doprovázel relativně velký entuziasmus, nakonec ale velké studie ukázaly, že efekt je zřejmý jen zhruba kolem 20 % nemocných. V průběhu let se proto přesněji definoval okruh nemocných, kteří jsou ideálními kandidáty této terapie (s menší anémií, menší transfuzní dependencí a relativně nižší hladinou endogenního erytropoetinu), a navíc se ke zvýšení efektu začala používat kombinace erytropoetinů s růstovým faktorem bílé řady, a to G‑CSF (granulocyty stimulující faktor – Neupogen) pro jejich synergický antiapoptotický efekt [9 – 11]. Nyní zcela nově máme k dispozici levnější a pravděpodobně stejně dobře účinné „biosimilars“ (v případě červené řady je to u nás již používaný Binocrit). Posledními v řadě růstových faktorů, v současné době ve fázi ještě klinických studií, jsou dlouho očekávané trombopoézu stimulující látky. Do této skupiny léků patří u již autoimunní idiopatické trombocytopenie úspěšně používaný romiplostim (Nplate) a nový perorální preparát eltrombopag. Oba jsou trombopoetin‑mimetiky, stimulujícími trombopoetinový receptor. Mezi terapeutické možnosti nízce rizikových nemocných patří již od 90. let minulého století imunosupresivní léčba. V používání této terapie jsme přispěli i my jednou z prvních publikací popisujících úspěšnou léčbu MDS cyklosporinem v roce 1998 [12]. Používán je též antitymocytární globulin – ATG, stejně jako je tomu u aplastické anémie (AA) samostatně nebo v kombinaci s cyklosporinem [13]. Většinou je dosahováno odpovědi asi u 15 – 20 % pacientů [13,14]. Tato terapie je založena na teorii, že u určité skupiny nemocných s MDS autoimunní mechanizmus iniciovaný autoagresivními T buňkami, obdobně jako je tomu u aplastické anémie, může způsobit selhání hematopoézy či její poruchu [15,16]. Vhodnými kandidáty této terapie a podmínkami pro lepší odpověď jsou: nízce rizikoví nemocní zvláště s hypoplastickým MDS, mladší 60 let, krátce po stanovení diagnózy, nemocní s přidruženými autoimunitními onemocněními, HLA DR 15a PNH pozitivitou [17].
Nemocní s vyšším rizikem donedávna byli léčeni různými kombinacemi cytostatik více či méně obdobnými jako u terapie akutní myeloidní leukemie, či dle možností transplantací kostní dřeně. Bohužel MDS na rozdíl od jiných hematologických malignit je překvapivě rezistentní vůči standardní chemoterapii. Klasická chemoterapie byla v současné době vytěsněna v použití v širším měřítku demetylačními látkami. Chemoterapii u vysoce rizikových pacientů s MDS používáme dnes především v souvislosti s indikací k alogenní transplantaci, a to zvláště k redukci počtu blastů před transplantací. V tomto případě jde většinou o standardní chemoterapii jako u akutních myeloidních leukemií (založenou na použití cytosinarabinosidu). Samotná chemoterapie v průběhu let nezaznamenala u MDS žádný pokrok, nejsou nové lepší a účinnější preparáty.
U nemocných nad 65 let nebo nad 60 let s komorbiditami, ale ještě poměrně dobrým klinickým stavem, můžeme též zvolit klasickou terapii nízkými dávkami cytosinarabinosidu, a to v případě, nemáme‑li k dispozici demetylační látky. U starších pacientů a pacientů s významnými komorbiditami volíme buď monoterapii malými dávkami perorálních cytostatik, zvláště u nemocných s CMML, MDS/ MPS (hydroxycarbamid, mercaptopurin, melfalan), či pouze kvalitní podpůrnou léčbu.
Zatím jedinou kauzální terapií zůstává stále problematická alogenní transplantace kostní dřeně či dnes především periferních kmenových buněk (hemopoetic stem cell transplantation – HSCT), kterou vzhledem k věku toleruje jen malé procento nemocných. Transplantace je indikována pro nemocné mladší 60 let (individuálně 65 let) v dobrém celkovém stavu. Pokrokem, především s ohledem na starší populaci MDS nemocných, bylo zavedení transplantace s redukovaným přípravným režimem, který je méně toxický [18 – 20]. Problémem však je, že za cenu menších komplikací s ohledem k nižší dávce a toxicitě chemoterapie je sice snížena samotná transplantační mortalita, ale ještě stále zůstává dosti vysoké procento relapsů [21].
Čtyřletý odhad celkového přežívání po transplantaci u dospělé populace je zhruba 30 – 40 %.
Tato statistická data podtrhovala nezbytnost porozumění biologii MDS a v jeho důsledku rozšíření repertoáru „individualizované“ cílené biologické léčby.
Naštěstí se v posledních letech objevily pro obě skupiny, jak nemocné s nízkým, tak vysokým rizikem, nové terapeutické možnosti. Obě tyto nové skupiny léků znamenaly pro MDS doslova revoluci, a to nejen stran možností pro nemocné, ale i zájmem o tuto chorobu. Hrály proto i roli v intenzivnějším výzkumu patogeneze onemocnění. Jedná se o imunomodulační terapii a inhibitory metyltransferázy.
Imunomodulační terapie je zatím především terapií pro nemocné s nízkým rizikem, ale stále častěji se objevuje v kombinacích pro nemocné s vyšším rizikem.
Již léta prokazují mnohé studie, že dysregulace různých apoptotických, zánětlivých a angiogenních cytokinů může hrát důležitou roli v etiopatogenezi MDS. Imunomodulační terapie ovlivňuje hladiny těchto cytokinů, čímž působí na průběh, ne‑li na samotnou patogenezi onemocnění. Prvním preparátem použitým u MDS pacientů byl thalidomid, neblaze proslulý svým teratogenním efektem [22]. Důvodem jeho použití bylo zjištění, že tento lék má antiangiogennní vlastnosti, které pravděpodobně byly zodpovědné za jeho teratogenní efekt. U MDS je popisována větší vaskularizace dřeně. Výrazně lepší efekt má nový analog thalidomidu lenalidomid (Revlimide). Lenalidomid má efekt antiangiogenní, antiapoptotický, inhibuje TNF a, stimuluje T a NK buňky, produkci IL2, navíc pravděpodobně zvyšuje senzitivitu erytroidních progenitorů k erytropoetinu a možný je též přímý cytotoxický efekt na buňky patologického klonu. Výjimečný je jeho účinek zvláště u nemocných s delecí dlouhých ramének 5. chromozomu, zvláště 5q – syndromu. Delece dlouhého raménka 5. chromozomu je nejčastější cytogenetická abnormalita u MDS vyskytující se asi u 10 – 15 % nemocných. Na terapii lenalidomidem překvapivě dobře reagují i jiní MDS nemocní s touto chromozomální abnormalitou, a to jak izolovanou, tak v kombinaci s dalšími aberacemi. Právě pacienti s 5q – jsou často rezistentní na terapii ESP a většinou u nich nevyhnutelně dochází k rozvoji transfuzní dependence se všemi neblahými následky.
Lenalidomid vede u 60 – 70 % nemocných s 5q – aberací k erytrocytární odpovědi a transfuzní independenci s následnou dlouhodobou normalizací krevního obrazu [23,24]. Terapie vede též u asi 40 – 50 % nemocných ke kompletní cytogenetické odpovědi [24]. U nemocných s 5q – syndromem (starší ženy, 5q – izolovaná aberace, nízké procento blastů ve dřeni, normální či vyšší počet destiček) je dosahováno odpovědi až u 80 – 90 % nemocných (naše zkušenosti). Opatrnosti je třeba u nemocných s dalšími cytogenetickými aberacemi, zvýšeným počtem blastů a mutací p53, to jsou nemocní se zvýšeným rizikem časnější progrese choroby, a proto je u nich třeba zvážit agresivnější terapii [25]. U MDS nemocných bez 5q – aberace je nezávislosti na transfuzích dosahováno u zhruba 25 % [26]. Lenalidomid je relativně velmi dobře snášen, nejčastějšími vedlejšími účinky jsou neutropenie a trombocytopenie. Lenalidomid nezvyšuje u MDS v malých dávkách významně riziko trombóz, a tak zatím preventivní antitrombotická terapie není doporučována. Jde o perorální preparát, který se podává v jedné denní dávce.
Epigenetická terapie – demetylace. Epigenetická modulace zasahuje přímo do funkce genů, ovlivňuje genovou transkripci, a tím i expresi genů. DNA metylace je zprostředkována enzymem metyltransferázou. Pakliže dochází k hypermetylaci cytozinových reziduí v oblasti genového promotoru, dochází k poruše regulace transkripce genů a tím změně jejich exprese „gene silencing“. Inhibována může být exprese tumor supresorických genů a genů nezbytných pro normální regulaci proliferace, diferenciace a buněčné apoptózy [27 – 30]. Hypermetylaci DNA zabraňují 2 inhibitory metyltransferázy – 5 - azacitidin a 5 - aza ‑ 2’ - deoxycitidin (decitabin). U nás je povolen azacitidin (Vidaza). Zavedení tohoto preparátu do terapie MDS znamená relativně velký posun nejen v samotné terapii, ale i v poodhalování záhad samotné patogeneze MDS, kde se zdá, že epigenetická modulace hraje důležitou roli. Dnes se však s výzkumem funkce demetylačních preparátů objevují i jiné nové efekty těchto účinných léků, které pravděpodobně ovlivňují apoptózu, diferenciaci, diskutuje se i imunomodulační efekt. Cytostatický efekt azacitidinu byl popsán již v 60. letech minulého století, a to prvním naším vědcem Františkem Šormem (tehdy prezidentem Akademie věd a ředitelem Ústavu organické chemie a biochemie), který azacitidin syntetizoval.
Dnes již četné studie ukazují významný terapeutický efekt tohoto preparátu u všech skupin MDS nemocných [31 – 33]. Stěžejním výsledkem studií je dosažení významně delšího OS oproti dosud používané klasické terapii (podpůrná léčba, nízké dávky cytozin arabinosidu, intenzivní chemoterapie: 3 + 7 režim) u nemocných s MDS s vyšším rizikem [31,32]. Vedle toho se zdá, že azacitidin by mohl být používán v udržování kompletních remisí po standardní chemoterapii či alogenní transplantaci a v přípravách na transplantaci [34,35]. Specifický pro inhibitory metyltransferázy je jejich postupný a pozvolný nástup účinku, proto je účinek často patrný až po 4 – 6 cyklech terapie. Procento odpovědí stoupá s prodloužením terapie a efekt můžeme vidět i až po 8 a více cyklech [36].
Azacitidin je v současné době standardní terapií nemocných s vyšším rizikem dle IPSS a znamená pro tyto nemocné krok dopředu. Zvláště pro nemocné nad 65 let, kdy již transplantace může být diskutabilní a kdy velmi často pro současné komorbidity není možno podat standardní chemoterapii, která navíc měla u nemocných s vysokým rizikem (dle IPSS) stejně malé procento odpovědí. Velkou výhodou této terapie je možnost ambulantního podávání, únosné procento nežádoucích účinků, méně infekčních komplikací vyžadujících hospitalizaci a zvláště vysoké procento hematologických odpovědí, které jsou hlavním důvodem zkvalitnění života nemocných. Na cestě je též perorální forma tohoto preparátu. Nicméně i s touto terapií se stále pohybujeme kolem 50 % odpovědí a prodloužení života z 6 – 12 měsíců na 20 – 24 měsíců.
Je tedy stále ještě velký prostor pro nové léky. V klinických studiích fáze 1 či 2 je v současné době mnoho dalších preparátů, zatím není jasné, zda některý z nových preparátů povede k tak významnému zvýšení odpovědí či prodloužení přežívání jako 2 výše uvedené skupiny léků, nicméně jejich použití bude jistě v kombinacích právě s azacitidinem nebo lenalidomidem pro nemocné s nedostatečnou odpovědí. Do této skupiny patří např. nukleozidové analogy: sepacitabin, clofarabin, inhibitory kináz: Arry ‑ 614, ON1910 – rigosertib, Scio ‑ 649, Erlotinib, inhibitor TGF‑b (transforming growth facotr) sotatercept, protilátka neutralizující IL‑6 (interleukin 6) siltuximab, glutationový analog ezatiostat, aminopeptidázový inhibitor tosedostat a mnoho dalších.
Doufejme, že se v blízké budoucnosti dočkáme opět nové vlny dalšího zkvalitnění terapie pro nemocné s myelodysplastickým syndromem.
MU Dr. Anna Jonášová
www.vfn.cz
e‑mail: atjonas@hotmail.com; anna.jonasova@vfn.cz
Doručeno do redakce: 30. 4. 2013
Sources
1. Bennett JM, Catovsky D, Daniel MT et al. Proposals for the classification of the myelodysplastic syndromes. Br J Haematol 1982; 51 : 189 – 199.
2. Harris NL, Jaffe ES, Diebold J et al. World Health Organization classification of neoplastic diseases of the hematopoietic and lymphoid tissues: report of the Clinical Advisory Committee meeting ‑ Airlie House, Virginia, November 1997. J Clin Oncol 1999; 17 : 3835 – 3849.
3. Greenberg P, Cox C, LeBeau MM et al. International scoring system for evaluating prognosis in myelodysplastic syndromes. Blood 1997; 89 : 2079 – 2088. Erratum Blood 1998; 91 : 1100.
4. Greenberg PL, Tuechler H, Schanz J et al. Revised international prognostic scoring system for myelodysplastic syndromes. Blood 2012; 120 : 2454 – 2465.
5. Schanz J, Tüchler H, Solé F et al. New comprehensive cytogenetic scoring system for primary myelodysplastic syndromes (MDS) and oligoblastic acute myeloid leukemia after MDS derived from an international database merge. J Clin Oncol 2012; 30 : 820 – 829.
6. Armand P, Kim HT, Aleya EP et al. Prognostic impact of elevated pretransplantation serum ferritin in patients undergoing myeloablative stem cell transplantation. Blood 2007; 109 : 4586 – 4588.
7. Leitch HA, Wong D, Leger C et al. Improved leukemia‑free and overall survival in patients with myelodysplastic syndrome receiving iron chelation therapy: a subgroup analysis. Blood 2007; 110: abstract 1469.
8. Rose C, Brechignac S, Fenaux P et al. Positive impact of iron chelation therapy (CT) on survival in regularly transfused MDS patients. A prospective analysis by the GFM. Blood 2007; 110: Abstract 249.
9. Park S, Grabar S, Kelaidi C et al. GFM group (Groupe Francophone des Myélodysplasies). Predictive factors of response and survival in myelodysplastic syndrome treated with erythropoietin and G‑CSF: the GFM experience. Blood 2008; 111 : 574 – 582.
10. Hellström ‑ Lindberg E, Gulbrandsen N, Lindberg G et al. Scandinavian MDS Group. A validated decision model for treating the anaemia of myelodysplastic syndromes with erythropoietin + granulocyte colony ‑ stimulating factor: significant effects on quality of life. Br J Haematol 2003; 120 : 1037 – 1046.
11. Thompson JA, Gilliland DG, Prchal JT et al. Effect of recombinant human erythropoietin combined with granulocyte/ macrophage colony ‑ stimulating factor in the treatment of patients with myelodysplastic syndrome. GM/ EPO MDS Study Group. Blood 2000; 95 : 1175 – 1179.
12. Jonasova A, Neuwirtova R, Cermak J et al. Cyclosporin A therapy in hypoplastic MDS patients and certain refractory anaemias without hypoplastic bone marrow. Br J Haematol 1998; 100 : 304 – 309.
13. Killick SB, Mufti G, Cavenagh JD et al. A pilot study of antithymocyte globulin (ATG) in the treatment of patients with ‘low ‑ risk’ myelodysplasia. Br J Haematol 2003; 120 : 679 – 684.
14. Shimamoto T, Tohyama K, Okamoto T et al. Cyclosporin A therapy for patients with myelodysplastic syndrome: multicenter pilot studies in Japan. Leuk Res 2003; 27 : 783 – 788.
15. Molldrem JJ, Jiang YZ, Barrett AJ et al. Haematological response of patients with myelodysplastic syndrome to antithymocyte globulin is associated with a loss of lymphocyte ‑ mediated inhibition of CFU ‑ GM and alterations in T ‑ cell receptor Vbeta profiles. Br J Haematol 1998; 102 : 1314 – 1322.
16. Sloand EM, Mainwaring L, Barrett AJ et al. Preferential suppression of trisomy 8 compared with normal hematopoietic cell growth by autologous lymphocytes in patients with trisomy 8 myelodysplastic syndrome. Blood 2005; 106 : 841 – 851.
17. Barrett J, Sloand E, Young N. Determining which patients with myelodysplastic syndrome will respond to immunosuppressive treatment. Haematologica 2006; 91 : 583 – 584.
18. Lee SE, Kim YJ, Yahng SA et al. Survival benefits from reduced ‑ intensity conditioning in allogeneic stem cell transplantation for young lower ‑ risk MDS patients without significant comorbidities. Eur J Haematol 2011; 87 : 510 – 520.
19. Luger SM, Ringdén O, Zhang MJ et al. Similar outcomes using myeloablative vs reduced ‑ intensity allogeneic transplant preparative regimens for AML or MDS. Bone Marrow Transplant 2012; 47 : 203 – 211.
20. Lee SE, Lim J, Yahng SA et al. Reduced ‑ intensity conditioning regimen combined with low‑dose total body irradiation in the treatment of myelodysplastic syndrome. Acta Haematol 2011; 126 : 21 – 29.
21. Jabbour E, Mathisen MS, Garcia ‑ Manero Get al. Allogeneic hematopoietic stem cell transplantation versus hypomethylating agents in patients with myelodysplastic syndrome: a retrospective case ‑ control study. Am J Hematol 2013; 88 : 198 – 200.
22. Raza A, Meyer P, Dutt D et al. Thalidomide produces transfusion independence in long‑standing refractory anemias of patients with myelodysplastic syndromes. Blood 2001; 98 : 958 – 965.
23. List A, Dewald G, Raza A et al. Myelodysplastic Syndrome ‑ 003 Study Investigators. Lenalidomide in the myelodysplastic syndrome with chromosome 5q deletion. N Engl J Med 2006; 355 : 1456 – 1465.
24. Fenaux P, Giagounidis A, Selleslag D et al. MDS ‑ 004 Lenalidomide del5q Study Group. A randomized phase 3 study of lenalidomide versus placebo in RBC transfusion ‑ dependent patients with Low ‑ / Intermediate ‑ 1 - risk myelodysplastic syndromes with del5q. Blood 2011; 118 : 3765 – 3776.
25. Jädersten M, Saft L, Mufti GJ et al. TP53 mutations in low ‑ risk myelodysplastic syndromes with del(5q) predict disease progression. J Clin Oncol 2011; 29 : 1971 – 1979.
26. Raza A, Reeves JA, List AF et al. Phase 2 study of lenalidomide in transfusion ‑ dependent, low ‑ risk, and intermediate ‑ 1 risk myelodysplastic syndromes with karyotypes other than deletion 5q. Blood 2008; 111 : 86 – 93.
27. Hofmann WK, Takeuchi S, Takeuchi N et al. Comparative analysis of hypermethylation of cell cycle control and DNA ‑ mismatch repair genes in low ‑ density and CD34+ bone marrow cells from patients with myelodysplastic syndrome. Leuk Res 2006; 30 : 1347 – 1353.
28. Christiansen DH, Andersen MK, Pedersen ‑ Bjergaard J. Methylation of p15INK4B is common, is associated with deletion of genes on chromosome arm 7q and predicts a poor prognosis in therapy‑related myelodysplasia and acute myeloid leukemia. Leukemia 2003; 17 : 1813 – 1819.
29. Curik N, Burda P, Vargova K et al. 5 - azacitidine in aggressive myelodysplastic syndromes regulates chromatin structure at PU.1 gene and cell differentiation capacity. Leukemia 2012; 26 : 1804 – 1811.
30. Shin DY, Park YS, Yang K et al. Decitabine, a DNA methyltransferase inhibitor, induces apoptosis in human leukemia cells through intracellular reactive oxygen species generation. Int J Oncol 2012; 41 : 910 – 918.
31. Silverman LR, Demakos EP, Peterson BL et al.Randomized controlled trial of azacitidine in patients with the myelodysplastic syndrome: a study of the cancer and leukemia group B. J Clin Oncol 2002; 20 : 2429 – 2440.
32. Fenaux P, Mufti GJ, Hellstrom ‑ Lindberg E et al. International Vidaza High‑Risk MDS Survival Study Group. Efficacy of azacitidine compared with that of conventional care regimens in the treatment of higher ‑ risk myelodysplastic syndromes: a randomised, open ‑ label, phase III study. Lancet Oncol 2009; 10 : 223 – 232.
33. Itzykson R, Thépot S, Quesnel B et al. Groupe Francophone des Myelodysplasies (GFM). Prognostic factors for response and overall survival in 282 patients with higher ‑ risk myelodysplastic syndromes treated with azacitidine. Blood 2011; 117 : 403 – 411.
34. Grövdal M, Khan R, Aggerholm A et al. Maintenance treatment with azacitidine for patients with high‑risk myelodysplastic syndromes (MDS) or acute myeloid leukaemia following MDS in complete remission after intensive chemotherapy. Br J Haematol 2010; 150 : 293 – 302.
35. Damaj G, Duhamel A, Robin M et al. Impact of azacitidine before allogeneic stem ‑ cell transplantation for myelodysplastic syndromes: a study by the Societe Francaise de Greffe de Moelle et de Therapie ‑ Cellulaire and the Groupe ‑ Francophone des Myelodysplasies. J Clin Oncol 2012; 30 : 4533 – 4540.
36. Silverman LR, Fenaux P, Mufti GJ et al. Continued azacitidine therapy beyond time of first response improves quality of response in patients with higher ‑ risk myelodysplastic syndromes. Cancer 2011; 117 : 2697 – 2702.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 7-
All articles in this issue
- Onemocnění jater u diabetiků
- Účinky GLP-1 (glucagon‑like peptide 1) na játra
- Polypózy trávicího traktu
- Vrozené hyperbilirubinemie a molekulární mechanizmy žloutenky
- Cystické nádory pankreatu – naše zkušenosti
- Wilsonova choroba
- Vliv jaterní cirhózy na farmakokinetiku a farmakodynamiku léčiv
- Katetrizace jaterních žil – vybrané aspekty hodnocení
- Reaktivace chronické hepatitidy B
- Akutní pankreatitida – novinky v léčbě
- Postižení jater u nemocných s ne-Hodgkinovým lymfomem
- Léčba chronické infekce virem hepatitidy C na začátku nové éry
- Vztah bilirubinu k nemocem vyvolaným zvýšeným oxidačním stresem
- Inhibitory tyrozinových kináz – zásadní změna v prognóze chronické myeloidní leukemie
- Mnohočetný myelom
- Pokroky v léčbě chronické lymfocytární leukemie
- Myelodysplastický syndrom – pokrok v léčbě v 21. století
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Vztah bilirubinu k nemocem vyvolaným zvýšeným oxidačním stresem
- Cystické nádory pankreatu – naše zkušenosti
- Onemocnění jater u diabetiků
- Akutní pankreatitida – novinky v léčbě
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


![IPSS [3].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/017630f38bc90dd00436243e4178051a.png)