-
Medical journals
- Career
Diabetes mellitus a jaterní cirhóza
: T. Fejfar 1; V. Šafka 2; V. Jirkovský 1; J. Štefánková 3; P. Hůlek 1
: II. interní klinika Lékařské fakulty UK a FN Hradec Králové, přednosta prof. MUDr. Jaroslav Malý, CSc. 1; Ústav fyziologie Lékařské fakulty Hradec Králové, přednostka prof. MUDr. Zuzana Červinková, CSc. 2; Diabetologická ambulance Hradec Králové 3
: Vnitř Lék 2011; 57(4): 368-371
: 12th national Symposium diabetes, "Diabetes and Gastroenterology", Hradec Kralove, 4 to 5 June 2010
Riziko rozvoje diabetes mellitus u nemocných s jaterní cirhózou výrazně stoupá, zejména u nemocných s jaterním onemocněním na podkladě hereditární hemochromatózy, autoimunitní hepatitidy, nealkoholové steatohepatitidy a chronické infekce virem hepatitidy C. Prognóza nemocných je určována zejména pokročilostí jaterního onemocnění a přidruženými komplikacemi z něho plynoucími. Pokročilé jaterní onemocnění modifikuje terapii jak diabetu, tak i diabetes ovlivňuje léčbu vlastního jaterního onemocnění, zejména asociované portální hypertenze. Autoři přinášejí krátký přehled jednotlivých chorob s vyšším výskytem diabetu a specifika léčby.
Klíčová slova:
jaterní cirhóza – diabetes mellitusÚvod
Jaterní cirhóza je konečným stadiem mnoha jaterních onemocnění. Přesná hranice mezi méně závažnou jaterní fibrózou a jaterní cirhózou, která je kromě přítomnosti vazivových sept a nekrózou hepatocytů charakterizována i přítomností uzlovité regenerace, prakticky neexistuje. Zlatým standardem pro diagnózu stále zůstává jaterní biopsie, i když v případě jasného klinického nálezu je pro diagnózu postačující charakteristický nález na zobrazovacích vyšetřeních (UZ, CT) a typický laboratorní obraz s alterací jaterního souboru, koagulopatií a hypoalbuminemií. Vzhledem k poruše portální cirkulace je toto onemocnění spojeno též se syndromem portální hypertenze. Klinická manifestace jaterního onemocnění poté závisí jak na tíži dysfunkce jaterního parenchymu, tak na tíži asociované portální hypertenze a může se pohybovat od zcela bezpříznakového stadia až po stavy ohrožující život nemocného. Pro popis tíže jaterní insuficience je nejčastěji používána Childova-Pughova klasifikace rozdělující nemocné do 3 kategorií (tab. 1).
1. Childova Pughova klasifi kace (pole Doporučeného postupu České hepatologické společnosti pro ambulantní péči o nemocné s jaterní cirhózou). 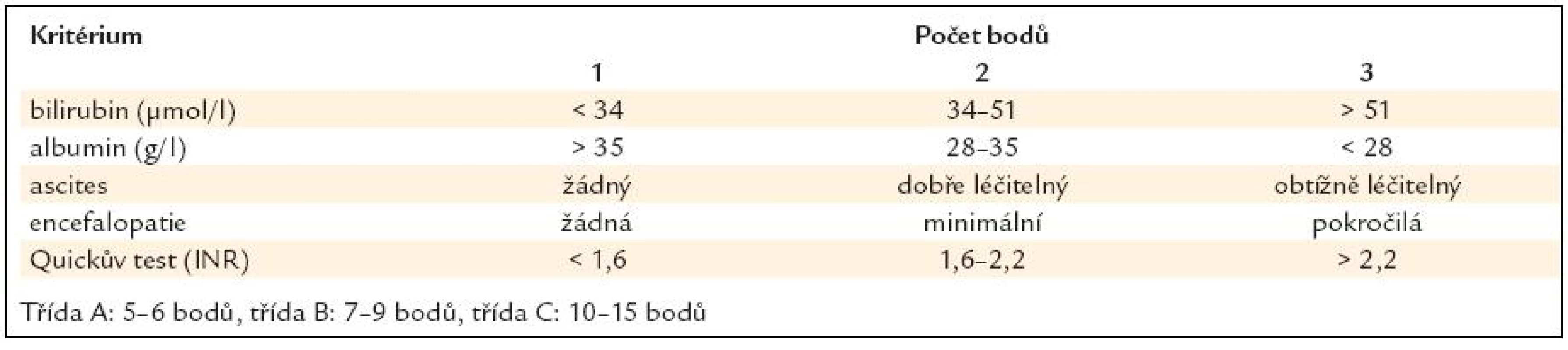
Závažnost portální hypertenze můžeme posoudit buď přímo invazivním měřením portosystémového gradientu (normální hodnoty tlaku v portální žíle jsou do 5 mm Hg), či nepřímo endoskopickým vyšetřením, popřípadě pomocí zobrazovacích metod (UZ, CT, MRI).
Dysfunkce jater, jako jednoho z hlavních orgánů glycidového metabolizmu, je spojena i s výskytem poruchy metabolizmu glukózy, která je popisována již od začátku minulého století. Poruchu glukózové tolerance nalézáme až u 80 % nemocných, manifestní diabetes mellitus u 15–20 % nemocných. Příčiny tohoto stavu, označovaného někdy jako „hepatogenní diabetes“, nejsou zcela jasné a kromě nutričního stavu, vlivu prostředí nebo hormonálních interakcí se uplatňuje také tíže dysfunkce hepatocytů. Základní charakteristikou je v úvodu přítomná periferní inzulinová rezistence a chronická hyperinzulinemie. Rozvoj manifestního diabetu je pak spojen s progredující dysfunkcí β buněk pankreatu, která je u nemocných s jaterní cirhózou významně modifikována etiologií jaterního onemocnění. U nemocných s jaterní cirhózou a diabetem se většinou nevyskytují klasické rizikové faktory jako věk, BMI a rodinná zátěž. I výskyt pro diabetes typických komplikací ve smyslu mikro - a makroangiopatií je významně nižší v porovnání s nemocnými bez jaterní cirhózy a prognóza nemocného je určována spíše tíží jaterní insuficience a asociované portální hypertenze. Na druhou stranu je však asociace diabetu pro nemocné s jaterní cirhózou významným rizikovým faktorem a je spojena s vyšší úmrtností [1]. Asociovaný diabetes mellitus je i rizikovým faktorem rozvoje další závažné komplikace jaterní cirhózy, kterou je hepatocelulární karcinom [2,3].
Jaterní onemocnění modifikuje i strategii léčby diabetu a v některých případech naopak znesnadňuje léčbu komplikací portální hypertenze.
V praxi diabetologa je vhodné myslet při vyšetření nemocného s diabetem nebo poruchou glukózové tolerance i na možnou asociaci s jaterním onemocněním. Mezi onemocnění, která mohou vést ke vzniku jaterní cirhózy a mají výrazně vyšší riziko rozvoje diabetu, patří zejména nealkoholová steatohepatitida, hereditární hemochromatóza, autoimunitní hepatitida a chronická infekce virem hepatitidy C. Proto by bylo vhodné na tyto choroby v diagnostickém algoritmu myslet i v ordinaci diabetologa.
Hereditární hemochromatóza
Hereditární hemochromatóza je autozomálně recesivně dědičné onemocnění s nízkou fenotypovou penetrancí. Genetický defekt je v úrovni genu pro HFE protein inhibující vstřebávání železa enterocytem (inhibice transferinu). 80 % nemocných s klinicky diagnostikovanou genetickou hemochromatózou má v HFE genu mutaci C2812Y (výměna aminokyseliny cysteinu za tyroxin). V naší populaci je výskyt této mutace poměrně vysoký a je udáván v rozmezí 9–10 %. Výskyt homozygotní formy má prevalenci 1 : 300–800, takže se jedná vůbec o jednu z nejčastěji přenášených genetických chorob. Klinická manifestace je však méně výrazná a podílí se na ní řada dalších faktorů (pohlaví, vrozené vlohy k fibrogenezi). Naopak, 5–15 % homozygotů klinicky manifestní hemochromatózu nevyvine. Akumulace železa probíhá v parenchymatózních orgánech a následně v retikuloendotelovém systému, z čehož plynou i klinické projevy onemocnění. Dominuje postižení jater až s rozvojem jaterní cirhózy, při kterém je fibrogeneze zprostředkována zejména aktivovanými hvězdicovými buňkami. Může dojít k rozvoji kardiomyopatie, atropatie a hypogonadotropického hypogonadizmu. Diabetes mellitus lze prokázat u 53–80 % manifestně nemocných. Naopak, prevalence hemochromatózy se u diabetiků pohybuje kolem 1,3 %, takže hereditární hemochromatóza není jasným etiologickým faktorem [4]. Nadbytek železa snižuje sekreci inzulinu i glukózovou toleranci již v časných fázích onemocnění. V patogenezi vzniku diabetu u těchto nemocných se spolu s rozvojem inzulinové rezistence, která je vlastní i dalším jaterním chorobám, uplatňuje i oxidativní poškozením β buněk pankreatu vlivem katalytické funkce železa.
Diagnostika této choroby je poměrně snadná. Kromě vysoké saturace transferinu (nad 60 % u mužů a nad 50 % u žen) nalézáme typicky vysoké hodnoty ferritinu, obvykle tisícové. Hodnoty jaterních aminotransferáz však bývají většinou zvýšené jen mírně. V současné době je možné provést i genetické vyšetření a stanovit nejčastější mutace (C282Y, H63D a S65C). Jaterní biopsie pak v některých případech není nutná. V případě jejího provedení zjišťujeme vysokou koncentraci železa v jaterní sušině (norma do 35 μmol/ g). Přínosná jsou i zobrazovací vyšetření, zejména magnetická rezonance [5]. Léčba je založena na provádění pravidelných krevních odběrů. Včasné zahájení je prevencí vzniku těžkých orgánových komplikací a v počátečním stadiu choroby vede i ke zlepšení glukózové tolerance. V počátku léčby jsou krevní odběry prováděny týdně a dále dle hodnot ferritinu (hodnoty se udržují pod 50 μg/ l).
Autoimunitní hepatitida
Autoimunitní hepatitida (AIH) je chronické zánětlivé onemocnění jater zatím ne zcela jasné etiologie se zcela typickými projevy autoimunitní choroby. Častěji postihuje mladé ženy (poměr muži : ženy je 1 : 4), ale výjimkou nejsou ani dětští pacienti a nemocní ve věku nad 60 let. Incidence choroby je asi 1–2/100 000. Typická je vazba na HLA B8, DR3 a DR4. K poškození hepatocytů dochází zejména T-lymfocyty zprostředkovanou cytotoxickou reakcí. Velice často bývají s autoimunitní hepatitidou asociovány i další autoimunitně podmíněné choroby, zejména tyreoditida, vitiligo, celiakie, ulcerózní kolitida a diabetes mellitus 1. typu. Na rozdíl od hereditární hemochromatózy bývá zvýšení jaterních aminotransferáz výrazné. Do diagnostické mozaiky patří i typická hypergamaglobulinemie a pozitivita cirkulujících autoprotilátek. Nejčastěji nalézáme protilátky antinukleární (AIH I. typu), protilátky proti hladkému svalu (ASMA), ANCA protilátky a protilátky proti jaterním a ledvinným mikrozomům (LKM1, AIH II. typu). Definitivní diagnóza je v tomto případě ale až histologická. Základem léčby je kombinovaná imunosupresivní terapie (kortikosteroidy, azathioprin, cyklosporin).
U nemocných s AIH a diabetem současně bývá tato léčba problematičtější, a zejména při vyšších dávkách glukokortikoidů bývá spolupráce diabetologa a hepatologa nezbytná.
Chronická infekce virem hepatitidy C
Chronická infekce virem hepatitidy C (RNA virus z čeledi Flaviviridae) je dalším onemocněním z řady jaterních chorob, u kterých je asociace diabetu vyšší než v běžné populaci nemocných se stejně pokročilým jaterním onemocnění. U nemocných s chronickou hepatitidou C je zvýšení rizika sice mírné, ale signifikantní a v porovnání se stejně rizikovými nemocnými téměř dvojnásobné. Příčiny tohoto stavu se stále studují a budou jistě multifaktoriální. Často je citována přímá interakce viru a inzulinové signální cesty [6] i nepřímý virový efekt mediovaný chronickým vzestupem TNFα [7].
Naopak, u nemocných s diabetes mellitus či poruchou glukózové tolerance je pozorována nižší odpověď na protivirovou léčbu (sustaind virological response – SVR) [8]. HOMA index je i jedním z negativních prediktivních faktorů odpovědi na virologickou léčbu. U nemocných, kteří SVR dosáhnou, naopak inzulinová rezistence klesá a snižuje se i incidence diabetu [7].
Hepatocelulární karcinom
Hepatocelulární karcinom (HCC) je celosvětově 5. nejčastější malignitou a 4. nejčastější příčinou úmrtí na maligní onemocnění. V České republice je incidence tohoto onemocnění 0,8/100 000. Až 8krát častěji je postižena mužská populace. 80–90 % případů je asociováno s jaterní cirhózou. Nejrizikovější nemocní jsou přitom pacienti s chronickou infekcí virem hepatitidy C a B, hereditární hemochromatózou, alkoholovým postižením jater a nealkoholovou steatohepatitidou. Mezi rizikovější skupiny nemocných této vážné komplikace konečného stadia jaterního onemocnění patří i pacienti s asociovaným diabetes mellitus (OR 3,12 vs 2,2) [2,3,9]. Za možný patofyziologický faktor je některými autory označován promitogenní efekt hyperinzulinemie a působení insulin like growth faktoru 1 (IGF1) na hepatocyty [9].
Pětileté přežití je v současné době, zejména v důsledku pozdní diagnostiky, jen 5 %. Diagnóza je založena na zobrazovacích vyšetřeních a sérové hladině α-fetoproteinu. Cílená biopsie ložiska bývá nutná většinou jen u lézí pod 2 cm. U nemocných v časném stadiu onemocnění je indikována anatomická či neanatomická resekce ložiska či jaterní transplantace (nemocní s již významnou portální hypertenzí a manifestní jaterní dysfunkcí). V případě lokálně pokročilého onemocnění je metodou volby radiofrekvenční ablace ložiska nebo intraarteriální embolizace. Progresi generalizované choroby u nemocných ve funkční třídě A a B dle Childa a Pugha lze zpomalit podáváním multityrosinkinázového inhibitoru sorafenibu [10].
Specifika léčby
Souběh obou onemocnění komplikuje i léčebnou strategii. Nemocní s jaterní cirhózou mají, v závislosti na pokročilosti jaterní choroby, větší tendenci k rozvoji hypoglykemických stavů. Z tohoto důvodu nebývají dobře tolerovány preparáty sulfonylurey. V pokročilých stadiích je vhodnější léčba inzulinem. Podání biguanidu bývá někdy u nemocných s jaterní cirhózou spojeno s obavou z rozvoje laktátové acidózy, ale u nemocných v kompenzovaném stavu nebylo toto riziko v prospektivních studiích prokázáno [11]. Navíc vede podávání metforminu při současné protivirové léčbě u nemocných s chronickou infekcí virem hepatitidy C podle některých prací k lepší virologické odpovědi na léčbu [12].
Vzhledem ke snížení inzulinové rezistence, jako jednoho z možných promitogenních faktorů, se dle některých prací i podání metforminu jeví, na rozdíl od preparátů sulfonylurey či dlouhodobé inzulinoterapie, jako protektivní faktor rozvoje hepatocelulárního karcinomu [3].
V případě symptomatické portální hypertenze, která bývá spojena s rozvojem významných jícnových, žaludečních či ektopických varixů, je indikována v rámci primární či sekundární prevence varikózního krvácení léčba neselektivním beta-blokátorem. U nemocných s nestabilním diabetem může být tato medikace obtížná či zcela kontraindikována, a je pak třeba volit endoskopické formy léčby.
Závěr
Riziko rozvoje diabetes mellitus u nemocných s jaterní cirhózou výrazně stoupá, zejména u některých jaterních onemocnění. V praxi diabetologa je třeba na tyto choroby myslet a po eventuálním asociovaném jaterním onemocnění pátrat. Pokročilé jaterní onemocnění modifikuje terapii jak diabetu, tak i vlastního jaterního onemocnění, zejména asociované portální hypertenze. Prognóza nemocných je určována zejména pokročilostí jaterního onemocnění a přidruženými komplikacemi z něho plynoucími.
Práce byla podpořena Grantem IGA MZŘ NS 10363-3 a VZ: MZO 00179906.
MUDr. Tomáš Fejfar, Ph.D.
www.lfhk.cuni.cz
e-mail: fejfar@fnhk.czDoručeno do redakce: 31. 10. 2010
Sources
1. Bianchi G, Marchesini G, Zoli M et al. Prognostic significance of diabetes in patients with cirrhosis. Hepatology 1994; 20 : 119–125.
2. Lai MS, Hsieh MS, Chiu YH et al. Type 2 diabetes and hepatocellular carcinoma: A cohort study in high prevalence area of hepatitis virus infection. Hepatology 2006; 43 : 1295–1302.
3. Donadon V, Balbi M, Mas MD et al. Metformin and reduced risk of hepatocellular carcinoma in diabetic patients with chronic liver disease. Liver Int 2010; 30 : 750–758.
4. Horák J. Genetická hemochromatóza. In: Ehrmann J, Hůlek P et al (eds). Hepatologie. 1. vyd. Praha: Grada 2010 : 339–345.
5. DuBois S, Kowdley V. Review article: targeted screening for hereditary haemochromatosis in high-risc groups. Aliment Pharmacol Ther 2004; 20 : 1–14.
6. Aytug S, Reich D, Sapiro LE et al. Impaired IRS-1/PI3-kinase signalling in patients with HCV: a mechanism for increase prevalence of type 2 diabetes. Hepatology 2003; 38 : 1384–1392.
7. Alaei M, Negro R. Hepatitis C virus and glucose and lipid metabolism. Diabetes Metab 2008; 34 : 692–700.
8. Romeo-Gómez M, Fernández-Rodriguez CM, Andrare RJ at al. Effect of sustained virological response to treatment on the incidence of abnormal glucose values in chronic hepatitis C. J Hepatol 2008; 48 : 721–727.
9. Donadon V, Balbi M, Ghersetti M et al. Antidiabetic therapy and increased risk of hepatocellular carcinoma in chronic liver disease. World J Gastroenterol 2009; 15 : 2506–2511.
10. Keating GM, Santoro A. Sorafenib: a review of its use in advanced hepatocellular carcinoma. Drugs 2009; 69 : 223–240.
11. Salpeter SR, Greyber E, Pasternak GA et al. Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus. Cochrane Database Syst Rev 2010; 20: CD002967.
12. Romero-Gómez M, Diago M, Andrade RJ et al. Spanish Treatment of Resistance to Insulin in Hepatitis C Genotype 1 Group. Treatment of insulin resistance with metformin in naïve genotype 1 chronic hepatitis C patients receiving peginterferon alfa-2a plus ribavirin. Hepatology 2009; 50 : 1702–1708.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2011 Issue 4-
All articles in this issue
- Diabetes mellitus and the oral cavity
- Xerostomia, hyposialia, sicca syndrome – quantitative disturbances of the salivary flow rate
- Peptic ulcer disease in patients with diabetes mellitus
- Motility disorders and gastric emptying in diabetes mellitus. Current diagnostics and treatment
- Current trends of surgical therapy of focal liver and pancreatic lesions
- Steatosis and steatohepatitis in diabetic patient
- Diabetes mellitus and the liver cirrhosis
- Acute pancreatitis in diabetics
- Coeliac disease and diabetes
- Colorectal cancer and diabetes
- Analogues of amylin, α-glucosidase inhibitors and the digestive system in homeostasis regulation
- Autonomic neuropathy of the gastrointestinal tract
- Dyspeptic syndrome associated with antidiabetic therapy
- Metabolic surgery – the most effective diabetes treatment
- Metabolic surgery – a new approach to the management of selected diseases
- Incretin hormones
- Treatment of type 2 diabetes mellitus with GLP-1 antagonists
- Incretin therapy and the metabolic syndrome
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Xerostomia, hyposialia, sicca syndrome – quantitative disturbances of the salivary flow rate
- Treatment of type 2 diabetes mellitus with GLP-1 antagonists
- Autonomic neuropathy of the gastrointestinal tract
- Diabetes mellitus and the liver cirrhosis
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

