-
Medical journals
- Career
Obojstranná flebotrombóza dolných končatín zapríčinená vrodenou malformáciou dolnej dutej žily
: A. Halčín 1; E. Kováčová 1; F. Mikla 1; A. Reptová 1; J. Bedeová 2
: I. interná klinika Lekárskej fakulty UK a FNsP Bratislava, pracovisko Staré mesto, Slovenská republika, prednosta doc. MU Dr. Soňa Kiňová, PhD. 1; I. rádiologická klinika Lekárskej fakulty UK a FNsP Bratislava, pracovisko Staré mesto, Slovenská republika, prednosta prof. MU Dr. Jozef Bilický, PhD. 2
: Vnitř Lék 2009; 55(12): 1189-1192
: Editorials
Agenéza/ atrézia v. cava inferior je zriedkavou vrodenou anomáliou, zapríčinenou poruchou embryonálneho vývoja venózneho systému. Vo väčšine prípadov je vzhľadom na rozvinutý kolaterálny venózny obeh asymptomatická. V časti prípadov sa však môže manifestovať vznikom hlbokej trombózy v oblasti panvy a dolných končatín. V tejto kazuistike opisujeme prípad 21 - ročného muža, u ktorého sa vyvinul bolestivý opuch oboch dolných končatín. Ultrasonografické vyšetrenie odhalilo obojstrannú trombózu hlbokého žilového systému dolných končatín a panvy. Následné CT angiografické vyšetrenie preukázalo atréziu infrarenálneho úseku v. cava inferior. Trombotickým procesom bol podľa CT vyšetrenia výrazne postihnutý aj kolaterálny venózny obeh, ktorý ústil prevažne do v. azygos a v. hemiazygos. Vyšetrenie koagulačného systému nevysvetľovalo príčinu vzniku trombózy. Realizovali sme systémovú trombolýzu streptokinázou v trvaní 5 dní, následne bol podávaný nízkomolekulárny heparín v antikoagulačnej dávke. Táto liečba preukázala dobrý klinický efekt. Pacient bol nastavený na dlhodobú perorálnu antikoagulačnú liečbu v kombinácii s kyselinou acetylsalicylovou a prepustený do ambulantnej starostlivosti. V priebehu 4 nasledujúcich mesiacov pri uvedenej liečbe nedošlo ku recidíve trombotického procesu ani k rozvoju krvácavej komplikácie.
Kľúčové slová:
agenéza – v. cava inferior – flebotrombózaÚvod
Agenéza v. cava inferior je zriedkavou vrodenou anomáliou, zapríčinenou poruchou embryonálneho vývoja venózneho systému. Vo väčšine prípadov je asymptomatická a funkciu venóznej drenáže dolných končatín a panvy preberá systém kolaterál. V časti prípadov, u ktorých je tento náhradný drenážny systém nedostatočný, sa však táto abnormalita môže manifestovať vznikom hlbokej trombózy v oblasti panvy a dolných končatín.
V tejto kazuistike predstavujeme prípad mladého muža, hospitalizovaného pre obojstrannú trombózu hlbokého žilového systému dolných končatín, u ktorého podrobnejšie vyšetrenie odhalilo hypopláziu až agenézu infrarenálneho úseku v. cava inferior. Rozsiahla trombotická komplikácia postihla aj kolaterálny venózny obeh.
Popis prípadu
21-ročný pacient, u ktorého sa objavil bolestivý opuch oboch dolných končatín, bol hospitalizovaný na našej klinike pre sonografickým vyšetrením potvrdenú bilaterálnu flebotrombózu dolných končatín, zasahujúcu až do sútoku vv. illiacae. Aktuálne ťažkosti pacienta sa objavili včasne ráno v deň príjmu do nemocnice. Pacient pre bolesti dolných končatín navštívil praktickú lekárku, ktorá ho odoslala do nemocnice s podozrením na flebotrombózu dolných končatín. Pri návšteve našej príjmovej ambulancie bol pre bolesti pacient schopný chôdze len s barlami. Dolné končatiny boli výrazne livídne sfarbené, edematózne bilaterálne až po stehná, palpačne taktiež až do výšky stehien tuhého pohmatu.
Bol afebrilný, v krvnom obraze však bola prítomná leukocytóza (15 × 109/l), hladina C-reaktívneho proteínu bola taktiež zvýšená (104mg/l). Dopplerovská ultrasonografia potvrdila prítomnosť akútnej hlbokej venóznej trombózy oboch dolných končatín, zasahujúcej až do sútoku vv. illiacae. Pacient bol následne prijatý na Jednotku intenzívnej starostlivosti našej kliniky.
Z anamnézy vyplynulo, že 3 dni pred príjmom na našu kliniku bol pacient prepustený z hospitalizačného pobytu v inom zariadení internistického charakteru, kde bol liečený pre infekt močových ciest komplikovaný akútnou postinfekčnou glomerulonefritídou. V deň príjmu do nášho zariadenia pacient už 9. deň užíval kombinovanú perorálnu antibiotickú terapiu (Augmentin, Ciphin).
V predchorobí pacient udával sporadický výskyt makroskopickej hematúrie v trvaní asi 8 mesiacov. Bol dispenzarizovaný urológom i nefrológom. Ultrasonografické vyšetrenie brušných orgánov vtedy vykázalo normálny nález, punkcia obličky realizovaná nebola.
Počas hospitalizácie u nás bolo realizované kontrastné CT vyšetrenie brucha a malej panvy s nepriamou kavografiou, ktoré ukázalo obraz hypoplázie až agenézy infrarenálneho úseku v. cava inferior (VCI) s prítomnosťou paravertebrálneho kolaterálneho obehu, aktuálne úplne tromboticky uzavretého (obr. 1). Súčasťou kolaterálneho obehu sa v CT obraze zdala byť aj dilatovaná v. renalis sinistra. Takmer identický výsledok bol o niekoľko dní získaný kontrolným CT vyšetrením s 3-dimenzionálnou rekonštrukciou. Malformácia VCI bola však tentokrát presnejšie určená ako atrézia tejto žily.
1. CT vyšetrenie. Na obrázku zhotovenom CT vyšetrením môžeme vidieť transverzálny rez trupom, vedený vo výške spodnej polovice obličiek. Šípka označuje miesto, kde by sa za normálnych podmienok mala zobrazovať dolná dutá žila. 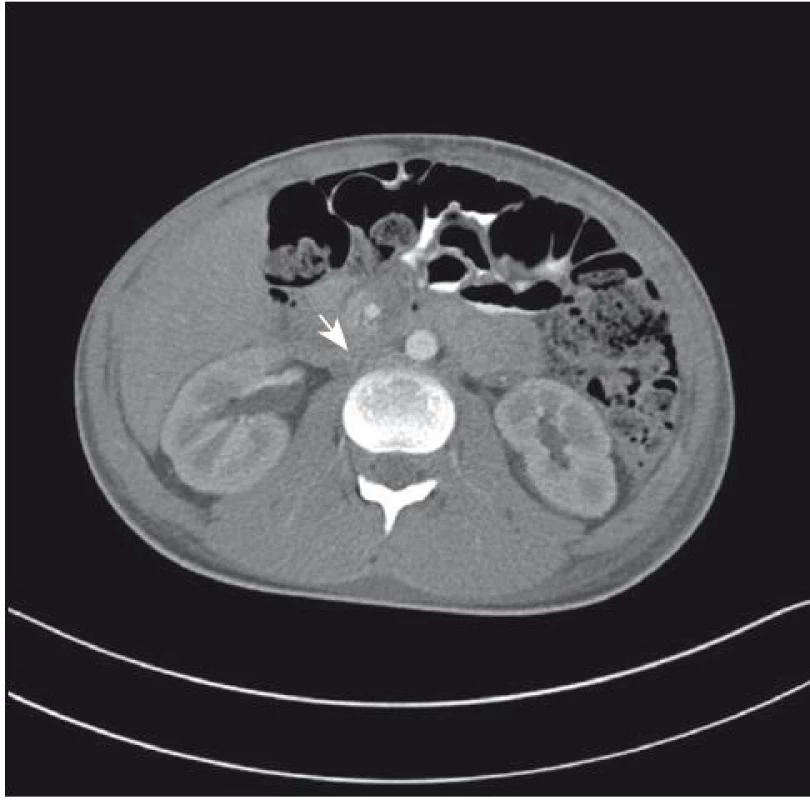
U pacienta bolo realizované genetické vyšetrenie zamerané na prítomnosť dedičných príčin trombofilného stavu. Týmto vyšetrením sa zistilo, že pacient je heterozygot pre mutáciu MTHFR 677C T génu pre enzým metyléntetrahydrofolátreduktáza. Táto mutácia však podľa dostupnej literatúry [1,2] genetický rizikový faktor pre vznik venóznej trombózy nepredstavuje, a to ani v homozygotnej forme. Prítomnosť mutácie génu pre faktor V Leiden či génu pre protrombín 20210G A dokázaná nebola. Hladiny proteínu C, proteínu S, fibrinogénu či antitrombínu III taktiež prítomnosť hlbokej venóznej trombózy nevysvetľovali (tab. 1).
1. Vybrané laboratórne hodnoty. 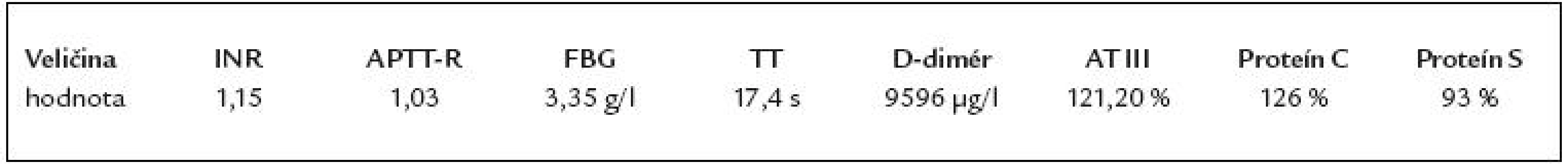
Stav pacienta bol počas diagnosticko terapeutického postupu opakovane konzultovaný s pracoviskom cievnej chirurgie, ktoré odporučilo konzervatívny postup. Realizovali sme systémovú trombolýzu streptokinázou v dĺžke trvania 5 dní, od 5. dňa bol podávaný nízkomolekulárny heparín v plnej dávke. Taktiež sme pokračovali v antibiotickej liečbe uroinfektu. Táto liečba preukázala v oboch smeroch dobrý klinický efekt. Závažnejšie krvácavé komplikácie antikoagulačnej liečby pozorované neboli. Pacient bol nastavený na perorálnu antikoagulačnú liečbu v kombinácii s kyselinou acetylsalicylovou v dávke 100mg denne a prepustený do ambulantnej starostlivosti.
V priebehu 4 nasledujúcich mesiacov pri uvedenej liečbe nedošlo ku recidíve trombotického procesu ani k rozvoju krvácavej komplikácie. Pri kontrolnej duplexnej ultrasonografii postihnutého venózneho riečiska vidno v lúmene zvyšky starého trombotického procesu s obrazom uspokojivej sekundárnej rekanalizácie.
Diskusia
Kongenitálna anomália v. cava inferior je zriedkavý vaskulárny defekt, ktorý je výsledkom aberantného vývoja venózneho systému tela počas embryogenézy, v 6.–8. gestačnom týždni.
Výsledná podoba tejto pravostranne uloženej veľkej žily je výsledkom procesu, ktorého sa zúčastňujú 3 párové embryonálne vény: v. supracardinales, v. subcardinales a v. postcardinales [3–5]. Ak počas tohto zložitého procesu dôjde k chybnému vývoju v spájaní, modelácii či regresii týchto vén, vznikajú rozličné anomálie VCI. Ich prevalencia v celkovej populácii sa odhaduje na 0,07–8,7% [6]. Škála výsledkov aberantného vývoja VCI je pomerne široká, od ľavostranne uloženej VCI, cez dvojitú VCI, poruchy vyústenia VCI, aberantný priebeh ľavej renálnej vény, až po poruchy kontinuity VCI, obvykle v infrarenálnom úseku [3]. Táto malformácia sa často asociuje i s ďalšími vrodenými aberáciami, ako sú napr. vrodené vývojové vady srdca, polysplénia alebo aberácie uloženia tráviacej trubice v brušnej dutine.
Klinický objav vývojovej anomálie VCI je obvykle následkom náhodného záchytu pri rádiologickom vyšetrovaní pacienta z iných dôvodov. Pacienti sú totiž vzhľadom na prítomnosť vlastnej anomálie obvykle asymptomatickí. Zriedkavejšie sa táto anomálie stáva symptomatickou nepriamo – skrze zapríčinenie vzniku hlbokej venóznej trombózy v oblasti panvy alebo dolných končatín. Príčinou tejto komplikácie vtedy býva nedostatočnosť drenáže venóznej krvi z dolných končatín, ktorá sa do pravej srdcovej predsiene v prípade nepriechodnosti VCI dostáva skrze systém kolaterál, väčšinou tvorený sakrálnymi, lumbálnymi a epigastrickými žilami [5]. Následkom prípadnej insuficiencie tejto náhradnej drenáže býva zvýšený venózny tlak, stáza žilovej krvi a nakoniec v prípade nepriaznivých podmienok vznik hlbokej trombózy [7,8].
U nášho pacienta bola anomália VCI odhalená práve z dôvodu bližšieho prešetrovania realizovaného pre vznik symptomatickej trombotickej komplikácie, ktorá vďaka svojmu rozsahu, veku pacienta a neprítomnosti zjavnej vyvolávajúcej príčiny toto prešetrenie vyžadovala.
Súvislosť medzi prítomnosťou hypoplázie/agenézy VCI a vznikom trombózy žilového systému panvy a dolných končatín sa zdá byť zrejmou. Otázkou samozrejme zostáva prítomnosť spúšťacieho momentu trombotického procesu a prítomnosti prípadných spolupríčinných faktorov.
V rámci odoberania rodinnej anamnézy sme u pacienta nezistili údaj o prekonaní trombózy ním alebo blízkym rodinným príslušníkom. Pacient taktiež neguje prekonanie traumy, podstúpenie chirurgického zákroku, či výnimočnejšiu fyzickú aktivitu v období pred vznikom hlbokej venóznej trombózy.
Vyšetrenie koagulačných parametrov ani vyšetrenie zamerané na najčastejšie genetické príčiny trombofilného stavu neodhalili prítomnosť inej predisponujúcej príčiny.
U pacienta bola pri recentnej hospitalizácii zachytená proteinúria (1,2g bielkovín/24 hod), bola však dávaná do súvisu s diagnózou postinfekčnej glomerulonefritídy pri liečenom uroinfekte. Hladina celkových plazmatických bielkovín či albumínu znížená nebola. Prítomnosť nefrotického syndrómu ako jednej z možných príčin hyperkoagulačného stavu za daných okolností nepredpokladáme.
Ako potenciálny spúšťací moment sa nám teda javí najmä prítomnosť zápalového procesu s origom v močových cestách, v dobe vzniku ťažkostí stále aktívneho, napriek prebiehajúcej antibiotickej liečbe. Do úvahy taktiež prichádza znížená mobilita, ktorú zo sebou hospitalizácia a akútny infekt obvykle prinášajú.
Podľa dostupnej lekárskej dokumentácie musel byť pacient krátko po pôrode operovaný pre peripartálnu ruptúru omfalokély, pričom bola diagnostikovaná i malrotácia mezentéria. Vzhľadom na častú asociáciu anomálie VCI s aberáciami vývinu črevnej rúry, predpokladáme v tomto prípade súvislosť nálezov.
Akademickou nateraz ostáva otázka možného súvisu opakovaných lumbalgií a hematúrie s prítomnosťou paravertebrálneho kolaterálneho obehu a s predpokladaným začlenením v. renalis sinistra do tohto obehu podľa CT obrazu. Pri vylúčení iných, pravdepodobnejších nefrologických príčin tohto javu, by snáď bolo možné uvažovať o zvýšenom tlaku v dilatovanej v. renalis sinistra ako o možnej príčine tohto rekurentného javu. Samotná bolestivosť v lumbálnej oblasti by mohla súvisieť aj s dilatáciou venóznych plexov v epidurálnom a paravertebrálnom priestore, ako to pri agenéze VCI s použitím MR angiografického vyšetrenia popísali Yigita et al vo svojej kazuistike u 13-ročného dievčaťa [9]. Takáto príčina lumbalgie je však v diagnostickom spektre lumbalgií veľmi zriedkavá.
Podľa štatistického spracovania štúdie Obernostera et al [10] vykonanej na vzorke 97 pacientov s hlbokou venóznou trombózou dolných končatín, pacienti s hlbokou venóznou trombózou zapríčinenou anomáliou VCI boli signifikantne mladší ako tí, u ktorých takáto trombóza vznikla z iných príčin. Autori tejto štúdie došli na základe týchto dát k záveru, že na anomáliu VCI ako príčinu hlbokej venóznej trombózy by sme mali pomýšľať najmä u pacientov s trombózou iliackých vén vo veku okolo 30 rokov a mladších.
Iná skupina autorov, Ruggeri, Tosetto et al [11] na základe svojich klinických dát odhaduje, že kongenitálna absencia VCI je u skupiny pacientov s vekom pod 30 rokov, ktorí prekonali hlbokú venóznu trombózu, prítomná asi v 5% prípadov. Ruggeri et al v závere svojej práce odporúčajú prítomnosť anomálie VCI zvažovať zvlášť u mladých pacientov s idiopatickou proximálnou hlbokou trombózou venózneho systému a zrealizovať u týchto pacientov rozsiahlejšie vyšetrenie (angiografické alebo CT vyšetrenie) na jej vylúčenie.
V prípade potvrdenia prítomnosti trombózy zapríčinenej anomáliou VCI konzervatívne riešenie pozostáva z podávania antitrombotickej terapie, či už ide o trombolytické prípravky (systémovo alebo lokálne podávané), alebo podávanie heparínu, s následným prechodom na perorálnu antikoaguláciu. V liečbe sa ďalej používa bandážovanie, elevácia dolných končatín a ich pohybové precvičovanie. Otázka dĺžky podávania perorálnej antikoagulácie závisí od konkrétnej anomálie, prítomnosti prídavných protrombotických faktorov a od údaja o primomanifestácii či rekurencii trombózy. V dnešnej dobe existuje už i možnosť rekonštrukčného chirurgického zákroku [12], táto však ostáva ponechaná pre prípady rekurentných trombotických komplikácií a komplikované, či na konzervatívnu terapiu nereagujúce prípady.
Pacienti, u ktorých je prítomnosť anomálie VCI už známa, by sa mali vyhýbať situáciám, ktoré zvyšujú riziko vzniku trombózy. Medzi ne patrí napr. dlhšia imobilizácia či záťaž nezvyčajnou fyzickou námahou [10,13].
MUDr. Andrej Halčín
www.nspr.sk
e mail: halcin@zoznam.sk
Sources
1. Bezemer ID, Doggen CJ, Vos HL et al. No association between the common MTHFR 677C ‑ T polymorphism and venous thrombosis: results from the MEGA study. Arch Intern Med 2007; 167 : 497 – 501.
2. Huisman MV, Rosendaal F. Thrombophilia. Curr Opin Hematol 1999; 6 : 291 – 297.
3. Bass JE, Redwine MD, Kramer LA et al. Spectrum of congenital anomalies of the inferior vena cava: cross ‑ sectional imaging findings. Radiographics 2000; 20 : 639 – 652.
4. Bass JE, Redwine MD, Kramer LA et al. Absence of the inferior vena cava with preservation of the suprarenal segment as revealed by CT and MR venography. AJR Am J Roentgenol 1999; 172 : 1610 – 1612.
5. Minniti S, Visenti S, Procacci C. Congenital anomalies of the venae cavae: embryological origin, imaging features and report of three new variants. Eur Radiol 2002; 12 : 2040 – 2055.
6. Kellman GM, Alpern MB, Sandler MA et al. Computed tomography of vena caval anomalies with embryologic correlation. Radiographics 1988; 8 : 533 – 556.
7. Sakellaris G, Tilemis S, Papakonstantinou O et al. Deep venous thrombosis in a child associated with an abnormal inferior vena cava. Acta Paediatr 2005; 94 : 242 – 244.
8. Chee YL, Culligan DJ, Watson HG. Inferior vena cava malformation as a risk factor for deep venous thrombosis in the young. Br J Haematol 2001; 114 : 878 – 880.
9. Yigita H, Yagmurlub B, Yigita N et al. Low Back Pain as the Initial Symptom of Inferior Vena Cava Agenesis. AJNR Am J Neuroradiol 2006; 27 : 593 – 595.
10. Obernosterer A, Aschauer M, Schnedl Wet al. Anomalies of the inferior vena cava in patients with iliac venous thrombosis. Ann Intern Med 2002; 136 : 37 – 41.
11. Ruggeri M, Tosetto A, Castaman G et al. Congenital absence of the inferior vena cava: a rare risk factor for idiopathic deep ‑ vein thrombosis. Lancet 2001; 357 : 441 – 441.
12. Dougherty MJ, Calligaro KD, DeLaurentis DA. Congenitally absent inferior vena cava presenting in adulthood with venous stasis and ulceration: a surgical treated case. J Vasc Surg 1996; 23 : 141 – 146.
13. Klessen C, Deutsch HJ, Karasch T et al. Thrombosis of the deep leg and pelvic veins in congenital agenesis of the vena cava inferior. Deutsch Med Wochenschr 1999; 124 : 523 – 526.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2009 Issue 12-
All articles in this issue
- The programme of managed ambulatory rehabilitation for patients after heart valve defect surgery
- Liver transplantation and peri- operative changes to renal function
- Impact of pandemic H1N1 2009 influenza virus on critical care in Australia: A single centre case series
- The complexity of interactions of the tumour growth process
- The complexity of interactions of the tumour growth process
- Pre‑eclampsia from the perspective of inter- professional collaboration
- Gender differences in pharmacotherapy of chronic heart failure
- Diabetes insipidus followed, after 4 years, with dysarthria and mild right‑ sided hemiparesis – the first clinical signs of Erdheim- Chester disease. Description and depiction of a case with a review of information on the disease
- Symmetrical phlebothrombosis of lower extremities resulting from congenital malformation of vena cava inferior
- Nuclear receptors gene polymorphisms and risk of restenosis and clinical events following coronary stenting
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Pre‑eclampsia from the perspective of inter- professional collaboration
- The programme of managed ambulatory rehabilitation for patients after heart valve defect surgery
- The complexity of interactions of the tumour growth process
- Symmetrical phlebothrombosis of lower extremities resulting from congenital malformation of vena cava inferior
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

