-
Medical journals
- Career
Radionuklidové zobrazovací metody používané v endokrinologii
: P. Vlček; K. Michalová; K. Táborská; P. Sýkorová
: Klinika nukleární medicíny a endokrinologie 2. lékařské fakulty UK a FN Motol, Praha, přednosta doc. MUDr. Petr Vlček, CSc.
: Vnitř Lék 2006; 52(10): 969-972
: Review
Autoři podávají přehled o současných možnostech využití metod nukleární medicíny v diagnostice a terapii v endokrinologii. V oblasti hypotalamo-hypofyzárního systému jde o využití analoga somatostatinových receptorů, v tyreologii kromě stanovení nádorových markerů je v monitorování zhoubných nádorů užíváno tenchecium značeného MIBI radiojodu 131. Novou možností před plánovanou léčbou nádorů štítné žlázy je využití rhTSH. V diagnostice neuroendokrinních tumorů se používá 123I-MIBG, při pozitivní scintigrafii lze podat terapeutický 131I-MIBG. V diagnostice příštítných tělísek jsou upřednostňována před metodami subtrakčními dvoufázová scintigrafie MIBI. U pokročilých málo diferencovaných zhoubných nádorů se s výhodou využívá pozitronové emisní tomografie.
Klíčová slova:
zobrazovací metody - radiofarmaka - štítná žláza - příštítná tělíska - neuroendokrinní tumoryÚvod
Je jen málo disciplín medicíny, kde by poznatky získané v jednom oboru přímo ovlivnily rozvoj oboru druhého, tak, jak je tomu u endokrinologie a nukleární medicíny. Vyšetření štítné žlázy pomocí radionuklidů patřilo k prvním diagnostickým nukleárně-medicínským počinům poloviny 20. století. Pomocí metod radioimunologické analýzy byly stanoveny prakticky všechny hormony včetně některých jejich metabolitů. Zobrazovací metody v nukleární medicíně, které jsou založeny na schopnosti metabolicky aktivní tkáně vychytávat a akumulovat dané radiofarmakum, zejména v endokrinologii v posledních letech dosáhly velkého rozmachu. Postupným zdokonalováním přístrojové techniky a moderním vybavením pracovišť se otevřely nové možnosti pro využití otevřených zářičů v diagnostice i léčbě. Nukleární medicína se tak může uplatnit při posuzování funkčních poruch, kdy dochází ke změně sekrece hormonů dané endokrinní žlázy, ať již ve smyslu snížené produkce (hypofunkce) či nadměrného vylučování daného hormonu (hyperfunkce), současně dobře hodnotí morfologické změny.
Zobrazovací metody
V oblasti hypotalamo-hypofyzárního systému nemáme v současné době k dispozici radiofarmakum, které by se selektivně vychytávalo v oblasti adenohypofýzy či neurohypofýzy. U některých nádorů adenohypofýzy lze prokázat somatostatinové receptory - lze tedy pro lokalizační diagnostiku nádorů použít 111In-pentetreotidu, analoga somatostatinu. Dopaminové receptory D2 jsou přítomny u některých prolaktinomů. U nádorů secernujících gonadotropiny lze použít SPECT metodu v rámci receptorové diagnostiky pomocí aplikovaných ligandů, např. 123I-epidepridu. Laboratorními RIA metodami lze vyšetřit prakticky všechny hormony hypotalamu, hypofýzy i hormony cílových endokrinních žláz (např. ACTH, TSH, PRL, FSH, STH, LH a další).
Nemoci štítné žlázy jsou nejčastějšími endokrinopatiemi ve většině zemí světa. V oblasti s jodovým deficitem mohou postihovat až 80-90 % obyvatelstva, ve vyspělých zemích v průměru asi 5 % populace. Význam tyreopatií nespočívá pouze v četnosti výskytu, ale i v dalších faktorech: výrazně častěji jsou postiženy ženy než muži, onemocnění stoupá s věkem, u žen po 45.-50. roce věku bývají častější autoimunitní tyreopatie. Nedostatek jodu či selénu v potravě stejně jako vyšší radiace prostředí patří mezi významné faktory uplatňující se v etiopatogenezi tyreopatií. Problematikou jodového deficitu se zabývaly rozsáhlé epidemiologické studie. Profesor Zamrazil se významnou měrou zasloužil o zdokumentování a řešení jodového deficitu v České republice (studie probíhají od počátku 90. let minulého století) a navázal tak na rozsáhlé epidemiologické studie doc. Šilinka et al z poloviny minulého století.
Štítná žláza produkuje denně kolem 100 µg tyroxinu a 10 µg trijodtyroninu, vlastního biologicky účinného hormonu štítné žlázy. Cílem funkční diagnostiky je rozlišení funkčních poruch, tj. hypotyreózy a hypertyreózy. In vitro metody se začaly vyvíjet již v 50. letech minulého století. Původní mikrochemické testy byly překonány a postupně nahrazeny metodami založenými na principu radiosaturační analýzy. Zpočátku se vyšetřovaly pouze celkové hladiny tyreoidálních hormonů, postupně se přešlo k hodnocení funkce štítné žlázy pomocí plazmatické hladiny TSH metodami 2. a 3. generace. V případě abnormálního výsledku se měření doplňuje o stanovení volné frakce tyroxinu (fT4) a trijodtyroninu (fT3), neboť celkové hladiny T4 či T3 neodrážejí jednoznačně funkční stav organizmu. Z dalších významných produktů tyreocytů je pro diagnostiku recidiv nádorů štítné žlázy nezbytné stanovení tyreoglobulinu v séru. Tyreoglobulin má význam nádorového markeru, je-li jeho koncentrace po totální tyreoidektomii a radioablaci radiojodem zvýšena. V případě štítné žlázy in situ je jeho význam nízký, pouze extrémně zvýšené hladiny mohou vzbudit podezření z nádorové diseminace. RIA metodou se zpočátku rovněž stanovoval imunoreaktivní kalcitonin (iCT). Jeho vysoké hladiny bývají spojeny s přítomností medulárního karcinomu štítné žlázy (nádorový marker). Pro posouzení některých tyreopatií má zásadní význam vyšetření protilátek proti tyreoglobulinu (antiTg) a proti tyreoidální peroxidáze (antiTPO). Zvýšená hladina těchto protilátek svědčí pro autoimunitní původ onemocnění. Chronická Hashimotova autoimunitní tyreoiditida bývá v dospělosti nejčastější příčinou hypotyreóz. Hladiny protilátek proti TSH receptoru (TRAK) vypovídají o aktivitě Graves-Basedowovy choroby. Zvýšené hladiny jsou u aktivní tyreoidální autoimunitní orbitopatie (TAO), spojené s očními komplikacemi, protruzí, diplopií či lagoftalmem.
Funkce štítné žlázy bývala hodnocena i podle měření akumulace s 131I. Smyslem tohoto akumulačního testu bylo odlišení eutyreózy od hypertyreózy. Nejznámějším byl Wernerův supresní test, který byl založen na stanovení útlumu akumulace po 5-7denním podávání trijodtyroninu v dávce 60 - 100 µg denně. U pacientů s tyreotoxikózou nedošlo k očekávanému poklesu akumulace na polovinu, v některých případech paradoxně docházelo ke zvýšení akumulace. Tento test byl však zatížen nepřesnostmi, zejména snadným arteficiálním ovlivněním akumulace léky bohatými na jod (amiodaron, jodované kontrastní látky apod), po kterých došlo k masivnímu zajodování organizmu. V současné době za jedinou indikaci pro provedení akumulačního testu jsou považovány stavy po chirurgickém výkonu pro karcinom štítné žlázy, kdy stanovení akumulace ve zbytkové tkáni štítné žlázy má význam pro výpočet léčebné dávky radiojodu.
2. Diagnostická scintigrafie <sup>123</sup>I-MIBG 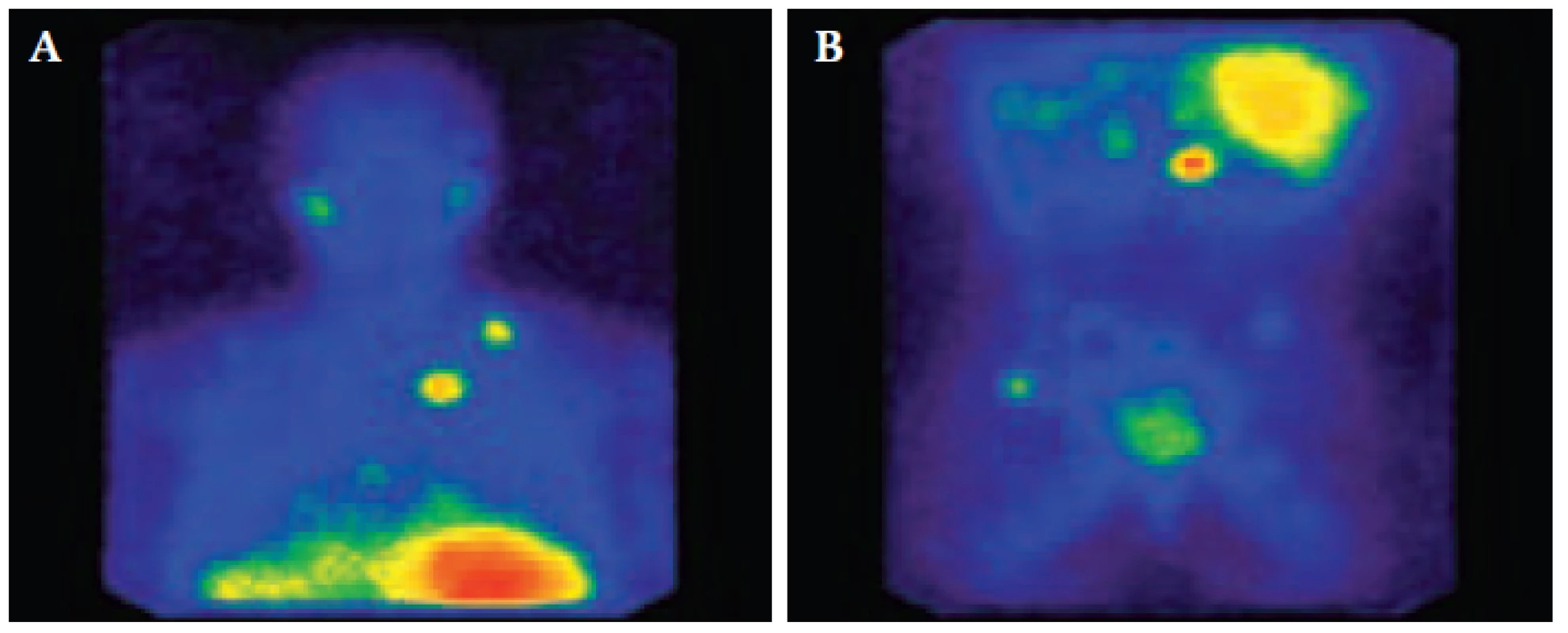
V současné době je základní zobrazovací metodou v tyreologii sonografie, zejména pro svou neinvazivnost a dostupnost. Ultrazvukové vyšetření využívá sond s frekvencí 7,5-10 MHz, metoda umožňuje s vysokou spolehlivostí určit celkový objem štítné žlázy, stanovit základní morfologické změny v jejím parenchymu, od prosté uzlové přestavby až po rozsáhlá degenerativně změněná cystická ložiska. Pomocí průtokové dopplerovské metody lze rozhodnout u hypertyreóz o aktivitě procesu. Sonografie má však i své limity, a to zejména v posouzení retrosternálních partií štítné žlázy. V tomto případě využíváme možností standardních zobrazovacích metod - RTG horní hrudní apertury či počítačové tomografie horního mediastina.
Metody nukleární medicíny jsou však stále nepřekonané v několika indikacích: průkaz funkční autonomie uzlů, diagnostika retrosternální strumy, průkaz ektopické tkáně štítné žlázy (např. lingvální strumy), stavy po chirurgii na štítné žláze s reziduem akumulující tkáně štítné žlázy, monitorování a vyhledávání lokálních a vzdálených metastáz u diferencovaného karcinomu štítné žlázy.
99mTcO4/pertechnetát sodný patří kromě radiojodu k nejpoužívanějším radionuklidům v diagnostice štítné žlázy. Jeho fyzikální vlastnosti jsou optimální pro scintigrafii, vykazuje malou radiační zátěž a je dobře dostupný. Pro průkaz metastatického postižení u karcinomu štítné žlázy je však nevhodný (krátký fyzikální poločas, poněkud odlišná distribuce radionuklidu). Normální záznam ukazuje štítnou žlázu jako symetrický útvar motýlovitého tvaru lokalizovaný mezi jugulem a chrupavkou štítnou s homogenní distribucí radiofarmaka. Pokud se vyskytují ložiska se sníženou či chybějící aktivitou, jde o tzv. „studené uzly“ (fotopenické oblasti), jsou-li zachycena ložiska se zvýšenou aktivitou, jde o „horké uzly“. Funkční autonomie bývá spjata s nálezem horkých uzlů. Difuzní snížení akumulace ve štítné žláze může být způsobeno zánětlivým postižením štítné žlázy, masivním „zajodováním“ organizmu (zablokování akumulace látkami s vysokým obsahem jodu).
Radiojodu 123 a 131 se využívá v tyreoidální diagnostice zhoubných nádorů. Pro diagnostickou scintigrafii je výhodnější 123I, vzhledem k získání kvalitnějších snímků, nevýhodou je jeho vysoká cena. Radiojod 131I je cenově dostupnější, jde o smíšený β a γ zářič o dlouhém fyzikálním poločasu, který lze tedy využít i terapii diferencovaného karcinomu štítné žlázy. Před vlastní scintigrafií radiojodem je nezbytné upozornit nemocného, aby před vyšetřením neužíval jod, který by mohl zablokovat akumulaci radionuklidu ve štítné žláze. Rovněž nesmí užívat léky s vysokým obsahem jodu, např. amiodaron či desinfekční preparáty typu Jodisol, některé oční kapky apod. Rovněž by neměl absolvovat RTG vyšetření, při kterých se používají kontrastní látky obsahující jod.
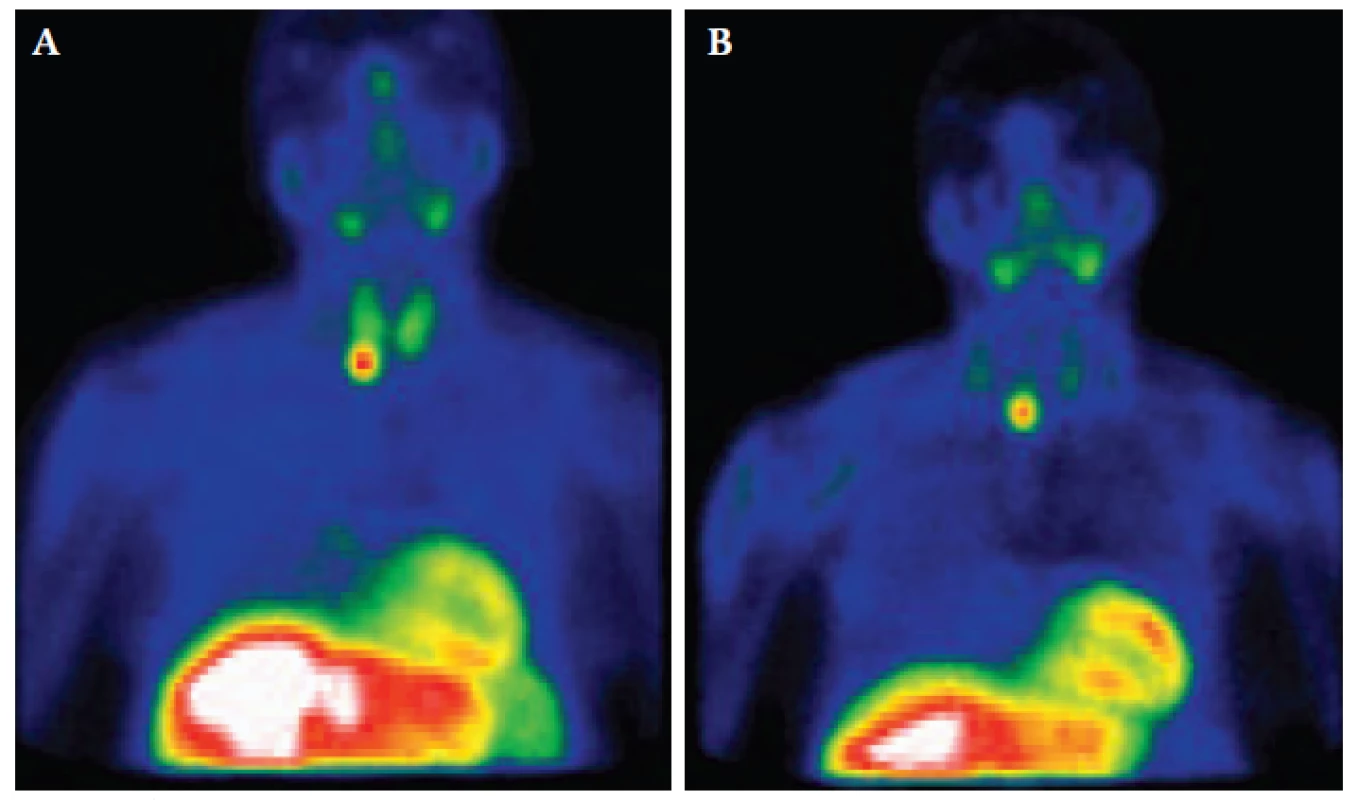
Při dlouhodobém monitorování nemocných s papilárním a folikulárním karcinomem lze využít metody, u které není nutné vysadit hormonální substituci. Výhodná je celotělová scintigrafie pomocí 99mTc-MIBI (metoxyizobutylizonitril), což je radiofarmakum, které pro akumulaci využívá svých lipofilních vlastností a míra akumulace je závislá na počtu mitochondrií v cytoplazmě buněk, takže v metabolicky aktivní tkáni se vychytává více podaného radiofarmaka [5].
V poslední době v dlouhodobém sledování nemocných se stále více osvědčuje podání rekombinantního humánního TSH (rhTSH), které umožní provést diagnostickou radiojodovou scintigrafii, aniž by předtím musel nemocný na 4 týdny vysazovat hormony štítné žlázy [2]. Tato nesmírná výhoda pro pacienta je však zastíněna ekonomickou náročností, takže větší využití rhTSH je našich podmínkách značně limitováno. V současné době je rhTSH schvalován zdravotními pojišťovnami jako příprava před léčebnou aplikací radiojodu u nemocných s aktivním nádorovým procesem, zvýšeným tyreogolobulinem a současně přítomnými lokálními či vzdálenými metastázami.
Diagnostika medulárního karcinomu štítné žlázy (MTC) je poněkud odlišná. Jde o nádor, který vychází z parafolikulárních buněk, jeho základ nutno hledat v neurální liště. Představuje kolem 5 - 8 % všech tyreoidálních malignit. Vyskytuje se sporadicky, kdy je diagnostikován na podkladě klinické symptomatologie, avšak asi u čtvrtiny nemocných s tímto nádorem prokazujeme familiární výskyt onemocnění. Podkladem této familiární formy MTC je zárodečná bodová mutace RET proto-onkogenu na 10. chromozómu. Vzhledem k tomu, že MTC neakumuluje radiojod, je základním léčebným opatřením chirurgem provedená totální tyreoidektomie. Na radikalitě výkonu pak závisí další osud nemocného [6].
Z radiofarmak se používá pro pooperační celotělový screening 99mTc-alkalinizovaná dimerkaptojantarová kyselina (99mTc-DMSA). Radiofarmakum se běžně neakumuluje v normální štítné žláze, proto je vhodné pro vyšetření pacientů s vyšší pooperační hladinou kalcitoninu pro průkaz lokálních či vzdálených metastáz. U části nemocných s MTC jsou prokazovány receptory proti somatostatinu, lze tedy využít jeho analoga v podobě scintigrafie 111In pentetreotidem (OctreoScanem). Kromě medulárního karcinomu štítné žlázy byly somatostatinové receptory prokázány i v orbitě, takže scintigrafie pomocí OctreoScanu pomáhá určit aktivitu onemocnění u tyreoidálních autoimunitních orbitopatií. Tato zobrazovací metoda bývá považována za „zlatý standard“.
123I či 131I-MIBG (metaiodobenzylguanidin) je syntetický analog norepinefrinu a guanetidinu. V diagnostice neuroendokrinních nádorů (včetně MTC) je dávána přednost značení jodem 123 pro jeho nižší radiační zátěž a získání kvalitnějších snímků. Senzitivita vyšetření pro MTC je poměrně nízká (25 - 40 %), ale při pozitivní akumulaci lze ho využít v terapii, podáním tzv. terapeutického MIBG, což je MIBG značený jodem 131.
S rozvojem moderního přístrojového vybavení, s možností tomografického zpracovávání obrazů, se na pracovištích nukleární medicíny stále častěji setkáváme se scintigrafickou diagnostikou adenomů příštítných tělísek. Rozlišovací schopnost současných gamakamer je kolem 1 cm, takže scintigraficky dokážeme zobrazit pouze zvětšená příštítná tělíska. Alternativou zůstává dobře dostupné sonografické vyšetření, přestože jeho výtěžnost pro lokalizaci adenomu příštítného tělíska nemusí být vždy vysoká. Důvodem může být změněná echogenita příštítného tělíska, popřípadě jeho mediastinální uložení (zejména dolních tělísek), které je pro sonografii prakticky nepřístupné [4]. Rovněž intratyreoidální lokalizace tělíska bývá pro sonografickou diagnostiku obtížná. S výhodou je provedení punkční aspirační biopsie předpokládaného tělíska se stanovením parathormonu v punktátu. Senzitivita sonografického vyšetření je pro adenomy 70-90 %, u hyperplastických tělísek bývá o něco nižší [3].
Jako jedna z výhodných metod pro zobrazení adenomů příštítných tělísek zůstává scintigrafie, která poskytuje informaci nejen o lokalizaci příštítného tělíska, ale i o jeho funkční aktivitě. Používají se metody subtrakční či dvoufázová scintigrafie MIBI.
K subtrakční scintigrafii se užívá nejčastěji 201Tl-chloridu a 123I nebo 99mTc-pertechnetátu. Zatímco se ve tkáních štítné žlázy a příštítných tělísek dobře akumuluje 201Tl-chlorid, radiojod a 99mTc-pertechnetát se akumuluje pouze ve štítné žláze. Odečtem těchto dvou obrazů zůstává akumulace pouze v místě lokalizace adenomu.
V poslední době se nejběžněji využívá, vzhledem k příznivým cenovým relacím, tzv. dvoufázové scintigrafie 99m Tc MIBI. Obraz časného MIBI, které se provádí za 10 min po podání radiofarmaka, ukazuje současnou akumulaci v tyreoidální i paratyreoidální tkáni. Rychlost vyplavení radiofarmaka ze štítné žlázy je vyšší než z adenomatózně změněného příštítného tělíska, takže na záznamu provedeném po 2 hodinách od aplikace radiofarmaka, je ložisková akumulace patrná pouze v příštítném tělísku. Specificita metody je vysoká.
Z ostatních indikací, kdy lze využít znalostí nukleární medicíny, má své místo již jen vyšetření dřeně nadledvin a pozitronová emisní tomografie.
Vyšetření dřeně nadledvin je zaměřeno na detekci feochromocytomu [1]. Vhodným radiofarmakem pro diagnostickou scintigrafii v této indikaci je OctreoScan, popř. 123I - MIBG.
Pozitronová emisní tomografie využívá v klinice nejčastěji radiofarmaka 18F-FDG (fluorodeoxyglukózu). Jde o funkční vyšetření založené na principu zvýšeného vychytávání radiofarmaka v metabolicky aktivních tkáních, které jsou schopny zvýšenou měrou vychytávat, akumulovat a utilizovat glukózu. Pozitivní akumulace FDG v tumoru je závislá na stupni jeho fosforylace, vlastním metabolizmu glukózy a perfuzi v tumoru. V onkologii štítné žlázy existují práce, které ukazují na možnost využití této metody k lokalizační diagnostice uzlinových syndromů na krku a v mediastinu. Zejména se hodí pro diagnostiku a monitorování radiojod nekumulujících tumorů či u hůře diferencovaných karcinomů štítné žlázy.
doc. MUDr. Petr Vlček, CSc.
www.fnmotol.cz
e-mail: petr.vlcek@fnmotol.cz
Doručeno do redakce: 29. 6. 2006
Sources
1. de Herder WW, Kwekkeboom DJ, Valkema R et al. L Neuroendocrine tumors and somatostatin: imaging techniques. J Endocrinol Invest 2005; 28(Suppl 11): 132-136.
2. Pacini F, Schlumberger M, Dralle H et al. European consensus for the management of patients with differentiated thyroid carcinoma of the follicular epithelium. Eur J Endocrinol 2006; 154 : 787-803.
3. Alexandrides TK, Kouloubi K, Vagenakis AG et al. The value of scintigraphy and ultrasonography in the preoperative localization of parathyroid glands in patients with primary hyperparathyroidism and concomitant thyroid disease. Hormones (Athens) 2006; 5 : 42-51.
4. Milas M, Mensah A, Alghoul M at al. The impact of office neck ultrasonography on reducing unnecessary thyroid surgery in patients undergoing parathyroidectomy. Thyroid 2005; 15 : 1055-1059.
5. Kucuk ON, Gultekin SS, Aras G et al. Radioiodine whole-body scans, thyroglobulin levels, 99mTc-MIBI scans and computed tomography: results in patients with lung metastases from differentiated thyroid cancer. Nucl Med Commun 2006; 27 : 261-266.
6. Peixoto Callejo I, Americo Brito J, Zagalo CM et al. Medullary thyroid carcinoma: multivariate analysis of prognostic factors influencing survival. Clin Transl Oncol 2006; 8 : 435-443.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2006 Issue 10-
All articles in this issue
-
Změny v zásobení jodem české dospělé populace po eradikaci jodového deficitu a jejich příčiny
Randomizovaná studie dospělé populace dvou regionů České republiky s odstupem 5 let - Thyroid autoimmunity in adults with diabetes mellitus type 1. Own experience gained by 11-year monitoring
- Iodine and thyroid hormones
- Autoimmune thyroiditis - selected etiopathogenic mechanisms
- Mechanisms of the in-cell activities of the thyroid gland hormones
- Hormonal diseases after traumatic brain injury
- Hashimoto’s encephalopathy
- Congenital adrenal hyperplasia due to 3-β-hydroxysteroid dehydrogenase deficiency
- Subclinical thyreopathies
- Radionuclid screening in endocrinology
- Natural antiglucocorticoids
- Contribution to the discussion about connection between mammary and thyroid gland diseases
- Testosterone and therapy of myasthenia
- Thyroid carcinomas and Hirschsprung’s disease – 10-year experience with molecular genetic testing of the RET proto-oncogene
-
Změny v zásobení jodem české dospělé populace po eradikaci jodového deficitu a jejich příčiny
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hashimoto’s encephalopathy
- Radionuclid screening in endocrinology
- Congenital adrenal hyperplasia due to 3-β-hydroxysteroid dehydrogenase deficiency
- Autoimmune thyroiditis - selected etiopathogenic mechanisms
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career