-
Medical journals
- Career
Ortostatická hypotenzia
: Z. Bartošová; B. Krahulec
: Prednosta: doc. MUDr. Ľudovít Gašpar, CSc. ; II. interná klinika UNB a LFUK, Bratislava
: Prakt. Lék. 2011; 91(9): 517-521
: Reviews
Ortostatická hypotenzia (OH), definovaná ako pokles systolického tlaku krvi o minimálne 20 mm Hg a/alebo diastolického tlaku krvi o najmenej 10 mm Hg do 3 minút po postavení sa alebo pri vyšetrení na tzv. ortostatickom stole (tzv. head-up tillt test), je častým javom v klinickej praxi, zvlášť u staršej populácie. Jej prítomnosť je asociovaná so signifikantne vyššou morbiditou a mortalitou.
Príčiny vzniku OH môžu byť jednak funkčné – napr. ako dôsledok medikácie či pri stavoch hypovolémie, alebo OH vzniká z tzv. neurogénnych príčin pri poškodeniach centrálneho alebo periférneho autonómneho nervového systému s léziami na úrovni aferentných, centrálnych či eferentných dráh regulácie tlaku krvi (TK).
Pacienti s OH môžu byť asymptomatickí alebo sa prezentovať závratmi, presynkopálnymi symptómami či slabosťou so zvýšeným rizikom pádov sprevádzaných synkopou a zhoršením kvality života.
Diagnostika sa opiera o dôkladné vyšetrenie aktívnej alebo pasívnej ortostázy, podrobnú anamnézu s pátraním po iných prejavoch autonómnej neuropatie, so zameraním sa na možný spolupodieľ sekundárnych príčin a o laboratórne a pomocné vyšetrovacie metódy s ohľadom na individuálneho pacienta.
Cieľom liečby je v prípade symptomatických pacientov snaha o zlepšenie kvality života a minimalizáciu symptómov, nie normalizáciu TK, v prvom rade sériou nefarmakologických opatrení za súčasneho odstránenia reverzibilných príčin OH, ako je napr. medikácia zhoršujúca alebo vedúca k OH. V prípade neúspechu nefarmakologickej liečby je na mieste použitie liečby farmakologickej, ako napr. midodrín, 9-α-fluorohydrokortizon, efedrín či nesteroidné antiflogistiká.Kľúčové slová:
ortostatická hypotenzia, funkčné a neurogénne príčiny, autonómna neuropatia, aktívna a pasívna ortostáza.Úvod
Regulácia tlaku krvi a teda aj posturálna homeostáza sú výsledkom komplexných mechanizmov, predominantne funkcie autonómneho nervového systému. Autonómna neuropatia môže viesť k fenoménu známemu ako „ortostatická hypotenzia“ (OH). Môže ísť pritom o idiopatické ochorenie, alebo vzniká ako komplikácia pri iných ochoreniach (1).
OH nevzniká však len z neurogénnych príčin, veľmi často ide o dôsledok funkčný napr. pri intenzívnej medikácii, hypovolémii z rozličných dôvodov, neadekvátnych homeostatických mechanizmoch napr. po gastrektómii, po dlhodobom pobyte na lôžku či v procese stárnutia.
Akákoľvek je už príčina, prítomnosť OH predstavuje pre pacientov závažný zdravotný problém s dopadom na ich kvalitu života, a to nielen zvýšeným rizikom kolapsových stavov, pádov či mozgových cievnych príhod, ale napr. aj limitáciou liečby konkomitantných ochorení, ako je napr. artériová hypertenzia (2) či srdcové zlyhávanie (3).
Problémom je aj prognóza pacientov s OH. Viaceré práce poukazujú na fakt, že OH zvyšuje mortalitu a riziko kardiovaskulárnych príhod u vysoko rizikových pacientov, a to bez závislosti od tradičných rizikových faktorov (4, 5, 6, 7).
Definícia
Ortostatická hypotenzia je podľa medzinárodných odporúčaní definovaná ako pokles systolického tlaku krvi o 20 mm Hg a viac a/alebo súčasne pokles diastolického tlaku krvi o 10 mm Hg a viac počas 3 minút státia alebo počas vyšetrenia na ortostatickom stole (tzv. head-up tilt test). Pri jej vyšetrovaní je pritom dôležité brať do úvahy aj ovplyvňujúce faktory, ako je
- príjem jedla,
- čas počas dňa,
- stav hydratácie,
- okolitú teplotu,
- predošlú polohu v ľahu,
- artériovú hypertenziu,
- užívané lieky,
- pohlavie a vek (8).
V bližšej definícii niektorí autori rozpoznávajú 2 formy OH:
- tzv. iniciálnu ortostatickú hypotenziu, ktorá sa prejaví do 15 sekúnd po postavení ako dôsledok prechodného nepomeru medzi srdcovým výdajom a periférnou cievnou rezistenciou (9), a
- tzv. neskorú ortostatickú hypotenziu po 3 minútach po postavení, ktorá predstavuje miernu alebo skorú formu dysfunkcie sympatikového autonómneho systému (10).
Prevalencia
OH nie je vôbec zriedkavý syndróm – jej prevalencia sa pohybuje v závislosti od charakteristiky pacientov od 5 % u pacientov žijúcich v komunite (11) až po 67 % u pacientov hospitalizovaných na geriatrických oddeleniach (12). Prevalencia sa zvyšuje tiež s vekom, v procese stárnutia dochádza k oslabeniu baroreflexných mechanizmov, zníženej kardiálnej odpovedi na sympatikovú stimuláciu a zníženej kardiálnej compliance (13). Akokoľvek, vek samotný rozhodne nie je dôvod vysvetlenia ortostatickej hypotenzie (14).
Regulácia krvného tlaku
Tlaková a objemová homeostáza je udržiavaná úzkou spoluprácou autonómneho nervového systému (ANS) a renín-angiotenzín-aldosterónového systému (RAAS).
Vazokonstrikcia spôsobená aktiváciou ANS a RAAS je regulovaná cez tzv. baroreflexné systémy s negatívnou spätnou väzbou. Aorto-karotický baroreflexný systém reaguje na akútne zmeny v systolickom TK s následným ovplyvnením ANS - modifikovanej periférnej vazokonstrikcie a srdcového výdaja. Kardio-pulmonálny baroreflexný systém odpovedá na zmeny centrálneho objemu krvi, s ovplyvnením periférnej venokonstrikcie a venózneho návratu za účelom udržania adekvátneho preloadu a vývrhového objemu (15).
V regulácii TK je kľúčový práve arteriálny baroreceptorový oblúk, ktorý zasahuje na úrovni srdca (srdcová frekvencia, kontraktilita) a systémovej cievnej rezistencie (16). Zlyhanie baroreflexného mechanizmu vedie k triáde:
- OH,
- hypertenzia v ľahu a,
- strata diurnálnej variácie TK (17).
Reakcia TK pri postavení sa
Pri postavení sa dochádza u zdravých jedincov v závislosti od ortostatického stresoru k presunu cca pol až litra krvi z intratorakálneho kompartmentu do oblasti brucha a dolných končatín, s najväčším podielom v priebehu prvých 10 s. Úplný presun je dokončený do 3–5 minút. Okrem tohto presunu, dochádza tiež v spomínaných oblastiach k poklesu systémového plazmatického objemu ako dôsledok transkapilárnej filtrácie tekutiny do intersticiálneho priestoru, s objemom až do 700 ml do 10 minút (18). Výsledkom týchto dejov je zníženie venózneho návratu a pokles vývrhového objemu o cca 20 % s následnou redukciou systémového TK.
Odpoveďou organizmu na pokles TK je znížená stimulácia baroreceptorov v karotických sínusoch, aortálnom oblúku a v menšej miere kardiopulmonálnych mechanoreceptorov lokalizovaných v srdcových oddieloch a pľúcach, čo v konečnom dôsledku vedie k oslabeniu vágovej excitácie a zvýšeniu sympatikovej aktivity, a teda
- zvýšeniu venózneho návratu,
- tachykardii,
- zvýšeniu srdcovej kontraktility a vazomotorického artériového tonusu (v splanchnickom a muskulokutánnom riečisku) s cieľom udržať TK v želateľných medziach (19).
Uvedené zmeny sa dejú rýchlo a sú výhradne pod vplyvom intaktného autonómneho nervového systému.
Pri pretrvávaní ortostatického podnetu sa ANS zapája do regulácie TK aj svojou humorálnou zložkou – reguláciou vyplavovania noradrenalínu zo sympatikových ganglií. Dochádza tiež k aktivácii RAAS. Pri blokáde RAAS naberá na dôležitosti úloha vazopresínu – v spojení s ANS. Aktivácia oboch systémov, RAAS i vazopresínového, sa zdá byť dôležitá pre reguláciu TK u stavov s depléciou soli (20).
Príčiny OH
V rámci diferenciálnej diagnostiky a následneho terapeutického ovplyvnenia je nutné rozdeliť príčiny OH na
- funkčné, a
- neurogénne – pri postihnutí centrálneho alebo periférneho ANS.
Pri funkčnom type OH (tab. 1)
1. Funkčné príčiny OH (25, 26) 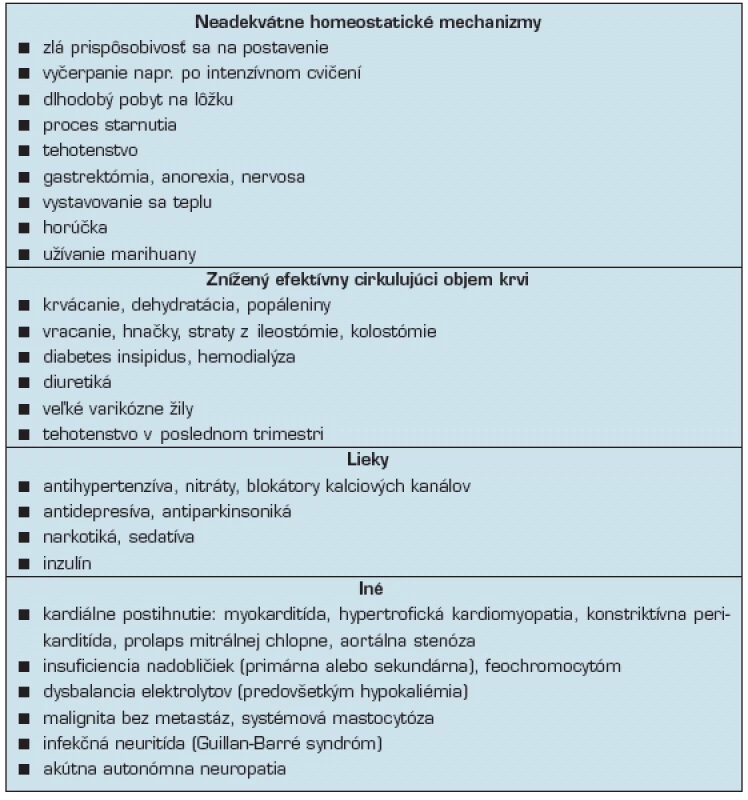
je baroreflexný oblúk nepoškodený, prítomná je normálna alebo zvýšená reakcia noradrenalínu na postavenie. Typicky je sprevádzaná tachykardiou pri postavení (21). Častou príčinou sú stavy deplécie tekutín, stavy po dlhodobom pobyte na lôžku alebo medikamentózna liečba:
- antihypertenzívna (diuretiká, blokátory kalciových kanálov, nitráty, inhibítory enzýmu konvertujúceho angiotenzín),
- psychiatrická (sedatíva, antidepresíva),
- neurologická (antiparkinsoniká).
V prípade funkčných príčin OH je pokles TK zvyčajne dočasný, môžu však vystupňovať závažnosť hypotenzie v prípade, ak je súčasne prítomné aj poškodenie autonómneho nervového systému.
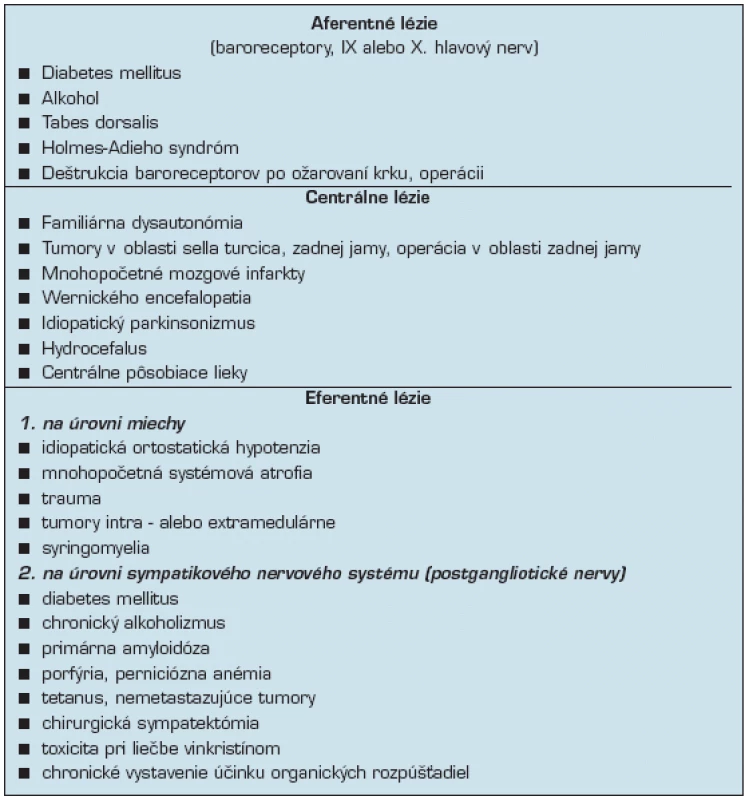
Neurogénna OH (tab. 2)
nastáva pri postihnutí nervového systému s porušením baroreflexného oblúka, s klinickými prejavmi v závislosti od rozsahu a miesta lézie. Vo väčšine prípadov nie je sprevádzaná kompenzačnou tachykardiou, u miernejších foriem dochádza ku zvýšeniu frekvencie, ktorá však nie je dostatočnou na udržanie tlakovej homeostázy (22).
Príčinou neurogénnej OH sú lézie alebo ochorenia centrálneho alebo periférneho ANS s poškodením na úrovni aferentných, centrálnych alebo eferentných dráh baroreflexného oblúka. OH je pritom typickým prejavom postihnutia eferentnej časti ANS (hovoríme o autonómnom zlyhaní) (23), nie je však charakteristickým prejavom izolovaného postihnutia aferentnej časti ANS (známym tiež ako baroreflexné zlyhanie) (29). Neurogénna OH je častokrát doprevádzaná aj autonómnym postihnutím iných systémov – urogenitálneho, gastrointestinálneho, endokrinnými či sudomotorickými abnormalitami.
Medzi primárne autonómne ochorenie asociované s OH patrí napr.
- mnohopočetná systémová atrofia (Shy-Dragerov syndróm),
- idiopatická ortostatická hypotenzia (Bradbury-Egglestonov syndróm),
- Parkinsonova choroba.
Akékoľvek poškodenie na úrovni predĺženej miechy môže byť doprevádzané ortostatickou hypotenciou. OH je tiež častým nálezom u ochorení s periférnou neuropatiou, ako je tomu napr. pri
- diabetes mellitus,
- amyloidóze,
- imunitne podmienených neuropatiách,
- hereditárnych senzorických, a
- autonómnych neuropatiách (napr. familiárna dysautonómia), porfýrii či alkoholizme (22, 25).
Klinická manifestácia
Posturálna hypotenzia sa manifestuje pod obrazom rozličných symptómov, ktoré sa objavujú pri postavení a zmierňujú pri posadení alebo ľahnutí. Charakteristickými symptómami sú
- zahmlievanie pred očami,
- závraty,
- presynkopálne stavy až synkopy pri postavení sa.
Môže sa však prezentovať aj nešpecificky pod obrazom
- celkovej slabosti,
- únavy,
- nauzey,
- ťažkosťami rozmýšľať jasne, či
- bolesťami hlavy.
Na bolesti krku v paracervikálnej a subokcipitálnej oblasti a v oblasti trapéziových svalov (tzv. „vešiaková“ bolesť) sa sťažuje cca 20 % pacientov. Poruchy pamäte pri státí, ktoré vymiznú pri sadnutí alebo ľahnutí boli dokumentované u približne 50 % pacientov s vekom nad 60 rokov (27). Pacienti tiež udávajú ortostatické dyspnoe (predpokladá sa, že ide o ventilačno-perfúzny nepomer neadekvátnej perfúzie ventilovaných častí pľúc) alebo anginózne bolesti (ako dôsledok porušenej perfúzie myokardu aj u pacientov s normálnymi koronárnymi artériami) (22).
U niektorých pacientov závažnosť ortostatických symtómov nekoreluje s poklesom TK, pravdepodobne vďaka dobrej cerebrálnej autoregulácii. Takisto je zaujímavé pozorovanie, že z pacientov, ktorí sú vysoko symptomatickí, u viac ako 75 % nedochádza ku synkope. Podobne ide zrejme o výsledok dobrých kompenzačných mechanizmov, alebo tzv. alarmujúcich systémov, ktorými synkopám predchádzajú (28).
Z funkčného hľadiska možno teda OH rozdeliť na
- asymptomatickú,
- symptomatickú bez anamnézy synkopy,
- symptomatickú spojenú so synkopou a asociovanú s častými synkopami, alebo
- symptomatickú spojenú závažnými symptómami výrazne zasahujúcimi do kvality života pacienta (tab. 3)
3. Funkčná klasifikácia ortostatickej hypotenzie (29) 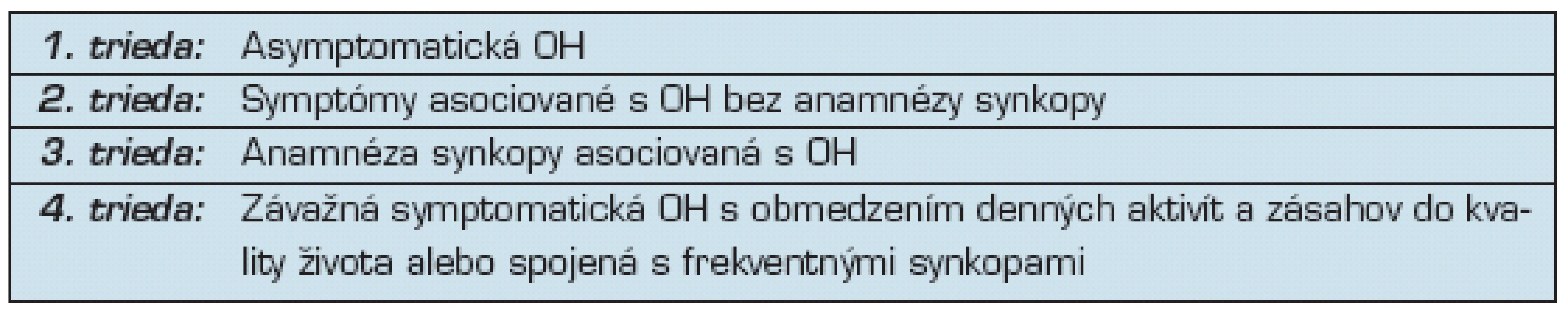
Stupeň OH je závislý od rady faktorov, ako je napr.
- rýchlosť postavenia sa,
- čas počas dňa so zhoršením v ranných hodinách,
- imobilita, či predĺžený pobyt na lôžku,
- zvýšený intratorakálny tlak, ako je tomu napr. pri močení, defekácii alebo kašli.
Symtómy sa môžu zhoršovať konzumáciou jedla, námahou, pri dlhom státí, či v teplom počasí. Užívanie vazodilatačných liekov môže zvýrazniť hypotenziu v prípade baroreflexového deficitu. Priťažujúcim faktorom, ktorý zvyšuje náchylnosť k cerebrálnej ischémii, je prítomnosť cievneho ochorenia, ako je to napr. u pacientov so stenózou karotickej artérie. Do úvahy treba brať i funkčné príčiny OH, ktoré v prípade autonómnej dysfunkcie prispievajú k zvýrazneniu hypotenzie (26).
Diagnostika
Pri hodnotení OH je nutné zamerať sa na možný podiel funkčných príčin ako je napr.
- dehydratácia,
- hypovolémia,
- medikácia,
- ochorenie srdca so zníženým srdcovým výdajom, či
- endokrinné ochorenia.
Anamnesticky cielene pátrame po možných iných prejavoch autonómnej neuropatie, ako je
- impotencia,
- dysfágia, poruchy motility v zmysle hnačiek alebo obstipácie,
- porušená potivosť,
- prejavoch cereberálnej ataxie či parkinsonizmu,
- prítomnosti periférnej neuropatie.
Rozsah laboratórnej diagnostiky sa odvíja od individuálneho pacienta. Laboratórny skríning by v závislosti od suponovaného ochorenia mal obsahovať vyšetrenie glykémie nalačno, ionogramu, renálnych parametrov, albumínu, krvného obrazu, imunoelektroforézy bielkovín v sére a v moči, vitamínu B12, kortizolového profilu, plazmatickej renínovej aktivity a aldosterónu.
Pomocné zobrazovacie metódy, ako napr. RTG hrudníka indikujeme pri podozrení na bronchogénny karcinóm pľúc, elektrokardiogram by mal byť štandardnou súčasťou vyšetrenia u každého pacienta. V prípade, že je suponované ochorenie CNS, je na mieste zrealizovať CT alebo MR vyšetrenie mozgu. U primárnych autonómnych degeneratívnych ochoreniach sa pri nejasnostiach doporučuje MR mozgu a rádionuklidové SPECT (single photon emission tomography) vyšetrenie srdca so sympatomimetickým amínom 123I-metaiodobenzylguanidine (MIBG). EMG vyšetrenie je vhodné doplniť pre určenie prípadnej periférnej neuropatie (29, 30).
Objektívna diagnostika OH sa opiera o vyšetrenie aktívnej ortostázy s meraním TK a pulzovej frekvencie do 3 minút v stoji a/alebo pasívnej ortostázy vyšetrením na ortostatickom stole počas 45 minút v 60-ti stupňovom uhle (tzv. head-up tilt test). Tachykardia v ľahu alebo absencia zvýšenia pulzovej frekvencie v stoji v prítomnosti hypotenzie poukazuje na možnú autonómnu neuropatiu a vyžaduje si komplexnejšie vyšetrenie (14).
Porušenú funkciu baroreflexného oblúku možno objektivizovať tzv. Ewingovou batériou kardiovaskulárnych testov, ktorej využitie je primárne v diagnostike kardiovaskulárnej autonómnej neuropatie u diabetikov. Ide o sériu testov, ktorými na základe analýzy odpovede TK a srdcovej frekvencie hodnotíme funkciu eferentných dráh parasympatikovej a sympatikovej vetvy ANS. Zahŕňa vyšetrenie variability frekvencie srdca pri hlbokom dýchaní a pri Valsalvovom mánevri ako funkčné hodnotenie parasympatikového nervového systému a vyšetrenie reakcie systolického TK pri Valsalvovom manévri a aktívnej ortostáze a diastolického TK na izometrický handgrip v rámci hodnotenia funkcie sympatikového nervového systému (31).
Terapia
Základným cieľom liečby OH je snaha o zlepšenie ortostatického TK bez nadmerného zvýšenia TK v ľahu, minimalizáciu symptómov OH a celkové zlepšenie pacientových možností vykonávať bežné denné aktivity. Vhodná liečba si preto vyžaduje presnú diagnózu, identifikáciu a úpravu reverzibilných príčin.
Non-farmakoterapia
Iniciálna terapia spočíva v dôkladnej edukácii pacienta o možných príčinách a možnostiach predchádzania hypotenzii. Pacient by sa mal vyhýbať nadmernému ležaniu, náhlej zmene polohy, a to predovšetkým v ranných hodinách po prebudení sa, kedy je ortostatická tolerancia najnižšia, ako dôsledok zvýšenej natriurézy počas noci. Doporučené je spať preto na mierne zdvihnutej posteli. Redukuje to jednak nyktúriu, pravdepodobne stimuláciou vyplavovania renínu, a tiež znižuje hypertenziu v ľahu. Opakovaním tohto úkonu možno dosiahnuť postupné zmiernenie OH. Ide zrejme o výsledok uvoľňovania renínu a vazopresínu, k čomu je potrebný predĺžený alebo opakovaný ortostatický stresor (8).
U niektorých pacientov sa javí vhodné používanie kompresných pančúch, ktoré znižujú hromadenie venóznej krvi v dolných končatinách a splanchnickom riečisku. Nápomocné sa javí aj použitie brušného pásu s aplikáciou tlaku 20 mm Hg (32).
Doporučené je cvičenie s cieľom aktivovať svalovú silu dolných končatín. Ako vhodné sa javia cvičenia v ležiacej alebo sediacej polohe. Používajú sa tiež fyzikálne kontra-manévre, ktorých cieľom je zvýšiť venózny návrat kontrakciou určitých svalových skupín dolných končatín a tak predĺžiť čas v stoji. Zahŕňajú
- prekríženie dolných končatín,
- pomalé kráčanie na mieste,
- podrep,
- opieranie sa nohou o stoličku,
- sťahovanie stehenných svalov (20).
Nefarmakologická terapia zahŕňa tiež zvýšenie príjmu soli a vody. Pacienti s autonómnym zlyhaním sú veľmi citliví na čo i len malé zmeny v krvnom objeme a mali by byť preto poučení vyhýbať sa čo i najmiernejšej dehydratácii. Suplementácia soli je v prípade nutnosti okrem bežného dosoľovania možná i tabletkami. Vhodné je odsledovať si účinok tejto liečby meraním 24 hodinového objemu moča a koncentrácie sodíka v moči.
Nápomocná sa tiež ukázala liečba bolusom vody, ktorá vedie k vzostupu systolického TK o viac ako 30 mm Hg do 5 minút po rýchlom vypití cca 2 pohárov vody s maximom účinku do 20–30 minút a trvaní až do hodiny. Je výsledkom sympatikovej adrenergnej aktivácie, so zvýšením hladiny plazmatického noradrenalínu. Z praktického hľadiska je tento spôsob využiteľný napr. pred plánovaným ortostatickým podnetom (8, 33).
Konzumácia jedla môže viesť k prehĺbeniu OH, doporučuje sa preto konzumovať malé dávky a často, vynechať alkohol a vyhýbať sa náhlemu vstávaniu a fyzickej aktivite bezprostredne po jedle. Je vhodné pacientov upozorniť aj na vyvarovanie sa namáhaniu pri močení a defekácii, ako i horúcim teplotným podmienkam – vrátane horúcich kúpeľov. Samozrejmosťou je tiež vynechanie alebo redukcia liekov s hypotenznými účinkami (34).
Farmakoterapia
Je indikovaná u pacientov, kde nie je dosiahnutá kontrola symptómov nefarmakologickou cestou, nie za účelom dosiahnutia normotenzie.
9-α-Fluorohydrokortizon.
Tento syntetický minelarokortikoid je liekom prvej voľby u pacientov s OH, u ktorých nedochádza k adekvátnemu zvýšeniu plazmatického objemu pri zvýšení prísunu vody a soli. Potenciálnou limitáciou tejto liečby je pri dávkach vyšších ako 0,4 mg/deň možnosť vývoja kongestívneho srdcového zlyhávania a nadmernej hypertenzie v ľahu (34, 35).
Ďalšou skupinou sú vazokonstrikčné látky.
Midodrín
je periférne účinkujúci selektívny α1 adrenergný agonista, vedúci k vazokonstrikcii ako v arteriálnom, tak venóznom riečisku. Signifikantne zvyšuje TK, čas v stoji, a zmierňuje klinické symptómy OH. V Spojených Štátoch Amerických (USA) je jediným liekom schváleným Úradom pre liečivá (Food and Drug Administration – FDA) v liečbe OH (36). Z ďalších liekov sú to napr. kombinované α-adrenergní agonisti, efedrín a pseudoefedrín, ich účinok sa však v liečbe OH ukázal byť v porovnaní s midodrínom horší (37). Obzvlášť výhodné pri OH a súčasnej hypertenzii v ľahu sa javí použitie β-antagonistov s vnútornou sympatikomimetickou aktivitou, napr. pindololu. Určitú kontrolu hypertenzie v ľahu prináša užitie nifedipinu alebo hydralazínu pred spaním.
U pacientov s OH a normocytárnou normochrómnou anémiou, ktorá je často asociovaná s autonómnym zlyhaním (ako dôsledok renálnej denervácie), je preferovaná liečba erytropoetínom (38).
Ďalšie liečebné možnosti ponúka napr.
- pyridostigmín,
- klonidín,
- somatostatín,
- dihydroergotamín,
- dopamínoví antagonisti či
- inhibítory cyklooxygenázy, napr. indometacin.
MUDr. Zuzana Bartošová
II. interná klinika LFUK
a UNB, Bratislava
Mickiewiczova 13
813 69 Bratislava
E-mail: zuzana.bartosova1@gmail.com
Sources
1. Ziegler, M. Postural hypotension. Annu. Rev. Med. 1980, 31, p. 239-245
2. Krahulec, B., Bartošová, Z. Artériová hypertenzia spojená s ortostatickou hypotenziou. Vnitř. Lék. 2010, 56(9), p. 951-954.
3. Weber, M.A., Wenger, N.K., Scheidt, S. Focus on heart failure and other age-related cardiovascular conditions. Am. J. Geriatr. Cardiol. 2005, 14 p. 221-223.
4. Fedorowski, A., Stavenow, L., Hedblad, B. et al. Orthostatic hypotension predicts all-cause mortality and coronary events in middle-aged individuals (The Malmo Preventive Project) European Heart Journal 2010, 31, p. 85-91
5. Gupta, V., Lipsitz, L.A. Orthostatic hypotension in the elderly: diagnosis and treatment. Am. J. Med. 2007, 120(10), p. 841-847.
6. Raiha, I., Luutonen, S., Piha, J. et al. Prevalence, predisposing factors and prognostic importance of postural hypotension. Arch. Intern. Med. 1995, 155 p. 930-935.
7. Luukinen. H-, Koski. K-, Laippala. P., Airaksinen. K.E. Orthostatic hypotension and the risk of myocardial infarction in the home-dwelling elderly. J. Intern. Med. 2004, 255, p. 486-493.
8. Low, P.A. Postural hypotension and anhidrosis. In: Veves A, Malik R. Contemporary Diabetes: Diabetic Neuropathy: Clinical Management. Totowa, New York, Humana Press Inc., 2007, p. 413-432.
9. Wieling, W., Krediet, C.T., van Dijk, N. et al. Initial orthostatic hypotension: review of a forgotten condition. Clin. Sci. (Lond) 2007, 112, p. 157-65.
10. Gibbons, C.H., Freeman, R. Delayed orthostatic hypotension: a frequent cause of orthostatic intolerance. Neurology 2006, 67, p. 28-32.
11. Mader, S.L., Josephson, K.R., Rubenstein, L.Z. Low prevalence of orthostatic hypotension among community-dwelling elderly. JAMA 1987, 258, p. 1511-1514.
12. Weiss, A., Grossman, E., Beloosesky, Y., Grinblat, J. Orthostatic hypotension in acute geriatric ward: is it a consistent finding? Arch. Intern. Med. 2002, 162, p. 2369–2374.
13. Lipsitz, L.A. Orthostatic hypotension in elderly. N. Engl. J. Med. 1989, 321, p. 952-957.
14. Mader, S.L. Orthostatic hypotension. Geriatric Medicine 1989, 73(6), p. 1337-1349.
15. Izzo, J.L., Taylor, A.A. The sympathetic nervous system and baroreflexes in hypertension and hypotension. Current Hypertension Reports 1999, 3, p. 254-263.
16. Eckberg, D.L., Sleight, P. (1992). Human baroreflexes in health and disease. Oxford University Press, Oxford.
17. Carvalho, M.J., van Den Meiracker, A.H., Boomsma, F. et al. Diurnal blood pressure variation in progressive autonomic failure. Hypertension 2000, 35, p. 892-897.
18. Smit, A.A.J., Halliwill, J.R., Low, P.A. et al. Pathophysiological basis of orthostatic hypotension in autonomic failure. Journal of Physiology 1999, 519, p. 1-10.
19. Wieling, W., Karemaker, J.M. Measurement of heart rate and blood pressure to evaluate disturbances in neurocardiovascular control. In: Mathias CJ, Bannister R. Autonomic failure. New York, Oxford University Press, 1999.
20. Sancho, J.R., Burton, J., Barger, A.C. & Haber, E. The role of the renin-angiotensin-aldosterone system in cardiovascular homeostasis in normal human subjects. Circulation 1976, 53, p. 400–405.
21. Cryer, P.E., Silverberg, A.B., Santiago, J.V. et al. Plasma catecholamines in diabetes: the syndromes of hypoadrenergic and hyperadrenergic postural hypotension. Am. J. Med. 1978, 64, p. 407-416.
22. Freeman, R. Neurogenic Orthostatic Hypotension. New England Journal of Medicine 2008, 358, p. 615-624.
23. Bradbury, S., Eggleston, C. Postural hypotension: a report of three cases. Am. Heart J. 1925, 1, p. 73-86.
24. Robertson, D., Hollister, A.S., Biaggioni, I. et al. The diagnosis and treatment of baroreflex failure. N. Engl. J. Med. 1993, 329, p. 1449-1455.
25. Schatz, I.J. Orthostatic hypotension. Functional and Neurogenic Causes. Arch. Intern. Med. 1984, 144, p. 773-777.
26. Mathias, C.J., Bannister, R. Investigation of autonomic disorders. In: Mathias CJ, Bannister R. Autonomic failure. New York, Oxford University Press, 1999.
27. Low, P.A, Opfer-Gehrking, T.L., McPhee, B.R. Prospective evaluation of clinical characteristics of orthostatic hypotension. Mayo Clin. Proc. 1995, 70, p. 617-622.
28. Low, P.A. Postural hypotension and anhidrosis. In: Veves A, Malik R. Contemporary Diabetes: Diabetic Neuropathy: Clinical Management. Totowa, New York, Humana Press Inc., 2007, p. 413-432.
29. Kochar, M.S. Management of postural hypotension. Curr. Hypert. Reports 2000, 2, p. 457-462.
30. Schatz, I.J. Orthostatic hypotension: Clinical diagnosis, testing and treatment. Arch. Int. Med. 1984, 144, p. 1037-1041.
31. Bannister, R., Mathias, C.J. Management of postural hypotension. In: Mathias CJ, Bannister, R. Autonomic failure. New York, Oxford University Press, 1999.
32. Low, P.A., Singer, W. Update on management of neurogenic orthostatic hypotension. Lancet Neurol. 2008, 7, p. 451-458.
33. Gupta, V., Lispitz, L.A. Orthostatic hypotension in the elderly: diagnosis and treatment. A. J. Med. 2007, 120, p. 841-847.
34. Low, P.A., Singer W. Update on management of neurogenic orthostatic hypotension. Lancet Neurol 2008, 7, p. 451-458.
35. Low, P.A., Gilden, J.L., Freeman, R. et al. Efficacy of midodrine vs placebo in neurogenic orthostatic hypotension: a randomized, double-blind multicenter study. JAMA 1997, 277, p. 1046-1051.
36. Fouad-Tarazi, F.M., Okabe, M., Goren, H. Alpha sympathomimetic treatment of autonomic insufficiency with orthostatic hypotension. Am. J. Med. 1995, 99, p. 604-610.
37. Hoeldtke, R.D., Streeten DH. Treatment of orthostatic hypotension with erytropoetin. N. Engl. J. Med. 1993, 329, p. 611-615.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2011 Issue 9-
All articles in this issue
- Demodicidosis
- Glomus tumour of a finger
- One hunfred years of allergen immunotherapy, first year in the form of sublingual tablets
-
Základy kognitivní, afektivní a sociální neurovědy
IX. Altruismus - Primary prevention of cancer
- Orthostatic hypotension
- Continuing Education of General Practitioners and new Czech Medical Chamber rules
-
Program Zdraví 2020
Budoucnost evropské zdravotní politiky - A view of young Czech practotioners on vocational training – research questionnaire
- Interaction of alcohol and other drugs: a serious problem
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Orthostatic hypotension
- Glomus tumour of a finger
- Demodicidosis
- Interaction of alcohol and other drugs: a serious problem
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career