-
Medical journals
- Career
Subakutní trombóza dvou stentů jako příčina akutního infarktu myokardu
Authors: F. Roháč; L. Lisá; P. Toušek
Authors‘ workplace: Univerzity Karlovy, Praha ; Přednosta: Prof. MUDr. Petr Widimský, DrSc., FESC. ; III. Interní-kardiologická klinika Fakultní nemocnice Královské Vinohrady a 3. lékařská fakulta
Published in: Prakt. Lék. 2009; 89(1): 40-42
Category: Case Report
Overview
V této kazuistice je popsán případ pacienta s akutní manifestací ischemické choroby srdeční v podobě akutního infarktu myokardu (IM) bez elevací ST. Dnes nejčastějším způsobem léčby akutního IM je koronární intervence s implantací stentu. Během implantace stentu a po ní se užívá ke snížení rizika trombózy stentu duální antiagregační léčba – kyselina acetylsalicylová a thienopyridinový derivát (clopidogrel, ticlopidin). Vysazení této léčby v časném období po implantaci stentu toto riziko enormně zvyšuje. Nejčastěji užívaný thienopydinový derivát clopidogrel vyžaduje finanční spoluúčast pacienta, která do nedávné doby byla poměrně vysoká. Z tohoto důvodu může mít snaha některých pacientů zkrátit dobu této léčby velmi nepříznivé následky.
Klíčová slova:
koronární stent, trombóza stentu, koronární angioplastika.Trombóza koronárního stentu se vyskytuje poměrně zřídka. Z časového hlediska ji rozlišujeme na akutní (do 24 hodin od koronární intervence), subakutní (24 hodin až 30 dní), pozdní (30 dní až 1 rok) a velmi pozdní (více než 1 rok) (1). Přestože je incidence koronární trombózy velmi nízká (okolo 1 %), klinické důsledky jsou velmi závažné (1, 2). Jejím projevem bývá rozsáhlý infarkt myokardu, nebo náhlá srdeční smrt. Proto je nutné znát její rizikové faktory, a pokud možno je minimalizovat.
Vlastní pozorování
Padesáti devítiletý pacient byl odeslán ke koronarografii z regionální nemocnice pro diagnózu akutního infarktu myokardu (IM) spodní stěny bez elevací ST. Pacient měl již v anamnéze non Q infarkt přední stěny, byl po ischemické cévní mozkové příhodě (CMP) a jednalo se o aktivního kuřáka. Při přijetí byly na EKG patrny deprese ST úseku ve svodech V2-V5.
V laboratoři byly zjištěny kardiospecifické enzymy, ostatní laboratorní nálezy byly v normě.
Echokardiografií byla zjištěna akineza distální části přední stěny a hrotu, hypokineza spodní stěny s ejekční frakce levé komory 40 %.
Koronarografie prokázala nemoc 3 tepen s chronickýmuzávěrem ramus interventricularis anterior (RIA), významnou 80% stenózu marginální tepny (RMS) a kritickou stenózu 95% na difuzně sklerotické pravé koronární tepně (ACD), kde byl patrný horší angiografický průtok (obr. 1).
Image 1. V levé části obrázku (A) je zobrazená pravá koronární tepna s významnými stenózami v její proximální a střední části (šipky). V pravé části obrázku (B) je patrný dobrý efekt po implantaci intrakoronárních stentů. 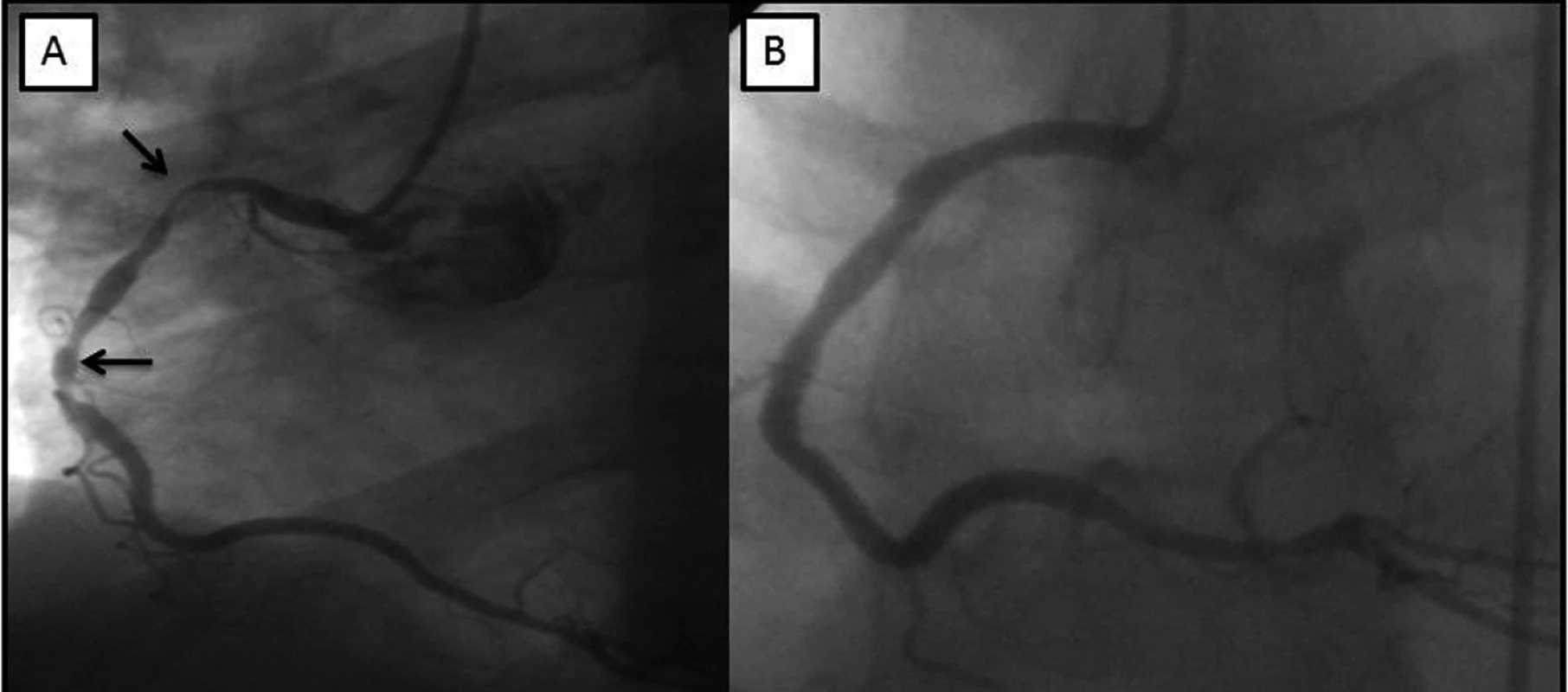
V návaznosti na koronarografii byla provedena koronární intervence (PCI) s implantací stentu dlouhé kritické stenózy ACD (3 kovové stenty průměru 4.0 mm, délek 19, 25 a 13 mm). V druhé době jsme provedli PCI se stentem stenózy RMS (kovový stent 3.5/13 mm) (obr. 2). Angiografický efekt obou koronárních intervencí byl dobrý. Pacient byl ve zcela stabilizovaném stavu propuštěn 4. den hospitalizace. Bylo mu doporučeno trvalé užívání 100 mg Anopyrinu a 75 mg clopidogrelu denně po dobu 6–12 měsíců. Vzhledem k tíživé finanční situaci však pacient užíval pacient clopidogrel pouze 7 dní od propuštění z nemocnice.
Image 2. V části A angiograficky patrná významná stenóza marginální tepny (šipka), v levé části obrázku stav po implantaci stentu s optimálním konečným výsledkem. 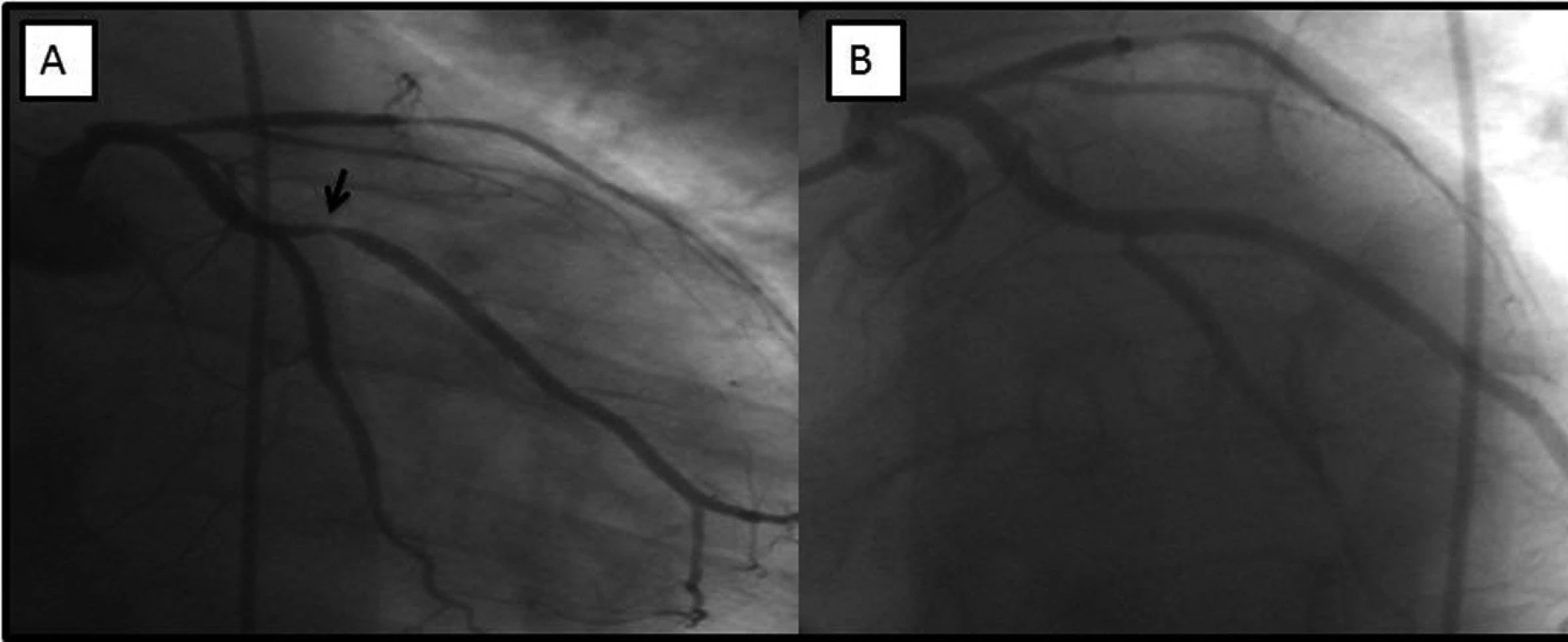
Znovu byl přivezen RZP na naší kliniku o 14 dní později po proběhlé synkopě s pádem, úderem do hlavy a s bolestí na hrudi. Na EKG byly patrny ST elevace na spodní stěně, deprese ST v hrudních svodech. Pacient jevil známky kardiogenního šoku, byl při vědomí. Byla provedena urgentní rekoronarografie, která prokázala trombotické uzávěry v recentně implantovaných stentech v ACD a RMS. Na obou trombotických uzávěrech byla provedena balónková angioplastika (PTCA). Během výkonu byl podán inhibitor glykoproteinu IIb/IIIa (abciximab) (obr. 3).
Image 3. V levé části (A) zobrazena trombóza začínající v proximálním okraji implantovaných stentů (šipka) s úplnou okluzí tepny. V části B patrná trombóza marginální tepny v místě implantovaného stentu (šipka). 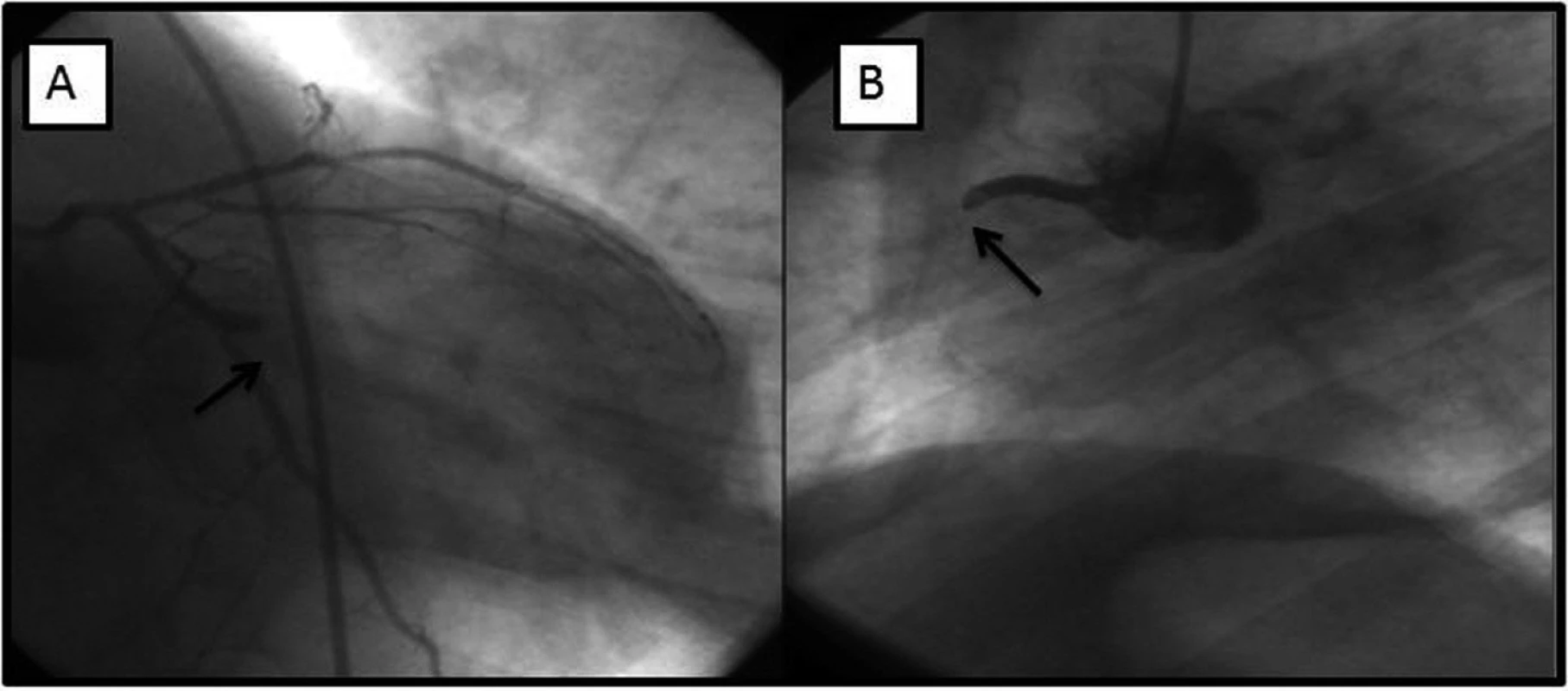
Po PTCA byl obnoven průtok oběma tepnami a pacienta se podařilo hemodynamicky stabilizovat. Několik hodin po výkonu došlo k rozvoji kvantitativní poruchy vědomí (somnolence). Provedli jsme CT mozku, které prokázalo intracerebrální hemorhagii (ložisko ve frontálním laloku vpravo, drobné ložisko i frontopolárně vlevo a subarachnoidálně frontolaterálně vpravo). Vzhledem k tomu, že nedošlo k další progresi neurologického stavu a recentnímu podání antikoagulační a antiagregační léčby byl neurochirurgem indikován konzervativní postup.
Po zotavení byl pacient bez omezení hybnosti, bradypsychický, s parézou pohledu doleva, jevil známky prefrontálního syndromu a za 14 dní byl přeložen na lůžko následné péče k další rehabilitaci.
Diskuse
V naší kazuistice popisujeme případ pacienta, u kterého vznikla krátce po implantaci intrakoronárních stentů trombóza stentů v důsledků špatné compliance léčby. Důsledkem této komplikace byl akutní infakt myokardu s incipientním kardiogenním šokem a nutností elektrické defibrilace pro fibrilaci komor v úvodu. Následná agresivní antikoagulační a antiagreagregační léčba v kombinaci s traumatem hlavy vedla k intracebrálnímu krvácení, které se podařilo konzervativně zvládnout.
Špatná compliance léčby, v našem případě vysazení duální antiagregační léčby, je pouze jedou z příčin trombózy intrakoronárního stentu. Mezi další rizikové faktory trombózy stentu patří farmakorezistence k antiagregační léčbě, technické periprocedurální komplikace při implantaci stentu (disekce koronární tepny, nedostatečná apozice stentu ke stěně cévy, špatné rozvinutí stentu) a z klinických rizikových faktorů se pak jedná především o pacienty s diabetes mellitus, s renálním selháním a vyšším věkem (3, 4, 5, 6).
Technické komplikace při implantaci stentu většinou dokáže intervenční kardiolog během výkonu rozpoznat a výkon dokončit tak, aby riziko trombózy bylo co nejmenší (implantace dalšího stentu pro disekci, postdilatace vysokotlakými balonky při špatném rozvinutí stentu, intravaskulární kontrola apozice stentu, atd.).
Vyhledání farmakorezistentních pacientů k antiagregační léčbě a stanovení reaktivity destiček umožňují nejnovější laboratorní metody (VerifyNow, VASP). Na základě výsledku lze pak navýšit antiagregační léčbu. Zatím se však rutinně v klinické praxi nepoužívají a jejich přínos musí prokázat větší klinické studie.
Asi nejvášnivější debata na poli intervenční kardiologie v posledních 2 letech se vedla o riziku trombózy lékových stentů. Nejčastěji používané lékové stenty obsahují látku sirolimus či paclitaxel, jejíž postupné uvolňování zabraňuje neoproliferalici a snižuje tak incidenci restenóz s nutností dalších revaskularizací. Po jejich zavedení do klinické praxe v roce 2002 tak vypukla velká euforie, kdy v některých zemích byly implantovany až v 90 % případů. Tato euforie byla následována obavami intervenčních kardiologů z trombózy lékových stentů, poté co byla představena data na kongresu Evropské kardiologické společnosti v roce 2006.
Za poslední 2 roky pak byla provedena řada metaanalýz studií srovnávající bezpečnost lékových (DES) a „normálních“ kovových stentů (BMS) až 5 let po jejich implantaci. Závěrem těchto prací je, že lékové stenty nezvyšují celkovou mortalitu, incidenci infarktu myokardu ani celkové riziko trombózy stentu (trombóza DES 0,9–1,4 % , trombóza BMS 0,6–1,3 %) (7). Nicméně riziko velmi pozdní trombózy DES (více než rok po implantaci) se zdá být vyšší než u BMS (7). Je to dáno především pomalou endotelizací DES. Proto se po implantaci DES doporučuje podávání duální antiagregační léčby po dobu 6–12 měsíců, ideální doba však není známa.
Závěr
Subakutní (24hodin–30. den od intervence) trombóza koronárního stentu se vyskytuje vzácně (kolem 1 %) a neliší se významněji mezi kovovými stenty a lékovými stenty. Nicméně v případě nutnosti vysadit duální antiagregační terapii riziko trombózy v tomto vulnerabilním období dramaticky zvyšuje. Nutno uvážit také complianci pacienta k terapii s finanční spoluúčastí při užívání clopidogrelu, která byla příčinnou trombózy stentů v této kazuistice.
MUDr. Filip Roháč
III. interní-kardiologická klinika
Fakultní nemocnice
Královské Vinohrady
Šrobárova 50
100 34 Praha 10
E-mail: filip.rohac@seznam.cz
Sources
1. Kuchulakanti, P.K., Chu, W.W., Torguson, R. et al. Correlates and long-term outcomes of angiographically proven stent thrombosis with sirolimus - and paclitaxel-eluting stents. Circulation 2006, 113, p. 1108-1113.
2. Airoldi, F., Colombo, A., Morici, N. et al. Incidence and predictors of drug-eluting stent thrombosis during after discontinuation of thienopyridine treatement. Circulation 2007, 116, p. 745-754.
3. Mauri, L., Hsieh, W.H., Massaro, J.M. et al. Stent thrombosis in randomized clinical trials of drug-eluting stents. NEJM 2007, 356, p. 1020-1029.
4. Roiron, C., Sanchez, P., Bouzamondo, A. et al. Drug-eluting stents: an updated metaanalysis of randomized controlled trials. Heart, 2006, 92, p. 641-649.
5. Machecourt, J., Danchin, N., Lablanche, J.M. et al. Risk factors for stent thrombosis after implantation of sirolimus-eluting stents in diabetic and nondiabetic patients: the EVASTENT matched-cohort registry. J. Am. Coll. Cardiol. 2007, 50, p. 501-508.
6. Cheneau, E., Leborgne, L., Mintz, G.S. et al. Predictors of subacute stent thrombosis. Circulation 2003, 108, p. 43-47.
7. Bavry, A.A., Bhatt, D.L. Appropriate use of drug-eluting stents: balancing the reduction in restenosis with the concern of late thrombosis. Lancet 2008, 371, p. 2134-2143.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2009 Issue 1-
All articles in this issue
- Postoj k dispenzarizaci a zvládání stresu u pacientů dlouhodobě sledovaných pro diagnózu melanom
- Procesy globalizace a harmonizace práce etických komisí v EU
- Léčba chronických ran u seniorů pod vedením geriatra
- Subakutní trombóza dvou stentů jako příčina akutního infarktu myokardu
- Posuzování změn ledvinové funkce na podkladě sérových koncentrací kreatininu – možnosti a omezení
- Identita etických komisí, identita členů etických komisí
- Očkování proti karcinomu hrdla děložního a dalším projevům HPV infekce
- Současné možnosti péče o pacienty s epilepsií
- Regulační T lymfocyty a jejich význam pro zhoubné novotvary hlavy a krku
- Péče o výživu nedonošeného novorozence po propuštění z nemocnice
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Léčba chronických ran u seniorů pod vedením geriatra
- Péče o výživu nedonošeného novorozence po propuštění z nemocnice
- Současné možnosti péče o pacienty s epilepsií
- Subakutní trombóza dvou stentů jako příčina akutního infarktu myokardu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

