-
Medical journals
- Career
Diabetická retinopatia 2: Liečba diabetickej retinopatie a diabetického edému makuly
Authors: Mária Molnárová
Authors‘ workplace: II. očná klinika SZU, NsP F. D. Roosevelta, Banská Bystrica
Published in: Forum Diab 2012; 1(2-3): 97-103
Category:
Overview
Liečba diabetickej retinopatie (DR) a diabetického edému makuly (DEM) vychádza z nových poznatkov v etiopatogenéze ochorenia. Liečba DR a DEM má dve úrovne: 1. dobrá kontrola glykémie, čo potvrdili svojimi závermi klinické štúdie Wisconsin Epidemiologic Study of Diabetic Retinopathy, Diabetes Control and Complications Trial, Diabetes Intervention and Complications Study a United Kingdom Prospective Diabetes Study, 2. vlastná liečba DEM a DR, ktorá môže byť laserová, intravitreálna farmakologická alebo chirurgická. Klinické štúdie ETDRS, DRS, DRCR.net, RESTORE, RESOLVE, READ 1, READ 2, Macugen Diabetic Retinopathy Study Group a Da Vinci dokázali, že centrálna zraková ostrosť sa liečbou DR a DEM laserkoaguláciou stabilizuje, pri intravitreálnej liečbe sa môže až u 50 % pacientov výrazne zlepšiť.
Kľúčové slová:
diabetická retinopatia – diabetický edém makuly – dobrá kontrola glykémie – laserová liečba – intravitreálna farmakologická liečba – chirurgická liečbaÚvod
Nové vedecké poznatky v etiopatogenéze diabetickej retinopatie (DR) a diabetického edému makuly (DEM) viedli k novým a efektívnejším možnostiam ich liečby. DR je mikroangiopatia, ktorá je výsledkom aldozoreduktázovej shuntovej cesty metabolizmu glukózy, formácie neskorých produktov glykácie, aktivácie beta izoformy protein-kinázy C, indukcie cievneho endotelového faktora (vascular endothelial grow factor – VEGF), oxidatívneho poškodenia a zápalu [1].
Liečba DR a DEM má v zásade dve úrovne: kontrolu glykémie a vlastnú liečbu DEM a DR, ktorá môže byť laserová, intravitreálna farmakologická alebo chirurgická.
Vzťah glykémie a diabetickej retinopatie
Glykémia má silný vplyv na mnohé indexy DR, ako sú prevalencia, incidencia, vznik a progresia retinopatie, čo vyžaduje fokálnu alebo panretinálnu laserkoaguláciu sietnice alebo intravitreálnu farmakologickú či chirurgickú liečbu a môže viesť k prípadnej strate zraku [2,3]. Vplyv glykémie je zrejmý u obidvoch typov DM.
HbA1c a diabetická retinopatia
Mnohé klinické štúdie ukazujú význam kontroly glykémie na vznik a vývoj orgánových komplikácií diabetu vrátane diabetickej retinopatie.
Wisconsin Epidemiologic Study of Diabetic Retinopathy (WESDR) ukázala, že zvýšenie HbA1c vedie k dvojnásobnému zhoršeniu DR [4], z čoho vyplýva, že zvýšený HbA1c je prediktorom progresie PDR pri diabetes mellitus 1. typu (DM1T).
Diabetes Control and Complications Trial (DCCT) bola randomizovaná klinická štúdia zameraná na efekt intenzifikovanej kontroly glykémie v porovnaní s konvenčnou kontrolou glykémie u pacientov s DM1T pri vývoji DR (graf 1 a 2). V prvom ramene tzv. primárnej prevencie bolo zaradených 726 pacientov, ktorí pri randomizácii nemali DR. Do druhého ramena tzv. sekundárnej intervencie bolo zaradených 715 pacientov s ľahkou alebo stredne závažnou NPDR pri vstupnom vyšetrení. Pacienti s intenzifikovanou kontrolou glykémie dostávali krátkodobo účinkujúci inzulín 3–4-krát denne subkutánne, glykémia sa im kontrolovala 4-krát denne z kapilárnej krvi prsta. V skupine s konvenčnou kontrolou glykémie pacienti dostávali inzulín 1–2-krát denne a glykémia sa kontrolovala 1-krát denne. Medián HbA1c bol v prvej skupine pacientov 7,3 %, v skupine s konvenčnou liečbou DM 9,1 % počas priemernej doby sledovania 6,5 roka. V prvom ramene tzv. primárnej prevencie bolo riziko vzniku diabetickej retinopatie pri intenzifikovanej liečbe DM redukované o 27 % za priemernú dobu sledovania 6,5 rokov (z 90 % pri konvenčnej liečbe DM na 70 % pri intenzifikovanom režime). Progresia diabetickej retinopatie za priemernú dobu sledovania bola u 11,5 % pacientov pri intenzifikovanom režime a v 54,1 % pre pri konvenčnej liečbe DM. V ramene sekundárnej intervencie počas priemernej doby sledovania 8,5 roka bola progresia retinopatie v 17,1 % pri intenzifikovanom režime liečby a v 49,2 % pri konvenčnej liečbe DM. Benefit intenzifikovanej kontroly glykémie sa ukázal po 2 až 3 rokoch liečby. Riziko laserkoagulačnej liečby počas priemernej doby sledovania 9 rokov bolo 30 % ku 7,9 % v prospech intenzifikovanej liečby DM (p = 0,001) [5,6].
Graph 1. DCCT Study: progresia DR pri intenzifi kovanej a konvenčnej kontrole glykémie 
Graph 2. DCCT Study: vzťah progresie DR ku kontrole DM 
Epidemiologická štúdia Diabetes Intervention and Complications Study (EDIC) zahŕňala 1 375 participantov s priemernou dobou sledovania 10 rokov. Pri intenzifikovanej kontrole glykémie (HbA1c 7,98 %) bola počas doby sledovania progresia diabetickej retinopatie v 53 %. Riziko progresie DR bolo počas prvých 4 rokov štúdie redukované u 70 % pacientov, v období medzi 4.–10. rokom štúdie u 38 % pacientov [7]. Táto štúdia v prvých 4 rokoch dokázala potrebu laserovej liečby diabetickej retinopatie v 6 % pri konvenčnej liečbe DM a iba v 1 % pri intenzifikovanom režime liečby DM (p = 0,002) [5].
Efekt dobrej kontroly glykémie u pacientov s diabetes mellitus 2. typu (DM2T) na vznik a vývoj DR sledovala randomizovaná klinická štúdia United Kingdom Prospective Diabetes Study (UKPDS). Do tejto štúdie bolo zaradených 3 867 pacientov s liečbou intenzifikovanou terapiou sulfonylureou alebo inzulínom a konvenčnou liečbou či diétou. Za priemernú dobu sledovania 10 rokov bola hodnota HbA1c v skupine s intenzifikovanou liečbou DM 7,0 %, v skupine konvenčnej liečby diabetu 7,9 %. Progresia retinopatie a potreba laserkoagulačnej liečby bola u pacientov s intenzifikovanou liečbou DM o 27 % nižšia ako v skupine s konvenčnou liečbou DM2T (p < 0,05) [3].
Vzťah kontroly glykémie a diabetickej retinopatie ovplyvňuje metabolická pamäť [5]. Obdobie nedostatočnej kontroly glykémie v pamäti buniek pretrváva a má negatívny vplyv na progresiu retinopatie [7]. V súvislosti s vyššou hladinou HbA1c bola dokázaná nedostatočná odpoveď DEM na fokálnu alebo mriežkovú laserkoagulačnú liečbu [8].
Zo záverov uvedených klinických štúdií vyplýva, že predpokladom úspešnosti liečby DR je správna liečba DM s dobre kontrolovanými glykémiami.
Intravitreálna liečba diabetickej retinopatie
Úspešnosť a bezpečnosť liečby diabetickej retinopatie a diabetického edému makuly laserkoaguláciou alebo intravitreálnou farmakologickou liečbou sledovali prospektívne klinické štúdie Early Treatment Diabetic Retinopathy Study (ETDRS), Diabetic Retinopathy Clinical Research Network (DRCR.net), RESTORE, RESOLVE, READ 1, READ 2, Macugen Diabetic Retinopathy Study Group, Da Vinci a Diabetic Retinopathy Study (DRS).
Early Treatment Diabetic Retinopathy Study (ETDRS) poskytla veľmi dôležité údaje prirodzeného vývoja neliečeného diabetického edému makuly (DEM) na veľkom súbore pacientov s diabetickým edémom makuly (DEM). Prvé 3 roky za každý rok sledovania stratilo 15 písmen ETDRS-optotypu 8 % neliečených očí, celkom 24 % neliečených očí za 3 roky. Stupeň a rýchlosť poklesu centrálnej zrakovej ostrosti (CZO) záviseli od vstupnej CZO a od závažnosti DR. Zhoršenie videnia bolo väčšie na očiach s horšou CZO pri vstupnom vyšetrení. Oči s ťažkou retinopatiou mali väčšiu stratu CZO po 3 rokoch sledovania [9].
V ETDRS štúdii u 22–25 % neliečených očí s klinicky nesignifikantným DEM v priebehu 1–3 rokov sledovania došlo k progresii do klinicky signifikantného DEM s postihnutím centra a adekvátnym poklesom zraku. Pomocou optickej koherentnej tomografie (OCT) sa zistilo, že 31 % očí so subklinickým edémom makuly za priemernú dobu sledovania 14 mesiacov progredovalo do klinicky signifikantného edému makuly vyžadujúceho liečbu [10,11], (obr. 1).
Image 1. Diabetický edém makuly pred a po laserovej liečbe 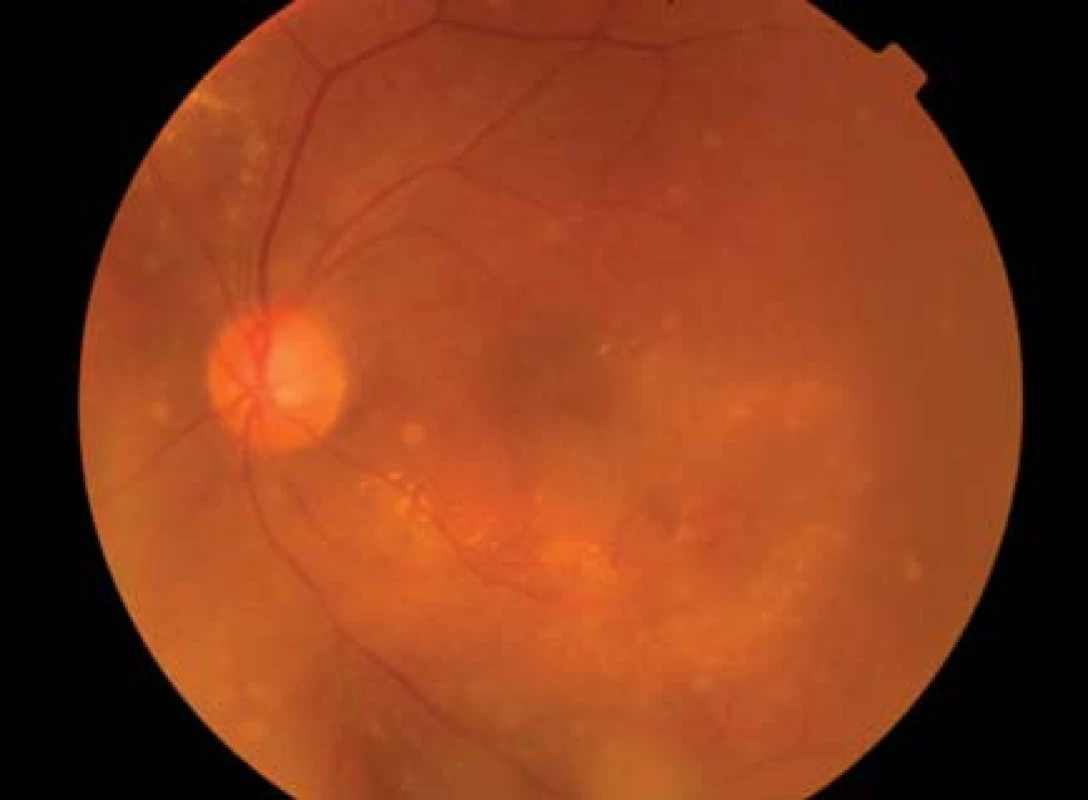
Štandardnou liečbou diabetického edému makuly podľa ETDRS je fokálna alebo mriežková laserkoagulácia sietnice v makule. Cieľom liečby je uzavretie presakujúcich lézií s výslednou redukciou edému sietnice, regresiou tvrdých exsudátov v makule a stabilizáciou alebo zlepšením centrálnej zrakovej ostrosti. Podkladom pre indikáciu laserovej liečby DEM je fluoresceínová angiografia (FAG). Spôsob koagulácie závisí od typu diabetického edému makuly. Pri fokálnom klinicky signifikantnom edéme makuly je indikovaná fokálna koagulácia liečiteľnej lézie – mikroaneuryziem, intraretinálnych mikrovaskulárnych abnormalít a rôznych presakujúcich lézií podľa FAG vo vzdialenosti 500 µm od foveoly, pri opakovanej koagulácii 300 µm od centra makuly. Pri difúznom klinicky signifikantnom edéme makuly je indikovaná mriežková (grid) koagulácia makuly vo vzdialenosti 500 µm až 2 000 µm od centra makuly v miestach jej difúzneho presiaknutia [9]. Pri fokálnej i mriežkovej laserkoagulačnej liečbe DEM sa používajú laserové zásahy veľkosti 50 až 100 µm, miernej intenzity s výsledným bledým neostro ohraničeným postkoagulačným ložiskom. Odporúčaná doba expozície laserového lúča je 0,1 maximálne 0,2 sekundy. V prípadoch pretrvávania klinicky signifikantného edému makuly možno liečbu opakovať v 4 mesačných intervaloch. V štúdii ETDRS bol pacient s klinicky signifikantným edémom makuly liečený laserom priemerne 3 - až 4-krát. Štandardne sa na laserkoagulačnú liečbu DEM používa zelené svetlo argónového lasera o vlnovej dĺžke 532 nm. Vhodné sú tiež kryptónový laser (647–670 nm), dvojite frekvenčný neodýmium YAG-laser (1 047 nm) a diódový mikropulzný laser (532 a 810 nm) s vyššou ochranou fotoreceptorov a neurónov v stredných vrstvách sietnice [13,14]. Kontraindikáciou laserovej liečby diabetického edému makuly je ischemická makulopatia, ktorá sa deteguje pomocou FAG. Laserkoagulačná liečba diabetického edému makuly môže mať aj svoje vedľajšie účinky: rozšírenie laserových ložísk v dôsledku sekundárnej atrofie pigmentového epitelu sietnice, vývoj subretinálnej fibrózy, prípadne subretinálnej neovaskularizácie [1].
Výsledky ETDRS ukazujú, že po 1 roku sledovania k zlepšeniu centrálnej zrakovej ostrosti došlo u 36 % liečených očí, v skupine neliečených očí len u 14 %. Po 3 rokoch sledovania malo 40 % liečených očí zlepšenie centrálnej zrakovej ostrosti v porovnaní s 20 % v skupine neliečených očí. Za dobu sledovania 3 rokov došlo k dvojnásobnej strate zraku u 24 % neliečených očí, u očí liečených laserkoaguláciou len u 12 %. Za dobu sledovania osleplo 12 % neliečených očí v porovnaní so 7 % v skupine liečených očí [9].
Intravitreálna farmakologická liečba
Nový prístup v liečbe diabetického edému makuly predstavuje intravitreálna farmakologická liečba. Jej história siaha do roku 2001, kedy Jonas a Sofker ako prví na svete podali intravitreálne triamcinolon-acetonid (TA) pri liečbe diabetického edému makuly [15]. Intravitreálna liečba sa vykonáva na operačnej sále za prísne aseptických podmienok. Vo vzdialenosti 3 až 3,5 mm od limbu sa do kavity sklovca aplikuje pomocou 27 až 30G-ihly liek v objeme 50 µl až 90 µl. Intravitreálne sa v liečbe diabetického edému makuly používajú steroidy a antirastové faktory antiVEGF.
Vo svete sa uskutočnilo niekoľko klinických randomizovaných štúdií, ktoré porovnávali efektívnosť a bezpečnosť intravitreálnej steroidnej liečby DEM s aplikáciou 1 alebo 4 mg triamcinolon-acetonida intravitreálne s fokálnou alebo mriežkovou laserkoagulačnou liečbou DEM.
Podľa výsledkov prospektívnej randomizovanej klinickej štúdie Diabetic Retinopathy Clinical Research Network Study (DRCR.net) po 2 rokoch sledovania fokálna alebo mriežková laserkoagulácia DEM ukázala väčšiu efektívnosť a bezpečnosť pri liečbe DEM v porovnaní s intravitreálne aplikovaným triamcinolon-acetonidom (TA) v dávke 1 alebo 4 mg. Po 2 rokoch sledovania bola priemerná centrálna zraková ostrosť (CZO) v skupine pacientov liečených laserkoaguláciou o 4 až 6 písmen ETDRS lepšia v porovnaní so skupinou pacientov liečených 1 mg alebo 4 mg TA intravitreálne. CZO v skupine pacientov liečených TA bola ovplyvnená aj vývojom či progresiou katarakty a sekundárnym steroidným glaukómom. V skupine pacientov s DEM liečených laserkoaguláciou bolo stenčenie sietnice v makule v dôsledku regresie jej edému po 2 rokoch sledovania priemerne o 53–62 µm lepšie než v skupine pacientov liečenej intravitreálne 1 alebo 4 mg triamcinolon-acetonida [12].
V súčasnosti sa vo svete realizujú prospektívne klinické štúdie, ktoré sledujú efektívnosť a bezpečnosť liečby diabetického edému makuly s intravitreálne aplikovaným dexametazónom na biodegradabilnom nosiči (OZURDEX) a fluorocinolónom na nebiodegradabilnom nosiči (ILLUVIEN).
Prelom v liečbe DEM predstavuje intravitreálna liečba s použitím antirastových faktorov (antiVEGF). AntiVEGF podané intravitreálne na rozdiel od steroidov nemajú tendenciu k vývoju katarakty a k zvyšovaniu vnútroočného tlaku [16]. Na základe vynikajúcich výsledkov prospektívnych randomizovaných klinických štúdií DRCR.net, RESTORE, RESOLVE, READ 1 a READ 2, ktoré sledovali efektívnosť a bezpečnosť liečby diabetického edému makuly intravitreálnou aplikáciou 0,5 mg ranibizumabu (Lucentis), je táto liečba DEM registrovaná na celom svete a od októbra 2011 je kategorizovaná aj na Slovensku, (obr. 2).
Image 2. Diabetický edém makuly v OCT obraze pred a po intravitreálnej liečbe s antiVEGF ranibizumabom 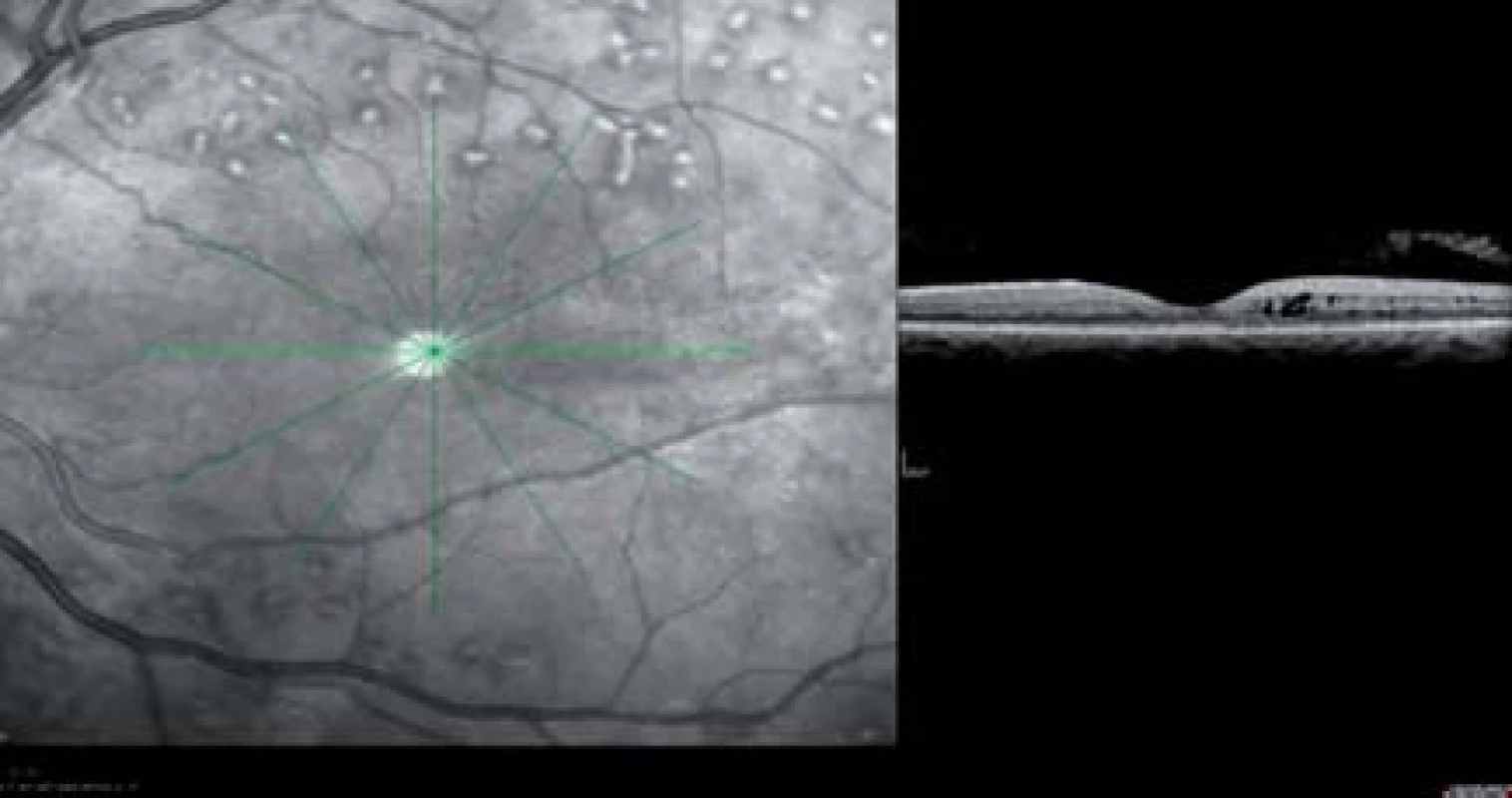
Diabetic Retinopathy Clinical Research Network Study sledovala efektívnosť a bezpečnosť liečby DEM v 4 ramenách: laserové rameno, rameno s intravitreálnou liečbou s 0,5 mg ranibizumabu a súčasne promptnou laserkoaguláciou, rameno s intravitreálnou liečbou s 0,5 mg ranibizumabu a súčasne oddialenou laserkoaguláciou, štvrté rameno tvorili pacienti liečení intravitreálnou aplikáciou 4 mg triamcinolon-acetonidu (TA). Výsledky DRCR.net ukazujú, že u pacientov liečených intravitreálnou aplikáciou ranibizumabu s promptnou alebo oddialenou laserkoaguláciou sa centrálna zraková ostrosť zlepšila o 9 písmen ETDRS za 1 rok sledovania oproti 3 písmenám v laserovom ramene a 4 písmenám v ramene s intravitreálnou liečbou 4 mg TA. Po 2 rokoch sledovania v oboch ramenách s ranibizumabom sa CZO zlepšila o 7 a 10 písmen ETDRS, v laserovom ramene len o 2 písmená ETDRS a v ramene liečenom intravitreálne 4 mg TA po 2 rokoch sledovania sa nezaznamenalo zlepšenie CZO. V oboch ramenách s ranibizumabom získalo 45 až 50 % liečených očí viac ako 10 písmen ETDRS a 30 % očí viac ako 15 písmen ETDRS. Naproti tomu zhoršenie o viac ako 10 písmen ETDRS sa po 2 rokoch sledovania našlo len u 5 až 9 % liečených očí v ranibizumabových ramenách a zhoršenie o viac ako 15 písmen ETDRS u 2–3 % očí. Podobné výsledky ukázali aj ďalšie klinické štúdie s intravitreálnou aplikáciou ranibizumabu (RESOLVE, RESTORE, READ 1, READ 2) [17].
Na základe dobrej klinickej skúsenosti sa na celom svete ako off label liečba DEM používa intravitreálne bevacizumab (Avastin) v dávke 1,25 mg s podobnou efektívnosťou ako pri liečbe s ranibizumabom.
Okrem týchto dvoch v praxi už používaných molekúl na intravitreálnu liečbu diabetického edému makuly antirastovými faktormi je ukončená klinická štúdia Macugen Diabetic Retinopathy Study Group a druhá fáza klinickej štúdie Da Vinci. Tieto štúdie sledovali efektívnosť a bezpečnosť intravitreálnej liečby DEM s pegaptanibom sodným (Macugen) a s antiVEGF Trap (aflibercept).
Proliferatívna diabetická retinopatia (PDR) ohrozuje zrak pacienta vývojom edému makuly, ischémiou, preretinálnymi a sklovcovými hemorágiami z novotvorených ciev, fibrovaskulárnymi epiretinálnymi membránami, vitreomakulárnou trakciou, trakčnou alebo regmatogénnou amóciou sietnice a vznikom neovaskulárneho glaukómu. Spôsob liečby PDR závisí od typu a rozsahu zmien a štádia ochorenia.
História liečby PDR laserkoagulačnou liečbou siaha do roku 1956, kedy Mayer-Schwickerath použil na liečbu PDR xenónový fotokoagulátor.
Diabetic Retinopathy Study (DRS) zaviedla do rutinnej praxe panretinálnu laserkoaguláciu (PRP) v liečbe PDR s cieľom redukovať hypoxickú perifériu sietnice a indukovať regresiu až uzavretie neovaskularizácií na očiach s PDR s vysokým rizikom. Panretinálna laserkoagulácia sa robí v lokálnej topickej anestézii, u citlivých jedincov na bolesť sa môže robiť v parabulbárnej, subtenonskej alebo retrobulbárnej anestézii. Niekedy je vhodné podávanie lokálnych alebo aj celkových nesteroidných antiflogistík [24]. Po funde sa v strednej a extrémnej periférii postupne aplikujú laserové zásahy veľkosti od 200 do 500 µm vo vzdialenosti 1 diametra stopy, intenzita zásahov sa volí tak, aby v mieste zásahu ostalo neostro ohraničené nablednutie sietnice, trvanie zásahu je obvykle 0,1 až 0,2 s. Ošetrenie celej sietnice sa rozdelí na dve alebo viac sedení.
Výsledky DRS ukazujú, že PRP redukuje riziko oslepnutia do 5 rokov u 90 % pacientov s PDR [18]. Zlepšenie metabolickej kontroly asociuje nielen so znížením progresie PDR, ale aj so zlepšením odpovede na panretinálnu laserkoaguláciu [19]. Fotoabláciou hypoxickej sietnice po panretinálnej laserkoagulácii sa signifikantne zníži stimul pre tvorbu cievneho endotelového rastového faktora (vascular endothelial grow factor – VEGF), zlepší sa prestup kyslíka z choriokapilaris do sietnice a po PRP sa dokázalo zníženie prietoku krvi veľkými cievami sietnice so znížením venóznej dilatácie [20,21]. Podľa DRS je na panretinálnu laserkoaguláciu (PRP) indikovaná proliferatívna diabetická retinopatia (PDR) s vysokým rizikom: pri prítomnosti neovaskularizácií terča zrakového nervu (NVD), pri preretinálnych hemorágiách v súvislosti s NVD a neovaskularizáciami sietnice (NVE). Riziko straty zraku na očiach s PDR s vysokým rizikom sa po PRP znížilo o viac ako 50 % počas 2 rokov sledovania.
Podľa ETDRS je na liečbu panretinálnou laserkoaguláciou indikovaná okrem PDR aj pokročilá neproliferatívna (tzv. preproliferatívna) diabetická retinopatia pre vysoké riziko progresie do PDR [22,23]. ETDRS demonštrovala, že plná panretinálna laserkoagulácia znižuje riziko vývoja proliferatívnej diabetickej retinopatie s vysokým rizikom približne u 50 % pacientov počas 2 rokov. Dokonca u pacientov so zlou prognózou pri závažnej neproliferatívnej (tzv. preproliferatívnej) diabetickej retinopatii s DEM došlo po neodkladnej panretinálnej laserkoagulácii k závažnej strate zraku len u 6,5 % počas 5 rokov sledovania.
Nízky vstupný vizus, závažná rozvinutá proliferatívna diabetická retinopatia s diabetickým edémom makuly pred začiatkom liečby sú nepriaznivé prognostické faktory pre výsledný vizus po panretinálnej laserkoagulačnej liečbe [22].
Klinické štúdie DRS a ETDRS podčiarkujú, že panretinálna laserkoagulácia je zásadnou liečbou PDR. Klinické skúsenosti ukazujú, že na regresiu reziduálnych neovaskularizácií je vhodná kombinácia laserovej liečby s intravitreálnou farmakologickou liečbou antirastovými faktormi [25].
Chirurgická liečba, a to pars plana vitrektómia je indikovaná a má svoje nezastupiteľné miesto pri riešení komplikácií PDR, ako sú hemoftalmus, fibrovaskulárne epiretinálne membrány, vitreomakulárna trakcia, trakčná alebo regmatogénna amócia sietnice a DEM rezistentný na laserovú alebo intravitreálnu liečbu. Klinické štúdie Early Treatment Diabetic Retinopathy Study (ETDRS) a Diabetic Retinopathy Vitrectomy Study (DRVS) určili indikačné kritéria pre chirurgickú liečbu proliferatívnej diabetickej retinopatie a diabetického edému makuly a sledovali jej efektívnosť a bezpečnosť [26], (obr. 3).
Image 3. PDR po liečbe panretinálnou laserkoaguláciou 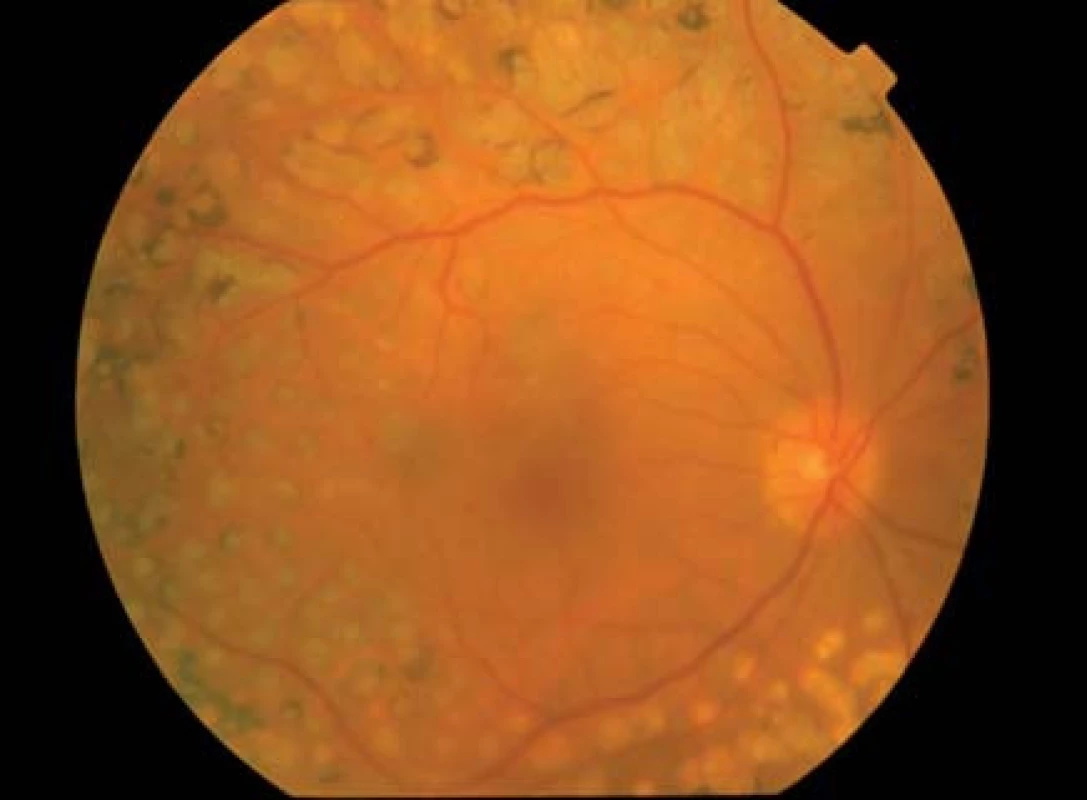
Záver
Epidemiologické štúdie Wisconsin Epidemiologic Study of Diabetic Retinopathy, Diabetes Control and Complications Trial, Diabetes Intervention and Complications Study a United Kingdom Prospective Diabetes Study poukázali na význam dobrej kontroly glykémie pri vzniku a progresii diabetickej retinopatie a diabetického edému makuly a pri odpovedi DR a DEM na liečbu.
DRS a ETDRS štúdie priniesli výsledky prirodzeného vývoja DR a DEM, ukázali prínos a nevyhnutnosť fokálnej alebo mriežkovej laserkoagulačnej liečby diabetického edému makuly a panretinálnej laserkoagulačnej liečby preproliferatívnej a proliferatívnej diabetickej retinopatie.
Intravitreálne aplikované antirastové faktory, a to samotné alebo v kombinácii s laserkoagulačnou liečbou, predstavujú novú éru v liečbe diabetického edému makuly a diabetickej retinopatie, čo potvrdzujú početné klinické štúdie (DRCR.net, RESTORE, RESOLVE, READ 1, READ 2, Macugen Diabetic Retinopathy Study Group, Da Vinci). Touto liečbou sa dá diabetická retinopatia a makulopatia a následne vizus nielen stabilizovať, ale priemerne u 50 % pacientov aj zlepšiť o viac ako 10 písmen ETDRS, čo významnou mierou ovplyvňuje kvalitu života pacientov s diabetickou retinopatiou a diabetickým edémom makuly.
Pre riziko katarakty a steroidného glaukómu intravitreálne aplikované steroidy predstavujú druhú voľbu liečby diabetického edému makuly v prípade, že diabetická retinopatia a DEM neodpovedajú na laserkoagulačnú ani intravitreálnu liečbu s antiVEGF.
MUDr. Mária Molnárová, PhD.
Doručené do redakcie 15. septembra 2012
Prijaté do tlače po recenzii 3. októbra 2012
Sources
1. Browning DJ. Diabetic Retinopathy, Evidence-Based Management. New York, Heidelberg, London: Springer Science & Business Media 2010. ISBN 978–0–387–85899–9.
2. Diabetes Control and Complication Trial research group. Progression of retinopathy with intensive versus conventional treatment in the diabetes control and complications trial. Ophthalmology 1995; 102(4): 647–661.
3. UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylurea or insulin compared with conventional treatment and risk of complications in patients type 2 diabetes (UKPDS 33). Lancet 1998; 352(9131): 837–853.
4. Klein R, Knudtson MD, Lee KE et al. The Wisconsin epidemiologic study of diabetic retinopathy XXII. The twenty-five-year progression of retinopathy in persons with type 1 diabetes. Ophthalmology 2008; 115(11): 1859–1868.
5. The Writing Team for The Diabetes Control and Complications Trial/ Epidemiology of Diabetes Interventions an Complications research group. Effect of Intensive therapy on the microvascular complications of type 1 diabetes mellitus. JAMA 2002; 287(19): 2563–2569.
6. The Diabetes Control and Complications Trial Research Group. The relationship of glycaemic exposure (HbA1c) to the risk of development and progression of retinopathy in the diabetes control and complications trial. Diabetes 1995; 44(8): 968–983.
7. The Diabetes Control and Complications Trial. Epidemiology of Diabetes Interventions and Complications Research group. Prolonged effect of intensive therapy on the risk of retinopathy comlications in patients with type 1 diabetes mellitus: 10 years after the diabetes control and complications trial. Arch Ophthalmol 1995; 113(1): 36–51.
8. Do DV, Shah SM, Sung JU et al. Persistent diabetic macular oedema is associated with elevated hemoglobin A1c. Am J Ophthalmol 2005; 139(4): 620–623.
9. Early Treatment Diabetic Retinopathy Study Research Group. Photocoagulation for diabetic macular oedema. Arch Ophthalmol 1985; 103(12): 1796–1806.
10. Gangnon R, Hubbard LD, Aiello LP et al. A severity scale for diabetic macular oedema developed from ETDRS data. Invest Ophthalmol Vis Sci 2008; 49(11): 5041–5047.
11. Browning DJ, Fraser CM. The predictive value of patient and eye characteristics on the course of subclinical diabetic macular edema? Am J Ophthalmol 2008; 145(1): 149–154.
12. Diabetic Retinopathy Clinical Research Network. A randomized trial comparing intravitreal triamcinolon acetonide and focal/grid photocoagulation for diabetic macular edema. Ophthalmology 2008; 115(9): 1447–1459.
13. Olk RJ, Wallow IH, Poulsen GL. Argon green (514) versus krypton red (647) modified grid laser photocoagulation for diffuse diabetic macular oedema. Ophthalmology 1990; 97(9): 1101–1113.
14. Larsen ML, Moeller F, Sander B et al. Subthreshold micropulse diode laser treatment in diabetic macular oedema? Br J Ophthalmol 2004; 88(9): 1173–1179.
15. Jonas JB, Sofker A. Intraocular injection of crystalline cortisone as adjunctive treatment for diabetic macular edema. Am J Ophthalmol 2001; 132(3): 425–427.
16. Roh MI, Bycon SH, Kwon OW. Repeated intravitreal injection of bevacizumab for clinically significant diabetic macular oedema. Retina 2008; 28(9): 1314–1318.
17. The Diabetic Retinopathy Clinical Research Network. Randomized Trial Evaluating Ranibizumab Plus Prompt or Deferred Laser or Triamcinolone Plus Prompt Laser for Diabetic Macular Edema. Fort Lauderdale. Ophthalmology 2010; 117(6): 1064–1077.
18. Lang GE. Laser treatment of diabetic retinopathy. Dev Ophthalmol 2007; 39 : 48–68.
19. Kotoula MG, Koukoulis GN, Zintzaras E et al. Metabolic control of diabetes is associated with an improved response of diabetic retinopathy to panretinal photocogalation. Diabetes Care 2005; 28(10): 2454–2457.
20. Fujio N, Feke GT, Goger DG, McMeel JW. Regional retinal blood flowreduction following half fundus photocoagulation treatment. Br J Ophthalmol 1994; 78(5): 335–338.
21. Remky A, Arend O, Beausencourt E et al. Retinal vessel before and after photocoagulation in diabetic retinopathy. Determining the diameter using digitized color fundus slides. Klin Monatsbl Augenheilkd 1996; 209(8–9): 79–83.
22. Early Treatment Diabetic Retinopathy Study Research Group. Early photocoagulation for diabetic retinopathy. ETDRS report number 9. Ophthalmology 1991; 98(Suppl 5): 766–785.
23. Early Treatment Diabetic Retinopathy Study Research Group. Fundus photographic risk factors for progression of diabetic retinopathy. ETDRS report number 12. Early Treatment Diabetic Retinopathy Study Research Group. Ophthalmology 1991; 98(Suppl 5): 823–833.
24. Wu WC, Hsu KH, Chen TL et al. Interventions for relieving pain associated with panretinal photocoagulation a prospective randomized trial. Eye 2006; 20(6): 712–719.
25. Schwartz SG, Flynn HW jr. Pharmacotherapies for diabetic retinopathy: present and future. Exp Diabetes Res 2007; 2007 : 52487. Dostupný z WWW(DOI): http://doi: 10.1155/2007/52487
26. Flynn HW jr, Chew EY, Simons BD et al. Pars plana vitrectomy in the Early Treatment Diabetic Retinopathy Study. ETDRS report number 17. The Early Treatment Diabetic Retinopathy Study Research Group. Ophthalmology 1992; 99(9): 1351–1357.
Labels
Diabetology Endocrinology Internal medicine
Article was published inForum Diabetologicum

2012 Issue 2-3-
All articles in this issue
- Glykemická variabilita: nový parametr kompenzace diabetu?
- Endotelová dysfunkcia a multiorgánovomultivaskulárna (polyorgánovopolyvaskulárna) choroba
-
Diabetes mellitus a hypertenzia – letálne duo
Čo rezonuje z tohoročných odporúčaní ESC a kongresu ESC? - Kontinuálne monitorovanie tkanivovej koncentrácie glukózy
- Diabetická retinopatia 2: Liečba diabetickej retinopatie a diabetického edému makuly
- Forum Diabetologicum
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Endotelová dysfunkcia a multiorgánovomultivaskulárna (polyorgánovopolyvaskulárna) choroba
- Diabetická retinopatia 2: Liečba diabetickej retinopatie a diabetického edému makuly
- Glykemická variabilita: nový parametr kompenzace diabetu?
- Kontinuálne monitorovanie tkanivovej koncentrácie glukózy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career



