-
Medical journals
- Career
Děti závislé na technické podpoře dýchání
Authors: T. Doušová
Authors‘ workplace: Pediatrická klinika 2. LF UK a FN Motol, Praha
Published in: Čes-slov Pediat 2020; 75 (7): 421-425.
Category:
Overview
Využití neinvazivní technické podpory dýchání stoupá v posledních letech u dětí s chronickými onemocněními různé etiologie. Jedná se zejména o pacienty, jejichž základní onemocnění postihuje funkci dýchacího svalstva, jehož snížená kapacita vede k narušení respirační rovnováhy a snížení efektivity mukociliární clearance. Obnovení této rovnováhy lze dosáhnout zahájením neinvazivní ventilační podpory a dále využitím přístrojové asistence kašle. Zvolený typ neinvazivní ventilace souvisí s patofyziologií vzniku respiračního selhání, indikace k jejímu zahájení a technické aspekty patří do rukou zkušeného multidisciplinárního týmu. K nastavení přístrojové podpory kašle a zhodnocení efektivity mukociliární clearance je nezbytná přítomnost respiračního terapeuta. Velká heterogenita onemocnění, široké věkové rozpětí pacientů a jejich odlišná prognóza představují pro multidisciplinární tým i rodinu pacienta vždy velkou výzvu.
Klíčová slova:
dýchací svaly – respirační rovnováha – neinvazivní ventilace – přístrojová podpora kašle – multidisciplinární tým
ÚVOD
V posledních letech stoupá využití neinvazivních podpůrných metod ke zlepšení respiračních parametrů u pacientů s komplexním chronickým onemocněním. Jedná se o pacienty, u kterých dochází k narušení tzv. respirační rovnováhy – u zdravého jedince spojené s minimálním dechovým úsilím, normální kapacitou dýchacích svalů a současně intaktním centrálním spouštěčem, který funkci dýchacích svalů řídí (obr. 1). Narušení rovnováhy vede bez adekvátní intervence k poruchám dýchání v průběhu dne a/nebo ve spánku a v konečném stadiu k projevům akutní nebo chronické respirační insuficience [1].
Image 1. Respirační rovnováha. 1A: Dechové úsilí, kapacita dýchacích svalů a centrální spouštěč jsou v rovnováze. 1B: Snížení aktivity centrálního spouštěče (přerušovaná čára) vede ke snížení aktivity dýchacích svalů a následně k alveolární hypoventilaci. 1C: Slabost dýchacího svalstva s jeho sníženou kapacitou nebo zvýšené dechové úsilí vedou ke zvýšení aktivity centrálního spouštěče (tučná šipka). Alveolární hypoventilace se objevuje v případě, že nerovnováha překročí určitý práh. 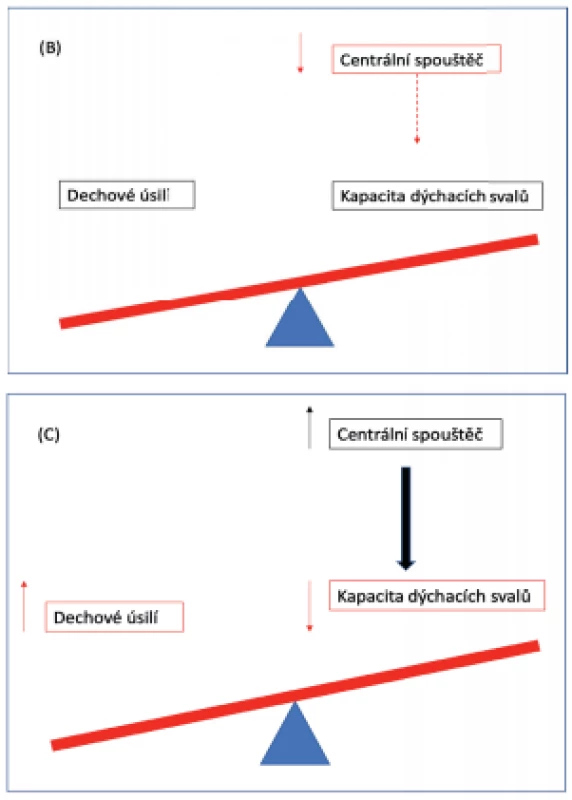
Skupiny pacientů vhodné k zahájení technické podpory dýchání
U mnoha pacientů se příčiny respirační dysbalance kombinují. Nejčastěji postiženou a poměrně širokou skupinu představují pacienti s vrozenou nebo získanou svalovou slabostí, která postihuje zejména svaly dýchací. Děti s progresivním nervosvalovým onemocněním procházejí poměrně stereotypním procesem postižení respiračního systému (obr. 2) [2].
Image 2. Algoritmus postižení respiračního systému u pacienta s (progresivním) nervosvalovým postižením (šedá), zhodnocení a intervence vhodná ke zvážení (bílá). Kyfoskolióza může zhoršovat funkci dýchacího a bulbárního svalstva, snižovat efektivitu airway clearance a ventilace (přerušované šipky). (Upraveno dle Panitch H, Respiratory Care, 2017) 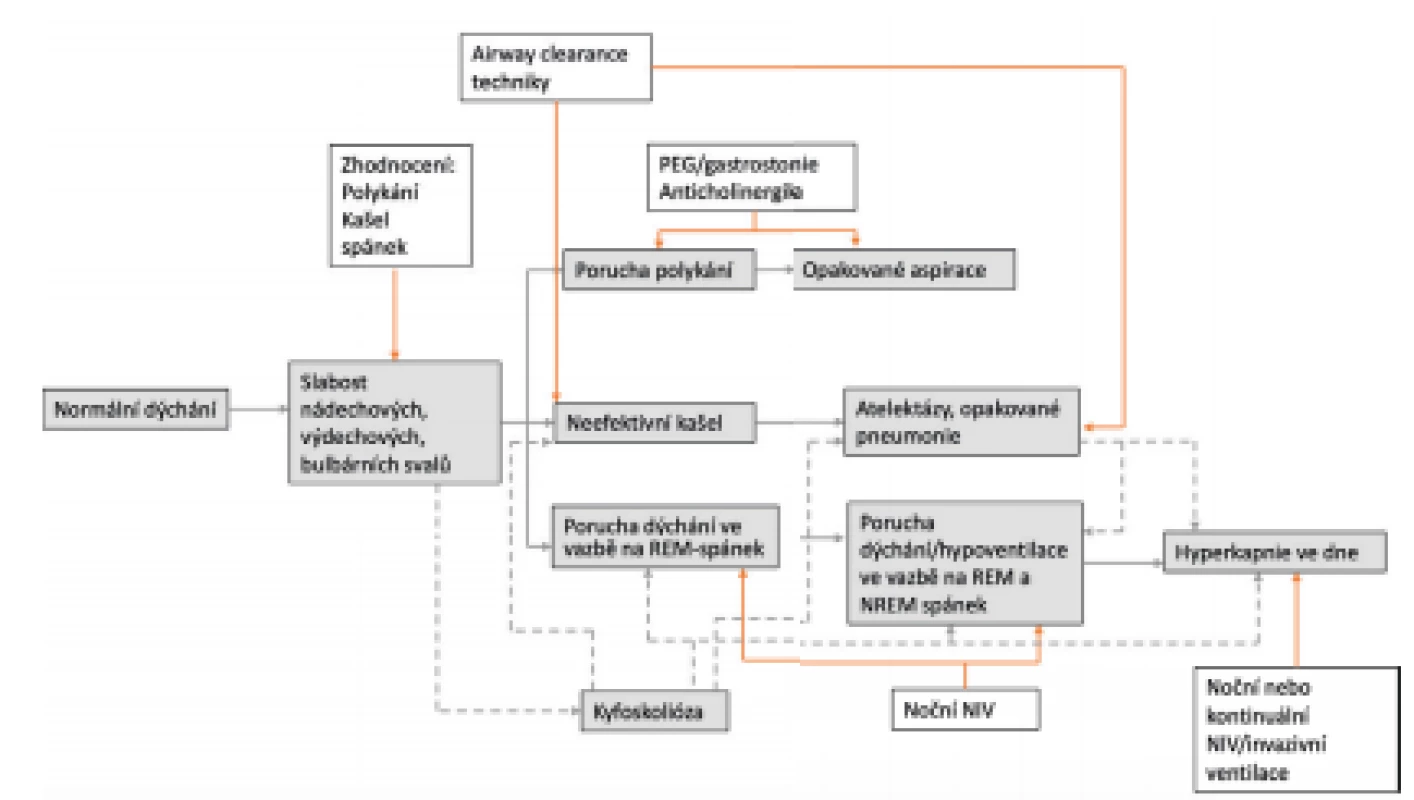
REM – rapid eye movement, NREM – non-REM, NIV – neinvazivní ventilace Svalová slabost postihuje nádechové, bulbární nebo výdechové svaly a vede k neschopnosti generovat dostatečný dechový objem a efektivní kašel [3]. Neschopnost efektivně odstranit sekret z dýchacích cest predisponuje pacienty ke vzniku opakovaných atelektáz a pneumonií. To vše má za následek sníženou plicní poddajnost a zvýšenou plicní rezistenci. V období bez infektu se první známky respirační insuficience objevují typicky ve vazbě na spánek, kdy je snížen svalový tonus kosterního svalstva a objevuje se epizodická generalizovaná atonie v průběhu REM (rapid eye movement) spánku [2]. Děti s jiným než primárně nervosvalovým onemocněním (např. DMO, poranění míchy), které způsobuje slabost dýchacího svalstva, dospějí při absenci vhodných intervencí k totožným komplikacím v různém časovém období svého života.
Narušená funkce dýchacích svalů může vést:
- k nedostatečnému vývoji hrudní stěny a plic,
- k narušení kašle, jehož nízká efektivita způsobí nedostatečné odstranění sekretu z dýchacích cest,
- k opakovaným respiračním infekcím, které svalovou slabost dále zhoršují a vedou ke vzniku chronických změn plicního parenchymu (zejména atelektáz),
- k noční hypoventilaci,
- k poruchám dýchání ve vazbě na REM a postupně i non-REM spánek,
- ke zhoršení celkového stavu pacienta.
Článek se v kontextu technické podpory dýchání zaměřuje na dva hlavní aspekty péče o tyto pacienty: 1. Narušená airway clearance, 2. Role neinvazivní ventilační podpory.
1. AIRWAY CLEARANCE
Za normálních okolností jsou plíce zbaveny od nečistot a bakterií pomocí dvou mechanismů: kašle a mukociliární clearance. Mukociliární clearance je hlavním mechanismem k očištění periferních dýchacích cest, zatímco kašel je primárně odpovědný za očistu cest centrálních [4]. Účinnost mukociliární clearance je zvyšována fyziologickou variabilitou průsvitu dýchacích cest: zúžení průsvitu intrathorakálních dýchacích cest při výdechu v průběhu klidového dýchání zvyšuje pohyblivost hlenu směrem k ústní dutině [5]. Dýchání s chronicky menšími dechovými objemy, nižšími exspiračními průtoky a tím i menší variabilitou v průsvitu dýchacích cest snižuje efektivitu mukociliární clearance. Na její snížené efektivitě se mohou současně podílet opakované aspirace, které chronicky poškozují výstelku dýchacích cest.
Table 1. Příklady onemocnění, které vedou k narušení respirační rovnováhy. 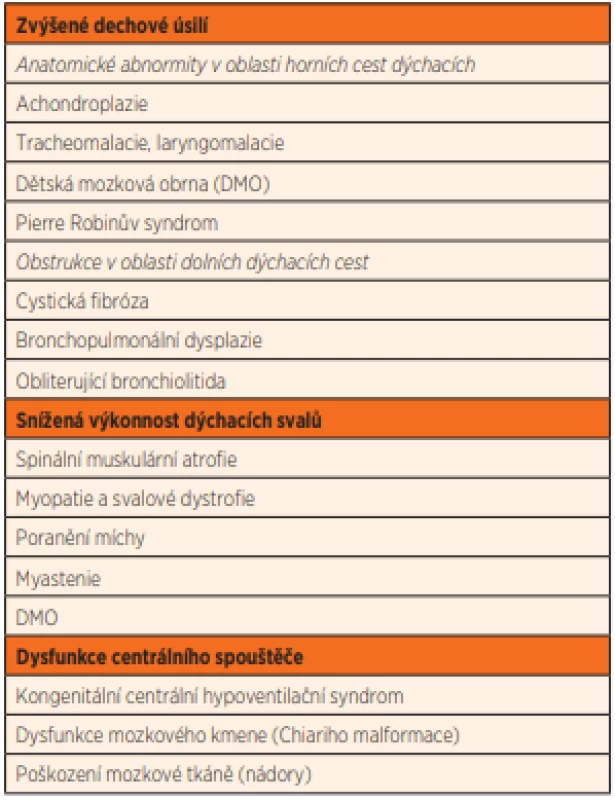
V posledních letech je přístup k pacientům velmi proaktivní, se snahou o zahájení airway clearance technik a neinvazivní ventilace již v počátku chronického onemocnění. Podstatné je zaučit v airway clearance technikách pacienta a jeho rodinu včas, před nástupem prvního respiračního infektu. K zácviku asistované airway clearance by měl být k dispozici respirační fyzioterapeut. Podle celkového stavu pacienta, síly jeho dýchacích svalů a schopnosti efektivní expektorace využíváme pro podporu očisty dýchacích cest různé techniky. Jakmile nejsou účinné běžně využívané techniky respirační fyzioterapie, je nezbytné do terapie zařadit přístrojovou podporu kašle za pomoci mechanické insuflace-exsuflace (MI-E, CoughAssist). Jeho použití by mělo předcházet zhodnocení efektivity kašle. Pacienti se zachovanou schopností samostatného sedu mají vyšší svalovou sílu dýchacích svalů, proto lze u této skupiny pro podporu mobilizace sekretu z periferních do centrálních dýchacích cest použít i techniky respirační fyzioterapie využívající oscilačního (např. PARI O-PEP, shaker, RC-Cornet, acapella) či kontinuálního přetlaku v dýchacích cestách (Threshold PEP, TheraPEP, Pari S System) [6].
MI-E je metodou asistovaného kašle, která napomáhá odstranění sekretu z dýchacích cest pacienta dodáním pozitivního tlaku (insuflace) následovaného náhlým přepnutím do negativních hodnot (exsuflace). Pro efektivní expektoraci je nutné u dospělých jedinců během výdechové fáze kašle dosáhnout PCF alespoň 160 l/min. U zdravých dospělých a dětí starších 12 let se tato hodnota pohybuje mezi 360–1200 l/min, u mladších dětí se mění v závislosti na pohlaví, věku a výšce. Dojde-li ke snížení PCF pod 120 l/min, je pacient ohrožen stagnací bronchiálního sekretu a tvorbou hlenových zátek s rozvojem atelektáz [7]. Asistovaný kašel může v určitých případech představovat jedinou možnost, jak sekret z dýchacích cest efektivně odstranit. Nastavené tlaky by měly být dostatečně vysoké k mobilizaci sekretu (nádechové a výdechové tlaky minimálně 30 cmH2O, ideálně až 40 cmH2O) [8]. Přesné hodnoty tlaků jsou však nastavovány respiračním fyzioterapeutem a odvíjí se od síly dechových svalů, spolupráce a věku dítěte. Přístroj je možné použít cestou obličejové masky nebo tracheostomie. Obecně doporučujeme provádět airway clearance s přístrojem CoughAssist 2–3krátx denně, pokud je dítě v klinicky dobrém stavu. Při infektu je zapotřebí přístroj používat častěji, podle potřeby a klinického stavu pacienta. Rodiny by měly obdržet písemný plán terapie k domácímu použití.
V rámci jedné terapeutické jednotky doporučujeme následující postup:
- 5–7 dechů s přístrojem CoughAssist, následovaných pauzou, opakovat 3x po sobě,
- následně v případě nutnosti odsát sputum z úst či tracheostomické kanyly.
U pacientů s menší mírou svalové slabosti se na podporu airway clearance soustředíme zejména po operačních výkonech a při těžším průběhu akutního respiračního onemocnění.
2. ROLE NEINVAZIVNÍ VENTILAČNÍ PODPORY
Rozlišujeme dva základní typy neinvazivní ventilační podpory (NIV, noninvasive ventilation). CPAP (continuous positive airway pressure), během kterého je pacientovi doručen konstatní tlak a jehož hlavním cílem je udržení průchodnosti dýchacích cest. Oproti tomu BiPAP (bilevel positive airway pressure) využívá dvě úrovně tlaků, kdy je vyšší tlak doručen pacientovi v průběhu každého nádechu.
Table 2. Nastavení ventilačního režimu s ohledem na základní onemocnění pacienta. 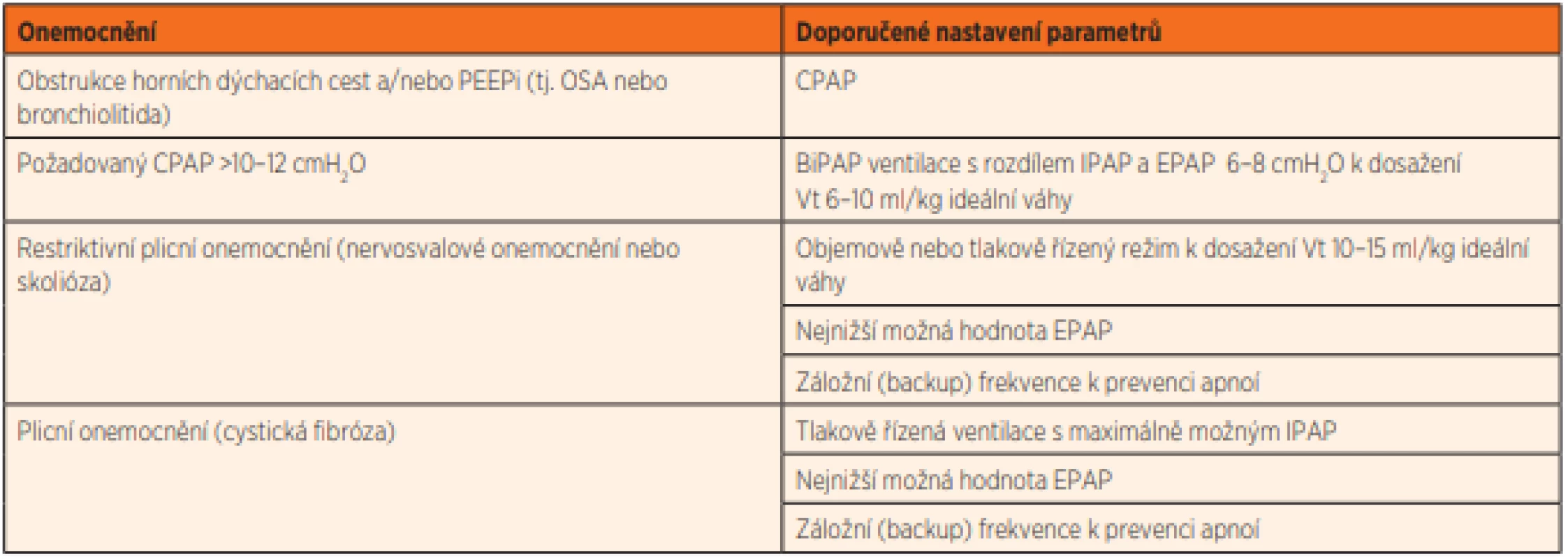
CPAP je nejjednodušším typem neinvazivní dechové podpory, který je indikován zejména v případech izolované obstrukce horních nebo dolních dýchacích cest. Jedná se o situace, kdy dochází ke zvýšenému dechovému úsilí, další dvě komponenty respirační rovnováhy (kapacita dýchacích svalů a centrální spouštěč) zůstávají nepostiženy. Obnovení průchodností dýchacích cest v průběhu dechového cyklu vede k úpravě sledovaných parametrů [9]. Nejčastější indikací k zahájení CPAP představuje syndrom obstrukční spánkové apnoe (OSA) [10]. Etiologie OSA u dětí je široká, obecně lze příčiny rozdělit na faktory vedoucí k zúžení průsvitu dýchacích cest, nebo k jejich zvýšené kolapsibilitě. Nejčastější příčinou OSA u dětí je hypertrofie nosních a/nebo krčních mandlí. Mezi další anatomické příčiny patří malá ustupující mandibula, makroglosie a hypoplazie střední obličejové části. Ve zvýšeném riziku vzniku OSA jsou děti s kraniofaciálními syndromy (Pierre Robinova sekvence, achondroplazie, Downův syndrom, mukopolysacharidózy) [10]. Zánětlivé změny a narušené obranné reflexy jsou faktory vedoucími ke zvýšené kolapsibilitě v oblasti horních dýchacích cest. Tento fakt je i vysvětlením, proč jsou pacienti s DMO, nervosvalovým onemocněním nebo např. meningomyelokélou ve zvýšeném riziku vzniku OSA. U většiny dětí s OSA je léčba pomocí CPAP efektivní [11]. V situaci, kdy dochází ke vzniku hyperkapnie, by měla být zahájena dvojúrovňová ventilace [12].
BiPAP, bilevel (dvojúrovňová) tlaková podpora, je určená zejména pro pacienty s narušenou více než jednou složkou respirační rovnováhy. V situaci zvýšeného dechového úsilí se jedná o důsledek snížené kapacity dýchacích svalů s intaktním (nervosvalová onemocnění) nebo narušeným centrálním spouštěčem (poškození mozkové tkáně, kongenitální centrální hypoventilační syndrom) [1]. Výjimečnou situaci představuje pacient se zvýšeným dechovým úsilím a primárně zachovalou kapacitou dýchacích svalů, např. pacient s cystickou fibrózou nebo intersticiálními plicními procesy. Bilevel ventilace dokáže asistovat nebo zcela nahradit funkci dýchacích svalů pozitivním tlakem doručeným v průběhu nádechu/výdechu. Přístroje mají možnost základního nastavení inspiračního tlaku (IPAP, inspiratory positive airway pressure), exspiračního tlaku (EPAP, expiratory positive airway pressure), dechové frekvence (RR, respiratory rate), inspiračního času (IT, inspiratory time) a času stoupání tlaku (raise time). Pro některé z pacientů nemusí být snadné spouštět ventilátor vlastním dechovým úsilím a je tedy nutná záložní (backup) dechová frekvence (minimum dechů doručených ventilátorem v průběhu jedné minuty), která se blíží fyziologické dechové frekvenci příslušné pro určitý věk. Hlavním cílem zahájení bilevel ventilace je obvykle léčba denní a/nebo noční hypoventilace. U dětí s nervosvalovým onemocněním má současně pozitivní efekt ve smyslu redukce respiračních exacerbací a prevence vzniku deformity hrudní stěny [13]. Vybavení potřebné k zahájení neinvazivní ventilační podpory představuje samotný přístroj, okruh a individuálně zvolený typ masky. Výběr velikosti a typu masky zkušeným lékařem je podmínkou úspěšného nastavení NIV. V dnešní době jsou již k dispozici různé typy nosních nebo celoobličejových masek, vhodných dokonce pro děti v kojeneckém věku. K zahájení léčby je doporučena zejména nosní maska, maska s jiným rozhraním pak ke střídaní (zejména z důvodu prevence otlaků v místech kontaktu s kůží). Při dlouhodobém užívání masky může dojít k iritaci kůže a hypoplazii středočárových obličejových struktur. Distenze žaludku a zvracení jsou další možné nežádoucí komplikace, které mohou vyústit v aspiraci, aspirační pneumonii a potenciálně až v náhlé úmrtí pacienta [14].
Nastavení ventilátoru závisí striktně na typu základního onemocnění. V praxi jsou preferovány tlakově řízené režimy nad objemově řízenými režimy, důvodem je lepší kompenzace úniků vzduchu v okolí masky [15]. Pro děti s obstrukcí horních cest dýchacích nebo u pacientů s onemocněním provázeným zvýšeným vnitřním PEEP (PEEPi, positive end expiratory pressure intrinsic) jako bronchiolitida je CPAP obvykle dostačující. U pacientů s restriktivním typem onemocnění nebo u těch, kteří vyžadují PEEP vyšší než 10–12 cmH2O, je obvykle nutné nastavení vyššího inspiračního tlaku k dosažení adekvátního dechového objemu (Vt). Rozdíl mezi inspiračním a exspiračním tlakem by měl být minimálně 6–8 cmH2O k dosažení dechového objemu 6–10 ml/kg ideální váhy dítěte [16]. Pacienti s nervosvalovým onemocněním nebo pacienti, jejichž onemocnění nemá za důsledek vznik PEEPi, mohou být ventilováni objemově řízeným nebo hybridním modem k zajištění adekvátní alveolární ventilace, s nejnižším možným exspiračním tlakem. Konkrétní nastavení přístroje však představuje největší výzvu zahájení neinvazivní ventilační podpory.
Jednotná doporučení k tomu, kdy přesně má být NIV zahájena u dětských pacientů, zatím neexistují. V klinické praxi se setkáváme nejčastěji s několika situacemi: případy akutního respiračního selhání, nemožnost pacienta odpojit od invazivního ventilačního režimu na jednotce intenzivní péče, případy narušené výměny krevních plynů zejména ve spánku (+/ - provázené zvýšeným počtem apnoí a hypopnoí). Obvyklými indikacemi k zahájení dlouhodobé NIV v domácím prostředí jsou hypoventilace nebo obstrukční spánková apnoe. Dalšími indikacemi však mohou být rekurentní pneumonie a atelektázy spojené s anamnézou opakovaných respiračních selhání, závažné deformity hrudní stěny, perioperační péče [17]. Virové respirační infekty prohlubují slabost dýchacích svalů a zvyšují sekreci hlenu. V rámci pooperačních komplikací se setkáváme s obstrukcí horních cest dýchacích, hypoventilací i vznikem atelektáz, které zvyšují riziko respiračního selhání. NIV má své místo i v rámci paliativní péče, a to zejména tam, kde je cílem úleva od symptomů zvýšeného dechového úsilí a pocitu dušnosti v terminálním stadiu onemocnění [18].
ZÁVĚR
V posledních letech se v čím dál tím ve větší míře setkáváme s pacienty, jejichž chronické onemocnění vyžaduje komplexní péči multidisciplinárních týmů. Jedná se zejména o děti, jejichž základní diagnóza dříve vedla k časnému úmrtí nebo postupné progresi celkového stavu s významně zkrácenou dobou přežití. Pro některé z těchto pacientů se objevují nové terapeutické možnosti včetně genové léčby (příkladem jsou pacienti se spinální muskulární atrofií), pro jiné (jako pacienti s DMO nebo kraniofaciálními syndromy) se výrazně zlepšily možnosti symptomatické terapie, a to především v souvislosti s prevencí vzniku akutního nebo chronického respiračního selhání.
Technická podpora dýchání je při správné indikaci vhodná i pro pacienty s izolovanou obstrukcí periferních nebo centrálních dýchacích cest (CF, obliterující bronchiolitida, tracheobronchomalacie) a v neposlední řadě se její využití čím dál tím více uplatňuje v rámci paliativní péče. Otázky spojené s nejlepším načasováním jednotlivých terapií a jejich typu nejsou dostatečně objasněny. Studií o jednoznačné souvislosti nastavení technické podpory dýchání se zlepšením kvality života dětských pacientů, nižším počtu akutních respiračních exacerbací i počtu hospitalizací je stále nedostatek. Tyto otázky by měly být předmětem dalších studií v dětské populaci tak, aby byly co nejlépe využity v klinické praxi.
MUDr. Tereza Doušová
Pediatrická klinika 2. LF UK a FN Motol
V Úvalu 84
150 06 Praha 5
e-mail: tereza.dousova@fnmotol.cz
Sources
1. Amaddeo A, Frapin A, Fauroux B. Long-term non-invasive ventilation in children. Lancet Respir Med 2016; 4 : 999–1008. https://doi.org/10.1016/S2213-2600(16)30151-5.
2. Perrin C, Unterborn JN, D’Ambrosio C, Hill NS. Pulmonary complica-tions of chronic neuromuscular diseases and their management. Muscle Nerve 2004; 29 (1): 5–27. https://doi.org/10.1002/mus.10487.
3. Laghi F, Tobin MJ. Disorders of the respiratory muscles. Am J Respir Crit Care Med 2003; 168 : 10–48. https://doi.org/10.1164/rccm.2206020.
4. Fink JB. Forced expiratory technique, directed cough, and autogenic drainage. Respir Care 2007; 52 : 1210–1221.
5. Warwick WJ. Mechanisms of mucous transport. Eur J Respir Dis 1983; 64 : 162–167.
6. Abusamra R, Ross Russell R. Management of respiratory disease in child-ren with muscular weakness. Paediatr Child Health (United Kingdom) 2015. https://doi.org/10.1016/j.paed.2015.06.011.
7. Neumannová K, Doušová T, Sedlák V, et al. Doporučený postup České pneumologické a ftizeologické společnosti a České společnosti dětské pneumologie pro dlouhodobou domácí léčbu poruch expektorace pomocí přístroje CoughAs sist. Cesk Slov Neurol N 2017; 80/113 (4): 480–484. https://doi.org/10.14735/amcsnn2017480.
8. Schroth MK. Special considerations in the respiratory management of spinal muscular atrophy. Pediatrics 2009 May; 123 (Suppl 4): S245–S249. https://doi.org/10.1542/peds.2008-2952K.
9. Fauroux B, Pigeot J, Polkey MI, et al. Chronic stridor caused by laryngomalacia in children: Work of breathing and effects of noninvasive ventilatory assistance. Am J Respir Crit Care Med 2001; 164 : 1874–1878. https://doi.org/10.1164/ajrccm.164.10.2012141.
10. Kaditis AG, Alvarez MLA, Boudewyns A, et al. Obstructive sleep disordered breathing in 2 - to 18-year-old children: Diagnosis and management. Eur Respir J 2016; 47 : 69–94. https://doi.org/10.1183/13993003.00385-2015.
11. Perriol MP, Jullian-Desayes I, Joyeux-Faure M, et al. Long-term adherence to ambulatory initiated continuous positive airway pressure in non-syndromic OSA children. Sleep Breath 2019; 23 (2): 575–578. https://doi.org/10.1007/s11325-018-01775-2.
12. Amaddeo A, Moreau J, Frapin A, et al. Long term continuous positive airway pressure (CPAP) and noninvasive ventilation (NIV) in children: Initiation criteria in real life. Pediatr Pulmonol 2016 Sep; 51 (9): 968–974. https://doi.org/10.1002/ppul.23416.
13. Panitch HB. Respiratory implications of pediatric neuromuscular disease. Respir Care 2017; 62 : 826–848. https://doi.org/10.4187/respcare.05250.
14. Ramirez A, Delord V, Khirani S, et al. Interfaces for long-term noninvasive positive pressure ventilation in children. Intensive Care Med 2012; 38 : 655–662. https://doi.org/10.1007/s00134-012-2516-1.
15. Gregoretti C, Pelosi P, Chidini G, et al. Non-invasive ventilation in pediatric intensive care. Minerva Pediatr 2010; 62 : 437–458. https://doi.org/10.1097/pcc.0000000000000390.
16. Dohna-Schwake C, Stehling F, Tschiedel E, et al. Non-invasive ventilation on a pediatric intensive care unit: Feasibility, efficacy, and predictors of success. Pediatr Pulmonol 2011; 46 : 1114–1120. https://doi.org/10.1002/ppul.21482.
17. Hull J. British Thoracic Society guideline for respiratory management of children with neuromuscular weakness: Commentary. Thorax 2012; 67 : 654–655. https://doi.org/10.1136/thoraxjnl-2012-202043.
18. Simonds AK (ed). ERS Practical Handbook of Noninvasive Ventilation. European Respiratory Society; 2015. https://doi.org/10.1183/9781849840767.eph01.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2020 Issue 7-
All articles in this issue
- Dětská pneumologie v Česku a na Slovensku
- Dlouhodobé dopady předčasného porodu na respirační systém u dětí
- Kdy pomýšlet na řasinkové dysfunkce?
- Jak a kdy vyšetřovat funkci plic u nespolupracujících dětí
- C-reaktívny proteín vo vzťahu k fenotypom obštrukčného spánkového apnoe u detských pacientov
- Děti závislé na technické podpoře dýchání
- Transplantace kmenových buněk krvetvorby u dětí s Fanconiho anémií po selhání krvetvorby v České republice a na Slovensku (2005–2016)
- Úsmevné príhody z Martinskej nemocnice – obytná budova
- Vplyv chorioamnionitídy na morbiditu predčasne narodených novorodencov a možné terapeutické intervencie
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Kdy pomýšlet na řasinkové dysfunkce?
- Jak a kdy vyšetřovat funkci plic u nespolupracujících dětí
- Dlouhodobé dopady předčasného porodu na respirační systém u dětí
- Dětská pneumologie v Česku a na Slovensku
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


