-
Medical journals
- Career
Rozšířené testování nosičství recesivních chorob (CarrierTest) v klinické praxi
Authors: J. Diblík; M. Bittóová; F. Lhota; F. Zembol; L. Dohnalová; Z. Vilímová; I. Soldátová; M. Hrabíková; I. Pavlechová; M. Koudová; D. Stejskal
Authors‘ workplace: Centrum lékařské genetiky a reprodukční medicíny Gennet, s. r. o., Praha
Published in: Čes-slov Pediat 2020; 75 (1): 5-10.
Category:
Overview
Cíl: Cílem práce je shrnutí zkušeností s rozšířeným testováním nosičství autosomálně recesivně dědičných chorob v rámci prekoncepční péče především u párů s poruchami plodnosti nebo opakovanými těhotenskými ztrátami.
Metody: CarrierTest je na našem pracovišti vyvinutý test založený na amplikonovém sekvenování kritických oblastí 77 genů k detekci 835 patogenních mutací způsobujících více než 61 dědičných chorob a stavů.
Výsledky: Ve sledovaném období jsme vyšetřili celkem 10 752 jedinců z vyšetřovaných párů. Celkem bylo zjištěno 3899 případů nosičství patogenních variant, nejčastěji v genech: GJB2 (4,9 % osob), CFTR (3,6 %), SERPINA1 (2,6 %), DHCR7 (2,6 %), SMN1 (2,5 %), PAH (2,3 %), NBN (1,8 %), CYP21A2 (3,3 %), ATP7B (1,2 %), PMM2 (1,1 %), ACADVL (1,1 %) a ACADM (1 %). U 67 párů (1,25 %) bylo prokázáno vysoké riziko závažného autosomálně recesivního onemocnění, nejčastěji se jednalo u obou partnerů o nosičství mutací genů: GJB2 (18×), CFTR (13×), SMN1 (6×), CYP21A2 (6×), SERPINA1 (3×), PAH (3×), MEFV (3×), DHCR7 (2×), PMM2 (2×), ACADVL (2×), ACADM (2×), HEXA (2×) a ARSA (2×).
Závěr: Výsledek CarrierTestu dává párům informaci o rizicích pro jejich potomky. Závažnost nálezů a zjištěných rizik se liší u jednotlivých genů i u různých mutací v těchto genech. Výsledky tedy musí být posouzeny a sděleny klinickým genetikem tak, aby se páry mohly rozhodnout o vhodném dalším postupu. Možná preventivní opatření zahrnují preimplantační genetické testování, prenatální diagnostiku, ale i postnatální diagnostiku (včetně novorozeneckého screeningu) s následující včasnou léčbou.
Klíčová slova:
autosomálně recesivně dědičná onemocnění – mutace – nosičství – prekoncepční testování
ÚVOD
Mnohá z nejzávažnějších chronických onemocnění dětského věku patří mezi recesivně dědičná. Většina rodičů se o tom, že jsou nosiči, dozví až po narození postiženého dítěte. Součástí prekoncepční genetické péče je snaha o odhalení těchto skrytých rizik dříve, aby mohlo být nabídnuto prenatální a preimplantační testování nebo včasná léčba před rozvinutím příznaků onemocnění.
Odhaduje se, že závažných onemocnění tohoto typu je přibližně 1300, postihují 3 děti z 1000, rizikových párů je v populaci 1–2 % [1]. Nosičem aspoň jedné mutace pro letální onemocnění je přibližně 50 % jedinců v populaci [2].
Výskyt recesivních chorob a zodpovědných mutací se liší v závislosti na etnickém původu. V evropské populaci patří mezi nejčastější nosičství cystické fibrózy (mutace genu CFTR), deficitu antitrypsinu (SERPINA1), hluchoty (GJB2) a spinální muskulární atrofie (SMN1). V populaci židovského původu jsou navíc časté například Gaucherova choroba (GBA), Tay-Sachsova choroba (HEXA) a familiální dysautonomie (ELP1/IKBKAP). Pro osoby afrického a středozemního původu je typický výskyt hemoglobinopatií, především srpkovité anemie a β-talasémie (mutace genu HBB) [3].
Tradiční přístup je založený na odhadu rizika nosičství podle rodinné anamnézy a předpokládaného původu s následným vyšetřením nosičství vybraných chorob. Nevýhodou tohoto postupu je, že zachytí jen menší část rizik, přičemž většina chorob se ve skutečnosti vyskytuje celosvětově.
Současné molekulárně genetické metody založené na paralelním sekvenování mnoha úseků DNA [4] umožňují současně vyšetřit velké množství genů a lze tedy sestavit test, který pokryje nejčastější mutace nacházené ve smíšené populaci. Takových testů je v současné době řada dostupných komerčně, ale žádný nebyl navržen s ohledem na českou populaci [5].
Při návrhu testu jsou možné 2 základní přístupy: kompletní sekvenování vybraných genů, nebo detekce pouze předem vybraných mutací (genotypování). Kompletní sekvenování přináší více informací, zachytí více mutací, ale i variant nejasného významu, jejichž interpretace může být obtížná.
Ze znalosti výskytu nosičství daného onemocnění a populační frekvence mutací, které test pokrývá, lze pro každého jedince stanovit zbytkové riziko R, že je nosičem i přesto, že výsledek je negativní.
R = 1/(P×(1–S)/(P×(1–S))+(1–P))
P – populační frekvence přenašečů, S – senzitivita testu – jakou část mutací publikovaných u postižených jedinců test zahrnuje, R – reziduální riziko přenašečství mutace.
Například frekvence přenašečů pro gen CFTR (cystická fibróza) je v české populaci 1/25. CarrierTest zahrnuje mutace, vyskytující se u 95 % pacientů s cystickou fibrózou [5]:
R=1/((1/25×(1–95/100))/((1/25×(1–95/100)) + (1–1/25)))=1/481
Pro vyšetření páru lze buďto vyšetřovat oba partnery najednou, anebo napřed vyšetřit jednoho z partnerů a v případě nálezu mutace v určitém genu pak vyšetřit u druhého pouze tento gen. Náklady na vyšetření jednoho genu jsou ale v současnosti podobné jako náklady na celý panel, takže je organizačně jednodušší vyšetřit rovnou oba partnery. Oba tak získají kompletní informaci, která navíc může sloužit pro záchyt nosičství v jejich příbuzenstvu.
Ve všech případech, kdy je zjištěno nosičství závažného onemocnění, je vhodné nabídnout vyšetření dalších příbuzných osob v riziku nosičství. V případě průkazu je indikováno vyšetření jejich partnerů, resp. partnerek.
Pro vyšetřovaný pár mohou nastat u každého z genů tyto možnosti:
- U obou partnerů zjištěno nosičství mutace v heterozygotním stavu. Potomci potom mají vysoké riziko, že budou danou chorobou postiženi: 1/4
- Mutace zjištěna u jednoho z partnerů, druhý je negativní. Riziko pro potomky je nízké, přesná výše závisí na reziduálním riziku: 1/(4×R)
- Oba partneři negativní. Riziko je velice nízké: 1/(4×R×R)
Výjimečně je možné testováním diagnostikovat i přítomnost dvou mutací u jedné osoby. Tyto mutace mohou být v pozici trans, tj. každá na jedné kopii genu a pak se může jednat o jedince postiženého daným onemocněním, obvykle jeho mírnou formou. Pokud obě mutace jsou v pozici cis, tj. na jedné kopii genu, jedná se o nosičství. Rozlišit to lze vyšetřením rodičů dané osoby.
Při přípravě prvního vlastního panelu (Gennet CarrierTest) jsme se rozhodli vycházet z dosavadních znalostí o výskytu zodpovědných mutací a zařadit mutace genů asociované s infertilitou nebo opakovanými těhotenskými ztrátami, s vysokou populační frekvencí nosičství, metabolické vady detekované novorozeneckým screeningem [6], smyslové poruchy i některé etnicky specifické (slovanské, židovské, romské, africké).
METODY A PACIENTI
Metody
CarrierTest využívá technologie amplikonového masivně paralelního sekvenování (NGS – next-generation sequencing) specificky upravené pro potřeby tohoto klinického panelu.
Při návrhu projektu byly cílové oblasti analyzovaných genů vybírány podle recentních informací obsažených v klinických databázích (NCBI ClinVar), dostupné vědecké literatury a populačně specifických, klinicky relevantních variant identifikovaných u pacientů našeho pracoviště. Tyto cílové lokusy v genech zájmu byly sloučeny v tzv. „target regions“ o velikostech v rozsahu 30–1172 bp a celkové délce 29 709 bp, na které bylo navrženo 684 amplikonových oblastí pro obohacení genomové DNA pacienta o pouze analyzované oblasti. V návrhu byla zohledněna i nutnost specifické analýzy některých patogenních variant většího rozsahu, jako je pseudogenní oblast genu SMN1 (delece exonu 8) a delece exonů 2–3 genu CFTR, které se v komerčně dostupných kitech pro amplikonové NGS nevyskytují.
Pro přípravu sekvenační knihovny bylo použito 250ng genomové DNA od 96 probandů. Sekvenační knihovny vytvořené za využití robotické stanice NGS Star (Hamilton), dle standardního protokolu pro TruSeq Custom Amplicon (prvních 7000 vzorků), později AmpliSeq (obojí Illumina) technologii, byly kvalitativně analyzovány pomocí kapilární gelové elektroforézy systémem TapeStation (Agilent Technologies) a sekvenovány na platformě NextSeq (Illumina) s využitím chemie 300c Mid Output.
Pro zpracování výsledných hrubých dat byla vyvinuta vlastní bioinformatická analýza s lokálně vystavěnou anotační databází Ensembl, automatickým nástrojem pro filtraci sekvenačních dat a reportování klíčových genotypů a relevantních patogenních variant. Zpracování zahrnuje FASTQ a BAM statistiky, možnost automatického zarovnání sekvenačních čtení k referenčnímu genomu, či manuální výběr nadřazeného zarovnání a tzv. realignmentu pro indel (inzerce-delece) varianty. Pro identifikaci variant je využíván algoritmus Varscan zvláště pro jednonukleotidové varianty (SNV – single-nucleotide variant) a varianty typu indel. Zvláštní zpracování v rámci zautomatizované analýzy vyžaduje hodnocení velkých delecí v genech SMN1 a CFTR, které analyzuje hloubku pokrytí v rámci sekvenačního běhu, dle vytvořené reference pro specifické oblasti cílových genů. Krom devíti klíčových genotypů, které jsou referovány vždy, jsou ostatní zjištěné varianty filtrovány podle přísných parametrů klinické významnosti, jako jsou populační alelické frekvence a dopad na fenotyp.
Sestavování výsledné zprávy je zajištěno prostřednictvím vyvinutého poloautomatického nástroje Carrepo, umožňujícího analýzu kompatibility páru i stanovení reprodukčních rizik pro jednotlivé pacienty.
Pacienti
V období od dubna 2017 do října 2019 jsme vyšetřili celkem 10 752 osob z vyšetřovaných párů s poruchami plodnosti nebo opakovanými spontánními potraty.
VÝSLEDKY
Celkem bylo zjištěno 3899 nosičství patogenních variant. Nejčastější nálezy jsou shrnuty v tabulce 1, uvedeny jsou pouze geny, u nichž frekvence nosičů ve vyšetřené skupině překročila 0,3 %: GJB2, CFTR1, SERPINA1, DHCR7, SMN1, PAH, NBN, CYP21A2, ATP7B, PMM2, ACADVL, ACADM, GALT, HADHA, MEFV, HEXA, BTD, SLC26A4, CBS, ARSA, MCCC1, USH2A, ALPL, IDUA, TPP1 a GBA.
Table 1. Nejčastější nálezy nosičství autosomálně recesivně dědičných onemocnění ve vyšetřené skupině pacientů. 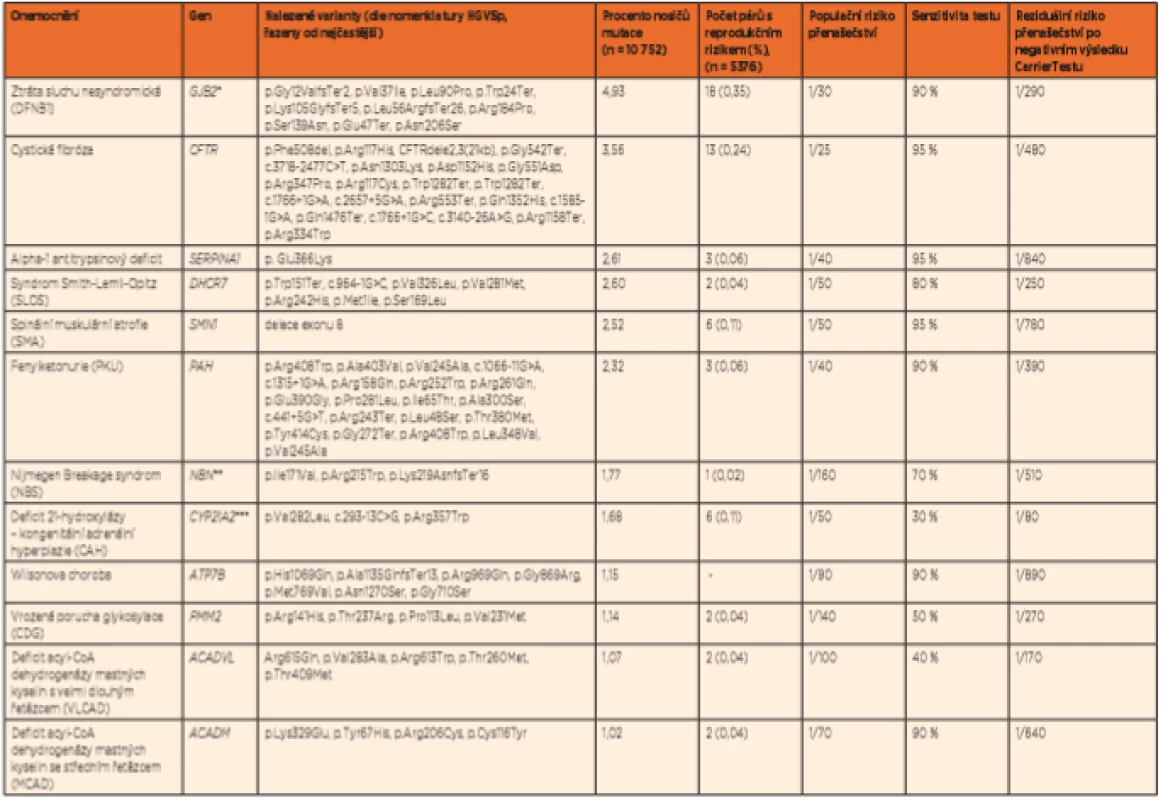

Vysvětlivky:
*bez varianty p.Met34Thr, která má jen mírné fenotypové projevy
**včetně varianty p.Ile171Val s konfliktní interpretací v klinických databázích
***včetně varianty p.Val282Leu, způsobující neklasickou formu CAH
****bez variant způsobujících mírný fenotyp p.Glu148Gln a p.Lys695Arg
*****bez variant způsobujících mírný fenotyp p.Asp444His a p.Gly45Arg
V dalších 33 genech bylo nalezeno nosičství s nižší frekvencí: ASL, FAH, NPC1, ACADS, ASPA, G6PC, TGM1, SGSH, CYP27A1, GCDH, PEX1, MCCC2, ASS1, ATM, GNPTAB, CHRNE, IKBKAP/ELP, NPC2, MYO7A, PCDH15, SMPD1, PEX7, GLB1, PEX12, HBB, PEX10, AGL, PEX2, ADGRV1, CDH23, CLRN1, CTNS a FKRP.
U 67 párů bylo prokázáno riziko závažného autosomálně recesivního onemocnění, jednalo se u obou partnerů o nosičství mutací genů: GJB2, CFTR1, SERPINA1, DHCR7, SMN1, PAH, NBN, CYP21A2, PMM2, ACADVL, ACADM, GALT, MEFV, HEXA, BTD a ARSA.
DISKUSE
Výsledek CarrierTestu dává párům informaci o rizicích pro jejich potomky. Závažnost nálezů a zjištěných rizik se liší u jednotlivých genů i u různých mutací v těchto genech. Výsledky tedy musí být posouzeny a sděleny klinickým genetikem tak, aby se páry mohly rozhodnout o vhodném dalším postupu.
Možná preventivní opatření zahrnují preimplantační genetické testování (PGT), prenatální diagnostiku, ale i postnatální diagnostiku (včetně novorozeneckého screeningu) s následující včasnou léčbou. V případě některých častých méně závažných nálezů závisí rozhodnutí o léčbě na klinických projevech. Tyto méně závažné mutace přitom mohou být velice časté, v některých genech častější než jasně popsané závažné patogenní mutace. To je vysvětlením, proč je u některých genů častější záchyt nosičství, než by vyplývalo z populačního výskytu odpovídajícího onemocnění. Zároveň ale tyto varianty nelze z testování vyřadit, protože se nejedná o zcela benigní varianty bez vlivu na fenotyp.
V genu GJB2 mezi časté a méně závažné mutace patří dvě varianty: p.Met34Thr a p.Val37Ile, které jsou v homozygotním stavu nebo v kombinaci s jinou patogenní variantou asociovány s mírnou až středně závažnou vrozenou poruchu sluchu, jedná se o variabilní expresivitu a neúplnou penetranci [7]. Vzhledem k vysoké četnosti není varianta p.Met34Thr ve výsledcích zahrnuta, u nosičů p.Val37Ile je nutné individuální hodnocení rizika.
Dalším možným vysvětlením pro nečekaně vyšší záchyt nosičství, než by odpovídalo výskytu onemocnění u dětí, může být prenatální letalita, která je v těžkých případech důsledkem postižení plodu syndromem Smith-Lemli-Opitz. Nejčastěji nacházená varianta v genu DHCR7 (p.Trp151Ter) je jednoznačně patogenní mutací, pro niž je v homozygotním stavu letalita typická [8].
V genu NBN je nejčastěji nacházena varianta p.Ile171Val, která je v literatuře opakovaně popsána jako patogenní mutace, i když některé studie ji popisují jako variantu s nejasným klinickým významem. Mutace byla opakovaně nalezena jak u dětí se syndromem Nijmegen Breakage, tak u pacientů s různými typy nádorových onemocnění (v heterozygotní formě), především karcinomu prsu [9].
Vyšetřením založeným na sekvenování krátkých úseků nelze detekovat některé ze závažných mutací genu CYP21A2, které jsou nacházeny u pacientů s klasickou kongenitální adrenální hyperplazií (CAH). Mezi ně patří delece a duplikace, nebo velké konverze mezi funkčním genem a jeho vysoce homologním pseudogenem [10]. Nejčastější varianta p.Val282Leu je naopak asociována pouze s mírnou, tzv. neklasickou CAH [11]. Klasickou formu způsobuje jen, pokud je přítomná v kombinaci s jinou závažnější mutací. Neklasická CAH je méně závažné relativně častější onemocnění, které se může projevovat předčasnou pubertou a nízkým vzrůstem, akné, neplodností a dalšími nespecifickými příznaky souvisejícími s hyperandrogenismem u žen. Projevy u mužů jsou mírnější a méně dobře popsané, obecně platí, že většina osob s tímto onemocněním není diagnostikována.
Překvapivým zjištěním je i v naší populaci vysoký výskyt nosičství mutací v genu MEFV, které jsou asociovány s familiární středomořskou horečkou. Ve více případech jsme zachytili i 2 mutace u zcela zdravých jedinců. Svědčí to pro multifaktoriální etiologii toho onemocnění, při níž mutace genu MEFV jsou spíše jen dědičným rizikovým faktorem. To platí především pro dvě časté varianty p.Glu148Gln a p.Lys695Arg, jejichž nález tedy není považován za významný z hlediska rizik pro potomky. Nejzávažnější mutace p.Met694Val, která je nacházená u pacientů s amyloidozou ledvin vyžadující léčbu kolchicinem, je ale v naší populaci vzácná.
V genu BTD jsme v naší populaci zjistili vysokou frekvenci dvou variant – p.Asp444His a p.Gly45Arg, které mohou být zodpovědné za mírnou formu deficitu biotinidázy [12]. Homozygoti pro p.Asp444His mají aktivitu sérové biotinidázy přibližně 50 %, tedy jako zdraví heterozygoti pro závažnou mutaci. V kombinaci s další významně deficitní mutací na druhé alele mohou být příčinou parciálního deficitu s mírnými příznaky a projevy při dlouhodobém stresu. Nejedná se ovšem o mutace způsobující závažnou formu s rizikem neurologického postižení u potomků.
ZÁVĚRY
CarrierTest umožnil zpřesnění populačně specifické frekvence variant, jejichž odhad byl založen na vyšetření více než 20 tisíc pacientů v rámci prekoncepční péče na našem pracovišti před jeho zavedením. Tento test nahrazuje různé laboratorní metody, které byly v minulosti používány pro prekoncepční testování IVF pacientů, včetně detekcí velkých delecí, a slučuje je do jednoho laboratorního vyšetření. Testování párů v rozšířeném počtu genů umožňuje zachytit větší množství nosičů závažných autosomálně recesivních onemocnění v porovnání se základním počtem genů doporučovaných současnými klinickými doporučeními [13] (0,24 % vs. 1,25 %), kterým lze následně nabídnout příslušnou prekoncepční a prenatální péči. CarrierTest tak párům umožňuje informované rozhodování o vlastní reprodukci.
MUDr. Jan Diblík, Ph.D.
Centrum lékařské genetiky
a reprodukční medicíny Gennet, s. r. o.
Kostelní 9
170 00 Praha 7
e-mail: jan.diblik@gennet.cz
Sources
1. Henneman L, Borry P, Chokoshvili D, et al. Responsible implementation of expanded carrier screening. Eur J Hum Genet 2016; 24 (6): e1–e12.
2. Gao Z, Waggoner D, Stephens M, et al. An estimate of the average number of recessive lethal mutations carried by humans. Genetics 2015; 199 (4): 1243–1254.
3. Lazarin G, Haque IS, Nazareth S, et al. An empirical estimate of carrier frequencies for 400+ causal Mendelian variants: results from an ethnically diverse clinical sample of 23,453 individuals. Genet Med 2013; 15 (3): 178–186.
4. Stejskal D. Klinická genetika ve 21. století. Cas Lek Cesk 2019; 158 (1): 4–8.
5. Chokoshvili D, Vears D, Borry P. Expanded carrier screening for monogenic disorders: where are we now? Prenat Diagn 2018; 38 (1): 59–66.
6. Pešková K, Chrastina P, Bártl J, et al. Novorozenecký screening dědičných metabolických poruch v České republice. Čes-slov Pediat 2018; 73 (6): 390–394.
7. Shen J, Oza AM, del Castillo I, et al. Consensus interpretation of the p.Met34Thr and p.Val37Ile variants in GJB2 by the ClinGen Hearing Loss Expert Panel. Genet Med 2019; 21 (11): 2442–2452.
8. Jezela-Stanek A, Ciara E, Małunowicz E, et al. Differences between predicted and established diagnoses of Smith-Lemli-Opitz syndrome in the Polish population: Underdiagnosis or loss of affected fetuses? J Inherit Metab Dis 2010; 33(Suppl 3): 241–248.
9. Rożnowski K, Januszkiewicz-Lewandowska D, Mosor M, et al. I171V germline mutation in the NBS1 gene significantly increases risk of breast cancer. Breast Cancer Res Treat 2008; 110 (2): 343–348.
10. Vrzalová Z, Hrubá Z, Hrabincová ES, et al. Chimeric CYP21A1P//CYP21A2 genes identified in Czech patients with congenital adrenal hyperplasia. Eur J Med Genet 2011; 54 (2): 112–117.
11. Novotná D, Vinohradská H, Hrubá Z. Deficit 21-hydroxylázy s genotypem p.I173N//chimérní gen CYP21A1P/CYP21A2 před a po screeningu. Čes-slov Pediat 2018; 73 (2): 95–99.
12. Borsatto T, Sperb-Ludwig F, Blom HJ, Schwartz IVD. Effect of BTD gene variants on in vitro biotinidase activity. Mol Genet Metab 2019; 127 (4): 361–367.
13. Harper JC, Aittomäki K, Borry P, et al. Recent developments in genetics and medically assisted reproduction: from research to clinical applications. Eur J Hum Genet 2017; 26 (1): 1–22.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2020 Issue 1-
All articles in this issue
- Editorial: Česko-slovenská Pediatrie v roce 2020
- Editorial: Současné možnosti genetické diagnostiky
- Expanded carrier screening of recessive disorders (CarrierTest) in clinical practice
- Children born after assisted reproduction in the Czech Republic in 2013–2015
- Congenital and hereditary diseases of respiratory tract from genetician’s view
- Genetic causes of sudden infant death syndrome in the era of next generation sequencing.
- Inherited arrhythmic syndromes in children
- It is never too late – HSV1-induced herepetic encephalitis
- Oxytocin and obesity
- Poděkování spolupracovníkům za rok 2019
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- It is never too late – HSV1-induced herepetic encephalitis
- Inherited arrhythmic syndromes in children
- Genetic causes of sudden infant death syndrome in the era of next generation sequencing.
- Expanded carrier screening of recessive disorders (CarrierTest) in clinical practice
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

