-
Medical journals
- Career
Toxický erytém vyvolaný chemoterapií
Authors: I. Píchová; V. Plechatá
Authors‘ workplace: Kožní oddělení, Oblastní nemocnice Kolín, a. s. prim. MUDr. Věra Plechatá
Published in: Čes-slov Derm, 86, 2011, No. 5, p. 236-239
Category: Case Reports
Overview
Toxický erytém vyvolaný chemoterapií (TEC) je souhrnné označení pro změny vznikající v souvislosti s léčbou některými chemoterapeutiky na podkladě vystupňované toxické reakce. Mezi časté klinické varianty TEC patří lokalizovaný akrální erytém, který je charakterizován rozvojem bolestivých erytémových ploch postihujících především dlaně a plosky. Autoři popisují případ 73letého pacienta s karcinomem tlustého střeva, metastazujícího do jater, u kterého došlo k rozvoji akrálního erytému v důsledku léčby capecitabinem.
Klíčová slova:
toxický erytém vyvolaný chemoterapií – capecitabinÚVOD
V následujícím kazuistickém sdělení je prezentována jedna z nejčastěji se vyskytujících klinických jednotek – akrální erytém – řazených k toxickému erytému vyvolaných chemoterapií.
POPIS PŘÍPADU
Pacientem byl 73letý muž, odeslaný na kožní oddělení spádovým dermatologem pro asi dva týdny trvající bolestivé postižení dlaní a plosek. Předchozí ambulantní léčba v místě bydliště nevedla k očekávanému zlepšení jak objektivních, tak subjektivních obtíží pacienta.
Rodinná anamnéza byla bez pozoruhodností. V osobní anamnéze pacient udával cholecystektomii v roce 1979. V roce 2000 prodělal radikální operaci tlustého střeva pro karcinom. V roce 2004 nastala progrese základního onemocnění s metastázami kolorektálního karcinomu v játrech, která vedla k zahájení série adjuvantní chemoterapie.
V době přijetí na naše oddělení byl pacient druhý den po ukončení páté série chemoterapie capecitabinem (Xeloda). Léčba tímto preparátem trvala tři měsíce. Jiné léky pacient neužíval. Nemocný pozoroval svědění až pálení chodidel trvající několik týdnů. Během několika posledních dní pozoroval intenzivní zarudnutí kůže dlaní a plosek, které přešlo v tvorbu puchýřů, které se nejdříve objevily nejprve v místech zvýšené mechanické zátěže na hranách chodidel. Při vyšetření byl patrný erytém a edém dlaní a plosek, omezující hybnost prstů s tvorbou ragád ve flekčních rýhách prstů, otok postihoval chodidla a celé bérce. Na hranách chodidel byly přítomny eroze po stržených puchýřích, jejichž výrazná bolestivost znemožňovala chůzi (obr. č. 1, 2). Pacient byl kompletně vyšetřen. V laboratorním vyšetření byla zjištěna hypokalémie a hypokalcémie, zvýšený sérový i konjugovaný bilirubin a snížená hladina cholesterolu. V krevním obraze byla popsána anizochromie, anizocytóza, makrocytóza, anémie, trombocytopénie s anizotrombocytózou, mírná leukocytóza a vakuolizace cytoplazmy monocytů. Tyto laboratorní nálezy odpovídaly změnám po prodělané onkologické léčbě capecitabinem [8]. Mikrobiologické vyšetření stěru z erozí bylo v primokultuře negativní, po pomnožení zachycen Enterococcus species. Celková medikace zahrnovala perorální suplementaci kalia. Analgetickou léčbu pacient nevyžadoval, pro intenzivní svědění chorobných ploch byl podáván bisulepin v dávce 2 mg denně. Dále byla nasazena perorální antibiotika a to klaritromycin v dávce 500 mg tbl. 2krát denně po dobu 12 dnů na základě výsledků mikrobiologického vyšetření stěru z erodovaných ploch. Dobrým ukazatelem úpravy celkového stavu pacienta bylo zvýšení hladiny hemoglobinu, pokles leukocytů a normalizace hodnot mineralogramu. Opatření zahrnovala odlehčení postižených ploch a edukaci pacienta. Převazy krycími materiály s obsahem stříbra byly prováděny lékařem 1krát denně. Během prvních tří dnů pobytu na kožním oddělení došlo ke stabilizaci lokálního nálezu. Objektivně došlo ke zmenšení otoku doprovázené problednutím akrálních částí. Postupná epitelizace erodovaných ploch a ragád ve flekčních rýhách prstů vedla i ke zlepšení hybnosti končetin. Při propuštění po třech týdnech hospitalizace byl již nález na chodidlech i rukou natolik zlepšen, že umožňoval pacientovi plný návrat k běžným aktivitám, na další kontroly se nedostavil.
Image 1. Klinický nález při přijetí pacienta 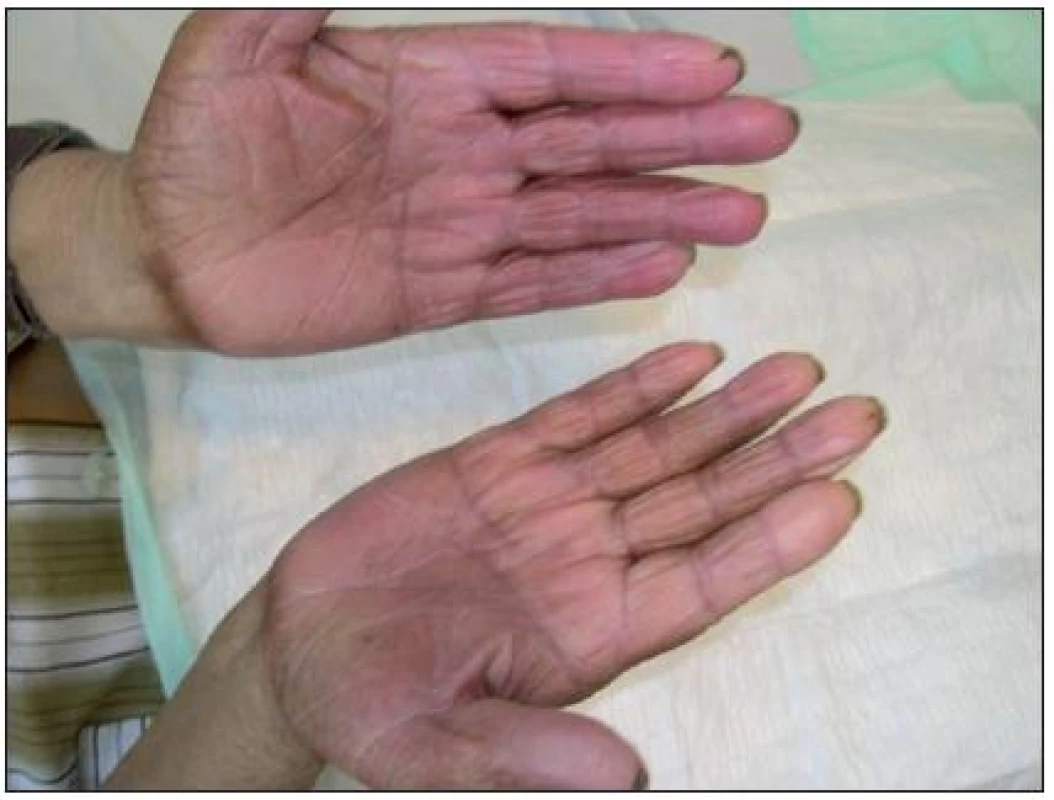
Image 2. Klinický nález při přijetí pacienta 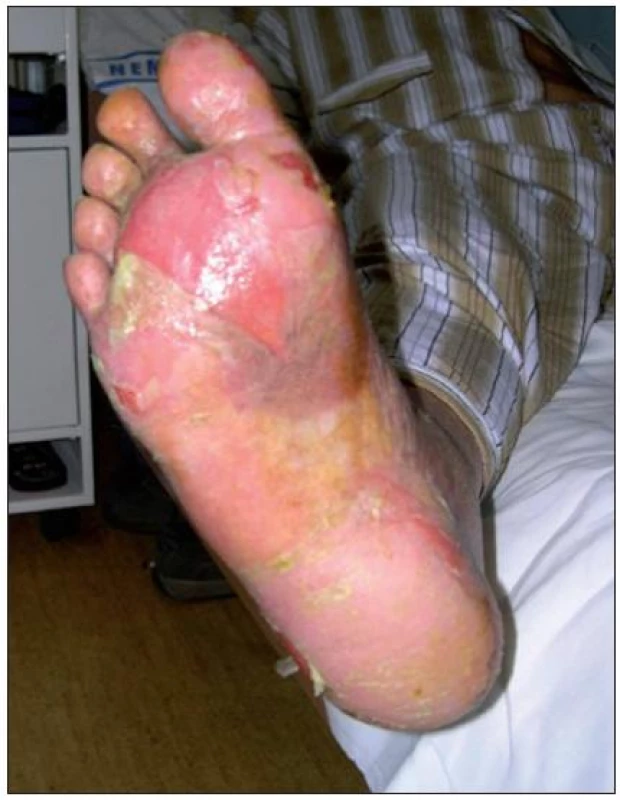
DISKUSE
Ve spojitosti s léčbou cytostatiky se setkáváme s celou řadou kožních příznaků vznikajících z různých příčin. V důsledku toxického působení vzniká řada reakcí na kůži s překrývajícími se příznaky charakterizovanými otoky, erytémy, puchýři, petechiemi či pozánětlivými hyperpigmentacemi. Popisy těchto příznaků vedly ke vzniku řady označení pro tento stav a tím tuto problematiku učinily velmi nepřehlednou nejenom pro dermatology, ale i pro ostatní specialisty pečující o onkologicky nemocné. Tato symptomatologie pod termínem palmoplantární erytrodysestezie byla v roce 1974 popsána Zuehlkem [12, 16] po preparátu Mitotan, v roce 1986 nacházíme zmínku o toxickém erytému dlaní a chodidel po preparátu Mercaptopurine v práci Coxe [5] a v literatuře je možné nalézt dvanáct různých synonym (tab. 1). Syntetický pohled na terminologii kožních chorob vznikajících vystupňovaným toxickým působením cytostatik přináší nový klinický termín „toxický erytém vyvolaný chemoterapií“, jenž zahrnuje více či méně popisné diagnózy a je v anglické literatuře uváděn pod zkratkou toxický erytém po chemoterapii (TEC) [1]. V naší literatuře je zaveden termín akrální erytém vyvolaný chemoterapií [3]. Nový klinický popisný termín TEC zahrnuje nejen výše uvedený akrální erytém, neutrofilní ekrinní hidradenitidu, ekrinní skvamózní syringometaplazii, ale i další klinické jednotky uvedené v tabulce 1 [1].
Table 1. Klinické jednotky řazené k TEC 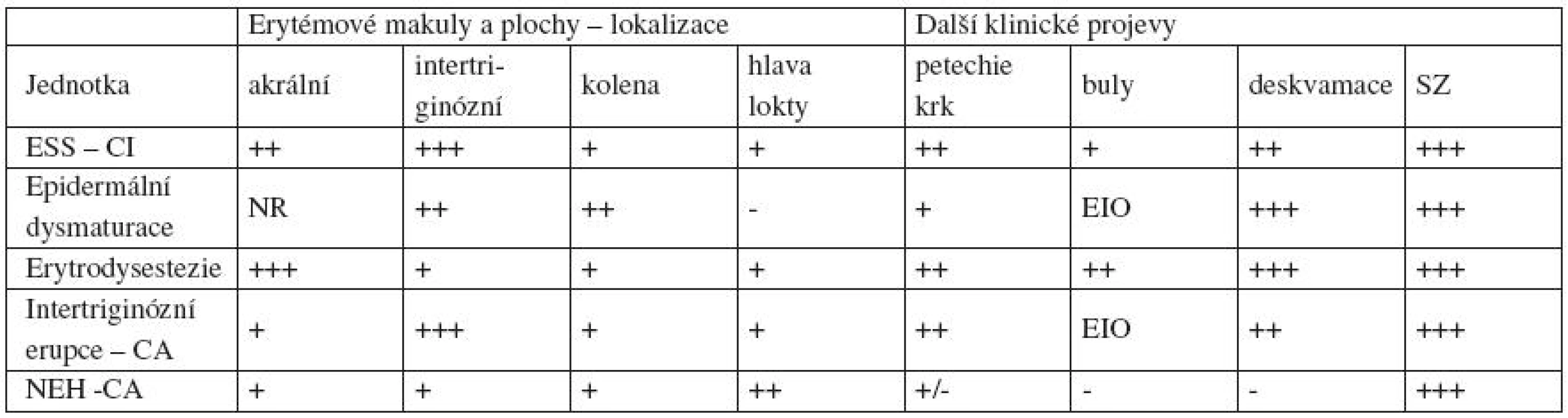
(upraveno podle Bolognia et al. [1]) ESS – ekrinní skvamózní syringometaplazie, NR – není referováno, NEH – neutrofilní ekrinní hidradenitida, EIO – eroze v intertriginozních oblastech, CA – asociovaná s chemoterapií, CI – indukovaná chemoterapií, SZ – spontánní zhojení Seznam látek způsobujících toxický erytém je obsáhlý. Nejčastěji je popisován v souvislosti s cytostatiky: capecitabinem, cytarabinem, 5-fluorouracilem, doxorubicinem či hydroxyureou [1, 3, 4, 12]. U našeho pacienta došlo ke vzniku toxického erytému v souvislosti s léčbou capecitabinem, která je indikována k adjuvantní léčbě pacientů po operaci karcinomu tlustého střeva stadia III (stadia C podle Dukese) [15]. Capecitabin působí jako perorálně podávaný prekurzor cytotoxické látky 5-fluorouracilu. Farmakodynamické působení spočívá v blokádě methylace deoxyuridinové a interferuje tak se syntézou DNA, což má za následek poruchu buněčného dělení a smrt buněk [8].
Akrální erytém vyvolaný chemoterapií je reverzibilní, vždy postihuje bilaterálně kůži dlaní a plosek, vyskytuje se v různém stupni rozvoje až u 53 % pacientů léčených capecitabinem. Z ostatních kožních, méně významných, nežádoucích účinků se vyskytují suchá kůže (7 %), alopecie (5 %), erytematózní exantém (6 %), hyperpigmentace (3 %), pruritus (3 %) a poškození nehtů (2 %) [8].
Patofyziologie akrálního erytému není přesně známa. Předpokládá se, že vyvolávajícím faktorem může být drobné trauma při běžných denních aktivitách, kdy dochází k průniku léku stěnou drobných kapilár [11]. Další hypotéza uvádí toxické působení cytostatika na vývodnou část potních žláz při jeho fyziologické sekreci, což by odpovídalo predilekčnímu postižení míst bohatých na ekrinní žlázy [1].
Histologický nález TEC je nespecifický. Nacházíme atypie keratinocytů vývodů potních žlách, metaplazii vývodů, apoptózu keratinocytů a ztrátu polarity (tab. 2) [1, 10].
Table 2. Histologický nález klinických jednotek řazených k TEC 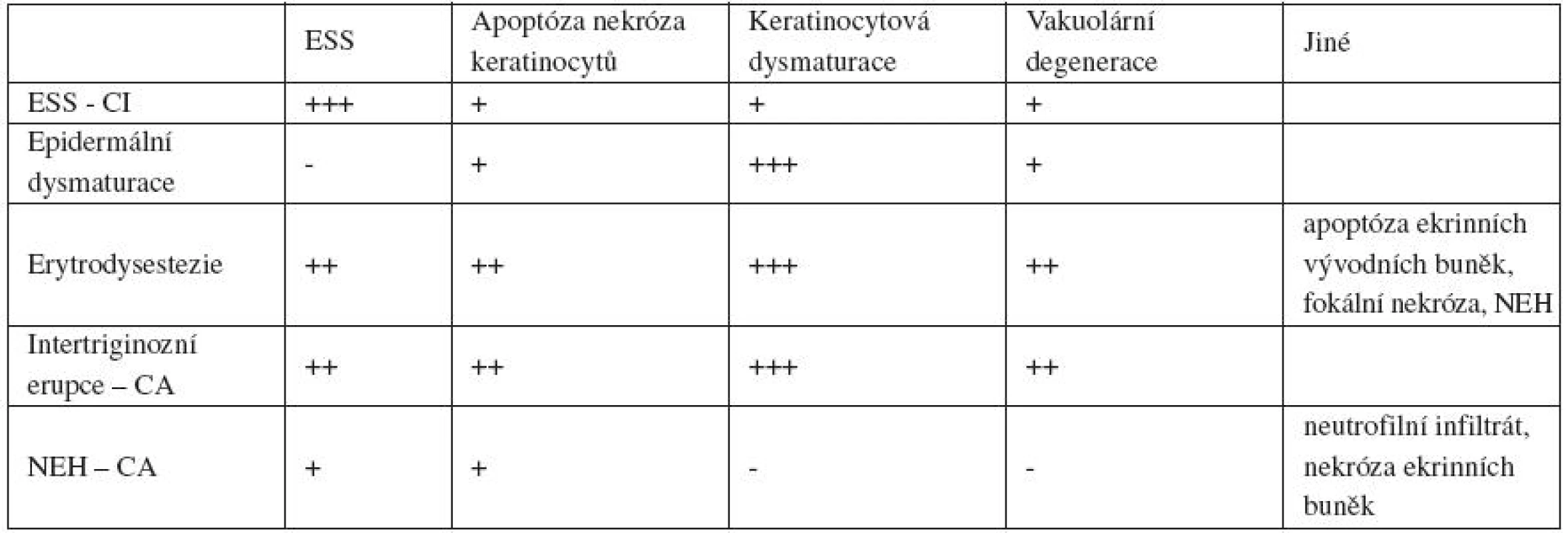
(upraveno podle Bolognia et al. [1]) ESS – epidermální skvamozní syringometaplazie, NEH – neutrofilní ekrinní hidradenitis, CA – asociovaná s chemoterapií, CI – indukovaná chemoterapií Podle míry postižení kůže a subjektivních obtíží pacienta hodnotíme klinický nález těmito třemi stupni [14]. První stupeň je definován jako dysestezie, anestezie, mravenčení rukou a nohou, nebolestivý otok nebo erytém, který nenarušuje běžné denní aktivity pacienta. Druhý stupeň je provázen bolestivým erytémem a otokem rukou a pocitem diskomfortu, který již ovlivňuje běžné denní aktivity. Třetí stupeň je charakterizován tvorbou puchýřů a výraznou bolestivostí rukou či nohou ovlivňující běžné denní aktivity. U našeho pacienta se jednalo o třetí stupeň vyskytující se u 16 % pacientů léčených capecitabinem [8].
Preventivní opatření rozvoje jsou jak nefarmakologická, tak farmakologická. Nefarmakologická prevence zahrnuje především řádnou edukaci pacienta tak, aby mohl včas rozpoznat počínající projevy toxického erytému a informovat lékaře. Pacient by se měl vyhýbat především kontaktu rukou s příliš teplou vodou, práci s ostrým a těžkým nářadím, nošení těsných bot. Vždy jsou doporučovány ochranné pracovní pomůcky a pravidelné používání ochranných krémů na ruce. V celkové léčbě byly zkoušeny různé látky. Nejčastěji jsou uváděny studie s celkově podávaným pyridoxinem nebo dexametazonem s různými výsledky [12]. Naopak znalost TEC uchrání nemocného od iracionální léčby celkovými imunosupresivy a necílenou antibiotickou léčbou odlišením od infekčního onemocnění, alergické reakce a GVHD [7]. Ke klinickému zlepšení stačí lokální léčba. Účinnost lokální aplikace 99% gelu s obsahem dimethylsulfoxidu vedoucí k rychlejšímu hojení byla taktéž předmětem klinických studií [13]. Lokální léčba odpovídá závažnosti kožních projevů a spočívá v aplikaci zvláčňujících krémů či mastí s antimikrobiální přísadou v případě infekce. Při rozvoji toxického erytému je nutné podle výše uvedeného stupně postižení redukovat dávku léku, při závažném postižení je nezbytné jeho vysazení [8].
Se stoupající incidencí kolorektálního karcinomu v naší populaci (v ČR nově diagnostikováno 8300 pacientů za rok s tímto karcinomem) lze tudíž očekávat i zvýšený výskyt akrálního erytému vyvolaného chemoterapií u pacientů přicházejících do kožních ambulancí [2, 6].
Do redakce došlo dne 26. 7. 2011.
Kontaktní adresa:
MUDr. Iva Píchová
Kožní oddělení oblastní nemocnice Kolín, a. s.
Žižkova 146
280 00 Kolín
e-mail: pichovai@seznam.cz
Sources
1. BOLOGNIA, J.,COOPER, D., GLUSAC, E. Toxic erythema of chemoterapy: A useful clinical term. J. Am. Acad. Dermatol., 2008, 59, p. 524–529.
2. ČEŠKA, R. et al. Interna. 1. vyd. Praha: Triton, 2010, s. 741. ISBN 978-80-7387-423-0.
3. CETKOVSKÁ, P., PIZINGER, K., ŠTORK, J. Kožní změny u interních onemocnění. 1. vyd. Praha: Grada Publishing, 2010, s. 177. ISBN 978-80-247-1004-4.
4. CETKOVSKÁ, P., PIZINGER, K. Kožní změny při chemoterapii hematologických nemocí. Čes-slov Derm., 2001, 76, 4, s. 199.
5. COX, G. J., ROBERTSON, D. B. Toxic erythema of palms and soles associated with hig-dose mercaptopurine chemotherapy. Arch. Dermatol., 1986, 122, p. 1413–1414.
6. DUŠEK, L., MUŽÍK, J., KUBÁSEK, M., KOPTÍKOVÁ, J., ŽALOUDÍK, J., VYZULA, R. Epidemiologie zhoubných nádorů v České republice [online]. Dostupný na www: www.kolorektum.cz
7. FABIAN, C. J., MOLINA, R., SLAVÍK, M. Pyridoxine therapy for palmar-plantar erythrodysesthesia associated with continous 5-fluorouracil infusion. Invest. New Drugs, 1990, 8, 1, p. 57–63.
8. KUBECOVÁ, M. Capecitabine. Čes-slov Farmakoterapie, 2005, Suppl. 1, s. 49–51.
9. LOKICH, J. J., MOORE, C. Chemotherapy-associated palmar-plantar erythrodysesthesia syndrome. Ann. Intern. Med., 1984, 101, 6, p. 798–799.
10. LORRUSO, D., DI STEFANO, A., CARONE, V., FAGOTTI, A., PISCONTI, S., SCAMBIA, G. Pegylated liposomal doxorubicin-related palmar-plantar erythrodysesthesia, (‘hand-foot’ syndrome). Annals of Oncology, 2007, 18, 7, p.1159–1164. doi:10.1093/annonc/mdl477.
11. MILANO, G., ETIENNE-GRIMALDI, M.-C., MARI, M. et al. Candidate mechanisms for capecitabine related hand-foot syndrome. Br. J. Clin. Pharmacol., 2008, 66, 1, p. 88–95.
12. MIŇOVSKÁ,V. Palmoplantární erytrodysestezie vyvolaná liposomálním doxorubinem. Čes.-slov. Derm., 2003, 78, 4, s. 159–161.
13. NAGORE, E., INSA, A., SANMARTIN, O. Antineoplastic therapy-induced palmar plantar erythrodysesthesia (‘hand-foot’) syndrome: incidence, recognition and management. Am. J. Clin. Dermatol., 2000, 1, 4, p. 225–234.
14. XELODA produktová monografie. Dostupný na www: www.xeloda.cz.
15. VORLÍČEK, J. Klinická onkologie. 2. díl, 1. vyd. MU Brno, 1996, s. 482, ISBN 80-2101257-9.
16. ZUEHLKE, R. L. Erythematous eruption of palms et soles associated with mitotane therapy. Dematologica, 1974, 148, s. 90–92.
Labels
Dermatology & STDs Paediatric dermatology & STDs
Article was published inCzech-Slovak Dermatology

2011 Issue 5
Most read in this issue- Chlamydiové infekce
- Toxický erytém vyvolaný chemoterapií
- Scabies crustosa u dojčaťa
-
Léčba psoriázy v roce 2011
(komentovaný přehled novinek z amerických a německých doporučených postupů se zaměřením na ustekinumab)
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

