-
Medical journals
- Career
Analýza tkáňové exprese proteomu cervikálního hlenu
Authors: Jan Vodička 1; J. Dostál 1; D. Holub 2; Radovan Pilka 1; P. Džubák 2; M. Hajdúch 2; T. Oždian 2
Authors‘ workplace: Porodnicko-gynekologická klinika LF UP a FN Olomouc 1; Ústav molekulární a translační medicíny, LF UP v Olomouci 2
Published in: Ceska Gynekol 2023; 88(1): 4-12
Category: Original Article
doi: https://doi.org/10.48095/cccg20234Overview
Cervikální hlen je viskózní kapalina fungující jako zátka děložního čípku. V cervikálním hlenu můžeme detekovat produkty endometriálních a cervikálních žláz. Cervikální hlen je dále obohacen transudátem pocházejícím z vejcovodů a proteiny pocházející z vaječníků, peritonea a vzdálených tkání. Se zvyšující se hladinou ovariálních estrogenů se vlastnosti cervikálního hlenu mění tak, že umožňují snadnější odběr a zpracování. Z tohoto důvodu jsme vybrali skupinu deseti pacientek léčených kontrolovanou ovariální hyperstimulací pro in vitro fertilizaci v centru asistované reprodukce. Tato studie se zaměřuje na proteomickou charakterizaci cervikálního hlenu a na buněčnou a tkáňovou lokalizaci identifikovaných proteinů. Nejvíce intenzivními proteiny identifikovanými v cervikálním hlenu jsou muciny, ale bylo nalezeno také mnoho méně abundantních proteinů vnitrobuněčného původu. Analýza tkáňových expresí odhalila mnoho proteinů, které jsou kromě tkání ženských reprodukčních orgánů exprimovány také v jiných tkáních a mimo jiné také proteiny specifické pro varlata, játra, placentu, oční sítnici a mozeček. Tato studie dále potvrzuje vhodnost cervikálního hlenu jako zdroje proteomických biomarkerů nejen pro diagnostiku ženského reprodukčního traktu.
Klíčová slova:
proteomika – cervikální hlen – tkáňové exprese
Úvod
Cervikální hlen je glykoproteinový gel tvořený žlázami děložního krčku. Je složen z vody (90–98 %), organických a anorganických látek, mucinů, polysacharidů, proteinů a lipidů [1]. V roce 1970 popsali Insler et al možnosti použití cervikálního hlenu při určování periovulační periody pomocí snížení viskozity a zvýšení vazkosti v závislosti na zvýšené hladině estrogenů [2]. V této fázi cyklu je viskozita hlenu snížena pro umožnění průchodu spermií. Cervikální hlen vykazuje parametry směsné tekutiny tím, že děloha funguje také jako svalově kontraktilní orgán nejen v období těhotenství a porodu. Děložní kontrakce ve formě peristaltických vln umožněných architekturou svalové vrstvy myometria a závislých na hladině hormonů v průběhu menstruačního cyklu byly popsány Kunzem et al v roce 2002 [3]. Během periovulační fáze napomáhá peristaltická aktivita dělohy průchodu spermií i vajíčka. Díky této peristaltické vlastnosti a díky relativní otevřenosti ženského reprodukčního orgánu může být cervikální hlen obohacen také o proteiny secernované jinými tkáněmi, což může být díky snadnosti odběru tohoto hlenu zajímavé pro budoucí hledání neinvazivních biomarkerů.
V naší předchozí práci [4] byl charakterizován cervikální hlen zdravých žen z hlediska proteinového složení a základních proteinových funkcí. Zajímavým zjištěním bylo nalezení velkého množství intracelulárních a imunitních proteinů. V této práci chceme s využitím bioinformatiky a porovnáním získaných výsledků se známými tkáňovými expresními profily rozšířit předchozí studii a zjistit tkáňový původ proteinů identifikovaných v cervikálním hlenu.
Materiál a metody
Charakteristika pacientek
Do studie byly zařazeny pacientky centra asistované reprodukce Fakultní nemocnice v Olomouci. Podmínkou zařazení byl podepsaný informovaný souhlas, řízená ovariální stimulace s cílem odběru oocytů, fertilizace a embryotransferu. Věk při odběru oocytů < 37 let, body mass index 19–29 kg/m2, žádné genetické, a/nebo endokrinní, a/nebo metabolické, a/nebo imunologické, anebo onkologické onemocnění v anamnéze. Pacientky měly předpokládanou dobrou ovariální rezervu dle hormonálního profilu. Vyloučeny ze studie byly pacientky s nálezem strukturálních změn pánevních orgánů a dále pacientky s prokázaným syndromem polycystických vaječníků, pacientky s těžkou formou endometriózy (III.–IV. ASRM – American Society for Reproductive Medicine) a kuřačky. Vylučovacím kritériem byly opakované (> 2) potraty, délka sterility > 5 let a více než dvě implantační selhání v předchozích léčebných IVF (in vitro fertilizace) cyklech.
Odběr cervikálního hlenu
Všechny pacientky podstoupily řízenou ovariální stimulaci pro IVF/ICSI/ET. Dle standardů byla provedena gonadotropní stimulace ovarií s hypofyzární supresí analogy gonadoliberinu. Při dosažení optimální velikosti vedoucí kohorty folikulů byl proveden triggering subkutánní aplikací 7 500 IU choriového gonadotropinu. Odběr oocytů byl naplánován 36 hod po jeho podání. Odběr cervikálního hlenu byl proveden bezprostředně před odběrem oocytů. Po inzerci poševních zrcadel v litotomické poloze byl neonatální pupečníkovou cévkou CP-01 (Gama Group, cat. No. V646958-ND) a stříkačkou aspirován cervikální hlen. Vzorky byly bezprostředně přeneseny do pejet se šroubovacím uzávěrem (SSI-bio, katalogové číslo 2320-00) a zamrazeny. Údaje o pacientkách byly uloženy v interně vyvinuté databázi ClinData (k dispozici na adrese clindata.imtm.cz) vytvořené pro ukládání klinických informací o lidských vzorcích.
Příprava vzorků pro proteomickou analýzu
Vzorky cervikálního hlenu byly rozpuštěny a zpracovány dle publikovaného protokolu [4] v 1 ml 100 mm Tris-HCl, 100 mm DTT, 4% SDS, pH 7,6 pufru a sonikovány jehlovým sonikátorem Bandelin sonopuls. Rozpuštěné vzorky byly zpracovány metodou multienzymové digesce na filtru (MED-FASP) dle Wiśniewského et al [5]. Získané peptidy byly přečištěny metodou Stop and Go extrakce (STAGE tips) [6], vysušeny ve vakuové centrifuze a rozpuštěny v 0,05% trifluorocytové kyselině ve vodě pro následující hmotnostně spektrometrickou (LC/MS) analýzu.
LC/MS analýza
Jeden mikrogram připraveného peptidového digestu byl separován kapalinovým chromatografem Dionex UltiMate 3000 spojeným s hmotnostním spektrometrem Thermo Orbitrap Fusion skrze iontový zdroj Proxeon Easy-Spray. Nano-HPLC separace probíhala na předkoloně Acclaim PrepMap 100 (100 μm × 2 cm, C18, 5 μm, 100 A) a analytické koloně PepMap RSLC (75 μm × 50 cm, C18, 2 μm, 100 A). Nanášení vzorku probíhalo s použitím loadovací pumpy s průtokem 6 µl.min–1 a použitím vody s 1% acetonitrilem a 0,05% trifluorooctovou kyselinou. Separace probíhala pomocí nanopumpy s průtokem 300 nl.min–1 a gradientem 2–40% B do 125 min ze 165 min celkové doby analýzy. Po 125. minutě následoval proplach pomocí 90% B a ekvilibrace 2% B po dobu 30 min. Mobilní fáze byly voda s 0,1% mravenčí kyselinou (A) a acetonitril s 0,1% mravenčí kyselinou (B). Hmotnostní spektrometr byl nastaven v režimu data dependentní akvizice se sběrem fragmentačních dat po dobu 3 s. Rozlišení orbitrapu bylo nastaveno na 120 000 a hmotnostní rozsah na 350–1 500. Fragmentace spekter probíhala v lineární iontové pasti s HCD (higher-energy C-trap dissociation) aktivací.
Vyhledání proteinů a statistická analýza
Zpracování hrubých dat vč. generování seznamů peaků a vyhledávání proteinů bylo provedeno v programu Thermo ProteomeDiscoverer 2.5 s nastavením popsaným dříve [4]. Základní statistické zpracování bylo kalkulováno v programech Thermo ProteomeDiscoverer 2.5 a Microsoft Excel.
Bioinformatická analýza
Bioinformatická analýza se skládala z několika kroků. V prvním kroku byla zjištěna buněčná lokalizace porovnáním identifikovaných proteinů proti databázi QuickGO (www.ebi.ac.uk/QuickGO). Pro stanovení možné tkáňové exprese proteinů jsme vybrali databázi Human protein atlas [7], která obsahuje proteinové a traskriptomické expresní data pro soubor lidských tkání. Normalizované exprese nTPM (normalized Trascript Per Million) byly získány ze stránky proteinatlas.org 9. 9. 2022. Výsledný soubor identifikovaných proteinů z našeho experimentu byl poté spojen s touto databází pomocí MS Excel na základě genového jména. Pro účely přímého porovnání exprese mezi tkáněmi jsme se rozhodli nTPM realtivizovat tak, že byl vytvořen poměr mezi každou tkání v databázi a tkání, kde měl daný transkript nejvyšší expresi. To nám umožnilo posoudit tkáňovou expresi díky snadným cut-off. V prvním experimentu jsme sledovali distribuci proteinů v jednotlivých tkáních seřazením relativních expresí od nejnižšího po nejvyšší a na základě zkušeností z tohoto experimentu jsme přistoupili k experimentu druhému. Pro všechny tkáně jsme vyexportovali pouze geny s relativní expresí rovnou 1 (tj. nejvyšší) a tyto proteiny jsme na základě zkušeností s databází dělili na konstitutivně exprimované (ve > 10 ostatních tkáních přesáhla relativní exprese hladiny 0,3), skupinově obohacené (v < 10 ostatních tkáních přesáhla relativní exprese hladiny 0,3) a tkáňově specifické (v žádné další tkáni nepřesáhla relativní exprese hladiny 0,3).
Výsledky
Pacientky
Soubor tvořilo deset pacientek vyhovujících kritériím. Nezaznamenali jsme statisticky významné rozdíly ve věku, hmotnosti, ovariální rezervě a délce sterility u pacientek. Hlavními indikacemi pro léčbu IVF metodami byly mužský faktor, tubární faktor a idiopatický faktor sterility. Průměrný počet oocytů získaných ve stimulaci byl 15 (7–21). Hladiny estradiolu v den triggeringu hCG byl v průměru 9 600 pmol/l (2 800–19 330 pmol/l). Výška endometria byla v průměru 10,4 mm (9–14 mm). U žádné z pacientek se nerozvinula časná forma ovariálního hyperstimulačního syndromu a u všech deseti byl proveden elektivní single embryo transfer vysoce kvalitní blastocysty. Ve skupině otěhotnělo šest žen, četnost těhotenství 60 %. Charakteristika pacientek je shrnuta v tab. 1.
Table 1. Charakteristika souboru pacientek.
Tab. 1. Characteristics of the group of patients.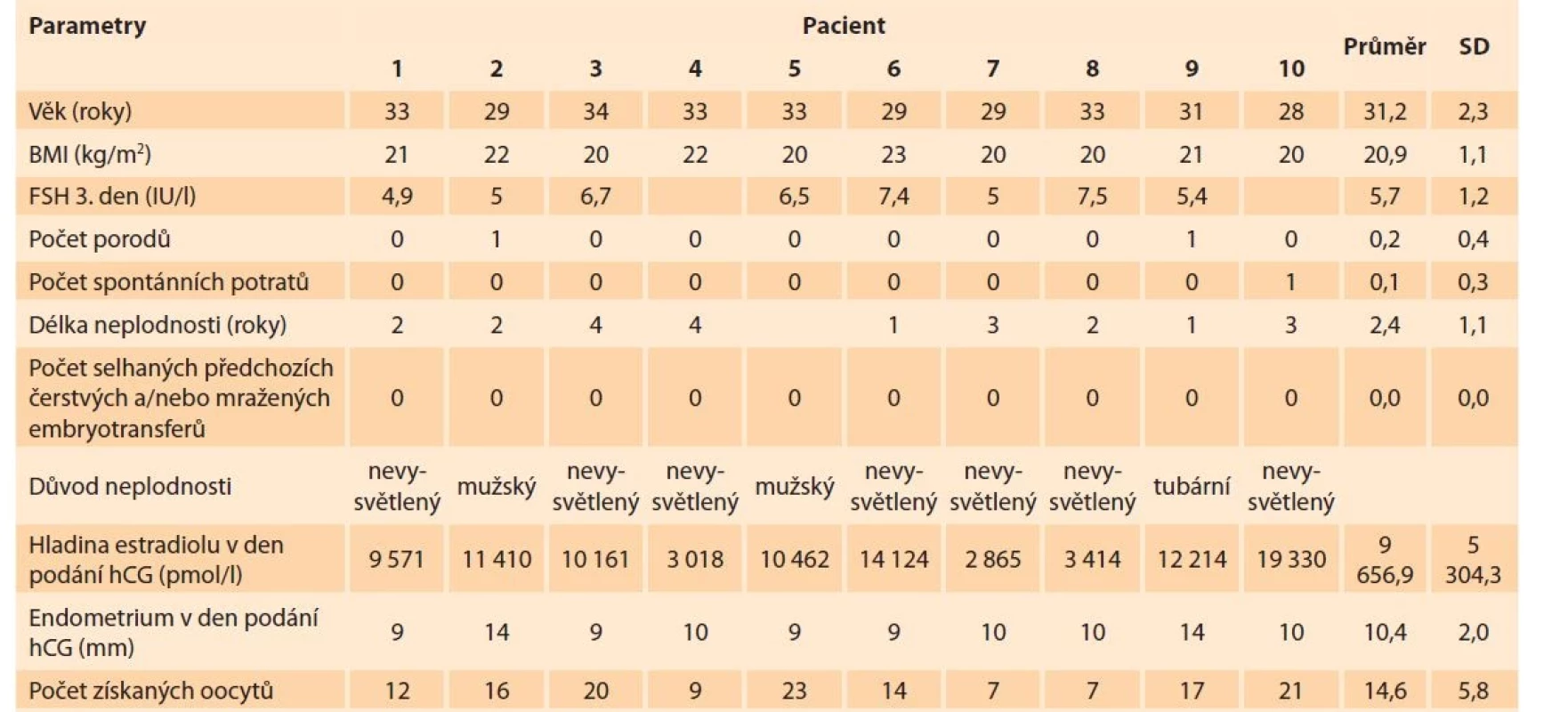
BMI – body mass index, FSH – folikulostimulační hormon, hCG – choriogonadropin, SD – směrodatná odchylka LC/MS
Při LC/MS analýze jsme analyzovali deset pacientských vzorků ve třech technických replikátech. S použitím programu ProteomeDiscoverer 2.5 jsme identifikovali 25 521 peptidových skupin v celém souboru a průměrně 11 265 ± 2 362 peptidů na vzorek (obr. 1A). Z těchto peptidů bylo složeno v průměru 1 847 ± 430 proteinů na vzorek a celkem 4 486 unikátních proteinů s vysokým hodnocením. Hmotnostně spektrometrická data a výsledky vyhledávání jsou dostupné na dotaz autorům.
Image 1. Proteomická charakteristika analyzovaného souboru. (A) jsou porovnány počty peptidů identifikovaných v jednotlivých vzorcích jako průměr ze tří technických replikátů ± směrodatná odchylka. (B) jsou stejným způsobem prezentovány počty proteinů identifikovaných v jednotlivých vzorcích.
Fig. 1. Proteomic characteristics of the analyzed set. (A) the numbers of peptides identified in individual samples are compared as the mean of three technical replicates ± standard deviation. (B) the numbers of proteins identified in individual samples are presented in the same way.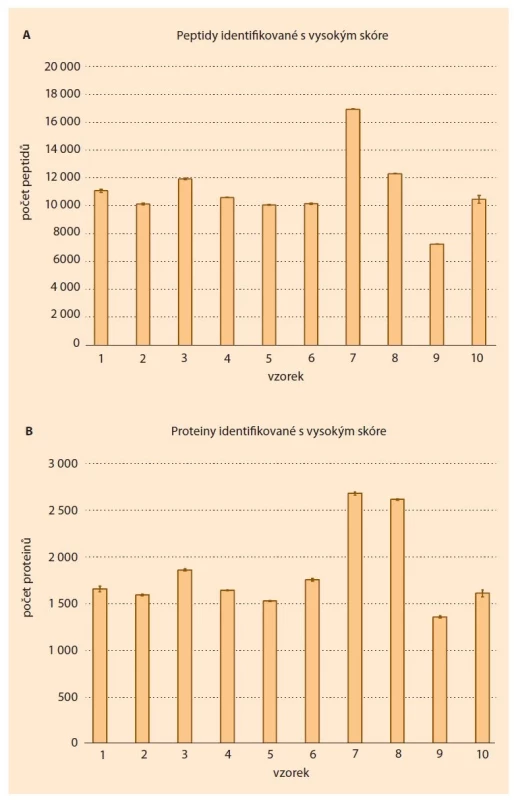
Lokalizace proteinů v buněčných organelách
Analýza vnitrobuněčné lokalizace proteinů byla provedena na základě složky „cellular localization“ databáze Gene Ontology (GO). Abychom mohli poskytnout přehlednou vizualizaci, ponechávali jsme u každého proteinu jen hesla položená nejvýše na úrovni organel. Výsledkem této analýzy bylo stanovení 22,3 % proteinů s jadernou lokalizací, 16,7 % s extracelulární a 16 % s cytoplasmickou (obr. 2). Zbytek organel byl zastoupen s četností < 10 %, jako např. mitochondrie s 8,2 % nebo membrány se 7,7 %. Tato analýza poskytuje informaci o četnosti proteinů v jednotlivých organelách a nezohledňuje intenzitu jednotlivých proteinů. Při zahrnutí mediánu intenzity identifikovaných proteinů pro jednotlivé organely vypadá celkový obraz trochu jinak (obr. 2B) a zobrazuje extracelulární a secernované proteiny jako více intenzivní a intracelulární organely s podobnou, ale celkově nižší intenzitou.
Image 2. Analýza buněčných komponent dle Gene Ontology (GO) zastoupených mezi proteiny identifikovanými v cervikálních hlenech. (A) poskytuje procentní zastoupení jednotlivých organel v proteomu a (B) přidává informaci o mediánu intenzity proteinů v těchto organelách zastoupených. Z důvodu kompatibility s databází jsou názvy buněčných komponent ponechány v původním znění.
Fig. 2. Gene Ontology (GO) analysis of cellular components represented among proteins identified in cervical mucus. (A) provides the percentage representation of individual organelles in the proteome and (B) adds information about the median intensity of the proteins represented in these organelles. For compatibility with the database, the cell component names are left as they were.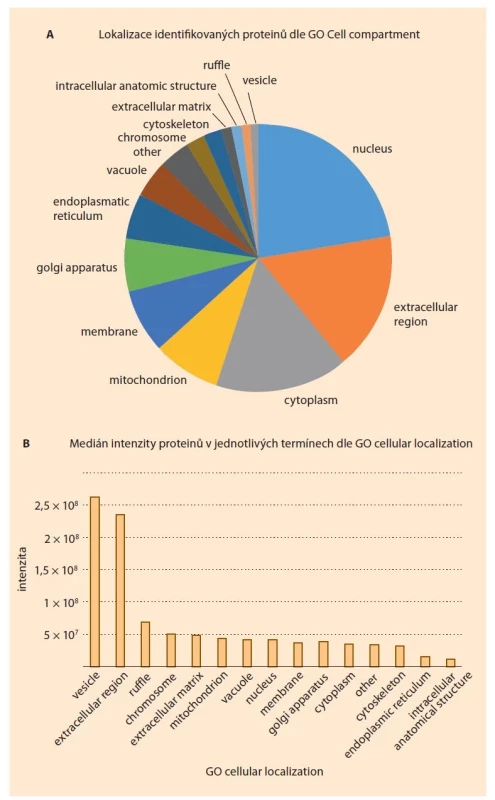
Tkáňová lokalizace identifikovaných proteinů
Jedna z výzkumných otázek byla, odkud pocházejí proteiny identifikované ve vzorcích z cervikálního hlenu. Pro tento účel jsme nalezli vhodnou databázi Human Protein Atlas (proteinatlas.org) [7]. Tato databáze obsahuje transkriptomická expresní data jednotlivých genů v různých tkáních. Architektura databáze je nastavena pro porovnání exprese jednotlivých genů mezi tkáněmi na jednotlivé úrovni a nikoli ve větším měřítku. Proto jsme se souhlasem Dr. Oksvolda přistoupili k relativizaci vstupních dat a umožnění takového porovnání i na úrovni proteomu. Výsledkem první aproximace ve zpracování těchto výsledků je distribuce relativní exprese proteinů ve zvolených tkáních (obr. 3). V tomto obrázku je distribuce relativních proteinových expresí ve zvolených tkáních, jejichž produkty můžeme očekávat v cervikálním hlenu.
Image 3. Distribuce relativní genové exprese ve vybraných tkáních. Distribuční graf ukazuje u většiny vybraných tkání velmi málo vysoce exprimovaných proteinů, většina proteinů je exprimována na střední úrovni a okolo 20 % proteinů má relativní expresi pod 0,1, kterou považujeme za hranici, že protein je pravděpodobněji exprimován v jiné tkáni. Z důvodu kompatibility s databází jsou názvy tkání ponechány v původním znění.
Fig. 3. Distribution of relative gene expression in selected tissues. The distribution graph shows very few highly expressed proteins in most of the selected tissues, most of the proteins are expressed at a medium level and about 20% of the proteins have a relative expression below 0.1, which we consider as the limit that the protein is more likely to be expressed in another tissue. For compatibility with the database, tissue names are left as they were.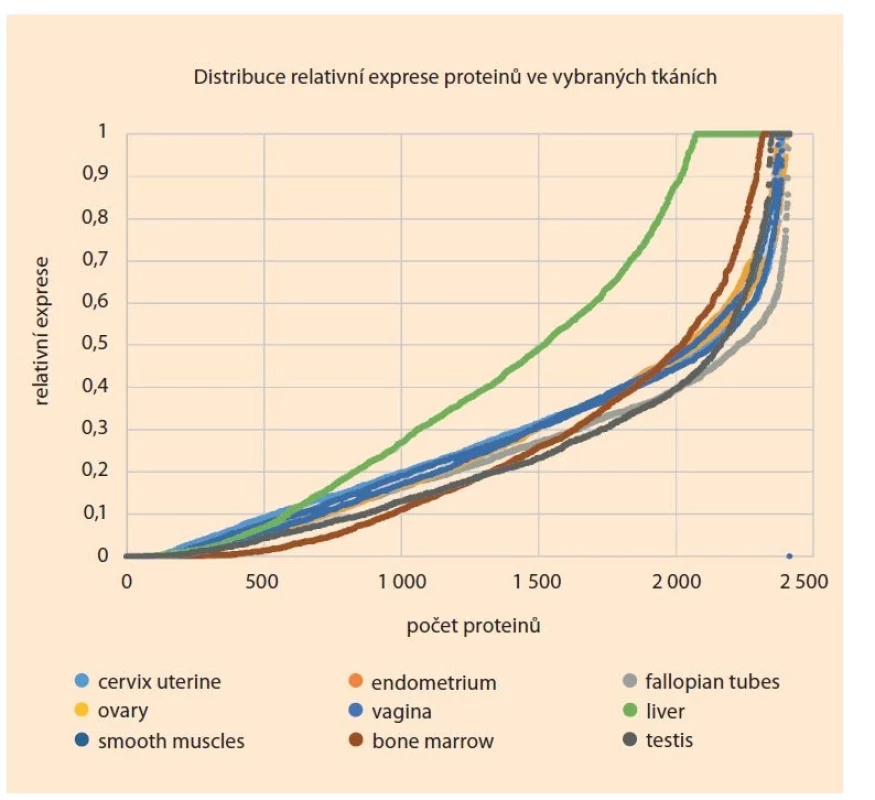
Z distribučního grafu vyplývá, že v zájmových tkáních bylo exprimováno jen málo proteinů na vysoké úrovni. Jedinou výjimkou byla játra, kde mělo maximální expresi 14 % proteinů. V děložním čípku mělo maximální expresi 2,2 % proteinů, v endometriu 2,4 % proteinů, ve vejcovodech 0,7 % proteinů, ve vaječnících 3,9 %, ve vagině 2,5 %, v hladkých svalech 1,5 %, v kostní dřeni 3,9 % a ve varlatech 2,6 % proteinů s maximální expresí.
Na druhou stranu jsme identifikovali 22,4 % proteinů s relativní expresí < 0,1 u tkání děložního krčku, 28,9 % v endometriu, 28,9 % ve vejcovodech, 30,2 % ve vaječnících, 25,5 % ve vagině, 8,5 % v játrech, 11,4 % v hladkých svalech, 18,9 % v kostní dřeni a 9,9 % ve varlatech. Relativní exprese < 0,1 naznačuje, že tyto proteiny byly s největší pravděpodobností tvořeny někde jinde.
Výsledky z obr. 4 naznačují, že většina proteinů identifikovaných v cervikálním hlenu patří buď ke konstitutivně exprimovaným proteinům, nebo že mohou být secernovány v jiných tkáních v souladu s hlavní hypotézou, že cervikální hlen je směsná tekutina obohacená o sekrece z jiných orgánů. Abychom byli schopni tyto jiné orgány identifikovat, exportovali jsme do tab. 2 všechny proteiny, které měly v dané tkáni relativní expresi 1 – tedy byly zde nejvíce exprimované.
Table 2. Počet specifických proteinů identifikovaných pro rozdílné tkáně. V prvním sloupci jsou počty proteinů s maximální relativní expresí v dané tkáni. V druhém sloupci jsou proteiny obohacené ve skupině tkání a v posledním sloupci jsou proteiny specifické pro konkrétní tkáně. Z důvodu kompatibility s databází jsou názvy tkání ponechány v původním znění.
Tab. 2. Number of specific proteins identified for different tissues. In the first column are the numbers of proteins with maximum relative expression in the given tissue. The second column shows proteins enriched in a group of tissues, and the last column shows tissue-specific proteins. For compatibility with the database, tissue names are left as they were.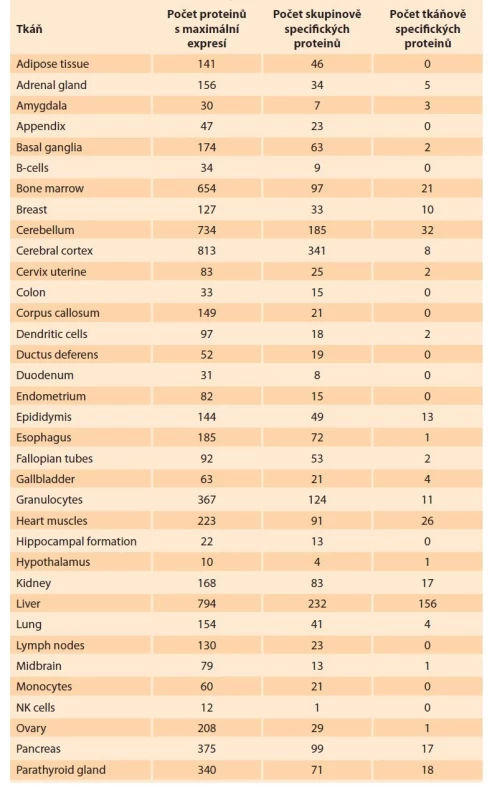
Tab. 2 – pokračování. Počet specifických proteinů identifikovaných pro rozdílné tkáně. V prvním sloupci jsou počty proteinů s maximální relativní expresí v dané tkáni. V druhém sloupci jsou proteiny obohacené ve skupině tkání a v posledním sloupci jsou proteiny specifické pro konkrétní tkáně. Z důvodu kompatibility s databází jsou názvy tkání ponechány v původním znění.
Tab. 2 – continuing. Number of specific proteins identified for different tissues. In the first column are the numbers of proteins with maximum relative expression in the given tissue. The second column shows proteins enriched in a group of tissues, and the last column shows tissue-specific proteins. For compatibility with the database, tissue names are left as they were.
Z dat v tab. 2 vyplývá, že průměrně 205 proteinů identifikovaných v cervikálním hlenu mělo maximální expresi v každé tkáni. Na základě manuálního průzkumu databáze proteinatlas.org a souboru proteinů použitého pro výpočet byly určeny tři hlavní typy proteinů, které se v databázi vykytují:
- proteiny, které jsou exprimovány konstitutivně a jejich maximální exprese v kterékoli tkáni je dílem statistiky, protože v ostatních tkáních se vyskytují v podobné míře;
- proteiny, které se vyskytují ve skupině tkání s podobnými vlastnostmi;
- proteiny, které jsou exprimovány specificky v jedné tkáni a v ostatních minimálně.
Proto jsme stanovili kritéria popsaná v metodice pro odlišení těchto skupin a dále se zaměřili primárně na tkáňově specifické proteiny, protože nám o přítomnosti proteinů pocházejících z jiných tkání než ženských reprodukčních orgánů mohou napovědět nejvíce.
Jak je znázorněno v tab. 2, nejvíce tkáňově specifických proteinů nebylo pozorováno v orgánech ženských reprodukčních orgánů. Nejvíce tkáňově specifických proteinů bylo pozorováno s původem ve varlatech (433 proteinů), kosterních svalech (192 proteinů) a játrech (156 proteinů). V menší míře jsme našli proteiny specifické pro placentu (56 proteinů), oční sítnici (46 proteinů) a mozeček (32 proteinů). Z ženských reprodukčních orgánů byly v analyzovaném souboru nalezeny tři proteiny specifické pro vaginu, dva proteiny specifické pro děložní krček, dva proteiny specifické pro vejcovody a jeden protein specifický pro vaječníky.
Diskuze
Hlavním cílem této studie bylo zjistit, které další tkáně přispívají k proteinovému složení cervikálního hlenu. Pro tyto účely jsme provedli celkem dvě analýzy. Oproti předchozí studii jsme rozšířili analýzu buněčných komponent a porovnali jsme získané výsledky s databází transkriptomických expresí proteinů v jednotlivých tkáních.
Detailní analýza buněčné komponenty nepřinesla nová zjištění v poměru intracelulárních proteinů vůči proteinům secernovaným. Kvantitativní analýza jednotlivých komponent ale potvrdila, že secernovaných proteinů je méně druhů, ale jsou intenzivněji zastoupené.
Na základě analýzy tkáňových expresních profilů jsme zjistili, že většina proteinů identifikovaných v cervikálním hlenu patří mezi konstitutivně exprimované a proteinů tkáňově specifických pro orgány ženského reprodukčního bylo identifikováno minimum.
Nejvyšší množství tkáňově specifických proteinů jsme nalezli pro varlata (433 proteinů). Jejich předpokládaným zdrojem jsou spermie a ejakulát pronikající do cervikálního hlenu postkoitálně. Ejakulát jako komplexní směs sekretů pocházejících z varlat, semenných váčků a přídatných žláz působí jako výživné, transportní a pufrovací medium s alkalickým pH, které definuje hlavní funkci sekretu [8]:
- ochranu spermií před kyselým poševním prostředím;
- metabolickou podporu spermií;
- zkapalnění.
Experimenty na modelech hlodavců demonstrují klíčovou úlohu ejakulátu pro implantaci embrya a optimální vývoj placenty. Semenná tekutina podporuje migraci leukocytů a tvorbu regulačních Th buněk, které usnadňují implantaci embrya potlačením zánětu, napomáhá adaptaci endometriálních arteriol a udržuje toleranci fetálních antigenů [9]. Tyto biologické mechanizmy mohou v klinickém významu podpořit vyšší pravděpodobnost otěhotnění v IVF/ET cyklech, v nichž dojde během stimulace ovarií k pohlavnímu styku s ejakulací do pochvy [10].
Je obtížné vysvětlit zastoupení většího množství proteinů specifických pro kosterní svalstvo (192 proteinů). Děloha a pochva jsou tvořeny hladkou svalovinou. Přítomnost proteinů původem hladkého svalstva v našem souboru je však nižší. Pro náš nález mohou existovat tři vysvětlení. První je, že databáze není zcela dokončena a proteiny popisované jako specifické pro kosterní svalstvo by bylo možné v budoucnu vidět i v hladkém svalstvu. Druhé vysvětlení je, že se proteiny kosterního svalstva mohou v cervikálním hlenu vyskytovat, doposud však nebylo žádné podobné zjištění publikováno. Posledním vysvětlením může být, že se jedná o artefakt vzniklý při odběru nebo zpracování vzorků. I zde se jedná o chabé vysvětlení, neboť kontaminace při odběru by pocházely z cervikálního a vaginálního epitelu a kontaminace při zpracování z kůže a vlasů.
Další tkání s vysokým zastoupením specifických proteinů byla játra (156 proteinů). V játrech je produkováno velké množství plazmatických proteinů [11] a současně v ženském reprodukčním traktu probíhá řada imunitních reakcí. Jsou zprostředkovány proteiny a cytokiny imunitního systému. Většina těchto proteinů v cervikálním hlenu je jaterního původu [12].
Přítomnost placentárních proteinů v cervikálním hlenu popsali Pockley et al v roce 1989 [13], který prokázal, že placentární proteiny působí supresivně. Tyto imunosupresivní faktory v cervikálním hlenu mohou chránit spermie a embryo v potenciálně hostilním prostředí ženského reprodukčního traktu. Je známo, že moduly spojené s imunitou jsou často exprimovány společně. Hees et al (2020) potvrdili imunitní moduly v mnoha tkáních, jako jsou játra, kůra ledvin, plíce, děloha, podkožní tuk a viscerální omentum. Tento koncept může vysvětlovat vysokou tkáňovou expresi placentárních proteinů v cervikálním hlenu [14].
Posledními tkáněmi s vysokým zastoupením specifických proteinů v cervikálním hlenu byla oční sítnice a mozeček. Přítomnost proteinů z těchto tkání by se dala vysvětlit jednoduše – v databázi nejsou proteiny periferních nervů ani nervů reprodukčního systému vedeny samostatně. Děloha je bohatě inervovaným orgánem. Je inervována četnými senzorickými, parasympatickými, sympatickými a peptidergními neurovlákny. Jejich distribuce je ve stromatu a kolem cévních stěn, ve vrstvách myometria a endometria. Imunohistochemická studie prokázala lokalizaci a kvantitativní distribuci neuronálních vláken ve fundu, těle a děložním čípku mladých žen ve fertilním věku [15]. Ženský reprodukční systém je úzce závislý na hormonální stimulaci. Nicméně autonomní inervační systém spolu s hormonální regulací je úzce provázán v regulaci fyziologických procesů v ženském reprodukčním traktu [16]. Tato skutečnost by mohla vysvětlit vysoký podíl peptidů neuronálního původu v naší studii. Protože v databázi nejsou nervy přítomné v děloze zavedeny, mohou mít nervově specifické proteiny falešně pozitivní lokalizaci v jiných nervových tkáních.
Závěr
V této studii jsme provedli analýzu proteomických dat se zaměřením na tkáně jejich možné exprese. Analýza tkáňové exprese dle proteinatlas.org nebyla podle naší literární rešerše v podobném měřítku provedena. Nejvíce tkáňově specifických proteinů však bylo pozorováno z jiných tkání než z ženských reprodukčních orgánů. To může naznačovat nízkou unikátnost proteinů secernovaných do cervikálního hlenu.
Hmotnostně spektrometrická a ostatní proteomická data jsou přístupná na vyžádání u autorů.
ORCID autorů
J. Vodička 0000-0003-0446-4454
J. Dostál 0000-0001-5070-0812
D. Holub 0000-0002-0750-6077
R. Pilka 0000-0001-8797-1894
P. Džubák 0000-0002-3098-5969
M. Hajdúch 0000-0002-4834-908X
T. Oždian 0000-0002-5756-6297
Doručeno/Submitted: 20. 1. 2023
Přijato/Accepted: 26. 1. 2023
Mgr. Tomáš Oždian, Ph.D.
Ústav molekulární a translační medicíny
LF UP v Olomouci
Hněvotínská 3
779 00 Olomouc
Sources
1. Crha K, Ventruba P, Žáková J et al. Cervical mucus and its role in reproduction. Ceska Gynekol 2020; 85 (5): 333–338.
2. Insler V, Melmed H, Eichenbrenner I et al. The cervical score: a simple, semi-quantitative method for monitoring of the menstrual cycle. Int J Gynecol Obstet 1972; 10 (6): 223–228. doi: 10.1002/j.1879-3479.1972.tb00857.x.
3. Kunz G, Leyendecker G. Uterine peristaltic activity during the menstrual cycle: characterization, regulation, function and dysfunction. Reprod Biomed Online 2002; 4 (Suppl 3): 5–9. doi: 10.1016/s1472-6483 (12) 60108-4.
4. Oždian T, Vodička J, Dostál J et al. Proteome mapping of cervical mucus and its potential as a source of biomarkers in female tract disorders. Int J Mol Sci 2023; 24 (2): 1038. doi: 10.3390/ijms24021038.
5. Wiśniewski JR. Quantitative evaluation of Filter Aided Sample Preparation (FASP) and multienzyme digestion FASP protocols. Anal Chem 2016; 88 (10): 5438–5443. doi: 10.1021/acs.analchem.6b00859.
6. Rappsilber J, Ishihama Y, Mann M. Stop and go extraction tips for matrix-assisted laser desorption/ionization, nanoelectrospray, and LC/MS sample pretreatment in proteomics. Anal Chem 2003; 75 (3): 663–670. doi: 10.1021/ac026 117i.
7. Thul PJ, Åkesson L, Wiking M et al. A subcellular map of the human proteome. Science 2017; 356 (6340): eaal3321. doi: 10.1126/science.aal3321.
8. Brazdova A, Senechal H, Peltre G et al. Immune aspects of female infertility. Int J Fertil Steril 2016; 10 (1): 1–10. doi: 10.22074/ijfs.2016. 4762.
9. Schjenken JE, Robertson SA. The female response to seminal fluid. Physiol Rev 2020; 100 (3): 1077–1117. doi: 10.1152/physrev.00013. 2018.
10. Robertson SA, Sharkey DJ. Seminal fluid and fertility in women. Fertil Steril 2016; 106 (3): 511–519. doi: 10.1016/j.fertnstert.2016.07. 1101.
11. Schreiber G. The synthesis and secretion of plasma proteins in the liver. Pathology (Phila.) 1978; 10 (4): 394. doi: 10.1016/S0031-3025 (16) 39817-8.
12. Adnane M, Meade KG, O’Farrelly C. Cervico-vaginal mucus (CVM) – an accessible source of immunologically informative biomolecules. Vet Res Commun 2018; 42 (4): 255–263. doi: 0.1007/s11259-018-9734-0.
13. Pockley AG, Barratt CL, Bolton AE. Placental protein 14 (PP14) content and immunosuppressive activity of human cervical mucus. Symp Soc Exp Biol 1989; 43 : 317–323.
14. He B, Xu J, Tian Y et al. Gene coexpression network and module analysis across 52 human tissues. Biomed Res Int 2020; 2020 : 6782046. doi: 10.1155/2020/6782046.
15. Kosmas IP, Malvasi A, Vergara D et al. Adrenergic and cholinergic uterine innervation and the impact on reproduction in aged women. Curr Pharm Des 2020; 26 (3): 358–362. doi: 10.2174/1381612826666200128092256.
16. Tommaso SD, Cavallotti C, Malvasi A et al. A qualitative and quantitative study of the innervation of the human non pregnant uterus. Curr Protein Pept Sci 2017; 18 (2): 140–148. doi: 10.2174/1389203717666160330105 341.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2023 Issue 1-
All articles in this issue
- Tissue expression analysis of cervical mucus proteome
- Acute recurrent pancreatitis during 3rd trimester of pregnancy
- The fertility sparing therapy in ectopic pregnancy
- Preterm premature rupture of membranes
- Traditional and contemporary views on the functional morphology of the fallopian tubes and their importance for gynecological practice
- Cryopreservation of ovarian tissue as a method for fertility preservation in women
- Experiences in the reconstruction of untreated severe obstetrical injuries including anal sphincter injuries
- Oxytocin and Further Uterotonic Peptide Agents: Their Early Research in Prague
- Seznam recenzentů
- Zápis z jednání volební komise pro volbu výboru Onkogynekologické sekce České gynekologické a porodnické společnosti ČLS JEP
- Epidermolysis in a newborn of a mother affected by covid-19 in the 3rd trimester of pregnancy
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Cryopreservation of ovarian tissue as a method for fertility preservation in women
- Preterm premature rupture of membranes
- The fertility sparing therapy in ectopic pregnancy
- Traditional and contemporary views on the functional morphology of the fallopian tubes and their importance for gynecological practice
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

