-
Medical journals
- Career
Dehiscencia laparotómie po hysterektómii – manažment hojenia rany
Authors: D. Karasová 1; M. Haško 2; K. Žiaková 1; P. Žúbor 2; A. Mikolajčík 3
Authors‘ workplace: Ústav ošetrovateľstva JLF UK, Martin, Slovensko, vedúca pracoviska doc. Mgr. K. Žiaková, PhD., mim. prof. 1; Gynekologicko-pôrodnícka klinika, JLF UK a UNM, Martin, Slovensko, prednosta prof. MUDr. J. Danko, CSc. 2; Chirurgická klinika JLF UK a UNM, Martin, Slovensko, prednosta doc. MUDr. D. Mištuna, PhD., mim. prof. 3
Published in: Ceska Gynekol 2012; 77(6): 486-491
Overview
Autori v príspevku prezentujú formou prospektívnej prípadovej štúdie priebeh ošetrovania a hojenia rozsiahlej dehiscencie dolnej strednej laparotómie u pacientky po operácii pre karcinóm endometria. Cieľom práce je opísať, analyzovať a vyhodnotiť priebeh hojenia komplikovanej pooperačnej rany s využitím podtlakovej a vlhkej terapie. Autori poukazujú na význam multiodborovej spolupráce a správneho „wound managementu“ v hojení komplikovanej rany. Dôraz kladú na využitie nových, ľahko dostupných technológií a postupov, na elimináciu rizikových faktorov a podporu faktorov pozitívne ovplyvňujúcich hojenie rán.
Kľúčové slová:
dehiscencia pooperačnej rany, podtlaková terapia, vlhké hojenie, kazuistika.ÚVOD
Dehiscencie operačnej rany predstavujú viac ako 50 % všetkých komplikácií v abdominálnej chirurgii s následnou mortalitou medzi 15–44 % [5]. Hlavnou príčinou ich vzniku sú predošlé operácie, trauma a pridružené infekcie [2]. Abdominálne dehiscencie vznikajú z rán akútnych, avšak pre dlhodobú a náročnú liečbu ich podľa najnovších klasifikácií radíme k ranám chronickým. Priemerná dĺžka ich hojenia sa udáva na 72 dní [18]. Hojenie takýchto rán je časovo i finančne náročné a vyžaduje kvalitný manažment (wound management). Jeho cieľom je rýchle zhojenie rany, zabránenie infekcie, minimalizácia faktorov negatívne ovplyvňujúcich proces hojenia rany a minimalizácia bolesti [8]. Ide o interdisciplinárnu snahu lekárov, predovšetkým chirurgických disciplín, špecializovaných sestier, diabetológov, infektológov, rehabilitačných pracovníkov a iných pracovníkov. Ich spolupráca by mala byť vykonávaná v súlade s najlepšími dostupnými dôkazmi praxe evidence based practices (EBP) pre optimalizáciu hojenia rán [1]. Jednou z úloh wound managementu je aj zlepšiť obmedzenú, resp. narušenú kvalitu života pacienta. Nejde len o lokálne ošetrenie rany, ale zohľadňujú sa i pridružené ochorenia a psychosociálne aspekty [11].
Základom správneho manažmentu abdominálnych dehiscencií je chirurgický debridement s následnou resutúrou brušnej steny v celkovej anestéze. V prípade infekcie rany je však potrebná konzervatívna liečba s odložením resutúry na neskoršie obdobie. V závislosti od typu a infekcie, veľkosti rany, prítomností fistúl a sínusov sa zošitie rany z liečby primárne vylučuje a indikuje sa celková i lokálna liečba zameraná na vyčistenie spodiny a približovanie okrajov (zmenšovanie rany).
V rámci ranového manažmentu sa stále častejšie používa terapia podtlakom (negative pressure wound therapy, NPWT), ktorá prebieha aplikáciou kontrolovaného subatmosferického (negatívneho) tlaku na špeciálne vyvinutú polyuretánovú penu aplikovanú do ranovej dutiny. Ide o ľahko použiteľnú, bezpečnú, dobre tolerovanú a efektívnu metódu hojenia a rekonštrukcie rán. Ako doplnková liečba dehiscencií sa používa už od svojho zavedenia v roku 1995. Podtlak spôsobuje mikro-deformácie tkaniva, ktoré majú za následok zvýšenú bunkovú proliferáciu a migráciu. Zároveň je ním odstraňovaný ranový exsudát spolu s inhibítormi mediátorov a matrix metaloproteázami (ďalej MMP), čím dochádza k zlepšeniu hojenia. NPWT zvyšuje miestne prekrvenie a zlepšuje lymfatický obeh, znižuje lokálny edém, znižuje bakteriálne osídlenie, podporuje angiogenézu, výrazne zvyšuje rast granulačného tkaniva a približovanie okrajov rany k sebe, čo je zvlášť dôležité v hojení rozsiahlych abdominálnych dehiscencií [2, 14].
Proces hojenia je mimoriadne zložitý dej, ktorý je u komplikovaných rán najviac ovplyvňovaný pôsobením mnohých sekundárnych negatívnych faktorov. Pri stanovení liečebnej stratégie si musíme uvedomiť, že nehojaca sa rana nie je len lokálny proces, ale podlieha zložitým morfologickým, látkovým a energetickým zmenám [9]. Skutočnosti ako pridružené ochorenia, infekcia, obezita a malnutrícia môžu ovplyvniť jednu alebo viac fáz procesu hojenia, čo vedie k oneskorenému alebo zhoršenému hojeniu rán. Tieto faktory je potrebné pri liečbe rán zohľadňovať, kompenzovať, prípadne ich eliminovať. Pochopenie ich vplyvu na ranu vedie k urýchleniu hojenia [13, 20].
PACIENTKA A METODIKA
Do prospektívnej štúdie bola zaradená pacientka s pooperačnou dehiscenciou rany po hysterektómii. Výber vzorky bol zámerný (komplikácia hojenia pooperačnej rany, ochota spolupracovať), podmienený získaním informovaného súhlasu pacientky.
Zber empirických údajov prebehol prostredníctvom merania (rozmery rany, zmeny exsudácie, monitoring laboratórnych parametrov), analýzou zdravotnej dokumentácie a fotodokumentácie. Údaje boli následne spracované formou prípadovej štúdie s diskusiou.
VLASTNÉ POZOROVANIE
Polymorbídna pacientka, 62-ročná, s arteriálnou hypertenziou, s ťažkou obezitou (BMI 44), diabetes mellitus 2. typu na perorálnej liečbe, s pridruženými ochoreniami – bilaterálnou koxartrózou, chronickou venóznou insuficienciou (zhojený vred pravého predkolenia), hepa-topatiou, chronickou trombocytopéniou a imunodeficienciou bola prijatá na gynekologicko-pôrodnícku kliniku s histologicky verifikovaným adenokarcinómom endometria, s propagáciou do krčka maternice, Gr 3. Po predoperačnej príprave bola u pacientky vykonaná abdominálna hysterektómia s bilaterálnou adnexektómiou a vzhľadom na obezitu len parciálnou pelvickou lymfadenektómiou. Peroperačne objavená veľká umbilikálna hernia (prítomných 5 herniálnych vakov), zresekovaná privolaným chirurgom. Pri sutúre brušnej steny boli na prevenciu dehiscencie (vzhľadom na rozsiahly výkon a obezitu pacientky) použité odľahčujúce stehy – Ventrofily. Pacientka prepustená na 6. deň po operácii do domáceho liečenia. Pri prepustení bez subjektívnych ťažkostí, afebrilná, abdomen voľné, priehmatné, palpačne mierne citlivé, bez peritoneálneho dráždenia. Operačná rana mierne erytematózna, s hematómom v rezorbcii, stehy in situ. Na operačnú ranu bol počas hospitalizácie lokálne aplikovaný antiseptický roztok s iodopovidonom a sterilné krytie.
Na 13. pooperačný deň bola pacientka pre sanguinopurulentný výtok z operačnej rany a bolesti brucha bilaterálne od operačnej rany znova prijatá na gynekologickú kliniku. Koža a podkožie boli jednoznačne inflamované.
Pri prijatí pacientka subfebrilná, v laboratórnych výsledkoch zvýšené hodnoty sedimentácie (FW), mukoproteínov, CRP, mierne zvýšené hodnoty leukocytov. Vykonaná toaleta operačnej rany – výplach peroxidom vodíka (H2O2), antiseptickým roztokom s iodopovidonom a priložené sterilné krytie. Empiricky nasadená antibiotická liečba (amoxicilín-klavulanát) (viz tab. 1).
Table 1. Porovnanie vybraných laboratórnych parametrov dôležitých pri hojení rán 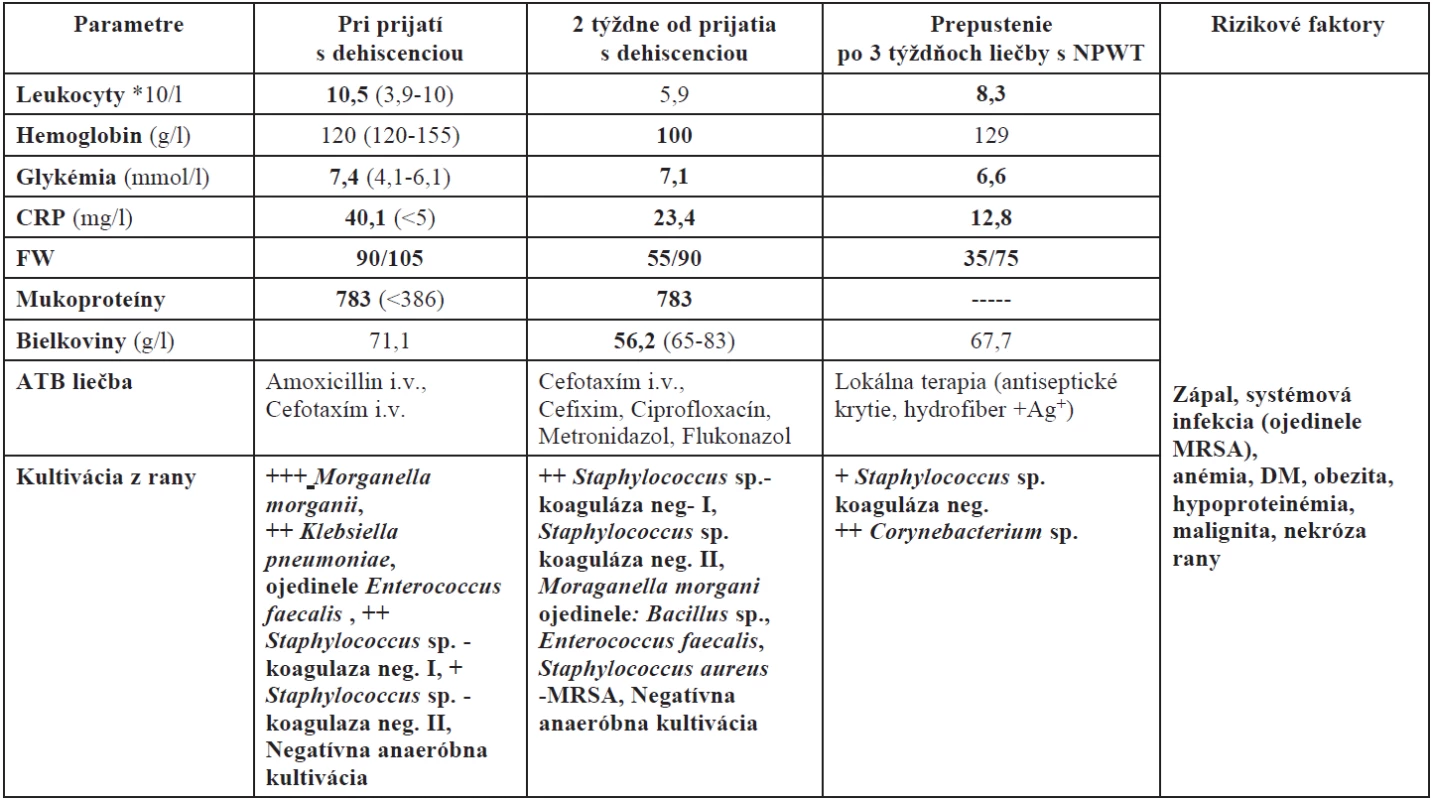
Indikované CT vyšetrenie brucha s nálezom tekutej kolekcie celkovej veľkosti 16 × 9 × 5 cm, ktorá zasahuje do svalovej vrstvy prednej brušnej steny, s obsahom plynových bublín. V intraperitoneálnom tukovom tkanive je prítomné len mierne edematózne presiaknutie, bez tekutej kolekcie, bez abscesu intraperitoneálne, bez známok dehiscencie priamych brušných svalov (obr. 1).
Image 1. CT nález; dĺžka rany CC 16,09 cm, hĺbka rany AP 5,99 cm, šírka rany LL 10,42 cm 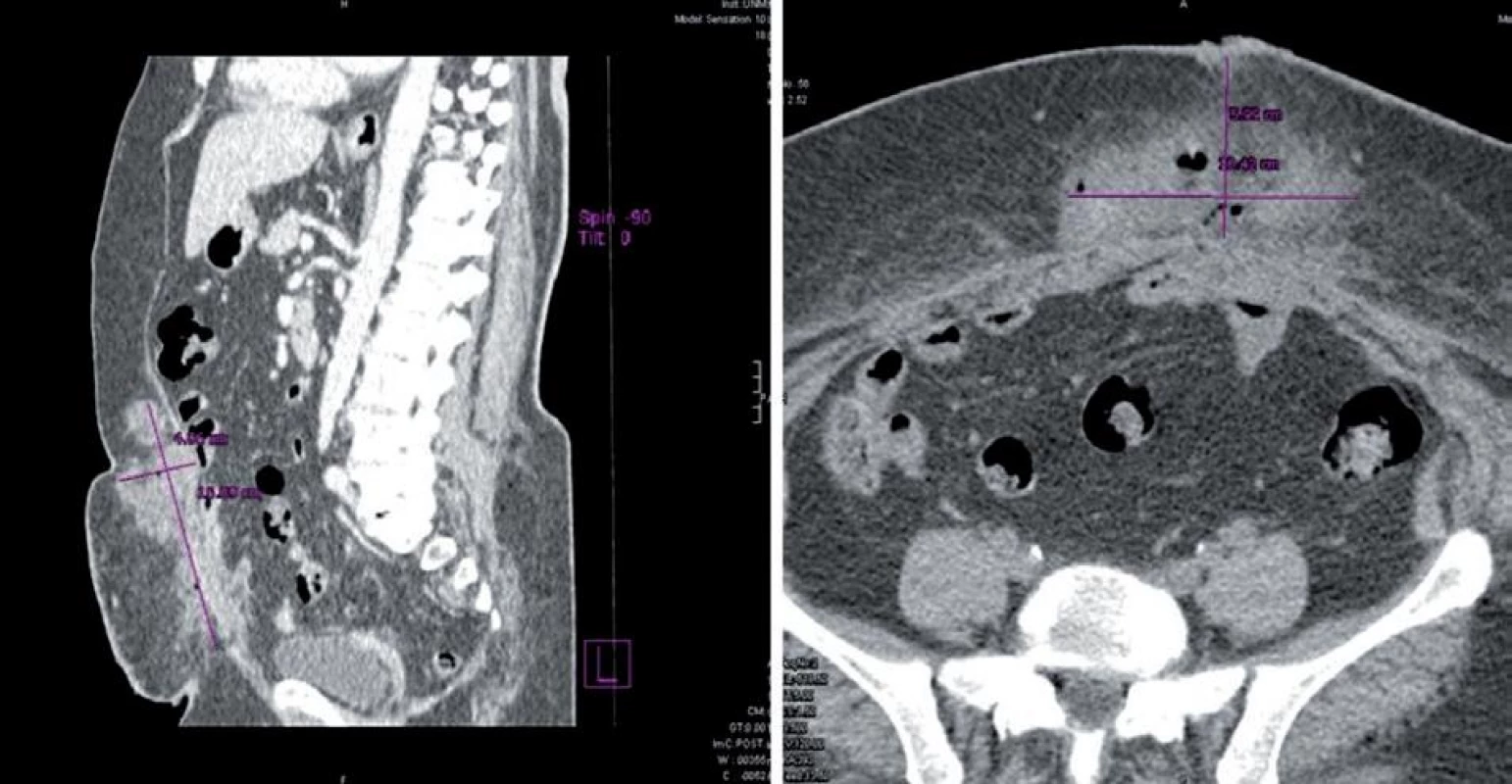
Na tretí deň rana posúdená chirurgom – stehy kože a podkožia insuficientné – extrahované, okraje nekrotické, flegmóna okolia, spodina povlečená, v podkoží periumbilikálnej oblasti prítomné štyri sínusy dĺžky do 4 cm (obr. 2A), vyplnené starými koagulami, fascia suficientná. Odobraté vzorky na kultiváciu a citlivosť, evakuácia starých koagúl, nekrektómia, chirurgický debridement, opakovane preplach H2O2 a antiseptickým roztokom s iodopovidonom. Sínusy i rana následne vyplnené longetami a štvorcami s antiseptickým roztokom, na povrch rany aplikované sterilné krytie. Koža po Ventrofiloch s dekubitmi 2. stupňa tiež ošetrená, vykonaný debridement, naložený antiseptický obväz a sterilné krytie. Pacientke bol pre ťažkú obezitu indikovaný brušný pás na sťahovanie rany, na lepšie udržanie obväzového materiálu a prevenciu herniácie. S výsledkami kultivácie z rany (tab. 1) konzultovaný infektológ, nasadená cielená antibiotická terapia podľa citlivosti (cefotaxím i.v., metronidazol i.v.). Prvých 5 dní boli preväzy vykonávané 2–3krát denne s opakovaným debridementom okrajov, spodiny a dekubitov po ventrofiloch. Na základe odporúčania chirurga bola na piaty deň od prijatia nasadená podtlaková terapia (ďalej NPWT). Úvodných 50 mm Hg bolo postupne za sledovania lokálnych i celkových prejavov (bolesť, tlak, pocit nepohodlia, objem, obsah sekrétu ap.) zvýšené na 125 mm Hg kontinuálneho podtlaku (obr. 2 B, C).
Image 2. Stav rany pri príjme. A – rana imflamovaná, zapáchajúca, prítomné dekubity po ventrofiloch, B – rana po extrakcii stehov, podmínovaná, s prítomnými sínusami do dĺžky 4 cm, vypustený skolikvovaný hematóm, C – aplikovaná klasická terapia 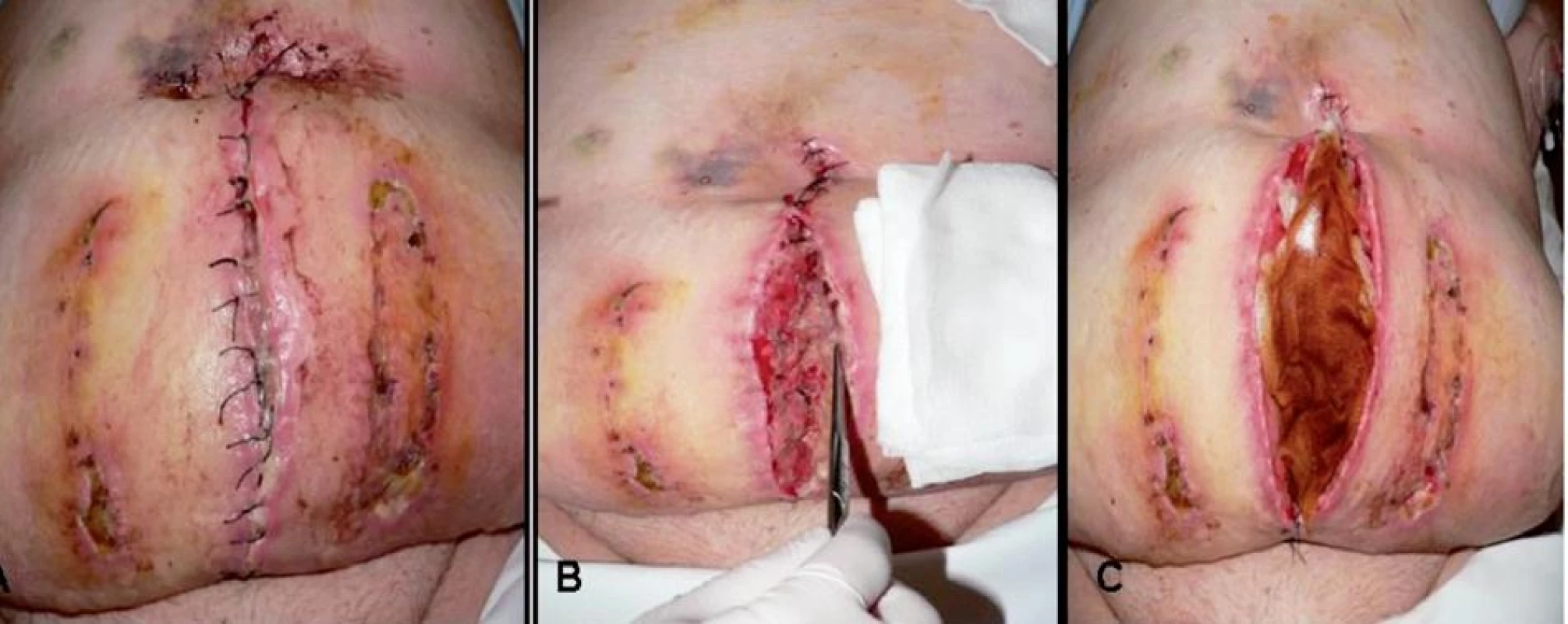
Liečba podtlakom trvala 26 dní s pravidelnými výmenami každých 48 hodín prvý týždeň, resp. každých 72 hodín ďalšie 2 týždne, s výrazným efektom. Už po prvom týždni sa zmenila veľkosť, hĺbka i šírka rany, došlo tiež k zmenšeniu prítomných sínusov (obr. 3).
Image 3. Nasadenie NPWT terapie. A – rana pred nasadením NPWT – dĺžka 16 cm, hĺbka 6 cm, šírka 10,4 cm (sínusy veľkosti 2,8 cm; 4 cm; 3,5 cm; 2,5 cm); B – vyplnenie sínusov PUR penou, spodina vypodložená sieťovinou so striebrom; C – ošetrenie dekubitov po ventrofiloch; D – naloženie NPWT 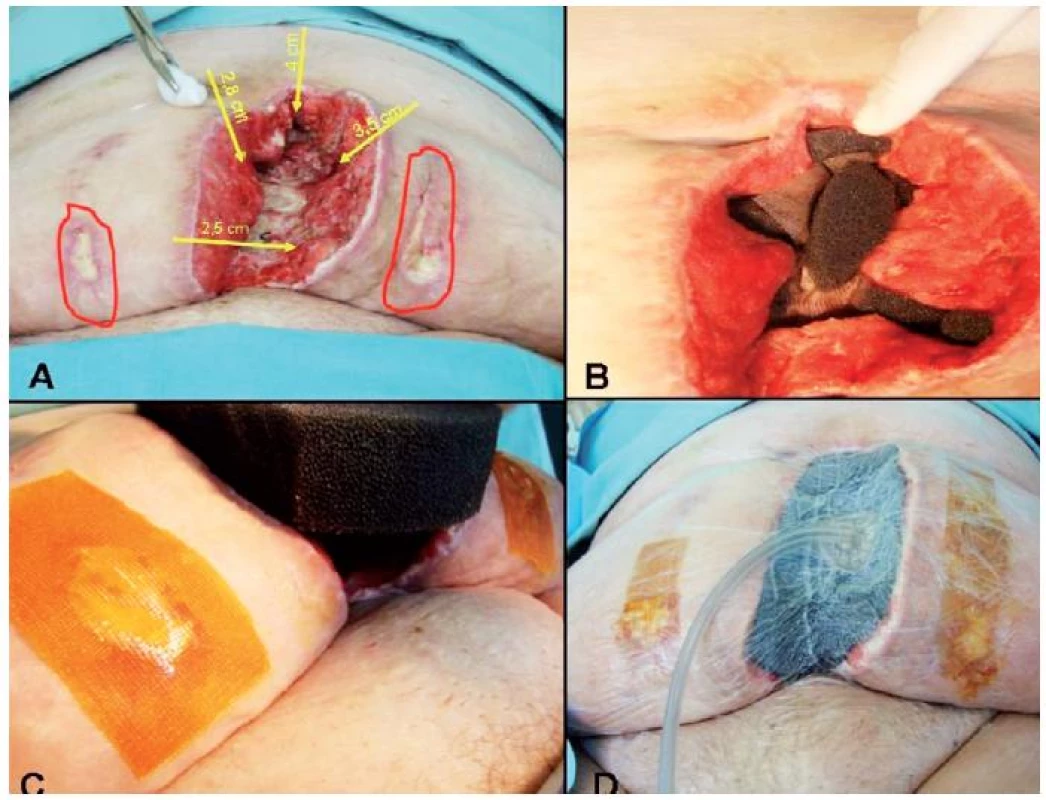
U pacientky bola na základe opakovaných sterov z rany v úzkej spolupráci s infektológom naďalej korigovaná liečba ATB – venózne podávanie cefotaxímu i.v., metronidazolu i.v, po týždni zmenené na perorálnu terapiu ciprofloxacínom, metronidazolom. Na prevenciu mykotickej infekcie bol perorálne podávaný fluconazol. Vzhľadom na hypoproteinémiu tvorila dôležitú súčasť terapie nutričná podpora (bielkovinové prídavky, nutričné nápoje, vitaminoterapia, enzymoterapia). Anémia bola korigovaná podaním erymasy. Pri každej výmene NPWT bol vykonaný chirurgický debridement spodiny, okrajov a sínusov rany a výplach rany Ringerovým roztokom. Pri neskorších výmenách bola pod polyuretánovú penu na spodinu rany a do sínusov opakovane naložená antimikrobiálna sieťovina s obsahom striebra.
Serosanguinolentná sekrécia rany sa počas preväzov s použitím NPWT postupne menila na seróznu a jej množstvo klesalo z počiatočných 420 ml/2 dni po konečných 300 ml/3 dni. Okraje rany sa približovali k sebe, spodina sa čistila a sínusy sa zmenšovali, resp. uzavreli. Objavila sa výrazná granulácia spodiny a epitelizácia okrajov (obr. 4 A, B). Po 26 dňoch liečby NPWT(na 35. deň od prijatia) bola pacientka prepustená do domácej starostlivosti, bez ATB liečby, lokálne vlhká terapia (aplikovaný hydrofiber so striebrom + hydropolymérové krytie), rana naďalej sťahovaná brušným pásom. Po prepustení bola rana ošetrovaná v spolupráci s agentúrou domácej ošetrovateľskej starostlivosti (ADOS), preväzy rany vykonávané po 48, neskôr po 72 hodinách. Každých 14 dní kontrola v chirurgickej ambulancii. Pokračovala substitúcia bielkovín, enzymoterapia, vitaminoterapia, kontroly glykémie, diabetická diéta a sledovanie hmotnosti.
Rana bola úplne zhojená za 90 dní (obr. 4 C).
Image 4. Stav rany po liečbe s NPWT. A – rana po 17 dňoch používania NPWT – spodina čistá, granulujúca, okraje epitelizujúce (dĺžka rany 10,5 cm, hĺbka 5,5 cm, šírka 7,8 cm); B – rana po mesiaci od ukončenia liečby NPWT, ošetrovaná vlhkou terapiou (lokálne hydrofiber so striebrom a sekundárne krytie; C – rana zhojená po 90 dňoch 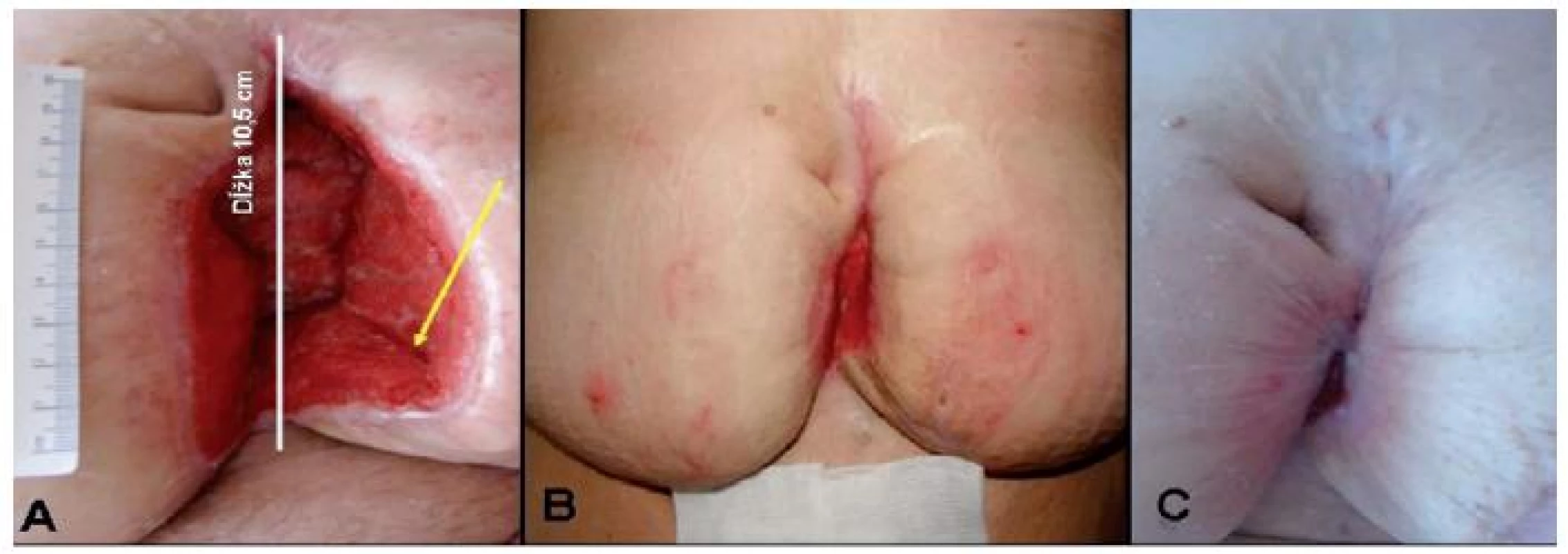
DISKUSIA
Štúdia prezentuje prípad polymorbídnej 62-ročnej pacientky s histologicky verifikovaným karcinómom maternice, po hysterektómii, s komplikovanou dehiscenciou dolnej strednej laparotómie. Liečenie prebehlo pod dohľadom multiodborového tímu s dôrazom kladeným na využitie nových, ľahko dostupných technológií a postupov v hojení rán. Dôraz bol kladený na elimináciu rizikových faktorov a podporu faktorov pozitívne ovplyvňujúcich hojenie rán.
Rozsiahle abdominálne dehiscencie sú častým, závažným a dlhodobým problémom, vyskytujúcim sa vo všetkých chirurgických odboroch. V riešení týchto rán je ešte stále zvykom uplatňovať konvenčné postupy (preväz gázou vlhčenou antiseptikom 2–3× denne). Následkom konvenčnej liečby však môže byť rozvoj závažných komplikácií, medzi ktoré patrí zvyšovanie bakteriálnej záťaže pacienta, rozširovanie rany, vznik abscesov a ich opakované drénovanie a debridment v lokálnej, no častokrát i celkovej anestéze, čo vedie k predlžovaniu hospitalizácie a zhoršovaniu zdravotného stavu pacienta. V neposlednom rade musíme brať do úvahy zvýšenú bolesť a frustráciu pacienta i celého ošetrujúceho tímu.
V nami prezentovanom prípade sa rana prvotne ošetrovala konvenčne, výplachmi 3% peroxidom vodíka a antiseptickým roztokom a neskôr vkladaním longiet a štvorcov nasiaknutých antiseptickým roztokom, bez výrazného efektu. H2O2 má krátkodobý baktericídny účinok, je cytotoxický na granulačné tkanivo (fibroblasty, keratinocyty), spôsobuje relatívne vysoké riziko vzduchovej embólie po aplikácií do hlbokých rán. Jeho antiseptický efekt s krátkodobým trvaním je pre jeho negatívne účinky na novovzniknuté tkanivo v liečbe chronických rán bezvýznamný [20].
Na tretí deň hospitalizácie bola rana otvorená s nálezom infikovanej spodiny, skolikvovaných hematómov a štyroch sínusov. Po odbornom chirurgickom konzíliu bola pacientke indikovaná podtlaková terapia.
Pred každou aplikáciou NPWT sme vykonali dôsledný debridement. Cieľom debridementu je odstránením nekrotického tkaniva a povlaku rany odhaliť zdravé tkanivo na spodine rany, podporiť hojenie, odstrániť bakteriálnu záťaž, znížiť zápalovú reakciu okolia, minimalizovať zápach a sekréciu a zlepšiť miestne prekrvenie a dostupnosť rastových faktorov. Najrýchlejším a najefektívnejším druhom čistenia rany je chirurgický (ostrý) debridement, vykonaný pomocou chirurgických nástrojov (chirurgická lyžička, skalpel, nožnice ap.). Jeho vykonanie je bezpodmienečné pri prítomnosti infikovaných káps, tunelov na určenie ich veľkosti a zabránenie rozvoja infekcie až sepsy [14].
V našom prípade sme po chirurgickom debridemente spodiny i okrajov rany aplikovali podtlakovú terapiu (s kontinuálnym podtlakom 125 mm Hg) po dobu 26 dní, s výrazným efektom. Už po prvom zložení (po 48 hodinách) sme pozorovali vyčistenie spodiny, zmenšenie sínusov a skrátenie ranovej dĺžky i hĺbky. Uvádza sa, že optimálne výsledky hojenia rán NPWT sa dosahujú pri kontinuálnom tlaku 120 mm Hg. Dĺžka používania liečby je závislá od lokálneho nálezu [4].
Okrem správne zvolenej terapie vplýva na urýchlenie hojenia chronických rán aj množstvo celkových i lokálnych faktorov. V nami prezentovanom prípade sme identifikovali a následne eliminovali mnohé rizikové faktory (viz tab. 1). Substituovali sme nedostatočnú hladinu bielkovín, vitamínov, enzýmov, eliminovali sme infekciu, korigovali anémiu, hyperglykémiu.
Rizikové faktory ovplyvňujúce hojenie rán sú multifaktoriálne, preto by sa k ich odstraňovaniu malo pristupovať interdisciplinárne. Dostatočný príjem bielkovín a aminokyselín je základnou podmienkou pre všetky procesy proliferácie, pre tvorbu spojivového a granulačného tkaniva, ako aj na produkciu enzýmov, hormónov a imunoglobulínov. Denná potreba bielkovín u zdravého človeka je 0,8 g/kg. Pri ich nedostatku sa potreba zvyšuje na 1,0-1,5 g/kg, podľa závažnosti ochorenia [20]. Najväčší podiel celkových bielkovín v organizme predstavuje albumín (50–60 %), ktorý sa podieľa na transporte aminokyselín, zinku a esenciál-nych mastných kyselín. Pokles sérového albumínu zapríčiňuje podľa Wilda riziko vzniku dehiscencie [24]. V hojení rán hrajú významnú rolu aj aminokyseliny ako L-arginin a glutamin. Majú imunomodulačné vlastnosti. Arginin podporuje syntézu bielkovín, prispieva k tvorbe kolagénu a podieľa sa na zlepšovaní imunitnej odpovede organizmu pri infekcii [20].
Prítomnosť infekcie tiež významne ovplyvňuje rýchlosť hojenia rany. U nami sledovanej pacientky boli z rany vykultivované rôzne druhy patogénov, vrátane ojedinelého výskytu zlatého stafylokoka rezistentného na meticilín (MRSA), ktoré boli následne eliminované v spolupráci s infektológmi. V slovenských nemocniciach podľa dostupných výsledkov je výskyt MRSA v intervale 5–8 %. Najviac invazívnych MRSA infekcií sa zvyčajne zisťuje u pacientov vo veku nad 75 rokov a u pacientov po chirurgickom zákroku [22]. Cielené užívanie antibiotík podľa výsledkov kultivácie vedie k znižovaniu osídlenia rany nežiaducimi patogénmi, k znižovaniu secernácie, a tým k jej zmenšovaniu. Infekcia je bežnou príčinou spomaleného hojenia rán. Chronická alebo ťažko sa hojaca rana zotrváva vo fáze prolongovaného zápalu. Baktérie predlžujú hojenie priamo alebo nepriamo. Obmedzujú proliferáciu a migráciu fibroblastov i ostatných buniek vrátane endotelu a stimulujú tiež matrix metaloproteázu (ďalej MMP) [12]. Proteázy sú skupiny enzýmov, ktoré štepia bielkoviny prítomné vo všetkých exsudujúcich ranách. Hrajú kľúčovú úlohu v hojení rán. Sú produkované v rôznych bunkách (granulocyty, keratinocyty, fibroblasty) v proaktívnej alebo latentnej forme a pre plné pôsobenie musia byť aktivované. Nadbytok proteáz a nedostatok ich inhibítorov udržuje ranu chronickú. Naviac nadbytok proteáz deštruuje rastové faktory. Najznámejšie z hľadiska hojenia rán sú MMP.
Baktérie sa na rane vyskytujú vo forme biofilmu (ide o zložité spoločenstvo baktérií, uložené v medzibunkovej hmote, adherujúce k neživým i živým povrchom), ktorý je často odolný voči tradičnej liečbe antibiotikami. Dôsledkom tejto skutočnosti je predĺženie, respektíve stagnácia hojenia v zápalovej fáze, flegmóna mäkkých tkanív v okolí, zvýšená koncentrácia bakteriálnych proteáz (má za následok rozpad nového granulačného tkaniva, kolagénu a rastových faktorov) a zvýšené hladiny prozápalových cytokínov na spodine rany. Infekčné ranové komplikácie sa môžu prejavovať abscesom, vznikom sepsy a následným predĺžením hojenia rany [13, 23]. Jedným z významných faktorov podieľajúcich sa na vzniku infekcie je aj zvýšená hladina glykémie. U pacientov s hyperglykémiou dochádza k potláčaniu funkcie neutrofilov a makrofágov, k oslabeniu imunity a následne k častejšiemu výskytu infekčných ranových komplikácií a k zvýšenej tvorbe hematómov v operačnej rane [17]. V nami prezentovanom prípade boli hodnoty glykémie korigované v spolupráci s diabetológom. Pacientka dodržiavala naordinovanú dietoterapiu, namerané hladiny glykémie neprevyšovali hodnoty nad 8 mmol/l.
Podporné užívanie vitamínov a enzýmov tiež viedlo k urýchleniu hojenia. Vitamíny sú kofaktormi viacerých enzýmov, ktoré sa podieľajú na procese hojenia rán. Dostatočný prísun vitamínu A podporuje epitelizáciu a granuláciu, antagonizuje inhibičný efekt steroidov pri hojení rán, zvyšuje influx makrofágov do rany, potencuje diferenciáciu fibroblastov a tvorbu kolagénu, zvyšuje bunkovú imunitnú odpoveď a má priaznivý účinok na sepsu. Vitamíny B12 a C sa podieľajú na syntéze kolagénu a stimulujú tvorbu ochranných protilátok pred infekciou. Pri nedostatku vitamínu C dochádza k poklesu regenerácie rany [3, 21]. Vitamíny B-komplex sú kofaktormi enzýmov podieľajúcich sa na premene cukrov, tukov a bielkovín. Ich nedostatok má negatívny vplyv na hojenie rán [19].
Fyziologické hojenie rán si vyžaduje dostatočné prekrvenie, vyváženú stravu, dobrý stav imunitného systému, vyhýbanie sa negatívnym mechanickým silám, (napr. nadmerný tlak, ťah ap.) [9]. Prítomnosť lokálnych alebo systémových faktorov ovplyvňujúcich hojenie rán má za následok spomalený rast granulačného tkaniva a zhoršenú reepitelizáciu. Často dochádza k infikovaniu rany a všetky tieto skutočnosti majú za následok stagnáciu hojenia a zhoršenie stavu rany [6]. Predlžuje sa hospitalizácia a stúpajú náklady na liečbu. Jednou z hlavných zásad hojenia rán je dbať na odstránenie, alebo aspoň minimalizáciu faktorov negatívne ovplyvňujúcich hojenie [8]. Rizikové faktory ovplyvňujúce hojenie rán sú multifaktoriálne, preto by sa k ich odstraňovaniu malo pristupovať interdisciplinárne. Zabezpečenie správneho algoritmu ošetrovania rán urýchľuje hojenie a optimalizuje ekonomické náklady [6].
ZÁVER
Proces hojenia rán je veľmi zložitý dej, ktorý je u chronických, komplikovaných rán najviac ovplyvňovaný pôsobením mnohých sekundárnych negatívnych faktorov. Pri stanovení liečebnej stratégie si musíme uvedomiť, že nehojaca sa rana nieje len lokálny proces, ale ide o zložitú zmenu morfologickú, látkovú i energetickú. Identifikáciou rizikových faktorov hojenia rán, ich elimináciou a zapojením ranového manažmentu (vrátane klinicky špecifických postupov) do starostlivosti o chronické rany dosiahneme skrátenie doby hospitalizácie, zníženie záťaže pacienta, jeho rodiny a v neposlednej rade i znížené finančné náklady na liečbu.
Dehiscencie laparotomických rán po operáciách pre zhubné nádory vnútorného genitálu predlžujú hospitalizáciu pacientky, zvyšujú náklady na liečbu a zároveň oddiaľujú adjuvantnú liečbu základného ochorenia, čo má v konečnom dôsledku negatívny dopad nielen na aktuálny zdravotný stav pacientky, ale aj na celkové zvyšovanie mortality pre nádorové ochorenia. Sú stálou oblasťou záujmu pre pacientov, lekárov, nemocnice a poisťovne. Okrem ich negatívneho vplyvu na kvalitu života negatívne vplývajú aj na ekonomický rozpočet zdravotníckych zariadení.
Podtlaková terapia je aj napriek prvotným vyšším nákladom užitočným doplnkom v liečbe abdominálnych dehiscencií a v konečnom dôsledku znižuje finančný rozpočet ich hojenia. Zabezpečenie správneho algoritmu ošetrovania rán, eliminácia rizikových faktorov a podpora pozitívne ovplyvňujúcich faktorov urýchľujú hojenie a optimalizujú ekonomické náklady.
Poďakovanie
Vzdelávanie v problematike ranového manažmentu bolo realizované vo švajčiarskom Zürichu za finančnej podpory európskych sociálnych fondov, z projektu Podpora rozvoja ľudských zdrojov s využitím najmodernejších postupov a foriem vzdelávania na JLF UK v Martine.
Práca bola podporená projektom Dobudovanie centra excelentnosti pre perinatologický výskum (CEPV II) ITMS 26220120036, ktorý je spolufinancovaný zo zdrojov EÚ.
„Podporujeme výskumné aktivity na Slovensku/ Projekt je spolufinancovaný zo zdrojov EÚ.“
Adresa pro korespondenci:
Mgr. Daniela Karasová
Univerzita Komenského v Bratislave
Jesseniova lekárska fakulta v Martine
Ústav ošetrovateľstva
Malá Hora 5
036 32 Martin
Slovensko
e-mail: karasova@jfmed.uniba.sk
Sources
1. Alexis, C. Holistic assessment and management of a complex wound. In Primary Intention., [online], 6/2006, 14, 2, p. 82–84. [23.11.2009]. Dostupné na: www.awma.com.au/journal/library/1402_04.pdf
2. Baherestani, MM., Gabriel, A. Use of negative pressure wound therapy in the management of infected abdominal wounds containing mesh: an analysis of outcomes. Int Wound J, 2011, 8, p. 118–125.
3. Blank, I. Wundversorgung und Verbandwechsel. Stuttgart: W. Kohl-hammer GmbH, 2007, 201 S.
4. Borgquist, O., et al. Wound edge microvascular blood flow during negative pressure wound therapy: examining the effects of pressures from −10 to −175 mmHg. Plast Reconstr Surg, 2010, 125, p. 502–509.
5. Bounovas, A., et al. Management of abdominal wound dehiscence with porcine dermal collagen implant: Report of case. 2008, [citované 24.10.2011]. dostupné na: http://www.o-wm.com/content/management-abdominal-wound-dehiscence-with-porcine-dermal-collagen-implant-report-a-case?page=0,0
6. Braumann, CH., et al. Komplieziert heilende Wunden und moderne Behandlungsstrategien. Perioperative Med, 2010, 2, S. 5–16.
7. Carlson, JW., et al. Multidisciplinary panel discussion of a gynecologic oncology patient: Preventing wound complications. Gynecol Oncol, 2008, 111, p. 98–100.
8. Daumann, S. Woundmanagement und Wounddokumentation. Stuttgart: W. Kohlhammer GmbH, 2009, 145 S.
9. Fonder, MA., et al. Treating the chronic wound: A practical approach to the care of nonhealing wounds and care dressings.J Am AcaD Dermatol, 2008, 58, 2, p. 185–206.
10. Germann, G. Kompendium rán a jejich ošetřování. Veverská Bítýška: Hartmann-Rico, 2002, 123 s.
11. Gillitzer, R. Modernes Wundmanagement. Hautarzt, 2002, 53, 2, S. 130–147.
12. Grofová, Z. Biologie rany. Čes geriatric Rev, 2006, 3, s. 157–162 [online]. [citované dňa 11.1.2012], dostupné na: http://www.geriatrickarevue.cz/
13. Guo, S., DiPietro, LA. Factors affecting wound healing. J Dental Res, 2010, 89, 3, p. 219–229, [online]. [citované dňa 30.10.2011], dostupné na: http://jdr.sagepub.com/content/89/3/219
14. Kitzinger, H., et al. Chirurgisches Debridement. In Manual der wundheilung. Wien: Springer-Verlag. 2007, S. 53–56.
15. Lee, DL., et al. Negative pressure wound therapy: an adjuvant to surgical reconstruction of large or difficult skin and soft tissue defects. Int Wound J, 2011, 8, p. 406–411.
16. Masumoto, K., et al. Successful treatment of an infected wound in infants by a combination of negative pressure wound therapy and arginine supplementation. Nutrition, 2011, 27, p. 1141–1145.
17. Mecott, G., et al. The role of hyperglycemia in burned patients: evidence based studies. Shock, 2010, 33, 1, p. 5–13.
18. Nugent, EK. Wound complications after gynecologic cancer surgery. Gynecol Oncol, 2011, 121, p. 347–352, [citované dňa 2-22-2012] dostupné na: journal homepage: www.elsevier.com/locate/ygyno
19. Panfil, ME., Schröder, G. Pflege von Menschen mit chronischen Wunden. 2. ed., Kösel: Verlag Hans Huber, Germany, 2010, 607 S.
20. Probst, W., Vasel-biergans, A. Wundmanagement. 2. ed., Stutt-gart: W. Kohlhammer, 2010, 527 S.
21. Siman, J., et al. Princípy chirurgie, Bratislava: SAP – Slovak Akademic Press, 2007, 923 s.
22. Smolár, M., et al. Meticilín-rezistentný Staphylococcus aureus (MRSA) v chirurgii. Slov Chirurgia, 2009, 6, 3, s. 13–15.
23. Stryja, J. Repetitorium hojení ran. 2. vyd. Praha: Vydavateľstvo GEUM, 2011. 371 s.
24. Wild, T., et al. Basics in nutrition and wound healing. Nutrition J, 2010, 26, p. 862–866.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2012 Issue 6-
All articles in this issue
- Follow-up po léčbě karcinomu ovaria –opravdu bez Ca 125?
- Srovnání vybraných parametrů oxidačního stresu ve folikulární tekutině u žen s poruchou plodnosti a u zdravých fertilních dárkyň oocytů
- Konzervativní postup v léčbě placenta accreta – dvě kazuistiky
- Bezpečnost domácích porodů a medicína založená na důkazech
- Domácí porody v České republice
- Štruktúrny základ transportnej funkcie vajíčkovodu
- Postižení vývoje dětí s nízkou porodní hmotnostíve 24 měsících korigovaného věku, narozených v České republice v letech 2000–2009
- Porody dětí velkých hmotností ve Fakultní nemocnici v Olomouci (1993–2010)
- Endovaskulární léčba krvácení v souvislostis porodem a těhotenstvím
- Úloha leptinu v lidské reprodukci (anorexie, bulimie)
- Dehiscencia laparotómie po hysterektómii – manažment hojenia rany
- Výskyt infekcie u novorodencov SAG pozitívnych matiek v závislosti na peripartálnej antibiotickej profylaxii a spôsobe pôrodu
- Možnosti ultrazvukové predikce placenta accreta v klinické praxi
- Nové technologie a perspektivy analýzymetabolomu embrya
- 3D MR-based brachyterapie v léčbě lokálně pokročilého karcinomu děložního hrdla – časné klinické výsledky
- Moderní chirurgická a biologická léčba karcinomu prsu
- Monochoriální biamniální gemini se společným žloutkovým váčkem při UZ vyšetření v I. trimestru –je zde zvýšené riziko vrozené vývojové vady?
- Subjektivní hodnocení vlastního zdraví a jeho souvislosti. Populační studie gravidních žen v Brně
-
Rychle progredující tumor dělohy
kazuistika
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Monochoriální biamniální gemini se společným žloutkovým váčkem při UZ vyšetření v I. trimestru –je zde zvýšené riziko vrozené vývojové vady?
- Domácí porody v České republice
- Konzervativní postup v léčbě placenta accreta – dvě kazuistiky
- Dehiscencia laparotómie po hysterektómii – manažment hojenia rany
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


