-
Medical journals
- Career
Analytické hodnotenie mono[{3-[4-(2-etoxyetoxy)--benzoyloxy]-2-hydroxypropyl}-terc-butylamónium]fumarátu
Authors: Ivan Malík; Lenka Mitterová; Fils Andriamainty; Petr Mokrý 1; Miloš Lukáč 2; Jozef Csöllei 1; Jana Gališinová; Janka Karlovská 3
Authors‘ workplace: Katedra farmaceutickej chémie, Farmaceutická fakulta Univerzity Komenského ; Ústav chemických léčiv, Farmaceutická fakulta, Veterinární a farmaceutická univerzita Brno 1; Katedra chemickej teórie liečiv, Farmaceutická fakulta, Univerzita Komenského v Bratislave 2; Laboratórium NMR, Farmaceutická fakulta, Univerzita Komenského v Bratislave 3
Published in: Čes. slov. Farm., 2012; 61, 44-52
Category: Original Articles
Overview
Predmetom publikácie je komplexné spektrálne a fyzikálno-chemické hodnotenie mono[{3-[4-(2-etoxyetoxy)-benzoyloxy]-2-hydroxypropyl}-terc-butylamónium]fumarátu, potenciálneho ultrakrátko pôsobiaceho blokátora ß1-adrenergných receptorov. Totožnosť hodnotenej zlúčeniny (pracovne označenej ako UPB-2) bola potvrdená 1H-, 13C-NMR a IR spektrami. V rámci stanovenia základných fyzikálno-chemických charakteristík bola určená hodnota teploty topenia, rozpustnosť v spektre rozpúšťadiel, čistota (adsorpčná chromatografia na tenkej vrstve), povrchová aktivita (nepriama Traubeho stalagmometrická metóda), acidobázické charakteristiky (hodnota pKa stanovená alkalimetrickou titráciou), hodnoty log ε (spektrofotometricky v UV//VIS oblasti), ako aj hodnotenie vplyvu kyslého a zásaditého prostredia na stabilitu UPB-2. Ďalšími experimentálne stanovenými parametrami boli lipohydrofilné deskriptory určené pomocou RP-HPLC (log k’), shake flask metódou stanovené hodnoty rozdeľovacích koeficientov Pexp (resp. log Pexp) v rôznych rozdeľovacích systémoch. Na základe log Pexp-údajov bola predpovedaná schopnosť UPB-2 prechádzať cez hematoencefalickú bariéru. Pre stanovenie obsahu UPB-2 bola aplikovaná RP HPLC (reversed-phase HPLC) metóda vnútorného štandardu a UV/VIS spektrofotometria pri vlnovej dĺžke 260 nm (vodné prostredie) a 258 nm (prostredie metanolu).
Kľúčové slová:
ß1-blokátory • analytické hodnotenie • spektrálna a fyzikálno-chemická charakteristika • stanovenie obsahuÚvod
Používanie niektorých antagonistov ß-adrenergných receptorov (ß-blokátorov, ßB) pri liečbe pacientov s akútnou myokardiálnou ischémiou môže viesť k srdcovému zlyhaniu, sínusovej bradykardii, progresívnej atrioventrikulárnej blokáde alebo k bronchospazmom1). Spomínané komplikácie nie sú často pred samotnou terapiou s ßB predpovedateľné, môžu byť dôsledkom priamej depresie myokardu a jeho funkcií ako aj špecializovaných konduktívnych tkanív. Zároveň relatívne dlhé pôsobenie štandardných ßB znemožňuje pohotovú elimináciu takýchto nežiaducich účinkov1, 2). Preto snaha výskumných tímov smerovala a smeruje k projekcii, príprave a hodnoteniu takých ßB, ktoré by sa vyznačovali okamžitým nástupom účinku, možnosťou titrovania dávky a relatívne krátkou dobou trvania ich pôsobenia. Esmolol je hydrofilným kardioselektívnym antagonistom ß1-adrenergných receptorov (ß1/ß2 = 33) bez vnútornej sympatomimetickej aktivity s polčasom eliminácie (T1/2) približne 9 minút. Tento relatívne krátky T1/2 je spôsobený hydrolýzou prítomnej esterovej väzby sérovými a tkanivovými esterázami3, 4). Časovo limitované trvanie účinku esmololu umožňuje pri intravenóznej aplikácii rýchle titrovanie dávky pre dosiahnutie optimálnej ß-adrenergnej blokády1). Vo vysokých dávkach však môže spôsobiť priamu kardiodepresiu, hypotenziu a srdcové zlyhanie1, 3, 4). Ešte kratší T1/2 (približne 4 minúty) je prisudzovaný landiololu, vysokoselektívnemu ßB (ß1/ß2 = 255), ktorý v porovnaní s esmololom5) vykazuje in vivo deväťnásobne účinnejšiu blokádu ß-adrenergných receptorov a in vitro osemnásobne vyššiu kardioselektivitu. Súčasne má landiolol aj rýchlejší nástup účinku ako aj elimináciu pri miernejšom negatívnom inotropnom pôsobení6, 7).
Cieľom predkladanej práce, analytického hodnotenia mono[{3-[4-(2-etoxyetoxy)-benzoyloxy]-2-hydroxypropyl}-terc-butylamónium]fumarátu (pracovne označeného ako UPB-2) je rozšíriť spektrum poznatkov o (potenciálnych) ultrakrátko pôsobiacich ßB z hľadiska určenia ich spektrálnych a fyzikálno-chemických parametrov využiteľných nielen v rámci QSAR štúdií, ale aj spätne v projekcii nových potenciálnych liečiv ovplyvňujúcich kardiovaskulárne funkcie.
Experimentálna časť
Spektrálna časť
1H - a 13C-NMR spektrometria
Použité chemikálie
Deuterovaná voda (rozpúšťadlo), ako vnútorný štandard bol použitý tetradeutero-3-trimetylsilylpropionát (Fluka AG, Buchs, Švajčiarsko; (CH3)3SiCD2COONa, Mr = 172,27). Pripravili sa roztoky hodnotenej substancie UPB-2 s koncentráciou 2 mg/650 μl D2O.
Prístroje a zariadenia
NMR spektrometer Varian Gemini 2000 (Varian, New Jersey, USA), magnet Oxford 300 MHz (Oxford, Veľká Británia).
Parametre pri meraní 1H-NMR spektier
Rozsah = 13 – -1 ppm, aktivačný čas = 3 s, počet akvizícií = 32, delay = 1 s, pracovná teplota = 20 °C.
Parametre pri meraní 13C-NMR spektier
Rozsah = 240 – -20 ppm, aktivačný čas = 1,815 s, počet akvizícií = 10 000, delay = 1 s, pracovná teplota = 20 °C.
1H-NMR (300 MHz) δ (ppm): 1,24 (t, 3H, CH2CH3, J = 7,0 Hz); 1,34 (s, 9H, C(CH3)3); 2,96–3,02 (m, 2H, CH2NH2+C(CH3)3); 3,55–3,62 (kva, 2H, CH2CH3, J = 7,0 Hz); 3,79 (t, 2H, CH2OCH2CH2, J = 4,7 Hz); 4,15 (t, 2H, CH2CH2OAr, J = 4,8 Hz); 4,25–4,39 (m, 2H, (OH)CHCH2NH2+); 4,40–4,50 (m, 1H, CH(OH)); 6,67 (s, 1/2, fumarát, 1H, CH=CH); 6,90; 6,93 (d, 2H, OArH, J = 8,9 Hz); 6,70–7,20 (broad peak, 3H, (OH), NH2+); 7,95; 7,98 (d, 2H, ArHCOO, J = 8,9 Hz).
13C-NMR (75 MHz) δ (ppm): 15,14 (CH3CH2O); 26,10 (NH2+C(CH3)3); 45,60 (CH2NH2+); 55,51 (C(CH3)3); 65,49 (CH3CH2O); 66,21 (OCH2CH(OH)); 66,89 (CH3CH2OCH2CH2OAr); 67,59 (CH3CH2 OCH2CH2OAr); 68,70 (CH(OH)); 114,27 (2C, OCArC2); 122,12 (1C, ArCCOO); 131,74 (2C, ArC2CCOO); 136,35 (fumarát, CH=CH); 162,76 (1C, OArC); 166,03 (COO); 173,11 (fumarát, COO).
IR spektrometria
Prístroje a zariadenia
Spektrometer FT-IR Impact 400D (Nicolet), merané v tabletách bromidu draselného v koncentrácii 2–3 mg látky/800 mg KBr.
IR cm-1: νas(C–H): 2972; νs(C–H): 2864; ν(C=O): 1699; νas(C=C): 1607; δ(N-H): 1508; δ(CH2): 1457; ν(C–N)sek. N: 1353, 1280; νas(C–O–C): 1171 (1118); ν(C–O)es: 1251, 1053; γ(C–H): 767, 660; v IR spektre nebola nepozorovaná vibrácia ν(NH2+) predpokladaná približne okolo 2700; δ(NH2+): 1600–1575 v prekryve; ν(C–OH): skryté v oblasti 1450–1500.
Spektrofotometria v UV/VIS oblasti
Použité chemikálie
Destilovaná voda, metanol p.a. (CentralChem, Bratislava, SR).
Príprava roztokov
Pripravili sa vodné a metanolové roztoky8) študovanej látky UPB-2 s c = 1 × 10-5 mol.l-1.
Prístroje a zariadenia
Analytické váhy Chyo JL-180 (Chyo Balance Corporation, Japonsko), UV/VIS spektrofotometer (8452 A, diode array spectrophotometer, typ Vectra 286/12) s kremennými kyvetami hrúbky 1 cm, osobný počítač, vyhodnocovací softvér (HP 845 × UV-Visible System).
Pracovný postup
Absorpčné spektrum UPB-2 sa meralo v destilovanej vode ako aj v metanole. Na základe Lambert-Beerovho zákona sa vypočítali hodnoty ε, resp. log ε pre všetky absorpčné maximá v obidvoch zvolených médiách.
UPB-2, vodné prostredie – UV λmax nm (absorbancia; log ε): 198 (1,29180; 5,11), 260 (0,88861; 4,95). UPB-2, metanolové prostredie – UV λmax nm (absorbancia; log ε): 210 (0,87086; 4,94), 258 (0,89619; 4,95).
Analytická časť
Stanovenie teploty topenia
Prístroje a zariadenia
STUART SMP 11 (Lennox Laboratory Suppliers, Dublin, Írsko).
Pracovný postup
Teplota topenia UPB-2 bola stanovená po 24-h sušení v exsikátore nad P2O5 pri tlaku 10 kPa a laboratórnej teplote, jej hodnoty sú uvedené v tabuľke 1.
Table 1. Základná charakteristika mono[{3-[4-(2-etoxyetoxy)-benzoyloxy]-2-hydroxypropyl}-<em>terc</em>-utylamónium]fumarátu (pracovné označenie UPB-2) ![Základná charakteristika mono[{3-[4-(2-etoxyetoxy)-benzoyloxy]-2-hydroxypropyl}-<em>terc</em>-utylamónium]fumarátu (pracovné označenie UPB-2)](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/7e7da6093a625c182f1fd095318346bd.png)
Stanovenie rozpustnosti
Použité chemikálie
Destilovaná voda, metanol p.a. (CentralChem, Bratislava, SR), lieh 96 % (Lachema, Brno, ČR), kyselina chlorovodíková s c = 0,1 mol.l-1 (CentralChem, Bratislava, SR), hydroxid sodný s c = 0,1 mol.l-1 (CentralChem, Bratislava, SR), chloroform p.a. (CentralChem, Bratislava, SR), acetón p.a. (Central Chem, Bratislava, SR), dietyléter p.a. (CentralChem, Bratislava, SR), dimetylsulfoxid p.a. (Lachema, Brno, ČR).
Prístroje a zariadenia
Analytické váhy Chyo JL-180 (Chyo Balance Corporation, Japonsko).
Pracovný postup
Rozpustnosť študovanej látky UPB-2 bola stanovená podľa SL 19). Návažok látky predstavoval jednotlivo 0,0100 g pre všetky rozpúšťadlá. Postupne sa hodnotila jej rozpustnosť v destilovanej vode, v metanole, v liehu 96 %, v kyseline chlorovodíkovej s c = 0,1 mol.l-1, v hydroxide sodnom s c = 0,1 mol.l-1, v chloroforme, v acetóne, v dietyléteri a v dimetylsulfoxide pri laboratórnej teplote. Objem pridávaných rozpúšťadiel bol adekvátne upravený vzhľadom na zvolený návažok.
Stanovenie hodnoty Rf pomocou adsorpčnej chromatografie na tenkej vrstve
Použité chemikálie
Lieh 96 % (Lachema, Brno, ČR), benzén p.a. (Lachema, Brno, ČR), dietylamín p.a. (Merck, Schudart, SRN), petroléter p.a. (Lach-Ner, Neratovice, ČR), dietyléter p.a. (CentralChem, Bratislava, SR), acetón p.a. (Spolchim, Bratislava, SR), propán-1-ol p.a. (Plichem, Darmstadt, SRN), cyklohexán p.a. (Lach-Ner, Neratovice, ČR), chloroform p.a. (CentralChem, Bratislava, SR), toluén p.a. (Lachema, Brno, ČR), etylacetát p.a. (CentralChem, Bratislava, SR).
Materiál, prístroje a zariadenia
Silufol® UV254 s vrstvou silikagélu s rozmermi 200 × 200 mm (nastrihaný na vhodne veľké časti), sklenené komory s rozmermi 190 × 180 × 80 mm, mikrokapilára (Hamilton Bonaduz, Švajčiarsko), UV-lampa (KRUSS UV 240, 230VAC, Hamburg, SRN).
Pracovný postup
Na komerčne vyrábané fólie Silufol® UV254 s vrstvou silikagélu sa na vyznačený štart mikrokapilárou naniesli 2 μl 1 % metanolových roztokov hodnotenej zlúčeniny UPB-2 a kyseliny p-hydroxybenzoovej (p-OHBA) ako „štandardu“, vstupnej substancie pri syntéze UPB‑2. Po ukončení vyvíjania sa chromatogramy sušili pri laboratórnej teplote a detegovali sa pod UV-lampou pri vlnovej dĺžke 254 nm8). Výsledné hodnoty sú priemerom zo šiestich paralelných stanovení (pozri časť Výsledky a diskusia).
Skúšanými vyvíjacími sústavami boli: S1: petroléter : dietyléter (ϕ = 1 : 2 ako aj 2 : 1); S2: acetón : petroléter (ϕ = 2 : 3); S3: acetón : toluén (ϕ = 1 : 2); S4: acetón : toluén : dietylamín : chloroform (ϕ = 1 : 2 : 0,5 : 1); S5: petroléter : dietylamín (ϕ = 8 : 2 ako aj 8 : 3); S6: propán-1-ol : cyklohexán (ϕ = 1 : 1); S7: etanol : benzén (ϕ = 10 : 3); S8: chloroform : dietylamín (ϕ = 6 : 0,1); S9: propán-1-ol : cyklohexán : dietylamín (ϕ = 5 : 5 : 0,1 ako aj 5 : 5 : 1); S10: acetón : petroléter : dietylamín (ϕ = 8 : 8 : 0,1 ako aj 8 : 8 : 1); S11: etanol : benzén : dietylamín (ϕ = 10 : 3 : 0,1); S12: chloroform : cyklohexán : dietylamín (ϕ = 6 : 3 : 1); S13: hexán : etylacetát (ϕ = 7 : 3). Optimálne hodnoty Rf pre UPB-2 a p-OHBA boli získané v sústave S11.
Stanovenie povrchového napätia
Použité chemikálie
Destilovaná voda, metanol p.a. (CentralChem, Bratislava, SR).
Prístroje a zariadenia
Analytické váhy Chyo JL-180 (Chyo Balance Corporation, Japonsko), sklenený Traubeho stalagmometer (Kavalier, ČR).
Pracovný postup
Povrchové napätie UPB-2 bolo stanovené, podobne ako v práci8), nepriamou stalagmometrickou metódou počítania kvapiek. Použitý bol sklenený Traubeho stalagmometer (Kavalier, ČR). Pripravil sa roztok UPB-2 s c = 1 × 10-3 mol.l-1. Ako referenčná kvapalina sa použila destilovaná voda, ktorej povrchové napätie je 0,07259 N.m-1 pri teplote t = 21 °C.
Stanovenie disociačnej konštanty
Použité chemikálie
Destilovaná voda, hydroxid sodný s c = 0,1 mol.l-1 (CentralChem, Bratislava, SR), metanol p.a. (Central Chem, Bratislava, SR).
Prístroje a zariadenia
Analytické váhy Chyo JL-180 (Chyo Balance Corporation, Japonsko), automatická byreta OP 930, digitálny pH-meter (HANNH Instruments HI 221, SRN), mikropipeta, elektromagnetické miešadlo (Laboratorní přístroje, Praha, ČR).
Príprava roztokov
Roztok hodnotenej látky UPB-2 bol pripravený rozpustením 0,025 g substancie v destilovanej vode na objem 50,0 ml.
Pracovný postup
Disociačná konštanta UPB-2 bola stanovená potenciometricky alkalimetrickou titráciou s použitím automatickej byrety OP 930 spojenej s digitálnym pH-metrom. Konštantný prídavok odmerného roztoku hydroxidu sodného s c = 0,1 mol.l-1 predstavoval 0,005 ml. Titrácia prebiehala pri teplote 21 °C. Zaznamenali sa hodnoty pH titrovaného roztoku, resp. roztokov v závislosti od pridaného množstva hydroxidu sodného. Po ukončení titrácie sa interpolačným stupňom podľa Hahna zistila presná spotreba odmerného roztoku a hodnota pri polovičnej spotrebe8). Z priebehu potenciometrickej titrácie sa podľa vhodnej polynomickej funkcie v programe Statistica 8.0 (Stat Soft, Tulsa, USA) pomocou V1/2 vypočítala disociačná konštanta. Výsledná hodnota pKa pre UPB-2 je v časti Výsledky a diskusia prezentovaná ako priemer troch paralelných stanovení.
Stanovenie logaritmu retenčného faktora k’ z RP‑HPLC
Použité chemikálie
Dusitan sodný s c = 0,1 mol.l-1, metanol p.a. (Central Chem, Bratislava, SR), nátriumacetát (Lachema, Brno, ČR) na úpravu mobilnej fázy.
Prístroje a zariadenia
Chromatograf s vysokotlakovou pumpou Delta Chrom SDS 030, (Watrex, SR), slučkový dávkovač s 20-μl slučkou (Watrex, SR), kolóna s nepolárnou chemicky viazanou fázou Separon SGX C18 7 μm, 250 × 4 mm (Lachema, Brno, ČR), prietokový UV-detektor Delta Chrom UVD 200 (Watrex, SR).
Pracovný postup
Hodnota retenčného faktora k’ (v literatúre uvádzaný aj ako kapacitný faktor k’) bola stanovená podľa práce10) na kvapalinovom chromatografe s vysokotlakovou pumpou, so slučkovým dávkovačom, nepolárnou chemicky viazanou fázou a prietokovým UV-detektorom. Pre študovanú látku UPB-2 a „štandard“ p-OHBA boli použité dve mobilné fázy s rozdielnym percentuálnym zastúpením metanolu, t.j. 90 % a 95 % (pripravené z metanolu p. a. a destilovanej vody).
Chromatografické podmienky
- A. Mobilná fáza – 90% metanol upravený vodným roztokom nátriumacetátu; prietoková rýchlosť – 0,6 ml.min-1; tlak – 7,9 MPa; vlnová dĺžka – 260 nm; pracovná teplota – 21–22 °C.
- B. Mobilná fáza – 95% metanol upravený vodným roztokom nátriumacetátu; prietoková rýchlosť – 0,6 ml.min-1; tlak – 5,9 MPa; vlnová dĺžka – 260 nm; pracovná teplota – 21–22 °C.
Mŕtvy čas kolóny (t0) sa stanovil roztokom dusitanu sodného s c = 0,1 mol.l-1, ktorý mal v použitom systéme nulovú retenciu. Hodnota(-y) log k’ boli vypočítané zo vzťahu: log k’ = log [(tR – t0) / t0], kde t0 je retenčný čas roztoku dusitanu sodného s c = 0,1 mol.l-1 a tR je retenčný čas roztoku vzorky10).
Roztoky UPB-2 boli pripravené rozpustením 0,005 g látky v metanole a upravené na objem 25,0 ml. Po odvzdušnení mobilnej fázy bol chromatografický systém premývaný približne 20 minút. Prvé dva nástreky bol roztok dusitanu sodného, potom sa aplikovali roztoky hodnotenej látky (20 μl). Každá vzorka bola aplikovaná trikrát10), pre výpočet sa použila priemerná hodnota tR. Získané hodnoty sú uvedené v tabuľke 2.
Table 2. Hodnota retenčného faktora k’ (log k’) študovanej substancie UPB-2 získaného z RP-HPLC v prostredí 90 % a 95 % metanolu 
*číslo merania Stanovenie rozdeľovacieho koeficientu a výpočet niektorých molekulových deskriptorov
Použité chemikálie
Oktán-1-ol p.a. (Merck, Schudardt, SRN), heptán p.a. (Mikrochem, Bratislava, SR), cyklohexán p.a. (Lach-Ner, Neratovice, ČR), roztok kyseliny citrónovej s c = 0,1 mol.l‑1 (Chemapol, Praha, ČR), hydrogenfosforečnan disodný p.a. s c = 0,2 mol.l-1 (Lachema, Brno, ČR).
Prístroje a zariadenia
Analytické váhy Chyo JL-180 (Chyo Balance Corporation, Japonsko), mechanická trepačka (Laboratórní přístroje, Praha, ČR), UV/VIS spektrofotometer (pozri UV/VIS spektrofotometriu).
Príprava roztokov
Tlmivý roztok s hodnotou pH = 7,2 sa pripravil zmiešaním 20,8 ml roztoku kyseliny citrónovej a 195,2 ml roztoku hydrogenfosforečnanu disodného, a potom sa hodnota pH upravila na 7,4. Základný roztok skúšanej látky UPB-2 sa pripravil navážením 0,100 g zlúčeniny, jej prenesením do 50-ml odmernej banky a rozpustením v 30–40 ml tlmivého roztoku8, 10). Po ochladení sa banka týmto roztokom doplnila na objem 50 ml.
Pracovný postup
Rozdeľovací koeficient Pexp študovanej zlúčeniny UPB-2 bol stanovený experimentálne klasickou shake flask metódou jej vytrepaním medzi dve nemiešateľné fázy tak, ako sa postupovalo aj v publikáciách8, 10). Lipofilnú fázu reprezentoval postupne oktán-1-ol, heptán, cyklohexán a ako vodná fáza bol použitý tlmivý fosforečnanový roztok (TFR) s hodnotou pH = 7,4. U analyzovanej substancie UPB-2 sa vykonali v každom deliacom systéme tri paralelné stanovenia.
Výpočet niektorých molekulových deskriptorov
Hodnota polárneho povrchu molekuly (PSA) a počtu akceptorov vodíkov (nacc) pre UPB-2 (forma bázy) bola generovaná programom ChemBioDraw Ultra 11 (CambridgeSoft Corporation, Cambridge, USA); PSA = 77,02; nacc = 6.
Stabilita študovanej substancie UPB-2
Pôsobenie kyslého prostredia (kyselina chlorovodíková s c = 0,1 mol.l-1)
Použité chemikálie
Metanol p.a. (CentralChem, Bratislava, SR), lieh 96 % p.a. (Lachema, Brno, ČR), benzén p.a. (Lachema, Brno, ČR), dietylamín p.a. (Merck, Schudart, SRN).
Pracovný postup
Pripravilo sa 5 ml 1 % metanolového(-ých) roztoku(‑ov) UPB-2 a „štandardu“ p-OHBA, z ktorých sa odobral 1 ml, pridal sa 1 ml kyseliny chlorovodíkovej s c = 0,1 mol.l-1. Po 5 min sa roztoky hodnotili chromatograficky na TLC. Na fóliu Silufol UV254 sa 1,5 cm od spodného okraja nanieslo 5 μl roztokov UPB-2 a p‑OHBA. Po vyvinutí vo vyvíjacej sústave S11 sa chromatogram vysušil a detegoval pod UV-lampou pri 254 nm. Získané hodnoty Rf (priemer troch paralelných stanovení) sú uvedené v diskusnej časti.
Pôsobenie zásaditého prostredia (hydroxid sodný s c = 0,1 mol.l-1)
Pracovný postup
Rovnako ako pri hodnotení stability v kyslom prostredí, ale namiesto kyseliny chlorovodíkovej s c = 0,1 mol.l‑1 sa použil hydroxid sodný s rovnakou koncentráciou. Získané hodnoty Rf (priemer troch paralelných stanovení) sú uvedené v diskusnej časti.
Pôsobenie UV/VIS žiarenia
Pracovný postup
Pripravil sa vodný a metanolový roztok UPB-2 s c = 1 × 10-5 mol.l-1. V priebehu 1 h sa v 5-min intervaloch sledovali (prípadné) posuny vo vlnových dĺžkach absorpčných maxím ako aj (prípadné) zmeny v absorbanciách pri jednotlivých absorpčných maximách v obidvoch zvolených prostrediach.
Stanovenie obsahu UPB-2
Stanovenie obsahu UPB-2 v UV/VIS oblasti spektra
Prístroje a zariadenia
Pozri UV/VIS spektrofotometriu.
Pracovný postup
Pripravil sa 0,002% roztok, resp. roztoky UPB-2 vo vode ako aj v metanole, ktorých spektrum sa zaznamenalo v oblasti 190–400 nm proti čistému rozpúšťadlu. Zo zásobného roztoku (0,002 %) UPB-2 sa jednotlivo odpipetovalo 2, 4, 6, 8 a 10 ml do piatich 10-ml odmerných baniek. Všetky odmerné banky sa doplnili po značku vodou, resp. metanolom a zaznamenala sa hodnota absorbancie (A) takto pripravených roztokov8). Z nameraných hodnôt A sa zostrojila kalibračná krivka; vo vodnom prostredí pri vlnovej dĺžke λmax = 260 nm, v metanolovom prostredí pri λmax = 258 nm. Hodnoty koncentrácií, A a log A sú uvedené v tabuľke 3.
Table 3. Parametre potrebné na zostrojenie kalibračnej krivky pre stanovenie obsahu <em>UPB-2</em> vo vodnom (<em>λ</em><sub>max</sub> = 260 nm) a v metanolovom (<em>λ</em><sub>max</sub> = 258 nm) prostredí pomocou UV/VIS spektrofotometrie 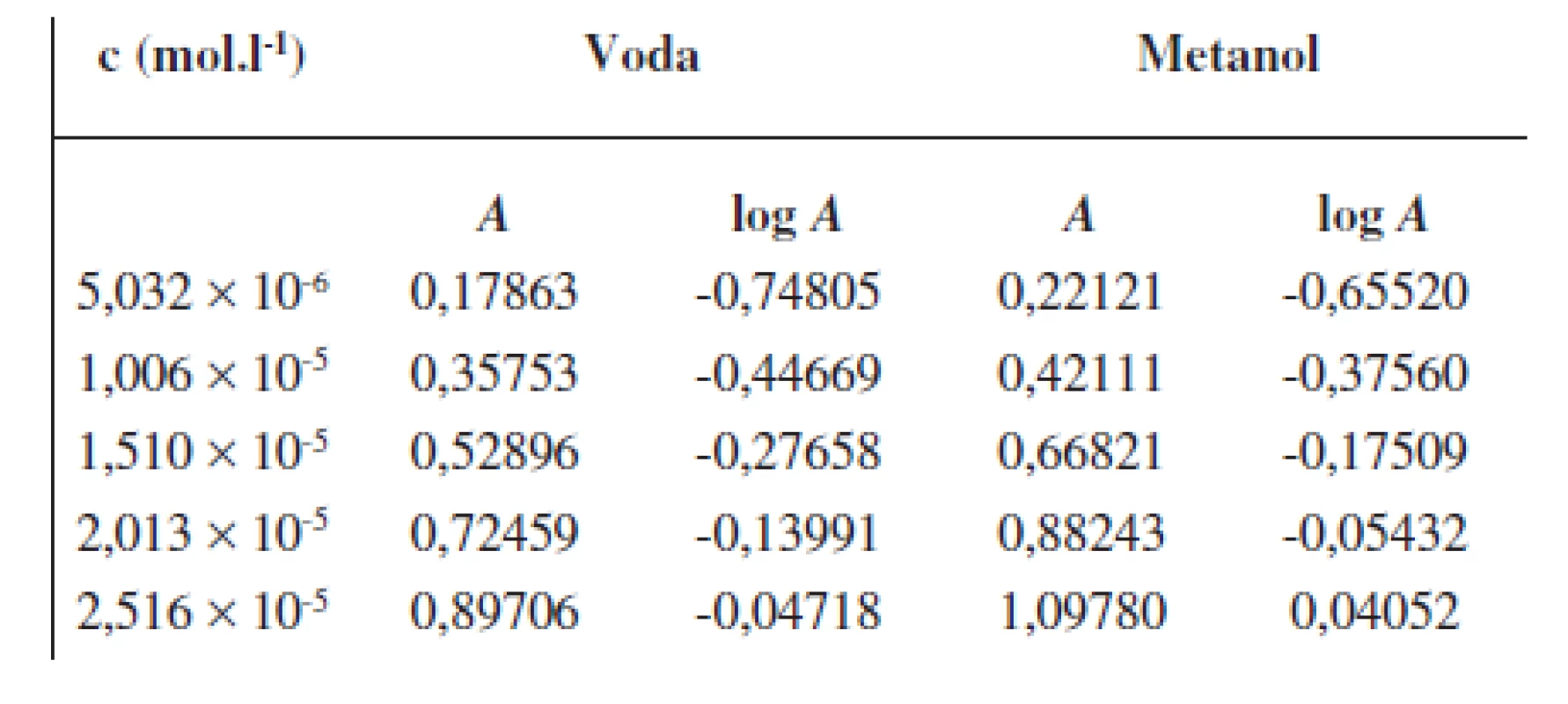
Vyhodnotenie výsledkov
Obsah UPB-2 sa stanovil z funkcie priamky (y = a x + b). Po zostrojení kalibračnej krivky a štatistickom vyhodnotení jednotlivé symboly znamenali: y = A (absorbancia), b = a0 (úsek na osi y), a = a1 (smernica priamky), x = c. Z týchto vzťahov vyplýva, že koncentrácia sa vypočíta podľa vzťahu: c = (A – a0) / a1. V získaných regresných rovniciach hodnota F je F-testom na testovanie štatistických hypotéz (štatistická indukcia) a n znamená počet prípadov.
Stanovenie obsahu UPB-2 RP-HPLC metódou vnútorného štandardu
Použité chemikálie
Metanol UV (Lachema, Brno, ČR), nátriumacetát tavený čistý (Spolana, Neratovice, ČR), vnútorný štandard – p-OHBA.
Prístroje a zariadenia
Pozri stanovenie retenčného faktora k’ pomocou RP-HPLC.
Chromatografické podmienky
Mobilná fáza – 90% metanol upravený roztokom nátriumacetátu; prietoková rýchlosť – 0,6 ml.min-1; tlak – 7,7 MPa; vlnová dĺžka – 248 nm; pracovná teplota – 21 °C.
Pracovný postup
Pripravil sa zásobný roztok UPB-2 navážením množstva 0,020 g substancie, ktoré sa kvantitatívne prenieslo do 25-ml odmernej banky a rozpustilo sa v metanole. Z tohto roztoku sa odpipetovalo do piatich 25-ml odmerných baniek postupne po 1, 2, 3, 4 a 6 ml, pridalo sa 5 ml vnútorného štandardu (pripraveného navážením 0,010 g p-OHBA, ktoré sa kvantitatívne prenieslo do 25-ml odmernej banky a doplnilo sa po značku metanolom) a doplnilo sa metanolom po značku10). Pomocou dávkovacieho ventilu sa z takto pripravených roztokov na kolónu nanášal objem 20 ml.
Vyhodnotenie výsledkov
Z pamäti počítača bol vyvolaný záznam analýzy vzorky, integrovali a opísali sa plochy zodpovedajúce analyzovanej látke (P1) a jej vnútornému štandardu (P2). Výsledky analýz10) sa vypočítali z pomeru plôch píkov P1/P2 (tab. 4).
Table 4. Parametre potrebné na zostrojenie kalibračnej krivky pre stanovenie obsahu UPB-2 pomocou RP-HPLC 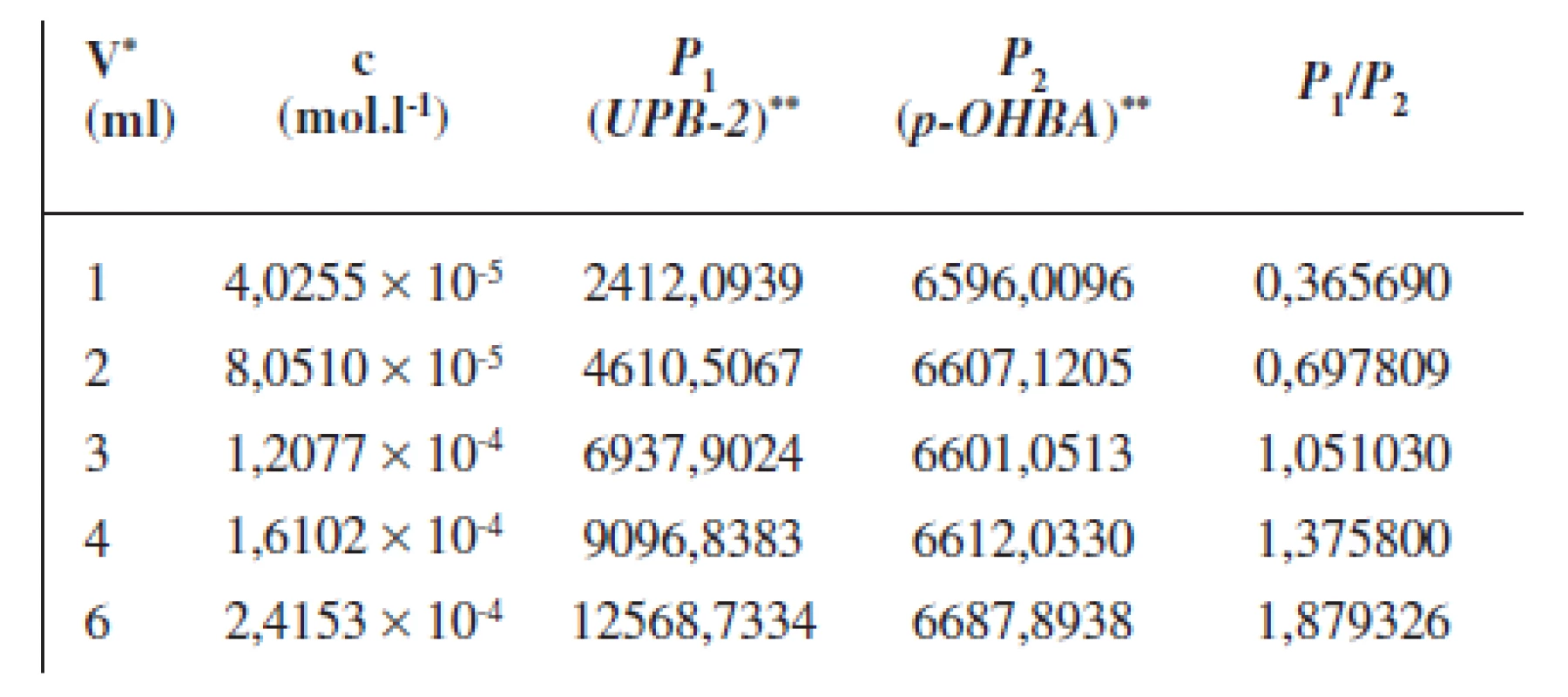
*Objem pridaného základného roztoku UPB-2 (0,0200 g/25 ml) **Plocha príslušných píkov formovaných UPB-2 (P1) a p-OHBA (P2) Výsledky a diskusia
V predchádzajúcej publikácii11) bola komplexne hodnotená zlúčenina s potenciálnym ultrakrátkym antagonistickým pôsobením na ß-adrenergné receptory s pracovným označením UPB-1, v ktorej štruktúre bola bázická časť tvorená izopropylamóniovou skupinou. Podobne ako UPB-1 aj UPB-2, chemicky mono[{3-[4--(2-etoxyetoxy)-benzoyloxy]-2-hydroxypropyl}-terc--butylamónium]fumarát, ktorej vypracovanie analytického profilu je predmetom tejto publikácie, bola pripravená na Ústavě chemických léčiv FaF VFU v Brne. Jedná sa o bielu kryštalickú látku, ktorej chemická štruktúra, sumárny vzorec (bázická forma ako aj forma soli), Mr a interval teploty topenia sú prezentované v tabuľke 1. Pri syntéze UPB-2 bola použitá ako vstupná reagencia kyselina p-hydroxybenzoová (p-OHBA), ktorej niektoré experimentálne stanovené fyzikálno-chemické parametre boli už sumarizované v práci11) a ktorá bola aj v tomto prípade využitá pri orientačnom hodnotení čistoty látky UPB-2 pomocou adsorpčnej chromatografie na tenkej vrstve, pri stabilitných skúškach ako aj pri stanovení jej obsahu s využitím RP-HPLC.
Totožnosť hodnotenej zlúčeniny UPB-2 bola potvrdená príslušnými spektrálnymi metódami. V 1H - a 13C--NMR spektre boli identifikované signály, ktoré prislúchali alkylovým fragmentom, resp. jednotlivým atómov vodíka a uhlíka v lipofilnej ako aj v bázickej oblasti molekuly. V 1H-NMR spektre boli v intervale 6,70 až 7,20 ppm pozorované signály troch protónov, u ktorých možno predpokladať, že zodpovedajú signálom protónu OH-skupiny v spojovacom 2-hydroxypropán-1,3-diylovom reťazci a protónom NH2+-skupiny. V 1H - a 13C--NMR-výstupoch boli identifikované a priradené signály protónov a atómov uhlíka tvoriacich aromatický skelet molekuly ako aj príslušný fumarátový anión.
Analýza IR spektier potvrdila prítomnosť terc-butylového substituenta, lipofilného aromatického jadra ako aj karboxylu. Pás IR spektra valenčnej vibrácie (C=O)-skupiny pri 1699 cm-1 sa môže pri UPB-2 využiť pre kvantitatívne hodnotenie, pri UPB-1 bol tento pás pozorovaný pri 1704 cm-1.
UPB-2 je pomerne hydrofilnou zlúčeninou; je ľahko rozpustná v kyseline chlorovodíkovej s c = 0,1 mol.l-1, v hydroxide sodnom s c = 0,1 mol.l-1 a v dimetylsulfoxide, dobre rozpustná v destilovanej vode, mierne rozpustná v metanole a v liehu 96 %, ťažko rozpustná v chloroforme a veľmi ťažko rozpustná v acetóne a v dietyléteri. Mierne zvýšenie lipofility hodnotenej štruktúry UPB-2 v porovnaní s UPB-1, t.j. zámena izopropylu (UPB-1) za terciárny butyl (UPB-2), však spôsobilo, že UPB-2 je relatívne ťažšie rozpustná v niektorých zvolených rozpúšťadlách ako UPB-1.
Na orientačné hodnotenie čistoty UPB-2 bola okrem RP-HPLC použitá adsorpčná chromatografia na tenkej vrstve. Súčasne s UPB-2 bola chromatograficky hodnotená aj p-OHBA. Z mnohých vyskúšaných dvoj - a trojzložkových vyvíjacích sústav bola ako najvhodnejšia vyhodnotená sústava S11: etanol : benzén : dietylamín (ϕ = 10 : 3 : 0,1). V systéme S11 nastalo jednoznačné oddelenie ohraničených škvŕn prislúchajúcich UPB-2 (Rf = 0,34) a p-OHBA (Rf = 0,58), pričom na príslušnom „stĺpci“ UPB-2 neboli pozorované iné škvrny. V identickej vyvíjacej sústave a pri rovnakých laboratórnych podmienkach bola pre UPB-111) stanovená nižšia hodnota Rf (0,29).
Povrchové napätie bolo študované nepriamou Traubeho stalagmometrickou metódou počítania kvapiek. Nárast lipofility spôsobil, že UPB-2 (γ = 0,06867 N.m-1) je mierne povrchovoaktívnejšou zlúčeninou ako UPB-1 (γ = 0,06954 N.m-1) pri zachovaní rovnakých experimentálnych podmienok.
Na štúdium acidobázických vlastností bola použitá metóda alkalimetrickej titrácie (roztok hydroxidu sodného s c = 0,1 mol.l-1) pri potenciometrickej indikácii bodu ekvivalencie. Študovaná zlúčenina UPB-2 mala mierne kyslý charakter, o čom svedčí stanovená hodnota pKa = 5,56. Zámena izopropylu za terciárny butyl znamenala pokles hodnoty pKa – pre UPB-1 bola v práci11) experimentálne určená hodnota pKa = 5,71.
Pri štúdiu spektier v UV/VIS oblasti vykazovala UPB‑2 dve absorpčné maximá. Vo vodnom roztoku sú to maximá pri λ1max = 198 nm a λ2max = 260 nm, v prostredí metanolu nastal mierny posun – absorpčné maximá boli zistené pri λ1max = 210 nm a λ2max = 258 nm. Modifikácia bázickej časti molekuly nemala vplyv na posun jednotlivých absorpčných maxím, keďže identické hodnoty boli indikované aj pre UPB-111).
Pri látke UPB-2 bola charakterizovaná aj jej lipofilita prostredníctvom určenia retenčných faktorov k’, resp. log k’ v sústavách s rozdielnym percentuálnym zastúpením metanolu ako súčasťou mobilnej fázy a rozdeľovacích koeficientov v troch rozdielnych rozdeľovacích systémoch.
Rozdielna miera lipofility UPB-2 a UPB-111) sa odzrkadlila v hodnotách log k’ v oboch systémoch (tab. 2); v 90 % metanole boli zistené takéto retenčné charakteristiky: log k’UPB-1 = –0,071; log k’UPB-2 = –0,027; v 95 % metanole boli získané tieto údaje: log k’UPB-1 = 0,015; log k’UPB-2 = 0,037. Pre porovnanie sú uvádzané aj stanovené hodnoty log k’ prislúchajúce p-OHBA: –2,153 (v 90 % metanole) a –2,643 (v 95 % metanole).
Hodnoty log Pexp pre UPB-2 boli určené klasickou shake flask metódou; pre určenie koncentrácie látky vo vodnej fáze sa využila UV/VIS spektrofotometria. V zvolených rozdeľovacích sústavách bol pozorovaný minimálny rozdiel v stanovených hodnotách log Pexp. V rozdeľovacom systéme oktán-1-ol/TFR predstavoval log Pexp hodnotu 1,92 (pre UPB-1 to bola hodnota 1,70); v sústave heptán/TFR bola hodnota log Pexp = 2,00 (pre UPB-1 predstavoval tento parameter hodnotu 1,66) a v systéme cyklohexán/TFR log Pexp = 2,03 (pre UPB-1 to bolo 1,62). Ako dokumentujú tieto výsledky, štruktúrny rozdiel medzi UPB-2 a UPB-1 sa pomerne výrazne odzrkadlil aj v hodnotách rozdeľovacích koeficientov určených vo všetkých troch systémoch.
Nežiaduce účinky ßB spojené so stimuláciou CNS sú známe dlhodobo – bežne je pozorovaná letargia, útlm, únava, menej často sa vyskytujú vážnejšie stavy spojené s užívaním ßB, ako napríklad depresie, živé sny, halucinácie, delírium, paranoidné psychózy alebo schizofrénia12). Schopnosť ßB pasívne prechádzať cez hematoencefalickú bariéru (blood-brain barrier, BBB) je determinovaná, okrem iných faktorov, mierou ich lipofility. Relatívna afinita ßB proti krvnému riečišťu a mozgovému tkanivu je vyjadriteľná vzťahom:
kde parametre Cmozog a Ckrv predstavujú rovnovážne koncentrácie liečiva v mozgu a v krvi13). Distribúciu liečiva do nepolárnych oblastí mozgu odzrkadľuje hodnota log Pexp stanovená pre systém cyklohexán/TFR (log Pexp c), zatiaľ čo hodnota log Pexp stanovená v rozdeľovacej sústave oktán-1-ol/TFR (log Pexp o) vyjadruje väzbu na proteíny v periférnom krvnom riečišti14). Zlúčenina má tým hydrofilnejší charakter, čím je jej hodnota log Pexp o-c (t.j. rozdiel medzi log Pexp o a log Pexp c) pozitívnejšia; to znamená, že ochotnejšie tvorí vodíkové väzby, v menšej miere preniká do nepolárnych oblastí mozgu a je v organizme distribuovaná prednostne do krvi. Hodnota logPexp o-c = –0,11 pre UPB-2 teda indikuje, že u nej existuje určitý predpoklad permeácie cez hematoencefalickú bariéru práve do nepolárnych oblastí mozgu.
Pre predikciu schopnosti UPB-2 prechádzať cez BBB bolo zvolených niekoľko modelov a schém. V Youngovom modeli15) vyjadreného vzťahom:
logBB = 0,889–0,485 × logPexp o-c,
hodnota log BB pre UPB-2 predstavovala 0,942, čo by znamenalo jej preferenčnú interakciu s mozgovým tkanivom. Hlavnou nevýhodou Youngovej schémy je pomerne limitovaný počet zlúčenín ako aj ich výber v pôvodnom training súbore, preto sa v rámci tejto práce aplikovali aj iné možnosti predikcie prechodu UPB-2 cez BBB.
Podľa Kaliszana16) pre koreláciu log Pexp o-c a logBB platí vzťah, v ktorom bola ako aditívna veličina implementovaná aj Mr: logBB = 0,888 + 0,272 × logPexp o-c – 0,00112 × Mr;
podľa tohto modelu je hodnota logBB látky UPB-2 –1,008.
Hodnota polárneho povrchu molekuly (polar surface area, PSA), je zakomponovaná aj v modeloch Keldera17) charakterizovaného vzťahom: logBB = 1,330 – 0,032 × PSA (logBB pre UPB-2 je –1,135) a Clarka18) definovaného rovnicou: logBB = 0,550 – 0,016 × PSA (logBB pre UPB-2 je –0,682).
Pri aplikovaní Panovej19) schémy: logBB = 0,064 + 0,200 × logPexp o – 0,010 × PSA bola hodnota logBB pre látku UPB-2 –0,322.
Podľa Abrahamovho a Weathersbyho modelu predikcie20) logBB platí nasledovný vzťah: logBB = 0,119 + 0,350 × logPexp o – 0,00502 × Mr. Po dosadení príslušných parametrov bola hodnota logBB v tomto prípade –3,200.
Feher21) navrhol model, v ktorom zohľadnil aj schopnosť látky vytvárať väzby vodíkovým mostíkom: logBB = 0,4275 – 0,0017 × PSA + 0,1092 × logP – 0,3873 × nacc, v ktorom logP = logPexp o a nacc bol počet akceptorov vodíkov v molekule vo vodnom prostredí (pre bázickú formu UPB-2 je to šesť akceptorov). Vypočítaná hodnota log BB pre UPB-2 bola –1,818.
Podľa Crucianiho et al.22) je liečivo schopné prestupovať hematoencefalickou bariérou vtedy, ak je jeho hodnota logBB vyššia ako –0,300. V prípade, ak nadobúda spomínaný parameter menšiu hodnotu ako –0,300, potom liečivo nie je schopné vstupovať do mozgového tkaniva. Na základe získaných údajov z jednotlivých prediktorových modelov možno predpokladať, že hodnotená zlúčenina UPB-2 bude s vysokou pravdepodobnosťou preferovať väzbu na proteíny krvného riečišťa pred prechodom cez hematoencefalickú bariéru (okrem výstupu z Youngovej schémy predikcie) podobne ako jej izopropylový analóg, UPB-111).
Podľa hodnoty log Pexp o-h (rozdiel medzi hodnotami log Pexp v systéme oktán-1-ol/TFR a v rozdeľovacej sústave heptán/TFR) pre látku UPB-2 (–0,08) možno usudzovať, že tá je ešte slabším donorom protónu ako UPB-1 (0,04).
Kyslé ako aj zásadité prostredie spôsobilo nestabilitu látky UPB-2, pri chromatografickom hodnotení (adsorpčná TLC) sa na chromatograme(-och) v „línii“ UPB-2 okrem jej „vlastnej“ škvrny objavili v oboch prostrediach aj ohraničené škvrny prislúchajúce jednak p-OHBA (ktorá bola súčasne nanášaná na chromatogram ako referenčná substancia), ako aj ďalším „štiepnym“ produktom vznikajúcim pri rozklade UPB-2 – zlúčeninám s pracovným označením X1 a X2. V kyslom prostredí boli určené z chromatogramov tieto Rf hodnoty: 0,35 (pre látku UPB‑2), 0,68 (p-OHBA), 0,48 (X1) a 0,80 (X2); hodnoty Rf spomínaných látok pri pôsobení zásaditého média boli len nepatrne nižšie: 0,33 (UPB-2), 0,65 (p-OHBA), 0,45 (X1) a 0,78 (X2). Pravdepodobne nastalo vplyvom príslušného prostredia parciálne štiepenie molekuly UPB-2 v jej esterovej časti alebo v alkoxylovom zoskupení v lipofilnom fragmente. Rovnako tomu bolo aj pri hodnotení stability látky UPB-1 v publikácii11).
UV/VIS žiarenie nemalo v priebehu 1 h negatívny vplyv na stabilitu vodného a metanolového roztoku UPB-2; nedošlo k zmene hodnôt absorbancií pri konkrétnych absorpčných maximách a ani k ich posunu. Identický záver11) bol formulovaný aj pri hodnotení látky UPB-1.
Na „metodickú prípravu“ pre (možné) stanovenie obsahu UPB-2 v konkrétnej liekovej forme alebo v telových tekutinách možno využiť spektrálne (UV/VIS spektrofotometriu) alebo aj chromatografické (RP-HPLC) metódy. Zlúčenina UPB-2 bola stanovená spektrofotometricky pri vlnovej dĺžke druhého absorpčného maxima, t.j. pri λ2max = 260 nm (pre vodné prostredie), resp. pri λ2max = 258 nm (pre prostredie metanolu). Na základe získaných údajov bola zostrojená kalibračná krivka, výsledkom stanovenia vo vodnom prostredí bolo formulovanie rovnice lineárnej regresie v tvare: y = 35844(±405)x – 0,0038(±0,0061); R2 = 0,999; F = 7831; n = 5 (tab. 3); resp. pre stanovenie obsahu v metanolovom prostredí: y = 44003(±715)x – 0,0061(±0,0119); R2 = 0,999; F = 3783; n = 5 (tab. 3). V týchto rovniciach parameter y predstavoval absorbanciu, x vyjadroval koncentráciu stanovovanej látky v mol.l-1.
Vhodnou mobilnou fázou pre analýzu UPB-2 pomocou vysokoúčinnej chromatografie s obráteným systémom fáz sa ukázal metanol 90 %. Pre stanovenie obsahu UPB-2 pomocou RP-HPLC (tab. 4) mala formulovaná regresná rovnica nasledujúci tvar: y = 7571(±347)x + 0,0986(±0,0571); R2 = 0,992; F = 477; n = 5; parameter y znamenal pomer plôch píkov študovanej látky UPB-2 a vnútorného štandardu (p-OHBA), x vyjadroval koncentráciu stanovovanej látky v mol.l-1.
V ďalších štúdiách sa bude pozornosť venovať spektrálnym identifikačným charakteristikám a stanoveniu niektorých fyzikálno-chemických konštánt štruktúrne podobných zlúčenín, v ktorých molekule bude, v porovnaní s UPB-2, variabilne substituovaná lipofilná časť molekuly. Všetky experimentálne získané údaje budú v budúcnosti slúžiť ako zdrojový súbor informácií pre komplexné hodnotenie vzťahov medzi chemickou štruktúrou a biologickou aktivitou.
Konflikt záujmov: žiadny.
Došlo 25. srpna 2011/ Přijato 17. října 2011
PharmDr. Ivan Malík
Katedra farmaceutickej chémie, Farmaceutická fakulta Univerzity Komenského
Odbojárov 10, 832 32 Bratislava, Slovenská republika
e-mail: malik@fpharm.uniba.sk
Sources
1. Kirshenbaum J. M., Kloner R. A., Antman E. M., Braunwald E. Use of an ultra short-acting ß-blocker in patients with acute myocardial ischemia. Circulation 1985; 72, 873–880.
2. Frishman W., Silverman R., Strom J., Elkayam U., Sonnenblick E. Clinical pharmacology of the new beta--adrenergic blocking drugs. Part 4. Adverse effects. Choosing a beta-adrenoceptor blocker. Am Heart 1979; 98, 256–262.
3. Yacobi, A., Kartzinel, R., Lai, C. M., Sum, C. Y. Esmolol: A pharmacokinetic profile of a new cardioselective beta-blocking agent. J Pharm Sci 1983; 72, 710–711.
4. Sum C. Y., Yacobi A., Kartzinel R., Stampfli H., Davis C. S., Lai C. M. Kinetics of esmolol, an ultra short-acting beta-blocker, and of its major metabolite. Clin Pharmacol Ther 1983; 34, 427–434.
5. Yasuda T., Kamiya H., Tanaka Y., Watanabe G. Ultra-short-acting cardioselective beta-blockade attenuates postischemic cardiac dysfunction in the isolated rat heart. Eur J Cardiothorac Surg 2001; 19, 647–652.
6. Uraoka M., Nakajima Y., Kurita T., Suzuki A., Takata K., Sato, S. Landiolol, an ultra short acting ß1-blocker, improves pulmonary edema after cardiopulmonary resuscitation with epinephrine in rats. J Anesth 2010; 24, 67–72.
7. Shiotsuka J., Sanui M., Lefor A. Safe use of landiolol hydrochloride in patient with marked pseudocholinesterase deficiency. J Anesth 2010; 24, 309–310.
8. Malík I., Sedlárová E., Čižmárik J., Andriamainty F., Csöllei, J.: Štúdium fyzikálno-chemických vlastností derivátov kyseliny 4-alkoxyfenylkarbámovej s bázickou časťou tvorenou substituovaným N-fenylpiperazínom. Farm Obzor 2005; 74, 211–215.
9. Slovenský liekopis, zväzok 1. 1. vyd. Bratislava: Herba 1997; s. 22.
10. Malík I., Sedlárová E., Csöllei J. Analytické hodnotenie 1-(dipropylamino-3-piperidino-propán-1-yl)-3-pentyloxyfenylkarbamátu (CK-3635). Čes slov Farm 2004; 53, 256–260.
11. Malík I., Andriamainty F., Sedlárová E., Čižmárik J., Gališinová J., Mokrý P., Csöllei J., Karlovská J., Lukáč, M. Analytické hodnotenie mono[{3-[4-(2-etoxyetoxy)-benzoyloxy]--2-hydroxypropyl}-izopropylamónium]fumarátu. Čes slov Farm 2011; 60, 84–93.
12. Fisher A. A., Davis M., Jeffery I. Acute delirium induced by metoprolol. Cardiovasc Drugs Ther 2002; 16, 161–165.
13. Kaznessis Y. N. A review of methods for computational prediction of blood-brain partitioning. Curr Med Chem Cent Nerv Syst Agents 2005; 5, 185–191.
14. Tsai R.-S., El Tayar N., Carrupt P.-A., Testa B. Physicochemical properties and transport behaviour of piribedil: Considerations on its membrane-crossing potential. Int J Pharm 1992; 80, 39–49.
15. Young R. C., Mitchell R. C., Brown T. H., Ganellin C. R., Griffiths R., Jones M., Rana K. K., Saunders D., Smith L. R., Sore N. E., Wilks T. J. Development of a new physicochemical model for brain penetration and its application to the design of centrally acting H2 receptor histamine antagonists. J Med Chem 1988; 31, 656–671.
16. Kaliszan R., Markuszewski M. Brain/blood distribution described by a combination of partition coefficient and molecular mass. Int J Pharm 1996; 145, 9–16.
17. Kelder J., Grootenhuis P. D. J., Bayada D. M., Delbressine L. P. C., Ploemen J.-P. Polar molecular surface as dominating determinant for oral absorption and brain penetration of drugs. Pharm Res 1999; 16, 1514–1519.
18. Clark D. E. Rapid calculation of polar molecular surface area and its application to the prediction of transport phenomena. 2. Prediction of blood-brain barrier penetration. J Pharm Sci 1999; 88, 815–821.
19. Pan D., Iyer M., Liu J. Constructing optimum blood barrier QSAR models using a combination of 4D-molecular similarity measures and cluster analysis. J Chem Inf Comput Sci 2004; 44, 2083–2098.
20. Abraham M. H., Weathersby P. K. Hydrogen bonding. 30. Solubility of gases and vapors in biological liquids and tissues. J Pharm Sci 1994; 83, 1450–1456.
21. Feher M., Sourial E., Schmidt J. M. A simple model for the prediction of blood-brain partitioning. Int J Pharm 2000; 201, 239–247.
22. Cruciani G., Pastor M., Guba W. VolSurf: a new tool for the pharmacokinetic optimization of lead compounds. Eur J Pharm Sci 2000; 11, 29–39.
Labels
Pharmacy Clinical pharmacology
Article was published inCzech and Slovak Pharmacy

2012 Issue 1-2-
All articles in this issue
- Zvažované farmakoterapeutické přístupy léčby Alzheimerovy choroby
- Možnosti inovace individuální přípravy léčivých přípravků v lékárnách v České republice
- Deriváty kyseliny fenylkarbamové jako potenciální antituberkulotika
- Metabolomika vo výskume fytoterapeutík
- Kompatibilita fosforečnanů se solemi vápníku v parenterální výživě
- Analytické hodnotenie mono[{3-[4-(2-etoxyetoxy)--benzoyloxy]-2-hydroxypropyl}-terc-butylamónium]fumarátu
- Identifikácia lipoxygenázy s ω-6 dioxygenázovou aktivitou kvapalinovou chromatografiou
- Hodnocení stability filmů z natrium-alginátu a chitosanu
- Sledovanie účinnosti niektorých preventívnych opatrení proti chrípke
- Štúdium lokálnych anestetík – časť 196* Formulácia lokálneho anestetika heptakaín do hydrogélov na báze chitosanu
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Možnosti inovace individuální přípravy léčivých přípravků v lékárnách v České republice
- Kompatibilita fosforečnanů se solemi vápníku v parenterální výživě
- Metabolomika vo výskume fytoterapeutík
- Zvažované farmakoterapeutické přístupy léčby Alzheimerovy choroby
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


